Учебное пособие
ВОЕННО-МЕДИЦИНСКАЯ АКАДЕМИЯ ИМЕНИ С.М. КИРОВА МИНИСТЕРСТВА ОБОРОНЫ РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОСУДАРСТВЕННЫЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИСПЫТАТЕЛЬНЫЙ ИНСТИТУТ ВОЕННОЙ МЕДИЦИНЫ МИНИСТЕРСТВА ОБОРОНЫ РОССИЙСКОЙ ФЕДЕРАЦИИ
Санкт-Петербург, 2021
УДК 616-099+616.24-005.98
ББК 52.84
Т51
Токсикология пульмонотоксикантов: уч. пособие / В.А. Башарин, С.В. Чепур, П.Г. Толкач и соавт. – СПб.: ООО «Издательство «Левша. Санкт-Петербург», 2021. – 88 с. ISBN 978-5-93356-234-4 |
В учебном пособии приведены данные литературы и результаты собственных экспериментальных исследований по проблеме отравления пульмонотоксикантами. Указаны основные источники их поступления в окружающую среду. Описаны современные представления о механизмах токсического действия пульмонотоксикантов. Дана токсикологическая характеристика некоторых представителей данной группы веществ (хлор, фосген, перфторизобутилен, хлороводород, диоксид азота, паракват). Обобщены сведения о подходах к проведению патогенетической и симптоматической терапии отравлений пульмонотоксикантами. Сформированы представления о патогенетических основах формирования последствий отравления пульмонотоксикантами и их клинические проявления.
Учебное пособие составлено с учетом Национального руководства по пульмонологии (Москва, 2014), клинических рекомендаций Федерации анестезиологов-реаниматологов (Москва, 2020), Методических рекомендаций по терапии дыхательной недостаточности у пораженных отравляющими и высокотоксичными веществами на этапах медицинской эвакуации (ГВМУ, 2016). Учебное пособие утверждено решением Ученого совета Военно-медицинской академии им. С.М. Кирова, предназначено для слушателей факультета повышения квалификации и профессиональной переподготовки и может быть использовано для изучения веществ пульмонотоксического действия врачами различных специальностей.
Авторский коллектив
д.м.н. профессор В.А. Башарин, д.м.н. профессор С.В. Чепур, к.м.н. П.Г. Толкач, д.м.н. Н.Г. Венгерович, д.м.н. доцент М.А. Юдин, д.б.н. доцент А.С. Никифоров, к.м.н. О.А. Кузнецов, к.м.н. Д.В. Овчинников, П.К. Потапов, Д.Т. Сизова.
Рецензент
Заслуженный врач Российской Федерации д.м.н. профессор Н.Н. Плужников
© Коллектив авторов, 2021
© Военно-медицинская академия, 2021
© ООО «Издательство «Левша. Санкт-Петербург», макет, 2021
5.1 Токсикологическая характеристика фосгена
Фосген (дихлорангидрид угольной кислоты) – соединение, широко используемое в химической промышленности. Общемировое производство фосгена превышает 5 млн. м3/год. Например, в 2015 году в мире было синтезировано около 8,5 млн. м3 фосгена. Основным производителем и потребителем фосгена на сегодняшний день считают Китай (36,6 % от всего произведённого фосгена в мире), Европу (30,67 %) и Северную Америку (19,83 %). Около 75 % всего производимого фосгена используют при синтезе изоцианатов, которые широко применяют в системах реактивного литья под давлением, для синтеза термопластичных смол, высокоэффективных термопластичных эластомеров, эластичных пенополиуретанов, клеев, герметиков и др. Фосген транспортируют в железнодорожных и автомобильных цистернах, контейнерах и баллонах, которые служат временным его хранилищем. Обычно фосген хранят в сжиженном состоянии при температуре окружающей среды под давлением собственных паров 6-18 кгс/см2 в наземных цилиндрических горизонтальных резервуарах. Максимальные объемы хранения составляют 52 тонны. Известны чрезвычайные ситуации на промышленных объектах, сопровождавшихся выбросом фосгена в окружающую среду с поражением людей (г. Цицикар, Китай, 2008 г., г. Ле-Пон-де-Кле, Франция, 2012 г., г. Уилмингтон, США, 2014 г. и др.).
Таким образом, сохраняется риск возникновения аварийных ситуаций техногенного характера на химически опасных объектах, использующих фосген, сопровождающихся поступлением его в окружающую среду с формированием не стойкого, смертельного очага химического поражения замедленного действия.
Физико-химические свойства[18]. В обычных условиях фосген – бесцветный газ (молекулярная масса – 98,9, плотность – 4,2 г/л, температура кипения – 8,3 °С, давление пара – 1216 мм рт.ст. (1,6 атм)[19]) с запахом гнилых яблок или прелого сена. При комнатной температуре фосген – стабильное соединение, при нагревании более 250 °С разлагается на молекулярный хлор и монооксид углерода, при температуре более 500 °С – полностью разрушается. Фосген отличается высокой летучестью (давление пара – 1,6 атм). Газообразный фосген в 2,5 раза тяжелее воздуха. Хорошо растворяется в органических растворителях и некоторых отравляющих веществах (иприт). Гидролизуется фосген до соляной и угольной кислот (период полураспада составляет 0,026 с). Скорость гидролиза увеличивается в щелочных растворах, на чём основано их применение для проведения дегазации. При высокой влажности воздуха облако фосгена за счёт частичного гидролиза может приобретать беловатый цвет.
Токсичность. Фосген относят к I классу опасности. Максимальная концентрация фосгена в воздухе, которая не оказывает побочных эффектов на здоровье, при повторном ежедневном воздействии составляет – 0,1 ppm (0,405 мг/м3). Мгновенно-опасная концентрация фосгена составляет – 2 ppm (8,1 мг/м3). Концентрация, при которой ощущается запах фосгена во вдыхаемом воздухе, составляет 3 ppm (12,15 мг/м3). Поражение лёгких у пострадавших, подвергшихся воздействию фосгена, наблюдали при его концентрации во вдыхаемом воздухе более 50 ppm (0,2 г/м3). Смертельная токсодоза (LCt50) фосгена при ингаляции человека[20] составляет около 750 ppm×мин (3,1 г×мин/м3).
Токсикокинетика. Фосген поступает в организм исключительно ингаляционным путём. Будучи липофильным газом, он проникает в глубокие отделы лёгких. Гидролиз фосгена в воде слизистых оболочек приводит к проявлению его слабо раздражающего действия на глаза и верхние дыхательные пути. Продукты гидролиза фосгена (соляная кислота, вода и диоксид углерода) удаляются из дыхательных путей с выдыхаемым воздухом и с ретроградным током слизи, обусловленным ритмичным сокращением ресничек мерцательного эпителия дыхательных путей.
Токсикодинамика. Попадая в альвеолы, фосген взаимодействует с –SH-, –NH2- и –OH-группами макромолекул АГБ, оказывая на них ацилирующее действие (рисунок 10).
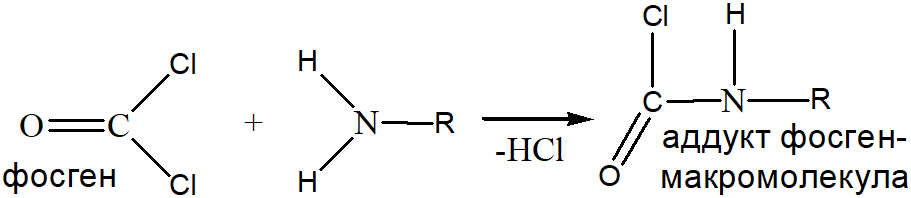
Глубина, на которую может проникнуть фосген, составляет около 6 мкм (толщина АГБ около 5-7 мкм). Таким образом, он может оказывать воздействие на все компоненты аэрогематического барьера (сурфактант, альвеолоциты или эндотелиоциты), тем не менее, первичная мишень фосгена на сегодняшний день окончательно не установлена. Изменение структуры и функции макромолекул компонентов АГБ приводит к образованию АФК, угнетению системы антиоксидантной защиты клеток и генерации провоспалительных медиаторов (интерлейкин-8, эндотелеин-1, NO-синтетаза, фосфолипаза А2, лейкотриены и др.) и дальнейшей активации провоспалительного каскада, сопровождающегося увеличением выхода жидкости из системного кровотока в интерстиций. Другой механизм пульмонотоксического действия фосгена обусловлен его нейрогенным действием. Фосген гидролизуется в нижних дыхательных путях до соляной кислоты, которая оказывает раздражающее действие на окончания чувствительных волокон n. vagus. Афферентная импульсация с блуждающего нерва активирует симпатические центры в ЦНС, что приводит к увеличению выброса катехоламинов в системный кровоток, увеличению сосудистого сопротивления и нарастанию гидростатического давления, в том числе и в системе легочной микроциркуляции. Нарастание гидростатического давления приводит к ещё большему выходу жидкости в интерстиций. В качестве дополнительного механизма токсического действия фосгена рассматривают прямое и/или опосредованное нарушение целостности плотных контактов между альвеолоцитами, сопровождающееся нарушением интеграции альвеолярной выстилки и нарушением целостности АГБ (рисунок 11).
Все вышеперечисленные патологические каскады в конечном итоге приводят к нарастанию гидростатического давления в легочных сосудах, увеличению проницаемости АГБ, выходу жидкости в интерстиций и альвеолярное пространство и манифестации токсического отёка лёгких (рисунок 12).
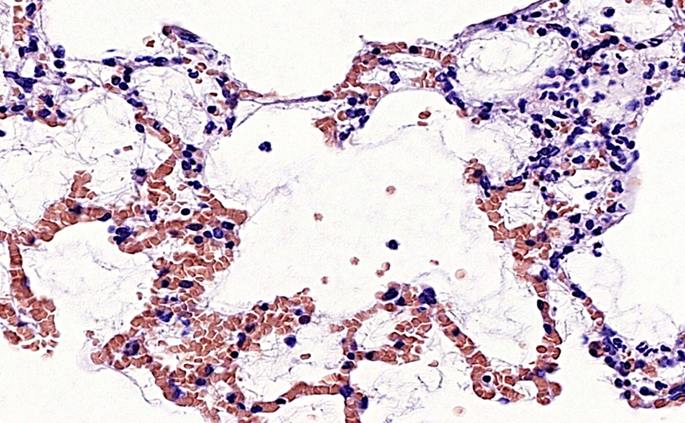
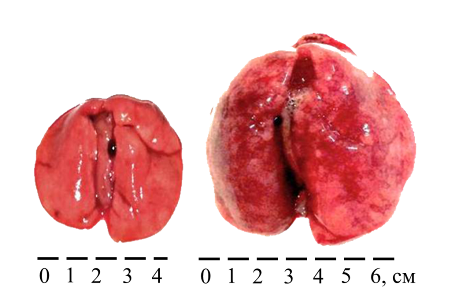
Клинические проявления интоксикации. В типичной клинической картине интоксикации фосгеном выделяют четыре основных периода: контакта, скрытый, основных проявлений, отдалённых осложнений (таблица 7).
| Период | Проявления интоксикации |
|---|---|
контакта |
|
Период |
Проявления интоксикации |
скрытый |
|
основных проявлений |
|
отдалённых осложнений |
|