Интенсивная терапия : национальное руководство : в 2 т. / под ред. И. Б. Заболотских, Д. Н. Проценко. - 2-е изд., перераб. и доп. - Москва : ГЭОТАР-Медиа, 2022. - Т. 2. - 1056 с. : ил. - (Серия "Национальные руководства"). - ISBN 978-5-9704-7191-3. |
Аннотация
Второе издание национального руководства "Интенсивная терапия" содержит современную информацию о диагностике и лечении критических состояний различной этиологии и патогенеза. Особое внимание уделено особенностям интенсивной терапии в периоперационный период у пациентов с сопутствующими заболеваниями. Благодаря объединению усилий ведущих специалистов России удалось отразить согласованную позицию по актуальным вопросам современной реаниматологии и интенсивной терапии и учесть сведения доказательной медицины. Все главы прошли этап независимого рецензирования.
Издание предназначено, прежде всего, анестезиологамреаниматологам, а также врачам всех специальностей, студентам старших курсов медицинских вузов, клиническим ординаторам, аспирантам.
13.14. ПЛЕВРАЛЬНЫЕ ВЫПОТЫ В ИНТЕНСИВНОЙ ТЕРАПИИ
С.Н. Авдеев
Эпидемиология
По данным нескольких исследований, плевральный выпот встречается более чем у 20% больных, находящихся в ОРИТ. Сам по себе плевральный выпот редко служит самостоятельной причиной госпитализации больных в ОРИТ (за исключением случаев массивного плеврального выпота с резко выраженной одышкой), однако плевральный выпот часто является осложнением многих заболеваний. Так, при пневмонии плевральный выпот встречается в 40-60%, при ТЭЛА - в 40%, при застойной СН - в 50%, у госпитализированных больных с ВИЧ-инфекцией - в 7-27%.
Плевральный выпот может возникать за счет нескольких механизмов, включая повышенную проницаемость плевральных листков, повышенное давление в легочных капиллярах, снижение отрицательного внутриплеврального давления, снижение онкотического давления и обструкцию лимфатических путей оттока.
В норме в плевральной полости содержится не более 30 мл жидкости, а общая продукция жидкости составляет около 0,3 мл/кг в сутки. Появление плеврального выпота означает наличие серьезной патологии легких, плевры или внелегочной патологии. В нормальных условиях дренажная система плевральных полостей может справиться с более чем 20-кратным повышением («700 мл) притока жидкости в плевральную полость. Поскольку дифференциальная диагностика включает широкий круг заболеваний, необходим систематический подход к обследованию такого больного с целью установить диагноз максимально быстро с минимумом инвазивных исследований.
Определение, классификация и причины плевральных выпотов
ПЛЕВРАЛЬНЫЙ ВЫПОТ - НАКОПЛЕНИЕ ЖИДКОСТИ В ПЛЕВРАЛЬНОЙ ПОЛОСТИ
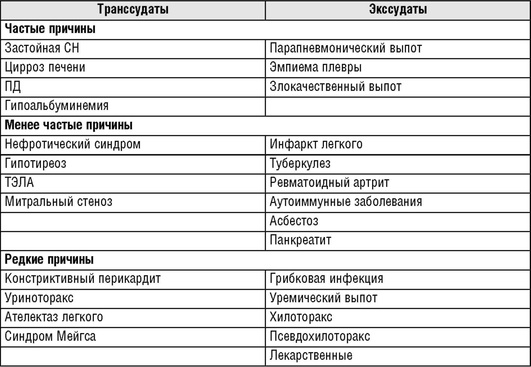
Плевральный выпот разделяется на транссудат и экссудат. Транссудат появляется, когда гидростатический баланс, влияющий на образование и абсорбцию плевральной жидкости, меняется в сторону накопления жидкости в полости плевры. Проницаемость капилляров для белка остается нормальной. Напротив, экссудат появляется, когда повреждается поверхность плевры и/или нарушается проницаемость местных капилляров. Причины транссудатов и экссудатов приведены в табл. 13.51.
|
Очень важной с практической точки зрения является классификация плевральных выпотов у больных с пневмонией. Парапневмонические выпоты можно разделить на три стадии:
С точки зрения распространенности плевральных выпотов в ОРИТ, по приблизительным данным, на долю транссудатов и экссудатов приходится более 20% (больше больных с транссудатами сердечной этиологии в ОРИТ медицинского профиля, больше инфекционных экссудатов - в ОРИТ хирургического профиля). Среди причин транссудатов в ОРИТ около 80% приходится на застойную СН, 8% - цирроз печени, 4% - нефротический синдром и др. Наиболее частой причиной экссудатов в ОРИТ являются легочные инфекции - 50%, злокачественные заболевания - 25%, ТЭЛА - 19% и др.
Диагностика
КЛИНИЧЕСКАЯ ОЦЕНКА И АНАМНЕЗ
Первый этап в оценке плеврального выпота - выяснить, является ли он экссудатом или транссудатом, сначала по данным анамнеза и врачебного осмотра, затем по результатам биохимического анализа плевральной жидкости.
Клиническая картина часто дает возможность идентифицировать транссудат. При соответствующей клинической ситуации, например при левожелудочковой недостаточности и рентгенологическом подтверждении наличия выпота, нет необходимости получать образец выпота для анализа, если только нет атипичных черт или выпот не отвечает на терапию. Аспирация не должна выполняться при двухстороннем выпоте при большой вероятности плеврального транссудата, кроме случаев с подозрением на атипичное течение, или неэффективности терапии.
Клиническая и лабораторная картина плеврального выпота на фоне пневмонии практически не отличается от таковой при пневмонии без плеврита. Лишь физикальное обследование позволяет выявить признаки плеврального выпота: ослабление дыхания на стороне поражения, притупление перкуторного звука и ослабление голосового дрожания.
Примерно 75% больных с ТЭЛА и плевральным выпотом жалуются на плевральные боли. Такие выпоты обычно занимают менее 1/3 гемоторакса, и тяжесть одышки часто не соответствует их размеру.
Также важен лекарственный анамнез. Многие лекарственные препараты (амиодарон, нитрофурантоин, фенитоин, метотрексат и др.), хотя и нечасто, могут быть причиной плеврального экссудата.
ОБЗОРНАЯ РЕНТГЕНОГРАФИЯ
Стандартная рентгенография грудной клетки является первым шагом выявления плеврального выпота (рис. 13.13) (уровень убедительности рекомендаций - III, уровень достоверности доказательств - С). Чувствительность и специфичность метода составляют 67 и 70% соответственно. При исследовании плеврального выпота рентгенограмма должна быть выполнена в прямой и боковой проекциях.
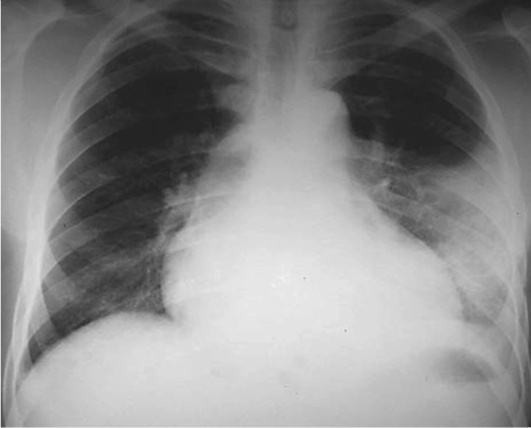
Изменения на рентгенограмме в прямой проекции, как правило, появляются при наличии в плевральной полости около 200 мл жидкости. Однако на рентгенограмме в латеральной позиции затемнение реберно-диафрагмального синуса происходит уже при наличии 50 мл жидкости. При количестве выпота до 1 л его уровень достигает, как правило, IV ребра.
Ценным методом для диагностики плеврального выпота является рентгенография грудной клетки в положении больного на боку - данная позиция позволяет оценить как объем выпота, так и способность плевральной жидкости к свободному перемещению внутри плевральной полости (то есть отсутствие осумкования) (рис. 13.14). При слое жидкости на рентгенограмме в позиции decubitus менее 10 мм торакоцентез не показан (уровень убедительности рекомендаций - II, уровень достоверности доказательств - С). Отсутствие слоя жидкости в декубитальной позиции при наличии признаков плеврального выпота в стандартных позициях может свидетельствовать о наличии осумкованного выпота. В ОРИТ рентгенологическое обследование часто выполняется больному в положении лежа, при этом свободная жидкость будет располагаться в задних отделах грудной клетки. На такой рентгенограмме жидкость в полости плевры часто выглядит как плохо очерченное затемнение одной половины грудной клетки при сохранении сосудистого рисунка. Другие симптомы включают исчезновение четкой границы купола диафрагмы на стороне выпота и утолщение малой междолевой щели. По рентгенограмме, выполненной в положении лежа, часто можно недооценить объем плеврального выпота.

УЛЬТРАЗВУКОВОЕ ИССЛЕДОВАНИЕ
УЗИ дает возможность выявления даже 5 мл жидкости, наличия спаек и вязкости плеврального выпота (уровень убедительности рекомендаций - II, уровень достоверности доказательств - С), однако возможности метода ограничены при расположении выпота вблизи средостения, в междолевом плевральном пространстве и под лопатками. Аспирация плевральной жидкости под ультразвуковым контролем является безопасным и точным методом получения жидкости при малом объеме выпота или его осумковании. После неуспешного торакоцентеза или при отграничении выпота плевральная пункция под ультразвуковым контролем дает положительный результат в 97% случаев. Плевральные выпоты со сложным эхо-генным паттерном с фибринозными перемычками или без них либо с однородной эхогенностью всегда экссудаты (рис. 13.15), а гипоэхогенные выпоты могут быть как экссудатами, так и транссудатами.
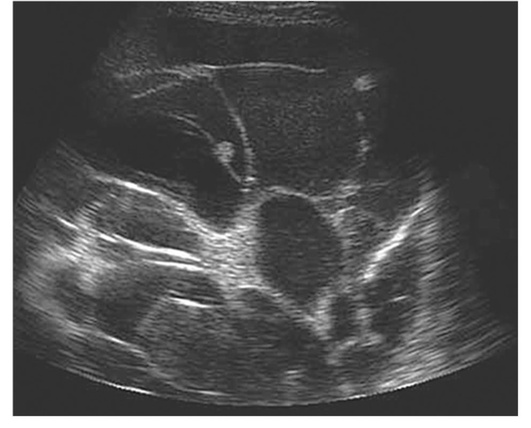
КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ
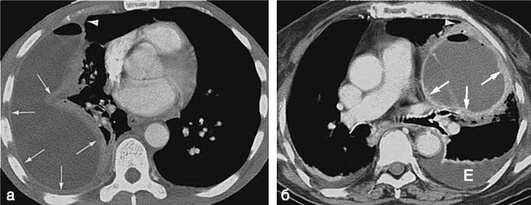
При КТ грудной клетки с контрастированием существуют признаки, которые помогают дифференцировать доброкачественное и злокачественное поражение плевры (уровень убедительности рекомендаций - II, уровень достоверности доказательств - С). При злокачественном заболевании выявляются узловатое утолщение плевры, утолщение медиастинальной плевры, утолщение париетальной плевры более 1 см и тотальное утолщение плевры. КТ позволяет определить плевральный выпот любой локализации, отличать эмпиему плевры с бронхоплевральной фистулой от абсцесса легких. Это особенно ценно при обследовании и ведении больных с отграниченным плевральным выпотом. Отграниченные выпоты на компьютерных томограммах имеют вытянутую форму с гладкими контурами и относительно гомогенную структуру (рис. 13.16). УЗИ и КТ дают возможность определения наиболее оптимального места и направления для установки дренажа.
Показано, что КТ превосходит обычную рентгенографию органов грудной клетки при дифференцировании патологии плевры и легочной паренхимы.
АСПИРАЦИЯ ПЛЕВРАЛЬНОЙ ЖИДКОСТИ
После подтверждения факта наличия плеврального выпота, по данным клинического обследования и методов визуализации, следующим диагностическим шагом является выполнение диагностической аспирации плевральной жидкости (торакоцентеза) (уровень убедительности рекомендаций - II, уровень достоверности доказательств - B). Образец плевральной жидкости для диагностики следует собирать тонкой полой иглой (21G). Жидкость помещают в стерильную пробирку и бутылку (как для посева крови) и исследуют содержание белка, ЛДГ, рН, окрашивают по Граму и для выявления кислотоустойчивых палочек проводят цитологическое и микробиологическое исследования. Это основные исследования, по результатам которых планируют дальнейшее обследование больного. Аспирация плевральной жидкости может проводиться в клинике или у постели больного, хотя при небольших объемах плеврального выпота часто требуется рентгенологический контроль. Полученную плевральную жидкость разливают на три порции в стерильные пробирки для отправки на микробиологическое, биохимическое и цитологическое исследования. Необходимо подчеркнуть, что проведение диагностической плевральной пункции может быть выполнено и у больных, находящихся на ИВЛ, по данным ряда исследований. Риск осложнений у таких больных невысок (пневмоторакс - у 7%), однако данная процедура позволяет уточнить диагноз у 45% больных и назначить адекватную терапию у 33% больных.
Микробиологическое исследование осадка плевральной жидкости с окраской по Граму необходимо во всех случаях, особенно при подозрении на парапневмонический выпот. Информативность посевов повышается, если жидкость транспортируют в лабораторию в бутылках для посевов крови, особенно при наличии анаэробных возбудителей. Транспортировка жидкости с добавлением цитрата предотвращает свертывание, что используется в некоторых лабораториях.
АНАЛИЗ ПЛЕВРАЛЬНОЙ ЖИДКОСТИ
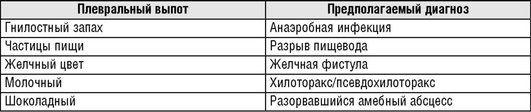
После аспирации плевральной жидкости следует оценить ее внешний вид и запах. При анаэробной инфекции появляется неприятный запах, что может помочь в выборе антибиотика. Плевральная жидкость может быть серозной, с примесью крови, либо полностью геморрагической или гнойной. Если плевральная жидкость мутная или молочного цвета, ее нужно центрифугировать. Если супернатант прозрачный, мутность жидкости может быть обусловлена клеточным детритом, при этом высока вероятность эмпиемы. Если супернатант мутный, это может быть при высоком содержании липидов, что встречается при хилотораксе или псевдохилотораксе. В табл. 13.52 представлена характеристика внешнего вида плевральной жидкости при различных заболеваниях плевры.
|
При примеси крови в плевральной жидкости следует определить гематокрит, особенно если есть сомнения о наличии гемоторакса. Если гематокрит превышает половину величины гематокрита периферической крови пациента, это признак гемоторакса. Если гематокрит плевральной жидкости менее чем 1%, примесь крови в плевральной жидкости не имеет значения. Выраженный геморрагический характер плевральной жидкости обычно встречается при злокачественных поражениях, ТЭЛА с инфарктом легкого, травме, доброкачественных плевральных выпотах при асбестозе и синдроме посткардиального повреждения.
ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ ЭКССУДАТА И ТРАНССУДАТА
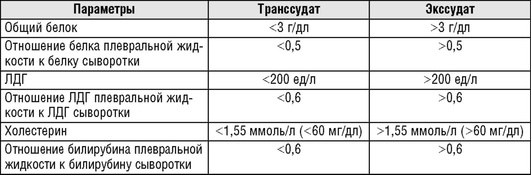
Классический способ отличить транссудат от экссудата - измерение концентрации белка в плевральной жидкости: экссудат содержит более 30 г/л белка, транссудат - менее 30 г/л белка. Однако следует с осторожностью интерпретировать эти результаты, если у больного изменен уровень сывороточного белка. К сожалению, плевральная жидкость часто имеет концентрацию белка, близкую к 30 г/л, что затрудняет дифференциальную диагностику. В таких случаях измеряют концентрацию белка и ЛДГ в сыворотке и плевральной жидкости, что позволяет применить критерии Лайта (табл. 13.53) для более точной диагностики.
|
Плевральная жидкость является экссудатом, если присутствуют один и более из критериев Лайта. Чувствительность критериев Лайта составляет 98%, специфичность 77%, общая аккуратность 95%. Недостаток критериев Лайта состоит в том, что они иногда определяют плевральный выпот у больного с левожелудочковой недостаточностью, получающего терапию мочегонными, как экссудат. В данных обстоятельствах следует учитывать клинические данные. Более полные критерии дифференциальной диагностики транссудатов и экссудатов представлены в табл. 13.54.
|
ЦИТОЛОГИЧЕСКИЙ И БИОХИМИЧЕСКИЙ СОСТАВ ПЛЕВРАЛЬНОЙ ЖИДКОСТИ
Преобладание в плевральной жидкости нейтрофилов говорит в пользу острого заболевания плевры (уровень убедительности рекомендаций - III, уровень достоверности доказательств - С). Если при этом определяется затемнение в легочной ткани, наиболее вероятным диагнозом является парапневмонический выпот либо ТЭЛА с инфарктом легкого. При отсутствии затемнения в легочной ткани наиболее часто диагностируется ТЭЛА, вирусные инфекции, острый туберкулез либо доброкачественный плевральный выпот при асбестозе.
Эозинофильный плевральный выпот диагностируется при наличии 10% и более эозинофилов в плевральной жидкости. Эозинофилия плевральной жидкости мало используется в дифференциальной диагностике плевральных выпотов. Доброкачественная этиология включает парапневмонический выпот, туберкулез, лекарственно-индуцированный плеврит, доброкачественный выпот при асбестозе, инфаркт легкого и паразитарные заболевания. Часто это результат попадания воздуха или крови в плевральную полость. Однако частой причиной эозинофильного выпота являются и злокачественные заболевания.
Если в клеточном составе плевральной жидкости преобладают лимфоциты, наиболее вероятными диагнозами являются туберкулез и злокачественные поражения. Высокий лимфоцитоз в плевральной жидкости увеличивает вероятность туберкулезного плеврита, но в 10% туберкулезных плевральных выпотов преобладают нейтрофилы. Лимфоцитарный плевральный выпот также могут вызвать лимфома, саркоидоз, ревматические заболевания, хилоторакс.
Снижение рН плевральной жидкости менее 7,2 при нормальном рН крови наблюдается при тех же заболеваниях, что и низкий уровень глюкозы в плевральной жидкости. рН менее 7,2 свидетельствует о значительном накоплении ионов водорода, поскольку нормальный уровень рН около 7,6 связан с накоплением бикарбонатов в плевральной полости. Основное клиническое значение плеврального рН состоит в выявлении инфекционного воспаления плевры. К другим заболеваниям, вызывающим экссудативный плевральный выпот с низким рН, относятся коллагеновые сосудистые заболевания (в частности, ревматоидный артрит), разрывы пищевода и злокачественные новообразования.
Уровень глюкозы в плевральной жидкости менее 3,3 ммоль/л обнаруживается при плевральных экссудатах при эмпиеме, ревматических заболеваниях, волчанке, туберкулезе, злокачественных опухолях или разрывах пищевода (табл. 13.55) (уровень убедительности рекомендаций - III, уровень достоверности доказательств - С). Самая низкая концентрация глюкозы выявляется при ревматоидных выпотах и эмпиеме. При инфекционном поражении плевры рН более информативен, чем глюкоза. Ревматоидный артрит редко бывает причиной выпота, если уровень глюкозы в плевральной жидкости выше 1,6 ммоль/л.
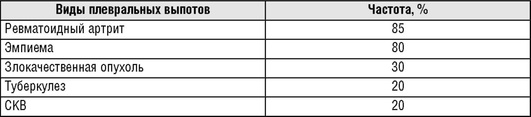 |
|---|
Уровень амилазы в плевральной жидкости помогает оценить экссудативный выпот. Амилаза плевральной жидкости считается повышенной, если она превышает верхний предел нормы для амилазы сыворотки или если соотношение амилазы плевральной жидкости к амилазе сыворотки более 1,0. Это является основанием заподозрить ОП, образование псевдокист в поджелудочной железе, разрывы пищевода, внематочную беременность с разрывом трубы или злокачественное заболевание плевры (особенно аденокарциному). Изоферментный анализ помогает поставить диагноз при подозрении на разрыв пищевода, так как при этом повышается уровень амилазы слюны. Если амилаза слюны повышена, но нет признаков разрыва пищевода, наиболее вероятным диагнозом является злокачественная опухоль. При плевральном выпоте, обусловленном патологией поджелудочной железы, в плевральной жидкости обычно определяется панкреатическая амилаза.
При подозрении на злокачественное поражение плевры цитологическое исследование плевральной жидкости является быстрым и минимально инвазивным диагностическим методом. Чувствительность варьирует от 40 до 87% со средним значением около 60%.
ИНВАЗИВНЫЕ ИССЛЕДОВАНИЯ
Для «слепой» чрескожной биопсии плевры чаще всего используют иглу Абрамса. Необходимо как минимум 4 фрагмента ткани для оптимальной точности диагноза из одного участка, так как биопсии из разных мест не повышают процент положительных результатов. Осложнения биопсии иглой Абрамса - локальная болезненность в месте прокола (1-15%), пневмоторакс (3-15%), вазовагальные реакции (1-5%), гемоторакс (менее 2%), локальная гематома в месте прокола (менее 1%), кратковременная лихорадка (менее 1%) и очень редко летальный исход из-за кровотечения. При развитии пневмоторакса только в 1% случаев требуется дренирование плевральной полости.
КТ грудной клетки с контрастным усилением у пациента с плевральным выпотом часто выявляет локальные изменения плевры. При проведении эксцизионной биопсии под имидж-контролем можно получить биоптат из этого измененного участка плевры, что повышает диагностическую точность в выявлении злокачественных поражений плевры по сравнению со «слепой» биопсией. Эта методика особенно рекомендуется у больных, которым невозможно выполнить торакоскопию.
Торакоскопия обычно применяется, когда менее инвазивные методики (торакоцентез, чрескожная закрытая биопсия плевры) не дают диагностической информации. Злокачественные заболевания плевры выявляются при торакоскопии в 66% у больных с предшествующей неинформативной закрытой биопсией плевры и в 69% с двумя отрицательными результатами цитологического исследования плевральной жидкости. Наиболее частыми побочными эффектами торакоскопии являются подкожная эмфизема (6,9%), нарушения сердечного ритма (0,35%), воздушная эмболия (1 случай).
СПЕЦИАЛЬНЫЕ ИССЛЕДОВАНИЯ
Парапневмонический выпот и эмпиема плевры
Около 55% всех случаев пневмоний, требующих госпитализации больных в стационар, сопровождается развитием выпота в плевральной полости. Парапневмонические плевральные выпоты могут значительно различаться по тяжести течения, варьируя от неосложненного выпота до развития эмпиемы плевры. Некоторые формы пара-пневмонического выпота не требуют специальной терапии, кроме антибактериальной, в то время как при осложненном течении плеврита может потребоваться хирургическое вмешательство. Условно парапневмонический выпот можно разделить на три стадии: неосложненный парапневмонический выпот; осложненный парапневмонический выпот; эмпиема плевры.
Неосложненный парапневмонический выпот представляет собой стерильный экссудат, который имеет нейтрофильный характер (число нейтрофилов обычно превышает 10 ×103/мл), не требует проведения специального лечения и процедур и исчезает по мере разрешения пневмонии.
Осложненный парапневмонический выпот связан с инвазией инфекционного агента в плевральную полость и также является нейтрофильным экссудатом. Бактерии приводят к метаболизму глюкозы по анаэробному пути, вследствие чего происходит снижение концентрации глюкозы и развитие ацидоза плевральной жидкости, а в результате лизиса лейкоцитов увеличивается концентрация ЛДГ выпота. Так как клиренс бактерий из плевральной полости происходит довольно быстро, а также больные получают антибактериальную терапию, осложненный парапневмонический выпот чаще всего оказывается стерильным. Персистирующее воспаление приводит к отложению фибрина на висцеральных и париетальных листках плевры, что может приводить к развитию спаечного процесса и осумкования выпота.
Эмпиема плевры определяется как наличие гноя в плевральной полости. Данная стадия парапневмонического выпота характеризуется высокой концентрацией лейкоцитов - более 25 × 103/мл (что приводит к макроскопической картине гнойного выпота) - и бактерий, легко выявляемых при окраске по Граму. Гнойный выпот практически всегда сопровождается формированием фибриновых сгустков и мембран на плевральных листках, осумкованием выпота, кроме того, на поздних этапах (2-3-я неделя) происходит миграция фибробластов в фибриновые наложения, что ведет к организации плевральной полости. Эмпиема требует обязательного проведения дренирования плевральной полости и часто - хирургической декортикации плевры.
К развитию осложненных плевральных выпотов и эмпиемы чаще всего предрасполагает наличие таких фоновых заболеваний, как СД, алкоголизм, ХОБЛ, бронхоэктатическая болезнь, ревматоидный артрит; у мужчин эти формы плеврита встречаются примерно в два раза чаще.
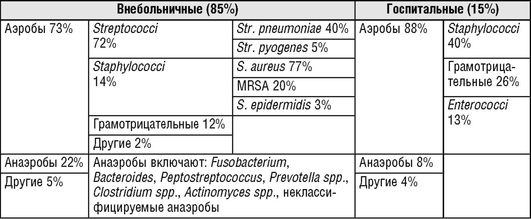
Микробиология парапневмонических выпотов отражает спектр причинных факторов пневмоний. Структура патогенов, вызывающих парапневмонический плеврит, претерпела заметные изменения за последние годы, что, возможно, связано с использованием АМП для терапии пневмоний (табл. 13.56). В настоящее время основной причиной осложненных парапневмонических выпотов являются аэробные бактерии - как грамположительные
(Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococous aureus), так и грамотрицательные (Escherichia coli, Haemophilus influenzae, Klebsiella spp., Pseudomonas spp.).
Анаэробные микроорганизмы являются причиной до 36-76% всех эмпием, чаще всего в ассоциации с аэробами, однако около 22% парапневмонических выпотов вызвано исключительно анаэробами. Наиболее частыми причинными анаэробными микроорганизмами осложненных парапневмонических выпотов являются Prevotella spp., Fusobacterium nucleatum, Streptococcus intermedius, Bacteroides spp.
|
ПЛЕВРАЛЬНЫЙ ВЫПОТ ПРИ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ
Плевральный выпот небольшого объема сопровождает до 40% случаев ТЭЛА. Среди них 80% выпотов являются экссудатами, 20% - транссудатами; в 80% в плевральной жидкости присутствует примесь крови. Содержание эритроцитов в плевральной жидкости более 100 000/мм3 требует исключения злокачественного заболевания, инфаркта легкого или травмы. Меньшее количество эритроцитов не имеет диагностического значения. Выпоты, вызванные ТЭЛА, не обладают специфическими чертами, и, таким образом, диагноз устанавливается на основании клинических данных, которые позволяют заподозрить ТЭЛА с высокой вероятностью.
ТУБЕРКУЛЕЗНЫЙ ПЛЕВРИТ
Обнаружение кислотоустойчивых палочек в мазках происходит только в 10-20% случаев туберкулезного плеврита, посев плевральной жидкости выявляет микобактерии туберкулеза только в 25-50%. Добавление гистологического исследования и посева биоптата плевры улучшает диагностику туберкулеза до 90%. При туберкулезе, по сравнению с экссудатами другой этиологии, в плевральной жидкости повышается уровень аденозиндезаминазы. Однако этот показатель также повышается при эмпиеме, ревматоидном плеврите и злокачественных заболеваниях, что снижает ценность этого теста в странах с низкой заболеваемостью туберкулезом. Уровень аденозиндезаминазы не повышается, если пациент имеет одновременно ВИЧ-инфекцию и туберкулез.
ПЛЕВРАЛЬНЫЙ ВЫПОТ ПРИ ВИЧ-ИНФЕКЦИИ
Плевральный выпот выявляется у 7-27% госпитализированных больных с ВИЧ-инфекцией. Основные причины поражения плевры у таких больных - саркома Капоши, парапневмонические выпоты, туберкулез. В одном проспективном исследовании с участием 58 больных с ВИЧ-инфекцией и рентгенологическими признаками плеврального выпота причинами выпота были в 1/3 случаев саркома Капоши, в 28% - парапневмонический выпот, в 14% - туберкулез, в 10% - пневмония, вызванная
Pneumocystis jirovecii, в остальных 7% - лимфома.
ХИЛОТОРАКС И ПСЕВДОХИЛОТОРАКС
Истинный хилоидный выпот возникает в результате разрыва грудного протока или его ветвей, что ведет к попаданию лимфы в плевральную полость. Примерно 50% таких случаев обусловлены злокачественным заболеванием (в основном лимфомой), 25% - травмой (особенно при хирургических вмешательствах), остальные случаи обусловлены разнообразными заболеваниями, такими как туберкулез, саркоидоз, амилоидоз.
Хилоторакс следует отличать от псевдохилоторакса, или «холестеринового плеврита», который возникает в результате скопления кристаллов холестерина в длительно существующем плевральном выпоте. В этих случаях плевра, как правило, значительно утолщена и фиброзирована. Основными причинами псевдохилоторакса являются туберкулез и ревматоидный артрит. Хилоторакс и псевдохилоторакс диагностируются по анализу липидов в плевральной жидкости (табл. 13.57).
В редких случаях при эмпиеме может встречаться выпот молочного цвета, похожий на хилоторакс. Эти состояния различают при центрифугировании, после чего при эмпиеме образуется прозрачный супернатант, а клеточная масса оседает. Хилезная жидкость после центрифугирования сохраняет молочный вид.
|
Лечение
Задачи терапии: лечение основного заболевания, удаление плеврального выпота, профилактика осложнений.
Транссудаты обычно не требуют механического удаления жидкости из плевральной полости, за исключением случаев массивных плевральных выпотов, приводящих к выраженной одышке (уровень убедительности рекомендаций - II, уровень достоверности доказательств - С). В большинстве случаев главной терапией транссудатов является терапия, направленная на лечение основного заболевания, например улучшение сократимости миокарда и коррекция водного обмена при застойной СН. Терапия диуретиками и раствором альбумина достаточно эффективна у больных с транссудатами на фоне гипопротеинемии. Коррекция тяжелой гипопротеинемии должна осуществляться постепенно, для того чтобы предупредить быстрое увеличение объема жидкости внутрисосудистого сектора. Длительные инфузии фуросемида более эффективны, чем его болюсное введение, однако необходима коррекция потери калия и магния. При тяжелых гипопротеинемических состояниях рекомендовано назначение спиронолактона.
Особую проблему представляет терапия больных с парапневмоническим плевральным выпотом и эмпиемой плевры.
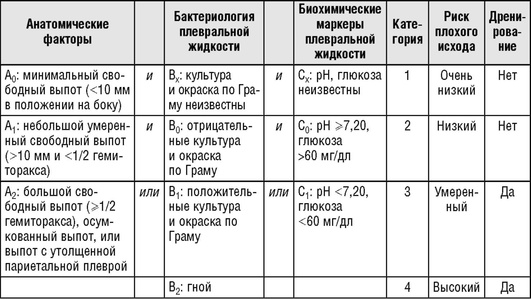
Терапия парапневмонического плеврального выпота прежде всего зависит от его стадии и риска неблагоприятного исхода. В 2000 г. American College of Chest Physicians была предложена классификация парапневмонических плевральных выпотов на основе анатомических характеристик плеврального выпота (А), бактериологии плевральной жидкости (B) и биохимического анализа плевральной жидкости (С) (табл. 13.58). На основании данной классификации АВС все парапневмонические выпоты можно разделить на 4 прогностические категории и определить показания к установке дренажной трубки (требуется у больных с 3-й и 4-й категориями риска).
При неосложненном парапневмоническом плевральном выпоте показано наблюдение и АМТ (уровень убедительности рекомендаций - II, уровень достоверности доказательств - B). Больным с ВП назначаются цефалоспорины второй или третьей генерации или ингибиторозащищенные пенициллины. При подозрении на анаэробную флору применяется комбинированная терапия с метронидазолом или клиндамицином, либо ингибиторозащищенные пенициллины, либо карбапенемы (табл. 13.59). К антибиотикам, хорошо проникающим в плевральную полость, относятся пенициллины, метронидазол, цефтриаксон, клиндамицин, ванкомицин, и практически не пенетрируют в полость плевры аминогликозиды. Доказательств эффективности прямых инстилляций антибактериальных препаратов в плевральную полость на сегодняшний день нет.
При осложненном плевральном выпоте показано проведение торакоцентезов при помощи повторных пункций или установка дренажной трубки (уровень убедительности рекомендаций - II, уровень достоверности доказательств - B). При эмпиеме метод выбора - проведение дренирования плевральной полости.
|
|
Дренажная трубка устанавливается обычно под контролем рентгеноскопического исследования, УЗИ или КТ-исследования. При наличии нескольких осумкованных полостей может потребоваться несколько дренажных трубок. Предпочтение имеют трубки большого диаметра (24-36F), особенно при наличии вязкого экссудата. Обычно используют отрицательное давление 10-20 см вод. ст. Правильная установка трубки приводит к быстрой эвакуации жидкости и расправлению легкого. При уменьшении плеврального отделяемого до 50 мл в сутки дренажную трубку удаляют.
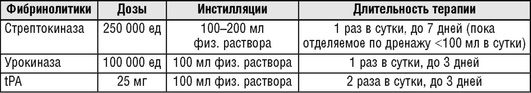
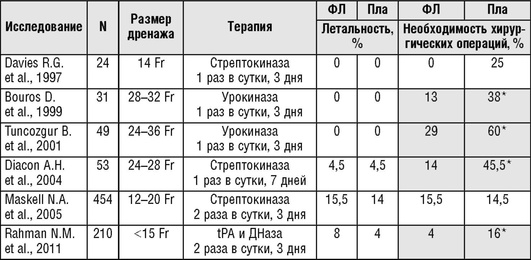
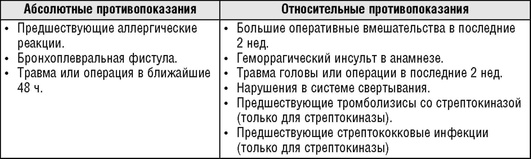
При наличии спаечного процесса в плевральной полости и осумкованных полостей адекватное дренирование плевральной полости может быть достигнуто при введении в нее фибринолитиков (уровень убедительности рекомендаций - II, уровень достоверности доказательств - A), которые позволяют растворить фибриновые сгустки и мембраны. Чаще всего используют стрептокиназу, урокиназу или альтеплазу (tPA), препараты вводят в дозах 250 000 единиц и 100 000 единиц и 25 мг соответственно в 100-200 мл изотонического раствора натрия хлорида, после чего дренажную трубку перекрывают на 2-4 ч и затем производят удаление плевральной жидкости (табл. 13.60). В зависимости от клинического ответа инстилляции фибринолитиков повторяют в течение 3-14 дней. Интраплевральное введение фибринолитиков не приводит к развитию системного фибринолиза. Эффективность фибролитической терапии при осумкованных плевральных выпотах составляет 70-90%. Согласно данным большинства РКИ, посвященных оценке эффективности фибринолитической терапии при эмпиеме плевры, внутриплевральное введение фибринолитиков позволяет значительно уменьшить число хирургических вмешательств (табл. 13.61). Противопоказания к фибринолитической терапии представлены в табл. 13.62.
|
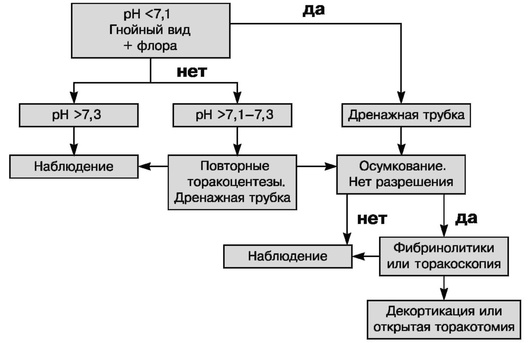
Торакоскопия является методом, альтернативным фибринолитикам для терапии осумкованных плевральных выпотов (уровень убедительности рекомендаций - II, уровень достоверности доказательств - С). Эффективность торакоскопии в дренировании эмпиемы плевры достигает 90%. При отсутствии эффекта от дренирования плевральной полости, фибринолитической терапии и торакоскопии прибегают к хирургическому дренированию - открытой торакотомии и декортикации легкого. Хирургические методы имеют высокую эффективность (до 95%), однако сопряжены с определенным операционным риском. Алгоритм ведения больных с парапневмоническим плевральным выпотом и эмпиемой плевры представлен на рис. 13.17.
|
Примегание. ФЛ - фибринолитик; Пла - плацебо. * р <0,05.
|
Прогноз
Прогноз при плевральных выпотах зависит в основном от их природы. Однако можно предположить, что появление плеврального выпота ухудшает прогноз больных. Плевральный выпот является одним из самостоятельных прогностических факторов при ВП и входит в состав некоторых прогностических индексов (например, PSI). В ряде исследований показано, что появление плеврального выпота является фактором плохого прогноза больных, например у больных с легионеллезной пневмонией и у больных с ВИЧ-инфекцией, госпитализированных в стационар.
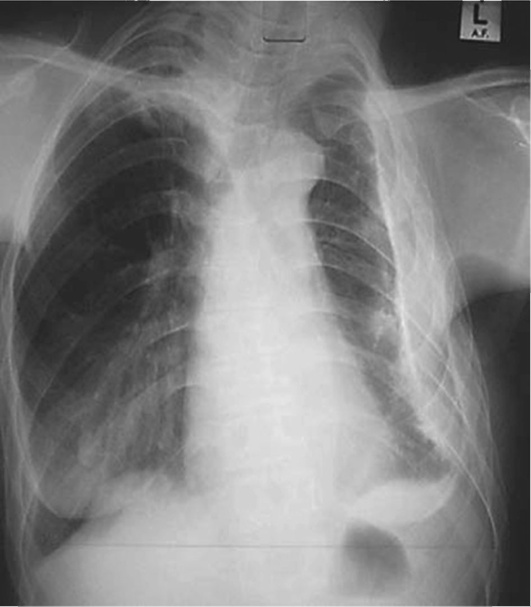
Несвоевременное и/или неполноценное лечение плевральных выпотов приводит к развитию хронических изменений функции внешнего дыхания по рестриктивному типу и может быть причиной развития хронической (каркасной) ДН (рис. 13.18).
Список литературы
-
Bhatnagar R., Maskell N.A. Treatment of complicated pleural effusions in 2013 // Clin. Chest Med. 2013. Vol. 34. P. 47-62.
-
Bielsa S., Salud A., Martinez M. et al. Prognostic significance of pleural fluid data in patients with malignant effusion // Eur. J. Int. Med. 2008. Vol. 19. P. 334-336.
-
Bowling M., Chatterjee A., Conforti J. Perceptions vs. reality: measuring of pleural fluid pH in North Carolina // NC Med. J. 2009. Vol. 70. P. 9-13.
-
Davies C., Gleeson F., Davies R. BTS guidelines for the management of pleural infection // Thorax. 2003. Vol. 58, suppl. II. P. 18-28.
-
Davies H.E., Davies R.J., Davies C.W. Management of pleural infection in adults: British Thoracic Society pleural disease guideline 2010 // Thorax. 2010. Vol. 65, suppl. 2. P. 41-53.
-
Heffner J., Klein J. Recent advances in the diagnosis and management of malignant pleural effusions // Mayo Clin. Proc. 2008. Vol. 83. P. 235-250.
-
Janda S., Swiston J. Intra-pleural fibrinolytic therapy for treatment of adult parap-neumonic effusions and empyemas: a systematic review and meta-analysis // Chest. 2012. Vol. 142. P. 401-411.
-
Light R.W. Pleural controversy: optimal chest tube size for drainage // Respirology. 2011. Vol. 16. P. 244-248.
-
Sahn S. The value of pleural fluid analysis // Am. J. Med. Sci. 2008. Vol. 335. P. 7-15.
-
Ahmed A.E., Yacoub T.E. Empyema thoracis // Clin. Med. Insights Circ. Respir. Pulm. Med. 2010. Vol. 4. P. 1-8.