Неврология : национальное руководство : в 2-х т. / под ред. Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой. - 2-е изд., перераб. и доп. - Москва : ГЭОТАР-Медиа, 2022. - Т. 1. - 880 с. - (Серия "Национальные руководства"). - ISBN 978-5-9704-6672-8. |
Аннотация
Во втором издании национального руководства значительное внимание уделено современным методам профилактики, диагностики, фармакотерапии заболеваний нервной системы, а также немедикаментозным методам их лечения. Отдельные разделы посвящены клиническим рекомендациям по основным синдромам и заболеваниям.
В подготовке настоящего издания принимали участие ведущие специалисты-неврологи.
Руководство предназначено неврологам, нейрохирургам, кардиологам, терапевтам, врачам общей практики и представителям других медицинских дисциплин, а также студентам старших курсов медицинских высших учебных заведений, интернам, ординаторам, аспирантам.
12.2.2. Геморрагический инсульт
Е.И. Гусев, В.И. Скворцова, А.Н. Коновалов, О.Б. Белоусова, М.Ю. Мартынов
Геморрагический инсульт — любое спонтанное (нетравматическое) кровоизлияние в полость черепа. Однако термин «геморрагический инсульт» в клинической практике используют, как правило, для обозначения внутримозгового кровоизлияния, обусловленного наиболее распространенными сосудистыми заболеваниями головного мозга: гипертонической болезнью, атеросклерозом и амилоидной ангиопатией.
12.2.2.1. Этиология и патогенез
Причиной геморрагического инсульта могут быть различные заболевания и патологические состояния: АГ различного генеза, амилоидная ангиопатия, аневризмы и сосудистые мальформации головного мозга, болезни крови (эритремия, тромбофилии), васкулиты, системные заболевания соединительной ткани. Кровоизлияния могут возникать при лечении антикоагулянтами и фибринолитическими средствами, а также при злоупотреблении другими препаратами, в частности психоактивными и наркотическими веществами, например амфетамином, кокаином и другими.
Наиболее частыми причинами геморрагического инсульта бывают гипертоническая болезнь и амилоидная ангиопатия. Патогенез кровоизлияния при этих заболеваниях связан с патологическими изменениями артерий и артериол паренхимы мозга, поэтому наиболее типичны для них внутримозговые кровоизлияния с формированием внутримозговых гематом.
12.2.2.2. Эпидемиология
Геморрагический инсульт составляет 12–15% всех церебральных инсультов. По данным Российской национальной ассоциации по борьбе с инсультом (НАБИ), в России ежегодно регистрируют около 40 тыс. кровоизлияний в мозг.
Полиэтиологичность геморрагического инсульта обусловливает возможность его развития в любом возрасте, включая детский, однако, если учитывать наиболее распространенные этиологические факторы, наиболее часто кровоизлияние в головной мозг переносят в возрасте 50–70 лет.
12.2.2.3. Классификация
Внутричерепные кровоизлияния в зависимости от локализации излившейся крови подразделяют на внутримозговые (паренхиматозные), субарахноидальные, вентрикулярные и смешанные (паренхиматозно-вентрикулярные, субарахноидально-паренхиматозные, субарахноидально-паренхиматозно-вентрикулярные и др.). Вид кровоизлияния в значительной степени зависит от этиологического фактора.
12.2.2.4. Внутримозговые гематомы
Коды по МКБ-10: I61.0–I61.9. Внутримозговое кровоизлияние.
Классификация
Внутримозговые гематомы, помимо этиологии, подразделяют по локализации и объему. В подавляющем большинстве случаев (до 90%) гематомы локализуются в супратенториальных отделах мозга. Различают лобарные, латеральные, медиальные и смешанные внутримозговые гематомы (рис. 12.1).
-
Лобарными называют кровоизлияния, при которых кровь не выходит за пределы коры и белого вещества соответствующей доли или долей головного мозга.
-
Кровоизлияния в подкорковые ядра (кнаружи от внутренней капсулы) принято обозначать как латеральный инсульт, а кровоизлияния в таламус — как медиальный инсульт (кнутри от внутренней капсулы).
-
На практике чаще всего встречают смешанные внутримозговые гематомы, когда кровь распространяется в пределах нескольких анатомических структур.
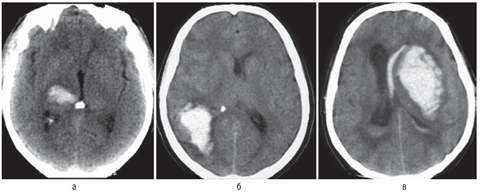
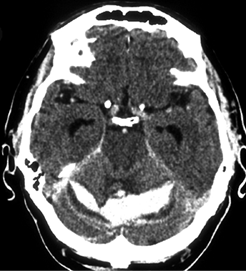
Гематомы задней черепной ямки составляют около 10% всех внутримозговых гематом. Чаще всего они расположены в мозжечке, реже — в стволе головного мозга, где их излюбленной локализацией бывает мост (рис. 12.2).
Кровоизлияния в медиальные отделы больших полушарий мозга, а также гематомы задней черепной ямки приблизительно в 30% случаев сопровождаются прорывом крови в желудочковую систему.
Объем внутримозговых гематом при геморрагическом инсульте может варьировать в очень широких пределах — от нескольких миллилитров до 100 мл и более (см. рис. 12.1, 12.2). Существуют различные способы определения объема гематомы. Наиболее простой из них — способ расчета объема по данным КТ с использованием следующей формулы: максимальная высота × максимальная длина × максимальная ширина : 2. Распределение гематом по объему весьма условно. Принято деление на небольшие (до 20–30 мл), средние (до 50–60 мл) и большие (>50–60 мл) гематомы. Небольшие, средние и большие гематомы встречаются приблизительно с одинаковой частотой.
Механизмы развития кровоизлияния
Геморрагический инсульт чаще развивается в результате разрыва сосуда, который обычно происходит при повышении АД и приводит к образованию гематомы. К этому предрасполагают значительное истончение и расслоение стенки измененного сосуда, образование милиарных аневризм, врожденные аневризмы, артериовенозные и другие сосудистые аномалии, изменения стенки сосуда при васкулитах. При АГ аневризмы формируются на протяжении длительного времени (многих месяцев и лет) и чаще локализуются в местах ветвления сосудов в подкорковых структурах, что обусловлено отхождением глубоких ветвей от основного ствола средней мозговой артерии почти под прямым углом. Значительно реже возникают кровоизлияния при повышении проницаемости сосудистой стенки. Диапедезное кровотечение — следствие вазомоторных нарушений, длительного спазма сосуда, приводящего к замедлению в нем кровотока, и последующей его дилатации. При этом повышается проницаемость стенки сосуда, из него выпотевают плазма и форменные элементы крови. Мелкие периваскулярные кровоизлияния, сливаясь, образуют небольшие или обширные геморрагические очаги.
Патофизиология повреждения вещества головного мозга
Разрыв сосуда и выход крови за его пределы запускает каскад событий, имеющих временную и пространственную характеристику. Большую роль в этих событиях играют процессы, связанные с разрушением эритроцитов, высвобождением гемоглобина и образованием продуктов его превращения. Разрушение эритроцитов, выход из них свободного двухвалентного железа (Fe2+) и переход его в трехвалентную форму (Fe3+), а также образование тромбина способствуют усилению локального окислительного стресса, развитию локальных метаболических нарушений. Кроме этого, оксигемоглобин из лизировавшихся эритроцитов превращается в деокси- и метгемоглобин, которые являются токсичными для окружающего вещества головного мозга. Поражение вещества головного мозга также происходит вследствие его сдавления гематомой и повышения ВЧД. Вследствие механического и рефлекторного сдавления сосудов при кровоизлиянии могут развиваться преходящие ишемические изменения прилежащих областей вещества головного мозга, что способствует усилению перифокального отека и метаболических расстройств.
Клиническая картина
Клиническая картина внутримозгового кровоизлияния довольно типична. Заболевание имеет острое внезапное начало, часто на фоне высокого АД. Характерны сильная ГБ, головокружение, тошнота и рвота, быстрое развитие очаговых симптомов, за этим следует прогрессирующее снижение уровня бодрствования — от умеренного оглушения вплоть до коматозного состояния. Угнетению сознания может предшествовать короткий период психомоторного возбуждения. Субкортикальные кровоизлияния могут начаться с эпилептического приступа.
Очаговые неврологические симптомы зависят от локализации гематомы. Типичными очаговыми симптомами с учетом наиболее частой локализации внутримозговых гематом бывают гемипарезы, нарушения речи и чувствительности, лобные симптомы в виде нарушений памяти, критики, поведения.
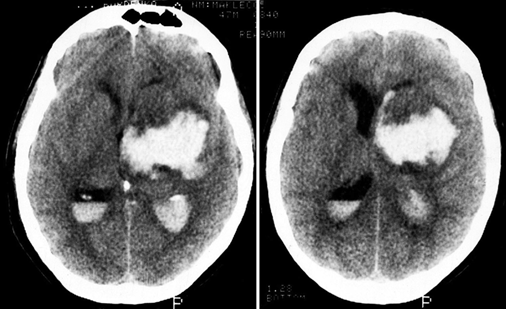
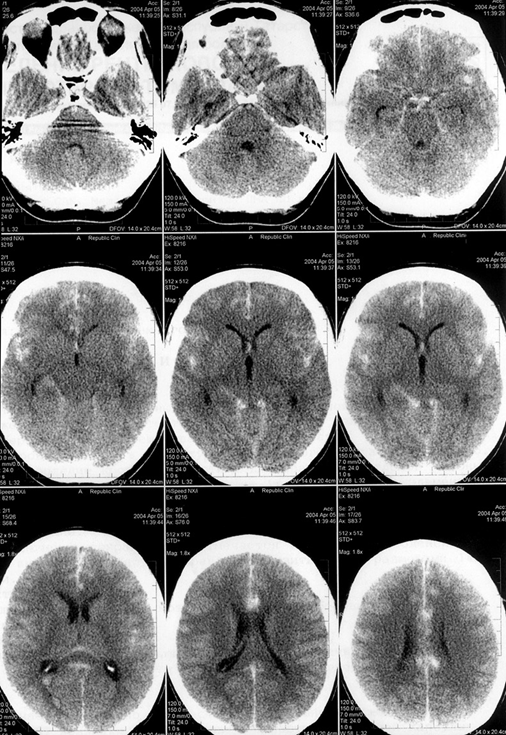
Тяжесть состояния больного непосредственно после кровоизлияния и в последующие дни определяется выраженностью общемозговых и дислокационных симптомов, в свою очередь обусловленных объемом внутримозговой гематомы и ее локализацией. При обширных кровоизлияниях и кровоизлияниях глубинной локализации в клинической картине довольно быстро появляется вторичная стволовая симптоматика, обусловленная дислокацией мозга. Для кровоизлияний в ствол мозга и обширных гематом мозжечка характерно быстрое нарушение сознания и витальных функций. Наиболее тяжело протекают кровоизлияния с прорывом в желудочковую систему (рис. 12.3). В большинстве случаев для них характерны появление горметонических судорог, гипертермии, менингеальных симптомов, быстрое угнетение сознания, развитие стволовых симптомов. В то же время, если не происходит окклюзии излившейся кровью ликворопроводящих путей, в частности сильвиева водопровода и IV желудочка, попадание крови в ликворную систему может не сопровождаться клиническим ухудшением.
Выраженность очаговых симптомов при паренхиматозных кровоизлияниях зависит главным образом от локализации гематомы. Небольшие гематомы в области внутренней капсулы могут приводить к значительно более выраженному очаговому синдрому, чем гематомы большего объема, расположенные в функционально менее значимых отделах мозга.
Течение
Наиболее тяжелым периодом кровоизлияния, особенно при обширных гематомах, бывают первые 2–3 нед болезни. Тяжесть состояния больного на этом этапе обусловлена как самой гематомой, так и нарастающим в первые дни заболевания отеком мозга, что проявляется в развитии и прогрессировании общемозговых и дислокационных симптомов. Отек и дислокация мозга становятся основной причиной смерти больных в остром периоде заболевания. Для этого периода типичны также присоединение или декомпенсация имевшихся ранее соматических осложнений (пневмония, нарушение функций печени и почек, СД и др.). В связи с обездвиженностью больного большую опасность на этом этапе заболевания представляет тромбоэмболия легочной артерии. К концу 2–3-й недели заболевания у выживших больных начинается регресс общемозговых симптомов, на первый план выходят последствия очагового поражения мозга, в дальнейшем определяющие степень инвалидизации больного.
Диагностика
Основной метод диагностики при остром нарушении мозгового кровообращения — КТ или МРТ. Эти методы позволяют дифференцировать тип инсульта, определить локализацию и объем внутримозговой гематомы, степень сопутствующего отека и дислокации мозга, наличие и распространенность вентрикулярного кровоизлияния. Исследование нужно выполнить как можно раньше, так как его результаты в значительной степени определяют тактику ведения и лечения больного. Необходимы также повторные КТ-исследования, позволяющие проследить эволюцию гематомы и состояние мозговой ткани в динамике. Последнее особенно важно для своевременной коррекции медикаментозной терапии. Оценка данных КТ, как правило, не представляет трудностей независимо от срока, прошедшего после начала заболевания. Трактовка данных МРТ представляется более сложной, что обусловлено изменением МР-сигнала в зависимости от эволюции гематомы. Наиболее частый ошибочный диагноз — «внутримозговая опухоль с кровоизлиянием».
Дифференциальная диагностика
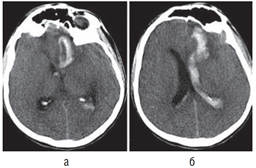
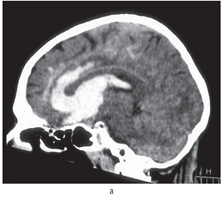
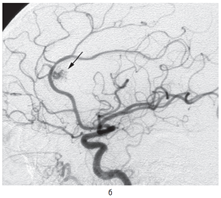
Геморрагический инсульт следует дифференцировать прежде всего от ишемического, составляющего до 80–85% всех инсультов. Поставить точный диагноз необходимо, чтобы как можно раньше начать соответствующую терапию. Дифференциальная диагностика по клиническим данным не всегда возможна, поэтому необходимо госпитализировать больных с диагнозом «инсульт» в стационары, оснащенные КТ- или МРТ-оборудованием. Для ишемического инсульта характерны более медленное нарастание общемозговых симптомов, отсутствие в большинстве случаев менингеальных симптомов, в ряде случаев — наличие предвестников в виде ПНМК, нарушения сердечного ритма в анамнезе. Ликвор при ишемическом инсульте обычно имеет нормальный состав, в то время как при геморрагическом — в большинстве случаев содержит примесь крови. Исключение составляют малые, не сообщающиеся с ликворными путями гематомы, при которых макроскопически ЦСЖ не изменена. Необходимо подчеркнуть, что при общем тяжелом состоянии больного, особенно при наличии стволового синдрома, люмбальную пункцию лучше не делать или выполнять с большой осторожностью, поскольку выведение ликвора может вызвать дислокацию головного мозга. Внутримозговые гематомы гипертонического генеза необходимо также дифференцировать от гематом другой этиологии, а также от кровоизлияний в очаг ишемии или опухоль. Большое значение при этом имеют анамнез заболевания, возраст больного, локализация гематомы в веществе мозга. При кровоизлиянии из аневризмы гематомы имеют типичную локализацию — медиобазальные отделы лобной доли при аневризмах передней мозговой/передней соединительной артерии (рис. 12.4) и базальные отделы лобной и височной долей, прилежащие к сильвиевой щели, при аневризмах внутренней сонной или средней мозговой артерии. При МРТ можно также видеть аневризму или патологические сосуды артериовенозной мальформации (рис. 12.5). При подозрении на разрыв аневризмы или артериовенозной мальформации, на что в первую очередь может указывать молодой возраст больного, необходимо проведение ангиографического обследования.
Лечение
Лечение больных с внутримозговой гематомой может быть консервативным и хирургическим.
Вопрос о тактике лечения необходимо решать на основании результатов комплексной клинико-инструментальной оценки больного и обязательной консультации нейрохирурга.
Медикаментозная терапия
Принципы консервативного лечения больных с внутримозговыми гематомами соответствуют общим принципам лечения больных с любым видом инсульта. Мероприятия по лечению больного с подозрением на внутримозговую гематому нужно начинать на догоспитальном этапе, где следует в первую очередь оценить адекватность внешнего дыхания и сердечно-сосудистой деятельности. При признаках дыхательной недостаточности необходима интубация с подключением ИВЛ. В коррекции состояния сердечно-сосудистой системы наибольшее значение имеет нормализация АД: как правило, у больных с геморрагическим инсультом оно резко повышено.
В стационаре следует продолжить мероприятия по обеспечению адекватного внешнего дыхания и оксигенации крови, нормализации функций сердечно-сосудистой системы, поддержанию водно-электролитного баланса. Важнейшее мероприятие — проведение терапии, направленной на уменьшение отека мозга. Рекомендуют применение препаратов, уменьшающих проницаемость сосудистой стенки. Активные гемостатические средства, особенно у больных с кровоизлиянием, развившимся вследствие АГ, и в сочетании с другими сосудистыми факторами риска, не показаны в связи с высокой вероятностью тромботических осложнений. Необходима профилактика тромбоэмболии. Большое значение имеет тщательный уход за больным.
При коррекции АД следует избегать его резкого и значительного снижения, так как это может привести к снижению перфузионного давления, особенно в условиях внутричерепной гипертензии. Рекомендуют поддерживать среднее АД на уровне 130 мм рт.ст. Для снижения ВЧД используют осмодиуретики в сочетании с салуретиками при условии контроля электролитов крови не реже 2 раз в сут, барбитураты, внутривенное введение коллоидных растворов. Использование глюкокортикоидов неэффективно. Медикаментозную терапию необходимо проводить в условиях мониторинга основных показателей, характеризующих состояние цереброваскулярной системы и жизненно важных функций. Объем мониторинга зависит от степени тяжести больного.
При лечении больного с внутримозговой гематомой необходимо учитывать, что гипертоническая болезнь приводит к поражению не только сосудистой системы мозга, но и других органов и систем. Больные с гипертонической болезнью часто имеют различные сопутствующие заболевания (СД, атеросклероз, ожирение), поэтому для больных с внутримозговой гематомой характерно быстрое присоединение различных соматических осложнений.
Хирургическое лечение
Решение вопроса о показаниях к хирургическому вмешательству по поводу внутримозговой гематомы зависит от многих факторов, наиболее важные из них — объем, локализация излившейся крови и состояние больного. Несмотря на многочисленные исследования, касающиеся целесообразности хирургического лечения внутримозговых гематом, единого мнения по этому вопросу нет. Рандомизированные исследования не смогли доказать преимущества того или иного метода. Нерандомизированные исследования свидетельствуют об эффективности операции при определенных условиях и в определенных группах больных.
При обосновании операции основная цель — спасение жизни больного, поэтому большинство вмешательств выполняют в ближайшие сроки после кровоизлияния. В некоторых случаях удалять гематомы можно, для того чтобы эффективнее устранить очаговые неврологические нарушения. Подобные операции могут быть отсроченными.
Сравнительный анализ результатов консервативного и хирургического лечения показал, что при супратенториальных гематомах объемом до 30 мл хирургическое лечение нецелесообразно независимо от локализации гематомы, так как гематомы небольшого объема редко бывают причиной витальных нарушений. При гематомах объемом более 60 мл исход в целом хуже при консервативном лечении.
У больных с гематомами среднего объема (30–60 мл) наиболее сложно определить показания к операции и выбрать способ хирургического вмешательства.
В этих случаях прогностически значимыми бывают степень нарушения сознания, выраженность дислокационных симптомов, локализация гематомы, выраженность перифокального отека мозга, наличие сопутствующего вентрикулярного кровоизлияния. Противопоказанием к операции считают коматозное состояние, особенно с выраженным нарушением стволовых функций, так как при попытках оперировать таких больных летальность достигает 100%. Неблагоприятна локализация гематом в глубинных структурах.
При гематомах мозжечка показания к операции шире, так как гематомы этой локализации могут приводить к быстрому нарушению витальных функций.
Таким образом, хирургические вмешательства, направленные на удаление внутримозговой гематомы, показаны преимущественно больным с лобарными или латеральными гематомами объемом более 50 мл, а также больным с гематомами мозжечка.
Выбор метода операции зависит прежде всего от локализации и размеров гематомы. Лобарные и латеральные гематомы лучше удалять прямым способом. В последние годы довольно широко применяют также пункционно-аспирационный метод с локальным фибринолизом. При медиальных и смешанных инсультах более щадящим считают стереотаксическое удаление гематом. Вместе с тем при стереотаксическом удалении рецидивы кровотечения возникают чаще, так как в ходе операции невозможно проведение тщательного гемостаза.
Помимо удаления гематом, при геморрагическом инсульте может возникнуть необходимость в дренировании желудочков. Наложение наружных вентрикулярных дренажей показано при массивном вентрикулярном кровоизлиянии, окклюзионной водянке у больных с гематомами мозжечка, а также для контроля ВЧД.
Прогноз
Прогноз при геморрагическом инсульте в целом неблагоприятен. Общая летальность достигает 60–70%, после удаления внутримозговых гематом — около 50%. Основными причинами смерти как оперированных, так и неоперированных больных бывают нарастающий отек и дислокация ствола головного мозга (30–40%). Вторая по частоте причина — рецидив кровоизлияния (10–20%). Примерно 2/3 больных, перенесших инсульт, остаются инвалидами. Основными факторами, определяющими прогноз и исход заболевания, считают объем гематомы, сопутствующий прорыв крови в желудочки, локализацию гематомы в стволе мозга, предшествующий прием антикоагулянтов, предшествующее заболевание сердца, пожилой возраст.
Профилактика
Неблагоприятные исходы геморрагического инсульта еще раз подчеркивают важнейшее значение профилактики заболевания. Основные мероприятия в этом направлении заключаются в том, чтобы как можно раньше выявить и провести систематическое адекватное медикаментозное лечение больных, страдающих гипертонической болезнью, что позволяет уменьшить риск инсульта на 40–50%, а также устранить факторы риска гипертонической болезни и инсульта: курение, прием больших доз алкоголя, СД, гиперхолестеринемию.
12.2.2.5. Субарахноидальное кровоизлияние
Субарахноидальное кровоизлияние — один из видов внутричерепного кровоизлияния, при котором кровь распространяется в субарахноидальном пространстве головного и спинного мозга. Различают субарахноидальное кровоизлияние при ЧМТ и вследствие какой-либо патологии церебральных сосудов. Для обозначения последнего используют термины «спонтанное субарахноидальное кровоизлияние» или «нетравматическое субарахноидальное кровоизлияние».
Коды по МКБ-10: I60.0–I60.9. Субарахноидальное кровоизлияние.
Эпидемиология
По данным регистров инсульта разных стран, заболеваемость субарахноидальным кровоизлиянием составляет 14–20 случаев на 100 тыс. населения в год. Доля субарахноидального кровоизлияния среди других видов инсульта не превышает 5%. Субарахноидальное кровоизлияние может случиться в любом возрасте, однако наиболее часто оно происходит в 40–60 лет.
Этиология
Причины субарахноидального кровоизлияния многообразны, но наиболее часто оно бывает следствием разрыва аневризм церебральных сосудов, на долю которых приходится 70–80% всех субарахноидальных кровоизлияний. Заболевания, при которых возможно развитие субарахноидального кровоизлияния, перечислены ниже.
Когда не удается установить этиологический фактор субарахноидального кровоизлияния, используют понятие «субарахноидальное кровоизлияние неясного генеза». На долю таких кровоизлияний приходится около 15%.
Классификация
Субарахноидальные кровоизлияния классифицируют по этиологическому фактору (см. выше) и по распространенности на основании данных КТ или МРТ. При этом учитывают как массивность кровоизлияния, так и его сочетание с другими компонентами внутричерепного кровоизлияния — паренхиматозным и вентрикулярным. В зависимости от этого фактора выделяют изолированное субарахноидальное кровоизлияние, субарахноидально-паренхиматозное, субарахноидально-вентрикулярное и субарахноидально-паренхиматозно-вентрикулярное кровоизлияния (рис. 12.6). В мировой практике широкое распространение получила классификация субарахноидальных кровоизлияний, предложенная M. Fisher (1980). Она характеризует распространенность субарахноидального кровоизлияния по результатам КТ (табл. 12.1).
Клиническая картина
Субарахноидальное кровоизлияние развивается остро, без каких-либо предвестников, и характеризуется возникновением внезапной интенсивной диффузной ГБ по типу «удара», «растекания горячей жидкости в голове», тошноты, рвоты. Типичны кратковременная утрата сознания и быстрое развитие менингеального синдрома при отсутствии очаговых неврологических расстройств. Длительная утрата сознания свидетельствует о тяжелом кровоизлиянии, как правило, с прорывом крови в желудочковую систему, а быстрое присоединение очаговых симптомов — о субарахноидально-паренхиматозном кровоизлиянии.
| Градация | Кровь по КТ |
|---|---|
1 |
Нет признаков крови |
2 |
Диффузные или вертикальные сгустки толщиной менее 1 мм |
3 |
Локальный сгусток или вертикальные слои толщиной более 1 мм |
4 |
Внутримозговой или внутрижелудочковый сгусток при наличии или отсутствии диффузного субарахноидального кровоизлияния |
Менингеальные симптомы — основной дифференциально-диагностический признак субарахноидального кровоизлияния. В зависимости от массивности субарахноидального кровоизлияния они могут быть выражены в разной степени и сохраняться от нескольких суток до 3–4 нед.
Наряду с развитием неврологической симптоматики субарахноидальное кровоизлияние может сопровождаться различными висцеровегетативными нарушениями.
Наиболее часто в момент кровоизлияния фиксируют повышение АД. Повышение АД — реакция на стрессовую ситуацию, одновременно имеющая компенсаторный характер, так как оно обеспечивает поддержание ЦПД в условиях внутричерепной гипертензии, возникающей в момент субарахноидального кровоизлияния. Высокое АД в момент кровоизлияния, особенно у больных, страдающих АГ, может стать причиной ошибочной трактовки острого состояния как гипертонического криза.
В случаях тяжелого субарахноидального кровоизлияния могут возникать нарушения сердечной деятельности и дыхания.
В острой стадии субарахноидального кровоизлияния нередко отмечают повышение температуры тела вплоть до фебрильных цифр, а также развитие лейкоцитоза. Эти симптомы могут быть неверно истолкованы как признаки инфекционного заболевания.
Тяжесть состояния больного в момент субарахноидального кровоизлияния и дальнейшее течение болезни зависят в первую очередь от массивности кровоизлияния и его этиологии. Наиболее тяжело протекают субарахноидальные кровоизлияния при разрыве аневризм сосудов мозга (см. подраздел 12.2.3.4 «Хирургическое лечение»).
Диагностика
Клинический диагноз субарахноидального кровоизлияния необходимо подтвердить инструментальными исследованиями. Наиболее надежным и доступным методом диагностики субарахноидального кровоизлияния до настоящего времени остается люмбальная пункция. Ликвор при субарахноидальном кровоизлиянии интенсивно окрашен кровью. Примесь крови в ликворе, постепенно уменьшаясь, сохраняется в течение 1–2 нед от начала болезни. В дальнейшем ликвор приобретает ксантохромную окраску.
Больным в бессознательном состоянии люмбальную пункцию следует проводить с большой осторожностью в связи с риском дислокации мозга.
В последние годы методом выбора в диагностике субарахноидального кровоизлияния стала КТ. КТ не только обнаруживает и оценивает распространенность крови в субарахноидальном пространстве, но и позволяет получить информацию о наличии вентрикулярного и паренхиматозного компонентов кровоизлияния, отека и дислокации мозга, состоянии ликворной системы. Без этих данных правильное ведение больного с субарахноидальным кровоизлиянием на современном этапе развития нейрохирургии невозможно. В некоторых случаях уже при обычной КТ можно установить или предположить причину кровоизлияния. Современные компьютерные томографы позволяют также выполнить высококачественное исследование сосудистой системы мозга (КТ-ангиографию), что обеспечивает 98% точности в диагностике источника кровотечения.
При КТ-диагностике субарахноидального кровоизлияния необходимо учитывать, что информативность метода находится в прямой зависимости от срока выполнения КТ (времени, прошедшего после кровоизлияния), что обусловлено изменением рентгеноконтрастных свойств излившейся крови. Уже через неделю после субарахноидального кровоизлияния кровь в субарахноидальном пространстве видна лишь в половине случаев. В связи с этим при негативных данных КТ больным с клинической картиной субарахноидального кровоизлияния необходима диагностическая люмбальная пункция.
Диагностика субарахноидального кровоизлияния с помощью МРТ менее точна в связи с быстрыми изменениями интенсивности сигнала, обусловленными трансформацией молекул гемоглобина в излившейся крови. Однако при отсутствии КТ можно с успехом использовать МРТ не только для диагностики субарахноидального кровоизлияния, но и для определения источника кровотечения (МРТ-ангиография).
Для диагностики ангиоспазма — одного из осложнений субарахноидального кровоизлияния — применяют ТКДГ. Это исследование позволяет выявить ангиоспазм в сосудах основания мозга, определить его распространенность и выраженность, проследить за его динамикой.
Принципы ведения
Первичную госпитализацию больных с клинической картиной субарахноидального кровоизлияния экстренно осуществляют в первичный сосудистый центр или в неврологический стационар. При неверной трактовке симптомов либо при стертой или атипичной клинической картине субарахноидального кровоизлияния больных иногда ошибочно госпитализируют в терапевтические, инфекционные, нейротравматологические, токсикологические и психиатрические отделения.
В стационаре необходимо провести КТ (МРТ) головного мозга для верификации субарахноидального кровоизлияния и определения анатомической формы кровоизлияния, а если есть возможность — одномоментное неинвазивное исследование сосудистой системы мозга (КТ-, МРТ-ангиографию). При отсутствии признаков кровоизлияния на КТ (МРТ) или при недоступности этих методов следует выполнить люмбальную пункцию.
После инструментального подтверждения диагноза субарахноидального кровоизлияния необходима срочная консультация нейрохирурга для решения следующих вопросов:
Лечебная тактика
Лечебная тактика у больных с субарахноидальным кровоизлиянием зависит от результатов ангиографического обследования.
При выявлении церебральных аневризм (самая частая и опасная причина субарахноидального кровоизлияния) либо другой сосудистой патологии, требующей нейрохирургического вмешательства, решение о сроках и методах операции принимают индивидуально в зависимости от вида патологии, общего состояния пациента, возраста, тяжести имеющегося неврологического дефицита, распространенности кровоизлияния, выраженности сопутствующего кровоизлиянию ангиоспазма, оснащенности и опыта специалистов стационара.
При отсутствии показаний к операции проводят медикаментозную терапию. Основными задачами становятся стабилизация состояния больного, поддержание гомеостаза, профилактика рецидива субарахноидального кровоизлияния, профилактика и лечение сосудистого спазма и ишемии мозга, специфическая терапия заболевания, ставшего причиной кровоизлияния.
Объем терапии зависит от тяжести состояния больного.
Рекомендации
-
Аналгезия и седация при возбуждении и проведении всех манипуляций.
-
Установка желудочного зонда больным, находящимся в состоянии оглушения или комы, из-за угрозы возможной аспирации.
-
Установка мочевого катетера больным, находящимся в состоянии оглушения или комы.
-
Назначение антиконвульсантов в случаях эпилептиформного приступа в момент кровоизлияния.
Нормализация дыхания и газообмена. Нормализация и поддержание стабильной гемодинамики. Больным без нарушения сознания интубацию и вспомогательную ИВЛ осуществляют при наличии клинических признаков дыхательной недостаточности: цианоза, тахипноэ более 40 в мин, при показателях paO2 менее 70 мм рт.ст. Больных с нарушенным сознанием (сопор, кома) следует интубировать и перевести на ИВЛ ввиду опасности развития гипоксии и аспирации. Рекомендуемый уровень систолического АД — 120–150 мм рт.ст. При АГ используют пероральные и внутривенные гипотензивные препараты. При возникновении артериальной гипотензии необходимо поддерживать нормоволемическое или умеренно гиперволемическое состояние (центральное венозное давление 6–12 см вод.ст.), этого достигают инфузией коллоидных и кристаллоидных растворов.
Терапия отека мозга. При клинических и КТ-признаках нарастающего отека мозга, угрожающих развитием дислокационного синдрома, наряду с перечисленными выше мероприятиями рекомендуют применение осмодиуретиков (15% маннитола) в сочетании с салуретиками (фуросемида). Лечение необходимо проводить под контролем электролитного состава крови (не реже 2 раз в сут). Лечение отека мозга, особенно у тяжелых больных, желательно проводить в условиях контроля ВЧД с использованием вентрикулярных или субдуральных датчиков.
Профилактика и терапия церебрального ангиоспазма и ишемии мозга
В настоящее время не существует доказанных методов лечения ангиоспазма. Для его профилактики рекомендуют применять блокаторы кальциевых каналов (нимодипин) в таблетированной форме по 60 мг каждые 4 ч перорально. Лечение следует начинать до появления инструментальных или клинических признаков ангиоспазма, так как при уже развившемся спазме препарат неэффективен. При лечении ангиоспазма и его последствий большое значение имеет поддержание адекватной перфузии мозговой ткани. Для этого используют коллоидные и кристаллоидные растворы, вазопрессоры. При развитии сегментарного симптоматического спазма положительный эффект можно обеспечить с помощью баллонной ангиопластики в сочетании с внутриартериальным введением папаверина или верапамила.
Показания к назначению антиоксидантов и нейропротекторов в целях профилактики и лечения ишемических осложнений субарахноидального кровоизлияния противоречивы, так как клинический эффект препаратов этих групп не доказан.
Прогноз
Прогноз заболевания у больных с субарахноидальным кровоизлиянием зависит от многих факторов. Наиболее значимый из них — этиология кровоизлияния. Субарахноидальное кровоизлияние из артериальной аневризмы сопровождается высокой летальностью и частотой повторного кровоизлияния. При отсутствии хирургического лечения аневризмы до 60% больных погибают в течение первого года от начала болезни. При своевременном хирургическом лечении аневризмы риск летального исхода уменьшается втрое. При субарахноидальном кровоизлиянии другой этиологии прогноз, как правило, благоприятен.