Неврология : национальное руководство : в 2-х т. / под ред. Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой. - 2-е изд., перераб. и доп. - Москва : ГЭОТАР-Медиа, 2022. - Т. 1. - 880 с. - (Серия "Национальные руководства"). - ISBN 978-5-9704-6672-8. |
Аннотация
Во втором издании национального руководства значительное внимание уделено современным методам профилактики, диагностики, фармакотерапии заболеваний нервной системы, а также немедикаментозным методам их лечения. Отдельные разделы посвящены клиническим рекомендациям по основным синдромам и заболеваниям.
В подготовке настоящего издания принимали участие ведущие специалисты-неврологи.
Руководство предназначено неврологам, нейрохирургам, кардиологам, терапевтам, врачам общей практики и представителям других медицинских дисциплин, а также студентам старших курсов медицинских высших учебных заведений, интернам, ординаторам, аспирантам.
2.5.3. Электромиография. Электронейромиография
Г.Н. Авакян, Л.Ф. Касаткина
Для изучения деятельности двигательной системы Н.А. Бернштейн (1947; 1954) предложил использовать ЭМГ, которая находит все более широкое применение в самых различных областях биологии и медицины. ЭМГ — методика исследования электрической активности периферического нейромоторного аппарата, регистрируемая с ее помощью кривая называется электромиограммой.
Стимуляционная ЭМГ, у нас в стране известная под названием электронейромиография (ЭНМГ), — это комплексный метод исследования функционального состояния нервно-мышечной системы, основанный на регистрации и качественно-количественном анализе различных видов электрической активности нервов и мышц в ответ на электрический стимул, позволяющий определять состояние аксонов и миелина периферических нервов и нервно-мышечной передачи.
Основателями клинической ЭМГ и ЭНМГ в России были известные неврологи профессор Б.М. Гехт и академик АМН СССР, профессор Л.О. Бадалян, а также их сотрудники. И это связано с тем, что в клинической практике исключительное значение имеет клинико-электромиографическая и клинико-электронейромиографическая диагностика: в идеале проводить исследование должен опытный клиницист, владеющий методами ЭМГ и ЭНМГ.
В большинстве ведущих нейрофизиологических лабораторий мира термин «электромиография» используют только для обозначения стандартного метода игольчатой ЭМГ (needle EMG), а методы стимуляционной ЭМГ подразделяют на методы изучения скорости распространения возбуждения (СРВ) по периферическим нервам (nerve conduction studies) и методы изучения нервно-мышечной передачи (repetitive motor nerve stimulation) — декремент-тест. Все эти методы при проведении диагностических исследований, как правило, дополняют друг друга.
ЭМГ широко применяется в медицине как диагностический метод, позволяющий оценить состояние ПНС и судить о нарушениях, связанных с патологией мотонейронов спинного мозга, аксонов периферических нервов, нервно-мышечной передачи, мышц, кортикоспинального (пирамидного) тракта, постганглионарных вегетативных волокон, определить уровень поражения, характер поражения, стадию процесса, прогноз болезни и оценить динамику процесса на фоне проводимой терапии.
Для оценки сегментарного и надсегментарного уровней поражений целесообразно применение глобальной (или, как еще ее называют, суммарной, поверхностной, интерференционной, накожной) ЭМГ. Как правило, это метод регистрации биопотенциалов мышц при их максимальном напряжении путем отведения биоэлектрической активности накожными электродами, располагаемыми над двигательной точкой мышцы. Этот метод позволяет с определенной степенью точности оценить электрическую активность всей мышцы, то есть суммарно.
2.5.3.1. Электромиография
Электромиографические методы представлены двумя видами исследований:
При глобальном ЭМГ-исследовании основное внимание уделяется изучению биоэлектрической активности мышц. Вместе с тем о процессах регуляции в ЦНС можно судить не столько на основании изучения деятельности отдельных мышц, сколько в результате исследования их взаимодействия (Охнянская Л.Г., Комарова А.А., 1970). В связи с этим уделяется большое внимание изучению корреляционных отношений различных групп мышц, а также оценке адекватности биоэлектрической реакции, силе и характеру раздражения.
Локальная ЭМГ с использованием концентрических игольчатых электродов, вводимых в мышцу, позволяет изучать состояние ДЕ мышц и мышечных волокон (Marinacci I., 1955; Buchthal F., 1957; 1982; 1992 и др.). При анализе локальной ЭМГ чаще используются классификации F. Buchthal (1957) и A. Subirana (1957).
В отечественной диагностической практике используют методические приемы и способы анализа поверхностной ЭМГ, предложенные Ю.С. Юсевич (1958; 1972). Автор выделяет четыре типа ЭМГ.
I тип ЭМГ характерен для нормальной мышцы и отражает суммарную активность большого числа ДЕ при максимальном сокращении.
Частота интерференционной кривой в норме около 50 Гц, амплитуда 1–2 мВ. ЭМГ I типа может наблюдаться не только при произвольном мышечном сокращении, но и при синергическом напряжении мышц. При таких тонических реакциях амплитуда соответственно ниже и распределяется следующим образом: при сокращении симметричной мышцы противоположной стороны она максимальная, при отдаленной синергии (например, сокращение мышц ноги при регистрации с неподвижной руки) она меньше, и при тонических реакциях на максимальном вдохе — наименьшая. Выраженное их снижение свидетельствует о выпадении части мышечных волокон из ДЕ и наблюдается при первичных мышечных или аксональных процессах.
II тип ЭМГ характеризуется относительно редкой ритмической активностью, возникающей в покое. IIа тип имеет частоту 6–20 Гц, амплитуду 50–150 мкВ, IIб тип — 21–50 Гц, 300–500 мкВ. ЭМГ II типа, по данным автора, характерна для поражения передних рогов спинного мозга, причем IIб тип соответствует относительно менее грубому поражению, чем IIа, и в начальных стадиях заболевания лучше выявляется при тонических пробах.
«Страдание» мотонейронов передних рогов спинного мозга и моторных ядер ствола головного мозга или поражение на уровне эфферентных проводящих путей приводит к «выпадению» ряда ДЕ, а в случае реиннервации — к «укрупнению» сохранных ДЕ.
III тип ЭМГ характерен для различного рода супраспинальных расстройств двигательной активности. При паркинсоническом треморе наблюдаются ритмические вспышки активности, соответствующие по частоте ритму дрожания, при экстрапирамидной ригидности — усиление активности покоя, при гиперкинезах — нерегулярные разряды активности на ЭМГ, соответствующие насильственным движениям тела вне произвольных движений или накладывающимся на нормальный процесс мышечного произвольного сокращения, при пирамидном спастическом параличе на ЭМГ регистрируется повышенная активность покоя в паретичных мышцах. Последнее объясняется тем, что при поражении центральных мотонейронов на уровне корково-подкорковых образований головного мозга или спинальных проводящих путей закономерно происходит «растормаживание» сегментарного аппарата.
IV тип ЭМГ характеризует полный паралич мышцы. Представлен биоэлектрическим молчанием мышцы при попытке произвольного сокращения. При периферическом параличе он может быть обусловлен полной атрофией мышечных волокон различного генеза, при остром невритическом поражении — свидетельствовать о временном функциональном блоке передачи по периферическому аксону. Этот тип кривой может наблюдаться при периодическом семейном параличе и в вялой фазе пирамидного паралича.
Учитывая условность выделения четырех основных типов в режиме максимального произвольного сокращения мышцы, на основе качественных характеристик электромиограмм и их вариабельности, анализа большого фактического материала: группы контроля, профессиональных спортсменов, специальных исследований в условиях длительной гиподинамии, а также клиническо-электромиографических исследований выделены следующие типы и подтипы кривых ЭМГ (Авакян Г.Н. и соавт., 1985, 2012).
2.5.3.2. Электронейромиография (стимуляционная электромиография)
Стимуляционная ЭМГ включает в себя различные методики исследования периферических нервов, вегетативной нервной системы и нервно-мышечной передачи:
Стимуляционные методы исследования проводящей функции моторных волокон, сенсорных волокон и ВКСП позволяют выявить патологию каждого из типов нервных волокон в нерве и определить локализацию поражения (дистальный тип поражения нервов характерен для ПНП, локальное нарушение проводящей функции — для туннельных синдромов и т.д.).
Варианты реакции периферического нерва на повреждение довольно ограничены. Любой патологический фактор, вызывающий нарушение функции нерва, в конечном счете приводит к повреждению аксонов (аксонопатии) или миелиновой оболочки (миелинопатии) либо обоих этих образований.
Цели исследования
Определение функционального состояния и степени поражения моторных, сенсорных и вегетативных структур нервов; локальных нарушений функции нервов — аксонопатии, миелинопатии, а также восстановления двигательных функций; диагностика и дифференциальная диагностика поражений сенсомоторных образований на сегментарном, надсегментарном, периферическом и нервно-мышечном уровне; выявление и оценка степени нарушения нервно-мышечной передачи при миастении и миастенических синдромах; оценка перспективности различных методов лечения и результатов применения определенных лекарственных препаратов, степени реабилитации больных и восстановления функции пораженных двигательных и чувствительных нервов.
Показания
Подозрение на заболевания, связанные с нарушением функции двигательных и чувствительных волокон периферических нервов или нервно-мышечной передачи:
Противопоказания
Каких-либо особых противопоказаний (в том числе наличие имплантатов, кардиостимуляторов, пароксизмальных состояний, эпилепсии) к проведению стимуляционной ЭМГ нет. При необходимости исследование можно проводить даже у больных в коматозном состоянии.
Подготовка к исследованию
Специальной подготовки не требуется. Перед началом исследования больной снимает часы, браслеты. Обычно пациент находится в положении полусидя в специальном кресле, мышцы должны быть максимально расслаблены. Исследуемая конечность иммобилизуется, чтобы исключить искажение формы потенциалов. Конечность при проведении исследования должна быть теплой (температура кожи 26–32 °С), так как при снижении температуры кожи на 1 °С происходит снижение СРВ на 1,1–2,1 м/с. Если конечность холодная, перед обследованием ее хорошо прогревают специальной лампой или любым источником тепла. Больной должен быть информирован о цели исследования и об ощущениях, которые он будет испытывать. Перед началом исследования на обработанную спиртом часть исследуемой конечности больного накладывается заземляющий электрод, смоченный в физиологическом растворе.
Методика и интерпретация результатов
В основе стимуляционной ЭМГ лежит регистрация суммарного ответа мышцы (М-ответа) или нерва на стимуляцию импульсом электрического тока. Исследуют проводящую функцию моторных, сенсорных и вегетативных аксонов периферических нервов или функциональное состояние нервно-мышечной передачи.
-
Стимуляционная ЭМГ выявляет снижение амплитуды М-ответа (аксональный процесс). Нарушение функции аксона ведет к развитию в мышце денервационно-реиннервационного процесса (ДРП), степень выраженности которого определяют с помощью игольчатой ЭМГ.
-
Нарушение функции миелиновой оболочки проявляется снижением СРВ по нерву, повышением порога вызывания М-ответа и увеличением резидуальной латентности (демиелинизирующий процесс).
Следует иметь в виду, что первично аксональный процесс часто вызывает вторичную демиелинизацию, а при демиелинизирующем процессе на определенном этапе болезни возникает вторичное поражение аксона. Задача исследователя — определить тип поражения нерва: аксональный, демиелинизирующий или смешанный (аксонально-демиелинизирующий).
Стимуляцию и регистрацию ответа мышцы проводят с помощью поверхностных электродов. В качестве отводящих электродов используют стандартные накожные хлорсеребряные (AgCl) дисковые или чашечковые электроды, которые крепятся с помощью лейкопластыря. Для уменьшения импеданса используют электропроводный гель или пасту, кожу перед наложением электрода тщательно протирают этанолом.
М-ответ
М-ответ — суммарный потенциал действия, возникающий в мышце при электрическом раздражении двигательного нерва, ее иннервирующего. М-ответ имеет максимальную амплитуду и площадь в зоне распределения концевых пластинок, то есть в двигательной точке мышцы. Двигательной точкой называют проекцию на кожу зоны концевых пластинок нерва. Двигательная точка обычно располагается на самом выпуклом участке (брюшке) мышцы.
При исследовании М-ответа используют биполярный способ отведения: один электрод является активным, второй — референтным. Активный регистрирующий электрод располагают в области двигательной точки мышцы, иннервируемой исследуемым нервом; референтный электрод — в области сухожилия данной мышцы или в месте прикрепления сухожилия к костному выступу (рис. 2.122, см. цв. вклейку).
При исследовании проводящей функции нервов используют стимулы супрамаксимальной интенсивности. Обычно М-ответ с нервов рук начинают регистрировать при величине стимула 6–8 мА, с нервов ног — 10–15 мА. По мере увеличения интенсивности стимула амплитуда М-ответа увеличивается за счет включения в М-ответ новых ДЕ.
Плавное повышение амплитуды М-ответа связано с различной возбудимостью нервных волокон: сначала возбуждаются низкопороговые быстропроводящие толстые волокна, затем тонкие, медленнопроводящие волокна. Когда в М-ответ включаются все мышечные волокна исследуемой мышцы, при дальнейшем увеличении интенсивности стимула амплитуда М-ответа перестает нарастать. Для достоверности исследования амплитуду стимула после этого увеличивают еще на 20–30%. Такая величина стимула и называется супрамаксимальной.
Стимуляцию проводят в нескольких точках по ходу нерва (рис. 2.123). Желательно, чтобы расстояние между точками стимуляции было не менее 10 см. Регистрируют М-ответ в каждой точке стимуляции. Разность латентности М-ответов и расстояние между точками стимуляции позволяют вычислить СРВ по нерву.

При исследовании проводящей функции моторных нервов анализируют следующие параметры:
Основными диагностически значимыми параметрами считают амплитуду М-ответа и СРВ. Амплитуда, площадь, форма и длительность М-ответа отражают количество и синхронность сокращения мышечных волокон в ответ на стимуляцию нерва.
Амплитуда М-ответа Амплитуду М-ответа оценивают по негативной фазе, так как ее форма более постоянна, и измеряют в милливольтах (мВ). Снижение амплитуды М-ответа — электрофизиологическое отражение уменьшения количества сокращающихся мышечных волокон в мышце.
Причины снижения амплитуды М-ответа:
-
нарушение возбудимости нервных волокон, когда часть нервных волокон не генерирует импульс в ответ на стимуляцию электрическим током (аксональный тип поражения нервов — аксональные ПНП);
-
демиелинизация нервных волокон, когда мышечные волокна не отвечают на нервный импульс, что приводит к снижению амплитуды М-ответа, однако трофическая функция нерва остается сохранной;
-
различные миопатии [прогрессирующая мышечная дистрофиия (ПМД), полимиозит и др.].
М-ответ отсутствует при атрофии мышцы, разрыве нерва или его полной дегенерации.
-
Для неврального уровня поражения характерны повышение порога вызывания М-ответа и нарушение СРВ, повышение резидуальной латентности, «рассыпанные» F-волны.
-
Для нейронального уровня поражения (БАС, спинальные амиотрофии, опухоль спинного мозга, миелопатия и т.п.), когда уменьшается количество мотонейронов и соответственно аксонов и мышечных волокон, характерны нормальный порог вызывания М-ответа, нормальная СРВ, «гигантские», крупные и повторные F-волны и полное их выпадение.
-
Для мышечного уровня поражения характерны нормальные СРВ и порог вызывания М-ответа, отсутствие F-волн или наличие низкоамплитудных F-волн.
Данные стимуляционной ЭМГ не позволяют однозначно оценить мышечный уровень поражения периферического нейромоторного аппарата — для этого необходима игольчатая ЭМГ.
Форма, площадь и длительность М-ответа В норме М-ответ представляет собой негативно-позитивное колебание сигнала. Длительность М-ответа измеряют по длительности негативной фазы, площадь М-ответа также измеряют по площади негативной фазы. Самостоятельного диагностического значения показатели площади и длительности М-ответа не имеют, но в совокупности с анализом его амплитуды и формы можно судить о процессах формирования М-ответа.
При демиелинизации нервных волокон происходит десинхронизация М-ответа с увеличением его длительности и снижением амплитуды, причем в проксимальных точках десинхронизация увеличивается.
Блок проведения возбуждения Блоком проведения возбуждения называют снижение (декремент) амплитуды М-ответа при стимуляции в двух соседних точках более чем на 25% (рассчитывают как отношение амплитуды А1:А2, выраженной в процентах, где А1 — амплитуда М-ответа в одной точке стимуляции, А2 — амплитуда М-ответа в следующей, более проксимальной точке стимуляции). При этом увеличение длительности негативной фазы М-ответа не должно превышать 15%.
В основе патогенеза блока проведения возбуждения лежит стойкий локальный очаг демиелинизации (не более 1 см), вызывающий нарушение проведения импульса. Классическим примером блоков проведения возбуждения являются туннельные синдромы.
Известны два заболевания с множественными стойкими блоками проведения возбуждения — моторно-сенсорная мультифокальная ПНП (Самнера–Льюиса) и мультифокальная моторная невропатия с блоками проведения возбуждения. Правильная диагностика мультифокальной моторной невропатии крайне важна, так как заболевание клинически и электромиографически имитирует БАС, что часто приводит к серьезным диагностическим ошибкам.
Адекватным методом, позволяющим выявить блоки проведения возбуждения при мультифокальной моторной невропатии, является метод пошагового исследования нерва — «инчинг» (inching), заключающийся в стимуляции нерва в нескольких точках с шагом 1–2 см. Расположение блоков проведения возбуждения при мультифокальной моторной невропатии не должно совпадать с местами сдавления нервов при типичных туннельных синдромах.
Порог вызывания М-ответа
Порогом вызывания М-ответа называют интенсивность стимула, при которой появляется минимальный М-ответ. Обычно М-ответ с нервов рук начинает регистрироваться при амплитуде стимула 15 мА и длительности 200 мкс, с ног — 20 мА и 200 мкс соответственно.
Для демиелинизирующих ПНП, особенно для наследственных форм, при которых начальный М-ответ может появляться при интенсивности стимула 100 мА и 200 мкс, характерно повышение порога вызывания М-ответов. Низкие пороги стимуляции наблюдают у детей и у худых пациентов (3–4 мА). Изменения порогов вызывания М-ответов не должны рассматриваться как самостоятельный диагностический критерий — оценивать их необходимо в совокупности с другими изменениями.
Скорость распространения возбуждения по моторным волокнам и латентность М-ответа
СРВ определяют как расстояние, которое проходит импульс по нервному волокну за единицу времени, и выражают в метрах в секунду (м/с). Время между подачей электрического стимула и началом М-ответа называется латентностью М-ответа.
СРВ снижается при демиелинизации (например, при демиелинизирующих ПНП), так как на участках разрушения миелиновой оболочки импульс распространяется не сальтаторно, а последовательно, как в безмиелиновых волокнах, что вызывает увеличение латентности М-ответа.
Латентность М-ответа зависит от расстояния между стимулирующим и отводящим электродами, поэтому при стимуляции в стандартных точках латентность зависит от роста пациента. Вычисление СРВ позволяет избежать зависимости результатов исследования от роста пациента.
СРВ на участке нерва вычисляют путем деления расстояния между точками стимуляции на разность латентностей М-ответов в этих точках:
V=(D2–D1)/(L2–L1),
где V — скорость проведения по двигательным волокнам; D2 — дистанция для второй точки стимуляции (расстояние между катодом стимулирующего электрода и активным отводящим электродом); D1 — дистанция для второй точки стимуляции (расстояние между катодом стимулирующего электрода и активным отводящим электродом); D2 –D1 отражает расстояние между точками стимуляции; L1 — латентность в первой точке стимуляции; L2 — латентность во второй точке стимуляции.
Снижение СРВ является маркером процесса полной или сегментарной демиелинизации нервных волокон при невропатиях, ПНП, таких как острая и хроническая демиелинизирующие ПНП (ХВДП), наследственные ПНП (болезнь Шарко–Мари–Тута, кроме ее аксональных форм), диабетическая ПНП (ДПН), компрессия нерва (туннельные синдромы, травмы). Определение СРВ позволяет выяснить, на каком участке нерва (дистальном, среднем или проксимальном) имеют место патологические изменения.
Резидуальная латентность
Резидуальной латентностью называют рассчитываемое время прохождения импульса по терминалям аксонов. На дистальном отрезке аксоны двигательных волокон ветвятся на терминали. Так как терминали не имеют миелиновой оболочки, СРВ по ним значительно ниже, чем по миелинизированным волокнам. Время между стимулом и началом М-ответа при стимуляции в дистальной точке складывается из времени прохождения по миелинизированным волокнам и времени прохождения по терминалям аксона.
Чтобы вычислить время прохождения импульса по терминалям, нужно из дистальной латентности в первой точке стимуляции вычесть время прохождения импульса по миелинизированной части. Это время можно рассчитать, приняв допущение, что СРВ на дистальном участке приблизительно равна СРВ на сегменте между первой и второй точками стимуляции.
Формула расчета резидуальной латентности:
R=L–(D:V1–2),
где R — резидуальная латентность; L — дистальная латентность (время от стимула до начала М-ответа при стимуляции в дистальной точке); D — дистанция (расстояние между активным отводящим электродом и катодом стимулирующего электрода); V1–2 — СРВ на сегменте между первой и второй точками стимуляции.
Изолированное увеличение резидуальной латентности на одном из нервов считают признаком туннельного синдрома. Наиболее частый туннельный синдром для срединного нерва — запястный туннельный синдром; для локтевого — синдром канала Гийона; для большеберцового — тарзальный туннельный синдром; для малоберцового — сдавление на уровне тыла стопы.
Увеличение резидуальных латентностей на всех исследуемых нервах характерно для невропатий демиелинизирующего типа.
Критерии нормальных значений
В клинической практике удобно использовать нижние границы нормы для амплитуды М-ответа и СРВ и верхние границы нормы для резидуальной латентности и порога вызывания М-ответа (табл. 2.16).
| Показатели | Длинные нервы верхних конечностей | Длинные нервы нижних конечностей |
|---|---|---|
Амплитуда М-ответа |
>3,5 мВ (срединный, лучевой), >6,0 мВ (локтевой) |
>3,5 мВ |
СРВ |
>50 м/с |
>40 м/с |
Резидуальная латентность |
<2,5 мс |
<3,0 мс |
Порог вызывания М-ответа |
<15 мА (200 мс) |
<20 мА (200 мс) |
В норме амплитуда М-ответа несколько выше в дистальных точках стимуляции, в проксимальных точках М-ответ несколько растягивается и десинхронизируется, что приводит к некоторому увеличению его длительности и снижению амплитуды (не более чем на 15%). СРВ по нервам немного выше в проксимальных точках стимуляции.
Клиническая значимость анализируемых показателей
Снижение СРВ, амплитуды и десинхронизация (увеличение длительности) М-ответа свидетельствуют о поражении нерва. Исследование СРВ по двигательным волокнам позволяет подтвердить или опровергнуть диагноз и провести дифференциальную диагностику при таких заболеваниях, как туннельные синдромы, аксональные и демиелинизирующие ПНП, мононевропатии, наследственные ПНП.
Электромиографические критерии поражения нерва демиелинизирующего характера. Классические примеры демиелинизирующих невропатий — острая и хроническая воспалительные демиелинизирующие ПНП, диспротеинемические невропатии, наследственная моторно-сенсорная невропатия (НМСН) I типа.
Основные критерии демиелинизирующих ПНП:
Электромиографические критерии поражения нерва аксонального характера. Классическими примерами аксональных невропатий считают большинство токсических (в том числе и лекарственных) невропатий, НМСН II типа (аксональный тип болезни Шарко–Мари–Тута).
Основные критерии аксональных ПНП:
При сочетании демиелинизирующих и аксональных признаков констатируют аксонально-демиелинизирующий тип поражения. Наиболее резкое снижение СРВ по периферическим нервам наблюдают при наследственных ПНП. При синдроме Русси–Леви СРВ может снижаться до 7–10 м/с, при болезни Шарко–Мари–Тута — до 15–20 м/с. При приобретенных ПНП степень снижения СРВ различна в зависимости от характера заболевания и степени патологии нервов. Наиболее выраженное снижение скоростей (до 40 м/с на нервах верхних конечностей и до 30 м/с на нервах нижних конечностей) наблюдают при демиелинизирующих ПНП, при которых процессы демиелинизации нервного волокна превалируют над поражением аксона: при хронической демиелинизирующей и острой демиелинизирующей ПНП [синдром Гийена–Барре (СГБ), синдром Миллера–Фишера].
Для преимущественно аксональных ПНП (например, токсических: уремической, алкогольной, диабетической, лекарственной и др.) характерна нормальная или незначительно сниженная СРВ при резко выраженном снижении амплитуды М-ответа. Чтобы установить диагноз ПНП, необходимо исследовать не менее трех-четырех нервов конечностей, однако на практике нередко приходится исследовать большее количество (шесть и более) нервов.
Увеличение длительности М-ответа служит дополнительным доказательством демиелинизирующих процессов в исследуемом нерве. Наличие блоков проведения возбуждения характерно для туннельных синдромов, а также для мультифокальной моторной невропатии с блоками проведения возбуждения.
Изолированное поражение одного нерва позволяет думать о мононевропатии, в том числе о туннельном синдроме. При радикулопатиях в начальных стадиях проводящая функция моторных нервов часто остается сохранной. При отсутствии адекватного лечения в течение 2–3 мес постепенно снижается амплитуда М-ответа, может повыситься порог его вызывания при сохранной СРВ.
Снижение амплитуды М-ответа при прочих абсолютно нормальных показателях требует расширения диагностического поиска и рассмотрения возможности первично-мышечного заболевания или заболевания мотонейронов спинного мозга, что можно определить только с помощью игольчатой ЭМГ.
2.5.3.3. Исследование проводящей функции сенсорных нервов
СРВ по сенсорным волокнам определяют с помощью регистрации потенциала действия афферентного (чувствительного) нерва в ответ на его «чрескожную» электрическую стимуляцию. Методики регистрации СРВ по сенсорным и двигательным волокнам имеют много общего, в то же время между ними существует важное патофизиологическое различие: при исследовании моторных волокон регистрируют рефлекторный ответ мышцы, а при исследовании сенсорных волокон — потенциал возбуждения чувствительного нерва.
Существует два способа проведения исследования: ортодромный, при котором стимулируют дистальные отделы нерва, а сигналы регистрируют в проксимальных точках, и антидромный, при котором регистрацию проводят дистальнее точки стимуляции. В клинической практике чаще используется антидромный способ как более простой, хотя и менее точный.
Методика
Положение больного, температурный режим, используемые электроды аналогичны таковым при исследовании функции моторных волокон. Можно использовать и специальные пальцевые электроды для исследования сенсорных волокон. При регистрации с нервов рук активный электрод накладывают на проксимальную фалангу II или III (для срединного нерва) либо V пальца (для локтевого нерва), референтный электрод располагается на дистальной фаланге того же пальца (рис. 2.124, см. цв. вклейку).
Положение заземляющего и стимулирующего электродов аналогично таковому при исследовании моторных волокон. При регистрации сенсорного ответа икроножного нерва активный электрод располагают на 2 см ниже и на 1 см кзади от латеральной лодыжки, референтный электрод — на 3–5 см дистальнее, стимулирующий электрод — по ходу икроножного нерва на заднелатеральной поверхности голени. При правильном расположении стимулирующего электрода больной ощущает иррадиацию электрического импульса по латеральной поверхности стопы. Заземляющий электрод располагается на голени дистальнее стимулирующего.
Сенсорный ответ значительно ниже по амплитуде (для локтевого нерва — 6–30 мкВ, в то время как моторный ответ — 6–16 мВ). Порог возбуждения толстых чувствительных волокон ниже, чем более тонких моторных, поэтому используют стимулы субпороговой (по отношению к моторным волокнам) интенсивности.
Наиболее часто исследуют срединный, локтевой, икроножный, реже — лучевой нерв. Наиболее значимые для клинической практики параметры:
Амплитуда сенсорного ответа
Амплитуду сенсорного ответа измеряют по методу «пик-пик» (максимум негативной — минимум позитивной фазы). Нарушение функции аксона характеризуется снижением амплитуды сенсорного ответа либо его полным выпадением.
Скорость распространения возбуждения и латентность
Как и при исследовании моторных волокон, латентность измеряют от артефакта стимула до начала ответа. СРВ рассчитывают так же, как и при исследовании моторных волокон. Снижение СРВ указывает на демиелинизацию.
Нормальные значения
В клинической практике удобно анализировать результаты относительно нижней границы нормальных значений (табл. 2.17).
| Нерв | Амплитуда, мкВ | СРВ, м/с |
|---|---|---|
N. medianus |
>6 |
>50 |
N. ulnaris |
>6 |
>50 |
N. suralis |
>5 |
>40 |
Клиническая значимость анализируемых показателей
Как и при исследовании моторных волокон, снижение СРВ характерно для демиелинизирующих, а снижение амплитуды — для аксональных процессов. При выраженной гипестезии сенсорный ответ иногда зарегистрировать не удается.
Сенсорные нарушения выявляют при туннельных синдромах, моно- и ПНП, радикулопатиях и др. Например, для запястного туннельного синдрома характерным считают изолированное снижение дистальной СРВ по срединному сенсорному нерву при нормальной скорости на уровне предплечья и по локтевому нерву. При этом в начальных стадиях СРВ снижается, но амплитуда остается в пределах нормы. При отсутствии адекватного лечения амплитуда сенсорного ответа также начинает снижаться. Для сдавления локтевого нерва в канале Гийона характерно изолированное снижение дистальной скорости по сенсорным волокнам локтевого нерва. Генерализованное снижение СРВ по сенсорным нервам характерно для сенсорной ПНП. Часто оно сочетается со снижением амплитуды сенсорного ответа. Равномерное уменьшение СРВ ниже 30 м/с характерно для наследственных ПНП.
Наличие анестезии/гипестезии при нормальной проводящей функции сенсорных волокон позволяет заподозрить более высокий уровень поражения (корешковый или центральный генез). В этом случае уточнить уровень сенсорных нарушений можно с помощью ССВП.
И.А. Скворцов и соавт. (1976) предложили метод определения СРВ по чувствительным и двигательным волокнам срединного нерва при однократной стимуляции его с применением парных регистрирующих и стимулирующих электродов.
Комплексное исследование СРВс и СРВм позволяет дифференцировать преимущественное поражение сенсорных и моторных волокон. Для этого введено понятие мотосенсорного коэффициента (Км/с), который вычисляется по формуле:
В норме он равен 90–100%. Увеличение Км/с говорит о преимущественно диссоциированном снижении СРВс, уменьшение коэффициента указывает на преобладание двигательного поражения.
Увеличение мотосенсорного коэффициента свидетельствует о преимущественном (диссоциированном) повышении СРВ по двигательным волокнам или преимущественном снижении СРВ по чувствительным волокнам. Снижение мотосенсорного коэффициента, наоборот, указывает на преимущественное повышение СРВс или понижение СРВм. Сопоставление величины мотосенсорного коэффициента с абсолютными показателями СРВ по двигательным и чувствительным волокнам позволяет получить объективное представление о соотношении СРВм и СРВс.
Коэффициент асимметрии определяется как отношение разности величины СРВ по одноименным нервам левой и правой конечностей к наименьшему из этих показателей, выраженное в процентах:
Кас =(СРВmax–СРВmin)×100%:СПИmin,
где СРВmax — наибольшая СРВ на одной из сторон; СРВmin — меньшая скорость на другой стороне.
2.5.3.4. Исследование F-волны
F-волна (F-ответ) — суммарный потенциал действия ДЕ мышцы, возникающий при электрическом раздражении смешанного нерва. Наиболее часто F-волны анализируют при исследовании срединного, локтевого, малоберцового, большеберцового нервов.
Методика
Во многом техника регистрации аналогична таковой при исследовании проводящей функции моторных волокон. В процессе исследования моторных волокон после регистрации М-ответа в дистальной точке стимуляции исследователь переключается в приложение регистрации F-волны, при тех же параметрах стимула записывает F-волны, после чего продолжает исследование моторных волокон в остальных точках стимуляции.
F-волна имеет небольшую амплитуду (обычно до 500 мкВ). При стимуляции периферического нерва в дистальной точке на экране монитора появляется М-ответ с латентностью 3–7 мс, F-ответ имеет латентность около 26–30 мс для нервов рук и около 48–55 мс для нервов ног (рис. 2.125). Стандартное исследование включает в себя регистрацию 20 F-волн.
Диагностически значимые показатели F-волны:
Латентность, диапазон скоростей распространения F-волн, «рассыпанные» F-волны
Латентность измеряют от артефакта стимула до начала F-волны. Поскольку латентность зависит от длины конечности, удобно пользоваться диапазоном скоростей распространения F-волн. Расширение диапазона скоростей в сторону низких величин указывает на замедление проведения по отдельным нервным волокнам, что может являться ранним признаком демиелинизирующего процесса. При этом часть F-волн может иметь нормальную латентность.Расчет СРВ по F-волне:
V=2×D:(LF–LM–1 мс),
где V — СРВ, определенная с помощью F-волны; D — дистанция, измеряемая от точки под катодом стимулирующего электрода до остистого отростка соответствующего позвонка; LF — латентность F-волны; LM — латентность М-ответа; 1 мс — время центральной задержки импульса.
При выраженном демиелинизирующем процессе часто выявляют феномен «рассыпанных» F-волн (рис. 2.126), а в самых поздних стадиях возможно полное их выпадение. Причиной «рассыпанных» F-волн считают наличие множественных очагов демиелинизации по ходу нерва, которые могут стать своего рода «отражателями» импульса.
Доходя до очага демиелинизации, импульс не распространяется дальше антидромно, а отражается и ортодромно распространяется к мышце, вызывая сокращение мышечных волокон. Феномен «рассыпанных» F-волн является маркером невритического уровня поражения и почти не встречается при нейрональных или первично-мышечных заболеваниях.
2.5.3.5. Амплитуда F-волн, феномен «гигантских» F-волн
В норме амплитуда F-волны составляет менее 5% амплитуды М-ответа в данной мышце. Обычно амплитуда F-волны не превышает 500 мкВ. Амплитуду F-волн измеряют «от пика до пика». При реиннервации F-волны укрупняются. Диагностически значимым считают отношение средней амплитуды F-волны к амплитуде М-ответа. Повышение амплитуды F-волны более чем на 5% амплитуды М-ответа (крупные F-волны) указывает на процесс реиннервации в мышце.
Диагностическую значимость имеет также появление так называемых гигантских F-волн амплитудой более 1000 мкВ, отражающих степень выраженной реиннервации в мышце. «Гигантские» F-волны чаще всего наблюдают при заболеваниях мотонейронов спинного мозга (рис. 2.127), хотя они могут появляться и при невральной патологии, протекающей с выраженной реиннервацией.
Выпадение F-волн
Выпадением F-волны называют ее отсутствие на линии регистрации. Причиной выпадения F-волны может быть поражение как нерва, так и мотонейрона. В норме допустимо выпадение 5–10% F-волн. Полное выпадение F-волн свидетельствует о наличии выраженной патологии (в частности, оно возможно в поздних стадиях заболеваний при выраженных мышечных атрофиях).
Повторные F-волны
В норме вероятность ответа одного и того же мотонейрона крайне мала. При уменьшении количества мотонейронов и изменении их возбудимости (одни мотонейроны становятся гипервозбудимыми, другие, наоборот, отвечают только на сильные раздражители) существует вероятность, что один и тот же мотонейрон будет отвечать многократно, поэтому появляются F-волны одинаковой латентности, формы и амплитуды, называемые повторными. Второй причиной появления повторных F-волн является повышение мышечного тонуса.
Нормальные значения
У здорового человека принято считать допустимым, если появляется до 10% выпадений, «гигантских» и повторных F-волн. При определении диапазона скоростей минимальная скорость не должна быть ниже 40 м/с для нервов рук и 30 м/с для нервов ног (табл. 2.18). «Рассыпанных» F-волн и полного выпадения F-волн в норме не наблюдают.
| Параметр | Для нервов ног | Для нервов рук |
|---|---|---|
Скорость распространения |
>30 м/с |
>40 м/с |
Амплитуда минимальная |
>50 мкВ |
|
Амплитуда максимальная |
Не более 10% «крупных» F-волн |
|
Нормальные значения минимальных латентностей F-волн в зависимости от роста представлены в табл. 2.19.
| Нерв | 150 см | 160 см | 170 см | 180 см | 190 см |
|---|---|---|---|---|---|
Срединный |
25 |
26,5 |
28–28,5 |
29,6–30 |
31,1–32 |
Локтевой |
25 |
28,5–29 |
30,2–31 |
32–33 |
|
26,8–27 |
|||||
Малоберцовый |
43–43,5 |
46–47,8 |
49–52 |
51–56,2 |
54–60,5 |
Большеберцовый |
41,2–44 |
45,4–48 |
49,6–53 |
53,8–57 |
58–62 |
При острой демиелинизирующей ПНП, как правило, обнаруживают лишь нарушение проведения F-волн, при хронической — F-волны могут отсутствовать (блоки F-волн). Частые повторные F-волны наблюдают при поражении мотонейронов спинного мозга. Особенно характерным для заболеваний мотонейронов является сочетание «гигантских» повторных F-волн и их выпадений. Еще один признак поражения мотонейронов — появление большого количества «гигантских» F-волн. Наличие крупных F-волн указывает на наличие реиннервационного процесса в мышце.
Несмотря на высокую чувствительность F-волн, этот метод можно использовать только в качестве дополнительного (в совокупности с данными исследования проводящей функции периферических нервов и игольчатой ЭМГ).
Клиническая значимость
Расширение диапазона СРВ, определяемой методом F-волн, и соответственно удлинение латентностей F-волн, феномен «рассыпанных» F-волн позволяют предположить наличие демиелинизирующего процесса.
2.5.3.6. Исследование H-рефлекса
H-рефлекс (H-ответ) — суммарный потенциал действия ДЕ мышцы, возникающий при слабом раздражении электрическим током афферентных нервных волокон, идущих из этой мышцы. Возбуждение передается по афферентным волокнам нерва через задние корешки спинного мозга на вставочный нейрон и на мотонейрон, а затем через передние корешки по эфферентным нервным волокнам на мышцу.
Анализируемые показатели Н-ответа: порог вызывания, форма, отношение амплитуды H-рефлекса к М-ответу, латентный период или скорость его рефлекторного ответа.
Клиническая значимость. При поражении пирамидных нейронов порог вызывания H-ответа снижается, а амплитуда рефлекторного ответа резко повышается. Причиной отсутствия или снижения амплитуды H-ответа могут быть патологические изменения в переднероговых структурах спинного мозга, афферентных или эфферентных нервных волокнах, задних или передних спинальных корешках нервов.
2.5.3.7. Исследование мигательного рефлекса
Blink рефлекс (от англ. blink — мигать, щуриться) является биоэлектрическим аналогом роговичного рефлекса. Рефлекторная дуга включает в себя волокна тройничного нерва (первая ветвь), чувствительное ядро тройничного нерва, ядро лицевого нерва, ствол лицевого нерва, мышцы, окружающие глаз.
Мигательный (орбикулярный, тригеминофациальный) рефлекс — суммарный потенциал действия, возникающий в обследуемой мышце лица (например, m. orbicularis oculi) при электрическом раздражении афферентных нервных волокон одной из ветвей n. trigemeni — I, II или III. Как правило, регистрируют два вызванных рефлекторных ответа: первый — с латентным периодом около 12 мс (моносинаптический, аналог Н-рефлекса), второй — с латентным периодом около 34 мс (экстероцептивный, с полисинаптическим распространением возбуждения в ответ на раздражение).
При нормальной СРВ по лицевому нерву увеличение времени рефлекторного мигательного ответа по одной из ветвей нерва указывает на ее поражение, а его увеличение по всем трем ветвям нерва свидетельствует о поражении узла или ядра.
С помощью исследования можно провести дифференциальную диагностику между повреждением лицевого нерва в костном канале (в этом случае рефлекторный мигательный ответ будет отсутствовать) и его поражением после выхода из шилососцевидного отверстия. Компоненты их выпадения имеют более четкие значения для диагностики поражения ядра лицевого нерва, а также поражения тройничного нерва.
2.5.3.8. Исследование бульбокавернозного рефлекса
Бульбокавернозный рефлекс — суммарный потенциал действия, возникающий в обследуемой мышце промежности при электрическом раздражении афферентных нервных волокон n. pudendus.
Рефлекторная дуга бульбокавернозного рефлекса проходит через крестцовые сегменты спинного мозга на уровне S1–S4, афферентные и эфферентные волокна находятся в стволе полового нерва. При исследовании функции рефлекторной дуги можно получить представление о спинальном уровне иннервации сфинктеров, мышц промежности, а также выявить расстройства регуляции половой функции у мужчин. Исследование бульбокавернозного рефлекса применяют у больных, страдающих половой дисфункцией и тазовыми расстройствами.
2.5.3.9. Исследование нервно-мышечной передачи (декремент-тест)
Нарушения синаптической передачи могут быть обусловлены пресинаптическими и постсинаптическими процессами (повреждение механизмов синтеза медиатора и его выделения, нарушение его действия на постсинаптическую мембрану и т.п.). Декремент-тест — электрофизиологический метод, с помощью которого оценивают состояние нервно-мышечной передачи, основанный на том, что в ответ на ритмическую стимуляцию нерва выявляют феномен снижения амплитуды М-ответа (ее декремента).
Исследование позволяет определить тип нарушения нервно-мышечной передачи, оценить тяжесть поражения и его обратимость в процессе фармакологических тестов (проба с неостигмина метилсульфатом), а также эффективность лечения.
Показания
Подозрение на миастению и миастенические синдромы. Многообразие клинических форм миастении, ее частая сочетаемость с тиреоидитом, опухолями, полимиозитом и другими аутоиммунными процессами, широкие вариации эффективности применения одних и тех же вмешательств у различных больных делают этот метод обследования чрезвычайно важным в системе функциональной диагностики.
Методика
Положение пациента, температурный режим и принципы наложения электродов аналогичны таковым при исследовании проводящей функции моторных нервов.
Исследование нервно-мышечной передачи проводят в клинически более слабой мышце, так как в интактной мышце нарушение нервно-мышечной передачи либо отсутствует, либо выражено минимально. При необходимости декремент-тест можно выполнить в различных мышцах верхних и нижних конечностей, лица и туловища, однако на практике исследование чаще всего проводится в дельтовидной мышце (стимуляция подмышечного нерва в точке Эрба). Если сила в дельтовидной мышце сохранна (5 баллов), но присутствует слабость мимической мускулатуры, необходимо тестировать круговую мышцу глаза. При необходимости декремент-тест выполняют в мышце, отводящей мизинец кисти, трехглавой мышце плеча, двубрюшной мышце и др.
В начале исследования, чтобы установить оптимальные параметры стимуляции, стандартным способом регистрируют М-ответ выбранной мышцы. Затем проводят непрямую электрическую низкочастотную стимуляцию нерва, иннервирующего исследуемую мышцу, с частотой 3 Гц. Используют пять стимулов и в последующем оценивают наличие декремента амплитуды последнего М-ответа по отношению к первому.
После выполнения стандартного декремент-теста проводят пробы с оценкой постактивационного облегчения, постактивационного истощения (тетанизация) и фармакологические пробы.
Интерпретация результатов
При ЭМГ-обследовании у здорового человека стимуляция частотой 3 Гц не выявляет декремента амплитуды (площади) М-ответа мышцы вследствие большого запаса надежности нервно-мышечной передачи, то есть амплитуда суммарного потенциала остается стабильной в течение всего периода стимуляции.
Если надежность нервно-мышечной передачи уменьшается, выключение мышечных волокон из суммарного М-ответа проявляется снижением амплитуды (площади) последующих М-ответов в серии импульсов по отношению к первому, то есть декрементом М-ответа (рис. 2.128). Для миастении характерен декремент амплитуды М-ответа более 10% при его нормальной исходной амплитуде. Декремент обычно соответствует степени снижения мышечной силы: при силе мышцы 4 балла он составляет 15–20%, 3 балла — 50%, 1 балл — до 90%. Если при силе мышцы 2 балла декремент незначителен (12–15%), диагноз миастении нужно поставить под сомнение.
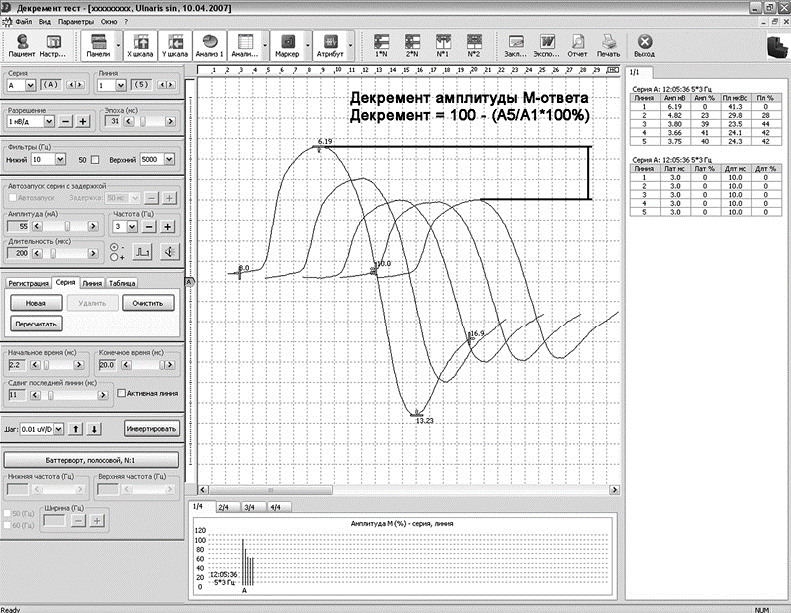
Для миастении также типична обратимость нарушений нервно-мышечной передачи: после введения неостигмина метилсульфата отмечают увеличение амплитуды М-ответа и/или уменьшение блока нервно-мышечной передачи.
Выраженное повышение амплитуды М-ответа в период постактивационного облегчения позволяет заподозрить пресинаптический уровень поражения, в данном случае проводят пробу с тетанизацией (стимуляция серией из 200 стимулов частотой 40–50 Гц) в мышце, отводящей мизинец кисти, которая выявляет инкремент амплитуды М-ответа. Инкремент амплитуды М-ответа более +30% патогномоничен для пресинаптического уровня поражения.
2.5.3.10. Игольчатая электромиография
Игольчатая ЭМГ включает следующие основные методики:
Стандартная игольчатая электромиография
Игольчатая ЭМГ — инвазивный метод исследования, осуществляемый с помощью вводимого в мышцу концентрического игольчатого электрода. Игольчатая ЭМГ позволяет оценить периферический нейромоторный аппарат: морфофункциональную организацию ДЕ скелетных мышц, состояние мышечных волокон (наличие или отсутствие их спонтанной активности), а при динамическом наблюдении — оценить эффективность проводимого лечения, динамику патологического процесса и прогноз заболевания.
Показания
Заболевания мотонейронов спинного мозга (БАС, спинальные амиотрофии, полиомиелит и постполиомиелитический синдром, сирингомиелия и др.), миелопатии, радикулопатии, различные невропатии (аксональные и демиелинизирующие), миопатии, воспалительные заболевания мышц (полимиозит и дерматомиозит), центральные двигательные расстройства, сфинктерные нарушения и ряд других ситуаций, когда необходимо объективизировать состояние двигательных функций и системы управления движением, оценить вовлечение в процесс различных структур периферического нейромоторного аппарата.
Противопоказания
Противопоказания к проведению игольчатой ЭМГ практически отсутствуют. Ограничением считают бессознательное состояние больного, когда он не может произвольно напрягать мышцу. Впрочем, и в этом случае можно определить наличие или отсутствие текущего процесса в мышцах (по наличию или отсутствию спонтанной активности мышечных волокон). С осторожностью следует проводить игольчатую ЭМГ в тех мышцах, в которых имеются выраженные гнойные раны, незаживающие язвы и глубокие ожоговые поражения.
Диагностическое значение
Стандартная игольчатая ЭМГ занимает центральное место среди электрофизиологических методов исследования при различных нервно-мышечных заболеваниях и имеет решающее значение в дифференциальной диагностике неврогенных и первично-мышечных заболеваний.
С помощью этого метода определяют выраженность денервации в мышце, иннервируемой пораженным нервом, степень его восстановления, эффективность реиннервации.
Игольчатая ЭМГ нашла свое применение не только в неврологии, но и в ревматологии, эндокринологии, спортивной и профессиональной медицине, в педиатрии, урологии, гинекологии, хирургии и нейрохирургии, офтальмологии, стоматологии и челюстно-лицевой хирургии, ортопедии и ряде других медицинских отраслей.
Подготовка к исследованию
Специальной подготовки больного к исследованию не требуется. Так как при проведении игольчатой ЭМГ необходимо полное расслабление обследуемых мышц, ее проводят в положении пациента лежа. Больному обнажают обследуемые мышцы, укладывают его на спину (или живот) на удобную мягкую кушетку с регулируемым подголовником, информируют его о предстоящем обследовании и объясняют, как он должен напрягать и затем расслаблять обследуемые мышцы.
Методика
Исследование проводят с помощью концентрического игольчатого электрода, введенного в двигательную точку мышцы (допустимый радиус — не более 1 см для крупных мышц и 0,5 см для мелких). Желательно использовать одноразовые стерильные игольчатые электроды, которые вскрывают непосредственно перед исследованием мышцы и после обследования утилизируют. Многоразовые игольчатые электроды предварительно стерилизуют в автоклаве или с помощью других методов стерилизации согласно инструкции. Существуют электроды разной длины, но наиболее часто используют электроды длиной 25, 37–40, 50 мм, которые можно различить по разному цвету наконечника (соответственно зеленый, синий, красный).
Регистрируют потенциалы двигательных единиц (ПДЕ), генерируемые при минимальном произвольном напряжении мышцы, достаточном для идентифицикации отдельных ПДЕ. Если больной будет слишком сильно напрягать мышцу, на экране появится слишком много ПДЕ, и проанализировать каждый из них будет невозможно. ПДЕ регистрируют при усилении 200–500 мкВ и 5–10 мс на деление. При выборе ПДЕ для анализа необходимо соблюдать определенные правила их отбора: ПДЕ должен повторяться три и более раз в абсолютно одинаковой форме, время нарастания ПДЕ не должно превышать 500 мкс (т.е. ПДЕ должен иметь острый пик). Для определения функционального состояния мышцы необходимо набрать и проанализировать 20 различных ПДЕ из разных точек мышцы (в зоне ее двигательной точки).
После введения электрода в полностью расслабленную мышцу и каждый раз при его перемещении в мышце по определенной схеме следят за возможным появлением спонтанной активности, которую регистрируют при усилении 50 мкВ и 20 мс на деление. Проводят либо количественный анализ выявляемой спонтанной активности (подсчет числа потенциалов спонтанной активности в каждой мышце), который особенно важен при наблюдении за состоянием больного в динамике и при определении эффективности терапии, либо выявляют ее общую характеристику (выраженная, средней выраженности, единичная). При представлении полученных результатов в таблице можно обозначать выраженность спонтанной активности крестиками, где «+» означает единичную спонтанную активность любого вида, «++» — средней выраженности, «+++» — выраженную.
В каждой точке мышцы отбирают не более четырех-пяти ПДЕ и анализируют их параметры: амплитуду (измеряется автоматически), длительность и полифазию ПДЕ.
Интерпретация результатов
ДЕ является структурно-функциональным элементом скелетной мышцы. Ее образуют двигательный мотонейрон, находящийся в переднем роге серого вещества спинного мозга, его аксон, выходящий в виде миелинизированного нервного волокна в составе двигательного корешка, и группа мышечных волокон, образующих с помощью синапса контакт с лишенными миелиновой оболочки многочисленными разветвлениями этого аксона — терминалями (рис. 2.129).
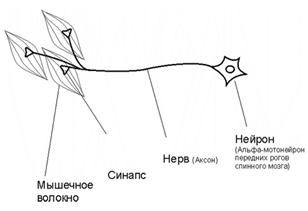
Каждое мышечное волокно мышцы имеет свою собственную терминаль, входит в состав только одной ДЕ и имеет свой собственный синапс. Аксоны начинают интенсивно ветвиться на уровне нескольких сантиметров до мышцы, чтобы обеспечить иннервацию каждого мышечного волокна, входящего в состав данной ДЕ. Мотонейрон генерирует нервный импульс, который передается по аксону, усиливается в синапсе и вызывает сокращение всех мышечных волокон, принадлежащих данной ДЕ по принципу «все или ничего». Суммарный биоэлектрический потенциал, регистрируемый при таком сокращении мышечных волокон, и называется потенциалом двигательной единицы.
2.5.3.11. Потенциалы двигательных единиц
Суждение о состоянии ДЕ скелетных мышц человека получают на основании анализа средних величин длительности (основной параметр) и амплитуды 20 ПДЕ. Форма ПДЕ оценивается с точки зрения их полифазии. Каждый ПДЕ формируется в результате алгебраического сложения потенциалов всех мышечных волокон, входящих в состав ДЕ, которая функционирует как единое целое.
При распространении волны возбуждения по мышечным волокнам по направлению к электроду на экране монитора появляется трехфазный потенциал: первое отклонение позитивное, затем идет быстрый негативный пик, а заканчивается потенциал третьим, вновь позитивным отклонением. Эти фазы могут иметь различные амплитуду, длительность и площадь, что зависит от того, как отводящая поверхность электрода расположена по отношению к мышечным волокнам центральной части регистрируемой ДЕ.
Параметры ПДЕ отражают размеры ДЕ, количество, взаимное расположение мышечных волокон и плотность их распределения в каждой конкретной ДЕ.
Длительность потенциалов двигательных единиц в норме
Основным параметром ПДЕ является его продолжительность, или длительность, измеряемая как время в миллисекундах от начала отклонения сигнала от осевой линии до полного возвращения к ней (рис. 2.130).

Длительность ПДЕ у здорового человека зависит от мышцы и возраста. С возрастом длительность ПДЕ постепенно увеличивается. Чтобы создать унифицированные критерии нормы при исследовании ПДЕ, разработаны специальные таблицы нормальных средних величин длительности для разных мышц людей разного возраста. Фрагмент таких таблиц приведен в табл. 2.20.
Таблица 2.20. Средняя длительность потенциалов двигательных единиц в наиболее часто исследуемых мышцах здоровых людей, мс
| Возраст, лет | M. deltoideus | M. extensor digiti comm. | M. abducto pollicis brevis | M. interosseus dorsalis | M. abductor digiti minimi manus | M. vastus lateralis | M. tibialis anterior | M. gastrocnemius |
|---|---|---|---|---|---|---|---|---|
0 |
7,6 |
7,1 |
6,2 |
7,2 |
6,2 |
7,9 |
7,5 |
7,2 |
3 |
8,1 |
7,6 |
6,8 |
7,5 |
6,8 |
8,4 |
8,0 |
7,7 |
5 |
8,4 |
7,8 |
7,1 |
7,9 |
7,0 |
8,7 |
8,2 |
8,0 |
8 |
8,8 |
8,2 |
7,4 |
8,3 |
7,3 |
9,0 |
8,5 |
8,4 |
10 |
9,0 |
8,4 |
7,6 |
8,7 |
7,6 |
9,3 |
8,8 |
8,6 |
13 |
9,3 |
8,6 |
7,8 |
8,9 |
7,9 |
9,6 |
9,0 |
8,8 |
15 |
9,5 |
8,8 |
8,2 |
9,0 |
8,2 |
9,8 |
9,3 |
8,9 |
18 |
9,7 |
9,0 |
8,5 |
9,2 |
8,5 |
10,1 |
9,5 |
9,2 |
20 |
10,0 |
9,2 |
9,0 |
9,4 |
9,0 |
10,2 |
10,0 |
9,4 |
25 |
10,2 |
9,5 |
9,2 |
9,5 |
9,2 |
10,4 |
10,3 |
9,6 |
30 |
10,4 |
9,8 |
9,3 |
9,8 |
9,3 |
10,8 |
10,6 |
9,8 |
35 |
10,8 |
10,0 |
9,3 |
9,9 |
9,3 |
11,2 |
10,8 |
10,0 |
40 |
11,0 |
10,2 |
9,3 |
10,0 |
9,3 |
11,4 |
11,0 |
10,2 |
45 |
11,1 |
10,3 |
9,4 |
10,0 |
9,4 |
11,5 |
11,2 |
10,4 |
50 |
11,3 |
10,5 |
9,4 |
10,0 |
9,4 |
11,7 |
11,3 |
10,5 |
55 |
11,5 |
10,7 |
9,4 |
10,1 |
9,4 |
11,9 |
11,5 |
10,7 |
60 |
11,7 |
10,9 |
9,5 |
10,1 |
9,5 |
12,0 |
11,7 |
10,9 |
65 |
12,0 |
11,1 |
9,5 |
10,2 |
9,5 |
12,2 |
11,8 |
11,0 |
70 |
12,1 |
11,2 |
9,5 |
10,3 |
9,5 |
12,2 |
12,0 |
11,0 |
75 |
12,2 |
11,3 |
9,5 |
10,3 |
9,5 |
12,4 |
12,0 |
11,1 |
80 |
12,3 |
11,4 |
9,5 |
10,3 |
9,5 |
12,4 |
12,0 |
11,1 |
Мерой оценки состояния ДЕ в мышце является средняя длительность 20 различных ПДЕ, зарегистрированных в разных точках изучаемой мышцы. Полученную при исследовании среднюю величину сравнивают с соответствующим показателем, представленным в таблице, и вычисляют отклонение от нормы (в процентах). Среднюю длительность ПДЕ считают нормальной, если она укладывается в границы ±12% величины, приведенной в таблице (за рубежом средняя длительность ПДЕ считается нормальной, если она укладывается в границы ±20%, однако проведенные нами исследования не выявили такого отклонения от нормы ни у одного здорового человека).
Длительность потенциалов двигательных единиц при патологии
Основная закономерность изменения длительности ПДЕ в условиях патологии заключается в том, что она увеличивается при неврогенных заболеваниях и уменьшается при синаптической и первично-мышечной патологии.
Чтобы более тщательно оценить степень изменения ПДЕ в мышцах при различных поражениях периферического нейромоторного аппарата, для каждой мышцы используют гистограмму распределения ПДЕ по длительности, так как их средняя величина может находиться в границах нормальных отклонений при явной патологии мышцы, если, например, регистрируются ПДЕ уменьшенной и увеличенной длительности. В норме гистограмма имеет форму нормального распределения, максимум которой совпадает со средней длительностью ПДЕ для данной мышцы. При любой патологии периферического нейромоторного аппарата форма гистограммы значительно меняется. Гистограмма распределения по длительности формируется автоматически во всех выпускаемых в настоящее время электромиографах.
Электромиографические стадии патологического процесса
На основании изменения длительности ПДЕ при заболеваниях мотонейронов спинного мозга, когда в относительно короткий срок можно проследить все происходящие в мышцах изменения, выделено шесть ЭМГ-стадий, отражающих общие закономерности перестройки ДЕ при ДРП, от самого начала заболевания до практически полной гибели мышцы (Гехт Б.М. и др., 1997; Касаткина Л.Ф., Гильванова О.В., 2010).
При всех неврогенных заболеваниях происходит гибель большего или меньшего количества мотонейронов или их аксонов. Сохранившиеся мотонейроны иннервируют лишенные нервного контроля «чужие» мышечные волокна, тем самым увеличивая их количество в своих ДЕ. На ЭМГ этот процесс проявляется постепенным увеличением параметров потенциалов таких ДЕ. Весь цикл изменения гистограммы распределения ПДЕ по длительности при нейрональных заболеваниях условно укладывается в пять ЭМГ-стадий (рис. 2.131), отражающих процесс компенсаторной иннервации в мышцах. Такое разделение, хотя и является условным, но помогает понять и проследить все этапы развития ДРП в каждой конкретной мышце, так как каждая стадия отражает определенную фазу реиннервации и степень ее выраженности. Шестую стадию представлять в виде гистограммы нецелесообразно, так как она отражает конечный пункт «обратного» процесса, то есть процесс декомпенсации и разрушения ДЕ мышцы.
Среди специалистов нашей страны эти стадии получили широкое распространение при диагностике различных нервно-мышечных заболеваний. Они включены в компьютерную программу отечественных электромиографов, что позволяет осуществлять автоматическое построение гистограмм с обозначением стадии процесса. Изменение стадии в ту или другую сторону при повторном обследовании больного показывает, каковы дальнейшие перспективы развития ДРП.
-
I стадия: средняя длительность ПДЕ уменьшена на 13–20%. Эта стадия отражает самую начальную фазу заболевания, когда денервация уже началась, а процесс реиннервации электромиографически еще не проявляется. Из состава некоторых ДЕ выпадает какая-то часть денервированных мышечных волокон, лишенных импульсного влияния по причине патологии либо мотонейрона, либо его аксона. Количество мышечных волокон в таких ДЕ уменьшается, что приводит к снижению длительности отдельных потенциалов.
В I очень короткой стадии появляется некоторое количество более узких, чем в здоровой мышце, потенциалов, что вызывает небольшое уменьшение средней длительности. Гистограмма распределения ПДЕ начинает смещаться влево, в сторону меньших величин.
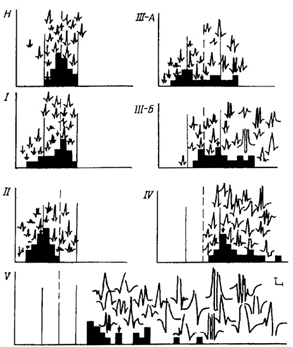 Рис. 2.131. Пять стадий денервационно-реиннервационного процесса в дельтовидной мышце больного с боковым амиотрофическим склерозом в процессе длительного наблюдения. Н (норма) — 20 потенциалов двигательных единиц и гистограмма их распределения по длительности в дельтовидной мышце здорового человека; I, II, IIIA, IIIБ, IV, V — потенциалы двигательных единиц и гистограммы их распределения в соответствующей стадии электромиографии. По оси абсцисс — длительность потенциалов двигательных единиц, по оси ординат — количество потенциалов двигательных единиц данной длительности. Сплошные линии — границы нормы, прерывистые линии — средняя длительность потенциалов двигательных единиц в норме, стрелками указаны средние величины длительности потенциалов двигательных единиц в данной мышце больного в разные периоды обследования (последовательно от I до V стадии). Масштаб: по вертикали 500 мкВ, по горизонтали 10 мс
Рис. 2.131. Пять стадий денервационно-реиннервационного процесса в дельтовидной мышце больного с боковым амиотрофическим склерозом в процессе длительного наблюдения. Н (норма) — 20 потенциалов двигательных единиц и гистограмма их распределения по длительности в дельтовидной мышце здорового человека; I, II, IIIA, IIIБ, IV, V — потенциалы двигательных единиц и гистограммы их распределения в соответствующей стадии электромиографии. По оси абсцисс — длительность потенциалов двигательных единиц, по оси ординат — количество потенциалов двигательных единиц данной длительности. Сплошные линии — границы нормы, прерывистые линии — средняя длительность потенциалов двигательных единиц в норме, стрелками указаны средние величины длительности потенциалов двигательных единиц в данной мышце больного в разные периоды обследования (последовательно от I до V стадии). Масштаб: по вертикали 500 мкВ, по горизонтали 10 мс -
II стадия: средняя длительность ПДЕ уменьшена на 21% и более. При ДРП эту стадию отмечают крайне редко и только в тех случаях, когда по каким-то причинам реиннервация не наступает или подавляется каким-то фактором (например, алкоголем, облучением и т.п.), а денервация, наоборот, нарастает и происходит массивная гибель мышечных волокон в ДЕ. Это приводит к тому, что большинство или практически все ПДЕ по длительности становятся меньше нормальных, в связи с чем средняя величина длительности продолжает уменьшаться. Гистограмма распределения ПДЕ значительно смещается в сторону меньших величин. I–II стадии отражают изменения в ДЕ, обусловленные уменьшением в них количества функционирующих мышечных волокон.
-
III стадия: средняя длительность ПДЕ находится в границах ±20% нормы для данной мышцы. Эта стадия характеризуется появлением определенного количества потенциалов увеличенной длительности, в норме не выявляемых. Появление этих ПДЕ свидетельствует о начале реиннервации, то есть денервированные мышечные волокна начинают включаться в состав других ДЕ, в связи с чем параметры их потенциалов увеличиваются. В мышце одновременно регистрируют ПДЕ как уменьшенной и нормальной, так и увеличенной длительности, количество укрупненных ПДЕ в мышце варьирует от одного до нескольких. Средняя величина длительности ПДЕ в III стадии может быть нормальной, но вид гистограммы отличается от нормы. Она не имеет форму нормального распределения, а «уплощена», растянута и начинает смещаться вправо, в сторону больших величин. Предложено разделять III стадию на две подгруппы — IIIА и IIIБ. Они различаются лишь тем, что при стадии IIIА средняя длительность ПДЕ уменьшена на 1–20%, а при стадии IIIБ она либо полностью совпадает со средней величиной нормы, либо увеличена на 1–20%. В стадии IIIБ регистрируют несколько большее количество ПДЕ увеличенной длительности, чем на стадии IIIА. Практика показала, что такое деление третьей стадии на две подгруппы особого значения не имеет. Фактически III стадия просто означает появление первых ЭМГ признаков реиннервации в мышце.
-
IV стадия: средняя длительность ПДЕ увеличена на 21–40%. Эта стадия характеризуется увеличением средней длительности ПДЕ за счет появления, наряду с нормальными ПДЕ, большого количества потенциалов увеличенной длительности. ПДЕ уменьшенной длительности в данной стадии регистрируют крайне редко. Гистограмма смещена вправо, в сторону больших величин, ее форма различна и зависит от соотношения ПДЕ нормальной и увеличенной длительности.
-
V стадия: средняя длительность ПДЕ увеличена на 41% и более. Эта стадия характеризуется наличием преимущественно крупных и «гигантских» ПДЕ, а ПДЕ нормальной длительности практически отсутствуют. Гистограмма значительно смещена вправо, растянута и, как правило, разомкнута. Эта стадия отражает максимальный объем реиннервации в мышце, а также ее эффективность: чем больше гигантских ПДЕ, тем эффективнее реиннервация.
-
VI стадия: средняя длительность ПДЕ находится в границах нормы или уменьшена более чем на 12%. Эта стадия характеризуется наличием измененных по форме ПДЕ (потенциалы разрушающихся ДЕ). Их параметры формально могут быть нормальными или сниженными, но форма ПДЕ изменена: потенциалы не имеют острых пиков, растянуты, округлены, время нарастания потенциалов резко увеличено. Эта стадия отмечается на последнем этапе декомпенсации ДРП, когда большая часть мотонейронов спинного мозга уже погибла и происходит интенсивная гибель остальных.
Декомпенсация процесса начинается с того момента, когда процесс денервации нарастает, а источников иннервации становится все меньше и меньше. На ЭМГ стадия декомпенсации характеризуется следующими признаками: параметры ПДЕ начинают уменьшаться, исчезают гигантские ПДЕ, интенсивность денервации и распада мышечных волокон резко нарастает, появляются признаки гибели многих рядом лежащих мышечных волокон [гигантские положительные острые волны (ПОВ)]. Эти признаки свидетельствуют о том, что в данной мышце мотонейроны исчерпали свои возможности к спраутингу в результате функциональной неполноценности и уже не способны осуществить полноценный контроль за своими мышечными волокнами. Вследствие этого количество мышечных волокон в ДЕ прогрессирующе сокращается, нарушаются механизмы проведения импульса, потенциалы таких ДЕ округляются, падает их амплитуда, уменьшается длительность. Построение гистограммы в этой стадии процесса нецелесообразно, поскольку она, так же как и средняя длительность ПДЕ, уже не отражает истинного состояния мышцы. Основной признак VI стадии — изменение формы всех ПДЕ, а ее конечный результат — замещение мышцы соединительной тканью.
ЭМГ-стадии можно использовать не только при неврогенных, но и при различных первично-мышечных заболеваниях, чтобы охарактеризовать глубину патологии мышцы. Но в этом случае ЭМГ-стадия отражает не ДРП, а выраженность патологии и называть ее следует «ЭМГ-стадией патологического процесса». При первично-мышечных заболеваниях, как правило, выявляют I и II стадии, но при прогрессирующих мышечных дистрофиях и полимиозите на определенном этапе болезни могут появляться резко полифазные ПДЕ увеличенной длительности, ПДЕ с сателлитами, что значительно увеличивает и среднюю ее величину, соответствующую III или даже IV ЭМГ стадии патологического процесса. Однако амплитуда таких ПДЕ повышена в незначительной степени в отличие от ПДЕ такой длительности, выявляемых при неврогенных заболеваниях.
Диагностическая значимость ЭМГ-стадий
-
При нейрональных заболеваниях у одного и того же больного в разных мышцах часто обнаруживают различные ЭМГ-стадии — от III до V. Первую и особенно вторую стадию выявляют очень редко — в самом начале заболевания, и лишь в отдельных мышцах.
-
При аксональных и демиелинизирующих заболеваниях чаще обнаруживают III и IV, реже — I, а II стадия может наблюдаться в самой начальной фазе демиелизирующего процесса, что иногда приводит к неправильной интерпретации результатов, расцениваемых обследователем как первично-мышечные изменения. При гибели значительного количества аксонов при длительно протекающей ХВДП в отдельных самых пораженных мышцах выявляют V стадию.
-
При первично-мышечных заболеваниях имеет место выпадение мышечных волокон из состава ДЕ вследствие какой-либо патологии мышцы: уменьшения диаметра мышечных волокон, их расщепления, фрагментации или другого их повреждения, сокращающего численность мышечных волокон в ДЕ или уменьшающего объем мышцы. Все это приводит к уменьшению (укорочению) длительности ПДЕ. Поэтому при большинстве первично-мышечных заболеваний, а также при патологии синапса (при миастении, миастенических синдромах) выявляют I и II стадии, при полимиозите — сначала только I и II, а при выздоровлении — III и даже IV стадии в случае вторичного вовлечения в процесс терминалей аксона.
В последние годы значимость стадий значительно снизилась в связи с тем, что клиницистам-неврологам не известна сущность ЭМГ-стадий, и это непонимание постепенно свело на нет применение стадий при оценке результатов обследования.
Амплитуда потенциалов двигательных единиц
Амплитуда — вспомогательный, но очень важный параметр при анализе ПДЕ. Ее измеряют «от пика до пика», то есть от самой низкой точки позитивного до самой высокой точки негативного пика. При регистрации ПДЕ на экране их амплитуда определяется автоматически. В каждой мышце определяют среднюю и максимальную величину амплитуды.
Средние величины амплитуды ПДЕ в проксимальных мышцах здоровых людей в большинстве случаев составляют 500–700 мкВ, в дистальных — 600–800 мкВ, при этом величина максимальной амплитуды не превышает 1500–1700 мкВ, и таких ПДЕ в мышце не должно быть более трех. Эти показатели весьма условны и могут в некоторой степени варьировать. У детей 8–12 лет средняя амплитуда ПДЕ, как правило, находится в пределах 300–400 мкВ, а максимальная не превышает 800 мкВ; у детей более старшего возраста эти показатели составляют 500 и 1000 мкВ соответственно. В мышцах лица амплитуда ПДЕ значительно ниже.
У спортсменов в тренированных мышцах регистрируют повышенную амплитуду ПДЕ, вызванную перестройкой ДЕ в связи с постоянной повышенной нагрузкой на мышцы. Поэтому повышение средней амплитуды ПДЕ в мышцах здоровых лиц, занимающихся спортом, нельзя считать патологией, и степень ее повышения не столь значительна.
При всех неврогенных заболеваниях амплитуда ПДЕ, как правило, увеличивается в соответствии с увеличением длительности: чем больше длительность потенциала, тем выше его амплитуда (рис. 2.132).
К увеличению амплитуды ПДЕ приводит перестройка ДЕ в мышце, нарастание концентрации мышечных волокон в зоне отведения электрода, синхронизация их активности, а также увеличение диаметра мышечных волокон. Самое значительное увеличение амплитуды ПДЕ наблюдают при нейрональных заболеваниях, таких как спинальная амиотрофия и последствия перенесенного полиомиелита, а также при нейрональной форме болезни Шарко–Мари–Тута. Амплитуда ПДЕ служит дополнительным критерием для диагностики неврогенного характера патологии в мышцах. Увеличение как средней, так и максимальной амплитуды ПДЕ иногда наблюдают и при некоторых первично-мышечных заболеваниях, таких как воспалительная миопатия (полимиозит), первичная мышечная дистрофия, дистрофическая миотония (ДМ) и др.
Форма потенциалов двигательных единиц
Форма ПДЕ зависит от структуры ДЕ, степени синхронизации потенциалов ее мышечных волокон, положения электрода по отношению к мышечным волокнам анализируемых ДЕ и их иннервационным зонам. Форма потенциала диагностического значения не имеет.
В клинической практике форму ПДЕ анализируют с точки зрения количества фаз и/или турнов в потенциале. Каждое позитивно-негативное отклонение потенциала, доходящее до изолинии и пересекающее ее, называется фазой, а позитивно-негативное отклонение потенциала, не доходящее до изолинии, — турном.
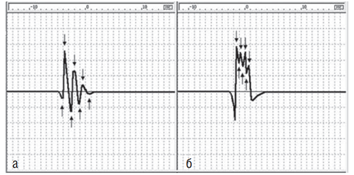
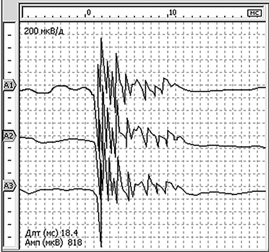
Полифазным считается потенциал, имеющий пять фаз и более и пересекающий осевую линию не менее четырех раз (рис. 2.133, а). В потенциале могут быть дополнительные турны, не пересекающие осевую линию (рис. 2.133, б). Турны бывают как в негативной, так и в позитивной части потенциала.В мышцах здоровых людей ПДЕ, как правило, представлены трехфазными колебаниями потенциала (см. рис. 2.130), однако при регистрации ПДЕ в зоне концевой пластинки он может иметь две фазы, утрачивая свою начальную позитивную часть.
В норме количество полифазных ПДЕ не превышает 5–15%. Увеличение количества полифазных ПДЕ рассматривают как признак нарушения структуры ДЕ вследствие наличия какого-то патологического процесса. Полифазные и политурновые ПДЕ регистрируют как при нейрональных и аксональных, так и при первично-мышечных заболеваниях (рис. 2.134).
2.5.3.12. Спонтанная активность
В нормальных условиях при неподвижном положении электрода в расслабленной мышце здорового человека какой-либо электрической активности не возникает. При патологии появляется спонтанная активность мышечных волокон или ДЕ. Спонтанная активность не зависит от воли больного, он не может ее прекратить или вызвать произвольно.
Спонтанная активность мышечных волокон
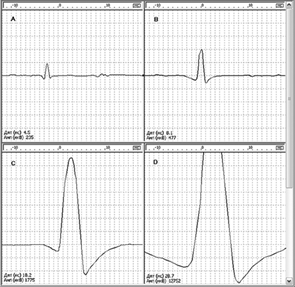
К спонтанной активности мышечных волокон относят потенциалы фибрилляций (ПФ) и положительные острые волны (ПОВ). ПФ и ПОВ регистрируют исключительно в условиях патологии при введении в мышцу концентрического игольчатого электрода (рис. 2.135). ПФ — потенциал одного мышечного волокна, ПОВ — медленное колебание, наступающее вслед за быстрым положительным отклонением, не имеющее острого негативного пика. ПОВ отражает участие как одного, так и нескольких рядом лежащих волокон.
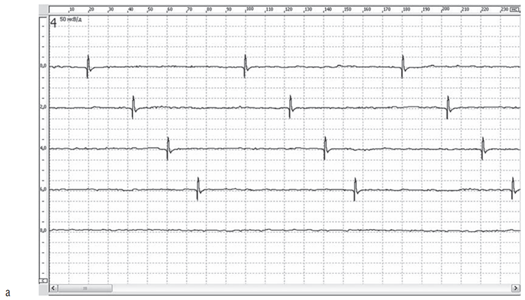
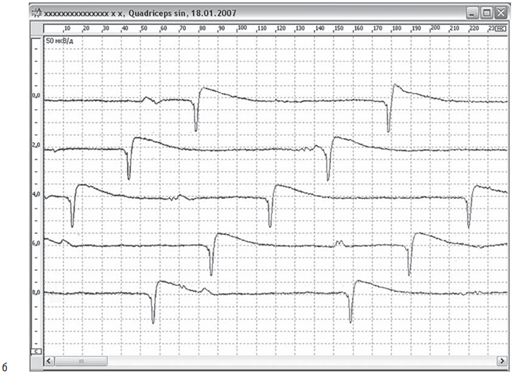
Изучение спонтанной активности мышечных волокон в условиях клинического исследования пациента — наиболее удобный электрофизиологический метод, позволяющий судить о степени полноценности и устойчивости нервных влияний на мышечные волокна скелетной мышцы при ее патологии.
Спонтанная активность мышечных волокон может возникать при любой патологии периферического нейромоторного аппарата. При неврогенных заболеваниях, а также при патологии синапса (миастения и миастенические синдромы) спонтанная активность мышечных волокон отражает процесс их денервации. При большинстве первично-мышечных заболеваний спонтанная активность мышечных волокон отражает какое-либо повреждение мышечных волокон (их расщепление, фрагментацию и т.п.), а также их патологию, вызванную воспалительным процессом (при воспалительных миопатиях — полимиозите, дерматомиозите).
И в том, и в другом случае ПФ свидетельствуют о наличии текущего процесса в мышце, ПОВ — о его последствиях; в норме ни ПФ, ни ПОВ никогда не выявляют.
-
Длительность ПФ составляет 1–5 мс (какого-либо диагностического значения она не имеет), а амплитуда колеблется в очень широких пределах, от 30 до 2500 мкВ, высокоамплитудные ПФ появляются обычно у больных с хронически протекающими заболеваниями. Сроки появления ПФ зависят от места поражения нерва. В большинстве случаев они возникают через 7–20 дней после денервации.
-
Если по каким-либо причинам реиннервация денервированного мышечного волокна не наступила, оно со временем погибает, генерируя ПОВ, которые считают ЭМГ-признаком гибели денервированного мышечного волокна, не получившего утраченную им ранее иннервацию. По числу ПФ и ПОВ, зарегистрированных в каждой мышце, можно косвенно судить о степени и глубине ее денервации или объеме погибших мышечных волокон. Длительность ПОВ составляет от 1,5 до 70 мс (в большинстве случаев до 10 мс). Так называемые «гигантские» ПОВ длительностью более 20 мс выявляют при продолжительной денервации большого количества рядом лежащих мышечных волокон, а также при полимиозите. Амплитуда ПОВ колеблется, как правило, в пределах от 10 до 1800 мкВ. ПОВ большой амплитуды и длительности чаще выявляются в более поздних стадиях денервации («гигантские» ПОВ). ПОВ начинают регистрировать через 16–30 дней после первого появления ПФ, они могут сохраняться в мышце в течение длительного времени. Как правило, у больных с воспалительными поражениями периферических нервов ПОВ выявляют позднее, чем у больных с травматическими поражениями.
ПФ и ПОВ наиболее быстро реагируют на начало терапии: если она эффективна, выраженность ПФ и ПОВ снижается уже через 2 нед после начала терапии. Наоборот, при неэффективности или недостаточной эффективности лечения их выраженность нарастает, что позволяет использовать анализ ПФ и ПОВ в качестве индикатора эффективности применяемых препаратов.
В зарубежных лабораториях применяют следующую методику оценки выраженности спонтанной активности. Используют схему от нуля (0) до четырех (4). Ноль — спонтанная активность (или ее отдельный вид) отсутствует. Если выявлен один ПФ (или одна ПОВ) только в одной точке мышцы, обозначение будет +1. Если ПФ/ПОВ выявлены в двух-трех точках мышцы и на экране их 1–2, обозначение будет +2, если на экране их несколько, обозначение будет +3. Если они полностью заполняют экран и выявлены во всех точках мышцы, обозначение будет +4. Однако такая оценка очень субъективна и не дает возможности точно определить выраженность спонтанной активности в мышце.
Миотонические и сложные повторяющиеся разряды
Миотонические и сложные повторяющиеся разряды (сomplex repetitive discharges), которые раньше называли псевдомиотоническими, разрядами высокой частоты, также относятся к спонтанной активности мышечных волокон. Миотонические и сложные повторяющиеся разряды характеризуются рядом особенностей, главная из которых — высокая повторяемость элементов, составляющих разряд, то есть высокая частота потенциалов в разряде.
-
Миотонические разряды — ЭМГ-феномен, выявляемый у больных при различных формах миотонии. При прослушивании он напоминает звук «пикирующего бомбардировщика». На экране монитора эти разряды выглядят как повторяющиеся потенциалы с постепенно падающей амплитудой, с прогрессивно увеличивающимися интервалами (что и вызывает снижение высоты звука, см. рис. 2.136). Миотонические разряды иногда наблюдают при некоторых формах эндокринной патологии (например, гипотиреозе). Возникают миотонические разряды либо спонтанно, либо после любого механического раздражения мышцы — введенным в нее игольчатым электродом, простым постукиванием по мышце.
-
Сложные повторяющиеся разряды (разряды высокой частоты) регистрируют при некоторых нервно-мышечных заболеваниях, как связанных, так и не связанных с денервацией мышечных волокон (рис. 2.137). Их считают следствием эфаптической передачи возбуждения при снижении изолирующих свойств мембраны мышечных волокон, создающих предпосылку для распространения возбуждения от одного волокна к рядом лежащему: пейсмекер одного из волокон задает ритм импульсации, который навязывается рядом лежащим волокнам, чем и обусловлена своеобразная форма комплексов. Разряды начинаются и прекращаются внезапно без изменения частоты следования их составляющих. Их основным отличием от миотонических разрядов является отсутствие падения амплитуды составляющих. Наблюдают сложные повторяющиеся разряды при различных формах миопатии (особенно при ПМД), полимиозитах, денервационных синдромах (в поздних стадиях реиннервации), при спинальных и невральных (болезни Шарко–Мари–Тута) амиотрофиях, эндокринной патологии, травмах или компрессии нерва, корешковой дисфункции и некоторых других заболеваниях.
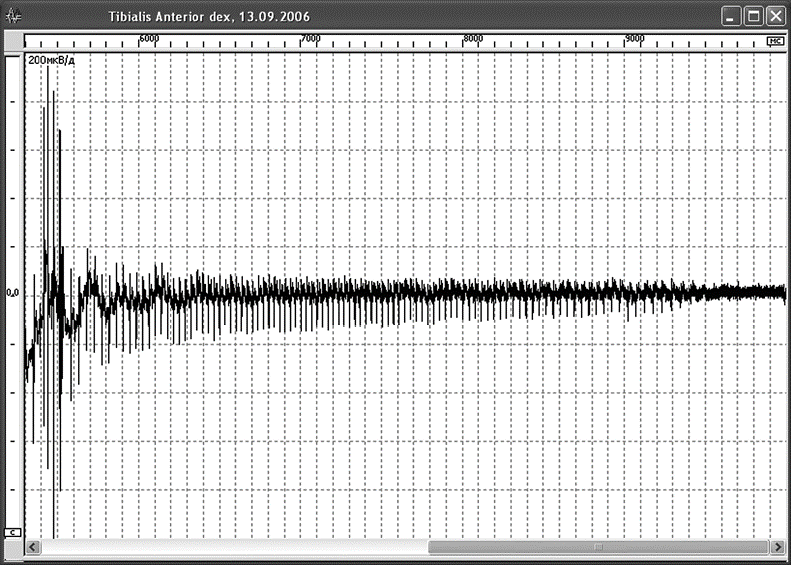
Спонтанная активность двигательных единиц
Спонтанная активность ДЕ представлена потенциалами фасцикуляций. Потенциалами фасцикуляций называют возникающие в полностью расслабленной мышце спонтанные сокращения всей ДЕ. Их возникновение связано с болезнями мотонейрона, его перегрузками мышечными волокнами, раздражением какого-либо из его участков, функционально-морфологическими перестройками (рис. 2.138).
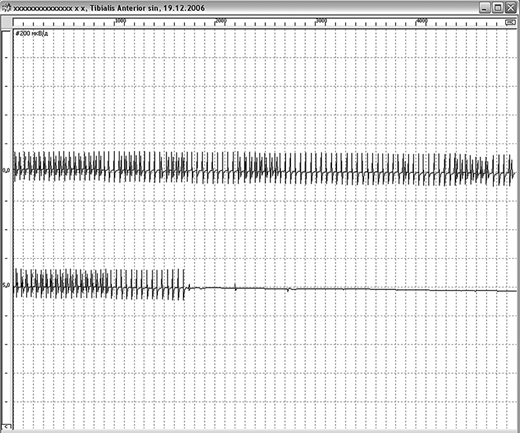
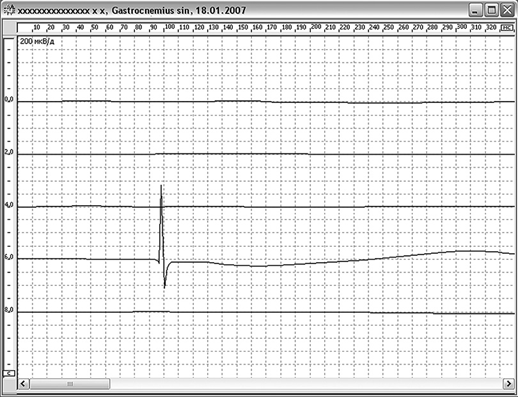
Появление множественных потенциалов фасцикуляций в мышцах считают одним из основных признаков поражения мотонейронов спинного мозга. Исключение составляют «доброкачественные» потенциалы фасцикуляций, иногда выявляемые у больных, которые жалуются на постоянные подергивания в мышцах, но не отмечают мышечной слабости и других симптомов.
Единичные потенциалы фасцикуляций можно выявить при всех неврогенных и даже первично-мышечных заболеваниях, таких как миотония, полимиозит, эндокринные, метаболические и митохондриальные миопатии. Однако в отличие от заболеваний мотонейронов их количество в мышце очень невелико.
Описаны потенциалы фасцикуляций, возникающие и у здоровых людей: у спортсменов высокой квалификации после изнуряющей физической нагрузки, легко возбудимых людей, беременных, пожилых людей, их параметры, как правило, нормальны.
Параметры потенциалов фасцикуляций (амплитуда и длительность) соответствуют параметрам ПДЕ, регистрируемым в данной мышце, и могут изменяться в соответствии с изменениями ПДЕ в процессе развития заболевания.
2.5.3.13. Игольчатая электромиография в диагностике заболеваний мотонейронов спинного мозга и периферических нервов
При любой неврогенной патологии имеет место ДРП, выраженность которого зависит от степени повреждения источников иннервации и от того, на каком уровне периферического нейромоторного аппарата — нейрональном или аксональном — произошло поражение. И в том, и в другом случае утраченная функция восстанавливается за счет сохранившихся нервных волокон, причем последние начинают интенсивно ветвиться, формируя многочисленные ростки, направляющиеся к денервированным мышечным волокнам. Это ветвление получило в литературе название «спраутинг» (англ. «sprout» — пускать ростки, ветвиться).
Существуют два основных вида спраутинга — коллатеральный и терминальный. Коллатеральный спраутинг — ветвление аксонов в области перехватов Ранвье, терминальный — ветвление конечного, немиелинизированного участка аксона. Показано, что характер спраутинга зависит от характера фактора, вызвавшего нарушение нервного контроля. Например, при ботулинической интоксикации ветвление происходит исключительно в зоне терминалей, а при хирургической денервации имеет место как терминальный, так и коллатеральный спраутинг.
На ЭМГ эти состояния ДЕ на различных этапах реиннервационного процесса характеризуются появлением ПДЕ увеличенной длительности и повышенной амплитуды. Исключением являются самые начальные стадии бульбарной формы БАС, при которой параметры ПДЕ в течение нескольких месяцев находятся в границах нормальных значений.
ЭМГ-критерии заболеваний мотонейронов спинного мозга
-
Наличие потенциалов фасцикуляций (основной критерий поражения мотонейронов спинного мозга, без которых диагноз ставится под сомнение).
-
Увеличение параметров ПДЕ и их полифазия, отражающие степень выраженности процесса реиннервации.
-
Появление в мышцах спонтанной активности мышечных волокон — ПФ и ПОВ, указывающих на наличие текущего денервационного процесса.
Потенциалы фасцикуляций — обязательный электрофизиологический признак поражения мотонейронов спинного мозга. Их обнаруживают уже в самых ранних стадиях патологического процесса, еще до появления признаков денервации и укрупнения параметров ПДЕ.
В связи с тем что нейрональные заболевания подразумевают постоянный текущий процесс денервации и реиннервации, когда одновременно погибает большое количество мотонейронов и разрушается соответственное число ДЕ, ПДЕ постепенно укрупняются, увеличивается их длительность и амплитуда, появляются гигантские ПДЕ (гигантским считается ПДЕ, амплитуда которого 5000 мкВ и более). Степень увеличения зависит от давности и стадии болезни.
Выраженность ПФ и ПОВ зависит от остроты патологического процесса и степени денервации мышцы. При быстропрогрессирующих заболеваниях (например, БАС) ПФ и ПОВ обнаруживают в большинстве мышц, при медленно прогрессирующих (некоторые формы спинальных амиотрофий) — только в половине мышц, а при постполиомиелитическом синдроме — менее чем в трети.
ЭМГ-критерии заболеваний аксонов периферических нервов
Игольчатая ЭМГ в диагностике заболеваний периферических нервов является дополнительным, но необходимым методом обследования, определяющим степень поражения мышцы, иннервируемой пораженным нервом. Это исследование позволяет уточнить наличие признаков денервации (ПФ), степень утраты мышечных волокон в мышце (общее количество ПОВ и наличие гигантских ПОВ), выраженность реиннервации и ее эффективность (степень увеличения параметров ПДЕ, максимальная величина амплитуды ПДЕ в мышце).
Основные ЭМГ признаки аксонального процесса:
При поражении аксонов периферических нервов (различные ПНП) также имеет место ДРП, но его выраженность значительно меньше, чем при нейрональных заболеваниях. Следовательно, ПДЕ увеличены в значительно меньшей степени, чем при нейрональных заболеваниях. Тем не менее основное правило изменения ПДЕ при неврогенных заболеваниях распространяется и на поражение аксонов двигательных нервов (то есть степень увеличения параметров ПДЕ и их полифазия зависят от степени поражения нерва и выраженности реиннервации). Исключение составляют патологические состояния, сопровождающиеся быстрой гибелью аксонов двигательных нервов вследствие травмы (или какого-то другого патологического состояния, приводящего к одновременной гибели большого количества аксонов). В этом случае появляются такие же гигантские ПДЕ (амплитудой более 5000 мкВ), что и при нейрональных заболеваниях. Такие ПДЕ, например, часто наблюдают при длительно текущих формах аксональной патологии, ХВДП, невральных амиотрофиях.
Если при аксональных ПНП в первую очередь увеличивается амплитуда ПДЕ, то при демиелинизирующем процессе с ухудшением функционального состояния мышцы (уменьшением ее силы) амплитуда ПДЕ сначала может падать, ПДЕ регистрируются с трудом, время нарастания ПДЕ значительно увеличивается, ПДЕ по своим параметрам могут имитировать первично-мышечное заболевание. Однако постепенно начинают увеличиваться средние величины длительности ПДЕ, при этом нарастание амплитуды не соответствует увеличению длительности; значительно чаще, чем при аксональном процессе, обнаруживают полифазные ПДЕ и потенциалы фасцикуляций, а появление ПФ и ПОВ указывает на вторичное вовлечение в процесс аксонов.
2.5.3.14. Игольчатая электромиография в диагностике синаптических и первично-мышечных заболеваний
Для синаптических и первично-мышечных заболеваний типично уменьшение средней длительности ПДЕ. Степень уменьшения длительности ПДЕ коррелирует со снижением силы. В некоторых случаях параметры ПДЕ находятся в границах нормальных отклонений, а при ПМД могут быть даже увеличены (см. рис. 2.133).
Игольчатая электромиография при синаптических заболеваниях
При синаптических заболеваниях игольчатую ЭМГ считают дополнительным методом исследования. При миастении она позволяет оценить степень «заблокированности» мышечных волокон в ДЕ, определяемой по степени уменьшения средней длительности ПДЕ в обследованных мышцах. Тем не менее основная цель игольчатой ЭМГ при миастении — исключение возможной сопутствующей патологии (полимиозита, миопатии, эндокринных нарушений, различных ПНП и др.). Игольчатую ЭМГ у больных миастенией также используют, чтобы определить степень реагирования на введение антихолинэстеразных препаратов, то есть оценить изменение параметров ПДЕ при введении неостигмина метилсульфата. После введения препарата длительность ПДЕ в большинстве случаев увеличивается. Отсутствие реакции может служить указанием на так называемую миастеническую миопатию.
Основные ЭМГ критерии синаптических заболеваний:
При миастении средняя длительность ПДЕ, как правило, уменьшена незначительно (на 10–35%). Преобладающее количество ПДЕ имеет нормальную амплитуду, но в каждой мышце регистрируют несколько ПДЕ сниженной амплитуды и уменьшенной длительности. Количество полифазных ПДЕ не превышает 15–30%. Спонтанная активность отсутствует. При выявлении у больного выраженных ПФ следует думать о сочетании миастении с гипотиреозом, полимиозитом или другими заболеваниями.
Игольчатая электромиография при первично-мышечных заболеваниях
Игольчатая ЭМГ — основной электрофизиологический метод диагностики первично-мышечных заболеваний (различных миопатий). В связи с уменьшением способности ДЕ развивать достаточную силу для поддержания даже минимального усилия больному с любой первично-мышечной патологией приходится рекрутировать большое количество ДЕ. Этим определяется особенность ЭМГ у таких больных. При минимальном произвольном напряжении мышцы трудно выделить отдельные ПДЕ, на экране появляется такое множество мелких потенциалов, что это делает невозможным их идентификацию. Это так называемый миопатический паттерн ЭМГ (рис. 2.139).
При воспалительных миопатиях (полимиозите) иногда наблюдается процесс реиннервации, что может вызвать увеличение параметров ПДЕ.
Основные ЭМГ критерии первично-мышечных заболеваний:
-
уменьшение величины средней длительности ПДЕ более чем на 12%;
-
снижение амплитуды отдельных ПДЕ (средняя амплитуда может быть как сниженной, так и нормальной, а иногда и повышенной);
-
выраженная спонтанная активность мышечных волокон при воспалительной миопатии (полимиозите) или ПМД, в остальных случаях она минимальна или отсутствует.
Уменьшение средней длительности ПДЕ — кардинальный признак любого первично-мышечного заболевания. Причина этого изменения заключается в том, что при миопатиях мышечные волокна подвергаются атрофии, часть из них выпадает из состава ДЕ из-за некроза, что и приводит к уменьшению параметров ПДЕ. Уменьшение длительности большинства ПДЕ выявляют почти во всех мышцах больных с миопатиями, хотя оно более выражено в клинически наиболее пораженных проксимальных мышцах.
Гистограмма распределения ПДЕ по длительности смещается в сторону меньших величин (I или II стадия). Исключением являются ПМД: за счет резкой полифазии ПДЕ, иногда достигающей 100%, средняя длительность ПДЕ может быть значительно увеличена.
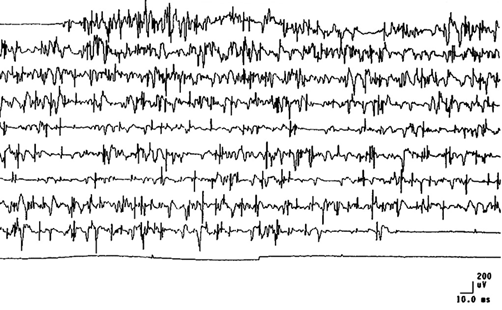
2.5.3.15. Электромиография одиночного мышечного волокна
ЭМГ одиночного мышечного волокна позволяет изучать электрическую активность отдельных мышечных волокон, в том числе определять их плотность в ДЕ мышц и надежность нервно-мышечной передачи с помощью метода измерения джиттера.
Для проведения исследования необходим специальный электрод с очень малой отводящей поверхностью диаметром 25 мкм, расположенной на ее боковой поверхности в 3 мм от конца. Малая отводящая поверхность позволяет регистрировать потенциалы одиночного мышечного волокна в зоне радиусом 300 мкм. Для этой методики в последнее время начали использовать концентрический электрод меньшего, чем обычный электрод, диаметра и с меньшей отводящей поверхностью (оранжевый цвет наконечника игольчатого электрода).
2.5.3.16. Исследование плотности мышечных волокон
В основе определения плотности мышечных волокон в ДЕ лежит тот факт, что зона отведения микроэлектрода для регистрации активности одиночного мышечного волокна строго определенна. Мерой плотности мышечных волокон в ДЕ является среднее количество потенциалов одиночных мышечных волокон, зарегистрированных в зоне его отведения при исследовании 20 различных ДЕ в различных зонах мышцы. В норме в этой зоне может находиться лишь одно (реже два) мышечное волокно, принадлежащее одной и той же ДЕ. С помощью специального методического приема (триггерное устройство) удается избежать появления на экране потенциалов одиночных мышечных волокон, принадлежащих другим ДЕ.
Среднюю плотность волокон измеряют в условных единицах, подсчитывая среднее количество потенциалов одиночных мышечных волокон, принадлежащих различным ДЕ. У здоровых людей эта величина колеблется в зависимости от мышцы и возраста от 1,2 до 1,8. Увеличение плотности мышечных волокон в ДЕ отражает изменение структуры ДЕ в мышце.
2.5.3.17. Исследование феномена джиттера
В норме всегда можно расположить электрод для регистрации одиночного мышечного волокна в мышце так, чтобы регистрировались потенциалы двух лежащих рядом мышечных волокон, принадлежащих одной ДЕ. Если потенциал первого волокна будет запускать триггерное устройство, то потенциал второго волокна будет несколько не совпадать во времени, так как для прохождения импульса по двум нервным терминалям разной длины требуется различное время. Это отражается в вариабельности межпикового интервала, то есть время регистрации второго потенциала колеблется по отношению к первому, определяемому как «пляска» потенциала, или «джиттер», величина которого в норме составляет 5–50 мкс.
Джиттер отражает вариабельность времени нервно-мышечной передачи в двух двигательных концевых пластинках, поэтому такой метод позволяет изучать меру устойчивости нервно-мышечной передачи. При ее нарушении, вызванном любой патологией, джиттер увеличивается. Наиболее выраженное его увеличение наблюдают при синаптических заболеваниях, в первую очередь при миастении (рис. 2.140).
При значительном ухудшении нервно-мышечной передачи наступает такое состояние, когда нервный импульс не может возбудить одно из двух рядом лежащих волокон и происходит так называемое блокирование импульса (рис. 2.141).
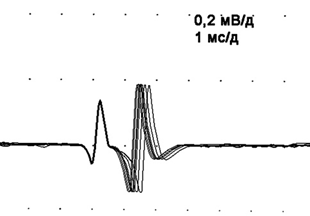
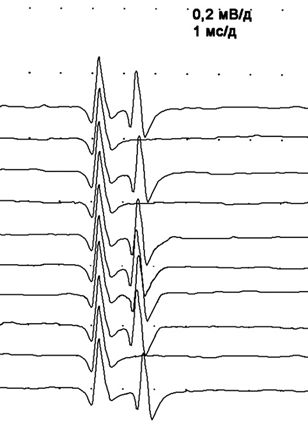
Значительное увеличение джиттера и нестабильность отдельных компонентов ПДЕ наблюдают и при БАС. Это объясняется тем, что вновь образованные в результате спраутинга терминали и незрелые синапсы работают с недостаточной степенью надежности. При этом у больных с быстрым прогрессированием процесса отмечается наиболее выраженное увеличение джиттера и блокирование импульсов.
2.5.3.18. Макроэлектромиография
Макро-ЭМГ позволяет судить о размерах ДЕ в скелетных мышцах. При исследовании одновременно используют два игольчатых электрода: специальный макроэлектрод, вводимый глубоко в мышцу так, чтобы отводящая боковая поверхность электрода находилась в толще мышцы, и обычный концентрический электрод, вводимый под кожу. Метод макро-ЭМГ основан на изучении потенциала, регистрируемого макроэлектродом с большой отводящей поверхностью.
Обычный концентрический электрод служит референтным, вводимым под кожу на расстояние не менее 30 см от основного макроэлектрода в зону минимальной активности исследуемой мышцы, то есть как можно дальше от двигательной точки мышцы.
Вмонтированный в канюлю другой электрод для записи потенциалов одиночных мышечных волокон регистрирует потенциал мышечного волокна изучаемой ДЕ, который служит триггером для усреднения макропотенциала. В усреднитель поступает и сигнал с канюли основного электрода. Усредняют 130–200 импульсов (эпоха в 80 мс, для анализа используют период в 60 мс) до тех пор, пока не появится стабильная изолиния и стабильный по амплитуде макропотенциал ДЕ. Регистрацию ведут на двух каналах: на одном записывают сигнал от одного мышечного волокна изучаемой ДЕ, запускающего усреднение, на другом воспроизводят сигнал между основным и референтным электродом.
Основной параметр, используемый для оценки макропотенциала ДЕ, — его амплитуда, измеряемая от пика до пика. Длительность потенциала при использовании данного метода не имеет значения. Можно оценивать площадь макропотенциалов ДЕ. В норме прослеживается широкий разброс величин его амплитуды, с возрастом она несколько увеличивается. При неврогенных заболеваниях амплитуда макропотенциалов ДЕ повышается в зависимости от степени реиннервации в мышце. При нейрональных заболеваниях она наиболее высока.
На поздних стадиях болезни амплитуда макропотенциалов ДЕ уменьшается, особенно при значительном снижении силы мышц, что совпадает с уменьшением параметров ПДЕ, регистрируемых при стандартной игольчатой ЭМГ.
При миопатиях отмечают снижение амплитуды макропотенциалов ДЕ, однако у некоторых больных их средние величины нормальны, но тем не менее все же отмечают некоторое количество потенциалов сниженной амплитуды. Ни в одном из исследований, изучавших мышцы больных миопатией, не выявлено увеличения средней амплитуды макропотенциалов ДЕ.
Метод макро-ЭМГ весьма трудоемкий, поэтому в рутинной практике широкого распространения он не получил.
2.5.3.19. Сканирующая электромиография
Метод позволяет изучать временное и пространственное распределение электрической активности ДЕ путем сканирования, то есть ступенчатого перемещения электрода в зоне расположения волокон изучаемой ДЕ. Сканирующая ЭМГ дает информацию о пространственном расположении мышечных волокон на всем пространстве ДЕ и может косвенно указывать на наличие мышечных группировок, которые формируются в результате процесса денервации мышечных волокон и повторной их реиннервации.
При минимальном произвольном напряжении мышцы введенный в нее электрод для регистрации одиночного мышечного волокна используют в качестве триггера, а с помощью отводящего концентрического игольчатого (сканирующего) электрода регистрируют ПДЕ со всех сторон в диаметре 50 мм. Метод основан на медленном поэтапном погружении в мышцу стандартного игольчатого электрода, накоплении информации об изменении параметров потенциала определенной ДЕ и построении соответствующего изображения на экране монитора. Сканирующая ЭМГ представляет собой серию расположенных друг под другом осциллограмм, каждая из которых отражает колебания биопотенциала, зарегистрированного в данной точке и улавливаемого отводящей поверхностью концентрического игольчатого электрода.
Последующий компьютерный анализ всех этих ПДЕ и анализ их трехмерного распределения дает представление об электрофизиологическом профиле мотонейронов.
При анализе данных сканирующей ЭМГ оценивают количество основных пиков ПДЕ, их смещение по времени появления, длительность интервалов между появлением отдельных фракций потенциала данной ДЕ, а также рассчитывают поперечник зоны распределения волокон в каждой из обследованных ДЕ.
При ДРП амплитуда и длительность, а также площадь колебаний потенциалов на сканирующей ЭМГ увеличиваются. Однако поперечник зоны распределения волокон отдельных ДЕ существенно не меняется. Не изменяется и характерное для данной мышцы количество фракций. Этот метод тоже не получил широкого распространения.
Список литературы
-
Авакян Г.Н. Структурно-функциональная характеристика двигательных нарушений при заболеваниях нервной и нервно-мышечной систем (Определение уровней поражения и лечебно-коррекционные мероприятия): дис. … д-ра мед. наук. М., 1985. 384 с.
-
Авакян Г.Н., Гроппа С.А. Нейрофизиологические методы исследования в неврологии. Кишинев: Tipografia Centrala, 2012. 280 с.
-
Бадалян Л.О., Скворцов И.А. Клиническая электронейромиография: рук-во для врачей. М.: Медицина. 368 с.
-
Бадалян Л.О., Скворцов И.А. Электронейромиография в детской неврологической клинике // Ж. невропатологии и психиатрии им. С.С. Корсакова. 1980. Вып. 10. С. 1441–1445.
-
Бернштейн Н.А. О построении движений. М.: Медгиз, 1947. 255 с.
-
Бернштейн Н.А. Координационные нарушения и восстановление биодинамики ходьбы после поражения головного мозга сосудистой этиологии // Тез. докладов 7-й научной сессии института неврологии АМН СССР. М., 1954. С. 28–30.
-
Гехт Б.М., Касаткина Л.Ф., Самойлов М.И., Санадзе А.Г. Электромиография в диагностике нервно-мышечных заболеваний. Таганрог, 1997. 370 с.
-
Гнездицкий В.В. Вызванные потенциалы мозга в клинической практике. Таганрог, 1997. 252 с.
-
Боковой амиотрофический склероз / под ред. И.А. Завалишина. М.: Евразия, 2007. 447 c.
-
Касаткина Л.Ф., Гильванова О.В. Электрофизиологическое проявление эффективности реиннервации при развитии денервационно-реиннервационного процесса // Функциональная диагностика. 2006. №2. С. 75–80.
-
Касаткина Л.Ф. Гильванова О.В. Электромиографические методы исследования в диагностике нервно-мышечных заболеваний. М.: Медика, 2010. 416 с.
-
Касаткина Л.Ф. Электромиография в диагностике заболеваний периферического нейромоторного аппарата // Функциональная диагностика. 2003. №1. C. 79–85.
-
Охнянская Л.Г., Комарова А.А. Электромиография в клинике профессиональных заболеваний. М.: Медицина, 1970. 198 с.
-
Санадзе А.Г., Касаткина Л.Ф. Клиническая электромиография для практикующего невролога: методическое пособие для врачей. М.: ГЭОТАР-Медиа, 2015. 65 с.
-
Скворцов И.А. Клинико-электронейромиографическое изучение заболеваний нервной и нервно-мышечной систем в возрастном аспекте: дис. … д-р мед. наук. М., 1982. 450 с.
-
Скворцов И.А., Авакян Г.Н. Методика электронейромиографического исследования. Методические рекомендации. М., 1976. 26 с.
-
Юсевич Ю.С. Электромиография в клинике нервных болезней. М.: Медгиз, 1958. 128 с.
-
Юсевич Ю.С. Очерки по клинической электромиографии. М.: Медицина, 1972. 95 с.
-
AANEM Recommended Policy for Electrodiagnostic Medicine Updated on 8.30.2014. https://aanem.org/getmedia//4eb449e2-c705-45b7-a5df-7ef024bb4b74/2014-Recommended_Policy_EDX_Medicine_qualified.PDF.aspx
-
American Association of Electrodiagnostic Medicine. Guidelines in electrodiagnostic medicine. Referral guidelines for electrodiagnostic medicine consultations // Muscle Nerve. 1999. Vol. 8. Р. 107–108.
-
American Association of Neuromuscular and Electrodiagnostic Medicine. Proper performance and interpretation of electrodiagnostic studies // Muscle Nerve. 2006. N33. P. 436–439.
-
Baxter R., Baxshi N., Fireman B., Lewis E., Ray P., at al. Lack of association of Guillain-Barre syndrome with vaccinations // Clin. Infect. Dis. Vol. 2013, N 57 (2). P. 197–202.
-
Bednarik J., Vondracek P., Dusik L., Moravkova E., Cundrle I. Risk factors for critical illness polyneuromyopathy // J. Neurol. 2005. Vol. 252. P. 343–351.
-
Buchthal F. An Introduction to electromyography. Kobenhavn, 1957. 230 p.
-
Buchthal F. Electromyography in the evaluation of muscles diseases // Methods in Clinical Neurophysiology. 1992. Vol. 2. P. 25–45.
-
Buchthal F. Spontaneous electrical activity: An overview // Muscle and Nerve. 1982. Vol. 5. P. 52–59.
-
Costa J., Swash M., de Carvalho V. Awaji criteria for the diagnosis of amyotrophic lateral sclerosis, a systemic review // Arch. Neurol. Vol. 69, N 11. P. 1410–1416.
-
Current Procedural Terminology, CPT Chicago. AMA Press, 2013.
-
Dumitru D. Electrodiagnostic Medicine. Philadelphia, PA: Hanley & Belfus, Inc., 1995. P. 39.
-
Disorders of voluntary muscle / Eds G. Karpati, D. Hilton-Jones, R. Griggs. Cambridge University press, 2001. 754 p.
-
Isaac Z., Lopez E. Lumbar spinal stenisis // Frontera W., Silver J., Rizzo T. (ed.). Essentials of Physical Medicine and Rehabilitation. Philadelphia: Elsevier, 2015. P. 257–263.
-
Kimura J. Elektrodiagnosis in diseases of nerve and muscle: principles and practice. Filadelphia: F.A. Davis company, 1989. 710 p.
-
Lacomis D. Electrophysiology of neuromuscular disorders in critical illness // Muscle Nerve, 2013. Vol. 47, N3. 452–63.
-
Marinacci I.A. Clinical electromyography. Los Angeles, 1955. P. 136.
-
Misulis K.E. Essentials of Clinical Neurophysiology. Newton, Massachusetts: Butterworth-Heinemann, 1997.
-
Preston D.C., Shapiro B.E. Electromyography and Neuromuscular Disorders. London: Elseviere, 2012.
-
Sanders D.B. Clinical neurophysiology of disorders of the neuromuscular junction // J. Clin. Neurophysiol. 1993. Vol. 10. P. 167–180.
-
Stalberg E., Fuglsang-Frederiksen A., Bischoff C. Quantitation and standardization in EMG and neurography // Suppl. Clin. Neurophysiol. 2000. N 53. P. 101–111.
-
Stalberg E., Trontelj J. Single fibre electromyography. N.Y., 1979. 224 p.
-
Subirana A., Maso-Subirana E. Correlactiones clinico-electromyograficasen la poliomyelitis // Med. esp. 1957. Vol. 216. P. 199.
-
Troeger M., Dengler R. The role of electromyography (EMG) in the diagnosis of ALS // ALS. London. UK, 2000. Vol. 1, N 2.
-
Vermino S., Fntibode testing in peripheral neuropathies // Neurol. Clin. 2007. Vol. 25. N 1. P. 29–46.
-
Weiss J., Weiss L., Silver J. Easy EMG. A Guide to Performing Nerve Conduction Studies and Electromyography. Elsevier, 2015.
-
WFN Research Group on Neuromuscular Diseases. El Escorial World Federation of Neurology criteria for the diagnosis of amyotrophic lateral sclerosis // J. Neurol. Sci. 1994. Vol. 124. P. 96–107.
-
Werner R. Electrodiagnostic evaluation of carpal tunnel syndrome and ulnar neuropathies. PM&R. 2013. Vol. 5. Suppl. 5. P. 14–21.