Медицинская генетика : учебник / под ред. Н. П. Бочкова. - Москва : ГЭОТАР-Медиа, 2022. - 224 с. - ISBN 978-5-9704-6583-7 |
Аннотация
В учебнике представлены современные основы общей генетики, подробная характеристика наследственной патологии, вопросы профилактики наследственных болезней.
Авторы учебника - преподаватели кафедры медицинской генетики Московской медицинской академии им. И.М. Сеченова - имеют большой опыт преподавания предмета студентам, врачам, ординаторам, аспирантам, а также пропаганды медико-генетических знаний среди среднего медицинского персонала и населения. Они непосредственно осуществляют медико-генетическое консультирование совместно с медицинскими сестрами, а лабораторные исследования проводят с фельдшерами-лаборантами.
Первое издание учебника (2001) было хорошо встречено студентами и преподавателями медицинских колледжей. За прошедшее время медицинская генетика обогатилась новыми фактами и концепциями, которые нашли отражение в новом издании.
7.2.1. Цитогенетические методы
Изучение строения и функции хромосом привело к выделению самостоятельного раздела области науки - цитогенетики. Началом развития цитогенетики человека можно считать 50-60 годы, когда впервые появились публикации работ, в которых удалось получить убедительные картины морфологии всех Х-хромосом человека и правильно определить их диплоидное число.
Суть цитогенетических методов, при всем разнообразии отдельных этапов, заключается в микроскопическом анализе хромосом, позволяющем выявить числовые и структурные изменения хромосомного набора (кариотипа), так называемые хромосомные и геномные мутации. В 50-х гг. нашего столетия использование цитогенетических методов послужило толчком к открытию этиологии нового класса заболеваний у человека - хромосомных болезней. В 1959 г. впервые появились сообщения о специфических изменениях числа хромосом при синдроме Дауна (добавочная 21-я хромосома), аномалиях в системе половых Х-хромосом. Далее, в течение достаточно короткого периода времени описаны и другие хромосомные болезни. Цитогенетические методы стали широко входить в медицину. Было выявлено, что множественные пороки развития у новорожденных часто обусловлены нарушением хромосом. Значительная часть хромосомных и геномных мутаций выявлена у мертворожденных и спонтанно абортированных эмбрионов. Стала развиваться и цитогенетика злокачественных опухолей человека. Таким образом, в настоящее время цитогенетика прочно вошла в клиническую медицину.
Методы цитогенетического исследования можно условно подразделить на прямые и непрямые. Прямые методы - это методы получения препаратов делящихся клеток без культивирования. Непрямые методы - это получение препаратов хромосом из клеток, культивированных в искусственных питательных средах. При обоих методах объектом цитогенетического исследования являются хромосомы в стадии метафазы митоза, поскольку, как уже говорилось выше, именно на этой стадии возможна точная идентификация хромосом и выявление их нарушений. Исследование хромосом в мейозе также возможно, однако у человека это связано с методическими трудностями в получении биоптатов из половых желез.
Прямые методы позволяют проводить хромосомный анализ клеток опухолей, но в основном используются для изучения костного мозга. Костный мозг получают при стернальной пункции, помещают его в питательную среду, добавляют колхицин (он останавливает деление клеток на стадии метафазы митоза), инкубируют клетки около 2-3 часов при 37 °С, а затем готовят препараты хромосом.
Непрямые методы связаны с культивированием клеток. Наиболее простым и доступным методом в клинической цитогенетике является анализ хромосом лимфоцитов периферической крови человека на стадии метафазы. Для этого используется цельная периферическая кровь, полученная при соблюдении стерильных условий, в количестве 1,0 мл. Кровь помещают в питательную среду с добавлением митогена ФГА (фитогемагглютинина), стимулирующего митотическое деление лимфоцитов. Далее культура помещается в термостат и при 37 °С культивируется 48-72 часа. За 2 часа до окончания культивирования вводится колхицин. Приготовление препаратов хромосом проводится по общепринятым методам, описанным в соответствующих лабораторных справочниках.
Препараты хромосом можно получать и из других клеток и тканей, используя различные модификации описанного метода культивирования лимфоцитов. Так, в пренатальной диагностике наиболее часто используют получение хромосом из клеток ворсин хориона, плаценты, пуповинной крови и амниотической жидкости, эмбриональных органов. Разработаны различные варианты приготовления препаратов хромосом путем «прямых» методов, краткосрочной культивации, культивирования в течение 2-3 суток и, наконец, длительного культивирования в течение нескольких недель.
Очень важным моментом для анализа хромосом является их окрашивание. Сплошное или равномерное окрашивание хромосом получило название рутинной окраски. Для рутинной окраски используют простые красители: азурэозин или краситель Гимза. Пример метафазной пластинки, окрашенной красителем Гимза, представлен на рисунке (рис. 7.1).

Рис. 7.1. Метафазная пластинка; окрашивание хромосом красителем Гимза
Использование такого метода окрашивания позволяет провести подсчет хромосом и их групповую принадлежность, проанализировать повреждения хромосом, называемые хромосомными аберрациями (рис. 7.2). Однако этот метод имеет ограничения при кариотипировании, поскольку не дает возможности индивидуальной идентификации хромосом. Методы окраски хромосом, дающие достаточно полное представление о кариотипе, появились в 70-х гг. нашего столетия - это методы дифференциального окрашивания хромосом. Большое практическое значение этих методов состоит в том, что дифференциальная окраска позволяет идентифицировать все хромосомы человека, благодаря специфическому линейному рисунку - продольной окрашиваемости для каждой хромосомы в соответствии с типом окраски. На практике наибольшее применение получили методы дифференциальной окраски красителем

Рис. 7.2. Метафазная пластинка с хромосомными абберациями (указаны стрелочками)
Гимза (G-окраска) и флюоресцирующим красителем акрихином или акрихин-пиритом (Q-окраска) (рис. 7.3).
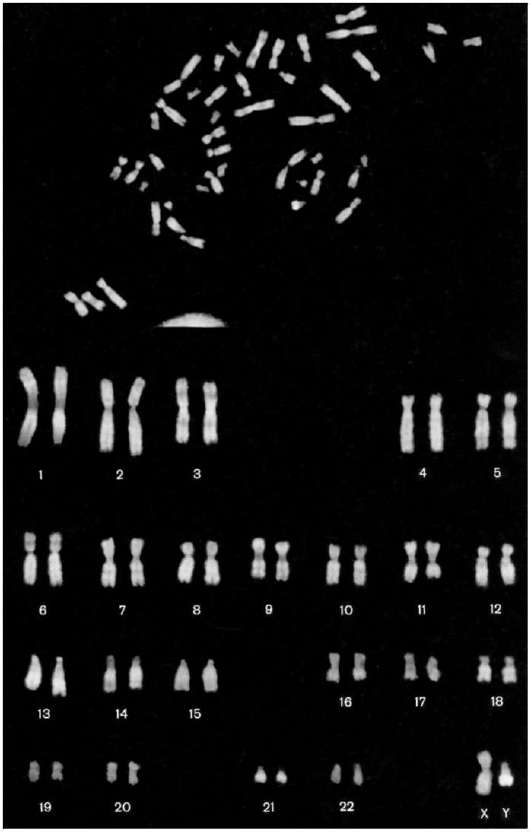
Рис. 7.3. Метафазная пластинка с дифференциальной окраской хромосом (46,XY) акрихин-ипритом
Для каждого из видов окраски разработаны многочисленные модификации технического выполнения этапов, в этих случаях применяется трехбуквенная система обозначения вида окраски. Например, G-метод с применением трипсина (GTG); Q-метод с использованием акрихина и его производных (QFQ) и т.д.
Методы дифференциального окрашивания пригодны для анализа хромосом, полученных из культур клеток любых тканей.
Цитогенетические методы сразу же нашли практическое применение в диагностике хромосомных болезней. Клиническая картина при хромосомных синдромах достаточно специфична, но есть и стертые формы, трудные для клинической диагностики. Их невозможно клинически дифференцировать. В этих ситуациях определяющей является цитогенетическая диагностика. Так, например, на консультацию по поводу бесплодия обратились супруги (23-24 лет), живущие в браке 3 года. Жена в течение 3 лет наблюдалась в женской консультации по поводу бесплодия и получала все это время достаточно интенсивную терапию. При этом муж не был обследован. При осмотре мужа врачом-генетиком был заподозрен синдром Клайнфельтера (высокий рост, скудное оволосение по женскому типу, избыточное развитие молочных желез, недоразвитие одного яичка). При цитогенетическом исследовании кариотипа подтвержден диагноз синдрома Клайфельтера. Его хромосомный набор - 47,XXY. Эта хромосомная патология и явилась причиной бесплодия.
В середине 70-х гг. исследования цитогенетиков показали, что большинство крупных и малых сегментов метафазных хромосом образуются путем слияния субсегментов, которые более четко видны на ранних стадиях митоза - профазы и прометафазы. На этих стадиях хромосомы менее конденсированы, недоспирализованы и поэтому имеют большую линейную подразделенность. Далее были разработаны различные методы получения делящихся клеток на стадии прометафазы. Таким образом, метод анализа хромосом на стадиях профазы и прометафазы дал возможность более точно устанавливать точки разрывов в перестроенных хромосомах, если в перестройку вовлечены небольшие участки хромосом. Такие аномалии называют микроперестройками. Использование этого методического подхода позволило получить хромосомы с разной степенью сегментации - от 550 до 2500 сегментов на гаплоидный набор (для сравнения в метафазных хромосомах средней конденсации число сегментов на гаплоидный набор составляет 350-400).
С точки зрения практического использования анализа прометафазных хромосом, этот метод целесообразно применять для диагностики болезней с микроперестройками в структуре одной или нескольких хромосом (транслокации, делеции, инверсии) для уточнения локализации точек разрывов хромосом.
Иногда аномальные хромосомы, претерпевшие транслокацию, появляются в результате разрывов двух различных хромосом и их последующего аберрантного объединения. Транслокация может происходить de novo в половых клетках одного из родителей, но может и представлять собой наследование мутации, произошедшее у одного из предков. Носители транслокаций клинически здоровы. Эти и другие структурные перестройки хромосом часто являются причиной спонтанных абортов, мертворождений, неонатальной смертности и бесплодия.
Например, в консультацию обратилась супружеская пара по поводу привычного невынашивания беременности. Из анамнеза: пять самопроизвольных выкидышей на сроке до 8 недель, клиническое обследование супругов не выявило особенностей. При цитогенетическом обследовании выявлено, что кариотип мужа нормальный (46, XY), а у жены - 45,XX,t(13;14), т.е. выявлена транслокация. При такой транслокации нет изменений у носительницы, но в мейозе у нее образуются аномальные гаметы.
Некоторые микроструктурные перестройки хромосом выявляют при множественных врожденных пороках развития, при различных злокачественных новообразованиях до развития клинических проявлений. Так, показано, что в ряде случаев в клетках ретинобластомы, остеосаркомы, феохромоцитомы, имеются хромосомные перестройки (делеции хромосом).
Однако при некоторых нозологических формах даже использование таких высокоразрешающих методов хромосомного анализа не приводит к обнаружению хромосомных повреждений. Это может свидетельствовать о генетической гетерогенности самих заболеваний, а также, возможно, и о пределе разрешающих возможностей описанного метода.
Относительно недавно в арсенале лабораторной цитогенетики появились высокоразрешающие методы - молекулярно-цитогенетический метод гибридизации in situ, в частности флуоресцентная гибридизация in situ, или FISH-метод.
Метод гибридизации in situ основан на обработке препаратов хромосом специфическим ДНК-зондом, который присоединяется к исследуемой хромосоме, и после обработки специальными соединениями и флуоресцентными красителями препарат исследуют с помощью флуоресцентного микроскопа. Для сравнения разрешающих способностей метода приведем следующие сведения. При рутинной окраске хромосом самый маленький нарушенный участок хромосомы в виде делеции или дупликации, который можно различить под обычным световым микроскопом, содержит 30 х 106 нуклеотидов. Применение дифференциальных методов окраски увеличивает такую возможность до (7-10) х 106 нуклеотидов. При анализе хромосом на стадии ранней метафазы или профазы различимы микроперестройки размером (1-3) х 106 нуклеотидов. А вот следующий уровень разрешения уже обеспечивается только молекулярно-цитогенетическим методом. Такая высокая разрешающая способность метода позволяет применять непосредственно FISH-метод или его варианты в достаточно широких пределах: от определения локализации гена до расшифровки сложных перестроек хромосом. Как пример практических возможностей метода можно привести следующее.
У ребенка с множественными врожденными аномалиями при использовании метода дифференциального окрашивания обнаружены сложные перестройки в шести хромосомах (1, 4, 7, 8, 9, 12) с десятью разрывами. Полная идентификация разрывов стала возможной только с помощью FISH-метода. Этот же метод можно применять для диагностики анеуплоидий в интерфазных ядрах. Например, специфический для 21-й хромосомы зонд ДНК гибридизируется с денатурированной ДНК в клетках из амниотической жидкости на предметном стекле. Если у плода две 21-Х-хромосомы (норма), то везде будут видны 2 флюоресцирующие соответствующим цветом точки. При наличии у плода трисомии-21 в ядре визуализируются три светящиеся точки.
Как и для других цитогенетических методов, в зависимости от цели исследования, используются различные варианты FISH-метода. Так, в онкоцитогенетике достаточно сложно получить хромосомы хорошего качества, поэтому используется метод сравнительной геномной гибридизации, основанный на гибридизации ДНК пациента с контрольными препаратами хромосом. При таком подходе можно выявить участки ДНК с делециями (потерями) и дупликациями (удвоениями). Метод применяют и для составления карт генов, вовлеченных в опухолевый процесс.
Таким образом, цитогенетические методы стали практически незаменимыми процедурами в разных областях науки и клинической практики. Кроме диагностики заболеваний, цитогенетические методы широко используются в профилактической медицине. Уже давно показано повышение уровня хромосомных повреждений (аберраций) у курильщиков, у лиц, подвергшихся действию ионизирующей радиации, при воздействии на организм человека вредных химических факторов производства и окружающей среды, употреблении ряда лекарственных препаратов. В определенной степени типы хромосомных аберраций специфичны для разных групп мутагенных факторов. Так, при воздействии химических мутагенов чаще возникают аберрации хроматидного типа (повреждена одна хроматида; рис. 7.4), а при воздействии ионизирующего излучения - хромосомного типа (рис. 7.5).

Рис 7.4. Метафазная пластинка. Стрелкой указан одиночный фрагмент (абберация хроматидного типа)
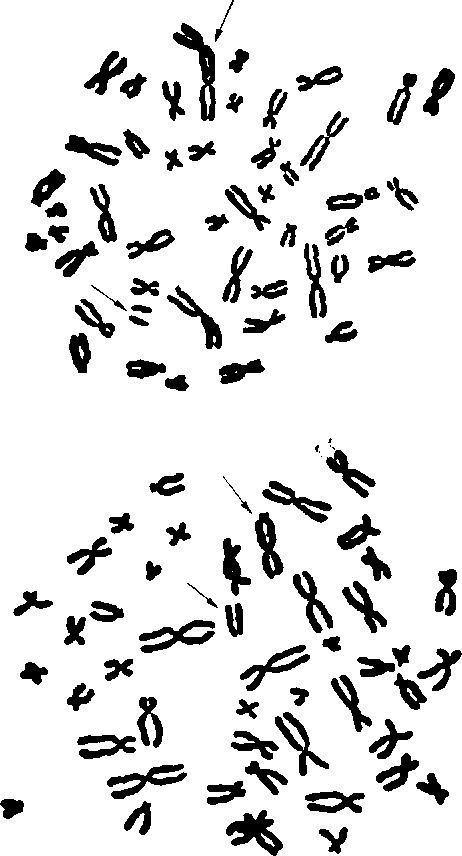
Рис. 7.5. Метафазная пластинка. Стрелками указаны парный фрагмент и дицентрическая хромосома
Изучены количественные закономерности спонтанного и индуцированного мутагенеза. На этой основе разработаны системы цитогенетического мониторинга (контроля), реально работающие во многих странах, в том числе и у нас. Они позволяют следить за уровнем мутагенных воздействий факторов окружающей среды на наследственность человека. Для целей клиники анализ хромосомных аберраций помогает оценить отрицательные эффекты применяемой терапии и корректировать длительность применения того или иного лекарственного средства.
Для описания нормального кариотипа человека, а также для обозначения структурных и количественных перестроек хромосом используется определенная универсальная схема и специальные символы. Описание кариотипа начинают с указания общего числа хромосом в клетке, затем ставится запятая и обозначается набор половых хромосом, который указывает пол обследуемого, в случае патологии далее ставится запятая, а затем обозначается хромосомная аномалия. Например, запись 46,XX характеризует нормальный кариотип женщины, 46,XY - нормальный кариотип мужчины, 47,XX,+21 кариотип больного с синдромом Дауна. Иногда при обследовании обнаруживают так называемый нормальный полиморфизм хромосом - индивидуальные особенности их строения. Как правило, полиморфизм отражает вариабельность размеров гетерохроматиновых сегментов, наличие спутников и спутничных нитей в области коротких плеч акроцентрических хромосом и их величину. В большинстве случаев наличие полиморфизма строения хромосом не приводит к возникновению патологических симптомов у их обладателя. Однако следует отметить, что иногда при наличии нормального полиморфизма хромосом может увеличиваться риск рождения ребенка с хромосомными аномалиями. Выявление полиморфизма хромосом обозначается при записи кариотипа. Например, запись 46,XX9gh+ означает увеличение размера гетерохроматинового участка в длинном плече хромосомы 9 женщины.
Изучение нормального полиморфизма хромосом может иметь значение для определения родительского происхождения хромосомной перестройки. Если установлено, от кого из родителей унаследован полиморфизм хромосом, то это обязательно указывается при записи кариотипа. Например, 46XY15ps+pat означает, что мужчиной унаследованы от отца увеличенные спутники на хромосоме 15.
Методы цитогенетической диагностики, применяемые в клинической генетике, часто используются в комплексе с другими методиками лабораторной диагностики, дополняя друг друга. Это позволяет более точно диагностировать сложные проявления наследственных и врожденных заболеваний человека. В нашей стране, как и во всем мире, цитогенетические методы прочно вошли в арсенал необходимых диагностических процедур для решения сложных дифференциально-диагностических задач практически во всех областях медицины. Особое же значение эти методы имеют при оказании помощи больным педиатрического, акушерско-гинекологического и эндокринологического профилей. Все вопросы назначения того или иного цитогенетического исследования осуществляются при медико-генетическом консультировании. В целом же все практические проблемы, решаемые лабораторными цитогенетическими методами, можно свести к следующим:
-
подозрение на хромосомную болезнь по клинической симптоматике;
-
наличие у ребенка множественных врожденных пороков развития, не относящихся к генному синдрому;
-
многократные спонтанные аборты, мертворождения или рождение детей с врожденными пороками развития;
-
нарушение репродуктивной функции неясного генеза у женщин и мужчин (первичная аменорея, бесплодный брак и др.);
-
существенная задержка умственного и физического развития ребенка;
-
пренатальная диагностика (риск по возрасту, в связи с наличием транслокации у родителей, при рождении предыдущего ребенка с хромосомной болезнью);
-
подозрение на синдромы, характеризующиеся хромосомной нестабильностью;
-
лейкозы (для дифференциальной диагностики, оценки эффективности лечения и прогноза течения);
Участие цитогенетиков в анализе трудных с диагностической точки зрения случаев часто приводит к более точной диагностике и, соответственно, к своевременному лечению и предупреждению рождения больного ребенка.