Интенсивная терапия : национальное руководство. Том 1
Интенсивная терапия : национальное руководство : в 2 т. Том 1 / под ред. И. Б. Заболотских, Д. Н. Проценко. - 2-е изд. , перераб. и доп. - Москва : ГЭОТАР-Медиа, 2021. - 1136 с. (Серия "Национальные руководства") - ISBN 978-5-9704-6258-4. |
Аннотация
Второе издание национального руководства "Интенсивная терапия" содержит современную информацию о диагностике и лечении критических состояний различной этиологии и патогенеза. Особое внимание уделено особенностям интенсивной терапии в периоперационный период у пациентов с сопутствующими заболеваниями. Благодаря объединению усилий ведущих специалистов России удалось отразить согласованную позицию по актуальным вопросам современной реаниматологии и интенсивной терапии и учесть сведения доказательной медицины. Все главы прошли этап независимого рецензирования.
Издание предназначено, прежде всего, анестезиологам-реаниматологам, а также врачам всех специальностей, студентам старших курсов медицинских вузов, клиническим ординаторам, аспирантам.
И73
4.3. СУДОРОЖНЫЙ СИНДРОМ
Д.А. Аверьянов, А.Н. Кондратьев, А.В. Щеголев
Коды по Международной классификации болезней 10-го пересмотра
G40 Эпилепсия.
G41 Эпилептический статус.
G41.0 Эпилептический статус grand mal (судорожных припадков).
G41.1 Эпилептический статус petit mal (малых припадков).
G41.2 Сложный парциальный эпилептический статус.
G41.8 Другой уточненный эпилептический статус.
G41.9 Эпилептический статус неуточненный.
Введение
Эпилептические приступы (далее - эпиприступы) могут осложнить лечение пациентов в ОРИТ. Часто их появление является первым симптомом поражения ЦНС. Позднее выявление и лечение эпиприступов ведет к увеличению риска летального исхода, вследствие чего своевременную диагностику и купирование данных расстройств и их причин следует считать абсолютной необходимостью. Немаловажным также является тот факт, что эпилепсией, как хроническим заболеванием, проявляющимся эпиприступами, страдают, по некоторым данным, 2% населения. Пациенты с эпилепсией периодически поступают для проведения им интенсивной терапии, и анестезиолог-реаниматолог должен обладать необходимым объемом знаний в этой области.
Эпилептический приступ - преходящее явление, характеризующееся признаками и/или симптомами вследствие аномально избыточной или синхронной активности нейронов ГМ [1].
Эпилептический статус - состояние, являющееся результатом либо несостоятельности механизмов, ответственных за прекращение эпиприступа, либо инициации механизмов, ведущих к аномальной длительности эпиприступа (за временной точкой t1). Это состояние, которое в зависимости от типа и длительности эпипри-ступов может иметь долгосрочные последствия (за временной точкой t2), включающие смерть нейронов, их повреждение или изменение работы нейронных сетей [1].
Эпистатус, как и эпиприступ, может быть как основным патологическим процессом, определяющим нахождение такого пациента в ОРИТ, так и осложнением основного заболевания (например, при новообразовании ГМ, инфекции ЦНС, постгипоксической, токсической, метаболической, септической энцефалопатии). В последние годы много внимания в литературе уделено ведению пациентов с так называемым бессудорожным эпистатусом. В отличие от эпиприступов и статуса с моторными проявлениями, их диагностика и, соответственно, лечение значительно затруднено в связи с отсутствием характерных проявлений. При этом сохраняются все другие составляющие эпиприступа, такие как аномально избыточная или синхронная активность нейронов отдельных локусов или всего ГМ, местные биохимические и разнообразные внешние проявления (изменения уровня сознания, вегетативные, сенсорные и др.), которые являются не менее губительными как для ГМ, так и для организма в целом.
Рефрактерный эпилептический статус - персистирующий эпиприступ с клиническими и/или электрографическими признаками, несмотря на проведенную медикаментозную терапию адекватными дозами бензодиазепина и введением препарата второй линии [5].
Классификация
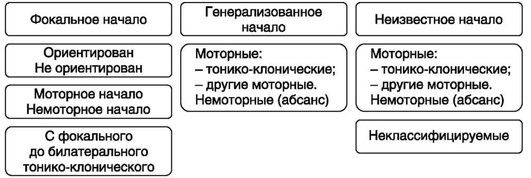
Классификация типов эпиприступов Международной лиги по борьбе с эпилепсией (ILAE - International League Against Epilepsy) в 2017 г. претерпела значительную модификацию, преследуя цель стать более практичной (рис. 4-8) [2]. Глобально все эпиприступы, согласно данной классификации, разделяют на приступы с фокальным, генерализованным и неопределенным началом, с дальнейшим делением на моторные, бессудорожные, с/без сохранения ориентации (awareness). При фокальном начале эпиактивность формируется в строго определенном локусе ГМ и клинические проявления зависят от функциональной специализации данного локуса (двигательный, чувствительный, вегетативный). При генерализованном же начале активируется вся или большая часть коры ГМ с обеих сторон. Под ориентацией подразумевают осознание своей личности, окружающей обстановки и происходящего. При этом классификация эпилептических статусов в настоящее время не изменилась с 2015 г. (табл. 4-17) [1]. Четыре оси классификации включают семиологию, этиологию, ЭЭГ-коррелят и возраст. Основу семиологической оси составляют деление на две большие группы: с отчетливыми моторными проявлениями и без них (бессудорожный эпистатус). Этиология эпиприступов многообразна и представлена в табл. 4-18.
Патофизиология
Влияние эпиприступа и его крайнего варианта - эпистатуса на организм пациента можно условно разделить на три взаимосвязанных уровня: клеточный, органный (ГМ) и системный. Аномально избыточная или синхронная активность нейронов приводит к открытию ионных каналов, сопряженных с рецепторами возбуждающих аминокислот. С точки зрения важности процесса можно выделить три типа таких каналов: AMPA (α-амино-3-гидрокси-5-метил-4-изоксазол-пропионовая кислота), NMDA (N-метил-D-аспартат) и метаботропные каналы (например, глу-таматные, GABAb, большинство серотониновых рецепторов, норадреналиновые, дофаминовые и др.). Активация данных рецепторов способна привести к повышению внутриклеточной концентрации кальция до токсического уровня.
| С отчетливыми моторными проявлениями | Без отчетливых моторных проявлений (бессудорожный эпистатус, БСЭС) |
|---|---|
А.1. Тонико-клонический эпистатус. А.1.a. С генерализованным началом. А.1.b. С фокальным началом. А.1.c. С неизвестным началом. А.2. Миоклонический эпистатус (отчетливые эпилептические миоклонические подергивания). А.2.a. С комой. А.2.b. Без комы. А.3. Фокальный моторный. А.3.a. Повторяющиеся фокальные моторные приступы (Джексоновские). А.3.b. Непрерывная парциальная эпилепсия (epilepsia partialis continua). А.3.c. Адверсивный статус. А.3.d. Окулоклонический статус. А.3.e. Иктальный (приступный) парез (фокальный ингибирующий эпистатус). А.4. Тонический статус. А.5. Гиперкинетический эпистатус |
B.1. БСЭС с комой. B.2. БСЭС без комы. B.2.a. Генерализованный. B.2.a.a. Типичный статус абсансов. B.2.a.b. Атипичный статус абсансов. B.2.a.c. Миоклонический статус абсансов. B.2.b. Фокальный. B.2.b.a. Без нарушения сознания (непрерывная аура, с вегетативными, чувствительными, зрительными, обонятельными, вкусовыми, эмоциональными/психическими/эмпирическими или слуховыми симптомами). B.2.b.b. Афатический статус. B.2.b.c. С нарушением сознания. B.2.c. С неизвестным (фокальным или генерализованным) началом. B.2.c.a. Вегетативный эпистатус |
Острый процесс |
|
Хронический процесс |
|
Важным патогенетическим механизмом возникновения необычной длительности медикаментозной резистентности эпиприступа является изменение баланса рецепторов, взаимодействующих с возбуждающими и тормозными медиаторами ЦНС. В англоязычной литературе это явление называют receptor trafficking («торговля рецепторами»). Например, уменьшается количество рецепторов гамма-оксимасляной кислоты (ГОМК) за счет их интернализации в эндоциты и разрушения. При этом NMDA-рецепторы транспортируются к синаптической мембране, их количество увеличивается. Изменяется функция ГОМК-рецепторов. В условиях увеличения содержания хлора во внеклеточном пространстве тормозные токи этих рецепторов становятся возбуждающими.
Существует большое количество лекарственных препаратов, блокирующих эти рецепторы, но их хроническое применение невозможно ввиду высокой токсичности.
Влияние избыточных количеств возбуждающих аминокислот на клеточном уровне сопровождается: накоплением токсической концентрации внутриклеточного свободного кальция; активацией систем аутолиза; образованием свободных радикалов и окиси азота (последний, в свою очередь, способствует дальнейшему возбуждению и одновременно является токсином); фосфорилированием ферментов и рецепторных систем, что повышает возбудимость; повышением внутриклеточной осмоляльности, что приводит к клеточному отеку.
При истощении механизма образования АТФ нарушается работа активных мембранных ионообменников с исходом в цитотоксический клеточный отек. Все перечисленное является механизмом повреждения нейронов в рамках эпиактивности. Выраженность процесса соответственно зависит от распространенности и длительности существования данной активности. Чем длительнее персистирует эпиприступ, тем выше вероятность формирования необратимого характера клеточного повреждения с утратой функции и появления различной степени рефрактерности к проводимому лечению.
При эпиактивности на органном уровне наиболее важен эффект увеличения мозгового кровотока. В ГМ существует сопряжение «метаболизм-кровоток». Данное сопряжение является следствием особенности строения и функции нейронов. Основной функцией нейронов как возбудимых клеток является генерирование и передача потенциала действия и быстрое восстановление потенциала покоя. Это требует обеспечения непрерывного потока нутриентов для наиболее эффективного пути синтеза энергоносителя АТФ, окислительного фосфорилирования в условиях практически полного отсутствия каких-либо запасов. Непрерывность поступления нутриентов достигается быстрым изменением кровотока в зависимости от потребности. При эпиактивности локально (при фокальном приступе) или во всех отделах ГМ (при генерализованном приступе) значительно повышается активность нейронов, что по механизму сопряжения «метаболизм-кровоток» приводит к увеличению мозгового кровотока. В зависимости от выраженности изменяется внутричерепной объем крови, который, согласно доктрине Монро-Келли, является одним из компонентов общего постоянного внутричерепного объема. При снижении резерва компенсации дополнительного объема (например, при травме ГМ, гидроцефалии и т.д.) последнее может приводить к повышению ВЧД.
Жизнеугрожающими системными эффектами обладает лишь генерализованный тонико-клонический приступ. Избыточная активация симпато-адреналовой системы приводит к выраженному подъему системного и легочного АД и гипергликемии. Мышцы работают с большим напряжением и, как следствие, в условиях анаэробного метаболизма продуцируют в кровь большое количество лактата. Обструкция дыхательных путей и аномальные сокращения диафрагмы нарушают вентиляцию легких. Повышению содержания в крови углекислого газа способствуют нарушения ее выведения и избыточная продукция. Мышечные сокращения также увеличивают выделение тепла, что приводит к возрастанию температуры ядра тела. Чем длительнее продолжается генерализованный приступ, тем более выражены перечисленные системные проявления. Комбинированные (респираторные и нереспираторные) нарушения часто характеризуются запредельной (pHa <7,0) ацидемией. Ацидемия может вызывать гиперкалиемию, что в дополнение к негативным влияниям на контрактильную способность миокарда вызывает персистирование эпиактивности. Несмотря на то что такая патофизиологическая последовательность редко приводит к остановке кровообращения в силу своей кратковременности и обратимости, в некоторых случаях (например, у истощенных пациентов с выраженной сопутствующей кардиопульмональной патологией) нельзя исключить ее из механизма внезапной смерти. Чаще гипер-симпатикотония и ее последствия являются причиной нейрогенного ОЛ. После длительного периода генерализованной судорожной активности состояние пациента может характеризоваться артериальной гипотензией с гипертермией, нарушение глюконеогенеза способно привести к гипогликемии. Часто во время приступа происходит аспирация содержимого ротоглотки и желудка. Нередко можно наблюдать рабдомиолиз с последующим развитием почечной недостаточности. Переломы костей, вывихи суставов, растяжения связок также характеризуются тяжелыми последствиями.
Механизмы, приводящие к спонтанному купированию эпиактивности, в настоящее время малопонятны. Наиболее вероятными, по всей видимости, являются ингибирующие механизмы ГАМК-ергических вставочных нейронов и таламических нейронов.
Клинические проявления
Внешние проявления эпиактивности характеризуются большим разнообразием в силу активации различных центров ГМ. Наиболее заметными в ОРИТ являются моторные эпиприступы. Следует отметить, что степень повреждающего воздействия на нейроны не зависит от внешних проявлений. В большей степени определяющим значением обладают распространенность и длительность эпиактивности.
У пациентов в ОРИТ может существовать ряд факторов, затрудняющих выявление эпиприступов и, соответственно, затягивающих проведение необходимого комплекса лечебно-диагностических мероприятий. К ним относятся применение миорелаксантов и/или медикаментозной седации для лечения основного заболевания и фоновое угнетение сознания. Нередки также ошибочная трактовка неэпилептических аномальных движений пациента в тяжелом состоянии и назначение противосудорожных препаратов.
Пациенты с метаболическими расстройствами, аноксией и другими типами повреждения нервной системы могут демонстрировать аномальные движения, которые можно принять за эпилептические. Астериксис - неритмичные асимметричные подергивания при тоническом напряжении мышц конечностей, шеи и туловища, которые являются неспецифическим признаком метаболической энцефалопатии любого генеза (например, при ПЭ). Астериксис возникает только при произвольном сокращении мышц, поэтому его не бывает при коме. Постаноксический (при восстановлении спонтанного кровообращения после гипоксической остановки кровообращения) миоклонус, провоцируемый различными стимулами (неожиданные звуки, прикосновения и т.д.), может иметь выраженный характер, при этом обычно самостоятельно проходит в течение нескольких дней. Данный синдром противоречив с точки зрения эпилептогенной природы своего происхождения. В литературе приведены случаи его развития у пациентов с полным подавлением биоэлектрической активности ГМ. Пациенты с травматическим повреждением ГМ демонстрируют пароксизмы симпатической гиперактивности (одно из названий - диэнцефально-катаболические кризы), которые часто сопровождаются ригидностью различных мышечных групп, напоминающей децеребрационную. Пациенты со столбняком не теряют сознание при спазмах, и движения носят больше сгибательный, чем разгибательный характер. Иногда проявления некоторых психических расстройств практически не отличаются по семиотике от эпилептических. Во всех сомнительных случаях для дифференциальной диагностики необходимо использовать ЭЭГ.
Судороги, развившиеся немедленно после ЧМТ, не являются специфическим прогностическим признаком эпилепсии. Но если они появляются в течение недели после ЧМТ, то являются специфическим прогностическим признаком. Не все пациенты с первичным эпиприпадком нуждаются в противосудорожной терапии. Только у 50% больных после первичного припадка наблюдается повтор в течение следующих 3-5 лет. Вероятность повтора высока при структурном повреждении мозга, при регистрации ЭЭГ с отчетливым эпилептиформным паттерном, у пациентов с инсультом в анамнезе и если первичный припадок проявился эпистатусом.
Проявления эпиактивности зависят от типа и при фокальном приступе от области коры ГМ с аномальной активностью нейронов. Приступы с генерализованным тонико-клоническим началом первично представлены тоническим разгибанием туловища и конечностей без предшествующих фокальных симптомов. Ауру перед приступом пациенты не отмечают, сознание же во время приступа отсутствует. После нескольких секунд тонического напряжения мышцы начинают вибрировать и происходят клонические (ритмичные) разгибания. Данная фаза ослабевает в течение нескольких минут. Далее описанные фазы (тоническая и клоническая) могут повторяться или проявления будут носить лишь клонический характер.
Генерализованный приступ с фокальным началом характеризуется первично локальными проявлениями с эволюцией в генерализованный тонико-клонический приступ. Иногда фокальное немоторное начало трудно определить в силу его типа (обонятельная аура, потеря речи) и малой длительности. Такие приступы подразумевают структурное повреждение ГМ (новообразование, инсульт, абсцесс и т.д.) и тщательные наблюдение и осмотр в приступно-межприступных периодах способны выявить симптомы латерализации.
Временем _t1 _ (аномальная длительность) для клонико-тонического приступа с генерализованным или фокальным началом в настоящее время принято считать 5 мин. Если моторные проявления не прекращаются в пределах этого времени или сознание пациента между приступами не восстанавливается до исходного уровня, такой приступ следует считать затянувшимся с низкой вероятностью самопроизвольного купирования, то есть эпистатусом. Временем _t2 _ считают интервал 30 мин от начала моторных проявлений. При выходе за данный интервал приступ может иметь долгосрочные последствия (повреждение нейронов, их смерть, нарушение работы нейронных сетей). Менее распространенным является миоклонический эпилептический статус (эпизоды билатеральных ритмичных подергиваний преимущественно проксимальных мышц иногда с переходом в генерализованный тонико-клонический приступ), обычно наблюдаемый у пациентов с постаноксической комой и являющийся плохим прогностическим фактором.
Среди различных форм бессудорожного эпистатуса наибольшей важностью для врача-реаниматолога обладает статус как последствие неадекватного лечения генерализованного тонико-клонического приступа. При введении такому пациенту недостаточных доз препаратов для купирования эпиактивности ее внешние проявления могут пройти, при этом электрографический коррелят будет персистировать, оказывая не меньшее пагубное воздействие на нейроны. Общим правилом следует считать, что если пациент не восстанавливает сознание до исходного уровня по истечении 20 мин после окончания генерализованных моторных проявлений, то такое состояние стоит рассматривать как бессудорожный эпистатус.
Отдельную проблему представляет бессудорожная эпиактивность ГМ у пациентов с тяжелым повреждением ГМ. Отсутствие типичных моторных клинических проявлений затрудняет своевременную диагностику и, соответственно, лечение такой активности. А нарушение сознания, ставшее результатом эпистатуса, трактуют как неврологический дефицит вследствие основного заболевания.
Абсансную эпиактивность чаще относят к молодому возрасту. Она характеризуется утратой контакта с пациентом, пустым взглядом, иктальной (внутриприступной) амнезией. Для статуса абсансов временем t1 определен интервал 10-15 мин, при этом существование времени t2 подвергается сомнению в силу специфичной патофизиологии приступа. В отличие от других приступов, данный тип характеризуется аномально избыточным и ритмичным ингибированием, а не возбуждением нейронов, вследствие чего не способен запустить механизм клеточной эксайтотоксичности.
Фокальный эпистатус с моторными проявлениями достаточно легко выявить. К сожалению, применение у пациентов в ОРИТ миорелаксантов или первоначальный моторный дефицит затрудняют диагностику. Бессудорожный фокальный статус может сопровождаться соматосенсорными проявлениями. Их выявление у пациентов, контакт с которыми затруднен (медикаментозная седация, угнетение сознания и т.д.), представляет большую сложность. Непрерывная парциальная эпилепсия (epilepsia partialis continua) характеризуется ритмичными движениями в строго определенной группе мышц в течение порой значительного периода (месяцы), при этом противосудорожные препараты обладают малой эффективностью. Данный тип эпиактивности часто наблюдают при гиперосмолярной гипергликемии или при локальном поражении ГМ. Симптомом сложного фокального приступа является лишь потеря пациентом ориентированности и у пациентов ОРИТ особенно затруднительна. Для данного типа приступа временем t1 считают 10 мин, t2 >60 мин.
Диагностика
Естественное стремление любого врача-реаниматолога, ставшего свидетелем генерализованного тонико-клонического эпиприступа, - постараться остановить его любыми доступными средствами. Часто это ведет к искажению клинической картины и ятрогенным осложнениям. При этом с точки зрения эффективности во время приступа мало что можно сделать, кроме мероприятий, направленных на защиту пациента от причинения вреда самому себе (укладка на бок, ограждение от твердых предметов, удержание в пределах кровати). Приступ, как правило, заканчивается до того момента, когда любое лекарство достигнет эффективной концентрации в крови. Наблюдение является наиболее важным мероприятием при появлении у пациента первого эпиприступа. Именно в это время необходимо обратить внимание, является ли приступ первоначально фокальным, что в дальнейшем будет свидетельствовать о структурном повреждении ГМ. Постприступный период также может содержать важную диагностическую информацию: речевые, моторные, сенсорные или аномалии рефлексов после явно первично-генерализованного приступа будут также указывать на локализованную природу патологии.
Эпиприступ у пациентов в ОРИТ может иметь ряд потенциальных причин (см. табл. 4-18), требующих дифференциальной диагностики. Одной из наиболее частых причин у данной категории пациентов являются лекарства, особенно на фоне нарушенной функции почек, печени или при нарушении ГЭБ (табл. 4-19). Аминофиллин (Эуфиллин♠ ) способен привести к развитию эпиприступа или статуса при быстром введении или при превышении рекомендованной концентрации в крови. При этом есть наблюдения их развития и в терапевтическом окне. Среди антибиотиков имипенем с циластатином и фторхинолоны обладают свойством снижать эпилептогенный порог. К ним иногда добавляют и другие антибиотики, в особенности это касается β-лактамов. Среди общих анестетиков дозозависимым эпилептогенным потенциалом обладает энфлуран.
Анальгетики |
ГОМК, меперидин [тримеперидин (Промедол♠)], трамадол |
Антибиотики |
β-Лактамы (пенициллин, ампициллин и др.), цефалоспорины, карбапе-немы (имипенем и др.), изониазид, метронидазол, налидиксовая кислота, пириметамин (противомалярийное средство) |
Антидепрессанты |
Амитриптилин, бупропион, циталопрам, флуоксетин, мапротилин, миан-серин, пароксетин, сертралин |
Противоопухолевые препараты |
Кармустин, бусульфан, хлорамбуцил, метотрексат, винкристин |
Антипсихотики |
Хлорпромазин, галоперидол, оланзапин, перфеназин, тиоридазин, трифлуоперазин, зипрасидон |
Бронходилататоры |
Аминофиллин, теофиллин |
Общие анестетики |
Энфлуран, кетамин |
Местные анестетики |
Бупивакаин, лидокаин, прокаин (Новокаин♠) |
Симпатомиметики |
Эфедрин |
Другие |
Алкоголь, амфетамины, антихолинергические препараты, антигистаминные, атенолол, баклофен, циклоспорин, домперидон, такролимус, флумазенил, фолиевая кислота, гипербарическая оксигенация (ГБО), инсулин, йодсодержащий контраст, литий, метилксантины (например, кофеин), окситоцин, фенциклидин |
Факт употребления медикаментозных средств, используемых для «расслабления», часто упускают из виду у пациентов с приступом, поступающих в ОРИТ. Острая интоксикация кокаином или метамфетамином характеризуется гиперсимпатикотонией, вслед за которой может последовать эпиприступ. Несмотря на то что именно СО алкоголя является частой причиной приступов, в целом любое прекращение приема препаратов гипноседативного ряда может привести к приступу в течение следующих нескольких суток. В литературе есть даже описание случаев развития приступов после отмены назначенных в стационаре наркотических анальгетиков. Общим принципом является выполнение полного токсикологического скрининга при отсутствии другой очевидной причины проявлений эпиактивности.
Всем пациентам в рамках дифференциальной диагностики следует выполнить анализ крови на глюкозу и электролитный состав. Тяжелая гипергликемия или гипонатриемия способны провоцировать развитие эпиприступа. В редких случаях эписиндром может манифестировать развитие у пациента СД. Гипокальциемия способна провоцировать приступ, но ее роль в качестве причины маловероятна вне неонатального периода, и поэтому ее выявление не должно останавливать диагностический процесс. Гипомагнезиемия часто ассоциирована с приступами у пациентов, длительно употреблявших алкоголь.
Любой пациент с эпиприступом должен быть в кратчайшие сроки осмотрен неврологом для выявления глобальных или фокальных признаков поражения ЦНС. При наличии у вновь поступившего в ОРИТ пациента с эпиприступом признаков системной воспалительной реакции или выраженных воспалительных явлений, например на слизистых, к осмотру также следует привлечь инфекциониста. По результатам собранного анамнеза, семиологии приступа, вероятных причин его развития и на основании консультации вызванных специалистов для дальнейшей диагностики может потребоваться выполнение КТ, магнитно-резонансной терапии и/или люмбальной пункции в неотложном порядке.
Скальповая ЭЭГ является высокоспецифичным методом определения патологической активности нейронов ГМ, в том числе и эпилептогенной, при этом показаний для ее экстренного выполнения после единичного приступа нет. Важнейшую роль данный метод приобретает при ведении пациента с очевидным эпистатусом или при подозрении на его развитие. Формирование рефрактерного эпистатуса является абсолютным показанием для проведения непрерывного ЭЭГ-мониторинга (наиболее оптимальным считают видео-ЭЭГ-мониторинг). Рефрактерный статус эпиприступов также является основанием для нахождения пациента в ОРИТ. К сожалению, интерпретация ЭЭГ требует специальной подготовки. Применение количественной ЭЭГ и как ее варианта амплитуд-интегрированной ЭЭГ может значительно облегчить ведение пациентов с рефрактерным эпистатусом. При выборе варианта терапии эпистатуса с применением общих анестетиков и достижением ЭЭГ-паттерна «вспышка-подавление» при отсутствии полноценного ЭЭГ ориентировочным способом подбора терапии является применение мониторов глубины анестезии, которые в качестве одного из показателей рассчитывают так называемое отношение вспышки к подавлению (BSR - burst-suppression ratio). При лечении генерализованного тонико-клонического эпистатуса купирование судорожных проявлений выходит на первый план вне зависимости от причины и сопутствующий диагностический процесс следует проводить параллельно.
Лечение
Чаще всего одиночные эпиприступы являются четко ограниченными по времени. При этом для разных типов эпиприступов характерно различное время t1 , за пределы которого в подавляющем большинстве случаев продолжительность приступа не выходит. Одиночный приступ, за исключением охранительных мероприятий (прекращение инфузии препарата, предположительно приведшего к приступу, при утрате контакта укладка на бок для профилактики регургитации и аспирации, освобождение окружающего пациента пространства от твердых и острых предметов, удержание в пределах кровати и т.д.), не требует, как правило, медикаментозного лечения. С точки зрения проводимых мероприятий при впервые выявленном эпиприступе основополагающее значение имеет диагностика возможной причины и фиксация продолжительности. При выходе последней за рамки _t1 _ эпиактивность следует рассматривать как статус и приступать к неотложному медикаментозному лечению вне зависимости от этиологии.
В соответствии с принципами медицины, основанной на доказательствах, ILAE в 2016 г. опубликовала алгоритм ведения пациента со статусом генерализованных тонико-клонических приступов [3]. С учетом отсутствия некоторых противосу-дорожных препаратов и/или их парентеральных форм на отечественном рынке к применению рекомендован следующий алгоритм действий (рис. 4-9). При диагностике эпистатуса диагностические и лечебные мероприятия следует проводить одновременно. Препаратами выбора первой линии являются парентеральные формы следующих БД: диазепам (допустимо двукратное введение) и мидазолам. В отношении диазепама следует помнить, что при внутривенном болюсном введении его не стоит растворять в изотоническом растворе натрия хлорида. Это приводит к помутнению и, вероятно, снижению антиэпилептических свойств. Несмотря на местное раздражающее действие, рекомендовано вводить 0,5% раствор диазепама с дальнейшим промыванием внутривенного катетера изотоническим раствором натрия хлорида. При капельном же введении растворять диазепам необходимо в не менее чем 100 мл изотонического раствора натрия хлорида.
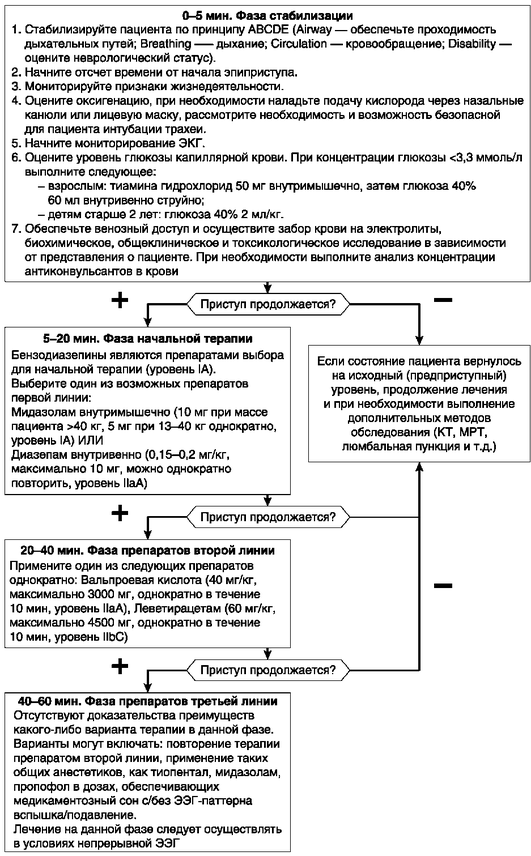
При персистенции эпистатуса после применения рекомендованных доз бензодиазепина необходимо начать парентеральное введение препаратов второй линии. У пациентов с купированным эпистатусом, обратимую причину эпиактивности которых немедленно устранить не представляется возможным, введение данных препаратов преследует цель быстрого достижения терапевтических дозировок антиконвульсанта для профилактики рецидива. Среди таких препаратов на отечественном рынке представлены вальпроевая кислота (Вальпроат натрия♠ ) и леветирацетам. Неотложность ситуации требует превышения рекомендованных отечественной инструкцией скорости и дозировок данных препаратов для быстрого достижения необходимой концентрации в плазме крови. Безопасность и эффективность такого варианта введения при эпистатусе отражена в многочисленных публикациях.
При неэффективности рекомендованных дозировок препаратов первой и второй линии эпистатус считают рефрактерным. В настоящее время не существует общепринятого мнения и рекомендаций по ведению пациентов с рефрактерным эпи-статусом. Сомнений нет лишь в том, что такой статус по возможности необходимо лечить в условиях непрерывного ЭЭГ-мониторинга в условиях ОРИТ. В порядке возрастания агрессивности медикаментозную терапию можно разделить на три варианта: повторение или добавление других препаратов второй линии, введение препаратов для общей анестезии (мидазолам, пропофол, тиопентал натрия) и введение данных препаратов с достижением ЭЭГ-паттерна «вспышка-подавление» (табл. 4-20). По всей видимости, при рефрактерном статусе сложных и фокальных приступов следует применять наименее агрессивный вариант, тогда как статус тонико-клонических судорог будет требовать максимальной агрессивности.
Мидазолам обладает меньшим кардиодепрессивным действием, но с точки зрения купирования рефрактерного статуса менее эффективен в сравнении с пентобарбиталом [6]. Пропофол при лечении удобен в силу выгодной фармакодинамики, при этом опасным осложнением при длительном (более 48 ч) введении является синдром инфузии пропофола, проявляющийся острой рефрактерной брадикардией с переходом в асистолию на фоне метаболического ацидоза, и/или рабдомиолиза, и/или гиперлипидемии, и/или увеличения печени. В целом в отношении непрерывной инфузии препаратов для неингаляционной анестезии для купирования рефрактерного статуса существует ряд обстоятельств, которые следует учитывать.
-
Пациент всегда будет нуждаться в длительном обеспечении проходимости дыхательных путей и ИВЛ.
-
При выборе тактики введения с достижением ЭЭГ-паттерна «вспышка-подавление» дозы для его достижения на начальных этапах для тиопентала натрия (Тиопентала♠ ) часто будут выше рекомендуемых (до 10 мг/кг/ч) в инструкции (3-5 мг/кг/ч), при этом уже через несколько часов (при насыщении жировой ткани) скорость инфузии может потребовать коррекции в сторону уменьшения.
-
Тиопентал натрия и пропофол обладают угнетающим влиянием на систему кровообращения, что в большинстве случаев будет требовать применения инотропной поддержки. Гипотензия носит обратимый характер и проходит при последующем прекращении инфузии. При этом важно не пропустить такие ассоциированные состояния, как сепсис, водно-электролитные нарушения (крайне редко - ИМ).
-
Тиопентал натрия способствует развитию гипотермии (поверхностная температура тела менее 35 °C) и возрастанию риска инфекционных осложнений [вентилятор-ассоциированная пневмония (ВАП), катетер-ассоциированные инфекции и инфекции мочеполовой системы].
-
Пациент при введении общих анестетиков полностью обездвижен, поэтому нуждается в комплексе мероприятий, направленных на профилактику пролежней.
-
Для тиопентала натрия в некоторых случаях описывают развитие ларинго-спазма или бронхоспазма, в связи с чем следует с осторожностью использовать у пациентов с ХОБЛ или астмой.
| Препарат | Начальная доза | Непрерывное введение под контролем ЭЭГ | Серьезные побочные эффекты | Особенности |
|---|---|---|---|---|
Мидазолам |
0,2 мг/кг со скоростью 2 мг/мин |
0,05-2 мг/кг/ч; «прорывной» приступ♠: 0,1-0,2 мг/кг болюс, увеличение скорости на 0,05- 0,1 мг/кг/ч каждые 3-4 ч |
Угнетение дыхания; гипотензия |
Тахифилаксия при длительном применении; активный метаболит, быстрое распределение (короткая длительность), не содержит про-пиленгликоль |
Пропофол |
1-2 мг/кг за 20-40 с |
4-12 мг/кг/ч; с осторожностью при длительности введения более 48 ч; «прорывной» приступ: 1 мг/кг болюс, увеличение скорости на 0,5 мг/кг/ч |
Гипотензия (особенно при введении нагрузочной дозы у пациентов в тяжелом состоянии); угнетение дыхания; недостаточность кровообращения; рабдомиолиз; метаболический ацидоз; почечная недостаточность |
Необходимо учитывать в суточном потреблении калорий (1,1 ккал/мл пропофола) |
Тиопентал натрия (Тиопентал♠) |
2-7 мг/кг (по 50 мг/мин) |
0,5-5 мг/кг/ч; «прорывной» приступ: 1-2 мг/кг болюс, увеличение скорости на 0,5-1 мг/кг/ч |
Гипотензия; угнетение дыхания; недостаточность кровообращения |
Метаболизируется до пентобарбитала |
* «Прорывной» приступ - эпиприступ на фоне проводимого лечения рефрактерного статуса препаратами третьей линии.
Перспективным препаратом для купирования эпистатуса является кетамин, однако в настоящее время недостаточно исследований, позволяющих рекомендовать его применение. Рекомендуется применять все методики купирования эпистатуса (ингаляционные и неингаляционные анестетики, ИВЛ и пр.) не менее 48 ч. В качестве дополнительных методик используются кетогенная диета (соотношение жиров с остальными компонентами 4:1), умеренная гипотермия, глюко-кортикоиды и иммуноглобулины (при подозрении на аутоиммунный энцефалит абсолютно показаны).
Список литературы
-
Trinka E., Cock H., Hesdorffer D. et al. A definition and classification of status epilep-ticus - Report of the ILAE Task Force on Classification of Status Epilepticus // Epilepsia. 2015. Vol. 56, N 10. P. 1515-1523.
-
Fisher R.S., Cross J.H., French J.A. et al. Operational classification of seizure types by the International League Against Epilepsy: Position Paper of the ILAE Commission for Classification and Terminology // Epilepsia. 2017. Vol. 58, N 4. P. 522-530.
-
Glauser Т., Shinnar Sh., Gloss D. et al. Evidence-based guideline: treatment of convulsive status epilepticus in children and adults: report of the guideline committee of the American Epilepsy Society // Epilepsy Curr. 2016. Vol. 16, N 1. P. 48-61.
-
Gilmore R.L. Seizures // Textbook of Neurointensive Care / eds A.J. Layon, A. Gabrielli, W.A. Friedman et al. Philadelphia : W.B. Saunders, 2004.
-
Brophy G.M., Bell R., Claassen J. et al. Guidelines for the evaluation and management of status epilepticus // Neurocrit. Care. 2012. Vol. 17, N 1. P. 3-23.
-
Claassen J., Hirsch L.J., Emerson R.G., Mayer S.A. Treatment of refractory status epi-lepticus with pentobarbital, propofol, or midazolam: a systematic review // Epilepsia. 2002. Vol. 43, N 2. P. 146-153.