Неонатология. Клинические рекомендации / под ред. Н. Н. Володина, Д. Н. Дегтярева, Д. С. Крючко. - Москва : ГЭОТАР-Медиа, 2021. - 320 с. - ISBN 978-5-9704-6213-3. |
Аннотация
Книга содержит клинические рекомендации по наиболее распространенным в неонатальной практике заболеваниям новорожденных, подготовленные ведущими специалистами Российского общества неонатологов и Российской ассоциации специалистов перинатальной медицины. В издании рассмотрены эпидемиология, патогенез, клиническая картина, классификация, современные методы диагностики и дифференциальной диагностики, а также подходы к медикаментозному и немедикаментозному лечению гемолитической и геморрагической болезней новорожденных, непрямой гипербилирубинемии, врожденной пневмонии, инвазивного кандидоза, мекониальной аспирации, открытого артериального протока у недоношенных. Подробно изложены также технологии парентерального питания, энтерального вскармливания и терапевтической гипотермии новорожденных. В разделе "В помощь практическому врачу" приведены методические рекомендации по профилактике и контролю госпитальной инфекции и по оказанию базовой помощи и организации грудного вскармливания в перинатальном центре. Соблюдение международной методологии, использование современных литературных источников в подготовке данного издания гарантируют его актуальность, достоверность и обобщение лучшего мирового опыта и знаний.
Клинические рекомендации по неонатологии предназначены практикующим врачам-неонатологам, педиатрам, терапевтам, врачам других специальностей, а также студентам старших курсов медицинских вузов.
Тактика ведения доношенных и недоношенных новорожденных с непрямой гипербилирубинемией
Согласовано и утверждено Российским обществом неонатологов и Российской ассоциацией специалистов перинатальной медицины
Авторы: Володин Н.Н., Дегтярев Д.Н., Дегтярева А.В., Карпова А.Л., Мебелова И.И., Пруткин М.Е., Сенькевич О.А. (модератор рабочей группы), Харламова Н.В.
ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
Гипербилирубинемия (от греч. hyper + билирубин + haima - «кровь») - любое увеличение концентрации билирубина в сыворотке или плазме крови сверх нормативных значений.
Непрямая гипербилирубинемия - повышение концентрации, обусловленное преимущественно (более чем на 80%) непрямой фракцией билирубина.
Гипербилирубинемия в неонатологии - состояния, при которых у доношенных и недоношенных ГВ 35-36 нед отмечается повышение концентрации ОБ в сыворотке крови более 256 мкмоль/л, а у детей, родившихся до 35-й недели гестации, - повышение концентрации ОБ более 171 мкмоль/л (уровень доказательности B).
Желтуха - визуальное проявление повышенного уровня билирубина в крови. У доношенных новорожденных появляется при уровне билирубина более 67 мкмоль/л, у недоношенных - более 120 мкмоль/л (уровень доказательности C).
Повышение концентрации билирубина в крови у новорожденных и развитие желтухи может быть вызвано как физиологическими, так и патологическими причинами. К раннему появлению, прогрессирующему нарастанию и высокой интенсивности желтухи следует относиться как к симптомам потенциально опасного заболевания (уровень доказательности D).
Нарушение структуры и функции головного мозга, обусловленное непрямой гипербилирубинемией, носит название билирубиновой энцефалопатии (БЭ), или ядерной желтухи.
Ранними предикторами повышенного риска развития БЭ у доношенных новорожденных являются концентрация ОБ в пуповинной крови более 51 мкмоль/л, почасовой прирост ОБ более 6,8 мкмоль/л в час, появление желтухи в первые 24 ч жизни.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Физиологическая желтуха
Основные физиологические причины повышения концентрации билирубина в сыворотке крови у детей в первые дни жизни (уровень доказательности D):
-
более высокая скорость образования билирубина, обусловленная физиологической полицитемией и более короткой продолжительностью жизни эритроцитов, содержащих фетальный гемоглобин (70-90 дней по сравнению с 110-120 днями у взрослых);
-
функционирующий венозный проток и уменьшенная перфузия крови в пространстве Диссе препятствуют полноценному захвату билирубина гепатоцитами;
-
сниженная активность фермента глюкуронилтрансферазы, обеспечивающей конъюгацию билирубина, и недостаточная концентрация Y-протеина, обеспечивающего транспорт билирубина в гепатоцитах;
-
исходно низкая экскреторная функция печени (1-2% экскреторной способности печени взрослого);
-
усиленная реабсорбция билирубина из тонкой кишки вследствие высвобождения билирубина из химической связи с глюкуроновой кислотой под влиянием повышенной активности фермента β-глюкоронидазы.
Непрямая гипербилирубинемия, вызванная патологическими причинами
Несоответствие хотя бы по одному из типичных для физиологической желтухи клинических и лабораторных признаков с высокой вероятностью свидетельствует о том, что нарушение обмена билирубина вызвано патологическими причинами.
Факторы риска патологической гипербилирубинемии у доношенных новорожденных.
-
Восточноазиатское или средиземноморское происхождение (уровень доказательности B).
-
Несовместимость по системе АВ0 или резус-фактору матери и плода (уровень доказательности B).
-
Использование окситоцина в родах (уровень доказательности D).
-
Желтуха, развившаяся в первые сутки жизни (уровень доказательностиB).
-
Кефалогематома/экхимозы, крупные гемангиомы (уровень доказательности B).
-
Гипогалактия при исключительно грудном вскармливании (уровень доказательности C).
-
Нарушенное сосание/недостаточное питание (уровень доказательности C).
-
Эксикоз (патологическая убыль массы тела) (уровень доказательности B).
-
Врожденные и перинатальные инфекции (уровень доказательности B).
-
Дефицит глюкозо-6-фосфатдегидрогеназы (уровень доказательности B).
Практически всегда гипербилирубинемия у недоношенных детей, родившихся ранее 35-й недели гестации, обусловлена нефизиологическими причинами.
В большинстве случаев патологической гипербилирубинемии, возникающей на первой неделе жизни, отмечается преобладание в крови непрямой фракции билирубина (уровень доказательности C).
ЭПИДЕМИОЛОГИЯ
Желтуха на первой неделе жизни регистрируется у 60-80% здоровых доношенных новорожденных (уровень доказательности A).
КОДЫ ПО МЕЖДУНАРОДНОЙ КЛАССИФИКАЦИИ БОЛЕЗНЕЙ 10-ГО ПЕРЕСМОТРА
-
Р59 Неонатальная желтуха, обусловленная другими и неуточненными причинами.
-
Р59.0 Неонатальная желтуха, связанная с преждевременным родоразрешением.
-
Р59.2 Неонатальная желтуха вследствие других и неуточненных повреждений клеток печени.
-
Р59.8 Неонатальная желтуха, обусловленная другими уточненными причинами.
КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ
По ведущим патогенетическим механизмам все случаи непрямой гипербилирубинемии у новорожденных можно разделить на четыре группы.
Наиболее вероятные причины, приводящие к непрямой патологической гипербилирубинемии у новорожденных с учетом ведущих патогенетических механизмов, перечислены в табл. 1 (уровень доказательности C).
Гиперпродукция билирубина |
|
Нарушение конъюгации билирубина |
|
Повышение кишечной реабсорбции |
Обструкция ЖКТ или кишечная непроходимость (при пилоростенозе, атрезиях кишечника, болезни Гиршпрунга, мекониальном илеусе или мекониальной пробке), парез кишечника |
Смешанного генеза |
Ранний и поздний неонатальный сепсис. Внутриутробная инфекция различной этиологии (листериоз, цитомегалия, краснуха, токсоплазмоз, гепатит В, герпес, сифилис и др.). Глубокая степень недоношенности (выраженная морфофункциональная незрелость) ребенка |
КЛИНИЧЕСКАЯ КАРТИНА
Ведущие патогенетические механизмы развития гипербилирубинемии во многом определяют время возникновения и степень выраженности гипербилирубинемии. Раннее распознавание конкретной причины нарушений билирубинового обмена позволяет не только прогнозировать течение желтухи, но и эффективно предупреждать осложнения, ассоциированные с гипербилирубинемией (уровень доказательности C).
Для физиологической желтухи характерны:
-
отсутствие клинико-лабораторных признаков анемии или полицитемии;
-
появление желтой окраски кожи в возрасте более 24 ч жизни (почасовой прирост билирубина в 1-е сут составляет менее 3,4 мкмоль/л, суммарно за первые сутки - менее 85,5 мкмоль/л);
-
максимальная выраженность желтой окраски лица, туловища и конечностей на 3-4-е сутки жизни, желтуха не распространяется на ладони и стопы;
-
не наблюдается патологических оттенков желтой окраски кожи (серого, зеленоватого, лимонного);
-
максимальная концентрация ОБ не более 255 мкмоль/л, концентрация прямой фракции билирубина не выше 34 мкмоль/л;
-
быстрое уменьшение интенсивности и распространенности желтухи после 4-х суток жизни, угасание желтухи к 8-10-м суткам жизни.
Примерно в половине случаев при физиологическом течении желтухи к 3-4-м суткам возникает кратковременная непрямая гипербилирубинемия, которая не имеет негативных клинических последствий и не требует никаких медицинских вмешательств (уровень доказательности D).
Понятие «физиологическая желтуха» применимо только по отношению к доношенным новорожденным и недоношенным ГВ 35-36 нед (уровень доказательности D). Это состояние кодированию по МКБ не подлежит и при анализе заболеваемости новорожденных не учитывается.
Патологическая желтуха. Любые отклонения в клинической картине и динамике лабораторных показателей, характеризующих билирубиновый обмен, от физиологических должны рассматриваться как признаки патологической желтухи, причина которой требует дополнительного клинико-лабораторного обследования ребенка.
NB! Во всех случаях развития патологической гипербилирубинемии, обусловленной гиперпродукцией билирубина и в части случаев нарушением конъюгации билирубина, возникает риск развития метаболического поражения центральной нервной системы (ЦНС) за счет потенциальной нейротоксичности высокой концентрации неконъюгированного билирубина в крови (уровень доказательности C).
Билирубиновая энцефалопатия
При использовании современных перинатальных технологий БЭ (код по МКБ-10 - Р57) является предотвратимым состоянием (уровень доказательности D).
БЭ у доношенных новорожденных развивается в случаях превышения концентрации ОБ в сыворотке крови выше 342 мкмоль/л с выраженными индивидуальными различиями концентраций (от 342 до 684 мкмоль/л), при которых происходит метаболическое поражение головного мозга (уровень доказательности B).
В последние два десятилетия частота БЭ в различных странах мира находится в диапазоне от 0,4 до 2,7 на 100 000 популяции (уровень доказательности В).
Вероятность развития БЭ при патологической гипербилирубинемии повышается на фоне таких факторов риска, как (уровень доказательности B):
-
недоношенность или морфофункциональная незрелость организма ребенка (уровень доказательности B);
-
тяжелая врожденная и неонатальная инфекция (сепсис, менингит) (уровень доказательности B);
-
дефицит глюкозо-6-фосфатдегидрогеназы (уровень доказательностиC);
-
гипоальбуминемия (концентрация сывороточного альбумина менее 25 г/л) (уровень доказательности C);
-
выраженный метаболический ацидоз (pH артериальной крови менее 7,15 более 1 ч) (уровень доказательности C);
-
тяжелая асфиксия новорожденного (оценка по шкале Апгар менее 4 баллов), артериальная гипотензия, апноэ, потребность в ИВЛ (уровень доказательности C);
-
гипотермия (ректальная температура менее 35 °С) (уровень доказательности C);
-
обширная травма мягких тканей в родах, массивные кефалогематомы, перивентрикулярные, ВЖК и субарахноидальные кровоизлияния (уровень доказательности C);
Кроме того, ряд препаратов (в первую очередь, антибиотиков), могут вытеснять билирубин из связи с альбумином (уровень доказательности C).
У недоношенных детей вероятность БЭ развивается при более низких концентрациях билирубина, чем у доношенных новорожденных, и зависит от концентрации билирубина в крови и массы тела ребенка при рождении.
У детей, родившихся с очень низкой и экстремально низкой массой тела (ОНМТ и ЭНМТ), БЭ может возникнуть даже после умеренного повышения концентрации ОБ в сыворотке крови (в диапазоне 171- 255 мкмоль/л) (уровень доказательности B).
В повседневной неонатологической практике при определении риска развития БЭ ориентируются на минимальные пороговые концентрации билирубина в сыворотке крови, при которых в прошлом регистрировались случаи развития ядерной желтухи.
В течении БЭ можно условно выделить четыре фазы.
-
Асфиктическую фазу. Характерно нарастание признаков билирубиновой интоксикации - угнетение безусловно-рефлекторной деятельности: апноэ, апатия, вялость, сонливость, вялое сосание, монотонный крик, срыгивания, рвота, блуждающий взгляд. При неблагоприятном течении эти признаки в большинстве случаев появляются на 4-й день жизни и в случаях экстренного проведения ОЗПК носят обратимый характер (уровень доказательности A).
-
Спастическую фазу. При неэффективном лечении появляются классические признаки ядерной желтухи: спастичность, ригидность затылочных мышц, вынужденное положение тела с опистотонусом, негнущимися конечностями и сжатыми в кулак кистями; периодическое возбуждение и резкий мозговой крик, выбухание большого родничка, подергивание мышц лица, крупноразмашистый тремор рук, исчезновение рефлекса Моро и видимой реакции на сильный звук, сосательного рефлекса; нистагм, апноэ, брадикардия, летаргия, иногда повышение температуры тела; судороги, симптом заходящего солнца. Эта фаза имеет продолжительность от нескольких дней до нескольких недель, поражение ЦНС носит необратимый характер.
-
Фазу ложного неврологического благополучия и полного или частичного исчезновения спастичности (2-3 мес жизни).
-
Фазу формирования клинической картины неврологических осложнений (после 3-5 мес жизни): параличи, парезы, атетоз, хореоатетоз, глухота, детский церебральный паралич, задержка психического развития, дизартрия (уровень доказательности B).
Первые две фазы заболевания являются признаком острого метаболического поражения ЦНС и обозначаются термином «острая БЭ». Отдаленные неврологические нарушения, вызванные нейротоксическим действием билирубина (4-я фаза), обозначаются термином «хроническая БЭ».
Развитие классических признаков острой БЭ в случаях непрямой гипербилирубинемии характерно для доношенных новорожденных и недоношенных, родившихся на 35-36-й нед гестации (уровень доказательности A). У глубоко недоношенных детей при надпороговых значениях гипербилирубинемии характерные клинические признаки острой БЭ могут отсутствовать или маскироваться симптомами других патологических состояний, но во втором полугодии жизни у них появляются типичные признаки хронической БЭ (уровень доказательности D).
В целях раннего выявления, оценки динамики и определения тяжести БЭ у новорожденных L. Jonson, V.K. Bhutani, K. Karp и соавт. предложили балльную шкалу, позволяющую учитывать степень выраженности неврологических дисфункций, характеризующих острую БЭ (табл. 2).
| Клинические симптомы | Билирубин-ассоциированная дисфункция центральной нервной системы, баллы | Острая билирубиновая энцефалопатия |
|---|---|---|
Психический статус |
||
Физиологический |
0 |
Нет |
Сонный, требует пробуждения на кормление |
1 |
Минимальная |
Летаргия/вялое сосание или раздражительность/возбуждение с повышенным сосательным рефлексом |
2 |
Умеренная |
Сопор, апноэ, отказ от еды, судороги, кома |
3 |
Тяжелая |
Мышечный тонус |
||
Физиологический |
0 |
Нет |
Гипотония от легкой до умеренной |
1 |
Минимальная |
Гипертония от легкой до умеренной, чередующаяся с гипотонией, разгибание шеи и туловища в ответ на стимуляцию |
2 |
Умеренная |
Персистирующий шейно-тонический синдром и опистотонус, стереотипные движения в виде педалирования или подергивания в руках и ногах |
3 |
Тяжелая |
Характер крика |
||
Физиологический |
0 |
Нет |
Высокотональный при пробуждении |
1 |
Минимальная |
Пронзительный, тяжело успокоить |
2 |
Умеренная |
Безутешный плач/слабый крик или отсутствует |
3 |
Тяжелая |
Суммарная оценка:* |
||
*Интерпретация результатов: 1-3 балла - минимальная; 4-6 баллов - умеренная; 7-9 баллов - тяжелая БЭ.
Предупреждение билирубиновой энцефалопатии
В случаях выявления патологической гипербилирубинемии первоочередные усилия должны быть направлены на предотвращение критических концентраций билирубина в крови, при которых вероятно развитие БЭ.
Медицинские мероприятия, направленные на профилактику БЭ, можно условно разделить на четыре этапа.
-
Клинико-анамнестический и клинико-лабораторный скрининг новорожденных на возможность развития или наличие патологической гипербилирубинемии (выявление группы риска).
-
Определение степени и выявление ведущего патогенетического механизма развития гипербилирубинемии.
-
Подготовка и проведение лечебных мероприятий, направленных на уменьшение концентрации непрямого билирубина (НБ) в сыворотке крови:
-
создание оптимальных условий медицинского ухода и при необходимости проведение интенсивной терапии основного и сопутствующих заболеваний;
-
в случаях недостаточной эффективности ФТ - подготовка и проведение ОЗПК, при необходимости - создание дополнительных условий, повышающих ее эффективность;
-
клинико-лабораторный мониторинг безопасности и эффективности комплекса лечебных мероприятий (до момента полного их завершения).
-
-
Выявление или подтверждение конкретной причины развития непрямой гипербилирубинемии, потребовавшей медицинского вмешательства, при необходимости (в диагностически сложных случаях) - продолжение дифференциально-диагностических мероприятий и лечения основного и сопутствующего заболеваний.
Первые три этапа должны быть организованы в любой медицинской организации акушерско-гинекологического или педиатрического профиля независимо от ее функционального уровня. Для организации четвертого этапа может потребоваться перевод ребенка в учреждение третьего уровня (в перинатальный центр или детскую многопрофильную или специализированную больницу).
Клиническая характеристика наиболее частых причин патологической непрямой гипербилирубинемии, возникающей в позднем неонатальном периоде
Конъюгационные желтухи
Желтуха, связанная с составом грудного молока, наблюдается у 0,5- 2,5% здоровых доношенных детей, находящихся на грудном вскармливании, вследствие повышенного содержания метаболитов прогестерона и неэстерифицированных длинноцепочечных жирных кислот, которые конкурентно ингибируют глюкуронилтрансферазу, наличия глюкуронидазы, высокой активности фермента липопротеинлипазы в молозиве и грудном молоке. Часто этот вариант гипербилирубинемии ассоциирован с приемом гормональных препаратов и некоторых других лекарственных средств во время беременности, стимуляции родовой деятельности. У новорожденных с желтухой, связанной с составом грудного молока, наблюдается более высокая концентрация НБ в крови к 4-6-му дню жизни, которая продолжает нарастать, достигая пика к 10-15-му дню жизни. Состояние ребенка при этом удовлетворительное, отмечается хорошая прибавка массы тела. Если ребенок продолжает получать грудное молоко, желтуха держится 4-6 нед и затем начинает постепенно ослабевать. Уровень НБ в крови нормализуется к 16-й неделе жизни. Прекращение грудного вскармливания на 48-72 ч способствует быстрому снижению концентрации НБ, как правило, не менее чем на 40% и имеет диагностическое значение при данном варианте гипербилирубинемии. После возобновления кормления грудью НБ может повыситься, но он не достигает исходного уровня и в дальнейшем постепенно снижается. Вместе с тем длительная отмена грудного молока в целях полной нормализации билирубина нецелесообразна, так как в большинстве случаев уровень билирубина не превышает 340 мкмоль/л.
Транзиторная семейная гипербилирубинемия новорожденных (синдром Люцея-Дрискола) является разновидностью желтухи, связанной с составом грудного молока, механизм ее развития связывают с наличием неидентифицированного фактора, ингибирующего ферментную систему трансферазы глюкуроновой кислоты в грудном молоке. Желтуха появляется с первых дней жизни, имеет тенденцию к прогрессивному нарастанию и затяжному течению. Уровень НБ в крови может превышать 340 мкмоль/л, что обусловливает необходимость своевременной диагностики и лечения. Отмена грудного вскармливания на 2-3 дня способствует снижению уровня билирубина и, следовательно, имеет диагностическое значение. Исследование химического состава грудного молока позволяет дифференцировать данный вариант гипербилирубинемии с другими желтухами, связанными с составом грудного молока, что не является принципиальным с практической точки зрения.
В основе желтухи, обусловленной исключительно грудным вскармливанием, лежит первоначально недостаточный объем питания, что способствует усилению липолиза и, как следствие, повышению в крови неэстерифицированных жирных кислот, нарушающих процесс захвата билирубина гепатоцитом и подавляющих активность глюкуронилтранс-феразы. Вторым фактором, способствующим гипербилирубинемии, является замедление пассажа по кишечнику и, как следствие, повышение реабсорбции билирубина. Этот вариант желтухи отмечается у 12% детей, находящихся на грудном вскармливании в период становления лактации и не получающих должный объем питания. Она появляется на 2-4-е сутки жизни, пик приходится на 3-6-й день, по мере увеличения объема кормления нормализуются обменные процессы, восстанавливается пассаж по кишечнику, и к концу первого месяца жизни желтуха купируется. Как правило, первоначальная потеря массы тела составляет 8-10% и более, общее состояние ребенка не страдает. В случае большой потери массы тела у детей на исключительно грудном вскармливании необходимо обеспечить докорм ребенка.
Конъюгационная желтуха при гипотиреозе. Гормоны щитовидной железы регулируют активность глюкуронилтрансферазы, их дефицит может стать причиной нарушения конъюгации билирубина. Подтверждением диагноза является низкий уровень Т3 , Т4 и повышение тиреотропного гормона в крови.
Наследственные формы конъюгационных желтух. Синдром Жильбе-ра - наследственное заболевание (частота в популяции составляет от 2 до 6%), передающееся по аутосомно-доминантному типу и связанное с нарушением захвата билирубина синусоидальной мембраной гепатоцита. Отмечается снижение до 50% нормы активности глюкуронил-трансферазы печени. Желтуха обычно выражена умеренно, в пределах 80-120 мкмоль/л, случаев БЭ не описано, общее состояние не нарушается. Клинические проявления могут отмечаться со 2-3-х суток жизни, причем интенсивность желтухи может меняться каждые 3-5 нед. С диагностической целью может быть использован фенобарбитал в терапевтической дозе 5 мг/кг в сутки в течение 3 дней; характерно снижение билирубина на 50-60%, что позволяет с высокой вероятностью предположить данный синдром. Дополнительное диагностическое значение имеет анализ родословной, свидетельствующий о синдроме Жильбера в семье. Подтверждение диагноза возможно на основании генетического тестирования.
Синдром Криглера-Найяра - наследуемая негемолитическая желтуха с повышением НБ вследствие врожденной недостаточности глюкуро-нилтрансферазы. Механизм желтухи сводится к полной или почти полной неспособности печени конъюгировать билирубин. Известны две генетически гетерогенные формы, и в связи с этим выделяют два типа.
Синдромом Криглера-Найяра I типа передается по аутосомно-рецессивному типу. Характерна интенсивная желтуха с 15-50-кратным превышением нормального уровня НБ в сыворотке крови, которая без лечения сопровождается развитием БЭ. Гипербилирубинемия развивается в течение первых дней после рождения и сохраняется всю жизнь. Назначение фенобарбитала (с дифференциально-диагностической целью) не приводит к уменьшению сывороточной концентрации билирубина. Диагноз устанавливается на основании прогрессивного нарастания уровня НБ, не связанного с гемолизом эритроцитов, и отрицательной реакции на назначение фенобарбитала с дифференциально-диагностической целью (отсутствие снижения концентрации билирубина после назначения фенобарбитала в возрастной дозе в течение 3 дней). Подтверждается молекулярно-генетическими методами. Использование ФТ является наиболее эффективным методом консервативного лечения детей раннего возраста, позволяющим несколько снизить уровень билирубина и зафиксировать его на некоторое время. В течение первых 10 дней жизни оптимально постоянное проведение ФТ в целях поддержания уровня билирубина ниже 340 мкмоль/л, затем продолжительность ФТ может быть уменьшена до 10-16 ч в сутки. В дальнейшем чувствительность гематоэнцефалического барьера снижается, в связи с чем уровень билирубина может подниматься выше 340 мкмоль/л, но не более чем до 500 мкмоль/л. Сегодня нет однозначного мнения об уровне билирубина у детей старше 1 мес, который является токсичным (диапазон колебаний литературных данных - от 500 до 800 мкмоль/л). Имеется собственный опыт наблюдения ребенка с синдромом Криглера-Найяра I типа с повышением уровня билирубина до 650 мкмоль/л без развития признаков БЭ). Радикальным методом лечения служит трансплантация печени или гепатоцитов; в ургентных ситуациях, при высоком риске развития БЭ, показано проведение ОЗПК или плазмафереза.
Синдром Криглера-Найяра II типа передается по аутосомно-доминантному типу, является прогностически более благоприятным заболеванием и сопровождается менее выраженной желтухой с 5-20-кратным повышением НБ в сыворотке крови. Отличительной особенностью этой формы служит уменьшение ОБ на фоне 3-дневного применения фенобарбитала не менее чем на 50-60%. Дефицит глюкуронилтрансферазы менее выражен, уровень ОБ в сыворотке крови варьирует от 91 до 640 мкмоль/л, но чаще всего не превышает 340 мкмоль/л. Развитие БЭ отмечается редко и в основном происходит в раннем неонатальном периоде при участии других патологических факторов. Динамический контроль за показателями НБ в сыворотке крови и раннее назначение фенобарбитала, своевременное и адекватное проведение ФТ позволяют эффективно снизить уровень ОБ и предупредить развитие энцефалопатии. В целях подтверждения диагноза возможно проведение молекулярно-генетического исследования.
Желтуха, обусловленная повышенной реабсорбцией билирубина в кишечнике, - вторичная вследствие повышения реабсорбции билирубина в кишечнике, что может быть обусловлено обструкцией ЖКТ или кишечной непроходимостью при пилоростенозе, болезни Гиршпрунга, мекониальном илеусе, при парезах кишечника и др. Исключение врожденных и приобретенных заболеваний ЖКТ должно входить в план дополнительного обследования ребенка с поздней или затянувшейся желтухой.
ДИАГНОСТИКА
Жалобы и анамнез (клинико-анамнестические данные)
В группу высокого риска по развитию непрямой гипербилирубинемии сразу после рождения должны быть выделены:
-
новорожденные, с клиническими и/или лабораторными признаками гемолитической болезни;
-
новорожденные с выраженными признаками морфофункциональной незрелости, в том числе глубоко недоношенные дети;
-
новорожденные с множественными подкожными кровоизлияниями и обширными кефалогематомами;
-
новорожденные, нуждающиеся в реанимационной и интенсивной терапии в раннем неонатальном периоде, включая детей с внутриутробной инфекцией и неонатальным сепсисом;
-
новорожденные с высоким риском раннего проявления болезней обмена или наследственных гемолитических анемий (отягощенный семейный анамнез или наличие соответствующих лабораторных признаков);
-
наличие в семье других детей с выраженной гипербилирубинемией, требующей лечения в неонатальном периоде.
Типичные проявления
Исторически сложилось, что в целях раннего выявления гипербилирубинемии многие неонатологи ориентируются в первую очередь на изменение цвета кожного покрова. Безусловно, раннее появление желтухи (до 24 ч жизни), нарастание после 4 сут и сохранение более 2 нед свидетельствуют о наличии патологической гипербилирубинемии. Появление желтухи в первые 24 ч свидетельствует о гиперпродукции билирубина, вызванного патологическим гемолизом эритроцитов, а нарастание желтухи после 4 сут жизни с высокой вероятностью указывает на нарушение конъюгации билирубина в печени и его недостаточной экскреции (уровень доказательности B).
Дополнительную информацию о патологической природе желтухи может иметь появление на ее фоне лимонного (типично для ГБН), зеленоватого (типично для холестаза) или сероватого (типично для сепсиса) оттенка кожи.
Первоначально желтый цвет приобретает кожа лица и туловища ребенка. Дальнейшее нарастание концентрации билирубина, независимо от причины, приводит к распространению желтухи и окрашиванию кожи конечностей. Увеличение концентрации билирубина более 255-306 мкмоль/л сопровождается прокрашиванием ладоней и стоп (уровень доказательности C).
Комментарии. В 1969 г. доктор Л.И. Крамер (Kramer L.I.) предложил выделять пять степеней выраженности желтухи новорожденных (приложение 1), каждой из которых соответствует свой диапазон концентрации билирубина в сыворотке крови. В настоящее время эксперты РОН считают, что клиническая оценка степени выраженности желтухи на основе шкалы Крамера субъективна и требует подтверждения гипербилирубинемии инструментальными и лабораторными методами. Шкала Крамера может быть использована для определения необходимости забора крови на биохимический анализ билирубина у доношенных новорожденных в тех медицинских организациях, в которых отсутствуют аппараты для чрескожного определения билирубина (уровень доказательности D).
NB! Однократная оценка по Крамеру в большинстве случаев не позволяет дифференцировать физиологическую и патологическую гипербилирубинемию.
Однако описание во врачебных дневниках желтухи с указанием кожных зон, предложенных Крамером, помогает определить показания к биохимическому исследованию крови. Желтое окрашивание двух и трех зон не позволяет исключить или подтвердить гипербилирубинемию, распространение желтухи на четвертую и пятую кожные зоны практически всегда свидетельствует о наличии гипербилирубинемии, но не позволяет объективно оценивать вероятность развития БЭ. Таким образом, распространение желтухи на четвертую и пятую зоны по Крамеру у доношенного новорожденного должно рассматриваться как показание к биохимическому исследованию крови. Вместе с тем при ранней выписке новорожденных из акушерского стационара такой подход не позволяет прогнозировать нарастание желтухи после 3 сут. Кроме того, шкалу Крамера нельзя применять у недоношенных и новорожденных с дефицитом массы тела. Шкала Крамера не может быть использована для оценки эффективности ФТ (уровень доказательности D).
Все вышеизложенное подчеркивает существенное ограничение возможностей использования визуальной оценки степени желтухи для скрининга детей, составляющих группу риска по развитию БЭ (уровень доказательности A).
Чрескожное измерение концентрации билирубина
Более объективным методом оценки скорости и степени накопления билирубина в коже ребенка, чем визуальная оценка, является чрескожное измерение отраженного от кожи и подкожных тканей света с помощью специальных приборов (уровень доказательности В). В настоящее время с этой целью в РФ успешно используются приборы отечественного и зарубежного производства («Билитест», производство «Техномедика», Россия; билирубинометры JM-103, JM-105, производство Draeger Medical Systems, США; BiliCheck, производство Philips, Нидерланды и др.).
Общим для всех приборов является то, что только в диапазоне концентраций ОБ от 100 до 255 мкмоль/л отмечается прямая линейная зависимость между показателями содержания билирубина в коже и сыворотке крови у доношенных и недоношенных новорожденных ГВ более 35 нед. При концентрации билирубина более 255 мкмоль/л требуется перепроверка уровня билирубина стандартными лабораторными методами (уровень доказательности B).
Особенности и ограничения чрескожного измерения уровня билирубина, не зависящие от конструкции прибора:
-
исследование уровня билирубина чрескожным методом показано всем доношенным новорожденным с желтухой независимо от степени ее выраженности;
-
измерение уровня билирубина должно проводиться только в области лба и/или грудины. Для определения показаний к повторному измерению или срочному определению концентрации ОБ в крови стандартными лабораторными методами могут быть использованы процентильные кривые V.K. Bhutani;
-
данный метод измерения билирубина не может быть использован после начала ФТ (уровень доказательности B).
Вместе с тем, учитывая определенные различия в диагностических алгоритмах и конструктивные особенности, чрескожное измерение билирубина должно выполняться в строгом соответствии с инструкцией по эксплуатации конкретного прибора.
Процентильные кривые уровня билирубина крови, измеренного чрескожным методом у детей, родившихся на сроке беременности более 34 нед, предназначенные для определения степени риска развития патологической гипербилирубинемии, представлены в приложении B2.
При ранней выписке новорожденного из акушерского стационара целесообразно воспользоваться алгоритмом, представленным на рис. 1 (уровень доказательности D).
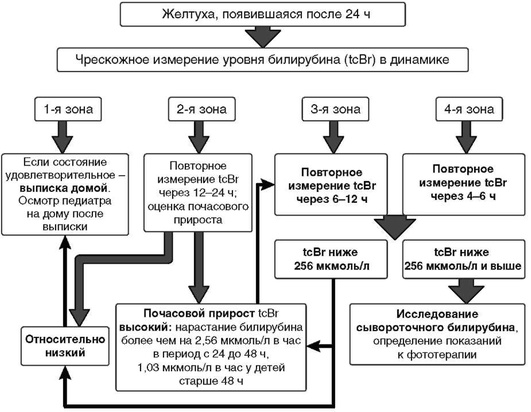
Рациональное использование приборов для чрескожного измерения билирубина у новорожденных в условиях акушерского стационара позволяет:
-
1) уменьшить неоправданно широкое использование забора крови на билирубин у доношенных новорожденных;
-
2) более объективно выделять среди клинически здоровых новорожденных группу риска по развитию непрямой патологической гипербилирубинемии;
-
3) предотвращать раннюю выписку домой новорожденных, у которых имеется потенциальный риск отсроченного развития БЭ (уровень доказательности B).
Особенности использования приборов для чрескожного измерения билирубина у недоношенных детей. Несмотря на попытки использования чрес-кожного измерения билирубина у глубоко недоношенных новорожденных, его прогностическая ценность у недоношенных детей, родившихся ранее 35-й нед беременности, требует дальнейшего изучения (уровень доказательности A).
Лабораторная диагностика
Методы измерения концентрации билирубина в крови у новорожденных
Своевременное измерение концентрации билирубина в крови у новорожденных имеет ключевое значение для определения медицинской тактики ведения при подозрении на патологическую желтуху. Несмотря на то что нейротоксическим действием обладает в основном непрямая фракция билирубина, лечебная стратегия на первой недели жизни, независимо от причины и характера развития желтухи, строится исходя из абсолютных значений ОБ в крови, а не его отдельных фракций.
Стандартное лабораторное исследование концентрации билирубина в крови показано (уровень доказательности A):
Клинико-лабораторные характеристики основных патологических причин непрямой гипербилирубинемии
Гипербилирубинемия, обусловленная избыточным гемолизом эритроцитов. Повышенное образование билирубина вследствие гемолиза эритроцитов может быть обусловлено иммунным конфликтом между эритроцитами матери и плода, наследственными нарушениями структуры или функции эритроцитов, гемоглобинопатиями, ятрогенными факторами (лекарственный гемолиз - высокие дозы Викасола♠ ), рядом инфекционных заболеваний (врожденные инфекции - цитомегалия, герпес, краснуха, токсоплазмоз, листериоз, сифилис; неонатальный сепсис).
Наиболее опасной с точки зрения развития БЭ причиной гипербилирубинемии является ГБН.
Клинико-лабораторная характеристика гемолитической болезни плода и новорожденного подробно описана в соответствующем протоколе
Лабораторные критерии ГЕН.
-
Концентрация билирубина в пуповинной крови (в момент рождения) - при легких формах по Rh и во всех случаях AB0-несовместимости не более 51 мкмоль/л; при тяжелых формах по Rh и редким факторам - существенно выше 51 мкмоль/л.
-
Концентрация гемоглобина в пуповинной крови в легких случаях - на нижней границе нормы, в тяжелых - существенно снижена.
-
Почасовой прирост билирубина в первые сутки жизни больше 5,1 мкмоль/л в час.
-
Максимальная концентрация ОБ на 3-4-е сутки в периферической или венозной крови у доношенных новорожденных; при отечной и желтушной формах она существенно выше 256 мкмоль/л.
-
ОБ крови повышается преимущественно за счет непрямой фракции.
-
Относительная доля прямой фракции (при условии отсутствия холестатических осложнений) составляет менее 20%.
-
Уменьшение количества эритроцитов и повышение количества ретикулоцитов в периферической и венозной крови в течение 1 нед жизни.
Для наследственных гемолитических желтух (дефицит глюкозо-6-фосфатдегидрогеназы, серповидноклеточная анемия, наследственный микросфероцитоз и др.) характерно отсроченное (после 24 ч жизни) появление признаков гемолиза, а также изменение формы и размеров эритроцитов при морфологическом исследовании мазка крови, нарушение их осмотической стойкости.
Несмотря на отличия в патогенезе, сходными клиническими и лабораторными признаками сопровождаются гипербилирубинемии, обусловленные полицитемией/повышенной вязкостью крови, а также повышенным экстравазальным образованием билирубина (при множественных и обширных экхимозах, больших кефалогематомах и др.).
Гипербилирубинемия, обусловленная нарушением конъюгации билирубина (конъюгационные желтухи)
Конъюгационные желтухи обусловлены преимущественным нарушением конъюгации билирубина в гепатоцитах [желтухи, связанные с исключительно грудным вскармливанием (при гипогалактии) и особенностями состава грудного молока (семейной транзиторной гипербилирубинемии Ариаса-Люцея-Дрискола) (при нормальном уровне лактации); желтухи, обусловленные диабетической фетопатией и врожденным гипотиреозом. Выраженные нарушения конъюгации билирубина отмечаются при ряде наследственных заболеваний: синдроме Криглера-Найяра I и II типа, синдроме Жильбера и др.].
Для конъюгационных желтух характерны следующие признаки.
-
-
концентрация ОБ в пуповинной крови (в момент рождения) - менее 51 мкмоль;
-
концентрация гемоглобина в пуповинной крови соответствует норме;
-
почасовой прирост билирубина в первые сутки жизни менее 6,8 мкмоль/л в час;
-
максимальная концентрация ОБ на 3-4-е сутки в периферической/ венозной крови у доношенных детей более 255 мкмоль/л;
-
Гипербилирубинемия, обусловленная повышением кишечной реабсорбции, чаще всего наблюдается при высокой кишечной непроходимости.
Клиническая картина зависит от причины кишечной непроходимости (атрезия двенадцатиперстной кишки, пилоростеноз, обструкция кишечника объемным образованием и т.п.), а также сопутствующих симптомов обезвоживания и гипогликемии.
Лабораторные критерии сходны с критериями конъюгационной желтухи.
Непрямая гипербилирубинемия смешанного генеза чаще всего является ранним клиническим проявлением врожденной или перинатальной инфекции. Клиническая картина и лабораторные признаки являются составной частью симптомокомплекса TORCHES или сепсиса.
Стандартный план обследования новорожденного с подозрением на патологическую желтуху
-
Физикальный осмотр (степень распространенности желтухи, размеры печени и селезенки, цвет стула и мочи).
-
Группа крови и резус-фактор, в случае подозрения на ГБН - проба Кумбса.
-
Клинический анализ крови (гемоглобин, ретикулоциты, особенности лейкоцитарной формулы крови и др.).
-
Биохимический анализ крови (билирубин и его фракции, другое - по показаниям).
ЛЕЧЕНИЕ
Консервативное лечение
Лечебные мероприятия, направленные на уменьшение концентрации непрямого билирубина в сыворотке крови
Общие принципы
-
Создание оптимальных условий для ранней неонатальной адаптации ребенка.
-
Все здоровые и условно здоровые новорожденные нуждаются в проведении раннего (начиная с первого часа жизни) и регулярного грудного вскармливания (уровень доказательности B). Необходимо рекомендовать матери кормить грудью [1] как минимум 8-12 раз в сутки без ночного перерыва в течение первых нескольких дней жизни. Увеличение частоты кормления грудью снижает вероятность последующей тяжелой гипербилирубинемии у новорожденных при грудном вскармливании (уровень доказательности D).
-
Дополнительное введение воды либо растворов декстрозы (Глюкозы♠ ) новорожденным, находящимся на грудном вскармливании, при отсутствии признаков дегидратации не показано, так как не предупреждает развитие гипербилирубинемии и не снижает уровень ОБ в сыворотке.
-
В качестве крайней меры может рассматриваться временное (1-3 дня) прекращение грудного вскармливания и переход на кормление адаптированной смесью, что может способствовать снижению уровня билирубина и/или повышению эффективности ФТ в случае желтухи, обусловленной составом грудного молока (уровень доказательности D). В случаях медицинских противопоказаний к раннему прикладыванию к груди или избыточной убыли первоначальной массы тела к 3-4-му дню жизни новорожденным необходимо организовать докорм адаптированной питательной смесью.
-
Поддержание оптимальной температуры тела, обеспечение достаточным количеством жидкости и питательных веществ, профилактика гипогликемии, гипоксемии и ацидоза.
Фототерапия
Основным методом лечения непрямой гипербилирубинемии является ФТ. При неэффективности ФТ и угрозе развития БЭ показано проведение ОЗПК (уровень доказательности A).
Виды фототерапии
-
Традиционная - использование одного источника света - люминесцентной лампы голубого света.
-
LED ФТ - использование светодиодов, обеспечивает меньшие потери жидкости организмом.
-
Фиброоптическая ФТ - использование одного источника света с волоконно-оптическим кабелем, через который световой луч проходит на гибкую светящуюся поверхность, на которую помещается ребенок или может быть ею обернут. Может быть использована у недоношенных новорожденных, не требует защиты глаз.
-
Комбинированная ФТ - осуществляется с помощью двух источников света и более (две единицы и более или сочетание ламп обычной и фиброоптической ФТ). Показана для лечения как доношенных, так и недоношенных новорожденных при наличии хотя бы одного признака:
Проведение ФТ в непрерывном режиме (в течение суток, допустимы лишь перерывы на кормление и манипуляции не более 30 мин) более предпочтительно (уровень доказательности A).
Техника фототерапии при использовании установок с традиционными и LED-источниками света
-
Обнаженный ребенок помещается в кувез или в кроватку с термоматрасом (выбор режима зависит от ГВ ребенка, особенностей терморегуляции, при этом температура тела ребенка должна быть в пределах 36,6-37,0 °С).
-
Глаза ребенка и половые органы мальчиков должны быть защищены светонепроницаемым материалом.
-
Источник ФТ располагается над ребенком на высоте 50-55 см; если ребенок находится в кувезе, то расстояние от верхней стенки кувеза до лампы ФТ должно быть 5 см.
-
ФТ с помощью установок, не предназначенных для домашнего использования, должна проводиться в палатах для новорожденных под контролем среднего медицинского персонала.
-
Каждые 1-2 ч ФТ необходимо менять положение ребенка по отношению к источнику света, переворачивая его поочередно вверх животом или спиной.
-
При отсутствии противопоказаний необходимо сохранять кормление материнским молоком в полном объеме.
-
Физиологическая потребность ребенка в жидкости увеличивается на 10-20%, при невозможности увеличения объема питания проводится инфузионная терапия.
-
В процессе ФТ нельзя ориентироваться на цвет кожного покрова и показатели приборов для чрескожного измерения билирубина.
-
Всем детям, получающим ФТ, необходимо ежедневно проводить биохимический анализ крови на билирубин (при угрозе БЭ - каждые 6-12 ч); только результаты стандартного биохимического анализа крови могут служить критерием эффективности ФТ.
-
ФТ может быть прекращена, если отсутствуют признаки патологического прироста билирубина, а концентрация ОБ в сыворотке крови стала ниже значений, послуживших основанием для начала ФТ.
-
Через 12 ч после окончания ФТ необходимо контрольное исследование уровня билирубина в крови.
-
У некоторых детей в ответ на ФТ может появиться аллергическая сыпь, участиться и измениться цвет стула, появиться бронзовый оттенок кожи, которые бесследно исчезают после прекращения ФТ.
Показания к фототерапии и операции заменного переливания крови у доношенных новорожденных и недоношенных детей гестационного возраста 35 нед и более при непрямой гипербилирубинемии, не связанной с гемолитической болезнью плода и новорожденного
В раннем неонатальном периоде основываются на определении пороговых значений ОБ в сыворотке крови в зависимости от постнаталь-ного возраста в часах и наличия или отсутствия факторов риска. При быстром нарастании уровня билирубина и при критической гипербилирубинемии ФТ необходимо проводить в непрерывном режиме (уровень доказательности B). Во всех случаях наличия у ребенка факторов риска, повышающих вероятность развития БЭ, ФТ необходимо начинать при минимальных значениях билирубина. Показания, разработанные Американской академией педиатрии в 2004 г., представлены в приложениях 3 и 4 (уровень доказательности D).
Комментарии. Важно отметить, что показания к ФТ и ОЗПК (Американская академия педиатрии, 2004), определяют тактику ведения только детей ГВ 35 нед и более и ограничены ранним неонатальном периодом. В связи с недостаточностью объективных данных об условиях, при которых БЭ может возникнуть у новорожденных после окончания первой недели жизни, большинство экспертов РОН предлагают расширить действие этих рекомендаций до конца неонатального периода. Вместе с тем у доношенных детей с наследственными нарушениями обмена (например, с синдромом Криглера- Найяра), нуждающихся в длительном проведении ФТ, показания к ОЗПК должны определяться консилиумом специалистов с учетом патогенеза заболевания и индивидуальной реакции ЦНС ребенка на хроническую непрямую гипербилирубинемию (мнение экспертов РОН, уровень доказательности D).
Показания к фототерапии и операции заменного переливания крови у недоношенных детей гестационного возраста менее 35 нед при непрямой гипербилирубинемии, не связанной с гемолитической болезнью плода и новорожденного
Эксперты РОН для определения показаний к ФТ и ОЗПК у недоношенных, с учетом ГВ и дополнительных факторов риска, рекомендуют использовать модифицированные рекомендации Американской академии педиатрии, представленные в приложениях 5 и 6.
Вместе с тем, учитывая высокий риск осложнений ОЗПК у глубоко недоношенных детей, окончательное решение о проведении операции у детей, родившихся ранее 32-й недели гестации, должен принимать консилиум врачей-специалистов (мнение экспертов РОН, уровень доказательности D).
Эффективность при непрямой гипербилирубинемии, не связанной с ГБН, должна оцениваться каждые 12 ч после ее начала путем измерения концентрации ОБ в сыворотке крови стандартными лабораторными методами. В случае неэффективности ФТ осуществляется подготовка и проведение ОЗПК (уровень доказательности A). Показания к операции, разработанные Американской академией педиатрии в 2004 г., представлены в приложении 6 (уровень доказательности A).
При снижении концентрации ОБ на фоне проводимой ФТ лечение продолжается до момента, когда при плановом биохимическом исследовании билирубина его концентрация оказывается на 25% ниже значений, явившихся показанием к началу ФТ. Через 12 ч после завершения ФТ должно быть проведено контрольное исследование билирубина; продолжение ФТ при концентрациях билирубина ниже указанных в приложениях 3 и 5 является необоснованным и потенциально опасным.
Оперативное лечение
При неэффективности ФТ основным методом оперативного лечения гипербилирубинемии, угрожающей развитием БЭ, является ОЗПК.
Правила подготовки и проведения операции
-
Обязательно получение от родителей информированного согласия на проведение ОЗПК.
-
Дети не должны получать ЭП в течение последних 3 ч до предполагаемого начала операции.
-
В желудок перед операцией должен быть введен постоянный зонд, через который необходимо периодически удалять содержимое желудка.
-
В течение всего процесса подготовки к ОЗПК, выполнения операции и последующего ведения ребенка необходим постоянный мониторинг витальных функций (ЧCC, частоты дыхания, сатурации, артериального давления, температуры тела).
-
Донорская кровь и/или ее компоненты при ОЗПК переливают из расчета 150-170 мл/кг массы тела для доношенного ребенка и 170-180 мл/кг для недоношенного (пример расчета объема замещения представлен в приложении 7).
-
Соотношение эритроцитарной массы/взвеси и СЗП составляет 2:1.
-
Согласно Приказу Минздрава России от 2 апреля 2013 г. № 183н «Об утверждении правил клинического использования донорской крови и/ или ее компонентов», при трансфузии (переливании) донорской крови и/или эритроцитсодержащих компонентов новорожденным:
-
переливают эритроцитсодержащие компоненты, обедненные лейкоцитами (эритроцитарная взвесь, эритроцитарная масса, отмытые эритроциты, размороженные и отмытые эритроциты);
-
при подборе компонентов донорской крови для трансфузии (переливания) учитывается, что мать является нежелательным донором СЗП для новорожденного, поскольку плазма матери может содержать аллоиммунные антитела против эритроцитов новорожденного, а отец является нежелательным донором эритроцитсодержащих компонентов, поскольку против антигенов отца в крови новорожденного могут быть антитела, проникшие из кровотока матери через плаценту;
-
наиболее предпочтительной является трансфузия негативного по цитомегаловирусу эритроцитсодержащего компонента;
-
для ОЗПК используются эритроцитсодержащие компоненты со сроком хранения не более 5 дней с момента заготовки компонента;
-
подбор компонентов донорской крови осуществляется в соответствии с группой крови и резус-фактором реципиента.
-
-
Манипуляцию выполняют в ПИТН/ОРИТН (в акушерских отделениях медицинской организации I уровня оказания перинатальной помощи - в процедурном кабинете).
-
До начала операции у новорожденных, которые находятся в тяжелом состоянии, стандартными методами интенсивной терапии должны быть устранены ацидоз, гипоксемия, гипогликемия, электролитные нарушения, гемодинамические расстройства, гипотермия и т.д.
-
ОЗПК проводит бригада, состоящая как минимум из двух человек: врача (неонатолога/анестезиолога-реаниматолога/педиатра) и детской медицинской сестры.
-
Обязательно строгое соблюдение правил асептики и антисептики.
Техника проведения операции заменного переливания крови
-
Следует уложить ребенка в заранее согретую открытую реанимационную систему с сервоконтролем.
-
Зафиксировать конечности ребенка путем надежного пеленания, кожа живота остается открытой.
-
При строгом соблюдении правил асептики и антисептики установить и зафиксировать пупочный катетер с присоединенным к нему заранее тройником.
-
При наличии противопоказаний к катетеризации пупочной вены ОЗПК проводят через любую другую центральную вену.
-
Компоненты донорской крови предварительно необходимо согреть до температуры 36-37 °С.
-
Первую порцию выводимой крови необходимо отобрать для биохимического исследования на уровень билирубина.
-
Далее последовательно проводят постепенное выведение крови ребенка и последующее восполнение выведенного объема.
-
Объем одного замещения (однократного выведения крови) и одного восполнения (однократного введения компонентов крови) зависит от массы тела ребенка, ГВ и тяжести состояния ребенка (у доношенных - 10-20 мл/кг, у недоношенных - 5-10 мл/кг под обязательным контролем показателей гемодинамики, дыхания и функций почек).
-
После каждых 100 мл замещающей среды (эритроцитарной массы и плазмы) вводят 1-2 мл 10% раствора кальция глюконата или 0,5 мл 10% раствора хлористого кальция, предварительно разведенных в 5 мл 5% декстрозы (Глюкозы♠ ) (только между шприцами с эритроцитарной массой!).
-
Перед окончанием операции осуществляется забор крови на билирубин.
-
В результате операции (с учетом крови, взятой на биохимическое исследование) суммарный объем вводимых компонентов донорской крови должен быть равен суммарному объему выведенной крови ребенка.
NB! О безусловной эффективности ОЗПК свидетельствует более чем двукратное снижение концентрации билирубина в сыворотке крови ребенка к концу операции.
Ведение ребенка в послеоперационном периоде
-
ЭП после ОЗПК начинают с осторожностью, малыми порциями (дробно), под контролем кишечной перистальтики, с постепенным расширением объема кормления при условии удовлетворительной переносимости кормления.
-
Удаление пупочного катетера сразу после операции не рекомендуется в связи с вероятностью повторного проведения ОЗПК.
-
Контроль за уровнем билирубина выполняется через 12 ч после ОЗПК, далее по показаниям, но не реже 1 раза в 24 ч до 7 сут жизни.
-
Контроль за гликемией - через 1 ч после ОЗПК, далее по показаниям. Согласно Приказу Минздрава России № 183н, после окончания трансфузии (переливания) донорской крови и/или ее компонентов донорский контейнер с оставшейся донорской кровью и/или ее компонентами (5 мл), а также пробирка с кровью реципиента, использованная для проведения проб на индивидуальную совместимость, подлежат обязательному сохранению в течение 48 ч при температуре 2-6 °С в холодильном оборудовании.
Возможные осложнения операции заменного переливания крови
В процессе ОЗПК и в раннем постоперационном периоде возможно развитие следующих осложнений (уровень доказательности С).
Неэффективные и потенциально опасные методы лечения, которые следует исключить из клинической практики
-
Инфузионная терапия имеет ограниченные показания при гипербилирубинемии, если нет других показаний, так как уровень токсического непрямого жирорастворимого билирубина не может быть снижен введением дополнительных водных растворов. Дополнительная инфузия водного раствора 5-10% декстрозы (Глюкозы♠ ) новорожденным с гипербилирубинемией показана только при развитии эксикоза на фоне интенсивной ФТ, парентеральное введение жидкости определяется другими показаниями (рвота, патологическая потеря жидкости и др.) (мнение экспертов РОН, уровень доказательности D).
-
Включение в программу инфузионной терапии СЗП и альбумина человека при гипербилирубинемии не рекомендуется и не оправдано с позиции доказательной медицины. Данные препараты должны применяться по строгим показаниям (уровень доказательности B).
-
Назначение фенобарбитала. Значимая индукция ферментов печени происходит не ранее 3 дней от момента его применения, чаще к концу первой недели жизни. Кроме того, при лечении желтухи фенобарбиталом возникают нежелательные эффекты в виде вялости, угнетения дыхания и снижения активности сосания. По этим причинам в течение последних 15-20 лет фенобарбитал для лечения гипербилирубинемии в мире не применяется (уровень доказательности A).
-
Нет убедительных научных доказательств и патогенетического обоснования для лечения непрямой гипербилирубинемии гепатопротективными и желчегонными препаратами [такими как фосфолипиды (Эссенциале Н ♠ ), каперсы колючей экстракт + кассии западной экстракт + паслена черного плодов экстракт + тамарикса двудомного плодов экстракт + терминалии чебулы плодов экстракт (Лив.52♠), артишока листьев экстракт (Хофитол♠) и др.].
Препараты урсодезоксихолевой кислоты показаны только при развитии синдрома холестаза (мнение экспертов РОН, уровень доказательности D).
ВЫПИСКА ИЗ СТАЦИОНАРА
Условия выписки из стационара доношенных новорожденных с непрямой гипербилирубинемией
Условия выписки доношенных новорожденных, получавших ФТ по поводу непрямой гипербилирубинемии, не связанной с ГБН:
-
концентрация билирубина в сыворотке крови менее той, которая требует лечения спустя 12 ч и более после окончания ФТ;
-
в случае ранней выписки необходимо ориентироваться на центильную кривую V.K. Bhutani и учитывать реальные возможности педиатрической службы региона обеспечить динамическое наблюдение за ребенком после выписки из стационара.
При выписке ребенка из отделения патологии новорожденных и недоношенных детей следует помнить, что непрямая гипербилирубинемия редко является единственным патологическим состоянием, определяющим длительность стационарного лечения. Сроки выписки ребенка зависят от результатов лечения основного и сопутствующих заболеваний.
Особенности наблюдения на амбулаторном этапе за новорожденным с гипербилирубинемией
Наиболее опасным периодом с точки зрения риска развития БЭ являются первые 7 дней жизни (уровень доказательности B), следовательно, тактика наблюдения и лечения ребенка не отличается от таковой в условиях стационара. У детей старше 7 дней жизни риск БЭ уменьшается, однако недостаточно объективных данных для изменения показаний к лечению в позднем неонатальном периоде (мнение экспертов РОН, уровень доказательности D).
Во всех случаях патологической желтухи, генез которой не уточнен, необходимо проведение дополнительного обследования.
Таким образом, поводом для госпитализации ребенка в отделение патологии новорожденных и недоношенных детей перинатального центра или детской больницы являются как необходимость дополнительного обследования, которое трудно организовать в условиях детской поликлиники, так и необходимость лечения патологической гипербилирубинемии.
СПИСОК ЛИТЕРАТУРЫ
-
Таболин В.А. Билирубиновый обмен у новорожденных. М.: Медицина,1967.
-
Савельева Г.М., Коноплянников А.Г., Курцер М.А., Панина О.Б. Гемолитическая болезнь плода и новорожденного. М.: ГЭОТАР-Медиа, 2011.
-
Шабалов Н.П. Неонатология: учебное пособие: в 2 т. 5-е изд. М.: ГЭО-ТАР-Медиа, 2016.
-
Неонатология: национальное руководство. Краткая версия / под ред. Н.Н Володина. М.: ГЭОТАР-Медиа, 2013.
-
Сидельникова В.М., Антонов А.Г. Гемолитическая болезнь плода и новорожденного. М.: Триада-Х, 2004.
-
Практическое руководство по неонатологии / под ред. Г.В. Яцык. М.: Медицинское информационное агентство, 2008.
-
Дегтярева А.В., Дегтярев Д.Н. Современные принципы диагностики и лечения негемолитической гипербилирубинемии у доношенных и поздних недоношенных детей в раннем неонатальном периоде // Неонатология: новости, мнения, обучение. 2014. № 3 (5). С. 67-76.
-
Gomella T.L., Cunningham M.D. Neonatology: Management, Procedures, On Call Problems, Diseases, and Drugs. 7th ed. McGraw-Hill, 2013.
-
Bhutani V.K., Johnson L., Sivieri E.M. Predictive ability of a predischarge hour-specific serum bilirubin for subsequent significant hyperbilirubinemia in healthy-term and near-term newborns // Pediatrics. 1999. Vol. 103, N 1. P. 6-14.
-
Keren R., Tremont K., Luan X. et al. Visual assessment ofjaundice in term and late preterm infants // Arch. Dis. Child. Fetal Neonatal Ed. 2009. Vol. 94, N 5. F317-F322.
-
Volpe J.J. Bilirubin and brain injury // Neurology of the Newborn. 5th ed. Philadelphia, PA: W.B. Saunders, 2008. P. 619.
-
Wennberg R.P., Ahlfors C.E., Bhutani V. et al. Toward understanding ker-nicterus: a challenge to improve the management ofjaundiced newborns // Pediatrics. 2006. Vol. 117, N 2. P. 474-485.
-
Bellarosa C., Muchova L., Vitek L. et al. Bilirubin metabolism and transport // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko J.F. New York: McGraw-Hill, 2012. P. 55.
-
Hansen T.W.R., Bratlid D. Physiology of neonatal unconjugated hyperbilirubinemia // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko J.F. New York: McGraw-Hill, 2012. P. 65.
-
Kaplan M., Muraca M., Hammerman C. et al. Imbalance between production and conjugation of bilirubin: a fundamental concept in the mechanism of neonatal jaundice // Pediatrics. 2002. Vol. 110, N 4. P. e47.
-
Bhutani V.K., Stark A.R., Lazzeroni L.C. et al. Predischarge screening for severe neonatal hyperbilirubinemia identifies infants who need phototherapy // J. Pediatr. 1999. Vol. 162, N 3. P. 477-482.
-
Maisels M.J., Newman Т.В. The epidemiology of neonatal hyperbilirubinemia // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko J.F. New York: McGraw-Hill, 2012. P. 97.
-
Watchko J.F., Lin Z. Genetics of neonatal jaundice // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko J.F. New York:McGraw-Hill, 2012. P. 1.
-
Newman Т.В., Liljestrand P., Escobar G.J. Jaundice noted in the first 24 hours after birth in a managed care organization // Arch. Pediatr. Adolesc. Med. 2002. Vol. 156, N 12. P. 1244-1250.
-
Maisels M.J., DeRidder J.M., Kring E.A. et al. Routine transcutaneous bili-rubin measurements combined with clinical risk factors improve the prediction of subsequent hyperbilirubinemia // J. Perinatol. 2009. Vol. 29, N 9. P. 612-617.
-
Keren R., Luan X., Friedman S. et al. A comparison of alternative risk-assessment strategies for predicting significant neonatal hyperbilirubinemia in term and near-term infants // Pediatrics. 2008. Vol. 121, N 1. P. e170-179.
-
Bertini G., Dani C., Trochin M. et al. Is breastfeeding really favoring early neonatal jaundice? // Pediatrics. 2001. Vol. 107, N 3. P. E41.
-
Garcia F.J., Nager A.L. Jaundice as an early diagnostic sign of urinary tract infection in infancy // Pediatrics. 2002. Vol. 109. P. 846-851.
-
Maisels M.J., Newman Т.В. Neonatal jaundice and urinary tract infections // Pediatrics. 2003. Vol. 112. P. 1213-1214.
-
Bender G.J., Cashore W.J., Oh W. Ontogeny of bilirubin-binding capacity and the effect of clinical status in premature infants born at less than 1300 grams //Pediatrics. 2007. Vol. 120. P. 1067-1073.
-
Ross M.E., Waldron P.E., Cashore W.J. et al. Hemolytic disease of the fetus and newborn // Neonatal Hematology, Pathogenesis, Diagnosis, and Management of Hematologic Problems. 2nd ed. / eds P.A. de Alarcon, E.J. Werner, R.D. Chris-tensen. Cambridge, UK: Cambridge University Press, 2013. P. 65.
-
Maisels M.J., Newman Т.В. Bilirubin and neurological dysfunction - do we need to change what we are doing? // Pediatr. Res. 2001. Vol. 50, N 6. P. 677.
-
Heimler R., Sasidharan P. Neurodevelopmental and audiological outcome of healthy term newborns with moderately severe non-haemolytic hyperbilirubinemia // J. Paediatr. Child Health. 2010. Vol. 46. P. 588-591.
-
Watchko J.F., Tiribelli C. Bilirubin-induced neurologic damage - mechanisms and management approaches // N. Engl. J. Med. 2013. Vol. 369, N 21.P. 2021-2030.
-
Okumura A., Kidokoro H., Shoji H. et al. Kernicterus in preterm infants //Pediatrics. 2009. Vol. 123. P. e1052-e1058.
-
Huang M.-J., Kua K.-E., Teng H.-C. et al. Risk factors for severe hyperbilirubinemia in neonates // Pediatr. Res. 2004. Vol. 56. P. 682-689.
-
Watchko J.F., Maisels M.J. Jaundice in low birth weight infants - pathobiology and outcome // Arch. Dis. Child. Fetal Neonatal Ed. 2003. Vol. 88.P. F455-F458.
-
Morris B.H., Oh W., Tyson J.E. et al. Aggressive vs. conservative phototherapy for infants with extremely low birth weight // N. Engl. J. Med. 2008. Vol. 359.P. 1885-1896.
-
Wagle S., Deshpande P.G., Itani O., Windle M.L. et al. Hemolytic Disease of Newborn. Updated: Sep 26. 2014. URL: http://emedicine.medscape.com/ar-ticle/974349.
-
Amin S.B., Charafeddine L., Guillet R. Transient bilirubin encephalopathy and apnea of prematurity in 28 to 32 weeks gestational age infants // J. Perinatol.2005. Vol. 25. P. 386-390.
-
Shapiro S.M. Kernicterus // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko. New York: McGraw-Hill, 2012. P. 229-242.
-
Shapiro S.M. Chronic bilirubin encephalopathy: diagnosis and outcome // Semin. Fetal Neonatal Med. 2010. Vol. 15. P. 157-163.
-
Ip S., Glicken S., Kulig J. et al. Management of Neonatal Hyperbilirubinemia. Rockville, MD: U.S. Department of Health and Human Services, Agency for Healthcare Research and Quality. AHRQ Publication, 2003.
-
Maisels M.J., Clune S., Coleman K. et al. The natural history ofjaundice in predominantly breast-fed infants // Pediatrics. 2014. Vol. 134, N 2. P. E340-e345.doi: 10.1542/peds.2013-4299.
-
Davis A.R., Rosenthal P., Escobar G. et al. Interpreting conjugated bilirubin levels in newborns // J. Pediatr. 2011. Vol. 158. P. 562-565.
-
Maisels M.J., Baltz R.D., Bhutani V. et al. Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation // Pediatrics. 2004. Vol.114. P. 297-316.
-
Kramer L.I. Advancement of dermal icterus in the jaundiced newborn // Am. J. Dis. Child. 1969. Vol. 118. P. 454-458.
-
Maisels M.J., Bhutani V.K., Bogen D. et al. Hyperbilirubinemia in the newborn infant >35 weeks' gestation: an update with clarifications // Pediatrics. 2009. Vol. 124, N 4. P. 1193-1198.
-
Jaundice in Newborn Babies under 28 Days. Neonatal Jaundice. National Institute for Health and Clinical Excellence, 2010.
-
Bhutani V.K., Stark A.R. et al. Predischarge Screening for Severe Neonatal Hyperbilirubinemia Identifies Infants Who Need Phototherapy. Department of Neonatal and Developmental Medicine, Lucile Packard Children’s Hospital, Department of Pediatrics, Stanford University. Stanford, 2012.
-
DeLuca D., Engle W., Jackson G. Transcutaneous bilirubinometry: hepatol-ogy research and clinical developments. New York: Nova Biomedical, 2013.
-
Schumacher R. Transcutaneous bilirrubinometry and diagnostic tests: «The right job for the tool» // Pediatrics. 2002. Vol. 110. P. 407-408.
-
Maisels M.J., Newman Т.В. Prevention, screening, and postnatal management of neonatal hyperbilirubinemia // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko. New York: McGraw-Hill, 2012. P. 175.
-
Wainer S., Rabi Y., Parmar S.M. et al. Impact of skin tone on the performance of a transcutaneous jaundice meter // Acta Paediatr. 2009. Vol. 98. P. 1909.
-
Nagar G., Vandermeer B., Campbell S. et al. Reliability of transcutaneous bilirubin devices in preterm infants: a systematic review // Pediatrics. 2013. Vol.132. P. 871-881.
-
De Luca D., Jackson G.L., Tridente A. et al. Trans cutaneous bilirubin nomograms: a systematic review of population differences and analysis of bilirubin kinetics // Arch. Pediatr. Adolesc. Med. 2009. Vol. 163, N 11. P. 1054-1059.
-
Poland R.L., Hartenberger C., McHenry H. et al. Comparison of skin sites for estimating serum total bilirubin in in-patients and out-patients: chest is superior to brow // J. Perinatol. 2004. Vol. 24. P. 541.
-
Yaser A., Tooke L., Rhoda N. Interscapular site for transcutaneous bilirubin measurement in preterm infants: a better and safer screening site // J. Perinatol.2014. Vol. 34. P. 209.
-
Maisels M.J., Kring E. Transcutaneous bilirubin levels in the first 96 hours in a normal newborn population of 35 or more weeks' of gestation // Pediatrics.2006. Vol. 117. P. 1169.
-
Tan K.L., Dong F. Transcutaneous bilirubinometry during and after phototherapy // Acta Paediatr. 2003. Vol. 92. P. 327.
-
Brumbaugh J.E., Gourley G.R. Bilirubin and its various fractions // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko. NewYork: McGraw-Hill, 2012. P. 41.
-
Glader B., Allen G.A. Neonatal hemolysis // Neonatal Hematology, Pathogenesis, Diagnosis, and Management of Hematologic Problems. 2nd ed. / eds P.A. de Alarcon, E.J. Werner, R.D. Christensen. Cambridge, UK: Cambridge University Press, 2013. P. 91.
-
Stevenson D.K., Fanaroff A.A., Maisels M.J. et al. Prediction of hyperbili-rubinemia in near-term and term infants // Pediatrics. 2001. Vol. 108. P. 31-39.
-
Mehta S., Kumar P., Narang A. A randomized controlled trial of fluid supplementation in term neonates with severe hyperbilirubinemia // J. Pediatr. 2005.Vol. 147. P. 781-785.
-
Boo N.Y., Lee H-T. Randomized controlled trial of oral versus intravenous fluid supplementation on serum bilirubin level during phototherapy of term infants with severe hyperbilirubinemia // J. Paediatr. Child Health. 2002. Vol. 38.P. 151-155.
-
Maisels M.J., McDonagh A.F. Phototherapy for neonatal jaundice // N.Engl. J. Med. 2008. Vol. 358. P. 920-928.
-
Maisels M.J., Newman Т.В. Phototherapy and other treatments // Care of the Jaundiced Neonate / eds D.K. Stevenson, M.J. Maisels, J.F. Watchko. NewYork: McGraw-Hill, 2012. P. 195.
-
Newman Т.В., Liljestrand P., Jeremy R.J. et al. Outcomes among newborns with total serum bilirubin levels of 25 mg per deciliter or more // N. Engl. J. Med.2006. Vol. 354. P. 1889-1900.
-
Bhutani V.K. Committee on Fetus and Newborn. Technical report: phototherapy to prevent severe neonatal hyperbilirubinemia in the newborn infant 35 or more weeks of gestation // Pediatrics. 2011. Vol. 128. P. e1046.
-
Maisels M.J., Kring E.A., DeRidder J. Randomized controlled trial of light-emitting diode phototherapy // J. Perinatol. 2007. Vol. 27. P. 565-567.
-
Maisels M.J., Watchko J.F., Bhutani V.K. et al. An approach to the management of hyperbilirubinemia in the preterm infant less than 35 weeks of gestation //J. Perinatol. 2012. Vol. 32. P. 660.
-
Clinical Practice Guideline. Management of hyperbilirubinemia in the newborn infant >35 weeks of gestation // Pediatrics. 2004. Vol. 114. P. 297-316.
-
Ip S., Chung M., Kulig J. et al. An evidence-based review of important issues concerning neonatal hyperbilirubinemia // Pediatrics. 2004. Vol. 114.P. e130-e153.
-
Barrington K.J., Sankaran K. Canadian Paediatric Society Fetus and Newborn Committee. Guidelines for the detection, management and prevention of hyperbilirubinemia in term and late preterm newborn infants // Paediatr. Child Health. 2007. Vol. 12, suppl. B. P. 1B-12B.
ПРИЛОЖЕНИЯ
Приложение 1. Клиническая оценка распространенности желтухи у новорожденных по Крамеру (Kramer L.I., 1969)
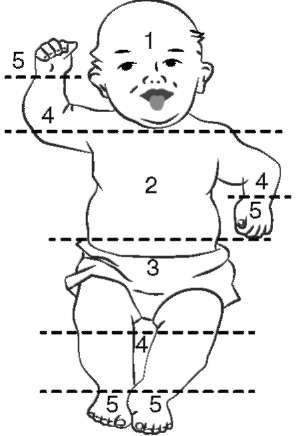
| Зоны по Крамеру | Предполагаемый уровень билирубина, мкмоль/л |
|---|---|
1-я |
31,5-136 |
2-я |
93,5-204 |
3-я |
136-280 |
4-я |
187-306 |
5-я |
>255 |
Приложение 2. Процентильные кривые уровня билирубина в крови, измеренного чрескожным методом у доношенных и недоношенных детей гестационного возраста 35-37 нед (Bhutani V.K. et al., 1999)
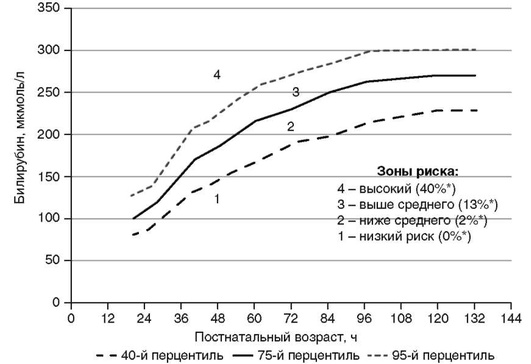
* Вероятность отсроченного развития клинически значимой гипербилирубинемии.
Приложение 3. Показания к фототерапии у доношенных и недоношенных детей гестационного возраста 35 нед и более в раннем неонатальном периоде
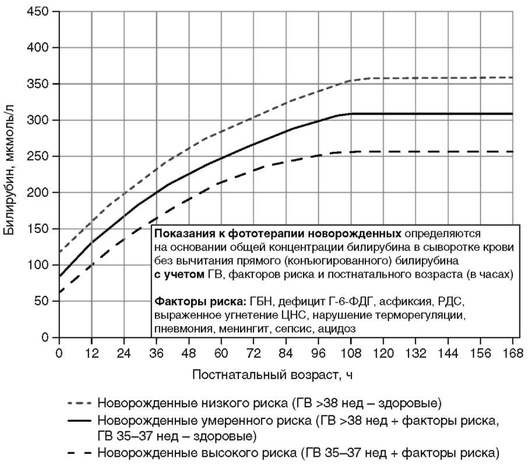
Приложение 4. Показания к операции обменного переливания крови у доношенных и недоношенных детей гестационного возраста 35 нед и более в раннем неонатальном периоде
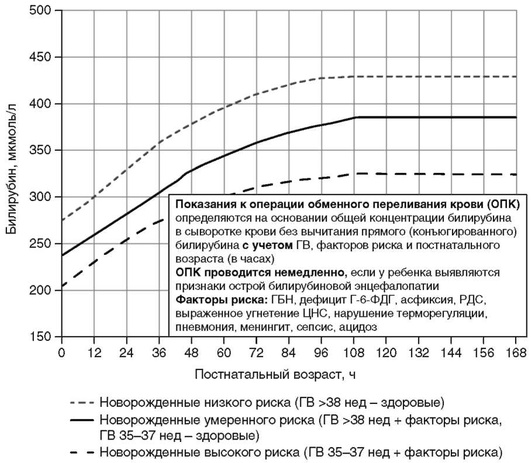
Приложение 5. Показания к фототерапии в раннем неонатальном периоде у недоношенных детей разного гестационного возраста
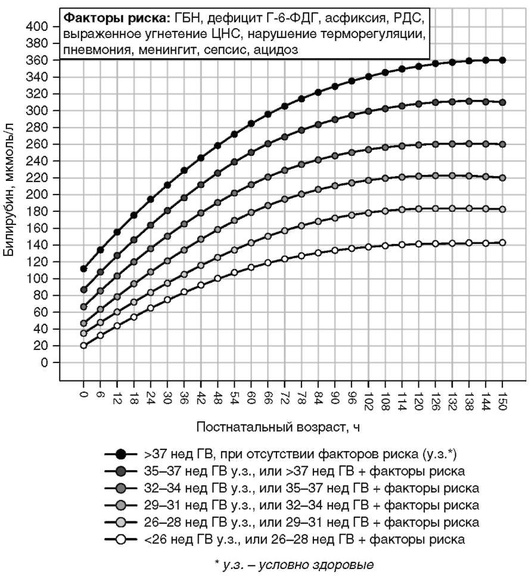
Приложение 6. Показания к операции обменного переливания крови в раннем неонатальном периоде у недоношенных детей разного гестационного возраста
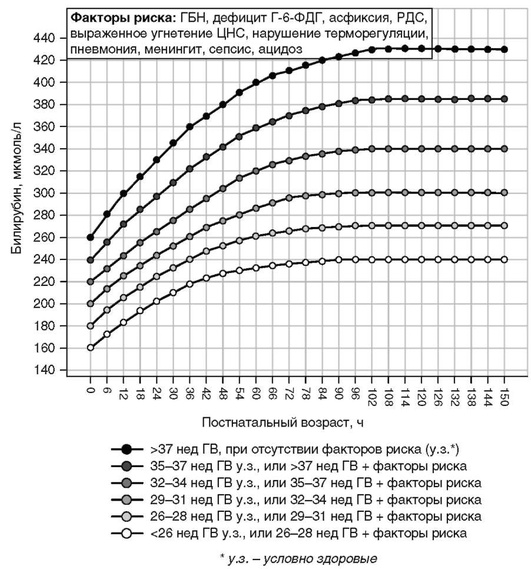
Приложение 7. Пример расчета объема компонентов крови для операции заменного переливания крови
-
Масса тела ребенка - 3000 г = 3 кг [2].
Приложение 8. Операция заменного переливания крови/частичной обменной трансфузии [3]
Ф.И.О. ребенка ______ Дата рождения «______» ______ 20 ____ г. № истории_
Дата выполнения процедуры «______» ______ 20 ___ г. Врач ______ М/с ______
Показания к проведению ОЗПК/ЧОТ ______ .
Порядок проведения ОЗПК/ЧОТ.
-
В ___ ч ___ мин после проверки группы крови и резус-фактора больного и донора двумя сериями стандартных сывороток, после проведения пробы на совместимость крови донора и больного по группе АВ0 и резус-фактору, после проведения биологической пробы сделан вывод о том, что кровь совместима.
-
Способ введения и выведения сред: внутривенно дробно медленно путем выведения ___ мл крови ребенка и выведения ___ мл эритроцитарной массы/СЗП/физиологического раствора.
-
ОЗПК/ЧОТ начато «_» ___ 20 ___ г. в ___ ч ___ мин, закончено «_» ___ 20 ___ г. в ___ ч ___ мин.
-
-
Эритроцитарной массы ___ ( ), Rh( ) ___ в количестве ___ мл.
-
Эритроцитарной массы ___ ( ), Rh( ) ___ в количестве ___ мл.
-
Номер флакона ___ дата изготовления « ___ » ___ 20 ___ г. Донор ___ .
-
Свежезамороженная плазма ___ ( ), Rh( ) ___ в количестве ___ мл.
-
Номер флакона ___ дата изготовления « ___ » ___ 20 ___ г. Донор ___ .
-
-
Патологических реакций во время ОЗПК/ЧОТ не отмечено/отмечено ___ .
Подпись врача, проводившего ОЗПК/ЧОТ ___ .
Подпись ассистента (врач, медицинская сестра) ___ .