Внутренние болезни : учебник : в 2 т. / под ред. А. И. Мартынова, Ж. Д. Кобалава, С. В. Моисеева. - 4-е изд., перераб. - Москва : ГЭОТАР-Медиа, 2021. - Т. I. - 784 с. : ил. - DOI: 10.33029/9704-5886-0-VNB-2021-1-784. - ISBN 978-5-9704-5886-0. |
Аннотация
Четвертое издание учебника, подготовленное авторским коллективом ведущих отечественных специалистов различных отраслей внутренней медицины под руководством академика А.И. Мартынова, содержит актуальную информацию об основных терапевтических заболеваниях. В книге приведены современные данные по этиологии, патогенезу, диагностике, лечению и профилактике болезней внутренних органов. Традиционное изложение материала построено с учетом действующих рекомендаций профессиональных врачебных сообществ и последних научных достижений.
Учебник написан в соответствии с требованиями учебной программы дисциплин "Факультетская терапия" и "Госпитальная терапия" и предназначен студентам старших курсов медицинских вузов, обучающимся по специальностям "Лечебное дело", "Педиатрия", "Медико-профилактическое дело", "Медицинская биофизика", "Медицинская биохимия", а также клиническим ординаторам, обучающимся по специальности "Терапия".
Глава 20. Дыхательная недостаточность
Дыхательная недостаточность (ДН) - неспособность системы дыхания обеспечить нормальный газовый состав артериальной крови. Более практично следующее определение.
ДН - патологический синдром, при котором парциальное напряжение кислорода в артериальной крови (РаО2) меньше 60 мм рт.ст. и/или РаСО2 больше 45 мм рт.ст.
Следует отметить, что напряжение газов крови для конкретного индивидуума может зависеть от разных факторов, таких как барометрическое давление, фракция кислорода во вдыхаемом воздухе, положение и возраст пациента и др. Зависимость РаО2 от возраста выражается уравнением:
РаО2 =104 - 0,27× возраст, лет.
Классификация
Существует несколько типов классификаций ДН:
Патогенетическая классификация. Различают две большие категории ДН: гипоксемическую (паренхиматозную, легочную или ДН I типа) и гиперкапническую (вентиляционную, «насосную» или ДН II типа) (рис. 20.1).
Гипоксемическая ДН характеризуется гипоксемией, трудно корригируемой кислородотерапией. Обычно эта форма ДН возникает на фоне таких тяжелых паренхиматозных заболеваний легких, как пневмония, ОРДС, отек легких, диффузные интерстициальные заболевания (альвеолиты).
Основные механизмы гипоксемии:
Кардинальным признаком вентиляционной ДН служит гиперкапния; гипоксемия также присутствует, но она обычно хорошо поддается терапии кислородом. Вентиляционная ДН может развиваться вследствие нарушений функции «дыхательной помпы» и дыхательного центра. К заболеваниям, которые могут быть ассоциированы с гиперкапнической ДН, относят нарушения центральной регуляции дыхания, нейромышечные заболевания, болезни грудной клетки и плевры и обструктивные заболевания дыхательных путей (ХОБЛ и др.).
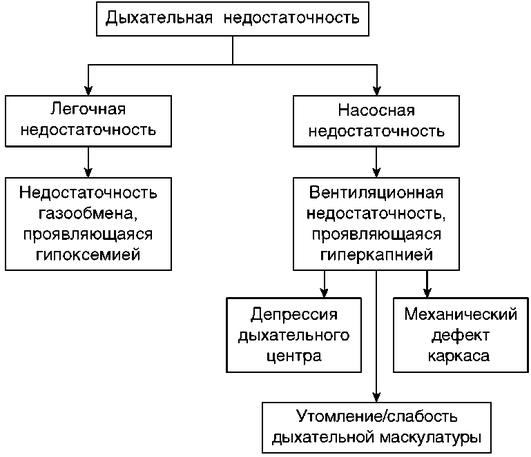
Основные механизмы гиперкапнии:
По скорости развития различают острую и хроническую ДН. Острая дыхательная недостаточность (ОДН) развивается в течение нескольких дней, часов или даже минут и требует проведения интенсивной терапии, так как может представлять непосредственную угрозу для жизни больного. При быстром развитии ДН не успевают включиться компенсаторные механизмы со стороны систем дыхания, кровообращения, кислотно-основного состояния (КОС) крови. Характерный признак ОДН - нарушение КОС крови - респираторный ацидоз при вентиляционной ДН (pH <7,35) и респираторный алкалоз при паренхиматозной ДН (pH >7,45). ОДН практически всегда сопровождается нарушениями гемодинамики.
Хроническая дыхательная недостаточность (ХДН) развивается в течение месяцев-лет. Начало ХДН может быть незаметным, постепенным, исподволь или она может развивается при неполном восстановлении после ОДН.
Длительное существование XДH позволяет включиться компенсаторным механизмам - полицитемия, повышение сердечного выброса, нормализация респираторного ацидоза за счет задержки почками бикарбонатов.
ОДH может развиваться и у пациентов с уже существующей XДH - «ОДH на фоне XДH». Синонимами этой формы ДH являются «обострение XДH» или «декомпенсация XДH».
Классификация ДН по степени тяжести основана на газометрических показателях (табл. 20.1). Эта классификация универсальна и имеет большое практическое значение; так, например, степень II предполагает обязательное назначение кислородотерапии, а степень III - чаще всего респираторной поддержки.
| Степень | РаО2, мм рт.ст. | SpО2,% |
|---|---|---|
Норма |
>80 |
>95 |
I |
60-79 |
90-94 |
II |
40-59 |
75-89 |
III |
<40 |
<75 |
Классификация ДН по анатомическому принципу. Кроме заболеваний легких, к развитию ДH может приводить и множество внелегочных заболеваний. ДH может развиться при поражении любого отдела или звена системы внешнего дыхания. Условно среди причин ДH принято выделять поражение ЦHС и дыхательного центра, нейромышечные заболевания, болезни грудной клетки, болезни дыхательных путей и альвеол (табл. 20.2).
| Поражение звена аппарата дыхания | Пример дыхательной недостаточности |
|---|---|
ЦНС и дыхательный центр |
Передозировка наркотических средств; гипотиреоз, центральное апноэ; нарушение мозгового кровообращения |
Нейромышечная система |
Синдром Гийена-Барре; ботулизм; миастения; болезнь Дюшенна; слабость и утомление дыхательных мышц |
Грудная клетка |
Кифосколиоз; ожирение; состояние после торакопластики; пневмоторакс; плевральный выпот |
Дыхательные пути |
Ларингоспазм; отек гортани; БА; ХОБЛ; муковисцидоз; облитерирующий бронхиолит |
Альвеолы |
Пневмония; ОРДС; отек легких; альвеолиты; легочные фиброзы; саркоидоз |
Клинические проявления
Клинические проявления ДH зависят от ее этиологии и типа, тяжести. Hаиболее универсальные симптомы ДH - диспноэ, признаки и симптомы гипоксемии, гиперкапнии, дисфункции дыхательной мускулатуры.
Один из наиболее универсальных симптомов ДH - диспноэ или одышка, т.е. некомфортное или неприятное ощущение собственного дыхания. Диспноэ при ДН чаще всего определяется больным как «ощущения дыхательного усилия» и очень тесно связано с активностью инспираторных мышц и дыхательного центра. Гипоксемия и гиперкапния также вносят важный вклад в развитие диспноэ, однако корреляция между РаО2, РаСО2 и диспноэ довольно слабая, поэтому классификации ДН не могут быть основаны на градациях диспноэ. У пациентов с вентиляционной ДН респираторная поддержка служит наиболее эффективным методом коррекции диспноэ, и если одышка не уменьшается, то следует исключить другие ее возможные причины, например ТЭЛА, пневмоторакс и др.
Клинические проявления гипоксемии (РаО2 ≤60 мм рт.ст.) трудно отграничить от других проявлений ДН (например, гиперкапнии). Наиболее чувствительный орган-мишень для гипоксемии - головной мозг, поражение которого наступает раньше других органов. При снижении РаО2 до 55 мм рт.ст. у нормального индивидуума нарушается память на текущие события, а при уменьшении РаО2 до 30 мм рт.ст. происходит потеря сознания. У пациентов с сосудистыми поражениями головного мозга клинические симптомы могут появляться и при менее выраженном снижении РаО2.
Важным клиническим признаком гипоксемии служит цианоз. Цианоз отражает тяжесть гипоксемии, независимо от ее причины и появляется при повышении концентрации восстановленного гемоглобина в капиллярной крови более 5 г/дл, т.е. обычно при РаО2 <60 мм рт.ст. и SpО2 <90%. Для ДН характерен центральный цианоз, при котором артериальная кровь, покидающая ЛЖ, остается недостаточно оксигенированной. Характерные гемодинамические эффекты гипоксемии - тахикардия и умеренная артериальная гипотония. Маркерами хронической гипоксемии служат вторичная полицитемия и легочная гипертония. Длительно существующая легочная гипертония приводит к развитию легочного сердца и застойной СН.
Основные эффекты гипоксемии
Клинические эффекты гиперкапнии (РаСО2 ≥45 мм рт.ст.) могут быть результатом как повышенного ответа со стороны СНС, так и прямого действия избытка СО2 на ткани. Основные проявления повышения РаСО2 - гемодинамические эффекты (тахикардия, повышение сердечного выброса, системная вазодилатация - у больных с гиперкапнией, как правило, теплые конечности) и эффекты со стороны ЦНС (хлопающий тремор, бессонница, частые пробуждения ночью и сонливость в дневное время, утренние головные боли, тошнота). При быстром повышении РаСО2 возможно развитие гиперкапнической комы, что связано с повышением мозгового кровотока, внутричерепного давления и развитием отека мозга. Как правило, гиперкапническая кома сопровождается отеком сосков дисков зрительных нервов. Толерантность к хронической гиперкапнии при условии адекватной оксигенации может быть значительной, некоторые больные адаптированы к РаСО2 до 90-140 мм рт.ст.
Основные эффекты гиперкапнии
К физическим признакам, характеризующим дисфункцию (утомление и слабость) дыхательной мускулатуры, относятся тахипноэ и изменение дыхательного паттерна (стереотипа). Тахипноэ - частый признак легочных заболеваний и ССЗ, повышение ЧДД >25/мин может быть признаком начинающегося утомления дыхательных мышц. Брадипноэ (ЧДД <12/мин) - более серьезный прогностический признак, чем тахипноэ. Постепенная смена частого дыхания редким может быть предвестником остановки дыхания. «Новый» паттерн дыхания характеризуется вовлечением дополнительных групп дыхательных мышц, и, возможно, отражает попытку дыхательного центра выработать оптимальную стратегию во время стрессовых условий. Могут вовлекаться мышцы верхних дыхательных путей в виде активных раздуваний крыльев носа. При осмотре и пальпации надключичных областей может быть обнаружено синхронное с дыханием напряжение лестничных мышц. При быстро развившейся тяжелой бронхиальной обструкции происходит активное вовлечение в процесс дыхания грудино-ключично-сосцевидных мышц (рис. 20.2). При пальпации также можно обнаружить активное сокращение брюшных мышц во время выдоха. Данный признак присутствует при тяжелом ограничении воздушного потока и легочной гиперинфляции (ЛГИ).
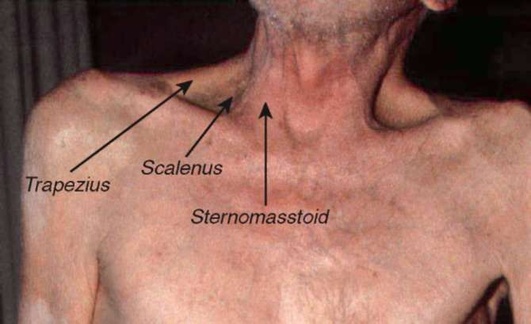
При высокой нагрузке на аппарат дыхания теряется мягкая и синхронная инспираторная экскурсия кнаружи груди и живота, что приводит к так называемой торако-абдоминальной асинхронии. В крайних случаях утомления и слабости дыхательных мышц может выявляться явное парадоксальное дыхание: во время вдоха живот втягивается внутрь, а грудная клетка движется кнаружи.
Работа дыхания при ОДН может увеличиться в 10-20 раз. К сожалению, клинически очень трудно аккуратно оценить «избыточную» работу дыхания. Ориентировочными признаками избыточной работы дыхания служат такие симптомы, как тахикардия, потливость, парадоксальный пульс, ЧДД выше 30-35/мин, использование в акте дыхания вспомогательной мускулатуры.
Диагностика
Основным инструментальным методом оценки ДН служит анализ газов артериальной крови. Современные газоанализаторы непосредственно измеряют PaО2, PaCО2 и pH, содержание общего количества гемоглобина (tHb), насыщение оксигемоглобина кислородом (О2 Hb), насыщение других форм гемоглобина, таких как карбоксигемоглобин (CОHb) и метгемоглобин (MetHb). Все остальные показатели обычно расчетные (например, уровень бикарбонатов плазмы и избыток/дефицит оснований). Нормальные значения параметров газов артериальной крови представлены в табл. 20.3.
| Параметры | Нормальные значения |
|---|---|
pH |
7,35-7,45 |
PaCО2, мм рт.ст. |
35-45 |
PaО2, мм рт.ст.[28] |
70-100 |
SpО2, % |
93-98 |
HCО3-, мэкв/л |
22-26 |
%MetHb, % |
<2,0 |
%CОHb, % |
<3,0 |
Избыток оснований (ВЕ), мэкв/л |
-2,0-2,0 |
CaО2, О2 /дл |
16-22 мл |
Примечания: PaО2 - парциальное давление кислорода в артериальной крови, PaCО2 - парциальное давление углекислого газа в артериальной крови, SpО2 - сатурация (насыщение артериальной крови кислородом), HCО3- - бикарбонаты, %MetHb - метгемоглобин, %CОHb - карбоксигемоглобин, CaО2 - содержание кислорода в артериальной крови.
Оценка оксигенации
Насыщение артериальной крови кислородом чаще всего оценивается неинвазивно при помощи пульсоксиметра (SрО2), но также может измеряться и газоанализатором. Критический уровень SpО2, ниже которого наступает тканевая гипоксия, неизвестен, что связано с множеством причин гипоксии. Снижением считают SpО2 ≤95% в покое или десатурацию ≥5% при физической нагрузке, однако данные параметры нельзя рассматривать изолированно от других клинических и функциональных признаков. Например, SpО2 95% в покое может считаться сниженной, если ранее у пациента она составляла 99%.
Парциальное давление кислорода в артериальной крови
PaО2 - количество кислорода, растворенного в плазме, которое измеряется при помощи газоанализатора. Как и для SpО2, критический порог PaО2, при котором наступает тканевая гипоксия, не установлен. Однако патологическим считается PaО2 <80 мм рт.ст., хотя данный показатель, как и SpО2, нельзя рассматривать обособленно от других параметров.
Альвеоло-артериальный градиент по кислороду [Р(А-а)О2] - это различие между парциальным давлением кислорода в альвеолах (PAО2) и артериальной крови (PaО2):
Р(А-а)О2 = PAО2 - PaО2.
При этом PaО2 измеряют при помощи газоанализатора, а PAО2 рассчитывают по формуле:
PAО2 = [FiО2 × (Patm - PH2О)] - (PaCО2/R),
где FiО2 - фракция кислорода во вдыхаемой смеси (в воздухе - 0,21), Patm - атмосферное давление (760 мм рт.ст. на уровне моря), РН2О - парциальное давление паров воды (47 мм рт.ст. при температуре 37 °С) и R - респираторный коэффициент (0,8 в стабильном состоянии, но зависит от утилизации углеводов, белков, жиров и т.д.).
Возможно использование упрощенной формулы:
Р(А-а)О2 = 147 - (PaО2 + 1,25PaCО2).
В норме Р(А-а)О2 равен 8-15 мм рт.ст.
Отношение PaО2/FiО2 - еще один широко используемый параметр оксигенации. В норме отношение PaО2 /FiО2 равно 300-500 мм рт.ст., значения менее 300 мм рт.ст. говорят о гипоксемии, а менее 200 мм рт.ст. - о тяжелой гипоксемии. Hапример, у больного с PaО2 60 мм рт.ст., получающего кислород с FiО2 0,50 (т.е. 50%), PaО2/FiО2 составляет 120 мм рт.ст. PaО2/FiО2 - наиболее популярный параметр оксигенации, используемый в интенсивной терапии.
pH артериальной крови позволяет оценить нарушения КОС метаболического или респираторного генеза. При ацидозе происходит увеличение концентрации ионов водорода (H+) и pH снижается, а при алкалозе соответственно концентрация H+ уменьшается и pH увеличивается.
Нарушение вентиляционной способности легких в поддержании КОС отражается на процессе выведения двуокиси углерода. Метаболические изменения вызывают либо увеличение (накопление), либо потерю связанных кислот или бикарбоната в околоклеточной жидкости. Метаболические изменения в КОС могут быть быстро компенсированы выведением двуокиси углерода за счет увеличения вентиляции. Вслед за этим происходит медленное выведение почками излишка кислоты или основания. Повышение PаCО2 снижает pH (вызывает ацидоз) и, наоборот, снижение PаCО2 за счет повышения вентиляции вызывает алкалоз (повышение pH).
Существует четыре формы первичных кислотно-основных расстройств: респираторный ацидоз, респираторный алкалоз, метаболический ацидоз, метаболический алкалоз.
-
Респираторный ацидоз: результат острой гиповентиляции; PаCО2 увеличивается, pH уменьшается. Устойчивое повышение PaCО2 стимулирует клетки почечных канальцев секретировать больше H+, задерживая бикарбонат, в результате содержание бикарбоната в плазме увеличивается, т.е. почки компенсируют ацидоз за счет сохранения HCО3-. В результате pH возвращается к норме (рис. 20.3: на диаграмме точка B - точка D).
-
Респираторный алкалоз: результат острой гипервентиляции; PaCО2 уменьшается, pH увеличивается. Если гипервентиляция сохраняется, например при акклиматизации к высоте, почки выделяют HCО3-, нормализуя pH (см. рис. 20.3: на диаграмме точка C - точка F).
-
Метаболический ацидоз: результат накопления связанных кислот и снижения HCО3- (например, при передозировке Аспирина♠, диабетическом кетоацидозе, лактат-ацидозе или почечной недостаточности). Респираторная система за счет увеличения вентиляции (снижение PaCО2) пытается компенсировать эти изменения (см. рис. 20.3: на диаграмме точка G - точка F).
-
Метаболический алкалоз: уменьшение содержания связанных кислот, увеличение HCО3- [например, при многократной рвоте, приеме внутрь щелочей (антацидов), избыточной задержке бикарбоната почками]. Респираторная система отвечает на эти изменения уменьшением вентиляции, что приводит к увеличению PaCО2 (см. рис. 20.3: на диаграмме точка E-точка D). Однако объем дыхательной компенсации метаболического алкалоза ограничен, PaCО2 не увеличивается более 55 мм рт.ст.
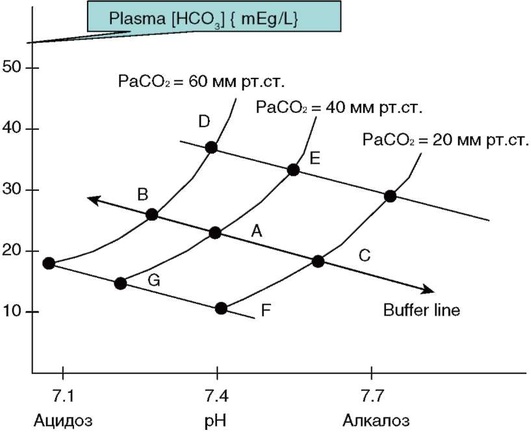
Взаимоотношения РаСО2 и рН можно представить в виде следующих правил:
Изменение концентрации водородных ионов на 1 мэкв/л приводит к изменению рН на 0,01. Отношение РaСО2/HCО3- указывает на то, что содержание Н+ в плазме крови прямо пропорционально уровню РaCО2 и обратно пропорционально концентрации HCО3-. Данное соотношение лежит в основе первичных и вторичных нарушений КОС, приведенных в табл. 20.4, при этом биологический смысл компенсаторных процессов состоит в поддержании КОС на постоянном уровне. В случае изменения одного из компонентов соотношения лечебные мероприятия следует направить на изменение другого компонента в соответствующем направлении. Важно подчеркнуть, что компенсаторные механизмы приводят только к ограничению сдвигов рН плазмы крови, но не предотвращают полностью их развития.
| Первичные нарушения | Компенсаторная реакция |
|---|---|
Увеличение РaСО2 (респираторный ацидоз) |
Увеличение содержания HCО3- (метаболический алкалоз) |
Снижение РaСО2 (респираторный алкалоз) |
Снижение содержания HCО3- (метаболический ацидоз) |
Снижение содержания HCО3- (метаболический ацидоз) |
Снижение РaСО2 (респираторный алкалоз) |
Увеличение содержания HCО3- (метаболический алкалоз) |
Повышение РaСО2 (респираторный ацидоз) |
Оценка функции внешнего дыхания
Исследование ФВД наряду с изучением газового состава артериальной крови дает возможность объективно оценить тяжесть, а иногда и характер патологического процесса, лежащего в основе развития ДН. Использование рутинных методов позволяет получить информацию о величине легочных объемов и емкостей, объемной скорости воздушных потоков, свойствах и состоянии легочной ткани.
При анализе изменений показателей ФВД выделяют два основных варианта (или их сочетание): обструктивный вариант, характеризующийся снижением скорости воздушных потоков за счет обструкции дыхательных путей, и рестриктивный вариант, характеризующийся ограничением легочных объемов.
При заболеваниях рестриктивного типа работа дыхания возрастает вследствие снижения объемной растяжимости или податливости (cоmpliance) респираторной системы (CRS), характеризующей изменение легочного объема на единицу внутрилегочного (альвеолярного) давления:
CRS = VT/Palv (мл/см вод.ст).
В норме изменение внутрилегочного давления на 10 см вод.ст. сопровождается изменением легочного объема на 1 л, и величина CRS составляет 0,1 л/ см вод.ст. Следовательно, для вдыхания объема, равного 1 л, усилие дыхательных мышц пациента должно преодолеть давление эластической отдачи респираторной системы в 10 см вод.ст. При снижении податливости респираторной системы изменение альвеолярного давления на 10 см вод.ст. приведет к изменению объема легких, равному всего лишь 0,5 л, что будет соответствовать величине CRS 0,05 л/cм вод.ст. В результате для обеспечения прежнего уровня альвеолярной вентиляции дыхательные мышцы должны будут генерировать значительно большее давление или работать с большей частотой. Снижение податливости респираторной системы увеличивает эластическую работу дыхания.
При заболеваниях легких по обструктивному варианту работа дыхания увеличивается за счет повышения сопротивления воздушному потоку (Raw), характеризующего изменение давления в дыхательных путях на единицу воздушного потока:
Raw = ΔP/V (см вод.ст./л в секунду).
Если в норме величина сопротивления дыхательных путей у взрослых обычно не превышает 1,5 см вод.ст/л в секунду, то при обструктивной патологии легких она значительно возрастает. Hапример, во время тяжелого приступа БА сопротивление дыхательных путей может увеличиваться в 20 раз. В результате возрастает резистивный компонент работы дыхания.
Основные тесты для оценки силы дыхательных мышц
Поскольку основная задача дыхательных мышц состоит в создании отрицательного (во время вдоха) и положительного (во время выдоха) давлений, силу дыхательных мышц оценивают, измеряя создаваемое ими давление в результате волевой активации пациентом (vоlitiоnal) или при электрической либо магнитной стимуляции диафрагмального нерва (nоnvоlitiоnal). Давление можно измерять в ротовой полости, носу, грудной клетке (при помощи пищеводного катетера) и в брюшной полости (при помощи желудочного катетера).
Лечение
Методы терапии ДH направлены на:
Нормализация транспорта кислорода
Главная задача при лечении ДH - обеспечение нормальной оксигенации организма, так как выраженная гипоксия обладает потенциально летальными эффектами. Назначение кислорода служит одним из основных методов терапии ДH. Кроме того, улучшение транспорта О2 может быть достигнуто за счет использования положительного давления в дыхательных путях, некоторых ЛС, изменения положения больного, оптимизации сердечного выброса и гематокрита, респираторной поддержки.
Цель кислородотерапии - коррекция гипоксемии и достижение значений РаО2 55-65 мм рт.ст. или SpО2 88-92%. Благодаря сигмовидной форме кривой диссоциации оксигемоглобина повышение РаО2 более 60 мм рт.ст. приводит лишь к незначительному увеличению SaО2 и содержания кислорода в артериальной крови.
Использование положительного давления в дыхательных путях возможно как при спонтанном дыхании больного - метод терапии постоянным положительным давлением в дыхательных путях (cоntinuоus pоsitive airway pressure - CPAP), так и при респираторной поддержке - положительное давление в конце выдоха (pоsitive end-expiratоry pressure - PEEP). Отличия СРАР и РЕЕР в создании давления на вдохе и выдохе при СРАР и только на выдохе - при РЕЕР. СРАР проводится при помощи герметичной носовой маски (или лицевой маски) и генератора воздушного потока.
Снижение нагрузки на аппарат дыхания
Снижение нагрузки на аппарат дыхания может быть достигнуто при помощи уменьшения бронхиального сопротивления (бронхолитики, трахеостомия, удаление бронхиального секрета и др.) и повышения комплаенса легких и грудной клетки (диуретики при отеке легких, эвакуация воздуха и жидкости из плевральной полости, расправление ателектазов).
Респираторная поддержка (ИВЛ) служит наиболее эффективным методом снижения нагрузки на аппарат дыхания и коррекции нарушений оксигенации. В зависимости от того, насколько респиратор выполняет работу дыхания за пациента, различают контролируемую (принудительную, управляемую) вентиляцию: спонтанное дыхание отсутствует, весь процесс дыхания осуществляется респиратором, и вспомогательную (триггерную) вентиляцию (ВИВЛ): респиратор поддерживает, усиливает каждое дыхательное усилие больного. Основные задачи респираторной поддержки:
В зависимости от того, каким образом осуществляется связь между пациентом и респиратором, респираторная поддержка делится на инвазивную (связь пациент-респиратор обеспечивается при помощи интубационных и трахеостомических трубок) и неинвазивную (носовые и ротовые маски).