Клиническая фармакология : учебник / В. Г. Кукес, Д. А. Сычев [и др. ] ; под ред. В. Г. Кукеса, Д. А. Сычева. - 6-е изд. , испр. и доп. - Москва : ГЭОТАР-Медиа, 2021. - 1024 с. : ил. - 1024 с. - ISBN 978-5-9704-58815 |
Аннотация
Шестое издание учебника исправлено и дополнено новыми сведениями с учетом последних достижений клинической фармакологии, а также новых государственных образовательных стандартов. Даны современные представления о фармакокинетических процессах, указаны принципы диагностики, коррекции и профилактики нежелательных лекарственных реакций, раскрыты новые механизмы взаимодействия лекарственных средств (на уровне транспортеров). В главе "Основы рациональной фармакотерапии" отражены основные клинико-фармакологические технологии эффективного и безопасного применения лекарственных средств. Клиническая фармакология отдельных групп лекарственных средств рассмотрена с учетом современных представлений о механизме действия, а также с позиций доказательной и персонализированной медицины. Изложена клиническая фармакология новых групп лекарственных средств. Главы, в которых освещены темы, не входящие в примерную программу, размещены в электронной версии учебника, код доступа к которой указан на первом форзаце книги под защитным слоем.
27.2. Глюкокортикоиды
Соединения, составляющие группу гормонально-активных веществ стероидной структуры с преимущественно глюкокортикоидной функцией, имеют общее название «глюкокортикоиды» (глюкокортикостероиды, глюкокортикоидные гормоны). Среди них можно выделить:
Синтез глюкокортикоидов в надпочечниках и их секреция в кровь происходит под контролем АКТГ, выделяющегося передней долей гипофиза, что стимулируется гипоталамическим кортиколиберином. Таким образом, формируется ось «гипоталамус-гипофизкора надпочечников», или гипоталамо-гипофизарно-надпочечниковая система (ГГНС), активирующаяся при стрессе, под влиянием медиаторов воспаления и др. ГГНС функционирует по принципу негативной обратной связи: при снижении уровня кортизола[71] в крови выброс АКТГ возрастает, а при повышении - падает[72]. Секреция глюкокортикоидов в физиологических условиях подчиняется циркадным ритмам - она достигает максимума в ранние утренние часы (акрофаза приходится на 6-8 ч) и снижается вечером и ночью.
История вопроса
История изучения глюкокортикоидов началась задолго до их открытия. В 1929 г. американский врач Филипп Шоултер Хенч (клиника Мейо) обратил внимание на то, что у заболевшего желтухой пожилого пациента с тяжелым ревматоидным артритом уменьшилась боль и увеличился объем движений в суставах. В последующем Филипп Хенч вместе с Чарльзом Слокумом отметили, что регресс клинической картины ревматоидного артрита пропорционален выраженности симптомов желтухи. Исходя из этих наблюдений к 1934 г. исследователи сформулировали идею о появлении при желтухе неизвестного вещества, обладающего лечебным эффектом, и назвали его «антиревматическая субстанция Х». Лишь по прошествии длительного времени стало известно, что эта субстанция, в норме метаболизируясь в печени, накапливается в организме при желтухе - заболевании, при котором печень оказывается несостоятельной.
К 1938 г. были накоплены данные о том, что ремиссия ревматоидного артрита может также наблюдаться на фоне беременности. Это позволило высказать мнение, что ремиссия при желтухе и беременности обусловливается одним и тем же фактором, т.е. предположить некую универсальность гипотетической «субстанции Х». Косвенным подтверждением этому предположению стали полученные позже факты о благоприятном влиянии как желтухи, так и беременности на клиническое течение ряда других заболеваний, включая бронхиальную астму. К 1942 г. стало известно, что симптоматические улучшения при ревматоидном артрите иногда вызывают и другие напряженные ситуации, например общий наркоз или противотифозная вакцинация.
В 1934 г. известный американский биохимик Эдуард Келвин Кендалл занимался идентификацией стероидных гормонов коры надпочечников. Он выделил в кристаллическом виде 5 соединений, обозначенных им в порядке получения A, B, C, D и E, наиболее активным из которых было признано вещество E. Позже ему удалось выделить еще и шестое вещество - F.
В это же время, независимо от американцев, шведский исследователь польского происхождения Тадеуш Рейхштейн занимался изучением веществ, выделяемых из коры надпочечников. Исследовав 30 соединений, он описал их стероидную структуру, синтезировал многие из них, идентифицировал кортизон (вещество E по Э.К. Кендаллу), а также более активный кортизол, или гидрокортизон[73] (по Э.К. Кендаллу - вещество F) и указал на возможности терапевтического использования гормонов коры надпочечников.
Однако первое клиническое применение глюкокортикоидов было выполнено в США. В 1938 г. произошло знакомство Э.К. Кендалла и Ф.Ш. Хенча, что и ознаменовало начало клинического этапа изучения гормонов коры надпочечников. Было высказано предположение, что вещество E идентично «антиревматической субстанции X» и является основным стероидным гормоном. Было решено испытать вещество E в клинических условиях.
После почти 10-летней подготовки Ф.Ш. Хенчу и Э.К. Кендаллу удалось получить достаточное количество кортизона, и с 21 по 23 сентября 1948 г. 29-летней больной, страдавшей тяжелым ревматоидным артритом, были сделаны 3 инъекции кортизона по 100 мг/сут. Результатом было значительное улучшение состояния пациентки и почти полное исчезновение всех функциональных нарушений, что превзошло все ожидания.
Филипп Шоултер Хенч, Эдуард Келвин Кендалл и Тадеуш Рейхштейн стали лауреатами Нобелевской премии по физиологии и медицине 1950 г. «За открытия, касающиеся гормонов коры надпочечников, их структуры и биологических эффектов».
Классификация
Все глюкокортикоиды обладают базовой структурой гидрокортизона, клиническое значение имеют их происхождение и некоторые минимальные изменения в структуре стероидного ядра, а также наличие или отсутствие в молекуле отдельных групп и фтора. Таким образом, среди глюкокортикоидов выделяют три группы препаратов (табл. 27.17):
Таблица 27.17. Структура глюкокортикоидов и их некоторые свойства
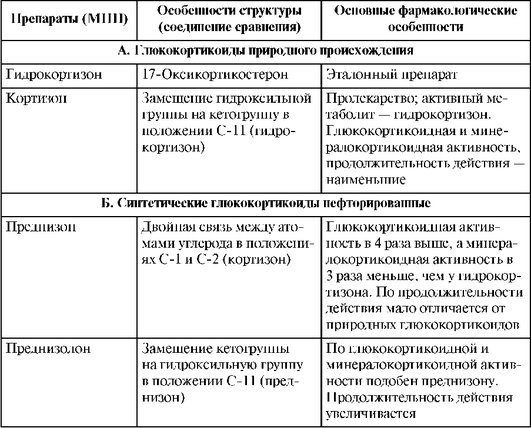
Окончание табл. 27.17
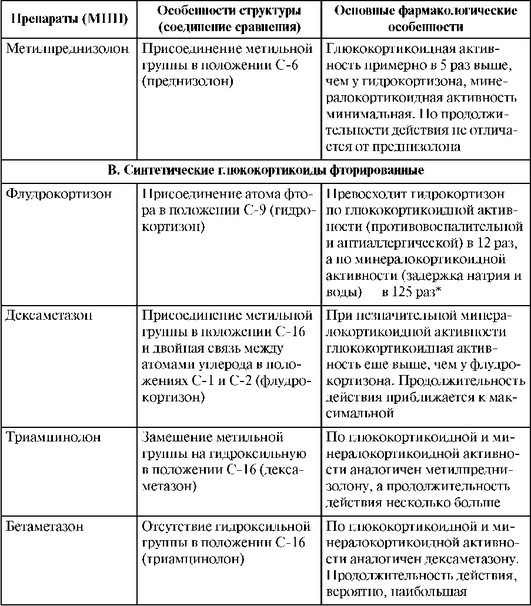
* Используется при заместительной терапии первичной надпочечниковой недостаточности или селективного гипоальдостеронизма, поскольку промышленное производство альдостерона технологически сложно и весьма затратно.
Препараты этих групп различаются, в частности, выраженностью глюкокортикоидной активности (часто отождествляемой с противовоспалительной активностью), соотношением глюкокортикоидной и минералокортикоидной активности (минералокортикоидная активность проявляется способностью задерживать натрий и воду), силой подавления функции ГГНС и некоторыми другими особенностями (табл. 27.18). Также по уровню активности классифицируют и глюкокортикоидные ЛС для наружного применения (табл. 27.19).
Механизм действия и фармакодинамические эффекты
Глюкокортикоиды обладают разнообразными эффектами, в основе которых лежат различные механизмы.
Рецепторы к глюкокортикоидам присутствуют практически во всех тканях и располагаются внутриклеточно. Комплекс «гормон-рецептор» поступает в ядро клетки и стимулирует образование информационной РНК, что обусловливает синтез различных регуляторных белков. Ряд биологически активных веществ (катехоламины, медиаторы воспаления) способны инактивировать комплексы «гормон-рецептор», снижая активность глюкокортикоидов. Среди регуляторных белков, образование которых стимулируется глюкокортикоидами, можно выделить липокортины, обладающие противовоспалительным (один из липокортинов ингибирует фосфолипазу А2, нарушая синтез медиаторов воспаления простагландинов и лейкотриенов) и противоотечным эффектами. Действие глюкокортикоидов опосредуется не только через ядро, но и через мембранный и цитоплазматический аппараты, что обеспечивает высокую скорость развития некоторых эффектов (например, гемодинамических), особенно при внутривенном введении высоких доз глюкокортикоидов.
Среди множества эффектов глюкокортикоидов можно выделить такие, которые всегда считаются терапевтическими (например, противовоспалительный, противоаллергический, противоотечный); клиническая же оценка других (иммуносупрессивное влияние на функции симпатико-адреналовой или эндокринной систем) зависит от ситуации. Сравнение наиболее клинически значимых свойств отдельных препаратов см. в табл. 27.18.
Сила ЛС для наружного применения зависит от химической структуры вещества, от его концентрации в лекарственной форме и от самой лекарственной формы: наибольшей силой обладают мази, меньшей - кремы, самой маленькой - лосьоны.
Таблица 27.18. Основные характеристики различных глюкокортикоидов, применяемых в клинических условиях
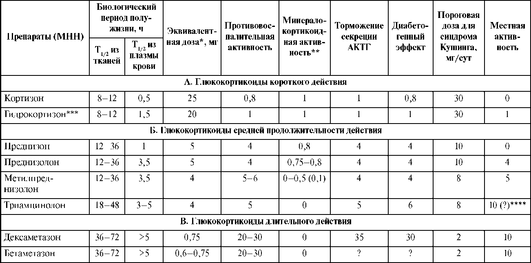
* Приведенные в таблице дозы относятся к системному применению глюкокортикоидов внутрь; для инъекционных лекарственных форм эквивалентными оказываются дозы, в 4-6-10 раз большие (у разных препаратов по-разному); исключение составляют кортизон и гидрокортизон, у которых дозы для инъекций и для приема внутрь не различаются.
** У всех имеющихся сегодня глюкокортикоидов присутствует какая-то минералокортикоидная активность, однако у последних четырех препаратов в таблице она столь невелика, что в клинических условиях ею можно пренебречь.
*** При оценке выраженности фармакодинамических эффектов глюкокортикоидов в условных величинах за единицу принимается активность гидрокортизона как эндогенного гормона, считающегося эталонным соединением.
**** Данные уточняются.
Таблица 27.19. Некоторые препараты глюкокортикоидов для наружного применения*, зарегистрированные в России
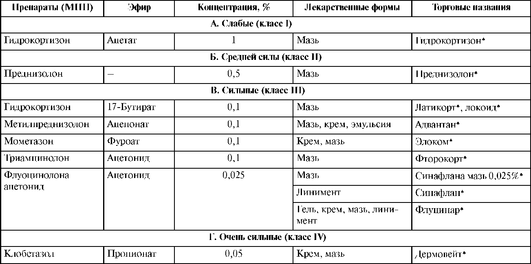
* Деление на классы по силе действия - на основе Европейской классификации потенциальной активности местных глюкокортикоидов.
В действии глюкокортикоидов можно выделить как анаболическую, так и катаболическую направленность с преобладанием последней при использовании фармакологических доз. Препараты этой группы оказывают:
-
влияние на углеводный обмен (что определило название «глюкокортикоиды»), выражающееся стимуляцией глюконеогенеза и синтеза гликогена в тканях при физиологических концентрациях (анаболизм) и стимуляцией по мере увеличения дозы гликогенолиза сначала в скелетных мышцах, а затем и в печени (катаболизм), что вместе с сохраняющимся глюконеогенезом, усилением всасывания глюкозы из ЖКТ и уменьшением проницаемости мембран для нее приводит к гипергликемии, а у ряда больных - к развитию стероидного диабета;
-
влияние на белковый обмен с преобладанием катаболизма над анаболизмом (отрицательный азотистый баланс), что определяет, в частности, их негативное действие на кожные покровы и скелетные мышцы (вплоть до развития атрофии кожи со стриями и кровоизлияниями, а также миодистрофий с мышечной слабостью и похудением), на костный матрикс, грануляционную и лимфоидную ткани (см. ниже);никает гипер-билирубинемия. В месте инъекции возможна кожная реакция.
-
влияние на белковый обмен с преобладанием катаболизма над анаболизмом (отрицательный азотистый баланс), что определяет, в частности, их негативное действие на кожные покровы и скелетные мышцы (вплоть до развития атрофии кожи со стриями и кровоизлияниями, а также миодистрофий с мышечной слабостью и похудением), на костный матрикс, грануляционную и лимфоидную ткани (см. ниже);
-
влияние на водно-электролитный обмен, обусловленное, по крайней мере, двумя механизмами:
-
во-первых, глюкокортикоиды, за счет сопутствующей минералокортикоидной активности, изменяют реабсорбцию в дистальных канальцах почек, задерживают в организме натрий и воду, выводя калий и магний (в отношении этих эффектов ЛС можно расположить в убывающей последовательности: флудрокортизон >> природные глюкокортикоиды > синтетические глюкокортикоиды >> фторированные глюкокортикоиды);
-
во-вторых, подавляя активность витамина D, они уменьшают всасывание и усиливают выведение кальция, снижая его накопление в костях и формируя остеопороз (этот эффект проявляется как при использовании высоких доз, так и при длительном применении относительно небольших доз);
-
-
противовоспалительное действие, наиболее часто используемое в клинической практике, затрагивает все фазы воспалительных реакций различных типов, благодаря торможению образования продуктов арахидонового каскада (простагландинов и лейкотриенов, циклических эндоперекисей), а также подавлению синтеза интерлейкинов (ИЛ-1, ИЛ-2, ИЛ-6) лимфоцитами и макрофагами, стабилизации лизосомальных мембран, уменьшению проницаемости капилляров, торможению миграции нейтрофилов и макрофагов в очаг воспаления, угнетению пролиферации фибробластов и синтеза коллагена;
-
обезболивающие и жаропонижающие свойства, выраженные у глюкокортикоидов в значительной степени, обусловлены теми же механизмами, что и противовоспалительное действие;
-
противоотечное (противоэкссудативное) действие, развивающееся в результате уменьшения проницаемости биологических мембран всех уровней (стабилизация клеточных, лизосомальных мембран и уменьшение проницаемости капилляров), выражено у глюкокортикоидов тем больше, чем слабее у них минералокортикоидная активность;
-
иммуносупрессивное, противоаллергическое и десенсибилизирующее действие обусловлено подавлением:
-
клеточного иммунитета (торможение миграции стволовых клеток, миграции В-лимфоцитов, взаимодействия Т- и В-лимфоцитов, пролиферации лимфоидной ткани);
-
гуморального иммунитета (угнетение синтеза антител, торможение системы комплемента и реакции антиген-антитело);
-
высвобождения медиаторов аллергии (угнетение взаимодействия иммуноглобулинов с тучными клетками и макрофагами, стабилизация мембран тучных клеток);
-
-
противозудное действие представляет собой результат противоаллергических и обезболивающих свойств;
-
воздействие на систему крови, имеющее различные механизмы и проявляющееся разнонаправленно в отношении отдельных ростков и клеточных элементов: глюкокортикоиды снижают количество лимфоцитов, моноцитов, эозинофилов и базофилов в периферической крови, одновременно стимулируют эритро- и тромбоцитопоэз, а также увеличивают содержание в крови нейтрофильных лейкоцитов, тормозя их миграцию из кровяного русла; эти изменения возникают уже после однократного приема глюкокортикоидов в сроки от 4-6 до 12 ч, а общая продолжительность достигает 24 ч (после длительного применения глюкокортикоидов эти изменения могут сохраняться до 4 нед);
-
влияние на эндокринные функции, выражающееся пропорциональным длительности применения (или длительности действия препарата) торможением секреции тропных гормонов - АКТГ, ТТГ и других по механизму обратной связи; торможение выброса АКТГ приводит к падению образования эндогенных глюкокортикоидов и минералокортикоидов;
-
влияние на симпатико-адреналовую систему опосредуется через стимуляцию синтеза α- и β-адренорецепторов и повышение чувствительности рецепторов к катехоламинам (этому способствует и задерживаемый в организме натрий), что обеспечивает лечебный эффект глюкокортикоидов в отношении бронхов и лечебный или НЛР в отношении ССС;
-
воздействие на ССС, проявляющееся поддержанием тонуса артериол и сократимости миокарда, увеличением ЧСС, сердечного выброса и АД за счет усиления эффектов катехоламинов и ангиотензина II;
-
антитоксический эффект, основанный на мембраностабилизирующем действии, препятствующем, в частности, высвобождению лизосомальных ферментов; он обусловлен еще и способностью синтетических глюкокортикоидов непосредственно связываться с эндотоксином;
-
психотропное действие, заключающееся в повышении активности и настроения вплоть до эйфории (иногда возникает агрессия), улучшении аппетита; изменения в психоэмоциональной сфере могут создавать иллюзию положительных сдвигов в клиническом течении болезни;
-
противорвотное действие, складывающееся из антитоксического и психотропного эффектов;
-
паллиативное антинеопластическое действие, которое обычно связывают с противовоспалительным, антитоксическим и психотропным влиянием;
-
адаптогенное действие, которым обладают глюкокортикоиды в физиологических условиях, складывается практически из всех перечисленных эффектов; может использоваться, в частности, в реанимационной практике для профилактики развития «шокового легкого», синдрома полиорганной недостаточности.
Указанные фармакодинамические эффекты проявляются как при системном, так и при местном назначении. Причем для последнего предпочтительнее препараты с наивысшей местной активностью (см. табл. 27.19).
Так, среди средств для наружного применения безусловными преимуществами обладают лекарства с наименьшей способностью к абсорбции через кожу (см. ниже), а для интраназального назначения наиболее приемлемы будесонид, флутиказона пропионатx, мометазона фуроатx, которые по местной активности в 100-500 раз превосходят дексаметазон.
Фармакокинетика
Абсорбция
Глюкокортикоиды труднорастворимы в воде, хорошо растворимы в жирах, благодаря чему быстро и полно всасываются в ЖКТ. Время достижения Cmax после приема внутрь составляет 30-90 мин, а биодоступность лежит в пределах от 20-30 до 70-90%. Эффект первого прохождения через печень существенного значения не имеет, за исключением пресистемного метаболизма кортизона и преднизона, в результате которого образуются соответственно активные гидрокортизон и преднизолон.
При внутримышечном введении водорастворимых глюкокортикоидов (сукцинатов, гемисукцинатов и фосфатов) максимальный эффект достигается через 1-2 ч. Высокую скорость наступления эффекта (по крайней мере, гемодинамического) обеспечивает их внутривенное введение, при котором абсорбция отсутствует.
Мелкокристаллические суспензии (ацетаты и ацетониды) не растворимы в воде и либо обеспечивают местный эффект при внутрисуставном или околосуставном введении с минимальной абсорбцией (лечебный эффект при внутрисуставном введении наступает в течение 6-24 ч и длится от нескольких дней до нескольких недель), либо при внутримышечном введении создают депо, благодаря чему они медленно всасываются: начинают действовать через 1-2 сут, оказывают максимальный эффект через 4-8 сут и действуют до 4 нед.
Суспензии нельзя вводить внутривенно!
Топическое применение (накожное, ингаляционное, интраназальное, интра- и периартикулярное) ЛС призвано минимизировать системные реакции, однако нередко также сопровождается абсорбцией глюкокортикоидов в кровь. Например, высокая всасываемость со слизистой оболочки полости носа приводит к тому, что системная биодоступность глюкокортикоидов при интраназальном применении обычно (за исключением флутиказона пропионатаx и мометазона) вдвое выше, чем при приеме внутрь[74]. Однако, поскольку местное назначение позволяет использовать минимальные дозы препаратов, при соблюдении рекомендуемых режимов дозирования системные концентрации также не бывают высокими (см. раздел «Способ применения, режим дозирования и дозы»).
Сравнение системной биодоступности при разных способах применения приведено в табл. 27.20. Прием пищи несильно замедляет абсорбцию, не уменьшая биодоступность.
Таблица 27.20. Биодоступность глюкокортикоидов при разных способах их применения*
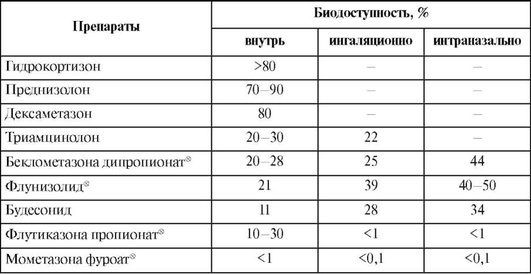
* В таблице приведены все имеющиеся данные по биодоступности глюкокортикоидов при трех способах их применения вне зависимости от того, существуют ли соответствующие лекарственные формы (см. раздел «Лекарственные формы») и используется ли препарат таким образом.
Глюкокортикоиды для наружного применения III и IV класса («сильные» и «очень сильные», см. табл. 27.19) всасываются с поверхности кожи незначительно. Они создают высокие местные концентрации и оказывают преимущественно местное действие. Более слабые препараты (I и II класса) обладают большей абсорбционной способностью с поверхности кожи и потому не только менее эффективны, но и создают угрозу системных НЛР.
Несмотря на то что при интраназальном введении глюкокортикоидов лекарственное вещество доставляется непосредственно в патологический очаг, немедленный клинический эффект получить невозможно - он бывает отсроченным (табл. 27.21).
Таблица 27.21. Время наступления эффекта интраназальных глюкокортикоидов
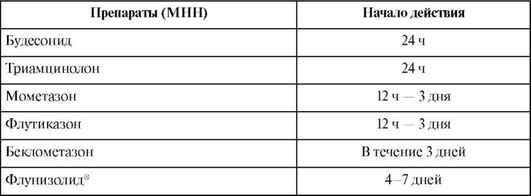
Аналогичные данные характеризуют и ингаляционные лекарственные формы глюкокортикоидов, используемые для лечения бронхиальной астмы. Они служат наиболее эффективным методом профилактического и поддерживающего лечения. Их применение базируется на местном противовоспалительном действии, а при длительном применении (в течение нескольких месяцев) - еще и на уменьшении гиперреактивности бронхов (что обусловлено ослаблением спазмогенных влияний многих биологически активных веществ: гистамина, брадикинина, ацетилхолина, аденозина, а также холодного и сырого воздуха, углекислого газа). Ингаляционные глюкокортикоиды нельзя использовать для купирования приступа бронхиальной астмы, поскольку их эффект развивается медленно, в течение 1 нед, а максимальное действие отмечается примерно через 6 нед от начала лечения.
Местные глюкокортикоиды активнее абсорбируются из воспаленных областей, чем со здоровых участков кожи; у детей сильнее, чем у взрослых. Кожа в разных областях тела обладает различной способностью к абсорбции (табл. 27.22). Ванна или увлажнение кожных покровов другими способами значительно увеличивают проницаемость кожи для местных глюкокортикоидов.
Таблица 27.22. Всасывание глюкокортикоидов с различных участков тела при наружном применении
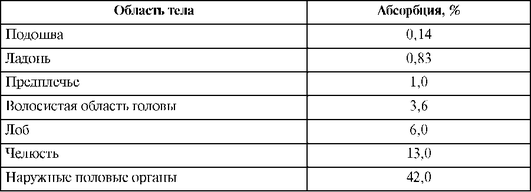
Распределение и связь с белками
В плазме крови разные глюкокортикоиды на 40-95% связываются с транскортином (кортизолсвязывающим α-глобулином) и альбумином. При концентрации гидрокортизона в плазме крови до 200 мкг/л его связанная фракция составляет 95%, а количество свободного гормона не превышает 10 мкг/л. При увеличении уровня гидрокортизона в плазме крови более 200 мкг/л наступает насыщение транскортина и возникает избыток гормона: при концентрации 1000 мкг/л величина связанной фракции уменьшается приблизительно до 70%. Все синтетические глюкокортикоиды, по сравнению с гидрокортизоном, меньше связываются с белками (60-70%), а увеличенная таким образом свободная фракция, полностью распределяясь в ткани, обеспечивает более высокую активность глюкокортикоидов. При снижении синтеза белка (цирроз печени) или большой его потере (нефротический синдром, спру, синдром мальабсорбции) наблюдается передозировка глюкокортикоидов при применении обычных терапевтических доз. Белки, сохраняющие глюкокортикоиды в циркулирующей крови, предохраняя их от биотрансформации и выведения, синтезируются в печени, поэтому при применении этих ЛС внутрь используются существенно меньшие дозы, чем при внутривенном введении.
Объем распределения глюкокортикоидов составляет около 0,4 л/кг.
Биотрансформация
Биотрансформация глюкокортикоидов происходит преимущественно в печени с образованием неактивных метаболитов (путем окисления, восстановления и конъюгирования) и частично в почках. Синтетические и природные глюкокортикоиды метаболизируются одинаково, лишь природный кортизон и синтетический преднизон сначала превращаются в активные формы (см. выше). Природные глюкокортикоиды метаболизируются наиболее быстро, синтетические - медленнее, из которых самой долгой биотрансформацией характеризуются фторированные препараты.
При ингаляционном введении только 10-20% глюкокортикоидов достигают дыхательных путей, в то время как 80-90% задерживаются в полости рта и затем проглатываются. После всасывания в ЖКТ значительная часть препарата подвергается пресистемному метаболизму.
Топические глюкокортикоиды метаболизируются в зонах их применения (в легких, слизистой оболочке носа, коже).
Элиминация
Неактивные метаболиты (конъюгаты серной и глюкуроновой кислот) и в небольшом количестве неизмененные глюкокортикоиды (для триамцинолона - 20%) экскретируются почками. T1/2 варьирует от 30 мин до 5 ч и более, что отличается от времени снижения глюкокортикоидной активности вдвое. Природные глюкокортикоиды имеют наименьший период биологической полужизни, фторированные препараты - наиболее длинный (см. табл. 27.17). Поскольку элиминация глюкокортикоидов из плазмы крови связана с их биотрансформацией, T1/2 при почечной недостаточности не меняется, и корригировать дозы не нужно.
Цели применения глюкокортикоидов (варианты глюкокортикоидного лечения[1])
-
Замещение утраченной гормональной функции (заместительная терапия):
-
Блокада высвобождения тропных (и соответствующих периферических) гормонов (блокирующая, супрессивная или подавляющая терапия и блокирующие фармакологические пробы):
-
наиболее активно ГГНС подавляют препараты с длительным тканевым периодом полужизни (синтетические, особенно фторированные);
-
применяются как физиологические, так и более высокие фармакологические дозы (с учетом эквивалентности при назначении внутрь и парентерально);
-
для наиболее эффективного подавления функции ГГНС используют режим дозирования глюкокортикоидов, не совпадающий с циркадным ритмом секреции АКТГ и кортизола.
-
-
Лечение неэндокринных заболеваний (фармакодинамическая терапия):
-
подразделяется на системную: внутрь, внутривенно, внутримышечно и местную: наружно (на кожу), внутрикожно (в рубцы), ингаляционно (топическими формами глюкокортикоидов), интраназально, интра- и периартикулярно, в полости, эпидурально, иногда проводят фонофорез;
-
деление на системную и местную терапию достаточно условно, поскольку абсорбция глюкокортикоидов местного применения в некоторых случаях может оказаться столь велика, что развиваются системные НЛР.
Показания к применению
Вводимые извне глюкокортикоиды не только играют необходимую при этом состоянии заместительную роль, но и уменьшают тиреоидную активность за счет:
-
-
дифференциальная диагностика гиперкортицизма (малые дозы дексаметазона уменьшают кортизолемию при «физиологическом» гиперкортицизме (стрессе, ожирении) и не подавляют «эндогенный» гиперкортицизм; последний может наблюдаться при болезни Иценко-Кушинга, и в этом случае секрецию кортизола возможно подавить большими дозами дексаметазона, которые неэффекивны при синдроме Кушинга, обусловленном гормонально-активными периферическими опухолями.
-
Показания к фармакодинамической терапии. В основном показания к фармакодинамическому лечению глюкокортикоидами основываются на противовоспалительном, противоотечном, противоаллергическом, иммуносупрессивном и противошоковом действии:
-
для системного применения среди ургентных ситуаций:
-
тяжелые аллергические реакции: отек Квинке, включая подсвязочный отек гортани; диссеминированная крапивница; анафилактический шок (глюкокортикоиды вводят одновременно с эпинефрином); сывороточная болезнь; гемотрансфузионный шок; реакции на ЛС, укусы змей и насекомых, анафилактоидные реакции;
-
различный шок (ожоговый, травматический, операционный, токсический) при неэффективности других методов лечения;
-
отек головного мозга при внутричерепных объемных процессах (паразитарные инвазии, опухоли, особенно метастазы), во время и после нейрохирургических операций, после черепно-мозговых травм (в первые 6-8 ч);
-
отравления прижигающими жидкостями (для уменьшения воспалительных явлений и предупреждения рубцовых осложнений);
-
лечение болезни гиалиновых мембран (респираторного дистресс-синдрома новорожденных) и профилактика[75] этой болезни при планировании проведения родов на сроках до 32-й недели беременности;
-
для системного применения среди заболеваний и патологических процессов, требующих длительного лечения:
-
воспалительные заболевания, прежде всего с выраженным иммунным компонентом (системные заболевания соединительной ткани и васкулиты: ревматизм, ревматоидный артрит, системная красная волчанка, узелковый периартериит, гранулематоз Вегенера, гигантоклеточный артериит и другие васкулиты, ревматическая полимиалгия, эозинофильный летучий инфильтрат легкого, эозинофильный фасцит, прочие «большие» и «малые» коллагенозы);
-
аллергические реакции (сезонный ринит, контактный дерматит и др.), дерматиты и дерматозы;
-
бронхиальная астма и ХОБЛ с выраженным обструктивным синдромом;
-
молниеносный (диссеминированный) туберкулез[76], туберкулез с выраженными экссудативными процессами (экссудативный плеврит, инфильтративные формы);
-
саркоидоз[77];
-
заболевания нервной системы (рассеянный склероз, боковой амиотрофический склероз);
-
-
для местного применения (обеспечивающего увеличение эффективности при уменьшении частоты и выраженности системных НЛР) среди острых и хронических заболеваний и синдромов наиболее частыми оказываются:
Противопоказания
-
Абсолютные[78]:
Беременность и кормление грудью
Все глюкокортикоиды проникают через плаценту, где гидрокортизон и преднизолон превращаются в менее активные кортизон и преднизон. Дексаметазон и бетаметазон, проникнув через плаценту, создают высокие концентрации в крови плода и могут привести к подавлению у него функции ГГНС.
Системное и местное применение любых глюкокортикоидов считается противопоказанным при беременности (особенно в I триместре) и в период грудного вскармливания. Однако в каждом случае нужно оценивать соотношение ожидаемой пользы для матери и возможного вреда для плода, в случае необходимости отдавая предпочтение гидрокортизону и преднизолону. Местное применение в этих случаях требует особой осторожности.
Способ применения, режим дозирования и дозы
Заместительная терапия
При хронической недостаточности коры надпочечников любой этиологии глюкокортикоиды назначают в дозах, близких к физиологической секреции кортизола. Заместительную терапию предпочтительнее проводить природным ЛС - гидрокортизоном (его синтетическим аналогом для приема внутрь - Кортефом*), обладающим глюкокортикоидной и слабой минералокортикоидной активностью. Физиологические дозы гидрокортизона составляют от 20-25 до 37,5 мг/сут (5-7,5 мг преднизолона). Существует два режима дозирования глюкокортикоидов: либо 2/3 дозы назначают утром, а 1/3 вечером, либо 1/2 дозы утром, а днем и вечером по 1/4. Однако никакой режим не обеспечивает полноценную имитацию суточной секреции кортизола, поскольку ее максимум отмечается в 5 часов утра, т.е. задолго до пробуждения. Следует учитывать, что даже небольшой избыток глюкокортикоидов в ходе заместительной терапии может снижать плотность костей.
При значительном выпадении не только глюкокортикоидной, но и минералокортикоидной функции (выраженная потеря соли, артериальная гипотензия) или при использовании преднизолона, который может оказаться более эффективным, добавляют глюкокортикоид с высокой минералокортикоидной и некоторой глюкокортикоидной активностью - флудрокортизон (Кортинефф*).
При острой надпочечниковой недостаточности также предпочтение отдают препаратам гидрокортизона. На фоне массивной инфузии изотонического раствора натрия хлорида вместе с 5% раствором декстрозы внутривенно болюсно вводят сразу 100-150 мг гидрокортизона и продолжают его капельное введение со скоростью по 100 мг каждые 8 ч. Такой режим приближается к секреции кортизола в условиях стресса. Используемые при этом дозы гидрокортизона обеспечивают не только глюкокортикоидную, но и минералокортикоидную активность. При улучшении состояния переходят на внутримышечное введение 25 мг 4-6 раз в сутки. После снижения дозы менее 100 мг/сут переходят на прием гидрокортизона внутрь, переходя к режиму, применяемому при хронической надпочечниковой недостаточности, с возможным добавлением минералокортикоида (см. выше).
Блокирующая терапия (супрессивная или подавляющая)
При лечении адреногенитального синдрома используют физиологические дозы глюкокортикоидов:
-
детям с открытыми зонами роста назначают гидрокортизон внутрь в суточной дозе 10-15 мг/м2 поверхности тела в 3 приема в равных частях (в 600, 1400 и 2200);
-
подросткам с близкими к закрытию зонами роста назначают дексаметазон внутрь 0,25-0,35 мг/м2 1 раз в сутки (вечером) или преднизолон 2-4 мг/м2 в 2 приема (1/3 дозы в 600 и 2/3 в 2300);
-
при развитии сольтеряющего криза применяют гидрокортизон внутривенно 3-5 мг/кг каждые 4 ч до достижения возможности применения глюкокортикоидов внутрь;
-
при невозможности приема лекарств внутрь из-за тяжелых интеркуррентных заболеваний и хирургических вмешательств используют гидрокортизона ацетатx в виде суспензии внутримышечно 25 мг/м2 4 раза в сутки;
-
в случаях стрессовых ситуаций (интеркуррентные заболевания с лихорадкой, рвота, травмы, хирургические вмешательства, тяжелые физические нагрузки, экзамены) суточную дозу глюкокортикоидов увеличивают в 2-3 раза.
При купировании тиреотоксического криза внутривенно или внутримышечно назначают 100 мг водорастворимого гидрокортизона натрия сукцината 1-3 раза в сутки до купирования симптомов криза. В случае невозможности использования водорастворимого гидрокортизона применяют другие водорастворимые глюкокортикоиды для парентерального введения в эквивалентных дозах (например, эта доза соответствует 150 мг преднизолона).
В целях дифференциальной диагностики гиперкортицизма проводят пробы с дексаметазоном в двух вариантах, которые, в зависимости от используемых доз, называются «малая» (малые дозы) и «большая» (большие дозы). В первом случае назначают либо 1 мг дексаметазона однократно в 2400 с контролем кортизолемии наутро, либо 0,5 мг каждые 6 ч в течение 2 сут с определением во второй день суточной экскреции с мочой свободного кортизола. Во втором случае при тех же режимах используют соответственно дозу 8 мг и дозу 2 мг.
Пробы считаются положительными при снижении анализируемых показателей по сравнению с исходным уровнем на 50% и более (трактовку результатов см. в разделе «Показания к применению»).
Фармакодинамическая терапия
В зависимости от тяжести состояния используют различные пути введения и режимы дозирования (табл. 27.23).
При ежедневном приеме для уменьшения НЛР применяют хронотерапевтический подход: поскольку ГГНС наименее чувствительна к экзогенным глюкокортикоидам в ранние утренние часы, малые дозы препаратов назначают именно в это время (между 6 и 8 часами), а если величина дозы не допускает одноразовый прием, в 6-8 часов назначают 2/3 суточной дозы, а оставшуюся 1/3 - около полудня.
Более перспективны прерывистые (альтернирующая и интермиттирующая) схемы, когда за счет увеличения суточной дозы препарат применяют не каждый день. Они не только обеспечивают высокую эффективность и относительную безопасность лечения, но и позволяют со временем уменьшить дозу глюкокортикоидов. При пульсовых режимах дозирования эффективность еще больше возрастает, но при этом снижается безопасность.
Таблица 27.23. Режимы дозирования глюкокортикоидов при системной фармакодинамической терапии (по Young L.Y., Koda-Kimble М.А., 1995, в модификации)
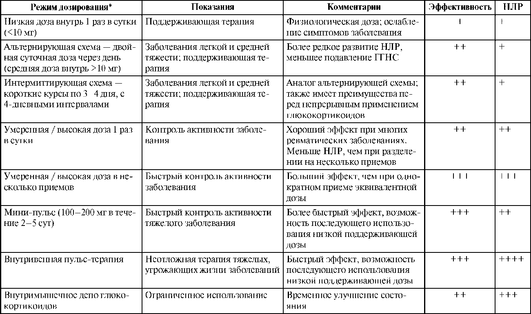
* В таблице рассмотрены дозы преднизолона; для других глюкокортикоидов пересчет осуществляется с использованием эквивалентных доз.
При различных патологических состояниях применяют глюкокортикоиды в различных суточных дозах, величина которых определяется видом проводимого лечения (табл. 27.24).
Таблица 27.24. Суточные дозы при различных видах лечения с применением глюкокортикоидов
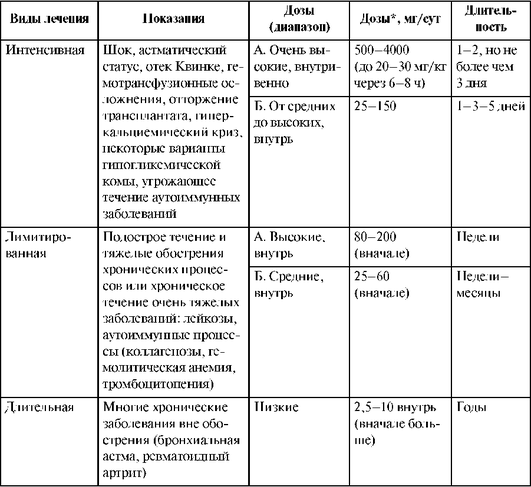
* В таблице рассмотрены дозы преднизолона; для других глюкокортикоидов пересчет осуществляется с использованием эквивалентных доз.
Проведение интенсивной терапии возможно как препаратами для внутривенного введения, так и для приема внутрь. Для преднизолона эти дозы относятся как 6/1 (необходимость применения более высоких доз при парентеральном введении обусловлена особенностями фармакокинетики глюкокортикоидов). Витальные показания к использованию высоких доз заставляют пренебрегать возможными осложнениями. При необходимости более или менее продолжительного применения высоких и средних доз длительность назначения глюкокортикоидов необходимо ограничить (лимитированная терапия). Длительная терапия низкими дозами, по сути, является поддерживающей. Однако дозы менее 5 мг преднизолона внутрь скорее всего выступают в качестве заместительной терапии и дают клинический эффект при атрофии коры надпочечников, вызванной продолжительным приемом глюкокортикоидов.
При любом режиме дозирования после достижения планируемого эффекта дозу глюкокортикоидов снижают до минимальной эффективной (поддерживающей) или препарат отменяют. Интенсивную терапию, проводимую в течение нескольких дней, следует прекращать сразу, без постепенного снижения дозы, поскольку при этом режиме торможение ГГНС развиться не успевает (см. ниже). Так, одно-, двух- или максимум 3-дневное применение очень высоких доз (до 20-30 мг/кг преднизолона через 6-8 ч внутривенно) или использование на протяжении нескольких суток (до 5-7 дней) доз от средних до высоких (25-150 мг/сут преднизолона внутрь) не требует постепенной отмены. Причем резкий обрыв терапии тем безопаснее, чем короче применение (величина дозы играет меньшую роль). В случаях длительного использования глюкокортикоидов лечение прекращают постепенно: скорость снижения суточной дозы определяется величиной самой дозы и патологическим процессом, послужившим причиной назначения препарата. Если при тяжелых формах ревматоидного артрита с высокой лихорадкой и висцеропатиями дозу преднизолона, достигающую 30-40 мг/сут, снижают на 2,5 мг (а при 15 мг/сут на 1,25 мг) каждые 5-7 дней, то при эозинофильном фасците дозу в 15-20 мг отменяют в течение 10-12 мес путем снижения на 1-2 мг/мес. Даже самая медленная схема прекращения лечения глюкокортикоидами не всегда предупреждает развитие синдрома отмены. Предварительный переход к прерывистым режимам дозирования облегчает последующую отмену препарата.
Местное применение глюкокортикоидов
Средства для наружного применения:
-
начинать лечение следует со слабых средств (см. табл. 27.19). При отсутствии эффекта в течение 2-3 нед переходят на более сильное лекарственное средство, а после достижения ожидаемого результата снова возвращаются к слабому глюкокортикоиду;
-
препараты IV класса («очень сильные») назначают только при тяжелых дерматозах;
-
ЛС наносят на чистую кожу тонким слоем, не втирая и не массируя, 2 раза в сутки. Длительно действующие мометазона фуроат® и флутиказона пропионатx наносят 1 раз в сутки, что удобно при длительном применении глюкокортикоидов (экзема, псориаз);
-
при поражении волосистой части головы следует применять гель или лосьон.
Средства для интраназального применения представлены в табл. 27.25.
Таблица 27.25. Режимы дозирования некоторых назальных глюкокортикоидов
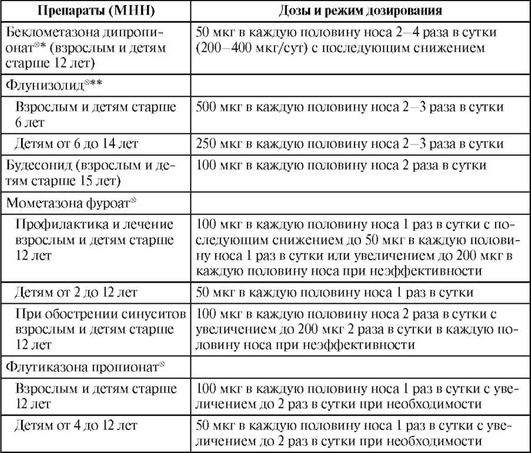
* Высшая суточная доза беклометазона дипропионатаx для взрослых - 1000 мкг, для детей старше 14 лет - 500 мкг.
** Высшая суточная доза флунизолидаx для взрослых и детей старше 14 лет - 2000 мкг в каждую половину носа, от 6 до 14 лет - 250 мкг в каждую половину носа 4 раза.
Средства для ингаляционного применения
Из ингаляционных глюкокортикоидов в настоящее время чаще всего применяют беклометазона дипропионатx (эталонный ингаляционный глюкокортикоид), будесонид, флутиказона пропионатx. Схемы применения ингаляционных глюкокортикоидов представлены в табл. 27.26.
Таблица 27.26. Режимы дозирования некоторых ингаляционных глюкокортикоидов
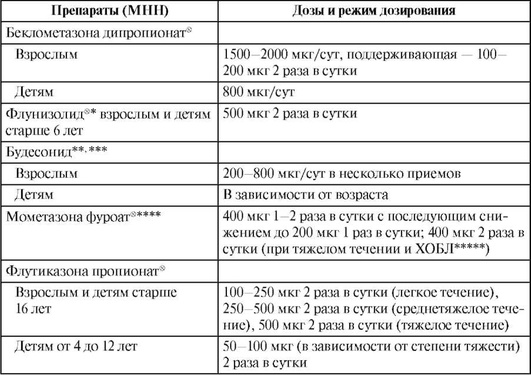
* Высшая суточная доза флунизолидаx для взрослых и детей старше 14 лет - 1000 мкг 2 раза в сутки, для детей от 6 до 14 лет - 500 мкг 2 раза в сутки, курс лечения - 4-6 нед.
** Дозы будесонида указаны для аэрозоля; для суспензии через небулайзер они больше, а для порошка из ингалятора «Турбухалер» меньше (о средствах доставки см. раздел «Лекарственные формы»).
*** Высшая суточная доза будесонида для взрослых - 1600-2000 мкг в 2-4 приема, для детей - 800 мкг в 2-4 приема.
**** Высшая суточная доза - 800 мкг.
***** В остальных случаях, разбираемых в таблице, речь идет преимущественно о бронхиальной астме.
Для увеличения части дозы препарата, достигающей бронхов, и уменьшения всасывания со слизистой оболочки полости рта, а следовательно, для увеличения эффективности и снижения системных НЛР следует применять спейсер[79] (в случае использования дозированных карманных ингаляторов) или небулайзер, для которого существуют специальные лекарственные формы. С целью снижения абсорбции, а также для профилактики местных НЛР после каждого сеанса следует полоскать водой рот и горло.
Нежелательные лекарственные реакции
Частота НЛР при применении глюкокортикоидов возрастает с увеличением дозы и (или) длительности лечения и составляет от 20 до 100%. Прерывистые схемы и местное применение (наружное, ингаляционное, внутрисуставное и др.) позволяют снизить риск осложнений применения глюкокортикоидов.
Метаболические и эндокринные нарушения
Подавление оси ГГНС: торможение секреции АКТГ - снижение функциональной активности коры надпочечников (вторичная надпочечниковая недостаточность) - атрофия коры (первичная надпочечниковая недостаточность) с отсутствием ее адекватной реакции на стресс (интеркуррентные заболевания, травмы, хирургические вмешательства, экзамены и т.п.), что проявляется как на фоне приема, так и в процессе или после отмены глюкокортикоидов.
К факторам риска развития надпочечниковой недостаточности относятся:
-
назначение таких суточных доз, которые превышают заместительные (более 3-5 мг в пересчете на преднизолон);
-
продолжение лечения в течение срока, при котором возможно подавление функции ГГНС (более 10-14 дней);
-
нарушение принципов хронофармакологии (назначение глюкокортикоидов в вечерние часы[80], неправильное распределение дозы в течение дня);
-
использование непрерывных схем назначения глюкокортикоидов[81];
-
применение фторированных глюкокортикоидов (т.е. препаратов длительного действия);
-
резкая отмена глюкокортикоидов после длительного применения.
Экзогенный синдром Кушинга, отдельные его проявления и некоторые другие осложнения применения глюкокортикоидов, встречающиеся изолированно или в сочетаниях:
-
повышение массы тела и диспластическое ожирение «кушингоидного типа» (наиболее ранний и часто встречающийся симптом) - перераспределение подкожного жира с конечностей на лицо («лунообразное» лицо), шею, верхнюю половину туловища (формирование «климактерического горбика), гиперлипидемия;
-
отрицательный азотистый баланс вследствие катаболизма белка, проявляющегося в частности:
-
миопатией - слабость и гипотрофия мышц, в первую очередь конечностей, а возможно, и дыхательных мышц (нарушения дыхания иногда требуют прекращения системного применения глюкокортикоидов, например, при бронхиальной астме), атрофия мышц передней брюшной стенки («лягушачий живот») и ягодиц («скошенные ягодицы»);
-
трофическими изменениями кожи: истончение, сухость, угри, склонность к гиперкератозу, багровоцианотичная окраска, особенно на лице («матронизм»), красно-фиолетовые стрии на бедрах, ягодицах, пояснице, животе, плечах;
-
-
нарушения углеводного обмена: гипергликемия, манифестация латентного сахарного диабета, стероидный диабет, гиперосмолярная кома;
-
нарушения водно-электролитного и минерального обмена: задержка натрия и воды, отеки, гипокалиемический алкалоз, потери магния и кальция с формированием остеопороза и угрозой патологических переломов;
-
синдром вегетативной дисфункции с преобладанием симпатико-адреналовой активности;
-
нарушения функции ССС: тахикардия, экстрасистолия, изменения конечной части желудочкового комплекса, ЭКГ, артериальная гипертензия, сердечная недостаточность;
-
асептический некроз трубчатых костей, обычно - головки бедренной кости;
-
нарушения функций половых гормонов: дис-, опсо- или аменорея, гирсутизм и гипертрихоз на груди у женщин, эректильная дисфункция и гинекомастия у мужчин, изменение темпов полового созревания у подростков;
Нарушения гемостаза
Повышенная ломкость сосудов кожи: кровоизлияния на коже (петехиальные высыпания).
Гиперкоагуляция: тромбозы.
Подавление иммунитета и клеточного деления
Снижение резистентности к инфекциям:
Основными возбудителями бактериальных инфекций оказываются стафилококки и кишечная группа.
На фоне глюкокортикоидов инфекционные процессы склонны к генерализации, затяжному течению, тканевому распаду и резистентности к специфическому лечению. Они могут протекать атипично («смазывание» клинической картины) в связи с противовоспалительным, анальгетическим и жаропонижающим эффектами.
Нарушение пролиферации и регенерации: замедление заживления ран и других дефектов кожи и слизистых оболочек.
Поражение желудочно-кишечного тракта и органов пищеварения
Желудок, кишечник: стероидные язвы располагаются не только в двенадцатиперстной кишке и (реже) в желудке, но и иногда в других отделах ЖКТ. Они отличаются бессимптомным течением («немые»), склонностью к кровотечениям и перфорациям. При этом желудочный дискомфорт, тошнота, другие диспепсические жалобы чаще не связаны с поражением слизистой оболочки, являясь результатом повышения секреции и нарушения моторики. Замена лекарственных форм для приема внутрь на парентеральные не уменьшает риск развития этих осложнений. Антисекреторные средства также не оказывают профилактического эффекта.
Пищевод: эзофагит.
Поджелудочная железа и брюшная полость: атипично протекающие панкреатит и перитонит.
Осложнения, касающиеся нервной системы, органов чувств и психоэмоциональной сферы.
Неврологические нарушения:
Поражение глаз:
Осложнения, обусловленные отменой глюкокортикоидов
Синдром отмены:
-
первый вариант - обострение заболевания, по поводу которого назначались глюкокортикоиды;
-
второй вариант - «псевдоревматизм» (легкая форма синдрома отмены), проявляющийся утомляемостью, эмоциональной нестабильностью, головной болью, потерей аппетита, бессонницей, тошнотой, миалгией;
-
третий вариант - «панмезенхимальная реакция» (тяжелая форма синдрома), проявляющаяся лихорадочным состоянием, генерализованными воспалительными реакциями (включая серозиты и легочные инфильтраты) с угрозой развития панартериита и системной красной волчанки;
-
различные клинические проявления острой и хронической надпочечниковой недостаточности.
Отсутствие адекватного ответа на стрессогенные факторы: в течение 6-12 мес после длительного применения даже малых доз глюкокортикоидов любые дополнительные нагрузки на ГГНС требуют назначения небольших доз глюкокортикоидов (2,5-5 мг преднизолона внутрь или до 25-30 мг внутривенно) в течение нескольких дней, причем в оптимальном варианте, начиная накануне планируемой стресс-ситуации.
Определенные НЛР при применении глюкокортикоидов чаще развиваются на свойственных им этапах их применения и при наличии различных дополнительных условий (табл. 27.27).
Таблица 27.27. Время и условия возникновения нежелательных лекарственных реакций при системном использовании глюкокортикоидов (по Boumpas D.T. et al., 1993, в модификации)
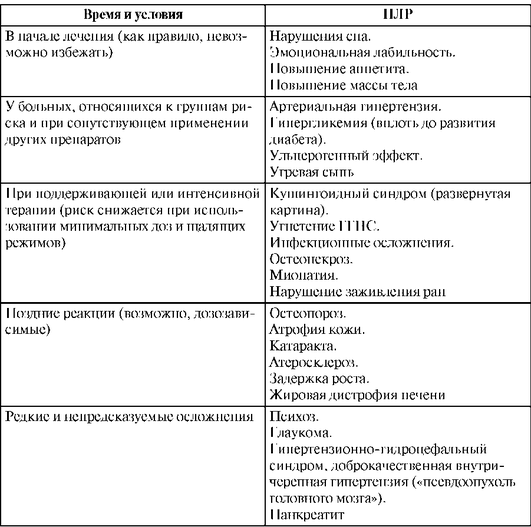
Осложнения, связанные с наружным применением глюкокортикоидов:
Осложнения, связанные с интраназальным применением глюкокортикоидов:
Передозировка
Применение избыточно высоких доз за короткое время может привести к появлению тошноты, рвоты, расстройств сна, эйфории, возбуждения, депрессии. При длительном использовании высоких доз развиваются остеопороз, задержка жидкости, повышение АД и другие проявления синдрома Кушинга, а также вторичная надпочечниковая недостаточность за счет подавления ГГНС.
Лечение: на фоне постепенной отмены препарата поддержание жизненно важных функций, коррекция электролитного баланса, антациды, фенотиазины, препараты лития; при синдроме Кушинга - аминоглутетимидx.
Чрезмерное и продолжительное использование глюкокортикоидов для местного применения может вызвать подавление гипофизарно-адреналовой функции, ведущее к вторичной адреналовой недостаточности.
Лекарственное взаимодействие
Фармакокинетическое взаимодействие
Средства, потенцирующие эффекты глюкокортикоидов, увеличивая их концентрацию или длительность жизни, - лекарственные вещества, тормозящие биотрансформацию глюкокортикоидов в печени (например, эритромицин) или конкурирующие с глюкокортикоидами за сывороточный альбумин (например, салицилаты и другие НПВС, эстрогены), увеличивая их свободную циркулирующую фракцию глюкокортикоидов, усиливают их эффекты.
Средства, ослабляющие эффекты глюкокортикоидов, - индукторы микросомальных ферментов печени (например, барбитураты, фенитоин, рифампицин и др.), снижают эффекты глюкокортикоидов, усиливая их печеночную биотрансформацию.
Фармакодинамическое и фармакологическое взаимодействие
-
Средства, эффекты которых (в том числе и НЛР):
-
потенцируют действие глюкокортикоидов: бронходилататоры (β2-агонисты и другие адреномиметики, теофиллин и аминофиллин, м-холиноблокаторы), цитостатики и иммуносупрессоры, НПВС, нортриптилинx, средства, повышающие АД (кардиотонические ЛС, включая катехоламины);
-
усиливают токсические эффекты глюкокортикоидов: салуретики (однонаправленное влияние на обмен электролитов и минералов), сердечные гликозиды (за счет гипокалиемии), препараты золота;
-
ослабляют действие глюкокортикоидов: антигистаминные препараты, ретинол.
-
-
Средства, эффекты которых ослабляются при одновременном применении с глюкокортикоидами: сахароснижающие ЛС, антикоагулянты, антигипертензивные ЛС, препараты золота, наркотические средства, вакцины, иммунные диагностические препараты (например, аллергены бактерий).
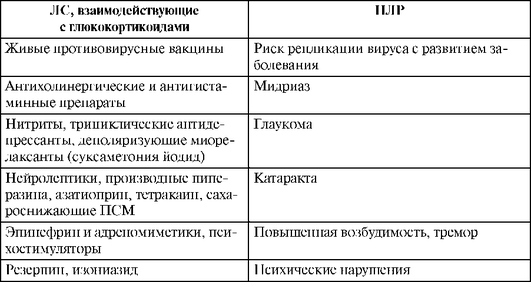
В результате лекарственного взаимодействия может развиться ряд осложнений применения глюкокортикоидов (табл. 27.28).
Таблица 27.28. Взаимодействия глюкокортикоидов с некоторыми лекарственными препаратами
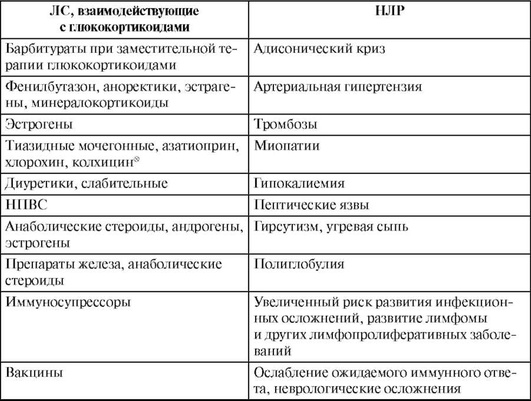
Окончание табл. 27.28
Взаимодействие с алкоголем
Глюкокортикоиды ослабляют действие алкоголя. Алкоголь увеличивает риск ульцерогенного эффекта.
Особые указания
Глюкокортикоидные препараты для системного применения
До начала и во время применения глюкокортикоидов следует контролировать состояние периферической крови (клинический анализ крови), гликемию и глюкозурию, содержание электролитов в сыворотке.
Если во время применения глюкокортикоидов развиваются интеркуррентные инфекции или септические состояния, необходимо присоединить лечение соответствующими антибактериальными средствами. Детям, находившимся в период получения глюкокортикоидов в контакте с больными корью или ветряной оспой, профилактически назначают специфические иммуноглобулины.
Необходимо учитывать, что у пациентов с гипотиреозом клиренс глюкокортикоидов снижается, а с тиреотоксикозом - повышается.
Минимальные дозы глюкокортикоидов во всех выпускаемых лекарственных формах для системного применения (и для приема внутрь, и для парентерального введения) всех ЛС взаимоэквивалентны (исключение составляют кортизона ацетатx и гидрокортизона ацетатx, выпускаемые во флаконах, содержащих 10 и около 2-2,5 эквивалентных доз соответственно).
Глюкокортикоидные препараты для наружного применения
«Сильные» и «очень сильные» наружные глюкокортикоиды нельзя использовать в области лица и наружных половых органов, где высокая абсорбционная способность кожи создает условия для развития системных эффектов, а высокая местная активность глюкокортикоидов может приводить к поражению кожи.
Наносить на кожу препараты «очень сильные» и «сильные» рекомендуется в перчатке.
Для усиления лечебного эффекта (например, при псориазе) на участки кожи с нанесенным препаратом можно кратковременно накладывать окклюзионные повязки (не более чем в течение 2 сут).
При необходимости быстрого эффекта предпочтительнее использовать кремы, а при хронических процессах - мази, поскольку из последних лекарственное вещество высвобождается, как правило, медленнее.
Глюкокортикоидные препараты для интраназального применения
При долгосрочном лечении интраназальными лекарственными формами глюкокортикоидов (в течение нескольких месяцев и более) следует периодически проводить осмотры полости носа для выявления возможных изменений слизистой оболочки.
Эффективность, безопасность и переносимость интраназальных глюкокортикоидных препаратов во многом зависят от используемой системы их доставки в полость носа. Из интраназальных лекарственных форм глюкокортикоидов наиболее широко применяют дозированные аэрозоли и назальные спреи. Безусловно, более предпочтительно применение спреев, поскольку при высокой эффективности они реже вызывают местные осложнения в виде чиханья, сухости, зуда и жжения в носу, так как, в отличие от аэрозолей, они не содержат фреон.
Благодаря низким дозам риск воздействия на ГГНС минимален.
Интраназальное применение глюкокортикоидов у детей не вызывает задержки роста.
При многократном назначении глюкокортикоидов к ним может развиться устойчивость тканей (толерантность), что проявляется тахифилаксией, т.е. прогрессивным уменьшением клинической эффективности применяемых препаратов с потребностью увеличения дозы. Этот эффект особенно часто наблюдается при местном применении глюкокортикоидов, которое обеспечивает наибольшие концентрации лекарственных веществ в зонах воздействия. В связи с этим для сохранения или восстановления чувствительности тканей рекомендуется прерывать длительное применение местных глюкокортикоидов.
Лекарственные формы
Для системного применения: таблетки, растворы для инъекций, суспензии для внутримышечного введения[82] (табл. 27.29).
Для наружного применения: мази, кремы, гели и лосьоны.
Для интраназального применения: капли, дозированные аэрозоли, назальные спреи.
Таблица 27.29. Лекарственные формы отдельных глюкокортикоидов
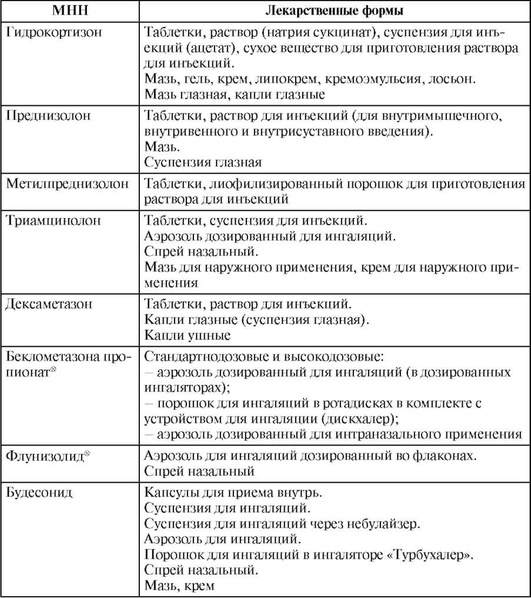
Окончание табл. 27.29

Для ингаляционного применения: аэрозоли (спреи) для ингаляций дозированные - в карманных дозированных ингаляторах (баллонах аэрозольных с клапаном дозирующего действия), суспензии для ингаляций дозированные (через небулайзер[83]), порошок для ингаляций дозированный с дозирующими устройствами (ингалятором «Турбухалер»[84] либо в ротадисках с дискхалером[85]).
Контрольные вопросы и задание
-
Чем различаются механизмы действия пероральных гипогликемических средств?
-
Как осуществлять контроль за эффективностью при проведении фармакотерапии у пациентов с сахарным диабетом 1-го и 2-го типа?
-
Как осуществлять контроль за безопасностью при проведении фармакотерапии у пациентов с сахарным диабетом 1-го и 2-го типа?
-
Какие НЛР могут вызвать препараты гормонов щитовидной железы?
Приложения
Материал размещен в электронной версии учебника, код доступа к которой указан на первом форзаце книги.