Пищевая аллергия у детей и взрослых : клиника, диагностика, лечение
Пищевая аллергия у детей и взрослых . Клиника, диагностика, лечение / Д. Ш. Мачарадзе. - Москва : ГЭОТАР-Медиа, 2020. - 392 с. - 392 с. - ISBN 978-5-9704-5501-2 |
Аннотация
Книга содержит последние эпидемиологические и иммунопатологические данные, касающиеся особенностей пищевой аллергии у детей и взрослых, характера клинического течения болезни. Предложен рациональный, научно обоснованный подход к ее диагностике (алгоритмы обследования пациентов, включая компонентную аллергодиагностику), а также новые задачи лечения и профилактики пищевой аллергии. Описаны особенности дифференциальной диагностики данной болезни, рассмотрен вопрос о взаимосвязи пищевой аллергии с атопическим дерматитом, изложены особенности диагностики и терапии эозинофильного эзофагита, роль пищи в поддержании контактного дерматита на металл (никель), а также особенности реакций на алкоголь. Издание предназначено для аллергологов-иммунологов, гастроэнтерологов, дерматологов, педиатров, терапевтов, врачей общей практики.
ГЭОТАР-Медиа
ПА не имеет общепринятого определения. Этим термином обозначают иммуноопосредованный ответ организма на пищевой продукт [1]. В Национальном руководстве Японии [2] ПА определена как «феномен, при котором у человека в ответ на прием пищевых продуктов возникают побочные реакции (симптомы на коже и слизистой оболочке, в пищеварительной, респираторной системах, анафилаксия), опосредованные иммунологическими механизмами». Согласно заключению экспертов Национального института аллергии и инфекционных заболеваний США [3], ПА - это неблагоприятные реакции, связанные со специфическим иммунным ответом организма на пищевые продукты.
Все определения включают несколько типов ПА в зависимости от иммунопатофизиологических механизмов их развития: IgE-зависимую, не-IgE-зависимую, или клеточно-опосредованную, а также смешанную форму иммунных реакций - не всегда (не только) IgE-зависимую (табл. 1-1) [1-4].
| Орган-мишень | IgE-опосредованный тип | Смешанный тип | Не-IgE-опосредованный тип |
|---|---|---|---|
Гастроинтестинальный тракт |
Немедленная гастроинтестинальная гиперчувствительность |
Эозинофильный гастроэнтероколит |
Синдром энтероколита, индуцированный пищевыми протеинами |
Оральный аллергический синдром (ОАС) |
- |
Синдром проктоколита, индуцированный пищевыми протеинами |
|
Энтеропатия, индуцированная пищевыми протеинами Целиакия |
|||
Кожа |
Крапивница. Отек Квинке |
АтД |
Герпетиформный дерматит (ГД) |
Респираторный тракт |
Аллергический ринит |
БА |
Легочный гемосидероз, индуцированный пищей (синдром Гейнера) |
Системная реакция |
Aнафилаксия |
- |
- |
Неблагоприятные реакции на пищу, которые не опосредованы IgE, не считаются ПА. Примерами, по заключению американских экспертов, могут служить метаболические (непереносимость лактозы или недостаток ферментов в результате нарушения функции поджелудочной железы или печени); токсические реакции [например, скумброидоз - отравление скомбротоксином, или сигуатера - отравление токсином зараженных рифовых рыб (сигуатоксином)]; фармакологическое действие ряда активных веществ пищевых продуктов (например, гистамина - в вине, тирамина - в сыре, кофеина и теобромина - в кофе и чае) (рис. 1-1) [3].
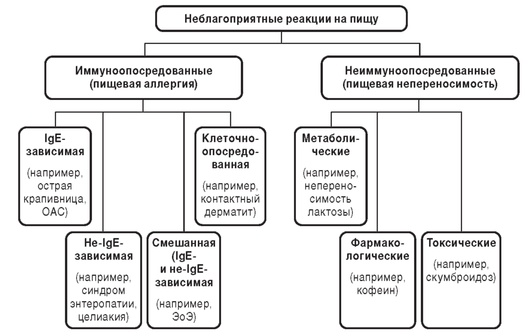
Как правило, IgE-опосредованная ПА характеризуется острым началом: обычно в интервале от нескольких минут до 2 ч у больного появляются кожные (крапивница, отек Квинке, обострение АтД/экземы), гастроинтестинальные (тошнота, рвота, диарея) и (или) респираторные симптомы. Эта категория включает также ОАС, который связан с употреблением сырых фруктов и овощей у людей, страдающих в основном аллергией на пыльцу.
В наиболее тяжелой форме IgE-опосредованная ПА проявляется как анафилаксия. Иногда последняя возникает только при условии сочетания приема пищи и физических упражнений - так называемая пищевая анафилаксия, индуцированная физической нагрузкой.
Не-IgЕ-опосредованные реакции характеризуются отсроченным началом и длительными симптомами, обычно со стороны желудочно-кишечного тракта (ЖКТ). К ним относят синдром проктоколита, индуцированный пищевыми протеинами (в литературе применяется также термин «аллергический проктоколит»), ГД, легочный гемосидероз (синдром Гейнера) и целиакию.
Смешанные расстройства патофизиологически включает IgE-и Т-клеточно-опосредованные болезни с хроническим рецидивирующим течением - так называемая эозинофильная гастроэнтеропатия, или гастроинтестинальный синдром, индуцированный пищевыми протеинами: эозинофильный гастроэнтероколит («аллергический гастроэнтероколит»), а также ЭоЭ [1, 3].
Патофизиология эозинофильных гастроинтестинальных заболеваний изучена недостаточно; для них характерным является такой морфологический признак, как плотная эозинофильная инфильтрация различных слоев ЖКТ. ЭоЭ встречается сравнительно чаще, чем эозинофильный проктоколит и эозинофильный гастроэнтерит.
Первые сообщения об ЭоЭ появились в 90-е годы прошлого века. У большинства таких больных обнаруживают сенсибилизацию к пищевыми (или) даже ингаляционным аллергенам, однако, является ли это достоверной причиной заболеваний, неясно. Несмотря на четко сформированные диагностические критерии, российские врачи редко диагностируют в своей практике у больных ЭоЭ. Недостаточная осведомленность клиницистов (и прежде всего педиатров и гастроэнтерологов) становится причиной гиподиагностики других состояний (например, синдрома энтероколита/проктоколита, индуцированного пищевыми протеинами и т.п.). Эту группу потенциально серьезных, не-IgЕ-опосредованных гастроинтестинальных заболеваний чаще вызывают коровье молоко, соя, реже - другие продукты (рис, овсяная крупа, фрукты или овощи) [5, 6]. До сих пор точная распространенность данной патологии неизвестна. По данным Y. Katz и соавт. [7], из 13 тыс. обследованных младенцев у 0,34% на первом году жизни отмечался энтероколит, индуцированный протеинами молока (это почти сопоставимо с 0,5% детей, страдающих IgE-опосредованной аллергией на белки коровьего молока).
В литературе опубликована отдельная классификация гастроинтестинальной формы ПА (табл. 1-2) [8].
| IgE-опосредованная ПА | Смешанная (не-IgE/IgE-опосредованная) ПА | Не-IgE-опосредованная ПА |
|---|---|---|
Гастроинтестинальная реакция гиперчувствительности немедленного типа |
Аллергический ЭоЭ |
Синдром энтероколита, индуцированный пищевыми протеинами |
Аллергический эозинофильный гастрит |
Аллергическая энтеропатия |
|
ОАС |
Аллергический эозинофильный гастроэнтероколит |
Аллергический проктоколит |
К группе смешанных заболеваний относят также АтД, при котором примерно у 35% детей со среднетяжелой или тяжелой формой болезни обнаруживают ПА [1-4].
Таким образом, первым шагом на пути установления правильного диагноза и выбора лечения ПА становится способность врача вовремя распознать патофизиологические механизмы, задействованные в ее развитии. Поскольку ПА представляет собой гетерогенную группу заболеваний, незнание данных механизмов и отсутствие результатов клинико-лабораторных исследований однозначно приведут к полному слиянию таких понятий, как ПА и, например, эозинофильный гастроинтестинальный синдром (табл. 1-1-1-3), что, в свою очередь, напрямую повлияет на исход лечения. Кроме того, следует четко отграничивать значение ранее распространенного термина «пищевая гиперчувствительность» от истинной IgE-опосредованной ПА. Напомним, что термин «пищевая гиперчувствительность» используется для описания любой неблагоприятной реакции на пищу [9].
По последним данным, пищевые расстройства, связанные с употреблением алкоголя и наркотических препаратов, составляют около 1,2%. Пищевая аверсия - еще одна распространенная причина таких расстройств. Так, в одном из недавних исследований родители 1090 детей при опросе сообщили, что в 51% случаев их ребенок избегал приема определенных продуктов питания, 23% указали, что дети ели избирательно, а 26% - что они вообще отказывались от новой пищи [10].
На данный момент, пожалуй, наиболее полно клинические проявления и механизмы развития ПА отражает классификация, разработанная в Японии (см. табл. 1-3) [2].
| Клинический тип | Возрастная группа | Основные продукты | Развитие толерантности (ремиссии) | Вероятность развития анафилаксии | Механизмы развития ПА |
|---|---|---|---|---|---|
Гастроинтестинальная аллергия новорожденных и детей раннего возраста |
Новорожденные, дети раннего возраста |
Коровье молоко (сухое молоко для младенцев), соя, рис |
+ |
± |
В основном не-IgE-опосредованный тип |
АтД, ассоциированный с ПА* |
Дети раннего возраста |
Яйца, коровье молоко, пшеница, соя и др. |
+ Во многих случаях |
+ |
В основном IgE-опосредованный тип |
Немедленный тип (крапивница, анафилаксия и т.д.) |
Дети раннего возраста - взрослые |
У младенцев и детей: яйца, коровье молоко, пшеница, гречиха, рыба и т.д. У школьников и взрослых: ракообразные, креветки, моллюски, рыба, пшеница, фрукты, гречка, арахис и т.д. |
Яйца, коровье молоко, пшеница, соя и т.д. |
++ |
IgE-опосредованный тип |
Конкретный тип. Пищевая анафилаксия, индуцированная физической нагрузкой |
Дети школьного возраста, взрослые |
Пшеница, креветки, кальмары и т.д. |
± |
+++ |
IgE-опосредованный тип |
ОАС |
Дети - взрослые |
Фрукты, овощи и т.д. |
± |
+ |
Примечание. * Иногда осложняется такими симптомами, как хроническая диарея, гипопротеинемия. Не всегда в развитии АтД у детей раннего возраста участвуют пищевые аллергены.
СПИСОК ЛИТЕРАТУРЫ
-
Burks А., Tang М., Sicherer S. et al. ICON: Food allergy // J. Allergy Clin. Immunol. - 2012. - Vol. 129. - P. 906-920.
-
Urisu A., Ebisawa M., Mukoyama T. et al. Japanese guideline for food allergy // Allergol. Int. - 2011. - Vol. 60. - P. 221-236.
-
Boyce J., Assa’ad A., Burks A. et al. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID-sponsored expert panel // J. Allergy Clin. Immunol. - 2010. - Vol. 126. - N 6. - Suppl. - P. S1-S58.
-
Sampson H., Aceves S., Bock A. et al. Food allergy: A practice parameter update - 2014 // J. Allergy Clin. Immunol. - 2014. - Vol. 134. - P. 1016-1025.
-
Motala C. Gastrointestinal syndromes in food allergy // Curr. Allergy Clin. Immunol. - 2008. - Vol. 21. - P. 76-79.
-
Dellon E., Gonsalves N., Hirano I. et al. ACG clinical guideline: evidenced based approach to the diagnosis and management of esophageal eosinophilia and eosinophilic esophagitis (EoE) // Am. J. Gastroenterol. - 2013. - Vol. 108. - P. 679-692.
-
Katz Y., Goldberg M., Rajuan N. et al. The prevalence and natural course of food protein-induced enterocolitis syndrome to cows milk // J. Allergy Clin. Immunol. - 2011. - Vol. 127. - P. 647-653.
-
Lee B., Aw M., Chiang W. et al. Academy of Medicine, Singapore - Ministry of Health Clinical Practice Guidelines: management of food allergy // Singapore Med. J. - 2010. - Vol. 51. - P. 599-607.
-
Johansson S., Hourihane J., Bousquet J. et al. A revised nomenclature for allergy. An EAACI position statement from the EAACI nomenclature task force // Allergy. - 2001. - Vol. 56. - P. 813-824.
-
Equit M., Pälmke M., Becker N. et al. Eating problems in young children - a population-based study // Acta Paediatr. - 2013. - Vol. 102. - P. 149-155.