Российские клинические рекомендации. Ревматология / Е. Л. Насонов - Москва : ГЭОТАР-Медиа, 2017. - 464 с. - ISBN 978-5-9704-4261-6 |
Аннотация
Издание содержит клинические рекомендации по наиболее распространенным ревматическим заболеваниям и синдромам, подготовленные Ассоциацией ревматологов России. Они детально описывают действия врача по диагностике, лечению, профилактике и реабилитации. Соблюдение международной методологии при подготовке клинических рекомендаций гарантирует их современность, достоверность, обобщение лучшего мирового опыта и знаний, применимость на практике. Поэтому клинические рекомендации имеют преимущества перед традиционными источниками информации (учебники, монографии, руководства) и позволяют врачу принимать обоснованные клинические решения. Клинические рекомендации по ревматологии предназначены практикующим врачам-ревматологам, терапевтам, врачам всех специальностей, студентам старших курсов медицинских вузов.
ВВЕДЕНИЕ
По современной классификации РЗ относятся к континууму ИВРЗ человека, в патогенезе которых ключевую роль играют аутоиммунитет и аутовоспаление, связанные с генетически детерминированными и индуцированными факторами внешней среды (инфекциями, курением и др.), дефектами активации приобретенного и врожденного иммунного ответа.
Материалы российских, международных (EULAR, ACR) и национальных рекомендаций по лабораторной диагностике ИВРЗ, основанных на принципах доказательной медицины, обеспечивают оптимальное применение лабораторных тестов для ранней диагностики, оценки активности, тяжести течения, прогноза болезни и эффективности терапии. Доказано, что среди лабораторных биомаркеров ИВРЗ наибольшее клиническое значение имеют аутоантитела и острофазовые биомаркеры. Однако в реальной практике показатели диагностической чувствительности и специфичности лабораторных биомаркеров могут отличаться от таковых при исследовании специально отобранных групп пациентов и здоровых лиц. Поскольку большинство иммунологических лабораторных тестов имеют недостаточную специфичность, назначение и оценку результатов лабораторных исследований следует проводить в строгом соответствии с предполагаемым диагнозом и данными тщательного клинического исследования больных. Актуальной проблемой лабораторной диагностики ИВРЗ является стандартизация и клиническая валидация новых высокопроизводительных иммунологических и молекулярно-биологических методов определения биомаркеров, основанных на использовании автоматизированных систем и мультиплексных технологий.
ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
Биомаркер (биологический маркер) - исследуемый параметр, измерение которого отличается высокой точностью и воспроизводимостью, что позволяет оценить состояние здоровья, и/или степень риска, или факт развития заболевания, его стадию и прогноз.
Аутоантитела - антитела, способные взаимодействовать с антигенами собственного организма.
ДИАГНОСТИКА
Цели лабораторной диагностики ИВРЗ.
Основные цели: подтверждение диагноза заболевания, оценка активности и характера иммунопатологического процесса и на этой основе прогнозирование исходов и характеристика эффективности проводимой терапии.
Оценка клинической информативности лабораторных исследований.
Клиническая информативность лабораторных исследований определяется путем расчета диагностической чувствительности и специфичности, соотношения правдоподобия положительных и отрицательных результатов.
Лабораторные биомаркеры ИВРЗ.
Центральное место в лабораторной диагностике ИВРЗ занимают серологические тесты на обнаружение циркулирующих органонеспецифических аутоантител в сыворотках (или других биологических жидкостях) больных. Положительные результаты определения аутоантител:
При ИВРЗ определение аутоантител проводится в первую очередь в целях подтверждения диагноза у пациентов, в том числе с недостаточным числом клинических критериев заболевания.
-
Обнаружение аутоантител при отсутствии клинических признаков не является достаточным для постановки диагноза аутоиммунного заболевания.
-
Характерно нарастание частоты выявления аутоантител у лиц пожилого и старческого возраста, на фоне приема лекарственных препаратов, при вирусных и бактериальных инфекциях, злокачественных новообразованиях, у здоровых родственников больных аутоиммунными заболеваниями.
-
При оценке клинического значения аутоантител необходимо учитывать стойкость и выраженность их гиперпродукции.
-
При инфекциях наблюдается умеренное транзиторное образование аутоантител, а при ИВРЗ - стойкая выраженная гиперпродукция.
-
-
Аутоантитела, специфичные только для одного ИВРЗ, встречаются очень редко.
-
Для ИВРЗ характерна одномоментная гиперпродукция нескольких типов аутоантител, так называемый профиль аутоантител, который используется для диагностики ИВРЗ (табл. 17.1; рис. 17.1).
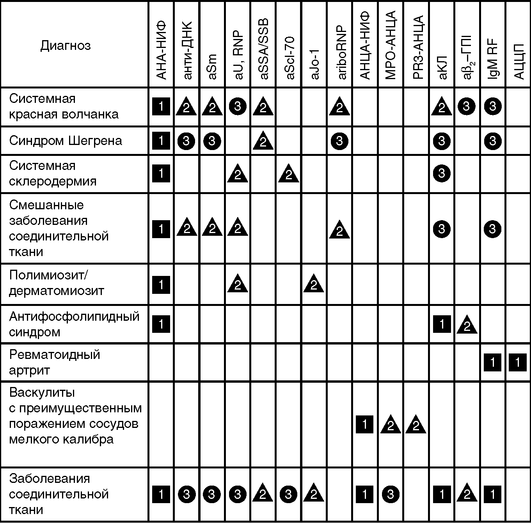
Рис. 17.1. Алгоритм лабораторной диагностики иммуновоспалительных ревматических заболеваний: 1 - первичные скрининговые тесты; 2 - подтверждающие тесты; 3 - дополнительные тесты. Добавить подтверждающие тесты для диагностики ССД (антицентромерные антитела, антитела к РНК-полимеразе-3), ПМ/ДМ (антитела к аминоацилсинтетазам т-РНК, SRP, Mi-2, PM-Scl, Ku) и АФС (волчаночный антикоагулянт)
Таблица 17.1. Стандартные профили аутоантител для диагностики иммуновоспалительных ревматических заболеваний
| Заболевание | Профиль |
|---|---|
СКВ |
АНФ, антитела, реагирующие с нативной ДНК, aSm, аКо/SS-A, aLa/SS-B, антитела к рибонуклеопротеину, аКЛ, aC1q, проба Кумбса |
РА |
IgM/IgA РФ, АЦБ (АЦЦП, антитела к модифицированному цитруллинированному виментину) антитела к Ra 33, BiP (P-68) |
АФС |
IgG/IgM аКЛ, IgG/IgM-антитела к β2-гликопротеину I, ВА |
ССД |
аБе1-70, антицентромерные антитела, антинуклеарные антитела (к aTh/ To, аРНК-полимеразе III, aPM-Scl, aU1 рНП, фибрилларину - aU3 рНП) |
ПМ/ДМ |
Антитела к аминоацилсинтетазам тРНК - Jo-1, PL-7, PL-12, EJ, OJ, KS; антитела к SRP, Mi-2, PM-Scl, KJ |
СВ |
АНЦА с цитоплазматическим типом иммунофлюоресцентного свечения, АНЦА с перинуклеарным типом свечения, антитела к протеиназе-3 и миелопероксидазе |
Основными диагностическими лабораторными маркерами ИВРЗ являются (рис. 17.2): антинуклеарные антитела; РФ; АЦБ; АНЦА; аФЛ (уровень доказательности А).
Для оценки активности воспаления, характера прогрессирования и прогноза исходов ИВРЗ, а также эффективности противовоспалительной терапии наибольшее клиническое значение имеет определение СОЭ и содержания СРБ.
Другие лабораторные биомаркеры ИВРЗ (цитокины, маркеры активации эндотелия, Ig, иммунные комплексы, криоглобулины, компоненты системы комплемента, субпопуляции лимфоцитов, генетические маркеры, показатели метаболизма костной и хрящевой тканей, маркеры апоптоза и др.) имеют меньшее клиническое значение по сравнению с аутоантителами и показателями острой фазы воспаления. Они могут быть полезными для мониторирования активности заболевания и прогнозирования эффективности проводимой терапии, но их не рекомендуется использовать в клинической практике.
Общие рекомендации по кратности определения аутоантител.
При определении кратности исследований лабораторных биомаркеров должны учитываться следующие факторы.
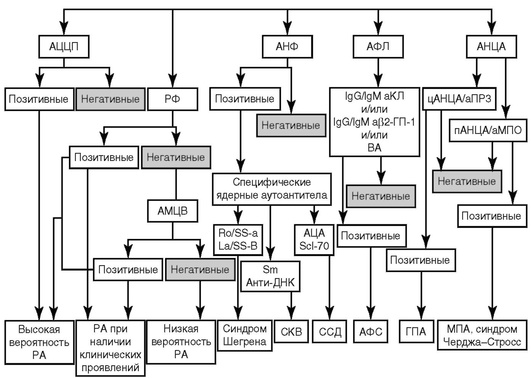
Рис. 17.2. Диагностическое значение аутоантител при иммуновоспалительных ревматических заболеваниях
Аутоантитела
Антинуклеарные антитела
Антинуклеарные антитела - гетерогенная группа аутоантител, реагирующих с различными компонентами ядра.
-
«Золотым стандартом» для первичного скрининга больных на антинуклеарные антитела в сыворотке крови является НРИФ с использованием в качестве субстрата криостатных срезов мышиной или крысиной печени (почек) либо клеток линии HEp-2 (Human Epithelial Type - эпителиальные клетки рака гортани человека).
-
При тестировании на антинуклеарные антитела методом НРИФ их традиционно обозначают как АНФ.
-
Оценка результатов НРИФ проводится с указанием максимального титра обнаружения АНФ в исследуемых сыворотках, а также интенсивности и типа иммунофлюоресценции.
-
Характер свечения отражает присутствие различных типов антинуклеарных антител, в определенной степени специфичных для ряда аутоиммунных ИВРЗ (уровень доказательности А).
-
Другие методы определения антинуклеарных антител [ИФА, иммуно-блоттинг (ИБ), новые методы твердофазного анализа, включая мультиплексные диагностические платформы на основе микрочастиц], устанавливающие наличие в сыворотках антител к смеси ядерных антигенов, увеличивают процент ложноотрицательных и ложноположительных результатов и не могут заменить тестирование АНФ с помощью НРИФ (уровень доказательности А).
-
У пациентов с положительными результатами определения АНФ рекомендуется проведение подтверждающих тестов на специфические антинуклеарные антитела к отдельным ядерным антигенам.
-
Некоторые типы антинуклеарных антител [антицентромерные, антитела к ядерному антигену пролиферирующих клеток (proliferating cell nuclear antigen; PCNA), антитела к митотическому аппарату клетки (nuclear mitotic apparatus; NUMA)] обнаруживаются только методом НРИФ на HEp-2-клетках.
-
Некоторые типы антител к экстрагируемым ядерным антигенам, в частности антитела к SS-A/Ro, рибосомальному белку P и Jo-1, не выявляются методом НРИФ-Hep-2.
Клиническое значение.
-
Тестирование АНФ очень полезно для диагностики СКВ (положительные результаты обнаружения АНФ служат диагностическим критерием СКВ) (уровень доказательности А) и ССД (уровень доказательности А), полезно для диагностики СШ, ассоциирующегося с СКВ (уровень доказательности А), и менее полезно для диагностики ПМ/ДМ (уровень доказательности А).
-
Позитивность по АНФ рассматривается в качестве диагностического критерия лекарственной волчанки, системных заболеваний соединительной ткани, аутоиммунного гепатита (уровень доказательности А).
-
АНФ является очень полезным маркером для оценки прогноза и мониторинга течения ювенильного хронического артрита в сочетании с увеитом (уровень доказательности А) и вторичного феномена Рейно, ассоциирующегося с системными РЗ (уровень доказательности А).
-
Положительные результаты определения АНФ не имеют доказанного диагностического и прогностического значения при РА, рассеянном склерозе, заболеваниях щитовидной железы, инфекциях, идиопатической тромбоцитопенической пурпуре и фибромиалгии (уровень доказательности А).
Показания к определению антинуклеарных антител.
Антитела к дезоксирибонуклеиновой кислоте
Антитела к ДНК подразделяются на два основных типа: антитела, реагирующие с двуспиральной (нативной) ДНК, и антитела, реагирующие с односпиральной (денатурированной) ДНК.
-
Антитела к ДНК являются серологическим маркером СКВ. Антитела к двуспиральной ДНК более специфичны для диагностики СКВ, чем антитела к односпиральной ДНК, которые присутствуют в сыворотках больных при других ИВРЗ и не имеют существенного диагностического значения (уровень доказательности А).
-
Стандартными методами определения антител к двуспиральной ДНК в сыворотке крови служат ИФА, НРИФ с использованием в качестве субстрата Crithidia luciliae и радиоиммунный анализ (РИА; тест Farr) (уровень доказательности А). Первичным скрининговым тестом для обнаружения антител к двуспиральной ДНК является метод ИФА (уровень доказательности А).
Клиническое значение.
-
Тестирование антител к двуспиральной ДНК очень полезно для диагностики СКВ у пациентов с положительными результатами определения АНФ (уровень доказательности А).
-
Наличие антител к двуспиральной ДНК является обязательным диагностическим критерием СКВ.
-
Определение антител к двуспиральной ДНК при СКВ полезно для оценки активности патологического процесса и поражения почек.
Антитела к гистонам
Гистоны - основные белковые компоненты ядра клетки, которые подразделяются на пять классов (Н1, Н2А, Н2В, Н3, Н4).
Клиническое значение.
Антитела к нуклеосомам
Антитела к нуклеосомам (антихроматиновые антитела, антитела к дезоксинуклеопротеину) взаимодействуют с эпитопами комплекса Н2А-Н2В-ДНК.
Клиническое значение.
-
Определение IgG-антител к нуклеосомам может быть полезно для диагностики СКВ (уровень доказательности С) и лекарственной волчанки, индуцированной новокаинамидом (уровень доказательности С).
-
Обнаружение антител к нуклеосомам ассоциируется с поражением почек при СКВ (уровень доказательности С) и развитием аутоиммунного гепатита типа 1 (уровень доказательности С).
Антитела к Sm-антигену (Smith)
Sm-антиген состоит из пяти малых ядерных (мя) РНК (U1, U2, U4, U5, U6), связанных с 11 полипептидами и более (70 kd, A, B/B', C, C', D, E, F, G). При СКВ антитела к Sm реагируют с B/B'- и D-полипептидами, общими для U1, U2, U4/U6 малых ядерных рибонуклеопротеинов, участвующих в сплайсинге предшественника матричной РНК (пре-мРНК).
Клиническое значение.
Антитела к рибонуклеопротеину U1
Антитела к рибонуклеопротеину U1 реагируют с белковыми компонентами (70 кДа) U1 малого ядерного рибонуклеопротеина.
Клиническое значение.
-
Выявление антител к рибонуклеопротеину U1 в высоких титрах полезно для диагностики системных заболеваний соединительной ткани (уровень доказательности А), менее полезно для диагностики СКВ (уровень доказательности В).
-
Выявление антител к рибонуклеопротеину U1 полезно для прогнозирования неблагоприятного течения СКВ с развитием тяжелого поражения внутренних органов (уровень доказательности В).
-
В сыворотках 60% больных с положительными результатами определения антител к рибонуклеопротеину U1 выявляются антитела к Sm.
Антитела к SS-A/Ro (Robert)
SS-A/Ro-антигены - полипептиды с молекулярной массой 60 и 52 кДа, образующие комплекс с Ro-РНК (hY1, hY3 и hY5).
Клиническое значение.
-
Положительные результаты обнаружения антител к SS-A/Ro являются диагностическими критериями первичного и вторичного СШ (уровень доказательности А).
-
При беременности исследование сывороточного уровня антител к SS-A/Ro-52 кДа и SS-B/La-48 кДа полезно для прогнозирования риска развития полной поперечной блокады сердца у плода, антител к SS-A/ Ro - для прогнозирования риска развития неонатального волчаночно-подобного синдрома у новорожденных (уровень доказательности В).
-
У больных СКВ положительные результаты тестирования антител к SS-A/Ro ассоциируются с фотосенсибилизацией, СШ, гиперпродукцией РФ (уровень доказательности В).
Антитела к SS-B/La (Lane)
S-B/La-антиген - нуклеоцитоплазматический комплекс 48 кДа фосфопротеина с Ro РНК (hY1-hY5), являющийся терминальным транскрипционным фактором для РНК полимеразы-3.
Клиническое значение.
-
Положительные результаты определения антител к SS-B/La являются диагностическими критериями первичного и вторичного СШ (уровень доказательности А).
-
При беременности повышение сывороточного уровня антител к SS-B/ La служит прогностическим маркером развития полной поперечной блокады сердца у плода (уровень доказательности В).
-
При СШ обнаружение антител к SS-B/La ассоциируется с выраженной лимфоидной инфильтрацией слюнных желез (уровень доказательности С) и развитием экстрагландулярных проявлений (пурпуры, васкулита, лимфаденопатии) (уровень доказательности С).
-
При СКВ гиперпродукция антител к SS-B/La ассоциируется с низкой частотой поражения почек (уровень доказательности С).
Склеродермические аутоантитела
Склеродермические аутоантитела - группа аутоантител, которые с высокой частотой выявляются при различных вариантах ССД. К ним относятся антицентромерные антитела, антитела к Scl-70 и антинуклеолярные антитела.
Антицентромерные антитела распознают более шести центромерных нуклеопротеинов (A-F).
-
Стандартным методом определения антицентромерных антител в сыворотке крови является НРИФ с помощью HEp-2-клеток (дискретный крапчатый тип свечения) (уровень доказательности А). Исследование антицентромерных антител методами ИФА и ИБ не рекомендуется для широкого применения, так как диагностическая точность данных тестов недостаточно изучена.
Клиническое значение.
-
Выявление антицентромерных антител очень полезно для диагностики ССД (уровень доказательности А), особенно синдрома CREST (уровень доказательности А).
-
Положительные результаты определения антицентромерных антител являются полезным маркером для прогнозирования лимитированного поражения кожи (уровень доказательности А) и низкой вероятности развития рентгенологических признаков легочного фиброза (уровень доказательности А).
Антитела к Scl-70 реагируют с топоизомеразой I (основной негистоновый хромосомный белок с молекулярной массой 70 кДа).
Клиническое значение.
-
Определение антител к Scl-70 является очень полезным тестом для диагностики ССД (уровень доказательности А).
-
Положительные результаты определения антител к Scl-70 служат полезным маркером для прогнозирования диффузного поражения кожи (уровень доказательности А), высокой вероятности развития рентгенологических признаков легочного фиброза (уровень доказательности А) и нарушения функциональных легочных проб (уровень доказательности А).
Антинуклеолярные антитела - гетерогенная группа аутоантител, характеризующихся нуклеолярным типом свечения при исследовании методом НРИФ. Антинуклеолярные антитела включают антитела к PM-Scl, U3-рибонуклеопротеину, Th/To и семейству РНК-полимераз-1, -2, -3.
Клиническое значение.
-
Антинуклеолярные антитела имеют высокую специфичность, но низкую чувствительность при ССД (уровень доказательности С).
-
Наибольшее диагностическое и прогностическое значение имеют антитела к РНК-полимеразе-3, вошедшие в число диагностических критериев ССД и ассоциирующиеся с диффузным поражением кожи, развитием склеродермического почечного криза (уровень доказательности B).
Миозит-специфические антитела
Миозит-специфические антитела, реагирующие с различными ядерными и цитоплазматическими антигенами, являются серологическими маркерами ИВМ, включая ПМ и ДМ. К миозит-специфическим антителам относятся антитела к аминоацилсинтетазам т-РНК (Jo-1, PL-7, PL-12, EJ, OJ, KS), SRP и Mi-2, миозит-ассоциированным антигенам - антитела к PM-Scl, KJ.
Клиническое значение.
-
Миозит-специфические антитела имеют высокую специфичность, но низкую чувствительность в отношении диагностики и прогнозирования течения ПМ/ДМ.
-
Миозит-специфические антитела выявляются примерно у 40% больных ПМ/ДМ.
-
Положительные результаты определения антител к Jo-1 являются диагностическим критерием ПМ/ДМ с наличием антисинтетазного синдрома, который характеризуется острым началом миозита, ИПЛ, лихорадкой, артритом, феноменом Рейно и изменением кожи кистей по типу «руки механика» (уровень доказательности А).
-
Антитела к SRP обнаруживаются при ПМ, ассоциирующимся с острым началом заболевания, тяжелым течением миозита, кардиомиопатией и резистентностью к терапии ГК (уровень доказательности С).
-
Определение антител к Mi-2 полезно для диагностики классического стероидочувствительного ДМ с благоприятным прогнозом и редким развитием опухолевого миозита (уровень доказательности С).
-
Антитела к PM-Scl ассоциируются с субтипом диффузных болезней соединительной ткани (ДБСТ), включающего признаки ССД, ПМ и поражение почек (уровень доказательности С).
-
Антитела к KJ выявляются при миозите, феномене Рейно и ИПЛ (уровень доказательности С).
Ревматоидные факторы
РФ - аутоантитела классов IgM, IgA и IgG, реагирующие с Fc-фрагментом IgG.
-
Наибольшее значение в клинической практике имеет определение IgM РФ (уровень доказательности А).
-
Стандартными методами определения IgM РФ служат реакция агглютинации сенсибилизированных IgG частиц латекса (латекс-тест) или эритроцитов барана (реакция Ваалера-Розе), иммунонефелометрия и ИФА (уровень доказательности А).
-
Рекомендуются количественные методы измерения IgM РФ в международных единицах (МЕ/мл) в сыворотке крови (иммунонефелометрия, ИФА). Положительные результаты определения IgM РФ полуколичественными методами (латекс-агглютинация), даже в высоких титрах, всегда должны рассматриваться как низкоположительные.
Клиническое значение.
-
Положительные результаты обнаружения IgM РФ в сыворотке крови служат диагностическим критерием РА (уровень доказательности А).
-
IgM РФ - чувствительный, но недостаточно специфичный маркер для диагностики РА, так как обнаруживается в сыворотках при других ИВРЗ, хронических инфекциях, злокачественных новообразованиях и в пожилом возрасте.
-
IgM РФ в высокой концентрации является полезным маркером для прогнозирования быстропрогрессирующего деструктивного поражения суставов (уровень доказательности А) и системных проявлений при РА (уровень доказательности С).
-
Тестирование IgM РФ позволяет прогнозировать эффективность терапии ГИБП у больных РА. Серопозитивность по IgM РФ и высокий уровень этого маркера в крови до начала лечения рассматриваются в качестве предиктора эффективности РТМ (уровень доказательности A) при РА.
Показания к определению ревматоидного фактора.
Антитела к цитруллинированным белкам
АЦБ - гетерогенная группа аутоантител, которые распознают антигенные детерминанты филлагрина и других белков, содержащих атипичную аминокислоту цитруллин, образующуюся в результате посттрансляционной модификации остатков аргинина под действием фермента пептидиларгининдеиминазы. Семейство АЦБ включает АЦЦП, антиперинуклеарный фактор, антикератиновые антитела, антифиллагриновые антитела, антитела к цитруллинированному фибриногену и антитела к модифицированному цитруллинированному виментину.
-
АЦБ обладают высокой диагностической специфичностью (ДС) при РА (уровень доказательности А). Среди АЦБ ведущую роль в клинической практике имеет определение АЦЦП, которые являются наиболее стандартизованным маркером для ранней диагностики и оценки прогноза РА (уровень доказательности А).
-
Стандартными методами определения АЦЦП в сыворотке крови служит ИФА с использованием в качестве антигена синтетических циклических цитруллинированных пептидов II и III поколения, имеющих высокую связывающую активность в отношении широкого спектра антител, ассоциирующихся с РА (АЦЦП2 и АЦЦП3), а также хемилюминесцентный анализ на основе микрочастиц и электрохемилюминесцентный анализ.
-
В качестве скринингового теста может применяться полуколичественный иммунохроматографический экспресс-метод.
Клиническое значение.
-
Положительные результаты обнаружения АЦЦП в сыворотке крови служат диагностическим критерием РА (уровень доказательности А).
-
АЦЦП - более высокоспецифичный диагностический маркер РА, особенно на ранней стадии болезни, по сравнению с IgM РФ (уровень доказательности А).
-
Определение АЦЦП имеет важное значение для диагностики серо-негативного по IgV РФ РА (частота обнаружения АЦЦП у IgV РФ-отрицательных больных РА составляет 20-40%) (уровень доказательности А), дифференциальной диагностики РА с другими РЗ (уровень доказательности А).
-
Серопозитивность по АЦЦП является прогностическим маркером тяжелого эрозивного поражения суставов при РА (уровень доказательности А).
-
Обнаружение АЦЦП в сыворотке крови служит предиктором развития РА у здоровых лиц и у пациентов с ранним недифференцированным артритом (уровень доказательности А).
-
Тестирование АЦЦП позволяет прогнозировать эффективность терапии ГИБП у больных РА.
-
Серопозитивность по АЦЦП и высокий уровень этого маркера в крови до начала лечения рассматриваются в качестве предиктора хорошего ответа на терапию РТМ (уровень доказательности A) и АБЦ при РА.
-
Положительные результаты определения антител к модифицированному цитруллинированному виментину в сыворотке крови служат дополнительным диагностическим маркером РА при отрицательных результатах определения IgM РФ и АЦЦП в сыворотке крови (уровень доказательности C).
-
Антитела к модифицированному цитруллинированному виментину являются полезным маркером для прогнозирования тяжелого эрозивного поражения суставов у больных РА (уровень доказательности B).
Показания к определению антител к цитруллинированным белкам.
Антифосфолипидные антитела
Антифосфолипидные антитела (аФЛ) - гетерогенная популяция аутоантител, распознающих антигенные детерминанты анионных и нейтральных фосфолипидов, и комплексные эпитопы, образующиеся в процессе взаимодействия фосфолипидов и фосфолипидсвязывающих белков плазмы крови.
-
аФЛ являются серологическим маркером АФС и фактором риска развития тромботических осложнений и акушерской патологии при данном заболевании.
-
В число лабораторных диагностических критериев АФС входят положительные результаты обнаружения аКЛ классов IgG/IgM, антител к β2-гликопротеину I (анти-β2-гликопротеину I) классов IgG/IgM и ВА (уровень доказательности А).
-
IgG/IgM-аКЛ должны определяться в сыворотке в титрах, превышающих 40 GPL/MPL (1 единица GPL/MPL соответствует фосфолипид-связывающей активности 1 мкг/мл IgG/IgM-аКЛ), или 99-й процентиль у здоровых доноров, в двух исследованиях и более с интервалом не менее 12 нед с помощью стандартного ИФА, позволяющего выявлять β2-гликопротеин I-зависимые аКЛ (уровень доказательности А).
-
IgG/IgM анти-β2 -гликопротеин I должен определяться в сыворотке с помощью стандартного ИФА в диагностических титрах, превышающих 99-й процентиль у здоровых доноров, в двух исследованиях и более с интервалом не менее 12 нед (уровень доказательности А).
-
ВА должен определяться в плазме в двух исследованиях или более с интервалом не менее 12 нед в фосфолипидзависимых коагуляционных тестах стандартным методом, включающим несколько этапов (уровень доказательности А).
-
Удлинение фосфолипидзависимого свертывания крови при использовании скрининговых коагуляционных тестов (активированное частичное тромбопластиновое время, каолиновый тест, тест с ядом гадюки Рассела).
-
Отсутствие нормализации времени свертывания по данным скрининговых тестов при смешивании с нормальной, лишенной тромбоцитов плазмой.
-
Нормализация удлиненного времени свертывания крови при добавлении избытка фосфолипидов.
-
Исключение других коагулопатий (наличия в крови ингибиторов фактора VIII или гепарина).
-
-
Верхний предел референтного интервала при определении IgG аКЛ в сыворотке крови варьирует от 4 до 30 GPL; IgM аКЛ - от 3 до 20 MPL; IgG/IgM анти-β2-гликопротеин I - от 4 до 20 ЕД/мл в зависимости от фирмы-изготовителя коммерческих наборов реагентов. Рекомендуемый верхний предел референтного интервала для аФЛ соответствует 95-му процентилю (уровень доказательности B).
-
Рекомендуется выделение негативных (< верхний предел референтного интервала), низкопозитивных (между 95-м и 99-м процентилями), умеренно позитивных (99-й процентиль - 80 GPL/MPL) и высокопозитивных (>80 GPL/MPL) уровней аКЛ (уровень доказательности B).
-
При использовании в качестве диагностических критериев АФС положительные результаты определения IgG аКЛ и IgM аКЛ имеют умеренную чувствительность, но низкую специфичность. ВА и IgG/IgM анти-β2-гликопротеин I являются более специфичными, но менее чувствительными диагностическими маркерами АФС по сравнению с IgG/ IgM аКЛ (уровень доказательности А).
Клиническое значение.
-
Для постановки диагноза АФС достаточно одного из трех лабораторных критериев (ВА, аКЛ или анти-β2 -гликопротеин I); наличие у больного нескольких лабораторных критериев АФС сопровождается значительным увеличением риска тромботических осложнений (уровень доказательности А).
-
Диагноз АФС не может быть установлен, если промежуток между выявлением аФЛ и клиническими признаками заболевания составляет менее 12 нед и более 5 лет (уровень доказательности А).
-
Для прогнозирования риска развития тромботических осложнений при АФС наиболее полезными маркерами являются ВА, IgG аКЛ и IgG анти-β2 -гликопротеин I (уровень доказательности А).
-
Для прогнозирования риска развития акушерской патологии при АФС наиболее полезными маркерами являются ВА, IgG аКЛ и IgG анти-β2 -гликопротеин I (уровень доказательности А).
Показания к определению.
-
Необъяснимый тромбоз глубоких вен нижних конечностей или тромбоз легочных сосудов, особенно у лиц молодого возраста.
-
СКВ или другие аутоиммунные заболевания, протекающие с тромботическими осложнениями.
-
Рецидивирующая потеря плода или осложненная беременность с преждевременными родами.
-
Необычная локализация тромбоза (вены сетчатки, венозные синусы головного мозга, вены почек).
Антинейтрофильные цитоплазматические антитела
АНЦА - гетерогенная популяция аутоантител, реагирующих с ферментами цитоплазмы нейтрофилов. Различают два основных типа: АНЦА с цитоплазматическим типом иммунофлюоресцентного свечения, взаимодействующие с протеиназой-3, и АНЦА с перинуклеарным типом свечения, специфичные в отношении миелопероксидазы. В некоторых случаях выявляются атипичные АНЦА, направленные к неизвестным цитоплазматическим белкам и ламинам А, В1, С.
-
АНЦА являются серологическим маркером системных некротизирующих васкулитов сосудов среднего и мелкого калибра (АНЦА-СВ), к которым относятся ГПА, микроскопический полиангиит и синдром Черджа-Стросс (уровень доказательности А).
-
Первичным скрининговым тестом для определения АНЦА является метод НРИФ с использованием фиксированных этанолом нейтрофилов (уровень доказательности А).
-
АНЦА с цитоплазматическим типом иммунофлюоресцентного свечения дают диффузный цитоплазматический гранулярный тип свечения с большей интенсивностью по направлению к ядру нейтрофилов, чем к периферии. АНЦА с перинуклеарным типом свечения характеризуются перинуклеарным типом свечения.
-
Атипичные АНЦА характеризуются диффузным мелкокрапчатым, гомогенным или линейным цитоплазматическим типом свечения.
-
Перинуклеарный тип свечения расценивается как артефакт, связанный с фиксацией нейтрофилов этанолом, приводящей к перераспределению положительно заряженных белков (миелопероксидазы, лизоцима, эластазы, катепсина G, лактоферрина) вокруг отрицательно заряженной мембраны ядра, что может давать свечение, напоминающее АНФ.
-
При определении АНЦА с перинуклеарным типом свечения методом НРИФ необходима постановка соответствующих контролей с фиксированными формалином нейтрофилами и с НЕр-2-клетками. На фиксированных формалином нейтрофилах антинуклеарные антитела дают характерное ядерное свечение, а АНЦА с перинуклеарным типом свечения - цитоплазматическое гранулярное.
-
При положительных результатах определения АНЦА с цитоплазматическим типом иммунофлюоресцентного свечения и АНЦА с перинуклеарным типом свечения методом НРИФ рекомендуется проводить подтверждающее исследование сывороток на наличие антител к протеиназе-3 и миелопероксидазе с помощью ИФА (уровень доказательности А).
-
Клиническое значение.
-
Обнаружение АНЦА с цитоплазматическим типом иммунофлюоресцентного свечения методом НРИФ является высокоспецифичным диагностическим маркером ГПА и менее полезно для диагностики микроскопического полиангиита и синдрома Черджа-Стросс (уровень доказательности А).
-
Положительные результаты определения АНЦА с перинуклеарным типом свечения методом НРИФ в сочетании с ИФА миелопероксидазы-АНЦА служат полезным диагностическим маркером микроскопического полиангиита, синдрома Черджа-Стросс, быстропрогрессирующего гломерулонефрита и идиопатического альвеолярного геморрагического синдрома (уровень доказательности А).
-
Повышение уровня АНЦА с цитоплазматическим типом иммунофлю-оресцентного свечения/АНЦА к протеиназе 3 является фактором риска развития обострений ГПА на фоне ремиссии болезни (уровень доказательности В).
Показания к определению антинейтрофильных цитоплазматических антител.
Лабораторные маркеры воспаления
СОЭ - высокочувствительный, но неспецифичный и нестабильный маркер системного воспаления.
Клиническое значение.
-
Увеличение СОЭ служит лабораторным классификационным критерием РА. Повышение СОЭ более 50 мм/ч является классификационным критерием ГКА.
-
Повышение СОЭ более 35 мм/ч является диагностическим признаком РП.
-
Определение СОЭ может быть полезным для оценки активности воспаления при ГКА (уровень доказательности C), РП [используется при подсчете индекса SDAI PMR (simplified disease activity index polymyalgia rheumatica)] (уровень доказательности C) и РА (используется при подсчете индекса DAS28) (уровень доказательности А).
-
Наиболее важными факторами, приводящими к несовпадению результатов определения СОЭ и СРБ у больных РА и другими ИВРЗ, являются инфекция, почечная недостаточность и низкий уровень альбумина в крови (уровень доказательности С).
СРБ - классический острофазовый белок плазмы крови, который рассматривается как наиболее чувствительный лабораторный маркер инфекции, воспаления и тканевого повреждения.
-
В зависимости от цели исследования определение концентрации СРБ проводится классическими и высокочувствительными методами.
-
Методы количественного анализа СРБ в сыворотке крови, включая радиальную иммунодиффузию, иммунотурбидиметрию и иммунонефелометрию, предназначены для выявления повышенного уровня СРБ при остром воспалении и тканевом повреждении в пределах диапазона концентраций 5-500 мг/л.
-
Высокочувствительный анализ СРБ, основанный на усилении аналитической чувствительности иммунохимических методов (иммуноферментного, иммунотурбидиметрического и иммунонефелометрического) в 10 раз и более с помощью специальных реагентов, позволяет измерять концентрации СРБ ниже 5 мг/л и используется для оценки базального уровня СРБ, определяемого высокочувствительным анализом, и связанного с ним кардиоваскулярного риска (уровень доказательности А).
-
В норме у 50% здоровых доноров концентрация СРБ в сыворотке крови составляет 0,8 мг/л, у 90% - 3 мг/л, у 99% - 10 мг/л.
-
При этом индивидуальная базальная концентрация СРБ достаточно стабильна и не подвержена циркадным колебаниям.
-
Нормальный уровень СРБ у взрослых составляет менее 5 мг/л (однако значения, превышающие 3 мг/л, могут указывать на высокий риск развития кардиоваскулярной патологии), у новорожденных (до 3 нед) - менее 4,1 мг/л, у детей - менее 2,8 мг/л.
-
Клиническое значение.
-
Определение СРБ является полезным тестом для оценки активности патологического процесса у больных ИВРЗ (в том числе при подсчете индексов активности DAS28-СРБ и SDAI).
-
Мониторирование и контроль за эффективностью терапии интеркуррентных инфекций при СКВ, ССД, ДМ и других РЗ с незначительным повышением или нормальным уровнем СРБ (уровень доказательности С).
-
Увеличение базальной концентрации СРБ является предиктором развития рентгенологических изменений, свидетельствующих о тяжелом деструктивном поражении суставов при раннем РА (уровень доказательности С).
-
При АС рекомендуется использовать высокочувствительный анализ СРБ, лучше коррелирующий с клиническими параметрами воспалительной активности заболевания по сравнению с рутинным методом измерения данного маркера в сыворотке крови.
-
Увеличение сывороточной концентрации СРБ отмечено у 50-54% больных АС и входит в число классификационных критериев ASAS для аксиального спондилоартрита (уровень доказательности А).
-
Результаты исследования СРБ применяются при подсчете индекса активности ASDAS СРБ (уровень доказательности А).
-
Концентрация СРБ в сыворотках больных АС выше, чем при аксиальном спондилоартрите без рентгенологических изменений (уровень доказательности B).
-
Уровень СРБ умеренно коррелирует с индексами ASDAS, BASDAI и активностью локального воспаления по данным МРТ («золотого стандарта» для оценки воспалительной активности заболевания) (уровень доказательности B).
-
СРБ является информативным маркером для оценки эффективности терапии АС (уровень доказательности B).
-
-
Определение базального уровня СРБ, определяемого высокочувствительным методом, имеет важное значение для стратификации больных ИВРЗ по степени кардиоваскулярного риска.
-
Базальная концентрация СРБ, определяемого высокочувствительным методом, менее 1 мг/л соответствует низкому, 1-3 мг/л - среднему, более 3 мг/л - высокому кардиоваскулярному риску.
-
Уровень СРБ, определяемого высокочувствительным методом, от 3 до 10 мг/л ассоциируется с субклиническим low grade-воспалением , а более 10 мг/л - с системным персистирующим high grade-воспалением (уровень доказательности В).
-
Список литературы
-
Насонов Е.Л., Александрова Е.Н., Новиков А.А. Аутоиммунные ревматические заболевания - проблемы иммунопатологии и персонифицированной терапии // Вестн. РАМН. 2015. Т. 70, № 2. С. 169-182. doi: 10.15690/ vramn,v70i2.1310.
-
Александрова Е.Н., Новиков А.А, Насонов Е.Л. Современные стандарты лабораторной диагностики ревматических заболеваний и их применение в реальной клинической практике // Научно-практ. ревматология. 2013. Т. 51, № 4. С. 368-376. doi: http: //dx.doi.org/10.14412/1995-4484-2013-4.
-
Александрова Е.Н., Новиков А.А. Лабораторная диагностика ревматических заболеваний. Ревматология : клинические рекомендации / под ред. Е.Л. Насонова. М. : ГЭОТАР-Медиа, 2010. С. 19-76.
-
Bonaguri C., Melegari A., Ballabio A. et al. Italian multicentre study for application of a diagnostic algorithm in autoantibody testing for autoimmune rheumatic disease: conclusive results // Autoimmun. Rev. 2011. Vol. 11. P. 1-5. doi: 10.1016/j. autrev.2011.06.006.
-
Solomon D., Kavanaugh A., Schur P. American College of Rheumatology Ad Hoc Committee on Immunologic Testing Guidelines. Evidence-based guidelines for the use of immunologic tests: antinuclear antibody testing // Arthritis Rheum. 2002. Vol. 47. P. 434-444. doi: 10.1002/art.10561.
-
Kavanaugh A., Solomon D. American College of Rheumatology Ad Hoc Committee on Immunologic Testing Guidelines. Guidelines for immunologic laboratory testing in the rheumatic diseases: anti-DNA antibody tests // Arthritis Rheum. 2002. Vol. 47. P. 546-555. doi: 10.1002/art.10558.
-
Reveille J., Solomon D. American College of Rheumatology Ad Hoc Committee of Immunologic Testing Guidelines. Evidence-based guidelines for the use of immunologic tests: anticentromere, Scl-70, and nucleolar antibodies // Arthritis Rheum 2003. Vol. 49. P. 399-412. doi: 10.1002/art.11113.
-
Taylor P., Gartemann J., Hsieh J., Creeden J. A systematic review of serum biomarkers anti-cyclic citrullinated peptide and rheumatoid factor as tests for rheumatoid arthritis // Autoimmune Dis. 2011. Article ID 815038. doi: 10.4061/2011/815038.
-
Lakos G., Favaloro E., Harris E. et al. International consensus guidelines on anticardiolipin and anti-pyglycoprotein I testing: report from the 13th International Congress on Antiphospholipid Antibodies // Arthritis Rheum. 2012. Vol. 64. P. 1-10. doi: 10.1002/art.33349.
-
Mukhtyar C., Flossmann O., Hellmich B. et al. Outcomes from studies of antineutrophil cytoplasm antibody associated vasculitis: a systematic review by the European League against Rheumatism Systemic Vasculitis Task Force // Ann. Rheum. Dis. 2008. Vol. 67. P. 1004-1010. doi: 10.1136/ard.2007.071936.