Клиническая фармакология : национальное руководство / под ред. Ю. Б. Белоусова, В. Г. Кукеса, В. К. Лепахина, В. И. Петрова - Москва : ГЭОТАР-Медиа, 2014 |
Аннотация
Издание разработано и рекомендовано ведущими специалистами в области клинической фармакологии при участии специализированных научно-исследовательских учреждений, медицинских вузов.
В книгу вошли общие и частные вопросы клинической фармакологии, содержащие объединённую согласованную позицию ведущих отечественных специалистов из Москвы, Санкт-Петербурга, Волгограда, Воронежа, Смоленска, Ярославля, Казани, Ставрополя, Перми и других городов России. Имеется компакт-диск с дополнительными материалами к книге.
Руководство предназначено клиническим фармакологам, врачам-терапевтам, студентам старших курсов медицинских вузов, интернам, ординаторам, аспирантам.
Общие особенности антимикробных лекарственных средств
Антимикробные ЛС избирательно угнетают жизнедеятельность микроорганизмов. Под избирательностью понимают:
Антимикробные ЛС подразделяют:
Все антимикробные ЛС, несмотря на различия по химической структуре и механизмам действия, объединяет ряд уникальных качеств.
Во-первых, в отличие от большинства других ЛС мишень (рецептор) антимикробного ЛС находится не в тканях человека, а в клетке микроорганизма.
Во-вторых, активность антимикробного ЛС непостоянна и снижается со временем, что обусловлено формированием лекарственной устойчивости (резистентности). Резистентность - неизбежное биологическое явление, связанное с высокими адаптационными способностями микроорганизмов, и предотвратить её практически невозможно.
Выделяют следующие основные механизмы резистентности к антимикробным ЛС (рис. 20-1):
Резистентные возбудители представляют опасность не только для пациента, у которого они были выделены, но и для многих других людей, даже разделённых временем и пространством. Поэтому разработка мероприятий по сдерживанию лекарственной устойчивости приобрела сейчас глобальные масштабы.
Резистентность к антимикробному ЛС не носит универсального характера и зависит от места возникновения инфекции (домашние условия, стационар), типа стационара (чаще в отделении реанимации и интенсивной терапии, гнойной хирургии), предшествующего приёма препаратов и др. Планирование применения антимикробных ЛС должно опираться на глобальные данные, а также региональные и локальные сведения о резистентности.
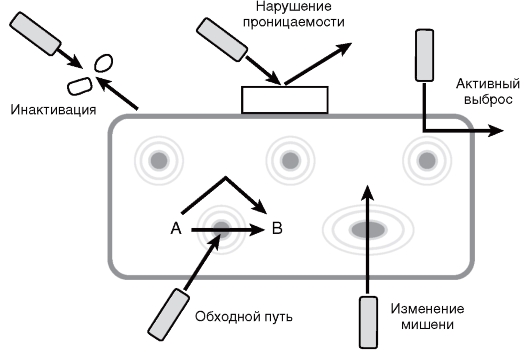
Рис. 20-1. Механизмы формирования резистентности к антимикробным лекарственным средствам.
Традиционно среди антимикробных ЛС принято выделять природные (собственно антибиотики, т.е. субстанции, продуцируемые микроорганизмами, например, пенициллины), полусинтетические (продукты модификации природных молекул: амоксициллин, цефазолин и др.) и синтетические (нитрофураны, нитроимидазолы и др.). Однако в настоящее время такое деление потеряло актуальность, так как ряд природных антимикробных ЛС получают путём синтеза (хлорамфеникол), а некоторые препараты, обычно называемые антибиотиками (например, фторхинолоны), de facto являются синтетическими соединениями.
Аналогично ЛС других фармакологических групп антимикробные ЛС разделяют на группы, классы, поколения, что имеет существенное значение с точки зрения понимания общности механизмов действия, спектра активности, фармакокинетических особенностей, характера НЛР и т.д. Тем не менее неверно рассматривать все антимикробные ЛС, входящие в одну группу (класс, поколение), как взаимозаменяемые. Между препаратами одного поколения и близкой химической структуры возможны существенные различия.
С избирательностью действия тесно связано понятие широты спектра активности антимикробного ЛС. Однако с позиций сегодняшнего дня деление на препараты широкого и узкого спектра условно и подвергается серьёзной критике в первую очередь вследствие отсутствия критериев для такой градации.
Спорно представление о том, что антимикробные ЛС широкого спектра активности более надёжны, более сильны, так как при этом не учитывают приобретённую резистентность микроорганизмов. Так, например, тетрациклины, бывшие в первые годы своего применения активными в отношении большинства клинически значимых микроорганизмов, в настоящее время утратили значительную часть своего спектра именно из-за приобретённой устойчивости пневмококков, стафилококков, гонококков и энтеробактерий. Цефалоспорины III поколения обычно рассматривают как препараты с широким спектром активности, но в то же время они не действуют на метициллинорезистентные стафилококки, многие анаэробы, энтерококки, листерии, внутриклеточные микроорганизмы.
Более целесообразно рассматривать антимикробные ЛС с точки зрения клинической эффективности при инфекции определённой локализации, так как клинические доказательства эффективности, полученные в хорошо контролируемых (сравнительных, рандомизированных, проспективных) клинических испытаниях, имеют, несомненно, более важное значение, чем условный ярлык «антибиотик широкого или узкого спектра».
ОСОБЕННОСТИ ФАРМАКОДИНАМИКИ
Поскольку мишенью действия антимикробного ЛС не выступает (или не должен) организм человека, к их основным фармакодинамическим характеристикам, кроме механизма действия, относят спектр и степень активности в отношении того или иного вида микроорганизмов. Количественное выражение активности антимикробного ЛС - его минимальная подавляющая концентрация: чем она меньше, тем более активен препарат.
В последние годы трактовка фармакодинамики антимикробного ЛС, в частности антибактериальных препаратов, расширилась. В неё включено взаимоотношение между концентрациями препарата в организме или в искусственной модели и выраженностью его антимикробного эффекта. Исходя из этого выделяют две группы антибиотиков: с концентрационно-зависимой и времязависимой активностью. Для первой группы (аминогликозиды, фторхинолоны) степень гибели бактерий коррелирует с концентрацией антибиотика в биологической среде, например, в сыворотке крови, поэтому цель режима дозирования - достижение максимально переносимой концентрации препарата. Для антимикробных ЛС с время-зависимым антимикробным действием важнейшим условием выступает длительное поддержание концентрации на относительно невысоком уровне (в 3-4 раза выше минимальной подавляющей концентрации, при повышении концентрации эффективность не возрастает). Цель режимов дозирования таких препаратов (пенициллины, цефалоспорины) - сохранение в сыворотке крови и очаге инфекции концентрации препарата, в 4 раза превышающей минимальную подавляющую концентрацию, в течение 40-60% временного интервала между дозами.
По характеру антимикробного эффекта выделяют антимикробные ЛС, вызывающие гибель инфекционного агента («цидное» действие: бактерицидное, фунгицидное и т.д.) либо приостанавливающие размножение микроорганизмов («статическое» действие: бактериостатическое, фунгистатическое и т.д.). При этом одни и те же препараты могут обладать «цидным» и «статическим» эффектами. Это может определять вид микроорганизма, концентрацию антимикробных ЛС и экспозицию препарата.
Выделение бактерицидных и бактериостатических антимикробных ЛС имеет существенное практическое значение при лечении жизнеугрожающих инфекций, особенно у пациентов с иммунодефицитом. Это связано с тем, что при нормальном иммунитете приостановление размножения микроорганизмов оказывается вполне достаточным, чтобы элиминацию патогенных микроорганизмов завершила иммунная система. Назначение бактерицидных препаратов необходимо при таких инфекциях, как эндокардит, остеомиелит, менингит, нейтропеническая лихорадка и некоторых других.
ОСОБЕННОСТИ ФАРМАКОКИНЕТИКИ
Из фармакокинетических характеристик антимикробных ЛС наиболее важны при выборе конкретного препарата способность проникать в очаг инфекции и создавать в нём концентрации, достаточные для «цидного» или «статического» действия. Поэтому микробиологическая активность препарата in vitro выступает только первой предпосылкой для обеспечения клинической и микробиологической эффективности.
Для антимикробных ЛС, которые принимают внутрь, важнейшее значение имеет такой фармакокинетический параметр, как биодоступность. Необходимо отметить, что биодоступность не является неизменным параметром препарата и при создании современных лекарственных форм её удаётся существенно повысить. Например, если амоксициллин в таблетках или капсулах имеет биодоступность около 75-80%, то у специальной растворимой формы («солютаб») она превышает 90%. Период полувыведения определяет кратность применения антимикробных ЛС. Его величина зависит от состояния органов, с помощью которых происходит экскреция антимикробных ЛС. Учитывая, что большинство антимикробных ЛС выводят почки, у всех пациентов, получающих антимикробные ЛС в стационаре (особенно в отделении реанимации и интенсивной терапии), следует определять концентрацию креатинина в сыворотке крови и рассчитывать его клиренс.
ОСОБЕННОСТИ НЕЖЕЛАТЕЛЬНЫХ ЛЕКАРСТВЕННЫХ РЕАКЦИЙ
Основная особенность НЛР антибиотиков и в меньшей степени других антимикробных ЛС - влияние на нормальную микрофлору человека, особенно полости рта и кишечника. В большинстве случаев количественные и качественные изменения микрофлоры клинически не проявляются и не требуют коррекции. Тем не менее иногда может возникнуть антибиотико-ассоциированная диарея, оральный или вагинальный кандидоз, которые требуют специальной терапии.
Рассматривая НЛР антибиотиков, следует особо отметить, что широко распространённое мнение о способности этих препаратов угнетать иммунитет - серьёзное заблуждение. Все препараты, способные вызвать иммуносупрессию у человека, отсеивают ещё на стадии доклинических исследований. Более того, ряд антимикробных ЛС способны стимулировать определённые звенья иммунной реакции (макролиды, линкозамиды, фторхинолоны).
Аллергические реакции на антимикробные ЛС принципиально неотличимы от таковых на другие ЛС. При этом следует учитывать три основных момента.
-
Риск аллергии на антимикробные ЛС существенно преувеличивают. Не существует «аллергии на все антибиотики», так как они имеют различную химическую структуру. Аллергия может быть на препараты определённого класса, иногда возможна перекрёстная аллергия на два класса, очень редко - на несколько.
-
Наиболее часто аллергические реакции вызывают β-лактамныеантибиотики, особенно пенициллины. Важнейшее средство профилактики - выяснение анамнеза. В ряде случаев проводят кожные аллергические пробы для выявления сенсибилизации либо провокационные пробы (при невозможности использовать другое антимикробное ЛС, проводит специалист).
-
Антигистаминные препараты не предотвращают развитие сенсибилизации к антимикробным ЛС, поэтому их не следует назначать вместе с антибиотиками.
Таким образом, антимикробные ЛС обладают определённым сходством, которое ещё больше усиливается внутри каждого класса или группы. Тем не менее при назначении этих препаратов следует учитывать особенности каждого из них, а также результаты рандомизированных контролируемых клинических исследований.
Общие принципы применения антимикробных лекарственных средств
Антимикробная терапия может быть этиотропной или эмпирической. Этиотропная терапия предполагает целенаправленное применение антимикробных ЛС против установленного возбудителя инфекции. Однако в повседневной клинической практике постановка микробиологического диагноза не всегда возможна, а иногда и необязательна. Поэтому чаще используют эмпирическую терапию, ключевая характеристика которой - выбор антимикробных ЛС с учётом наиболее вероятных возбудителей конкретной инфекции и наиболее вероятной чувствительности этих возбудителей.
Независимо от вида антимикробной терапии при её планировании и проведении необходимо руководствоваться несколькими основными принципами.
-
Уточнение необходимости назначения антимикробных ЛС (например, некоторые вирусные инфекции не требуют специфического лечения).
-
Выбор оптимального антимикробного ЛС с учётом активности в отношении предполагаемого или установленного возбудителя, характера антимикробного эффекта, фармакокинетических свойств, возможных НЛР, а также особенностей пациента (возраст, масса тела, аллергологический и фармакологический анамнез и др.).
При отсутствии эффекта от проводимой терапии следует определить, правильно ли поставлен диагноз; правильно ли выбрано антимикробное ЛС (или комбинация препаратов); не ослаблен ли эффект антимикробных ЛС другими ЛС; не присоединилась ли суперинфекция; не сформировался ли абсцесс; нет ли инородного тела; не провоцируется ли лихорадка самим антимикробным ЛС?
Замена одного антимикробного ЛС другим оправдана в следующих ситуациях при отсутствии эффекта (при исключении других факторов неэффективности); развитии серьёзных, угрожающих здоровью или жизни пациента НЛР, которые предположительно связаны с антимикробными ЛС; применении препаратов с кумулятивной токсичностью, для которых установлены лимитированные сроки назначения (например, аминогликозиды).
Если первично выбранное антимикробное ЛС эффективно, его необходимо назначать на полный курс в соответствии с особенностями данной инфекции. Рекомендации об обязательной смене препаратов каждые 5-7 дней в целях профилактики развития резистентности возбудителя не имеют под собой никакой доказательной основы.
АНТИБАКТЕРИАЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
β-Лактамные антибиотики
К β-лактамным антибиотикам (β-лактамам), общий элемент химической структуры которых включает четырёхчленное β-лактамное кольцо, относят пенициллины, цефалоспорины, карбапенемы и монобактамы. Наличие β-лактамного кольца обусловливает одинаковый механизм действия, бактерицидный эффект и развитие в некоторых случаях перекрёстной аллергии. β-Лактамы составляют основу современной антибактериальной терапии, так как занимают ведущие позиции в лечении большинства инфекций.
ПЕНИЦИЛЛИНЫ
Пенициллины - первые антимикробные ЛС, разработанные на основе активных веществ, продуцируемых микроорганизмами. Первый из пенициллинов - бензилпенициллин (пенициллин G*) применяют в клинической практике с начала 40-х гг.
Группа пенициллинов включает более десятка препаратов, которые, обладая рядом общих свойств, отличаются по происхождению, особенностям химической структуры, антимикробной активности и фармакокинетике (табл. 20-1). К природным пенициллинам относят бензилпенициллин (в виде различных солей) и феноксиметилпенициллин. Все другие представляют собой полусинтетические соединения, получаемые в результате химической модификации 6-аминопенициллиновой кислоты, которая выступает в качестве основы молекулы всех пенициллинов.
Таблица 20-1. Классификация пенициллинов
Природные |
Бензилпенициллин |
Полусинтетические |
|
Изоксазолилпенициллины (антистафилококковые) |
Оксациллин |
Аминопенициллины |
Ампициллин Амоксициллин |
Карбоксипенициллины |
Карбенициллин Тикарциллин |
Уреидопенициллин |
Азлоциллин Пиперациллин8 |
Ингибиторозащищённые пенициллины |
Амоксициллин + клавулановая кислота |
Фармакодинамика
Пенициллины (и все другие β-лактамы) обладают бактерицидным эффектом. Мишень их действия - пенициллиносвязывающие белки, выполняющие роль ферментов на завершающем этапе синтеза пептидогликана - основного компонента клеточной стенки бактерий. Блокирование образования пептидогликана приводит к гибели бактерии.
Для преодоления широко распространённой среди микроорганизмов приобретённой устойчивости, обусловленной продукцией особых ферментов - β-лактамаз, разрушающих β-лактамные антибиотики, были разработаны соединения, способные необратимо подавлять активность этих ферментов, так называемые ингибиторы β-лактамаз - клавулановая кислота, сульбактам и тазобактам8. На их основе создана группа ингибиторозащищённых пенициллинов.
Природные пенициллины активны преимущественно в отношении грамположительных бактерий - Streptococcus spp. (включая β-гемолитический стрептококк и пневмококки), Enterococcus faecalis, Bacillus spp., листерий, эризипелотрикса, большинства коринебактерий (включая Corynebacterium diphtheriae), спирохет (Treponema, Borrelia, Leptospira). Среди грамотрицательных бактерий чувствительны Neisseria spp., Pasteurella multocida и Haemophilus ducreyi. Среди анаэробов - актиномицеты, Peptostreptococcus spp., Clostridium spp.
Приобретённую резистентность чаще всего встречают среди стафилококков. Она связана с продукцией β-лактамаз (частота распространения - 60-80%) или появлением дополнительного пенициллиносвязывающего белка. Отмечают высокую частоту устойчивости среди гонококков (более 70%), связанную с модификацией пенициллиносвязывающего белка. Растёт резистентность пневмококков (Streptococcus pneumoniae), также обусловленная мутациями в генах пенициллиносвязывающего белка, достигая в отдельных регионах мира 56%. Довольно часто она связана с резистентностью к другим антимикробным ЛС (макролидам, тетрациклинам, ко-тримоксазолу). Как показало многоцентровое эпидемиологическое исследование ПеГАС-II (2004-2005 гг.), проблема пенициллинорезистентности пневмококков для России пока не актуальна: уровень резистентности клинических штаммов S. pneumoniae остаётся стабильным и не превышает 10%.
Основной представитель изоксазолилпенициллинов - оксациллин близок к природным пенициллинам, но уступает им по уровню активности в отношении большинства микроорганизмов. Главное клиническое значение имеет устойчивость оксациллина к стафилококковым β-лактамазам, благодаря чему он активен против большинства внебольничных штаммов стафилококков [включая пенициллинорезистентные Staphylococcus aureus (PRSA)]. Однако оксациллин не действует на стафилококки, резистентность которых к пенициллинам связана не с выработкой β-лактамаз, а с появлением атипичных пенициллиносвязывающих белков - так называемые метициллинорезистентные S. aureus (MRSA) и Staphylococcus epidermidis (MRSE).
Спектр активности аминопенициллинов расширен за счёт некоторых грамотрицательных бактерий семейства Enterobacteriaceae - Escherichia coli, Shigella spp., Salmonella spp., Proteus mirabilis. Преимущество аминопенициллинов перед природными отмечено в отношении Haemophilus spp. (особенно H. influenzae), E. faecalis и листерий. Важное значение имеет действие амоксициллина на Helicobacter pylori.
Антимикробный спектр ингибиторозащищённых аминопенициллинов охватывает такие грамотрицательные бактерии, как Klebsiella spp., Proteus vulgaris, Citrobacter diversus, а также анаэробы группы B. fragilis, которые синтезируют хромосомные β-лактамазы класса А. Кроме того, они активны в отношении микрофлоры с приобретённой резистентностью, обусловленной продукцией β-лактамаз: PRSA, Moraxella catarrhalis, Haemophilus spp., E. coli, P. mirabilis.
Карбоксипенициллины менее активны в отношении грамположительных бактерий. Изначально к ним были чувствительны многие представители Enterobacteriaceae, а также синегнойная палочка (Pseudomonas aeruginosa). Однако к настоящему времени эти антимикробные ЛС утратили клиническое значение ввиду широкого распространения β-лактамаз, к которым они высокочувствительны.
Тикарциллин + клавулановая кислота имеет более широкий спектр за счёт действия на Klebsiella spp., P. vulgaris, C. diversus, B. fragilis. К нему реже отмечают резистентность других грамотрицательных бактерий и стафилококков. Однако присутствие ингибитора β-лактамаз не обеспечивает активность в отношении грамотрицательной микрофлоры, вырабатывающей хромосомные β-лактамазы класса С или характеризуемой высоким уровнем продукции ферментов класса А.
Уреидопенициллины по действию на грамположительную микрофлору почти не уступают природным и аминопенициллинам. Высокоактивны практически против всех важнейших грамотрицательных бактерий (Enterobacteriaceae, P. aeruginosa), неферментирующих микроорганизмов (Stenotrophomonas maltophilia). Однако их самостоятельное клиническое значение невелико в связи с чувствительностью к большинству β-лактамаз. Этот недостаток существенно компенсирован у пиперациллина + тазобактама8, обладающего более широким спектром (включающим анаэробы) и высоким уровнем антибактериальной активности среди всех пенициллинов. Тем не менее подобно другим ингибиторозащищённым пенициллинам пиперациллин + тазобактам8 не действует на штаммы, вырабатывающие β-лактамазы класса С или гиперпродуценты ферментов класса А.
Фармакокинетика
Бензилпенициллин, карбокси- и уреидопенициллины лабильны к действию соляной кислоты желудочного сока, поэтому их применяют только парентерально. Феноксиметилпенициллин, оксациллин и аминопенициллины более кислотоустойчивы, могут назначаться внутрь. В пищеварительном тракте лучше других всасывается амоксициллин, причём наиболее высокую биодоступность (93%) имеют специальные растворимые лекарственные формы (флемоксин солютаб*). Биодоступность феноксиметилпенициллина - 40-60%, ампициллина - 35-40%, оксациллина - 25-30%, причём пища существенно уменьшает биодоступность двух последних (табл. 20-2). Биодоступность ингибитора β-лактамаз клавулановой кислоты - 75%, под влиянием пищи несколько увеличивается.
Таблица 20-2. Фармакокинетические свойства пенициллинов
Препарат |
Биодоступность в пищеварительном тракте, % |
Пища снижает всасывание |
Связывание с белками,% |
Экскреция |
T1/2, ч |
|
нормальная функция почек |
клиренс креатинина менее 10 мл/мин |
|||||
Бензилпенициллин |
20 |
Да |
55 |
Почки |
0,5 |
10 |
Феноксиметилпенициллин |
60 |
Нет |
80 |
Почки |
1 |
4 |
Оксациллин |
30 |
Да |
93 |
Почки, печень |
0,5 |
1 |
Ампициллин |
40 |
Да |
17 |
Почки |
1 |
8 |
Амоксициллин |
75-93 |
Нет |
17 |
Почки |
1 |
8 |
Карбенициллин |
- |
- |
47 |
Почки |
1,1 |
15 |
Тикарциллин |
- |
- |
50 |
Почки |
1,2 |
15 |
Азлоциллин |
- |
- |
20 |
Почки, печень |
0,8 |
4 |
Пиперациллин8 |
- |
- |
50 |
Почки, печень |
1,3 |
4 |
Бензилпенициллина новокаиновая соль* и бензатина бензилпенициллин вводят только внутримышечно. Медленно всасываясь, они создают более низкие по сравнению с солями натрия и калия бензилпенициллина концентрации в крови. Оказывают пролонгированное действие (объединяют термином «депопенициллины»). Терапевтические уровни бензилпенициллина новокаиновой соли* в крови сохраняются в течение 18-24 ч, бензатина бензилпенициллина - до 2-4 нед.
Пенициллины создают высокие концентрации в лёгких, почках, слизистой кишечника, репродуктивных органах, костях, плевральной и перитонеальной жидкости. В небольших количествах проникают через плаценту и в грудное молоко. Плохо проходят через ГЭБ и гематоофтальмический барьеры, в предстательную железу. При воспалении оболочек мозга проницаемость ГЭБ увеличивается. Распределение ингибиторов β-лактамаз в целом аналогично таковому пенициллинов.
В печени частично метаболизируются оксациллин (до 45%) и уреидопенициллины (до 30%). Среди ингибиторов β-лактамаз наиболее интенсивно метаболизируется клавуланат (около 50%), в меньшей степени - сульбактам (около 25%), ещё слабее - тазобактам+.
Большинство пенициллинов экскретируют почки. Их период полувыведения (Τ1/2) в норме колеблется около часа (кроме депо-пенициллинов), значительно возрастая при почечной недостаточности. Оксациллин и уреидопенициллины выводятся почками и через билиарную систему. Их Τ1/2 в меньшей степени изменяется при почечной недостаточности.
Показания
Бензилпенициллин - антибиотик первого ряда при стрептококковых инфекциях (тонзиллофарингите, роже, скарлатине, инфекциях мягких тканей, неонатальном сепсисе), сифилисе, газовой гангрене, столбняке, актиномикозе, сибирской язве, лептоспирозе, клещевом боррелиозе (табл. 20-3). Он используется при среднетяжёлом течении внебольничной пневмонии, при менингите у детей старше 2 лет и взрослых, при раневой инфекции после укусов кошек и собак (но не человека!). В сочетании с гентамицином или стрептомицином - в качестве эмпирической терапии инфекционного эндокардита (ИЭ).
Депо-пенициллины применяют для лечения тонзиллофарингита и сифилиса (кроме нейросифилиса), для профилактики рожи, скарлатины и ревматизма, феноксиметилпенициллин - для лечения тонзиллофарингита, рожи, профилактики ревматизма, профилактики пневмококковых инфекций после спленэктомии.
Оксациллин используют при подтверждённых или предполагаемых стафилококковых инфекциях (при доказательстве чувствительности или незначительном риске метициллинорезистентности): кожи, мягких тканей, костей, суставов, внебольничной пневмонии, ИЭ, менингите, сепсисе. Ввиду низкой биодоступности per os при тяжёлых инфекциях его следует применять парентерально.
Показания для применения аминопенициллинов и ингибиторозащищённых аминопенициллинов во многом совпадают. Назначение аминопенициллинов более обосновано при лёгких и неосложнённых инфекциях, а их ингибиторозащищённых производных - при более тяжёлых или рецидивирующих формах, при наличии данных о высокой распространённости β-лактамазопродуцирующих микроорганизмов. Ампициллин в большинстве случаев (кроме кишечных инфекций) следует применять парентерально. Внутрь целесообразно использовать амоксициллин, амоксициллин + клавулановую кислоту или амоксициллин + сульбактам.
Таблица 20-3. Режимы дозирования пенициллинов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Бензилпенициллин (калиевая и натриевая соль) |
4-12 млн ЕД/сут в 4-6 введений; при тонзиллофарингите - 500 тыс. ЕД каждые 8-12 ч в течение 10 дней; |
50-100 тыс. ЕД/(кг х сут) в 4 введения; при тонзиллофарингите - 25-50 тыс. ЕД/(кг х сут) в 2 введения в течение 10 дней; |
Бензилпенициллина новокаиновая соль* |
От 600 тыс. до 1,2 млн ЕД/сут в 1-2 введения |
50-100 тыс. ЕД/(кг х сут) в 1-2 введения |
Бензатина бензилпенициллин |
1,2-2,4 млн ЕД однократно; при сифилисе - 2,4 млн ЕД/сут каждые 5-7 дней (2-3 инъекции); для профилактики ревматизма и рецидивирующей рожи - 1,2-2,4 млн ЕД раз в мес |
1,2 млн ЕД однократно; |
Феноксиметилпенициллин |
0,25-0,5 г каждые 6 ч; при тонзиллофарингите - 0,25 г каждые 8-12 ч в течение 10 дней; для профилактики ревматизма - 0,25 г каждые 12 ч |
30-40 мг/(кг х сут) в 4 приёма; |
Оксациллин |
Внутрь 0,5-1,0 г каждые 6 ч за 1 ч до еды; |
Внутрь 40-60 мг/(кг х сут) в 3-4 приёма (не более 1,5 г/сут); парентерально 0,2-0,3 г/(кг х сут) в 4-6 введений |
Ампициллин |
Внутрь 0,5 г каждые 6 ч за 1 ч до еды; |
Внутрь 30-50 мг/(кг х сут) в 4 приёма; парентерально 50-100 мг/(кг х сут) в 4 введения; при менингите - 0,3 г/(кг х сут) в 6 введений |
Амоксициллин |
0,25-0,5 г каждые 8 ч; |
30-60 мг/(кг х сут) в 3 приёма |
Амоксициллин + клавулановая кислота |
Внутрь 0,375-0,625 г каждые 8 ч или 1,0 г каждые 12 ч во время еды; в/в 1,2 г каждые 6-8 ч; для профилактики - 1,2 г за 30 мин до операции (если операция более 3 ч, то повторно через 4 ч) |
Внутрь 20-40 мг/(кг х сут) (по амоксициллину) в 3 приёма; в/в 40-60 мг/(кг х сут) (по амоксициллину) в 3 введения |
Амоксициллин + сульбактам |
Внутрь 0,25-0,5 г каждые 8 ч или 1,0 г каждые 12 ч; |
Внутрь до 2 лет - 0,125 г каждые 8 ч; 2-6 лет - 0,25 г каждые 8 ч; 6-12 лет - 0,25-0,5 г каждые 8 ч; парентерально до 2 лет - 40-60 мг/(кг х сут) в 3 введения; 2-6 лет - 0,25 г каждые 8 ч; 6-12 лет - 0,5 г каждые 8 ч |
Ампициллин + сульбактам |
Внутрь 0,375-0,75 г каждые 12 ч; парентерально 1,5-12 г/сут в 3-4 введения; |
Внутрь 50 мг/(кг х сут) в 2 приёма; парентерально 150 мг/(кг х сут) 3-4 введения |
Тикарциллин + клавулановая кислота |
3,2 г каждые 4-8 ч |
0,2-0,3 г/(кг х сут) в 4-6 введений |
Пиперациллин + тазобактам+8 |
2,25-4,5 г каждые 6-8 ч |
Старше 12 лет - 2,25-4,5 г каждые 6-8 ч |
Аминопенициллины и ингибиторозащищённые аминопенициллины применяют при инфекциях верхних дыхательных путей - остром среднем отите, синусите; нижних дыхательных путей - обострении ХОБЛ, внебольничной пневмонии; внебольничных инфекциях мочевыводящих путей - остром цистите, пиелонефрите; для профилактики ИЭ.
Ампициллин используют при менингите, ИЭ (в сочетании с гентамицином или стрептомицином), кишечных инфекциях (шигеллёз, сальмонеллёз), амоксициллин - для эрадикации H. pylori при язвенной болезни желудка и двенадцатиперстной кишки (в составе трёх- или четырёхкомпонентной терапии).
Дополнительные показания для ингибиторозащищённых аминопенициллинов: инфекции кожи и мягких тканей, интраабдоминальные инфекции, периоперационная антибиотикопрофилактика.
Ингибиторозащищённые карбокси- и уреидопенициллины применяют при тяжёлых, преимущественно нозокомиальных инфекциях различной локализации, вызванных полирезистентной и смешанной (аэробно-анаэробной) микрофлорой: нижних дыхательных путей (пневмонии, абсцессе лёгкого, эмпиеме плевры), мочевыводящих путей, интраабдоминальных инфекций органов малого таза, кожи, мягких тканей, костей, суставов, сепсисе.
Противопоказания
Гиперчувствительность. Бензилпенициллина новокаиновая соль* противопоказана также при аллергии на прокаин.
Нежелательные лекарственные реакции. Наиболее часто встречаются аллергические реакции, перекрёстные ко всем пенициллинам. Профилактика: выяснение аллергического анамнеза, в сомнительных случаях - проведение кожных проб.
Другие НЛР встречают значительно реже: боль в животе, тошнота, рвота, диарея, псевдомембранозный колит (чаще при приёме ампициллина и ингибиторозащищённых пенициллинов). При появлении жидкого стула с примесью крови отменяют препарат, проводят исследование на наличие токсинов Clostridium difficile в стуле. Меры помощи: восстановление водно-электролитного баланса, при необходимости назначают внутрь метронидазол или ванкомицин.
У детей и пациентов с почечной недостаточностью при применении высоких доз бензилпенициллина возможны головная боль, тремор, судороги. Гиперкалиемия (большие дозы калиевой соли бензилпенициллина при почечной недостаточности); гипернатриемия (карбенициллин, реже уреидопенициллины и большие дозы натриевой соли бензилпенициллина). Болезненность и инфильтрат при внутримышечном введении (особенно калиевой соли бензилпенициллина). Повышение активности трансаминаз (чаще высокие дозы оксациллина и ингибиторозащищённых пенициллинов). Сосудистые осложнения (депо-пенициллины): ишемия и гангрена конечностей при введении в артерию; эмболия сосудов лёгких и головного мозга при введении в вену. Неаллергическая («ампициллиновая») макулопапулёзная сыпь, незудящая (аминопенициллины). Вагинальный и/или кандидоз полости рта.
Лекарственные взаимодействия
Фармацевтическое. Нельзя смешивать в одном шприце или одной инфузионной системе с аминогликозидами ввиду физико-химической несовместимости.
Фармакокинетическое. Колестирамин8 уменьшает биодоступность пенициллинов при приёме внутрь.
Пероральные пенициллины могут понижать эффективность оральных контрацептивов, нарушая энтерогепатическую циркуляцию эстрогенов.
Пенициллины замедляют выведение метотрексата, ингибируя его канальцевую секрецию.
Фармакодинамическое. При сочетании ампициллина с аллопуринолом возрастает риск «ампициллиновой» сыпи.
При сочетании высоких доз калиевой соли бензилпенициллина с калийсберегающими диуретиками, препаратами калия или ингибиторами АПФ повышается риск гиперкалиемии.
Следует избегать комбинации пенициллинов с сульфаниламидами ввиду возможного ослабления их бактерицидного эффекта.
Применение в особых ситуациях
Беременность. Пенициллины используют без каких-либо ограничений, хотя адекватных и строго контролируемых исследований безопасности у людей не проводилось.
Лактация. Применение у кормящих женщин может приводить к сенсибилизации новорождённых, появлению у них сыпи, развитию кандидоза и диареи.
Педиатрия. Повышен риск нейротоксичности с развитием судорог. Оксациллин может вызывать транзиторную гематурию. Пиперациллин + тазобактам8 не применяют у детей до 12 лет.
Гериатрия. Вследствие возрастных изменений функций почек может возникнуть необходимость коррекции дозы.
Нарушение функций почек. При почечной недостаточности необходимо корректировать дозы.
Инфекционный мононуклеоз. «Ампициллиновая» сыпь отмечается у 75-100% пациентов.
ЦЕФАЛОСПОРИНЫ
Цефалоспорины - один из наиболее обширных классов антибиотиков. Выделяют четыре поколения цефалоспоринов, причём первые три представлены препаратами для парентерального и перорального применения (табл. 20-4). Благодаря высокой эффективности и низкой токсичности цефалоспорины занимают одно из первых мест по частоте клинического использования среди всех антимикробных ЛС. Структурное сходство цефалоспоринов с пенициллинами определяет одинаковый механизм антимикробного действия и перекрёстную аллергию у некоторых пациентов.
Таблица 20-4. Классификация цефалоспоринов
| I поколение | II поколение | III поколение | IV поколение |
|---|---|---|---|
Парентеральные |
|||
Цефазолин |
Цефуроксим |
Цефотаксим |
Цефепим |
Цефтриаксон |
|||
Цефтазидим |
|||
Цефоперазон |
|||
Цефоперазон + сульбактам |
|||
Пероральные |
|||
Цефалексин |
Цефуроксим |
Цефиксим |
— |
Цефадроксил |
Цефаклор |
Цефтибутен |
— |
Фармакодинамика
Цефалоспорины оказывают бактерицидное действие, которое связано с нарушением образования клеточной стенки бактерий (см. раздел «Пенициллины»).
В ряду от I к III поколению для цефалоспоринов характерна тенденция к расширению спектра и повышению уровня активности в отношении грамотрицательных бактерий при некотором понижении активности против стафилококков. Общее для всех цефалоспоринов - отсутствие значимого действия на энтерококки, MRSA и листерии. По антианаэробный активности цефалоспорины не имеют существенных отличий от «незащищённых» пенициллинов, т.е. не действуют на B. fragilis и другие бактероиды.
Цефалоспорины I поколения активны в отношении Streptococcus spp. и метициллиночувствительных Staphylococcus spp. По антипневмококковой активности цефалоспорины I поколения уступают аминопенициллинам и большинству цефалоспоринов более поздних поколений, причём пенициллинорезистентные пневмококки характеризует полная перекрёстная устойчивость и к цефалоспоринам I поколения. Из представителей Enterobacteriaceae чувствительны только E. coli, Shigella spp., Salmonella spp. и P. mirabilis. Однако активность в отношении сальмонелл и шигелл не имеет клинического значения, а среди E. coli и P. mirabilis широко распространены устойчивые β-лактамазопродуцирующие штаммы.
Цефалоспорины II поколения, не уступая цефалоспоринам II поколения по действию на грамположительные кокки, имеют большую активность против многих грамотрицательных патогенов: H. influenzae, M. catarrhalis, гонококков, менингококков, некоторых бактерий семейства Enterobacteriaceae. Два основных представителя цефалоспоринов II поколения - цефуроксим и цефаклор - имеют некоторые различия. Цефуроксим более активен в отношении Streptococcus spp. (включая β-гемолитический стрептококк группы А и S. pneumoniae), метициллиночувствительных Staphylococcus spp., M. catarrhalis и H. influenzae (более стоек к β-лактамазам). Пневмококки, устойчивые к пенициллину, перекрёстно резистентны и к цефалоспоринам II поколения. Среди Enterobacteriaceae, помимо E. coli, Shigella spp., Salmonella spp. и P. mirabilis, чувствительны также Klebsiella spp., P. vulgaris и C. diversus.
Главная особенность антимикробного спектра цефалоспоринов III поколения - более высокая по сравнению с цефалоспоринами I и II поколений активность в отношении грамотрицательных бактерий, включая многие множественно устойчивые нозокомиальные штаммы. Это объясняют большей стабильностью цефалоспоринов III поколения к β-лактамазам, продуцируемым указанными микроорганизмами. Наряду с общими свойствами некоторые цефалоспорины III поколения имеют определённые отличия.
Базовые препараты данной группы - цефотаксим и цефтриаксон практически идентичны по своим антимикробным свойствам. Оба высокоактивны в отношении Streptococcus spp., при этом значительная часть пневмококков, устойчивых к пенициллину и цефалоспоринам I и II поколений, сохраняет чувствительность к цефотаксиму и цефтриаксону. Эта же закономерность характерна и для зеленящих стрептококков. Цефотаксим и цефтриаксон действуют на S. aureus, кроме MRSA (несколько слабее, чем цефалоспорины I и II поколений), менингококки, гонококки, H. influenzae, M. catarrhalis. Цефотаксим и цефтриаксон обладают высокой природной активностью практически против всех представителей Enterobacteriaceae. Устойчивость E. coli и Klebsiella spp. чаще всего обусловлена продукцией β-лактамаз расширенного спектра. Устойчивость Enterobacter spp., Citrobacter freundii, Serratia spp., Morganella morganii, Providencia spp. обычно связана с гиперпродукцией хромосомных β-лактамаз класса С.
К отличительным характеристикам цефтазидима и цефоперазона можно отнести выраженную (особенно у первого) активность в отношении P. aeruginosa и других неферментирующих бактерий, существенно меньшую активность против стрептококков (прежде всего S. pneumoniae), высокую чувствительность к гидролизу β-лактамазой расширенного спектра.
Пероральные цефалоспорины III поколения цефиксим и цефтибутен отличаются от цефотаксима и цефтриаксона отсутствием значимой активности в отношении Staphylococcus spp., Enterobacter spp., C. freundii, Serratia spp., M. morganii, Providencia spp. Цефтибутен, кроме того, малоактивен в отношении пневмококков и зеленящих стрептококков.
Основной представитель цефалоспоринов IV поколения - цефепим по многим характеристикам близок к цефалоспоринам III поколения, но благодаря некоторым нюансам химической структуры способен лучше проникать через внешнюю мембрану грамотрицательных бактерий и более устойчив к хромосомным β-лактамазам класса С. Поэтому наряду со свойствами, характерными для цефотаксима и цефтриаксона, цефепим проявляет высокую активность в отношении P. aeruginosa и неферментирующих бактерий (включая ряд штаммов, резистентных к цефтазидиму), активность против микроорганизмов-гиперпродуцентов хромосомных β-лактамаз класса С (Enterobacter spp., C. freundii, Serratia spp. и др). Кроме того, по сравнению с цефалоспоринами III поколения цефепим более активен в отношении стафилококков (кроме метициллинорезистентных).
Единственный ингибиторозащищённый цефалоспорин цефоперазон + сульбактам (сочетание цефалоспоринов III поколения цефоперазона с ингибитором β-лактамаз сульбактамом в соотношении 1:1) значительно более активен, чем «незащищённый» цефоперазон, в отношении микроорганизмов, вырабатывающих β-лактамазы широкого и расширенного спектров: стафилококков, H. influenzae, M. catarrrhalis, большинства штаммов семейства Enterobacteriaceae и анаэробов, включая B. fragilis. За счёт собственных антибактериальных свойств сульбактама цефоперазон + сульбактам действует на Acinetobacter spp.
Фармакокинетика
Пероральные цефалоспорины хорошо всасываются в пищеварительном тракте (табл. 20-6). Биодоступность цефиксима - 40-50%, цефалексина, цефадроксила и цефаклора - 95%. Цефуроксим в процессе всасывания гидролизуется, высвобождая активный цефуроксим, причём пища этому способствует. Поэтому биодоступность препарата выше при приёме во время или сразу после еды (52%), чем натощак (37%). Парентеральные цефалоспорины хорошо всасываются при внутримышечном введении (табл. 20-5).
Таблица 20-5. Фармакокинетические параметры парентеральных цефалоспоринов
| Препарат | Cmax, мкг/мл | T1/2, ч | Связывание с белками, % | Слик, мкг/мл* | Пути экскреции |
|---|---|---|---|---|---|
I поколение |
|||||
Цефазолин |
80 (1)* |
1,9 |
74-86 |
- |
Почки |
Цефалотин |
30 (1)* |
0,5-1 |
50-80 |
- |
Почки |
II поколение |
|||||
Цефуроксим |
100 (1,5)* |
1,2-1,8 |
33-50 |
1,1-17 |
Почки |
III поколение |
|||||
Цефотаксим |
130 (2)* |
1-1,2 |
35-40 |
5,6-44 |
Почки |
Цефтриаксон |
250 (2)* |
6,5-8 |
85-95 |
1,2-39 |
Почки (50 %), ЖВП (40 %) |
Цефтазидим |
160 (2)* |
1-2 |
17 |
0,5-30 |
Почки |
Цефоперазон |
250 (2)* |
1,6-2,1 |
87-93 |
- |
ЖВП (75 %), почки (25 %) |
IV поколение |
|||||
Цефепим |
130 (2)* |
2 |
16-19 |
- |
Почки |
Примечания: Cmax - пиковая концентрация в крови; Слик - концентрация в ликворе; - период полувыведения; ЖВП - желчевыводящие пути.
* В скобках указаны разовые дозы (г), при которых отмечались указанные Cmax .
Цефалоспорины распределяются во многие ткани, органы (кроме предстательной железы) и секреты. Высокие концентрации создаются в лёгких, почках, печени, мышцах, коже, мягких тканях, костях, синовиальной, перикардиальной, плевральной и перитонеальной жидкостях. В жёлчи наиболее высокие уровни характерны для цефтриаксона и цефоперазона.
Таблица 20-6. Фармакокинетические параметры пероральных цефалоспоринов
| Препарат | Биодоступность, % | Сmax, мкг/мл | Влияние пищи на всасывание | Т1/2 | Связывание с белками, % | Пути экскреции |
|---|---|---|---|---|---|---|
Цефалексин |
95 |
18 (0,5)* |
Снижает |
0,5-1,2 |
6-15 |
Почки |
Цефадроксил |
95 |
16 (0,5) |
Не влияет |
1,3-1,6 |
20 |
Почки |
Цефуроксим |
37-52 |
8-9 (0,5) |
Повышает |
1,3 |
33-50 |
Почки |
Цефаклор |
95 |
13 (0,5) |
Снижает |
0,5-1 |
25-50 |
Почки |
Цефиксим |
40-50 |
3,9 (0,4) |
Не влияет |
3-4 |
65-70 |
Почки (50%), ЖВП |
Цефтибутен |
65 |
11 (0,2) |
Не влияет |
2,5-4 |
65-77 |
Почки |
Примечания: Cmax - пиковая концентрация в крови; Слик - концентрация в ликворе; - период полувыведенияф; ЖВП - желчевыводящие пути.
* В скобках указаны разовые дозы (г), при которых отмечались указанные Cmax.
Способность преодолевать ГЭБ и создавать терапевтические концентрации в спинномозговой жидкости (СМЖ) в наибольшей степени выражена у цефотаксима, цефтриаксона, цефтазидима и цефепима. Цефуроксим умеренно проходит через ГЭБ только при воспалении оболочек мозга.
Большинство цефалоспоринов практически не метаболизируется. Исключение составляет цефотаксим, который трансформируется с образованием активного метаболита - дезацетилцефотаксима, пролонгирующего действие этого антибиотика. Экскрецию осуществляют преимущественно почки, в моче создаются очень высокие концентрации. Цефтриаксон и цефоперазон имеют двойной путь выведения - почками и печенью. Т1/2 большинства цефалоспоринов колеблется в пределах 1-2 ч. Более длительный Т1/2 имеют цефиксим, цефтибутен (3-4 ч) и цефтриаксон (до 8,5 ч), что обеспечивает возможность их назначения 1 раз в сутки. При почечной недостаточности режимы дозирования цефалоспоринов (кроме цефтриаксона и цефоперазона) требуют коррекции.
Показания
Основной парентеральный цефалоспорин I поколения - цефазолин, практически вытеснивший цефалотин, который обычно хуже переносится и вследствие более короткого Т1/2 , требует более частых введений. Наиболее важным показанием к применению цефазолина в настоящее время служит периоперационная антибиотикопрофилактика в хирургии. Его применяют также для лечения инфекций кожи и мягких тканей.
Пероральные цефалоспорины I поколения цефалексин и цефадроксил (табл. 20-8) рассматривают как препараты второго ряда при лечении стрептококкового тонзиллофарингита. Их используют также при нетяжёлых внебольничных инфекциях кожи и мягких тканей.
Цефуроксим применяют для лечения внебольничной пневмонии (иногда в сочетании с макролидами) у пациентов, госпитализированных в отделение общего профиля, при внебольничных инфекциях кожи и мягких тканей, инфекциях мочевыводящих путей, для периоперационной антибиотикопрофилактики в хирургии.
Цефуроксим рекомендуют для лечения острого среднего отита, острого синусита, неосложнённого обострения ХОБЛ и амбулаторных форм внебольничной пневмонии в качестве альтернативы ингибиторозащищённым аминопенициллинам.
Как цефуроксим, так и цефаклор можно использовать при внебольничных инфекциях мочевыводящих путей, нетяжёлых внебольничных инфекциях кожи и мягких тканей.
Цефуроксим и цефуроксим для приёма внутрь можно назначать ступенчато (сначала парентерально, затем внутрь).
Парентеральные цефалоспорины III поколения имеют очень широкие показания к применению. Цефотаксим и цефтриаксон применяют при лечении внебольничной пневмонии у пациентов, госпитализированных как в отделения общего профиля, так и в отделения реанимации и интенсивной терапии (возможно сочетание с макролидами или респираторными фторхинолонами). Эмпирическое назначение этих препаратов при нозокомиальной пневмонии возможно лишь в тех стационарах, где отмечают низкий уровень распространённости штаммов, продуцирующих β-лактамазы расширенного спектра, и хромосомные β-лактамазы класса С. Цефотаксим и цефтриаксон применяют также при лечении острой гонореи. Цефтриаксон можно применять трёхдневным курсом у детей с острым неосложнённым средним отитом.
Цефтазидим (более предпочтителен) и цефоперазон используют преимущественно при лечении нозокомиальной пневмонии, включая связанную с ИВЛ. Возможно также их назначение больным с тяжёлым обострением ХОБЛ в случае постоянного выделения гнойной мокроты и предшествующим обнаружением в ней синегнойной палочки, а также госпитализированным пациентам с внебольничной пневмонией тяжёлого течения при подозрении на P. aeruginosa в качестве этиологического фактора.
Парентеральные цефалоспорины (табл. 20-7) III поколения используют также при тяжёлом течении инфекций мочевыводящих путей, тяжёлых формах инфекций кожи, мягких тканей, костей, суставов, интраабдоминальных инфекциях, инфекциях органов малого таза, генерализованном сальмонеллёзе, менингите, сепсисе (как в монотерапии, так и в комбинации с антибиотиками других групп).
Таблица 20-7. Режимы дозирования парентеральных цефалоспоринов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Цефазолин |
В/в и в/м 2,0-6,0 г/сут в 2-3 введения; для профилактики - 1,0-2,0 г за 0,5-1 ч до операции (если операция более 3 ч, повторно через 4 ч) |
В/в и в/м 50-100 мг/(кгх сут) в 2-3 введения |
Цефуроксим |
В/в и в/м 2,25-4,5 г/сут в 3 введения; для профилактики - 1,5 г за 0,5-1 ч до операции (если операция более 3 ч, повторно через 4 ч) |
В/в и в/м 50-100 мг/(кгх сут) в 3-4 введения |
Цефотаксим |
В/в и в/м 3,0-8,0 г/сут в 3-4 введения; при менингите - 12-16 г/сут в 4-6 введений; при острой гонорее - 0,5 г в/м однократно |
В/в и в/м 50-100 мг/(кг х сут) в 2-3 введения; при менингите - 0,2 г/(кгх сут) в 4-6 введений |
Цефтриаксон |
В/в и в/м 1,0-2,0 г/сут в одно введение; при менингите - 2,0-4,0 г/сут в 2 введения; при острой гонорее - 0,25 г в/м однократно |
В/в и в/м 20-75 мг/(кг х сут) в 1-2 введения; при менингите - 100 мг/(кгх сут) в 2 введения (не более 4,0 г/сут); при остром среднем отите - 50 мг/кг в/м - в 1-3 инъекции (не более 1,0 г на введение) |
Цефтазидим |
В/в и в/м 3,0-6,0 г/сут в 2-3 введения |
В/в и в/м 30-100 мг/(кг х сут) в 2-3 введения; при менингите 0,2 г/(кгх сут) в 3 введения |
Цефоперазон |
В/в и в/м 4-12 г/сут в 2-4 введения |
В/в и в/м 50-100 мг/(кгх сут) в 2-3 введения |
Цефепим |
В/в и в/м 2,0-4,0 г/сут в 2 введения |
Старше 2 мес - в/в и в/м 50 мг/(кг х сут) в 3 введения; при муковисцидозе - 0,15 г/(кгх сут) в 3 введения (не более 2,0 г/сут) |
Цефоперазон/ сульбактам |
В/в и в/м 4,0-8,0 г/сут в 2 введения |
В/в и в/м 40-80 мг/сут в 2-3 введения |
Цефиксим и цефтибутен применяют при инфекциях мочевыводящих путей, а также на втором (пероральном) этапе ступенчатой терапии различных тяжёлых внебольничных и нозокомиальных грамотрицательных инфекций после достижения стойкого эффекта от применения парентеральных цефалоспоринов III поколения.
Цефалоспорин IV поколения - цефепим - применяют при тяжёлых, главным образом нозокомиальных инфекциях, вызванных полирезистентными микроорганизмами: инфекциях нижних дыхательных путей (пневмонии, абсцессе лёгкого, эмпиеме плевры); осложнённых инфекциях мочевыводящих путей; инфекциях кожи, мягких тканей, костей и суставов; интраабдоминальных инфекциях; сепсисе; инфекциях на фоне нейтропении и других иммунодефицитов.
Показания к назначению ингибиторозащищённого цефалоспорина цефоперазона + сульбактама - тяжёлые, преимущественно нозокомиальные инфекции различной локализации, вызванные полирезистентной и смешанной (аэробноанаэробной) микрофлорой.
Таблица 20-8. Режимы дозирования пероральных цефалоспоринов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Цефалексин |
0,5-1,0 г каждые 6 ч; при тонзиллофарингите - 0,5 г каждые 12 ч в течение 10 дней |
45 мг/(кгх сут) в 3 приёма; при тонзиллофарингите 12,5-25 мг/кг каждые 12 ч в течение 10 дней |
Цефуроксим для приёма внутрь |
0,25-0,5 г каждые 12 ч во время еды; при тонзиллофарингите - 0,25 г каждые 12 ч во время еды в течение 10 дней |
30 мг/(кг х сут) в 2 приёма во время еды; при среднем отите - 40 мг/(кгх сут) в 2 приёма во время еды; при тонзиллофарингите - 20 мг/(кгх сут) в 2 приёма во время еды в течение 10 дней |
Цефаклор |
0,25-0,5 г каждые 8 ч |
20-40 мг/(кгх сут) в 2-3 приёма |
Цефиксим |
0,4 г/сут в 1-2 приёма |
Старше 6 мес - 8 мг/(кгх сут) в 1-2 приёма |
Цефтибутен |
0,4 г/сут в один приём |
9 мг/(кгх сут) в 1-2 приёма |
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Обычно цефалоспорины хорошо переносятся.
Могут наблюдаться аллергические реакции (перекрёстные ко всем цефалоспоринам), причём у лиц с аллергией на пенициллины возрастает риск развития аллергических реакций на цефалоспорины I поколения. Перекрёстную аллергию отмечают у 10% людей. Поэтому при наличии в анамнезе аллергических реакций немедленного типа на пенициллины (бронхоспазм, крапивница, анафилактический шок) цефалоспорины I поколения следует применять крайне осторожно. Цефалоспорины II, III и IV поколений в таких случаях более безопасны.
Возможны боли в животе, тошнота, рвота, диарея (при появлении жидкого стула с примесью крови необходимо отменить препарат и провести исследование для исключения псевдомембранозного колита; см. гл. «Пенициллины»), положительная проба Кумбса, эозинофилия, лейкопения, нейтропения, повышение активности трансаминаз, кандидоз полости рта и/или влагалища.
Цефоперазон может нарушать синтез протромбина и некоторых других факторов свёртывания, что ведёт к гипокоагуляции и риску кровотечений.
При применении высоких доз цефтриаксона иногда отмечают сгущение жёлчи с развитием холестаза и псевдохолелитиаза.
Лекарственные взаимодействия
Фармакокинетическое. Антациды уменьшают всасывание пероральных цефалоспоринов в пищеварительном тракте (необходимы интервалы между приёмами не менее 2 ч).
Фармакодинамическое. При сочетании с аминогликозидами и/или петлевыми диуретиками, особенно у пациентов с нарушениями функции почек, возможно повышение риска нефротоксичности.
При сочетании цефоперазона с антикоагулянтами и антиагрегантами возрастает риск кровотечений, особенно желудочно-кишечных. Не рекомендуют сочетать с тромболитиками.
При употреблении алкоголя на фоне лечения цефоперазоном может развиться дисульфирамоподобная реакция.
Применение в особых ситуациях
Беременность. Цефалоспорины используют без каких-либо ограничений, хотя адекватных контролируемых исследований их безопасности для беременных и плода не проводилось.
Лактация. При использовании кормящими возможны изменение кишечной микрофлоры, сенсибилизация ребёнка, кожная сыпь, кандидоз. Применять с осторожностью. Не рекомендуют цефиксим и цефтибутен из-за отсутствия соответствующих клинических исследований.
Педиатрия. У новорождённых возможно увеличение Т1/2 цефалоспоринов в связи с замедленной почечной экскрецией. Цефтриаксон может вытеснять билирубин из связи с белками плазмы, поэтому его следует с осторожностью применять у новорождённых с гипербилирубинемией, особенно у недоношенных. Цефепим назначают с двух-, а цефиксим - с шестимесячного возраста.
Гериатрия. В связи с возрастными изменениями функций почек возможно замедление экскреции цефалоспоринов, что может потребовать коррекции режимов дозирования.
Нарушение функций почек. В связи с тем что большинство цефалоспоринов выводят из организма почки преимущественно в активном состоянии, режимы их дозирования (кроме цефтриаксона и цефоперазона) при почечной недостаточности подлежат коррекции.
Нарушение функции печени. Значительная часть цефоперазона выводится с жёлчью, поэтому при тяжёлых заболеваниях печени его дозу следует уменьшать. У пациентов с патологией печени отмечают повышенный риск гипопротромбинемии и кровотечений при использовании цефоперазона.
КАРБАПЕНЕМЫ
Карбапенемы по сравнению с пенициллинами и цефалоспоринами более устойчивы к β-лактамазам (в том числе к β-лактамазам расширенного спектра) и обладают более широким спектром активности. В последние годы карбапенемы стали подразделять на две группы. К первой относят эртапенем, характеризуемый низкой активностью в отношении неферментирующих грамотрицательных бактерий, поэтому его применение более предпочтительно при внебольничных инфекциях. Препараты второй группы - имипенем, меропенем - активны против неферментирующих грамотрицательных бактерий и используются преимущественно при нозокомиальных инфекциях (см. табл. 20-9).
Фармакодинамика
Карбапенемы обладают мощным бактерицидным действием, обусловленным нарушением образования клеточной стенки (см. гл. «Пенициллины»). По сравнению с другими β-лактамами карбапенемы быстрее проникают через наружную мембрану грамотрицательных бактерий и, кроме того, оказывают на них выраженный постантибиотический эффект.
К карбапенемам чувствительны стафилококки (кроме MRSA), стрептококки, (включая S. pneumoniae), гонококки, менингококки. Пенициллиночувствительные штаммы E. faecalis чувствительны к имипенему, но устойчивы к меропенему и эртапенему. Карбапенемы высокоактивны в отношении большинства грамотрицательных бактерий семейства Enterobacteriaceae (E. coli, Klebsiella spp., Enterobacter spp., Citrobacter spp., M. morganii, Proteus spp.), в том числе штаммов, резистентных к цефалоспоринам III и IV поколений и ингибиторозащищённым пенициллинам, продуцирующих β-лактамазы расширенного спектра и хромосомные β-лактамазы класса C. Несколько ниже активность в отношении Serratia spp. и Я. influenzae.
Имипенем и меропенем активны против P. aeruginosa и Acinetobacter spp., но в процессе их применения отмечают нарастание резистентности P. aeruginosa. При этом штаммы синегнойной палочки, которые приобрели устойчивость к имипенему, могут сохранять чувствительность к меропенему. Эртапенем не обладает значимой активностью в отношении P. aeruginosa и Acinetobacter spp.
Карбапенемы высокоактивны в отношении спорообразующих (кроме C. difficile) и неспорообразующих (включая B. fragilis) анаэробов.
Фармакокинетика
Карбапенемы применяют только парентерально. Хорошо распределяются в организме, создавая терапевтические концентрации во многих тканях и секретах. При воспалении оболочек мозга проникают через ГЭБ, создавая концентрации в СМЖ, равные 15-20% уровня в плазме крови. Имипенем не метаболизируется, меропенем подвергается незначительному метаболизму в печени с образованием единственного неактивного метаболита. Эртапенем метаболизируется с образованием неактивного производного с открытым β-лактамным кольцом. Карбапенемы выводят преимущественно почки, возможно значительное замедление элиминации при почечной недостаточности. В незначительных количествах проникают в грудное молоко.
Т1/2 имипенема у взрослых при внутривенном введении составляет 1 ч, при внутримышечном - 2-3 ч, меропенема - около 1 ч, эртапенема - 4,5 ч (это позволяет вводить эртапенем один раз в сутки).
В связи с тем что имипенем инактивируется в почечных канальцах ферментом дегидропептидазой I, не создающим терапевтических концентраций в моче, он используется в комбинации с селективным ингибитором дегидропептидазы I - циластатином.
Показания
Учитывая мощное бактерицидное действие и широкий антимикробный спектр карбапенемов, их применяют при тяжёлых инфекциях, вызванных полирезистентной и смешанной микрофлорой (табл. 20-9).
Показаниями к назначению всех карбапенемов служат осложнённые инфекции мочевыводящих путей, интраабдоминальные инфекции, инфекции органов малого таза, инфекции кожи и мягких тканей, сепсис. Имипенем и меропенем применяют при нозокомиальных инфекциях нижних дыхательных путей (пневмонии, абсцессе лёгкого, эмпиеме плевры), бактериальных инфекциях у пациентов с нейтропенией. Дополнительными показаниями для имипенема служат костно-суставные инфекции и ИЭ, для меропенема - менингит, для эртапенема - внебольничная пневмония у госпитализированных больных.
Таблица 20-9. Режимы дозирования карбапенемов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Имипенем + циластатин |
В/в 0,5-1,0 г каждые 6-8 ч (не более 4,0 г/сут); |
В/в при массе тела менее 40 кг - 15-25 мг/кг каждые 6 ч; более 40 кг - как у взрослых (не более 2,0 г/сут) |
Меропенем |
В/в 0,5-1,0 г каждые 8 ч; при менингите - 2,0 г каждые 8 ч |
Старше 3 мес - 10-20 мг/кг каждые 8 ч; при менингите, муковисцидозе - 40 мг/кг каждые 8 ч (не более 6 г/сут) |
Эртапенем |
В/в или в/м 1,0 г каждые 24 ч |
Старше 3 мес в/в или в/м 15 мг/(кгх сут) (не более 1,0 г/сут) в 2 введения |
Противопоказания
Гиперчувствительность. Имипенем + циластатин нельзя применять также при аллергии на циластатин.
Нежелательные лекарственные реакции
Аллергические реакции (возможна перекрёстная аллергия с пенициллинами). Флебит, тромбофлебит, локальная болезненность в месте введения. Глоссит, гиперсаливация, тошнота, рвота, в редких случаях - антибиотикоассоциированная диарея, псевдомембранозный колит. Головная боль, головокружение, тремор, судороги (имипенем; риск судорог увеличивается при дозе более 2 г/сут у пациентов с черепно-мозговой травмой, инсультом, эпилепсией, у людей пожилого возраста, при нарушении функции почек). Кандидоз полости рта и/или влагалища.
Лекарственные взаимодействия
Фармацевтическое. Эртапенем не следует смешивать и вводить вместе с растворами, содержащими глюкозу.
Фармакодинамическое. Карбапенемы нельзя применять в сочетании с другими β-лактамами (пенициллинами, цефалоспоринами, монобактамами) ввиду антагонизма.
Применение в особых ситуациях
Беременность. Применение у беременных допускается лишь в тех случаях, когда возможная польза превышает потенциальный риск.
Лактация. Применение у кормящих нежелательно, за исключением случаев абсолютной необходимости.
Педиатрия. У новорождённых величина Т1/2 имипенема и циластатина выше, чем у взрослых (4,0-8,5 ч). Меропенем и эртапенем нелья использовать в возрасте до 3 мес.
Гериатрия. У пациентов старше 60-65 лет возрастает риск развития судорог на фоне приёма имипенема, что требует соответствующего контроля.
Нарушение функций почек. Поскольку карбапенемы выводят из организма почки, у пациентов с нарушением их функций необходима коррекция режима дозирования.
Нарушение функции печени. Дозы карбапенемов не требуют коррекции у пациентов с патологией печени, но необходим соответствующий клиниколабораторный контроль.
МОНОБАКТАМЫ
Единственный представитель монобактамов (моноциклических β-лактамазов) - азтреонам8 имеет узкий антимикробный спектр и используется для лечения инфекций, вызванных аэробными грамотрицательными бактериями. Своеобразие спектра азтреонама обусловлено его устойчивостью ко многим β-лактамазам, продуцируемым аэробной грамотрицательной флорой, и чувствительностью к β-лактамазам стафилококков и бактероидов.
Фармакодинамика
По механизму действия азтреонам неотличим от других β-лактамов. Клиническое значение имеет активность в отношении многих представителей семейства Enterobacteriaceae (E. coli, Enterobacter spp., Klebsiella spp., Proteus spp., Serratia spp. и др.) и P. aeruginosa, в том числе нозокомиальных штаммов, устойчивых к уреидопенициллинам, цефалоспоринам и аминогликозидам.
Фармакокинетика
Азтреонам применяют только парентерально. Распределяется во многие ткани и среды организма. Проходит через ГЭБ при воспалении оболочек мозга, через плаценту, проникает в грудное молоко. Незначительно метаболизируется в печени, экскретируется преимущественно почками на 60-75% в неизменённом виде. Т1/2 в норме составляет 1,5-2 ч, при циррозе печени увеличивается до 2,5-3,5 ч, при почечной недостаточности - до 6-8 ч.
Показания
Азтреонам - препарат резерва для лечения инфекций различной локализации, вызванных аэробными грамотрицательными бактериями. Применяют при инфекциях нижних дыхательных путей (внебольничной и нозокомиальной пневмонии), органов малого таза, мочевыводящих путей, кожи, мягких тканей, костей и суставов, интраабдоминальных инфекциях, сепсисе.
Учитывая узкий антимикробный спектр азтреонама, при эмпирической терапии тяжёлых инфекций его следует назначать в сочетании с антимикробными ЛС, активными в отношении грамположительных кокков (оксациллин, цефалоспорины, линкозамиды, ванкомицин) и анаэробов (метронидазол).
Азтреонам назначают внутривенно или внутримышечно взрослым в дозе 3,0-12,0 г/сут в 3-4 введения, детям - 30-50 мг/кг каждые 6-8 ч.
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Боль или дискомфорт в животе, тошнота, рвота, диарея. Желтуха, гепатит. Флебит при внутривенном введении, боль и отёчность при внутримышечном введении. Аллергические реакции отмечают значительно реже, чем при использовании других β-лактамов.
Лекарственные взаимодействия
Фармакодинамическое. Не рекомендуют сочетать азтреонам с карбапенемами ввиду возможного антагонизма.
Применение в особых ситуациях
Беременность, лактация. Безопасность не установлена. Применять с осторожностью.
Гериатрия. У лиц пожилого возраста в связи с ослаблением функций почек может потребоваться коррекция дозы.
Нарушение функций почек. У пациентов с нарушениями функций почек экскреция азтреонама замедлена, поэтому требуется уменьшение его дозы.
Нарушение функции печени. При использовании высоких доз и длительном лечении может потребоваться уменьшение дозы на 20-25%.
Аминогликозиды
Аминогликозиды - один из ранних классов антибиотиков. Первый из них - стрептомицин - был получен в 1944 г. Выделяют три поколения аминогликозидов.
Наибольшее клиническое значение имеют аминогликозиды II и III поколений, применяемые при лечении нозокомиальных инфекций, вызванных аэробными грамотрицательными возбудителями. Аминогликозиды более токсичны по сравнению с β-лактамами, но учёт факторов риска, однократное введение всей суточной дозы, короткие курсы терапии и проведение терапевтического лекарственного мониторинга позволяют снизить риск НЛР.
Фармакодинамика
Аминогликозиды оказывают бактерицидное действие, которое связано с нарушением синтеза белка рибосомами. Степень активности зависит от их максимальной (пиковой) концентрации в сыворотке крови.
Аминогликозиды II и III поколений активны против Enterobacteriaceae (E. coli, Proteus spp., Klebsiella spp., Enterobacter spp., Serratia spp. и др.), неферментирующих грамотрицательных бактерий (P. aeruginosa, Acinetobacter spp.), стафилококков (кроме метициллинорезистентных).
Стрептомицин и канамицин действуют на Mycobacterium tuberculosis, в то время как амикацин более активен против M. avium и других атипичных микобактерий. Стрептомицин и гентамицин действуют на Enterococcus spp. (при сочетании с пенициллинами наблюдают синергизм). Стрептомицин активен против возбудителей чумы, туляремии, бруцеллёза.
Несмотря на то что аминогликозиды in vitro активны против гемофильных бактерий, шигелл сальмонелл, легионелл, клиническая эффективность при лечении соответствующих инфекций не установлена.
Фармакокинетика
В пищеварительном тракте аминогликозиды практически не всасываются. После внутримышечного введения всасываются быстро и полностью. Пиковые концентрации аминогликозидов варьируют у различных пациентов, так как зависят от объёма распределения. Объём распределения, в свою очередь, зависит от массы тела, объёма жидкости и жировой ткани, состояния пациента (при обширных ожогах и асците он повышен, а при дегидратации или мышечной дистрофии, наоборот, уменьшен).
Аминогликозиды распределяются во внеклеточной жидкости, включая сыворотку крови, лимфу, экссудат абсцессов, асцитическую, перикардиальную, плевральную, синовиальную и перитонеальную жидкость. Высокие концентрации создаются в печени, лёгких, почках; низкие - в мокроте, бронхиальном секрете, жёлчи, грудном молоке. Плохо проходят через ГЭБ (при воспалении оболочек проницаемость несколько увеличивается). У новорождённых в СМЖ достигаются более высокие концентрации, чем у взрослых.
Аминогликозиды не метаболизируются, выводятся почками в неизменённом виде, создавая высокие концентрации в моче. Скорость экскреции зависит от возраста, функций почек и сопутствующей патологии. У пациентов с лихорадкой она может быть увеличена, при снижении функций почек значительно замедляется. У пожилых людей ввиду возрастных изменений экскреция также может быть замедлена. Т1/2 всех аминогликозидов у взрослых и детей в норме составляет 2-4 ч, у новорождённых - 5-8 ч. При почечной недостаточности Т1/2 может возрастать до 70 ч и более.
Поскольку фармакокинетика аминогликозидов нестабильна, для достижения максимального клинического эффекта с одновременным снижением риска НЛР проводят терапевтический лекарственный мониторинг. При этом определяют пиковые и остаточные концентрации аминогликозидов в крови. Пиковые концентрации (через 60 мин после внутримышечного или через 15-30 мин после окончания внутривенного введения) должны составлять для гентамицина, тобрамицина и нетилмицина не менее 6-10 мкг/мл, для канамицина и амикацина - не менее 20-30 мкг/мл. Остаточные концентрации (перед очередным введением) для гентамицина, тобрамицина и нетилмицина должны быть менее 2 мкг/мл, для канамицина и амикацина - менее 10 мкг/мл. При однократном введении суточной дозы контролируют остаточную концентрацию. Проведение терапевтического лекарственного мониторинга прежде всего необходимо у пациентов с тяжёлыми инфекциями и при наличии других факторов риска токсичности аминогликозидов.
Показания
Аминогликозиды II и III поколений применяют при нозокомиальной пневмонии, пиелонефрите, интраабдоминальных инфекциях, инфекциях органов малого таза, послеоперационном или посттравматическом остеомиелите, сепсисе, лихорадке у пациентов с нейтропенией (табл. 20-10).
Как правило, их назначают в сочетании с β-лактамами, гликопептидами или антианаэробными антимикробными ЛС. Выбор аминогликозида для эмпирической терапии нозокомиальных инфекций должен учитывать локальные данные о резистентности возбудителей.
Стрептомицин и гентамицин можно применять при ИЭ (в сочетании с пенициллином или ампициллином), при туляремии. Стрептомицин и канамицин - при туберкулёзе. Стрептомицин, кроме того, используют при чуме и бруцеллёзе.
Таблица 20-10. Режимы дозирования аминогликозидов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Стрептомицин |
Парентерально 5 мг/(кг х сут) (не более 2,0 г/сут) в 1-2 введения; при туберкулёзе - 0,75-1,0 г/сут в 1 введение в/м, 2 раза в нед |
Парентерально 15 мг/(кг х сут) (не более 2,0 г/сут) в 1-2 введения; при туберкулёзе - 20 мг/(кг х сут) в 1 введение 2 раза в нед |
Канамицин |
Парентерально 15 мг/(кгх сут) в 1-2 введения |
Парентерально 15 мг/(кгх сут) в 1-2 введения |
Гентамицин |
Парентерально 3-5 мг/(кгх сут) в 1-2 введения; местно закапывают по 1-2 капли в поражённый глаз 3-4 раза в сут |
Парентерально 3-5 мг/(кгх сут) в 1-2 введения |
Тобрамицин |
Парентерально 3-5 мг/(кгх сут) в 1-2 введения; местно закапывают по 1-2 капли в поражённый глаз 3-4 раза в сут |
Парентерально 3-5 мг/(кгх сут) в 1-2 введения |
Нетилмицин |
Парентерально 4-7,5 мг/(кгх сут) в 1-2 введения |
Парентерально 4-7,5 мг/(кгх сут) в 1-2 введения |
Амикацин |
Парентерально 15-20 мг/(кгх сут) в 1-2 введения |
Парентерально 15-20 мг/(кгх сут) в 1-2 введения |
Примечание . «В/м» - внутримышечно.
Противопоказания
Гиперчувствительность
Нежелательные лекарственные реакции
Классическая триада НЛР аминогликозидов представлена нефротоксичностью, ото-вестибулотоксичностью и нервно-мышечной блокадой.
Нефротоксичность может проявляться полиурией или, наоборот, олигоурией, жаждой, повышением концентрации креатинина крови, снижением его клиренса. Факторы риска: исходные нарушения функций почек, пожилой возраст, высокие дозы, длительные курсы терапии, одновременное применение других нефротоксичных препаратов. Меры контроля: повторные анализы мочи, определение концентрации креатинина крови и расчёт его клиренса каждые 3 дня (при снижении последнего на 50% аминогликозиды следует отменить).
Ото-вестибулотоксичность: снижение слуха, шум, звон или заложенность в ушах, нарушение координации движений, головокружение. Факторы риска: пожилой возраст, исходные нарушения слуха, использование высоких доз, длительные курсы лечения, одновременное назначение других ототоксичных препаратов. Меры профилактики: контроль функции слуха и вестибулярного аппарата, включая проведение специальных проб.
Нервно-мышечная блокада проявляется угнетением дыхания вплоть до полного паралича дыхательных мышц. Факторы риска: исходные неврологические заболевания (паркинсонизм, миастения), ботулизм, одновременное или предшествующее применение миорелаксантов, нарушение функций почек.
Аллергические реакции возникают редко.
Лекарственные взаимодействия
Фармацевтическое. Нельзя смешивать в одном шприце или одной инфузионной системе с β-лактамами и гепарином натрия вследствие физико-химической несовместимости.
Фармакокинетическое. Индометацин, фенилбутазон и другие НПВС, нарушающие почечный кровоток, могут замедлять экскрецию аминогликозидов.
Фармакодинамическое. Усиление токсических эффектов при сочетании с другими нефро- и ототоксичными препаратами: полимиксином В, амфотерицином В, этакриновой кислотой, фуросемидом, ванкомицином.
Усиление нервно-мышечной блокады при одновременном применении средств для ингаляционного наркоза, опиоидных анальгетиков, магния сульфата и переливании больших объёмов крови с цитратными консервантами.
Применение в особых ситуациях
Беременность. Аминогликозиды проходят через плаценту и могут оказывать токсическое действие на плод. Применение у беременных возможно только по жизненным показаниям.
Лактация. Аминогликозиды проникают в грудное молоко в низких концентрациях. У женщин, кормящих грудью, применять с осторожностью.
Педиатрия. У недоношенных и новорождённых Т1/2 аминогликозидов увеличен за счёт пониженной функции почек, что может привести к накоплению и токсическому действию аминогликозидов. Применять с осторожностью.
Гериатрия. У пожилых лиц повышен риск нефро- и ототоксичности аминогликозидов. Их необходимо дозировать в соответствии с возрастом, массой тела и функциями почек. Не следует назначать максимальные дозы.
Нарушение функций почек. Аминогликозиды выводят из организма почки в неизменённом виде, поэтому при почечной недостаточности значительно увеличен их Т1/2 .
Необходимо корректировать дозы с учётом снижения клиренса креатинина, по возможности проводить терапевтический лекарственный мониторинг.
Неврологические заболевания. При паркинсонизме, миастении и ботулизме возрастает риск развития тяжёлой нервно-мышечной блокады.
Хинолоны
Класс хинолонов, применяемых в клинической практике с начала 60-х гг. прошлого века, включает две основные группы препаратов, различающихся по структуре, активности, фармакокинетике и широте показаний к применению: нефторированные хинолоны и фторхинолоны. По классификации R. Quintiliani (1999) хинолоны разделяют на четыре поколения.
Хинолоны I поколения активны преимущественно в отношении грамотрицательной микрофлоры. Они создают терапевтические концентрации только в мочевыводящих путях и пищеварительном тракте. Фторхинолоны характеризуются широким спектром антимикробного действия и хорошей фармакокинетикой, что позволяет применять их для лечения инфекций различной этиологии и локализации. Наличие у ряда препаратов лекарственных форм для внутривенного введения и приёма внутрь позволяет проводить ступенчатую терапию.
Фармакодинамика
Хинолоны обладают бактерицидным эффектом. Ингибируя два жизненно важных фермента микробной клетки - ДНК-гиразу и топоизомеразу IV, они нарушают синтез ДНК.
Хинолоны I поколения действуют на грамотрицательные бактерии семейства Enterobacteriaceae (Е. coli, Proteus spp., Shigella spp., Salmonella spp. и др.), Haemophilus spp. и Neisseria spp.
Фторхинолоны имеют значительно более широкий спектр. Они активны в отношении многих грамположительных аэробных бактерий (Staphylococcus spp., Strep tococcus spp., Bacillus anthracis и др.), большинства грамотрицательных бактерий, в том числе Е. coli (включая энтеротоксигенные штаммы), Shigella spp., Salmonella spp., Enterobacter spp., Klebsiella spp., Proteus spp., Serratia spp., Providencia spp., Citrobacter spp., M. morganii, Vibrio spp., Haemophilus spp., Neisseria spp., Pasteurella spp., Pseudomonas spp., Legionella spp., Brucella spp., Listeria spp., Yersinia spp., Mycobacterium spp. Фторхинолоны, как правило, активны против бактерий, устойчивых к хинолонам I поколения.
Фторхинолоны III и IV поколений высокоактивны в отношении пневмококков и стафилококков. По сравнению с препаратами II поколения они более активны против внутриклеточных возбудителей (Chlamydia spp., Mycoplasma spp.), M. tuberculosis. К фторхинолонам IV поколения чувствительны также анаэробы (кроме C. difficile).
Фторхинолоны III и IV поколений иногда называют «респираторными» фторхинолонами, хотя их терапевтические возможности существенно шире.
Фармакокинетика
Хинолоны хорошо всасываются в пищеварительном тракте. Пища может замедлять их всасывание, но существенного влияния на биодоступность не оказывает.
Хинолоны I поколения не создают терапевтических концентраций в крови, органах и тканях. Налидиксовая и оксолиновая кислоты метаболизируются в печени, выводятся в виде активных и неактивных метаболитов. Пипемидовая кислота экскретируется практически в неизменённом виде. Т1/2 налидиксовой кислоты составляет 1-2,5 ч, пипемидовой - 3-4 ч, оксолиновой - 6-7 ч. При нарушении функций почек эти величины значительно возрастают.
Фторхинолоны создают высокие концентрации во многих органах, тканях и средах организма, проникают внутрь клеток. Исключение составляет норфлоксацин, наиболее высокие концентрации которого отмечают в кишечнике, мочевыводящих путях и предстательной железе. Ципрофлоксацин, офлоксацин, левофлоксацин и пефлоксацин проходят через ГЭБ, достигая терапевтических концентраций в СМЖ.
В печени в наибольшей степени метаболизируется пефлоксацин, в наименьшей (менее 5%) - ломефлоксацин, офлоксацин, левофлоксацин.
Т1/2 норфлоксацина составляет 3-4 ч, ципрофлоксацина - 4-6 ч, офлоксацина - 4,5-7 ч, левофлоксацина и гемифлоксацина - 6-8 ч, пефлоксацина и моксифлоксацина - 8-13 ч, спарфлоксацина - 18-20 ч.
Большинство фторхинолонов выводят преимущественно почки. При нарушении функций почек выведение замедляется, наиболее значительно удлиняется Т1/2 офлоксацина, левофлоксацина и ломефлоксацина. При тяжёлой почечной недостаточности необходима коррекция доз всех фторхинолонов. При тяжёлых нарушениях функции печени может потребоваться коррекция дозы пефлоксацина.
Показания
Хинолоны I поколения применяют при остром цистите и для противорецидивной терапии при хронических формах инфекций мочевыводящих путей. Налидиксовая кислота может быть также использована при шигеллёзе и бактериальных энтероколитах.
Фторхинолоны используют значительно шире. Их применяют при ЛОРинфекциях (синусите, злокачественном наружном отите), инфекциях нижних дыхательных путей (обострении ХОБЛ, внебольничной и нозокомиальной пневмонии, легионеллёзе), кишечных инфекциях (шигеллёзе, брюшном тифе, генерализованном сальмонеллёзе, иерсиниозе, холере), интраабдоминальных инфекциях, инфекциях органов малого таза, мочевыводящих путей, кожи, мягких тканей, костей, суставов, глаз, простатите, гонорее, мягком шанкре, сепсисе, бактериальных инфекциях у пациентов с муковисцидозом, нейтропенической лихорадке (см. табл. 20-11).
Показаниями к назначению отдельных фторхинолонов II поколения служат вторичный гнойный менингит (ципрофлоксацин, офлоксацин, пефлоксацин), лекарственно-устойчивый туберкулёз (ципрофлоксацин, офлоксацин, ломефлоксацин в составе комбинированной терапии), зоонозные инфекции - сибирская язва, чума, туляремия (ципрофлоксацин, офлоксацин, левофлоксацин, моксифлоксацин).
Фторхинолоны III и IV поколений применяют при хламидийной и микоплазменной инфекции.
Норфлоксацин с учётом особенностей фармакокинетики используют только при кишечных инфекциях, инфекциях мочевыводящих путей и простатите.
Противопоказания
Все хинолоны противопоказаны при гиперчувствительности к ним и беременности. Кроме того, хинолоны I поколения не принимают при тяжёлых нарушениях функций печени и почек, тяжёлом церебральном атеросклерозе, фторхинолоны не назначают детям до 18 лет (возможно применение ципрофлоксацина по жизненным показаниям), женщинам при кормлении грудью.
Нежелательные лекарственные реакции
Все хинолоны могут вызывать изжогу, боль в животе, нарушение аппетита, тошноту, рвоту, диарею, головную боль, головокружение, нарушения слуха, парестезии, тремор, судороги, аллергические реакции, фотосенсибилизацию (чаще при приёме ломефлоксацина и спарфлоксацина; необходимо исключить пребывание на солнце и ультрафиолетовое облучение).
При использовании хинолонов I поколения возможны тромбоцитопения, лейкопения, холестатическая желтуха, гепатит.
Фторхинолоны в редких случаях могут вызывать НЛР со стороны опорнодвигательного аппарата (артропатия, артралгия, тендинит, разрыв сухожилий), почек (кристаллурия, транзиторный нефрит), сердца (удлинение интервала Q-T).
Таблица 20-11. Режимы дозирования хинолонов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Налидиксовая кислота |
0,5-1,0 г каждые 6 ч |
Старше 3 мес - 55 мг/(кгх сут) в 4 приёма |
Оксолиновая кислота |
0,5-0,75 г каждые 12 ч |
Старше 2 лет - 0,25 г каждые 12 ч |
Пипемидовая кислота |
0,4 г каждые 12 ч |
Старше 1 года - 15 мг/(кгх сут) в 2 приёма |
Ломефлоксацин |
Внутрь 0,4-0,8 г/сут в 1-2 приёма; местно закапывают по 1-2 капли в поражённый глаз каждые 4 ч, при тяжёлом течении - каждый час до улучшения |
Не применяют |
Норфлоксацин |
Внутрь 0,2-0,4 г каждые 12 ч; при остром цистите у женщин - 0,4 г каждые 12 ч в течение 3 дней; при острой гонорее - 0,8 г однократно; |
Не применяют |
Офлоксацин |
Внутрь 0,2-0,4 г каждые 12 ч; при остром цистите у женщин - 0,1 г каждые 12 ч в течение 3 дней; при острой гонорее - 0,4 г однократно; в/в 0,2-0,4 г/сут в 1-2 введения; местно (см. норфлоксацин) |
Не применяют |
Пефлоксацин |
Внутрь 0,8 г на первый приём, далее по 0,4 г каждые 12 ч; при остром цистите у женщин и острой гонорее - 0,8 г однократно; |
Не применяют |
Ципрофлоксацин |
Внутрь 0,25-0,75 г каждые 12 ч; при остром цистите у женщин - 0,1 г каждые 12 ч в течение 3 дней; при острой гонорее - 0,5 г однократно; таблетки замедленного высвобождения - 0,5-1,0 г каждые 24 ч; в/в 0,4-0,6 г каждые 12 ч; местно (см. норфлоксацин) |
Внутрь 10-15 мг/(кг х сут) в 2 приёма (не более 1,5 г в сут); в/в 7,5-10 мг/(кгх сут) в 2 введения (не более 0,8 г в сут)* |
Левофлоксацин |
Внутрь 0,25-0,5 г каждые 12-24 ч; при остром синусите - 0,5 г раз в сут; при пневмонии и тяжёлых формах инфекций - 0,5-0,75 г каждые 12 ч; в/в 0,25-0,5 г каждые 12-24 ч |
Не применяют |
Спарфлоксацин |
Внутрь в первый день 0,2-0,4 г в один приём, в последующие дни - 0,1-0,2 г раз в сут |
Не применяют |
Моксифлоксацин |
Внутрь и в/в 0,4 г каждые 24 ч |
Не применяют |
Гемифлоксацин |
Внутрь 0,32 г 1 раз в сут |
Не применяют |
* Только по жизненным показаниям.
Лекарственные взаимодействия
Фармакокинетическое. Антациды и другие ЛС, содержащие ионы магния, цинка, железа, висмута, снижают биодоступность хинолонов вследствие образования невсасывающихся хелатных комплексов.
Пипемидовая кислота, ципрофлоксацин, норфлоксацин и пефлоксацин за счёт ингибирования цитохрома P-450 нарушают печёночный метаболизм метилксантинов (теофиллин, кофеин) и варфарина, повышая их накопление в организме. В последнем случае возможно повышение риска кровотечений, может понадобиться коррекция дозы антикоагулянта.
Фармакодинамическое. При сочетании с НПВС, нитроимидазолами и метилксантинами повышается риск нейротоксичности.
Хинолоны проявляют антагонизм с нитрофуранами, поэтому следует избегать таких комбинаций.
При сочетании с ЛС, удлиняющими интервал Q-T, увеличивается риск развития нарушений сердечного ритма.
При сочетании с глюкокортикоидами повышается риск разрыва сухожилий, особенно у пожилых.
При сочетании ципрофлоксацина, норфлоксацина и пефлоксацина с ЛС, ощелачивающими мочу (ингибиторы карбоангидразы, цитраты, натрия бикарбонат), повышается риск кристаллурии.
Применение в особых ситуациях
Беременность. В связи с данными о развитии артропатий у неполовозрелых животных применять при беременности не рекомендовано. Исключение - применение ципрофлоксацина и офлоксацина для лечения и профилактики сибирской язвы и чумы.
Лактация. При назначении хинолонов кормящим матерям рекомендуют перевести ребёнка на искусственное вскармливание.
Педиатрия. Налидиксовая кислота противопоказана детям до 3 мес, пипемидовая - до 1 года, оксолиновая - до 2 лет. Фторхинолоны не рекомендуют назначать детям и подросткам. Допускают их назначение по жизненным показаниям при неэффективности предшествующей терапии (обострение инфекции при муковисцидозе; тяжёлые инфекции различной локализации, вызванные полирезистентными штаммами бактерий; сепсис; менингит; инфекции при нейтропении, сибирская язва, чума).
Гериатрия. У пожилых людей увеличивается риск разрыва сухожилий, особенно при сочетании фторхинолонов с глюкокортикоидами.
Заболевания ЦНС. Хинолоны оказывают возбуждающее действие на ЦНС, поэтому их не рекомендуют применять пациентам с судорожным синдромом в анамнезе. Риск развития судорог повышается у больных с нарушениями мозгового кровообращения, эпилепсией и паркинсонизмом.
Нарушения функций почек и печени. Хинолоны I поколения нельзя применять при почечной и печёночной недостаточности, так как ввиду кумуляции препаратов и их метаболитов повышается риск токсических эффектов. Дозы фторхинолонов при тяжёлой почечной недостаточности подлежат коррекции.
Макролиды
Структурную основу макролидов составляет макроциклическое лактонное кольцо. В зависимости от числа атомов углерода в кольце макролиды подразделяют на 14-членные (кларитромицин, рокситромицин, эритромицин), 15-членные (азитромицин) и 16-членные (джозамицин, мидекамицин, спирамицин) (табл. 20-12). Основное клиническое значение имеет активность в отношении грамположительных кокков и внутриклеточных возбудителей (микоплазмы, хламидии, легионеллы, кампилобактерии).
Таблица 20-12. Классификация макролидов
| Макролиды | ||
|---|---|---|
14-членные |
15-членные (азалиды) |
16-членные |
Природные |
||
Эритромицин |
— |
Спирамицин |
Джозамицин |
||
Мидекамицин |
||
Полусинтетические |
||
Кларитромицин |
Азитромицин |
Мидекамицина ацетат |
Рокситромицин |
— |
— |
Фармакодинамика
Антимикробный эффект обусловлен нарушением синтеза белка на рибосомах бактериальной клетки за счёт связывания с каталитическим центром рибосомальной 50S-субъединицы. Как правило, макролиды обладают бактериостатическим действием, но в ряде случаев (высокие концентрациии, низкая микробная обсеменённость) на β-гемолитические стрептококки группы А и пневмококки способны действовать бактерицидно. Многие макролиды оказывают также противовоспалительное и иммуномодулирующее действие. Они способны регулировать такие функции нейтрофилов, как фагоцитоз, хемотаксис, киллинг. 14-членные макролиды ингибируют окислительный «взрыв», уменьшая образование агрессивных кислородных радикалов, способных повреждать не только бактериальные клетки, но и собственные ткани.
К макролидам чувствительны β-гемолитические стрептококки группы А, S. pneumoniae, S. aureus (кроме MRSA). В последние годы отмечено нарастание резистентности, но при этом 16-членные макролиды могут сохранять активность в отношении некоторых β-гемолитических стрептококков группы А и пневмококков, устойчивых к 14- и 15-членным препаратам.
Макролиды действуют на возбудителей коклюша и дифтерии, моракселлы, легионеллы, кампилобактерии, листерии, спирохеты, хламидии, микоплазмы, уреаплазмы, некоторые анаэробы (активность против B. fragilis не имеет клинического значения).
Азитромицин превосходит другие макролиды по активности в отношении Я. influenzae, а кларитромицин - против Я. pylori и атипичных микобактерий (M. avium и др.). Кларитромицин действует на Я. influenzae за счёт образования активного метаболита - 14-гидроксикларитромицина. Спирамицин, азитромицин и рокситромицин проявляют наиболее высокую активность в отношении некоторых простейших (Toxoplasma gondii, Cryptosporidium spp.). Азитромицин активен против Shigella spp.
Фармакокинетика
Всасывание макролидов в пищеварительном тракте зависит от вида препарата, лекарственной формы и присутствия пищи (табл. 20-13). Пища значительно уменьшает биодоступность эритромицина, в меньшей степени - рокситромицина, азитромицина и мидекамицина и практически не влияет на биодоступность кларитромицина, джозамицина и спирамицина. Биодоступность полусинтетического препарата мидекамицина ацетата несколько выше, чем у природного мидекамицина.
Концентрации в сыворотке крови значительно ниже тканевых и варьируют у различных препаратов. Наиболее высокие сывороточные концентрации характерны для рокситромицина, самые низкие - для азитромицина.
Макролиды в различной степени связываются с белками плазмы крови. Наибольшее связывание отмечено у рокситромицина (более 90%), наименьшее - у джозамицина (15%). Макролиды хорошо распределяются в организме, создавая высокие концентрации в различных тканях и органах (в том числе в предстательной железе), особенно при воспалении. При этом макролиды проникают внутрь клеток и создают высокие внутриклеточные концентрации, ряд препаратов способен накапливаться в полиморфноядерных нейтрофилах, макрофагах, моноцитах. Плохо проникают через ГЭБ и гематоофтальмический барьер. В небольшой степени проходят через плаценту, проникают в грудное молоко.
Таблица 20-13. Фармакокинетические свойства макролидов
| Препарат | Биодоступность, % | Связывание с белками, % | ПФК, (мг х ч)/л | Т1/2, ч |
|---|---|---|---|---|
Эритромицин |
30-65 |
74 |
5,8-11,2 (0,5) |
1,5-2,5 |
Кларитромицин |
50-55 |
70 |
15,9 (0,5) |
3-7 |
Рокситромицин |
50 |
92 |
53,0-81,0 (0,15) |
10-12 |
Азитромицин |
37 |
23-50 |
6,7 (0,5) |
35-55 |
Джозамицин |
Нет данных |
15 |
7,9 (1,0) |
1,5-2,5 |
Мидекамицин |
Нет данных |
47 |
Нет данных |
1,0-1,5 |
Спирамицин |
10-60 |
18 |
8,5 (2,0) |
6-12 |
В скобках указана доза в граммах, при которой установлено данное значение ПФК.
Метаболизируются макролиды в печени при участии микросомальной системы цитохрома P-450, метаболиты выводятся преимущественно с жёлчью. Почечная экскреция составляет 5-10%. Т1/2 мидекамицина составляет 1-1,5 ч, эритромицина и джозамицина - 1,5-2,5 ч, кларитромицина - 3-8 ч, спирамицина - 6-12 ч, рокситромицина - 10-12 ч, азитромицина - 35-55 ч. При почечной недостаточности у большинства макролидов (кроме кларитромицина) эти величины существенно не изменяются. При печёночной недостаточности возможно значительное удлинение Т1/2 эритромицина, рокситромицина, спирамицина, мидекамицина и джозамицина.
Показания
Макролиды рассматривают как препараты выбора при амбулаторных формах внебольничной пневмонии у лиц моложе 50 лет и как альтернативные - при нетяжёлых обострениях ХОБЛ без тяжёлых сопутствующих заболеваний, стрептококковом тонзиллофарингите, остром синусите, остром среднем отите.
Показаниями к назначению служат также коклюш, дифтерия (в сочетании с антидифтерийной сывороткой), инфекции кожи и мягких тканей, урогенитальные инфекции хламидиоз, микоплазмоз, сифилис (кроме нейросифилиса), мягкий шанкр, венерическая лимфогранулёма, инфекции полости рта (периодонтит, периостит, гингивит), тяжёлая угревая сыпь (см. табл. 20-14).
Эритромицин и азитромицин применяют при кампилобактерном гастроэнтерите, кларитромицин - для эрадикация H. pylori при язвенной болезни (в составе комбинированной терапии), азитромицин - при шигеллёзе у детей, спирамицин - при токсоплазмозе, азитромицин и кларитромицин - для профилактики и лечения инфекции M. avium при ВИЧ-инфекции.
Иммуномодулирующие свойства макролидов используют при диффузном панбронхиолите (эритромицин, рокситромицин, кларитромицин) и муковисцидозе (азитромицин).
Профилактическое применение включает:
-
профилактику коклюша и дифтерии у людей, находившихся в тесном контакте с больными; круглогодичную профилактику ревматической лихорадки при аллергии на пенициллин (эритромицин);
-
профилактику эндокардита при стоматологических манипуляциях, вмешательствах на полости рта, дыхательных путях, пищеводе при аллергии на β-лактамы (азитромицин, кларитромицин).
Таблица 20-14. Режимы дозирования макролидов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Эритромицин |
Внутрь (за 1 ч до еды) 0,25-0,5 г каждые 6 ч; при тонзиллофарингите - 0,25 г каждые 8-12 ч; для профилактики ревматической лихорадки - 0,25 г каждые 12 ч; в/в 0,5-1,0 г каждые 6 ч |
Внутрь (за 1 ч до еды) 40-50 мг/(кг х сут) в 3-4 приёма (можно применять ректально); в/в 30 мг/(кгх сут) в 2-4 введения |
Кларитромицин |
Внутрь 0,25-0,5 г каждые 12 ч; для профилактики эндокардита - 0,5 г за 1 ч до процедуры; таблетки с замедленным высвобождением - 1,0 г каждые 24 ч (во время еды); в/в 0,5 г каждые 12 ч |
Старше 6 мес - внутрь 15 мг/(кгх сут) в 2 приёма; для профилактики эндокардита - 15 мг/кг за 1 ч до процедуры |
Рокситромицин |
Внутрь (за 1 ч до еды) 0,3 г/сут в 1-2 приёма |
Внутрь (за 1 ч до еды) 5-8 мг/(кгх сут) в 2 приёма |
Азитромицин |
Внутрь (за 1 ч до еды) 0,5 г/сут в течение 3 дней или в 1-й день 0,5 г, 2-5-й дни - по 0,25 г в один приём; при остром хламидийном уретрите и цервиците - 1,0 г однократно; в/в 0,5 г каждые 24 ч |
Внутрь (за 1 ч до еды) 10 мг/(кгх сут) в течение 3 дней или в 1-й день 10 мг/кг, 2-5-й дни - по 5 мг/кг в один приём; в/в (старше 16 лет) 0,5 г каждые 24 ч |
Спирамицин |
Внутрь 1,5-3 млн МЕ/сут каждые 8-12 ч; в/в 1,5-3 млн МЕ/сут каждые 8 ч |
Внутрь при массе тела 10-20 кг 1,5 МЕ каждые 12 ч; более 20 кг - 750 тыс. МЕ/10 кг каждые 12 ч |
Джозамицин |
Внутрь 0,5 г каждые 8 ч или 1,0 г каждые 12 ч; при хламидиозе у беременных - 0,75 мг каждые 12 ч |
Внутрь 30-50 мг/(кгх сут) в 2-3 приёма |
Мидекамицин |
Внутрь (за 1 ч до еды) взрослые и дети старше 12 лет - 0,4 г каждые 8 ч |
— |
Мидекамицина ацетатP |
— |
Внутрь (за 1 ч до еды) до 12 лет - 30-50 мг/(кгх сут) в 2-3 приёма |
Примечание: В/в - внутривенно.
Противопоказания
Гиперчувствительность, беременность (кларитромицин, мидекамицин, рокситромицин); кормление грудью (кроме эритромицина).
Нежелательные лекарственные реакции
Макролиды - один из самых безопасных классов антимикробных ЛС.
Возможны НЛР со стороны пищеварительного тракта (боль или дискомфорт, тошнота, рвота, диарея - чаще при приёме эритромицина за счёт прокинетического действия), печени (транзиторное повышение активности трансаминаз, холестатический гепатит), ЦНС (головная боль, головокружение, обратимые нарушения слуха; чаще при внутривенном введении), сердца (удлинение интервала Q-T [эритромицин, кларитромицин], флебит и тромбофлебит при внутривенном введении «необходимо вводить только путём медленной инфузии»). Аллергические реакции возникают крайне редко.
Лекарственные взаимодействия
Фармакокинетическое. Большинство взаимодействий обусловлено угнетением цитохрома P-450 (преимущественно CYP3A4) в печени. По степени сродства к этой ферментной системе и, следовательно, вероятности взаимодействий макролиды делят на три группы:
Макролиды ингибируют метаболизм и повышают концентрацию в крови варфарина, теофиллина, карбамазепина, бромокриптина, вальпроевой кислоты, дизопирамида 8, препаратов спорыньи, циклоспорина, мидазолама, триазолама8, ингибиторов протонного насоса (омепразол, лансопразол), что повышает риск развития НЛР, свойственных перечисленным ЛС, и может потребовать коррекции режима их дозирования. Не рекомендуют сочетать макролиды с терфенадином8, астемизолом8, цизапридом8, пимозидом8 (риск тяжёлых нарушений сердечного ритма), с осторожностью применять вместе со статинами (возрастает риск развития рабдомиолиза). Макролиды могут увеличивать биодоступность дигоксина при приёме внутрь за счёт ослабления его инактивации кишечной микрофлорой.
Рифампицин усиливает метаболизм макролидов в печени и снижает их концентрацию в крови.
Фармакодинамическое. Макролиды не следует сочетать с линкозамидами ввиду сходного механизма действия и возможной конкуренции.
Применение в особых ситуациях
Беременность. Азитромицин, джозамицин и спирамицин не оказывают отрицательного действия на плод и могут быть назначены беременным. При применении эритромицина на ранних сроках беременности (I триместр) отмечено увеличение риска развития врождённых аномалий со стороны сердечно-сосудистой системы. Другие макролиды противопоказаны.
Лактация. Большинство макролидов проникает в грудное молоко. Информация о безопасности для ребёнка, находящегося на грудном вскармливании, имеется только для эритромицина. Применения других макролидов женщинам, кормящим грудью, следует по возможности избегать.
Педиатрия. Безопасность кларитромицина у детей до 6 мес не установлена. Т1/2 рокситромицина может увеличиваться до 20 ч. Эритромицин повышает риск развития гипертрофического пилоростеноза у новорождённых.
Гериатрия. Учитывать возможные возрастные изменения функции печени и повышенный риск нарушений слуха.
Нарушение функций почек. При снижении клиренса креатинина менее 30 мл/мин Т1/2 кларитромицина может увеличиваться до 30-45 ч, поэтому необходима коррекция режима его дозирования.
Нарушение функции печени. При тяжёлых заболеваниях печени применять с осторожностью, так как может увеличиваться Т1/2 и возрастать риск гепатотоксичности; может потребоваться коррекция режимов дозирования (кроме азитромицина и кларитромицина).
Заболевания сердца. С осторожностью использовать при удлинении интервала Q-T, особенно эритромицин и кларитромицин.
Кетолиды
Кетолиды - новый подкласс полусинтетических 14-членных макролидных антибиотиков, в лактонном кольце которых присутствует кетонная группа. Единственный используемый в практике кетолид в настоящее время - телитромицин.
Фармакодинамика
Телитромицин связывается с 50S-субъединицей рибосомальной рибонуклеиновой кислоты (РНК) бактериальной клетки и ингибирует синтез белка на этапе трансляции. Различия в участках связывания с 50S-субъединицей рибосомы у кетолидов и макролидов обусловливает отсутствие перекрёстной резистентности микроорганизмов.
Активен в отношении Streptococcus spp. (включая полирезистентные штаммы), S. aureus (за исключением MRSA), C. diphtheriae, M. catarrhalis, Я. influenzae, B. pertussis, Chlamydia spp., Mycoplasma spp., Legionella spp.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 57%, не зависит от приёма пищи. Связывание с белками плазмы составляет 60-70%. Быстрое распределение телитромицина в тканях приводит к созданию значительно более высоких тканевых концентраций по сравнению с его уровнем в плазме. Проникает в грудное молоко. На 70% метаболизируется в печени. Экскретируется преимущественно через пищеварительный тракт. Т1/2 - 10 ч.
Показания
Телитромицин применяют как альтернативный препарат (например, при аллергии к пенициллинам и устойчивости к макролидам) при остром синусите, тонзиллофарингите, амбулаторных формах внебольничной пневмонии, нетяжёлом обострении ХОБЛ.
Назначают внутрь взрослым и детям старше 12 лет в дозе 0,8 г 1 раз в сутки.
Противопоказания
Гиперчувствительность, удлинение интервала Q-T на ЭКГ, беременность, кормление грудью, возраст до 12 лет.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота, диарея, изменение вкуса. Повышение активности трансаминаз, холестатическая желтуха, гепатит. Головная боль, головокружение, сонливость, бессонница, парестезии, нарушения зрения, тремор. Сердцебиение, аритмия, снижение АД, брадикардия. Аллергические реакции (редко).
Лекарственные взаимодействия
Фармакокинетическое. Телитромицин, являясь ингибитором цитохрома P-450 (CYP3A4), уменьшает клиренс симвастатина. При сочетании с аторвастатином и ловастатином увеличивается риск развития миопатий. При одновременном применении цизаприда 8, пимозида8, астемизола8, терфенадина8 повышается риск удлинения интервала Q-T и развития аритмий. Одновременный приём телитромицина, итраконазола, кетоконазола и метопролола приводит к увеличению концентрации этих ЛС в плазме. Телитромицин способен увеличивать плазменные концентрации дигоксина, повышая тем самым риск гликозидной интоксикации. При одновременном применении варфарина необходим строгий контроль коагулограммы. Рифампицин, фенитоин и карбамазепин снижают концентрацию телитромицина в плазме и ослабляют его эффект.
Применение в особых ситуациях
Беременность, лактация. Адекватных исследований безопасности не проводилось. Применять не рекомендуется.
Педиатрия. Безопасность у детей в возрасте до 12 лет не установлена. Применение в этой возрастной группе противопоказано.
Нарушение функций почек. При клиренсе креатинина менее 30 мл/мин дозу следует уменьшить в два раза.
Нарушение функции печени. Повышается риск гепатотоксичности. Следует применять с осторожностью.
Миастения. Возможно обострение миастении. Отмечены случаи развития острой дыхательной недостаточности у пациентов с миастенией, принимавших телитромицин.
Линкозамиды
Группа включает природный антибиотик линкомицин и его полусинтетический аналог клиндамицин, обладающие узким спектром антимикробной активности. Их используют при инфекциях, вызванных грамположительными кокками (преимущественно в качестве препаратов второго ряда) и неспорообразующей анаэробной микрофлорой. У микрофлоры, особенно стафилококков, довольно быстро развивается резистентность к линкозамидам, перекрёстная к обоим препаратам. Возможна перекрёстная резистентность с макролидами.
Фармакодинамика
Линкозамиды обладают бактериостатическим эффектом, обусловленным ингибированием синтеза белка рибосомами (см. гл. «Макролиды»). В высоких концентрациях на высокочувствительные микроорганизмы могут действовать бактерицидно.
Чувствительны стафилококки (в том числе некоторые внебольничные штаммы MRSA), стрептококки, пневмококки и неспорообразующие анаэробы (включая большинство штаммов B. fragilis). Клиндамицин умеренно активен в отношении некоторых простейших - токсоплазм, пневмоцист, Plasmodium falciparum.
Фармакокинетика
Линкозамиды достаточно быстро всасываются в пищеварительном тракте. При этом биодоступность клиндамицина значительно выше (90%), чем линкомицина (30% натощак, 5% после еды), и не зависит от приёма пищи.
Распределяются в большинстве тканей и сред организма, за исключением СМЖ. Высокие концентрации достигаются в бронхолёгочном секрете, костной ткани, жёлчи. Проходят через плаценту и проникают в грудное молоко.
Метаболизируются в печени, выводятся преимущественно через пищеварительный тракт, почками экскретируется 10-30% принятой дозы. Т1/2 линкомицина составляет 4-6 ч, клиндамицина - 2,5-3 ч. При тяжёлой почечной недостаточности и тяжёлой патологии печени Т1/2 обоих препаратов может значительно увеличиваться.
Показания
Линкозамиды применяют при инфекциях кожи, мягких тканей, костей и суставов, инфекциях нижних дыхательных путей (аспирационной пневмонии, абсцессе лёгкого, эмпиеме плевры), интраабдоминальных инфекциях, инфекциях органов малого таза, стрептококковом тонзиллофарингите (при аллергии на β-лактамы) (см. табл. 20-15).
Клиндамицин в сочетании с хинином используют при хлорохинорезистентной тропической малярии, в сочетании с пириметамином - при токсоплазмозе. Местно - при бактериальном вагинозе и тяжёлой угревой сыпи.
Учитывая узкий спектр активности линкозамидов, при тяжёлых инфекциях их следует сочетать с антимикробными ЛС, действующими на грамотрицательные бактерии (аминогликозиды II и III поколений, фторхинолоны).
Таблица 20-15. Режимы дозирования линкозамидов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Линкомицин |
Внутрь 0,5 г каждые 6-8 ч за 1 ч до еды; парентерально 0,6-1,2 каждые 12 ч |
Внутрь 30-60 мг/(кгх сут) в 3-4 приёма за 1 ч до еды; |
Клиндамицин |
Внутрь 0,15-0,6 г каждые 6 ч; парентерально 0,3-0,6 г каждые 6 ч или 0,9 г каждые 8 ч; |
Внутрь 10-25 мг/(кгх сут) (не более 2,0 г/сут) за 3-4 приёма; |
Противопоказания
Гиперчувствительность, заболевания органов пищеварения в анамнезе (неспецифический язвенный колит, энтерит или колит, связанный с применением антимикробных ЛС), беременность, кормление грудью, тяжёлая почечная и печёночная недостаточность.
Нежелательные лекарственные реакции
Чаще всего со стороны пищеварительного тракта: боль в животе, диарея, тошнота, рвота, возможна С. difficile-ассоциированная диарея/псевдомембранозный колит (меры контроля и помощи см. в гл. «Пенициллины»). Иногда отмечают нейтропению, тромбоцитопению. Аллергические реакции встречают редко. При быстром внутривенном введении клиндамицина возможна гипотензия вплоть до коллапса .
Лекарственные взаимодействия
Фармакокинетическое. Каолин- и аттапульгитсодержащие антидиарейные ЛС уменьшают всасывание линкозамидов в пищеварительном тракте (между приёмами необходимы интервалы 3-4 ч).
Фармакодинамическое. При сочетании с ингаляционными наркотическими средствами или миорелаксантами возможно усиление нервно-мышечной блокады, как следствие - мышечная слабость, угнетение или остановка дыхания. Меры помощи: антихолинэстеразные ЛС или кальция хлорид.
При сочетании с опиоидными анальгетиками повышается риск угнетения дыхания вплоть до апноэ.
Не рекомендуют сочетать с хлорамфениколом или макролидами ввиду антагонизма.
Применение в особых ситуациях
Педиатрия. У новорождённых клиндамицин следует применять с осторожностью, так как инъекционная форма содержит бензиловый спирт, с которым связывают развитие синдрома фатальной асфиксии у новорождённых.
Нарушение функций почек, печени. При тяжёлых нарушениях может потребоваться коррекция дозы.
Тетрациклины
Тетрациклины - один из ранних классов антимикробных ЛС, используемых с конца 40-х гг. прошлого столетия. В связи с появлением большого количества резистентных к тетрациклинам микроорганизмов и многочисленными НЛР, свойственными этим препаратам, их применение сократилось. Наибольшее значение тетрациклины (природный тетрациклин и полусинтетический доксициклин) сохраняют при хламидийной инфекции, риккетсиозах, некоторых зоонозах.
Фармакодинамика
Тетрациклины обладают бактериостатическим эффектом, который связан с нарушением синтеза белка в микробной клетке за счёт связывания с 30S-субъединицей рибосомы.
В настоящее время клиническое значение имеет активность в отношении листерий, H. influenzae, H. ducreyi, иерсиний, H. pylori, бруцелл, бартонелл, вибрионов (включая холерный), возбудителей паховой гранулёмы, сибирской язвы, чумы, туляремии, спирохет, лептоспир, боррелий, риккетсий, хламидий, микоплазм, актиномицетов, некоторых простейших (P. falciparum, Entamoeba histolytica). Среди анаэробной флоры чувствительны клостридии (кроме C. difficile), фузобактерии, P. acnes.
Фармакокинетика
В пищеварительном тракте тетрациклины хорошо всасываются, причём доксициклин лучше, чем тетрациклин. Биодоступность доксициклина (90-100%) не изменяется, а тетрациклина (75%) - в 2 раза уменьшается под влиянием пищи.
Тетрациклины распределяются во многие органы и среды организма, при этом доксициклин создаёт более высокие тканевые концентрации, чем тетрациклин. Концентрации в СМЖ составляют 10-25% уровня в сыворотке крови, концентрации в жёлчи в 5-20 раз выше, чем в крови. Тетрациклины проходят через плаценту и проникают в грудное молоко.
Экскреция гидрофильного тетрациклина осуществляется преимущественно почками, поэтому при почечной недостаточности его выведение значительно нарушается. Более липофильный доксициклин выводится не только через почки, но и пищеварительный тракт, причём при нарушении функции почек этот путь - основной. Т1/2 тетрациклина - 16-24 ч, тетрациклина - 8 ч. При гемодиализе тетрациклин удаляется медленно, а доксициклин не удаляется вообще.
Показания
Тетрациклины применяют при хламидийных и микоплазменных инфекциях, боррелиозах (лаймская болезнь, возвратный тиф), риккетсиозах (Ку-лихорадка, пятнистая лихорадка Скалистых гор, сыпной тиф, лихорадка цуцугамуши), бактериальных зоонозах (бруцеллёз, лептоспироз, сибирская язва, чума, туляремия), бартонеллёзах (болезнь кошачьей царапины, бациллярный ангиоматоз), кишечных инфекциях (холера, иерсиниоз), тяжёлой угревой сыпи, раневой инфекции после укусов животных, периодонтите, инфекционных заболеваниях, передающихся половым путём (сифилис - при аллергии к пенициллину, паховая гранулёма, венерическая лимфогранулёма), инфекциях глаз (острый конъюнктивит с включениями, трахома), актиномикозе, для профилактики тропической малярии (см. табл. 20-16).
Тетрациклин используют для эрадикации H. pylori при язвенной болезни (в составе резервной четырёхкомпонентной схемы в сочетании с антисекреторными ЛС, препаратами висмута и другими антимикробными ЛС).
Таблица 20-16. Режимы дозирования тетрациклинов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Тетрациклин |
Внутрь 0,3-0,5 г каждые 6 ч за 1 ч до еды; мазь наносят на поражённые участки кожи 4-6 раз в сут; |
Старше 8 лет - внутрь (за 1 ч до еды) 25-50 мг/(кгх сут) (но не более 3 г/сут) в 4 приёма |
Доксициклин |
Внутрь 0,2 г/сут в 1-2 приёма; |
Старше 8 лет - внутрь 4 мг/(кг х сут) (не более 0,2 г/сут) в 1-2 приёма; в/в (за 1 ч) 4 мг/(кгх сут) в 2 введения |
Противопоказания
Гиперчувствительность, возраст до 8 лет, беременность, кормление грудью, тяжёлая патология печени, почечная недостаточность (тетрациклин).
Нежелательные лекарственные реакции
Тетрациклины довольно часто вызывают НЛР (доксициклин несколько реже, чем тетрациклин).
Со стороны пищеварительного тракта - глоссит с гипертрофией сосочков и почернением языка, эзофагит, эрозии пищевода (чаще при приёме капсул), боль или дискомфорт в животе, тошнота, рвота, диарея; ЦНС - головокружение, синдром псевдоопухоли мозга; печени - изменения активности трансаминаз, холестатический гепатит, в тяжёлых случаях - жировая дистрофия или некроз (факторы риска: исходные нарушения функции печени, беременность, быстрое внутривенное введение, почечная недостаточность); костей - нарушение образования костной ткани, замедление линейного роста у детей; зубов - дисколорация, дефекты эмали; обмена веществ - преобладание катаболизма белков, нарастание азотемии при почечной недостаточности; кожи - сыпь и дерматит под влиянием солнечного света (фотосенсибилизация, нередко сочетание поражения кожи и ногтей).
Встречаются аллергические (сыпь, крапивница и др.) и местные (тромбофлебит при внутривенном введении) реакции, кандидоз (орофарингеальный, кишечный, вагинальный), явления гематотоксичности.
Лекарственные взаимодействия
Фармакокинетическое. Антациды, содержащие кальций, алюминий и магний, а также натрия гидрокарбонат и колестирамин8, снижают биодоступность тетрациклинов вследствие образования невсасывающихся комплексов (между приёмами необходимы интервалы 1-3 ч).
Не рекомендуют сочетать тетрациклины с препаратами железа, поскольку при этом нарушается всасывание и тех и других.
Карбамазепин, фенитоин и барбитураты усиливают метаболизм доксициклина и уменьшают его концентрацию в крови, что может потребовать коррекции его дозы или замены на тетрациклин.
Тетрациклины могут усиливать действие непрямых антикоагулянтов вследствие ингибирования их метаболизма в печени (требуется тщательный контроль МНО и протромбинового времени).
Фармакодинамическое. При сочетании с препаратами витамина А возрастает риск синдрома псевдоопухоли мозга.
Применение в особых ситуациях
Педиатрия. Тетрациклины противопоказаны детям до 8 лет, так как они могут вызывать замедление роста костей, изменение цвета зубов, гипоплазию эмали.
Нарушение функций почек. Тетрациклин противопоказан при почечной недостаточности. Доксициклин можно использовать, поскольку основным путём его экскреции в этом случае выступает пищеварительный тракт.
Нарушение функции печени. Тетрациклины противопоказаны при тяжёлых нарушениях в связи с риском гепатотоксичности.
Гликопептиды
Гликопептиды - природные антибиотики, продуцируемые почвенными актиномицетами. К гликопептидам относят ванкомицин (один из ранних антимикробных ЛС, полученный в 50-х гг. ХХ в.) и тейкопланин8. На различных стадиях разработки находятся несколько новых гликопептидов (телеванцинP и др.). Основное значение гликопептиды имеют при лечении инфекций, вызванных полирезистентными грамположительными бактериями.
Фармакодинамика
Гликопептиды нарушают формирование клеточной стенки бактерий за счёт связывания мономеров пептидогликана. Оказывают медленное бактерицидное действие, в связи с чем клинический и микробиологический эффект часто развивается более длительно, чем при применении β-лактамов.
Гликопептиды активны в отношении практически всех грамположительных аэробных и анаэробных микроорганизмов, включая стафилококки (в том числе MRSA и MRSE), стрептококки, пневмококки, энтерококки (бактериостатический эффект), листерии, коринебактерии, пептострептококки, пептококки, клостридии (включая C. difficile).
С 80-х гг. прошлого столетия во многих странах отмечено появление и распространение ванкомицинорезистентных штаммов энтерококков (VRE). В России до настоящего времени отмечают только единичные случаи их выделения в онкологических и гематологических стационарах. С конца 90-х гг. начали отмечаться случаи выделения штаммов S. aureus со сниженной чувствительностью к гликопептидам.
Фармакокинетика
Практически не всасывается в пищеварительном тракте. Биодоступность тейкопланина8 при внутримышечном введении составлет около 90%.
Гликопептиды хорошо распределются в организме, проникая во многие органы, ткани и среды. Высокие концентрации создаются в плевральной, синивиальной и асцитической жидкости. Через ГЭБ проходят только при воспалении оболочек. Не метаболизируются, выводятся почками в неизменённом виде, поэтому при почечной недостаточности требуется коррекция дозы. Учитывая относительно узкий терапевтический диапазон, при использовании ванкомицина у пациентов с почечной недостаточностью желательно проведение терапевтического лекарственного мониторинга.
Т1/2 ванкомицина при нормальной функции почек составляет 6-8 ч, тейкопланина8 - 40-70 ч. При нарушениях функции печени фармакокинетика гликопептидов существенно не изменяется.
Показания
Гликопептиды применяют при тяжёлых инфекциях, вызванных полирезистентными грамположительными патогенами (MRSA, MRSE, E. faecium, антибиотикорезистентный пневмококк), а также при грамположительных инфекциях у пациентов с аллергией к β-лактамам: при ИЭ, менингите, катетер-ассоциированном сепсисе, перитоните, нейтропенической лихорадке и др. (см. табл. 20-17).
Ванкомицин внутрь используют при антибиотикоассоциированной диарее, вызванной C. difficile, парентерально - для профилактики послеоперационных инфекций при ортопедических, кардиоили нейрохирургических операциях в лечебных учреждениях с высоким распространением MRSA или при аллергии на β-лактамы.
Таблица 20-17. Режимы дозирования гликопептидов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Ванкомицин |
В/в 1,0 г каждые 12 ч или 30 мг/(кгх сут) в 2 введения; для профилактики - 1,0 г за 30-60 мин до вмешательства; внутрь 0,125 г каждые 6 ч |
В/в 40 мг/(кгх сут) (не более 2 г/сут) в 4 введения |
Тейкопланин8 |
В/в 0,4 г в первый день, в последующие по 0,2 г за одно введение; |
В/в три первые дозы по 10 мг/кг каждые 12 ч, далее по 6-10 мг/(кгх сут) |
Противопоказания
Гиперчувствительность, беременность (тейкопланин8), кормление грудью.
Нежелательные лекарственные реакции
Нефротоксичность (чаще ванкомицин) может проявляться обратимым снижением функции почек (повышение уровня креатинина и мочевины в крови). Факторы риска: высокая доза, длительное применение, пожилой возраст.
Возможны НЛР со стороны ЦНС (головокружение, головная боль), проявления ото-вестибулотоксичности, гематотоксичности, местные (боль, жжение, флебит) и аллергические реакции.
При быстром внутривенном введении ванкомицина может развиваться гипотензия, боль за грудиной, тахикардия, гиперемия лица и верхней половины туловища (синдром «красного человека»). Причина - высвобождение гистамина из тучных клеток. Профилактика - медленная инфузия ванкомицина (не менее 60 мин).
Лекарственные взаимодействия
Фармакодинамическое. При сочетании с местными анестетиками увеличивается риск гистаминовой реакции.
Аминогликозиды, амфотерицин В, полимиксин В, циклоспорин, петлевые диуретики увеличивают риск нефротоксичности гликопептидов.
Применение в особых ситуациях
Беременность. Достоверных данных о токсическом действии на плод нет, однако ванкомицин можно назначать беременным (кроме I триместра) только по жизненным показаниям. Тейкопланин8 противопоказан.
Педиатрия. У детей и новорождённых применять с осторожностью, только при тяжёлых инфекциях.
Гериатрия. У лиц пожилого возраста в связи с понижением функции почек может потребоваться коррекция режимов дозирования. Повышается риск ототоксичности.
Нарушение функций почек. Рекомендуют контролировать диурез, уровень креатинина сыворотки, проводить терапевтический лекарственный мониторинг. Остаточные концентрации ванкомицина в крови не должны превышать 10 мг/л.
Нарушение слуха и вестибулярные расстройства. Повышается риск отовестибулотоксичности. Применять с осторожностью.
Оксазолидиноны
Единственный представитель оксазолидинонов - линезолид имеет основное значение как препарат для терапии инфекций, вызванных полирезистентными грамположительными микроорганизмами.
Фармакодинамика
Линезолид оказывает преимущественно бактериостатическое действие за счёт нарушения синтеза белка. Чувствительны подавляющее большинство как аэробных, так и анаэробных грамположительных бактерий: Staphylococcus spp. (включая MRSA и MRSE), Enterococcus spp. (включая ванкомицинрезистентные штаммы), Streptococcus spp. (включая полирезистентные S. pneumoniae), листерии, Clostridium spp., Peptostreptococcus spp. и др. Умеренная активность in vitro в отношении M. catarrhalis, H. influenzae, Legionella spp., N. gonorrhoeae, Bacteroides spp., Prevotella spp.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - около 100%, не зависит от пищи. Связывание с белками плазмы - 30%. Создаёт высокие концентрации во многих органах, тканях и средах организма. Проходит через ГЭБ. Метаболизируется в печени без участия цитохрома P-450. Выводится в основном почками, преимущественно в виде неактивных метаболитов (в неизменённой форме 30-35%). Небольшая часть метаболитов выделяется через кишечник. Период полувыведения - 4,5-5,5 ч. Клиренс выше у детей и несколько снижается с увеличением возраста. Фармакокинетика не изменяется при почечной недостаточности, а также у пациентов с умеренной и средней печёночной недостаточностью.
Показания
Линезолид применяют при инфекциях, вызванных полирезистентными грамположительными кокками (в том числе MRSA, MRSE, VRE и др.): осложнённых и неосложнённых инфекциях кожи и мягких тканей, внебольничной и нозокомиальной пневмонии.
Назначают внутривенно взрослым и детям старше 12 лет в дозе 0,6 г каждые 12 ч. Детям до 12 лет по 10 мг/кг (не более 0,4 г) каждые 8 ч. Вводят путём медленной инфузии в течение 30 мин. Внутрь взрослым и детям старше 12 лет применяют по 0,6 г каждые 12 ч.
При доказанной или предполагаемой сопутствующей грамотрицательной инфекции необходимо использовать в сочетании с антимикробными ЛС, обладающих соответствующей активностью.
Противопоказания
Гиперчувствительность, беременность, кормление грудью.
Нежелательные лекарственные реакции
Линезолид обычно хорошо переносится.
Иногда отмечают боль в животе, тошноту, рвоту, диарею, изменение вкуса, обратимую анемию и тромбоцитопению, повышение активности трансаминаз и ЩФ, увеличение уровня билирубина в крови, головную боль. Риск гемато- и нейротоксичности повышается при лечении более 28 дней.
Лекарственные взаимодействия
Фармацевтическое. Линезолид в растворе для инфузий несовместим с цефтриаксоном, амфотерицином В, диазепамом, пентамидином, фенитоином, эритромицином, ко-тримоксазолом.
Фармакодинамическое. Линезолид - слабый обратимый ингибитор МАО, поэтому он может усиливать прессорное действие допамина, псевдоэфедрина и фенилпропаноламина8.
При сочетании с селективными ингибиторами обратного захвата серотонина возможно развитие серотонинового синдрома.
Применение в особых ситуациях
Нарушения гемопоэза и коагулопатии. У пациентов с анемией и/или тромбоцитопенией в анамнезе, а также у получающих антикоагулянты повышен риск развития анемии и/или тромбоцитопении, особенно при терапии линезолидом более двух недель; необходим контроль числа тромбоцитов и уровня гемоглобина.
Полимиксины
Полимиксины (полимиксин В, полимиксин М) - природные антимикробные ЛС, открытые в 1947 г., циклические полипептиды, синтезируемые спорообразующей палочкой Bacillus polymixa. Характеризуются узким спектром активности и высокой токсичностью. Применяют в качестве препаратов резерва при инфекциях, вызванных полирезистентными штаммами грамотрицательных бактерий.
Фармакодинамика
Полимиксины обладают бактерицидным действием, обусловленным нарушением структуры клеточной мембраны грамотрицательных бактерий за счёт вытеснения катионов кальция и магния из образующих её липополисахаридов. Кроме того, полимиксины нейтрализуют эндотоксин грамотрицательных бактерий.
Основное клиническое значение имеет активность против E. coli, Klebsiella spp., Enterobacter spp., Salmonella spp., Shigella spp., P. aeruginosa, Acinetobacter spp., включая штаммы, резистентные к другим антимикробным ЛС. Умеренно чувствительны фузобактерии и бактероиды (кроме B. fragilis). Природной устойчивостью обладают все виды Proteus spp., Serratia spp., грамотрицательные кокки и вся грамположительная микрофлора.
Фармакокинетика
Полимиксины не всасываются в пищеварительном тракте, со слизистых оболочек и с кожи. Однако при длительном использовании в виде ушных или глазных капель частичная абсорбция возможна. При парентеральном введении полимиксин В плохо проникает через тканевые барьеры, не создаёт высоких концентраций в жёлчи, плевральной и синовиальной жидкостях, воспалительных экссудатах. Не проходит через ГЭБ, но способен в небольших количествах проникать через плаценту и в грудное молоко. Не метаболизируется, выводится почками в неизменённом виде. Т1/2 - 3-4 ч, при почечной недостаточности может возрастать до 2-3 сут. Назначаемый внутрь полимиксин М полностью выводится через пищеварительный тракт.
Показания
Полимиксин В применяют при синегнойной инфекции (в случае устойчивости к цефалоспоринам, карбапенемам, аминогликозидам, фторхинолонам), тяжёлых нозокомиальных грамотрицательных инфекциях, вызванных полирезистентными штаммами (кроме Proteus spp., Serratia spp.). Его назначают взрослым и детям по 1,5-2,5 мг/(кгх сут) (не более 0,2 г/сут) за 3-4 введения. Местно (в составе комбинированных лекарственных форм) - при бактериальных инфекциях глаз, наружном отите без повреждения барабанной перепонки, вагините.
Полимиксин М используют для местного лечения синегнойной инфекции при инфицированных ранах и ожогах.
Противопоказания
Гиперчувствительность, почечная недостаточность, миастения, ботулизм. Для местного применения - перфорация барабанной перепонки, обширные поражения кожи.
Нежелательные лекарственные реакции
Полимиксины обладают высокой токсичностью.
Нефротоксическое действие (у 10-18%) первоначально может проявляться повышением креатинина и мочевины в сыворотке крови, снижением клиренса креатинина. Возможно развитие острого тубулярного некроза, гематурии, протеинурии, цилиндрурии и олигоурии. Факторы риска: предшествующая почечная патология, высокие дозы, сочетание с другими нефротоксичными ЛС. Меры контроля: расчёт клиренса креатинина каждые 3 дня, регулярные клинические анализы мочи.
Проявлениями нейротоксичности могут быть парестезии, головокружение, мышечная слабость, периферические полиневропатии, нарушение сознания, зрительные и слуховые расстройства и др.
Возможна нервно-мышечная блокада с угрозой развития паралича дыхательных мышц. Факторы риска: почечная недостаточность, миастения, одновременное или предшествующее применение миорелаксантов и анестетиков.
Могут отмечаться боль в животе, тошнота, рвота, диарея, болезненность и повреждение тканей при внутримышечном введении, флебит и тромбофлебит - при внутривенном, аллергические реакции, гипотония.
Лекарственные взаимодействия
Фармакодинамическое. Следует избегать сочетания полимиксина В с аминогликозидами и амфотерицином В (увеличение риска нефротоксичности), миорелаксантами и анестетиками (риск нервно-мышечной блокады и паралича дыхательных мышц). Это касается и его использования в виде глазных или ушных капель.
Применение в особых ситуациях
Беременность. Полимиксин В проходит через плаценту и может оказать токсическое действие на плод. Применять только по жизненным показаниям. При длительном использовании ушных и глазных капель возможен риск ототоксичности для плода.
Лактация. Данные о проникновении полимиксина В в грудное молоко отсутствуют. Применять с осторожностью.
Педиатрия. У детей полимиксин В следует применять с осторожностью.
Гериатрия. Использовать с осторожностью ввиду повышенного риска нефро- и нейротоксичности (особенно нарушений слуха). В связи с изменениями функций почек у лиц пожилого возраста возможно замедление экскреции полимиксина В, что может потребовать коррекции режима дозирования.
Нарушение функций почек. Полимиксин В экскретируют почки в неизменённом виде, поэтому при почечной недостаточности необходимо корректировать режим дозирования. При исходной почечной патологии повышается риск нефрои нейротоксичности.
Сульфаниламиды
Сульфаниламиды были получены в конце 30-х гг. прошлого века и являются самым первым классом антимикробных ЛС для широкого применения. Показания к применению сульфаниламидов сейчас ограничены лишь несколькими инфекциями, так как по активности они значительно уступают современным антибиотикам и обладают высокой токсичностью. Существенно и то, что большинство микроорганизмов выработали резистентность к сульфаниламидам.
Фармакодинамика
Сульфаниламиды обладают бактериостатическим эффектом. Являясь химическими аналогами парааминобензойной кислоты, они конкурентно ингибируют фермент дигидроптероат синтетазу, нарушая тем самым синтез дигидрофолиевой кислоты - предшественника фолиевой кислоты. В средах, содержащих большое количество парааминобензойной кислоты (гной, продукты распада тканей), антимикробное действие сульфаниламидов значительно ослабляется.
Первоначально сульфаниламиды были активны в отношении многих грамположительных и грамотрицательных бактерий, но в настоящее время стафилококки, стрептококки, пневмококки, гонококки, менингококки, энтеробактерии характеризуются высокой степенью резистентности. Природной устойчивостью обладают энтерококки, синегнойная палочка и большинство анаэробов. Чувствительность сохраняют нокардии, пневмоцисты, актиномицеты, малярийные плазмодии, токсоплазмы.
Препараты сульфаниламидов для местного применения содержат серебро (сульфазина серебряная соль, сульфатиазол серебра), которое медленно высвобождается, оказывая бактерицидное действие (за счёт связывания с ДНК), не зависящее от концентрации парааминобензойной кислоты в области применения. Они активны против многих возбудителей раневых инфекций - Staphylococcus spp., P. aeruginosa, E. coli, Proteus spp., Klebsiella spp., грибов Candida.
Фармакокинетика
Сульфаниламиды хорошо всасываются в пищеварительном тракте (70-100%). Более высокие концентрации в крови отмечают при использовании препаратов короткого (сульфадимидин и др.) и средней продолжительности (сульфадиазин, сульфаметоксазол) действия. С белками плазмы крови в большей степени связываются сульфаниламидами длительного (сульфадиметоксин и др.) и сверхдлительного (сульфален, сульфадоксин) действия.
Распределяются во многих тканях и жидкостях организма, включая плевральный выпот, перитонеальную и синовиальную жидкости, экссудат среднего уха, камерную влагу, ткани урогенитального тракта. Сульфадиазин и сульфадиметоксин проходят через ГЭБ, достигая в СМЖ 32-65 и 14-30% сывороточных концентраций соответственно, через плаценту и проникают в грудное молоко.
Метаболизируются в печени, в основном путём ацетилирования, с образованием неактивных, но токсичных метаболитов. Экскретируются почками примерно наполовину в неизменённом виде, при щелочной реакции мочи выведение усиливается; небольшие количества выводятся с жёлчью. При почечной недостаточности возможна кумуляция сульфаниламидов и их метаболитов в организме.
При местном применении сульфаниламидов, содержащих серебро, создаются высокие локальные концентрации активных компонентов. Системная абсорбция через повреждённую (раневую, ожоговую) поверхность кожи сульфаниламидов может достигать 10, серебра - 1%.
Показания
Системные сульфаниламиды применяют для лечения нокардиоза, токсоплазмоза (чаще сульфадиазин в сочетании с пириметамином), тропической малярии при устойчивости к хлорохину (в сочетании с пириметамином), для профилактики чумы, местные - при ожогах, трофических язвах, пролежнях.
Противопоказания
Гиперчувствительность, аллергия на фуросемид, тиазиды, ингибиторы карбоангидразы и производные сульфонилмочевины, почечная недостаточность, тяжёлые нарушения функции печени, возраст до 2 мес.
Нежелательные лекарственные реакции
Системные сульфаниламиды могут вызывать аллергические реакции - лихорадку, кожную сыпь, зуд, синдромы Стивенса-Джонсона и Лайелла (чаще сульфаниламиды длительного и сверхдлительного действия). Возможны проявления гематотоксичности (лейкопения, агранулоцитоз, гипопластическая анемия, тромбоцитопения), гепатотоксичности (гепатит, токсическая дистрофия печени), нейротоксичности (головная боль, головокружение, спутанность сознания, дезориентация, эйфория и др.), нефротоксичности (кристаллурия, гематурия, интерстициальный нефрит, некроз канальцев). Наблюдают симптомы со стороны пищеварительного тракта (боль, анорексию, тошноту, рвоту, диарею, псевдомембранозный колит), нарушения функции щитовидной железы, фотосенсибилизацию.
При местном применении могут отмечаться жжение, зуд, болевые ощущения (обычно кратковременные), аллергические реакции, гиперемия кожи, ринит, бронхоспазм, лейкопения (при длительном применении на больших поверхностях).
Лекарственные взаимодействия
Фармакокинетическое. Усиление эффекта и/или токсического действия непрямых антикоагулянтов, противосудорожных ЛС, пероральных противодиабетических ЛС и метотрексата за счёт вытеснения их из связи с белками и/или ослабления метаболизма.
Усиление метаболизма циклоспорина, сопровождаемое уменьшением его сывороточных концентраций и эффективности.
Ослабление эффекта оральных контрацептивов за счёт нарушения энтерогепатической циркуляции эстрогенов, возрастание частоты маточных кровотечений.
Фенилбутазон, салицилаты и индометацин могут вытеснять сульфаниламиды из связи с белками плазмы, увеличивая их концентрацию в крови.
Фармакодинамическое. Повышение риска токсичности при сочетании с ЛС, вызывающими угнетение костного мозга, гемолиз, гепатотоксическое или нефротоксическое действие.
Применение в особых ситуациях
Беременность. Поскольку сульфаниламиды проходят через плаценту, а в исследованиях на животных выявлено их неблагоприятное действие на плод, применять их следует с большой осторожностью.
Лактация. Сульфаниламиды проникают в грудное молоко и могут вызвать ядерную желтуху у детей, находящихся на грудном вскармливании, а также гемолитическую анемию у детей с дефицитом глюкозо-6-фосфат дегидрогеназы. Применять с осторожностью.
Педиатрия. Сульфаниламиды конкурируют с билирубином за связывание с белками плазмы крови, повышая риск ядерной желтухи у новорождённых. Поскольку у новорождённого не полностью сформированы ферментные системы печени, повышенные концентрации свободного сульфаниламида - дополнительный фактор риска ядерной желтухи. Поэтому сульфаниламиды противопоказаны детям до 2 мес. Исключение - врождённый токсоплазмоз, при котором их применяют по жизненным показаниям.
Гериатрия. У лиц пожилого возраста повышен риск тяжёлых НЛР со стороны кожи, угнетения кроветворения, развития тромбоцитопенической пурпуры (чаще при сочетании с тиазидными диуретиками). Требуется строгий контроль. По возможности следует избегать назначения лицам старше 65 лет.
Нарушение функций почек. Накопление в организме сульфаниламидов и их метаболитов существенно повышает риск токсического действия, в частности нефротоксичности вплоть до развития тяжёлого интерстициального нефрита и некроза почечных канальцев. Поэтому сульфаниламиды противопоказаны при почечной недостаточности.
Нарушения функции печени. Замедление метаболизма сульфаниламидов с повышением риска токсичности. Сульфаниламиды противопоказаны при тяжёлой печёночной патологии.
Патологические изменения крови. Повышается риск гематотоксичности.
КО-ТРИМОКСАЗОЛ
Комбинированный препарат, состоящий из пяти частей сульфаметоксазола (сульфаниламиды средней длительности действия) и одной части триметоприма.
Фармакодинамика
Ко-тримоксазол оказывает бактерицидное действие, обусловленное двухэтапным влиянием на метаболизм фолиевой кислоты: сульфаметоксазол конкурентно замещает парааминобензойную кислоту, препятствуя образованию дигидрофолиевой кислоты, а триметоприм ингибирует фермент дигидрофолат редуктазу, нарушая синтез тетрагидрофолиевой кислоты.
Ко-тримоксазол активен в отношении стафилококков (включая ряд MRSA), менингококков, M. catarrhalis, Haemophilus spp., E. coli, многих видов Klebsiella, Citrobacter, Enterobacter, Salmonella, B. cepacia, S. maltophilia, нокардий и пневмоцист.
По данным исследования, проведённого в 2004-2005 гг., в России к ко-тримоксазолу резистентны более 40% штаммов S. pneumoniae, около 20% E. coli и H. influenzae, около 100% шигелл.
Природной устойчивостью обладают энтерококки, синегнойная палочка, анаэробы.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте, биодоступность - 90-100%. Распределяется во многие органы, ткани и среды организма. Проникает через ГЭБ, особенно при воспалении оболочек. Компоненты ко-тримоксазола (триметоприм и сульфаметоксазол) связываются с белками плазмы крови на 45 и 60% соответственно. Частично метаболизируются в печени, экскретируются преимущественно почками в неизменённом виде, в небольшом количестве с жёлчью. Т1/2 обоих компонентов составляет около 10 ч. При почечной недостаточности возможна их кумуляция в организме.
Показания
Ко-тримоксазол применяют при кишечных инфекциях (сальмонеллёз, диарея путешественников); внебольничных инфекциях мочевыводящих путей (острый цистит, хронический рецидивирующий цистит, пиелонефрит - в регионах с низким уровнем резистентности патогенов); стафилококковых инфекциях (в качестве резервного препарата); нозокомиальных инфекциях, вызванных S. maltophilia и B. cepacia; нокардиозе; токсоплазмозе; бруцеллёзе; пневмоцистной пневмонии.
Внутрь назначают взрослым по 0,96 г каждые 12 ч, детям - 6-8 мг/(кгхсут) (расчёт по триметоприму) в два приёма. Внутривенно взрослым при тяжёлых инфекциях - 8-10 мг/(кгхсут) в 2-3 введения, при пневмоцистной пневмонии - 20 мг/(кгхсут) в 3-4 введения; детям при тяжёлых инфекциях (включая пневмоцистную пневмонию) - 15-20 мг/(кгхсут) в 3-4 введения.
Противопоказания
Гиперчувствительность к сульфаниламидам, триметоприму, фуросемиду, тиазидным диуретикам, ингибиторам карбоангидразы, производным сульфонилмочевины, беременность, кормление грудью, тяжёлая почечная недостаточность, тяжёлые нарушения функции печени, мегалобластная фолиеводефицитная анемия, возраст до 2 мес (кроме детей, родившихся у ВИЧ-инфицированных матерей).
Нежелательные лекарственные реакции
Те же, что и у остальных сульфаниламидов. Кроме того, ко-тримоксазол может вызывать гиперкалиемию, гипогликемию, асептический менингит (последний чаще у пациентов с коллагенозами), тромбофлебит (при внутривенном введении).
Риск развития НЛР значительно возрастает у пациентов со СПИДом.
Лекарственные взаимодействия
Не следует сочетать с пенициллинами, так как сульфаниламиды ослабляют их бактерицидный эффект.
Применение в особых ситуациях
Беременность. Применять (особенно в I и III триместрах) не рекомендуют, поскольку сульфаметоксазол может вызывать ядерную желтуху и гемолитическую анемию, а триметоприм нарушает метаболизм фолиевой кислоты.
Педиатрия. Ко-тримоксазол противопоказан детям до 2 мес (можно применять у детей с возраста 4-6 нед, родившихся у ВИЧ-инфицированных матерей).
Гериатрия. С учётом возрастного нарушения функций почек возрастает риск гиперкалиемии. Требуется строгий контроль. По возможности избегать длительных курсов.
Нарушение функций почек. Нарушение почечной экскреции ведёт к кумуляции компонентов ко-тримоксазола и повышению риска токсичности. Возрастает риск гиперкалиемии. Не следует применять при клиренсе креатинина менее 15 мл/мин.
Нарушения функции печени. Замедление метаболизма, повышение риска токсичности. Возможно развитие токсической дистрофии печени.
Нарушение функции щитовидной железы. Возможно усугубление нарушения функции. Применять с осторожностью.
Патологические изменения крови. Повышается риск нарушений кроветворения.
Нитроимидазолы
Нитроимидазолы - синтетические антимикробные ЛС, обладающие высокой активностью в отношении анаэробных бактерий и простейших. Основной препарат данного класса - метронидазол, применяемый в клинической практике с 1960 г. Позднее появились тинидазол, орнидазол, секнидазол8.
Фармакодинамика
Нитроимидазолы проявляют бактерицидный эффект в отношении тех микроорганизмов, ферментные системы которых способны переводить их в активные восстановленные формы. Последние нарушают репликацию ДНК и синтез белка в микробной клетке, ингибируют клеточное дыхание, оказывают прямое цитотоксическое действие.
Чувствительны большинство анаэробов - бактероиды (включая B. fragilis), клостридии (включая C. difficile), Fusobacterium spp., Peptostreptococcus spp. и др. Устойчива P. acnes.
Нитроимидазолы активны также в отношении H. pylori, Gardnerella vaginalis, многих простейших (трихомонад, лямблий, амёб и др.).
Фармакокинетика
Хорошо всасываются в пищеварительном тракте. Биодоступность - 80-90%, не зависит от приёма пищи. Метронидазол хорошо всасывается при интравагинальном введении в виде таблеток. Пиковые концентрации в крови в этом случае составляют примерно 50% уровней, достигаемых при приёме эквивалентной дозы внутрь. При использовании вагинального геля абсорбция значительно ниже. При наружном применении метронидазол практически не всасывается.
Нитроимидазолы распределяются во многие ткани и биологические жидкости, проходят через ГЭБ (высокие концентрации в СМЖ и ткани мозга) и плацентарный барьер, проникают в грудное молоко, активно секретируются со слюной и желудочным соком. Метаболизируются в печени при участии цитохрома P-450, выводятся преимущественно с мочой. Т1/2 метронидазола - 6-8 ч, тинидазола - 11-12 ч, орнидазола - 12-14 ч, секнидазола8 - 20 ч. При почечной недостаточности эти величины не изменяются.
Показания
Метронидазол и тинидазол применяют при анаэробных и аэробно-анаэробных инфекциях различной локализации: нижних дыхательных путей (аспирационной пневмонии, эмпиеме плевры, абсцессе лёгкого), ЦНС (менингите, абсцессе мозга), интраабдоминальных, органов малого таза, полости рта, при псевдомембранозном колите (см. табл. 20-18). Их используют также для эрадикации H. pylori при язвенной болезни (в сочетании с антисекреторными ЛС и другими антимикробными ЛС) и для периоперационной профилактики при интраабдоминальных и гинекологических вмешательствах.
Все нитроимидазолы применяют при протозойных инфекциях: трихомониазе, лямблиозе, балантидиазе, кишечном и внекишечном амёбиазе (гепатит, абсцесс печени и мозга).
Местно нитроимидазолы можно применять для лечения вагинитов, бактериального вагиноза, розовых угрей, себорейной экземы, околоротового дерматита.
Таблица 20-18. Режимы дозирования нитроимидазолов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Метронидазол |
Внутрь 0,25 г каждые 8 ч или 0,4-0,5 г каждые 12 ч; |
Внутрь и в/в 7,5 мг/кг каждые 8 ч |
Орнидазол |
Внутрь 0,5 г каждые 12 ч |
Внутрь 25-40 мг/(кгх сут) в 1-2 приёма |
Секнидазол8 |
Внутрь 1,5-2,0 г однократно (трихомониаз, лямблиоз) или в течение 3-5 дней (амёбиаз) |
Внутрь 30 мг/(кгх сут) в 1, 2 или 3 приёма, курс - в зависимости от этиологии инфекции |
Тинидазол |
Внутрь 2,0 г в первый день в один приём, затем - по 1 г/сут в 1-2 приёма |
Внутрь 50-60 мг/(кгх сут) в один приём |
Противопоказания
Гиперчувствительность, беременность (I триместр), кормление грудью.
Нежелательные лекарственные реакции
Нитроимидазолы могут вызывать НЛР со стороны пищеварительного тракта (неприятный привкус во рту, боль в животе, тошноту, рвоту, диарею), ЦНС (головную боль, головокружение, нарушение координации движений, нарушения сознания, судороги, в редких случаях - эпилептические припадки), аллергические, гематологические (лейкопения, нейтропения) и местные (флебит и тромбофлебит при внутривенном введении) реакции.
При интравагинальном применении возможны зуд, жжение во влагалище или вульве, отёк вульвы, появление или усиление выделений, учащённое мочеиспускание, при наружном - явления фотодерматита.
Лекарственные взаимодействия
Фармакокинетическое. Активность нитроимидазолов уменьшается при сочетании с индукторами цитохрома P450 (фенобарбитал, рифампицин и др.) и повышается на фоне применения его ингибиторов (циметидин и др.).
За счёт ингибирования цитохрома P450 нитроимидазолы могут нарушать метаболизм в печени варфарина, фенитоина, повышать их концентрации в крови и усиливать эффект (необходим строгий контроль, может потребоваться коррекция дозы варфарина и фенитоина).
Фармакодинамическое. При сочетании с карбамазепином и препаратами лития повышается риск нейротоксичности.
При приёме алкоголя на фоне лечения метронидазолом, тинидазолом и секнидазолом8 возможна дисульфирамоподобная реакция.
Применение в особых ситуациях
Беременность. Нитроимидазолы противопоказаны в I триместре, во II и III допустимо применение по жизненным показаниям при отсутствии более безопасной альтернативы.
Педиатрия. Возможна кумуляция нитроимидазолов в организме ребенка. У новорождённых T1/2 может увеличиваться до суток и более.
Гериатрия. В связи с возможными возрастными изменениями функции печени может потребоваться уменьшение дозы.
Нарушение функции печени. При тяжёлых заболеваниях печени возможно нарушение метаболизма нитроимидазолов, что может потребовать коррекции дозы.
Заболевания ЦНС. Применять с осторожностью ввиду нейротоксичности, у пациентов с органическими заболеваниями ЦНС возрастает риск судорог и эпилептических припадков.
Нарушения кроветворения. Применять с осторожностью, так как возрастает риск лейкопении и нейтропении.
Нитрофураны
К классу нитрофуранов относят нитрофурантоин, фуразидин, нифуроксазид, фуразолидон и нифурател. По уровню антимикробной активности они уступают большинству антибиотиков, но могут действовать на некоторые антибиотикорезистентные штаммы. Особенности фармакокинетики отдельных препаратов определяют различия в их клиническом применении. Как правило, нитрофураны выступают в качестве препаратов резерва.
Фармакодинамика
Как акцепторы кислорода нитрофураны нарушают процесс клеточного дыхания бактерий, ингибируют биосинтез нуклеиновых кислот. В зависимости от концентрации оказывают бактериостатический или бактерицидный эффект.
К нитрофуранам чувствительны многие грамотрицательные (E. coli, K. pneumoniae сальмонеллы, шигеллы и др.) и грамположительные (стрептококки, стафилококки, энтерококки) аэробные бактерии. Кроме того, фуразолидон и нифурател активны в отношении некоторых простейших (лямблии, трихомонады).
Устойчивы P. aeruginosa, большинство штаммов Proteus spp., Serratia spp., Providencia spp., Acinetobacter spp.
Фармакокинетика
Хорошо и быстро всасываются в пищеварительном тракте (кроме нифуроксазида). Не создают высоких концентраций в крови и тканях (включая почки), поскольку быстро выводятся из организма (Т1/2 около часа). Нитрофурантоин и фуразидин накапливаются в моче в высоких концентрациях, фуразолидон - только 5% от принятой дозы, так как в значительной степени метаболизируется. Частично экскретируются с жёлчью и создают высокие концентрации в просвете кишечника. При почечной недостаточности выведение существенно замедлено. Нифуроксазид не всасывается в пищеварительном тракте и полностью выводится с калом.
Показания
Нитрофурантоин и фуразидин применяют для лечения инфекций нижних отделов мочевыводящих путей (острого цистита, супрессивной терапии хронических инфекций), для профилактики инфекционных осложнений при урологических операциях, цистоскопии, катетеризации мочевого пузыря. Нифуроксазид и нифурател - при кишечных инфекциях (острой инфекционной диарее, энтероколите). Фуразолидон и нифурател - при лямблиозе и трихомониазе (уступают по активности нитроимидазолам) (см. табл. 20-19).
Таблица 20-19. Режимы дозирования нитрофуранов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Нитрофурантоин |
0,05-0,1 г каждые 6 ч; для длительной супрессивной терапии - 0,05-0,1 г/сут |
5-7 мг/(к гх сут) в 4 приёма |
Нифурател |
0,2-0,4 г каждые 8-12 ч |
10-20 мг/(кг х сут) в 2-3 приёма |
Нифуроксазид |
0,2 г каждые 6 ч |
Младше 2,5 лет - 0,1 г каждые 8-12 ч; старше 2,5 лет - 0,2 г каждые 8 ч |
Фуразолидон |
0,1 г каждые 6 ч |
6-7 мг/(кг х сут) в 4 приёма |
Фуразидин |
0,1-0,2 г каждые 6-8 ч |
7,5 мг/(кг х сут) в 2-3 приёма |
Противопоказания
Гиперчувствительность, дефицит глюкозо-6-фосфат дегидрогеназы, беременность (нитрофурантоин разрешён во II триместре), кормление грудью, период новорождённости.
Нитрофурантоин и фуразидин противопоказаны при почечной недостаточности, а фуразолидон - при тяжёлой патологии печени.
Нежелательные лекарственные реакции
НЛР отмечают довольно часто. Возможны симптомы со стороны пищеварительного тракта (тошнота, рвота, диарея), печени (транзиторное повышение активности трансаминаз, холестаз, гепатит), проявления гематотоксичности (лейкопения, мегалобластная или гемолитическая анемия), нейротоксичности (головокружение, головная боль, общая слабость, сонливость, периферические полинейропатии), аллергические реакции.
Нитрофурантоин вызывает лёгочные реакции: пневмонит, бронхоспазм, кашель, боль в грудной клетке.
Лекарственные взаимодействия
Фармакодинамическое. Хинолоны ослабляют эффект нитрофурантоина и фуразидина.
При сочетании с хлорамфениколом увеличивается риск угнетения кроветворения.
При сочетании фуразолидона, умеренно ингибирующего МАО, с другими ингибиторами этого фермента, симпатомиметиками, трициклическими антидепрессантами возникает риск гипертонического криза.
При приёме алкоголя на фоне лечения фуразолидоном возможна дисульфирамоподобная реакция.
Применение в особых ситуациях
Беременность. Применение нитрофурантоина возможно только во II триместре. Другие нитрофураны противопоказаны.
Педиатрия. Не применять новорождённым в связи с незрелостью ферментных систем, что сопряжено с риском гемолитической анемии.
Гериатрия. У пожилых возрастает риск пневмонита и периферических полинейропатий. Применять с осторожностью в связи с возможными изменениями функций почек. Может потребоваться уменьшение дозы.
Нарушение функций почек. Нитрофурантоин и фуразидин противопоказаны при почечной недостаточности, так как в этом случае они не создают терапевтических концентраций в моче, кумулируют и могут оказать токсическое действие.
Нарушение функции печени. Возрастает риск гепатотоксичности. Применять с осторожностью.
Другие сопутствующие заболевания. Риск периферических полиневропатий повышается при анемии, сахарном диабете, нарушениях электролитного баланса, недостаточности витаминов группы В. В целях профилактики следует назначать витамины группы В.
Отдельные антимикробные препараты
НИТРОКСОЛИН
Нитроксолин - производное 8-оксихинолина. В связи с особенностями фармакокинетики используют только при инфекциях мочевыводящих путей.
Фармакодинамика
Обладает бактериостатическим действием за счёт нарушения синтеза бактериальной ДНК. Уменьшает адгезию E. coli к эпителию мочевыводящих путей и поверхности мочевых катетеров. Клиническое значение имеет активность против Enterobacteriaceae (E. coli, Salmonella spp., Shigella spp., Proteus spp.), Mycoplasma spp. и грибов Candida.
Фармакокинетика
Хорошо и быстро всасывается в пищеварительном тракте. Высокие концентрации создаются только в моче, определяются в ней через час после приёма и сохраняются до 24 ч. Т1/2 варьирует, в среднем составляя 2,6 ч.
Показания
Применяют для лечения и профилактики острого неосложнённого цистита (в качестве препарата резерва). Назначают внутрь взрослым по 0,1-0,2 г каждые 6 ч за час до еды, детям старше месяца - по 5-8 мг/(кгхсут) в 2-3 приёма.
Противопоказания
Гиперчувствительность, заболевания периферической нервной системы, зрительного нерва, тяжёлые заболевания печени, почечная недостаточность, беременность, кормление грудью, недоношенным и новорождённым детям.
Нежелательные лекарственные реакции
Возможны проявления нейротоксичности в виде головной боли, головокружения, парестезий, полинейропатии. Описано развитие подострой миелооптической нейропатии (SMON-синдром), при которой сначала возникают боль в животе и диарея, а затем - тяжёлый периферический полиневрит и атрофия зрительного нерва.
Могут наблюдаться аллергические реакции, тошнота, рвота, потеря аппетита, повышение активности трансаминаз, тахикардия.
Применение в особых ситуациях
Педиатрия. Противопоказан недоношенным и новорождённым ввиду возможной кумуляции и токсичности. У более старших детей применять с осторожностью.
Гериатрия. У пожилых лиц применять с осторожностью ввиду возможной кумуляции и токсичности.
Нарушение функций почек и печени. Возможна кумуляция и токсическое действие. При тяжёлых нарушениях препарат противопоказан.
СПЕКТИНОМИЦИН
Спектиномицин - представитель группы аминоциклитолов, имеющих структурное сходство с аминогликозидами. Обладает узким спектром антимикробной активности. Используют для лечения гонореи в качестве альтернативного препарата.
Фармакодинамика
Нарушает синтез белка рибосомами, оказывает бактериостатическое, а в высоких дозах - бактерицидное действие. Основное клиническое значение имеет активность в отношении гонококков, в том числе резистентных к пенициллину.
Фармакокинетика
Плохо всасывается в пищеварительном тракте, применяют только внутримышечно. Незначительно связывается с белками плазмы. Не метаболизируется, выводится почками в активной форме. T1/2 - 1-3 ч, при клиренсе креатинина менее 20 мл/мин возрастает до 10-30 ч.
Показания
Лечение урогенитальной, осложнённой и генерализованной гонореи. Профилактика гонококковой инфекции у контактных лиц.
Назначают внутримышечно взрослым при неосложнённой гонорее 2,0 г однократно; при осложнённой и диссеминированной гонорее - 2,0 г каждые 12 ч не менее 3 дней. Детям с массой тела до 45 кг - 40 мг/кг (не более 2,0 г) однократно, более 45 кг - 2,0 г однократно.
Противопоказания
Гиперчувствительность, возраст до года.
Нежелательные лекарственные реакции
Аллергические и местные (болезненность, инфильтраты) реакции, головная боль, головокружение, боль в животе, тошнота, рвота, снижение уровня гемоглобина и гематокрита.
Лекарственные взаимодействия
Фармакокинетическое. Спектиномицин снижает клиренс препаратов лития, повышая их токсичность. При совместном применении необходим мониторинг концентрации лития в крови.
Применение в особых ситуациях
Беременность, лактация. Адекватных исследований безопасности у людей не проводилось. Применять с осторожностью.
Педиатрия. Прилагаемый к препарату растворитель содержит бензиловый спирт, с которым связывают развитие смертельной асфиксии у детей первого года жизни. Не использовать в этой возрастной группе.
ФОСФОМИЦИН
Фосфомицин - природный антибиотик с достаточно широким спектром активности, выпускаемый в виде различных солей. В России применяют фосфомицина трометамол* для приёма внутрь и фосфомицин натрия* для парентерального введения.
Фамакодинамика
Фосфомицин обладает бактерицидным эффектом, связанным с нарушением начальных этапов образования клеточной стенки, снижает адгезию бактерий к эпителию мочевыводящих путей. К фосфомицину чувствителен ряд грамотрицательных (кишечная палочка, сальмонеллы, шигеллы, протей и др., включая штаммы, резистентные к другим антимикробным ЛС) и грамположительные (стафилококки и энтерококки, включая VRE) бактерии. Малоактивен в отношении стрептококков. Не действует на синегнойную палочку и анаэробы.
Фармакокинетика
Фосфомицина трометамол* хорошо всасывается из пищеварительного тракта, биодоступность при приёме натощак - 60%. Не связывается с белками плазмы. После однократного приёма в дозе 3,0 г высокие уровни препарата в моче сохраняются в течение 36-48 ч. Проникает в различные органы и ткани. Накапливается в терапевтических концентрациях в почках, мочевом пузыре, предстательной железе. Не метаболизируется, экскретируется почками в неизменённом виде. Т1/2 составляет 4 ч при приёме внутрь и 1,5-2,0 ч - при внутривенном введении.
Показания
Фосфомицина трометамол* применяют при остром и рецидивирующем цистите, бессимптомной бактериурии у беременных, для профилактики инфекций мочевыводящих путей при трансуретральных урологических вмешательствах (см. табл. 20-20).
Фосфомицин натрия* используют как препарат резерва при инфекциях различной локализации (нижних дыхательных путей, кожи и мягких тканей, сепсисе и др.). Возможны комбинации с другими антимикробными ЛС.
Таблица 20-20. Режимы дозирования препаратов фосфомицина
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Фосфомицина трометамолр |
Внутрь при остром цистите и бессимптомной бактериурии 3,0 г однократно; |
Старше 5 лет - внутрь 2,0 г однократно |
Фосфомицин натрия* |
Парентерально 2,0-4,0 г каждые 8 ч |
Парентерально 50-80 мг/(кгх сут) за 2-3 введения |
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Аллергические реакции, повышение активности трансаминаз, головная боль, головокружение, диарея, тошнота, рвота, боль в животе.
Лекарственные взаимодействия
Фармакокинетическое. Метоклопрамид ослабляет всасывание фосфомицина трометамолаP и снижает его концентрацию в крови.
Применение в особых ситуациях
Беременность, лактация. Применять с осторожностью.
Педиатрия. Фосфомицина трометамолP не рекомендуют применять у детей до 5 лет, так как его эффективность и безопасность в этой возрастной группе не изучена.
Гериатрия. У лиц старше 75 лет повышен риск гепатотоксичности.
Нарушение функций почек. При почечной недостаточности в 1,5-2 раза повышаются сывороточные концентрации, снижается клиренс фосфомицина, что может потребовать уменьшения дозы.
Нарушение функции печени. Возможно усугубление печёночной дисфункции.
ХЛОРАМФЕНИКОЛ
Хлорамфеникол - один из ранних природных антибиотиков, получен в конце 40-х гг. прошлого века. Применение данного препарата в настоящее время ограничено ввиду гематотоксичности. Он сохраняет значение при лечении менингита, риккетсиозов, сальмонеллёзов и анаэробных инфекций.
Фармакодинамика
Хлорамфеникол обладает преимущественно бактериостатическим эффектом, связанным с нарушением синтеза белка рибосомами. Изначально имел широкий антимикробный спектр, но в процессе многолетнего использования многие бактерии приобрели устойчивость.
Чувствительны пневмококки (кроме пенициллинорезистентных), менингококки, H. influenzae, E. coli, отдельные штаммы сальмонелл, шигелл, возбудители дифтерии, коклюша, сибирской язвы, бруцеллёза, чумы, спирохеты, риккетсии, актиномицеты, анаэробы (включая B. fragilis).
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 70-80%, не зависит от пищи. Высокие концентрации создаются в ткани мозга, бронхиальном секрете, плевральной и синовиальной жидкостях, низкие - в жёлчи. Хорошо проходит через ГЭБ и плаценту, проникает в грудное молоко. Концентрации в сыворотке крови плода могут составлять 30-80% от материнского уровня. Метаболизируется в печени при участии цитохрома P-450. Экскреция осуществляется почками преимущественно в неактивном состоянии, поэтому при почечной недостаточности коррекции дозы не требуется. T1/2 у взрослых составляет 1,5-3,5 ч, у детей может увеличиваться до 6,5 ч, у новорождённых - до 24 ч и более.
При использовании глазных лекарственных форм (капли, линимент) происходит внутриглазное и частичное системное всасывание хлорамфеникола. Создаются высокие концентрации во внутриглазной жидкости.
Для повышения безопасности лечения (особенно у новорождённых и пациентов с заболеваниями печени) следует, по возможности, проводить терапевтический лекарственный мониторинг. Терапевтический диапазон составляет 10-25 мкг/мл.
Показания
Применяют (обычно в качестве препарата резерва) при бактериальном менингите, абсцессе мозга, генерализованных формах сальмонеллёзов, брюшном тифе, риккетсиозах (Ку-лихорадка, пятнистая лихорадка Скалистых гор, сыпной тиф), интраабдоминальных инфекциях, инфекциях органов малого таза, газовой гангрене, чуме. Назначают в дозе 50-100 мг/(кгхсут) за 4 введения.
Местно - при бактериальных инфекциях глаз.
Противопоказания
Гиперчувствительность, беременность, кормление грудью.
Нежелательные лекарственные реакции
Наиболее серьёзными считают гематотоксические реакции, которые могут быть обратимыми (дозозависимая тромбоцитопения, анемия, лейкопения) и необратимыми (апластическая анемия, отмечают даже после отмены препарата, однократного и местного применения; у детей может сочетаться с развитием миелобластного лейкоза).
Возможны проявления нейротоксичности (спутанность сознания, головная боль, полинейропатии и др.; при длительном применении может развиться неврит зрительного нерва с угрозой потери зрения), симптомы со стороны пищеварительного тракта (глоссит, стоматит, боль или дискомфорт в животе, тошнота, рвота, диарея).
У новорождённых вследствие незрелости ферментных систем печени хлорамфеникол может накапливаться в токсических концентрациях и вызывать «серый синдром», проявляниями которого служат рвота, вздутие живота, дыхательные расстройства, кожа приобретает серый оттенок, далее присоединяются вазомоторный коллапс, гипотермия, ацидоз. Летальность достигает 40%.
Лекарственные взаимодействия
Фармакокинетическое. Ингибируя цитохром P-450, хлорамфеникол увеличивает T1/2 и усиливает эффекты производных сульфонилмочевины, фенитоина, варфарина.
Индукторы цитохрома P-450 (рифампицин и др.) уменьшают концентрацию хлорамфеникола в крови.
Фармакодинамическое. Хлорамфеникол ослабляет гемопоэтическую эффективность препаратов железа, фолиевой кислоты и витамина В12 .
При сочетании с циметидином и цитостатиками повышается риск апластической анемии.
Не рекомендуют сочетание с макролидами и линкозамидами ввиду антагонизма.
Применение в особых ситуациях
Педиатрия. У новорождённых применять с осторожностью ввиду риска развития «серого синдрома». По возможности проводить терапевтический лекарственный мониторинг.
Нарушение функции печени. Применять с осторожностью. По возможности проводить терапевтический лекарственный мониторинг.
АНТИМИКОБАКТЕРИАЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Противотуберкулёзные препараты формируют наиболее представительную группу противогрибковых средств, некоторые из которых активны не только в отношении M. tuberculosis, но и ряда других микобактерий.
В основу классификации противотуберкулёзных препаратов положена их клиническая эффективность, переносимость и лекарственная резистентность: противотуберкулёзные препараты I ряда - основные (изониазид, рифампицин, рифабутин, стрептомицин, пиразинамид, этамбутол); противотуберкулёзные препараты II ряда - резервные (этионамид, протионамид, циклосерин, капреомицин, канамицин, амикацин, ципрофлоксацин, офлоксацин, ломефлоксацин левофлоксацин, аминосалициловая кислота «ПАСК*»).
Свойства аминогликозидов и фторхинолонов, входящих в группу противотуберкулёзных препаратов, описаны в соответствующих главах и в этом разделе не рассмотрены.
Лечение ограниченных форм туберкулёза без выделения M. tuberculosis начинают с назначения комбинации изониазида и рифампицина с другими основными противотуберкулёзными препаратами I ряда. При лечении распространённых форм с выделением M. tuberculosis применяют комбинацию изониазида рифампицина, пиразинамида, этамбутола в сочетании с фторхинолоном, канамицином и/или протионамидом.
В лечении выделяют две фазы.
-
Начальная (интенсивная) терапия, направленная на прекращение размножения и уменьшение количества бактерий (назначают 4 и более противотуберкулёзных препаратов на 3-4 мес).
-
Продолжение лечения для уничтожения персистирующих, преимущественно внутриклеточных форм (2-3 противотуберкулёзных препарата, к которым M. tuberculosis проявляют полную чувствительность, на 4-6 мес).
При лекарственно-резистентном туберкулёзе интенсивную фазу лечения проводят в течение 6 мес с назначением 4-5 противотуберкулёзных препаратов II ряда. Длительность фазы продолжения определяется исходной лекарственной резистентностью микобактерий и составляет более 12 мес.
Противотуберкулёзные препараты I ряда
ИЗОНИАЗИД
Изониазид - производное гидразида изоникотиновой кислоты. Другие производные гидразида изоникотиновой кислоты - фтивазид, метазид, опиниазид - обладают меньшей клинической эффективностью и используются очень редко.
Фармакодинамика
Является пролекарством. После активации микобактериальной каталазой нарушает синтез миколевой кислоты в клеточной стенке. Оказывает бактерицидное действие на размножающиеся M. tuberculosis, бактериостатическое - на находящиеся в стадии покоя. При монотерапии быстро развивается резистетность.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте, биодоступность - 80-90%. Проходит через тканевые барьеры, проникая в клетки и биологические жидкости, в том числе плевральную, асцитическую, СМЖ. Метаболизируется в печени, причём скорость инактивации генетически детерминирована системой цитохрома P-450. Среди людей различают «быстрых инактиваторов», у которых T1/2 составляет около 1 ч, и «медленных инактиваторов» с T1/2 3-4 ч. Выводится преимущественно с жёлчью, около 1 /3 дозы - с мочой.
Показания
Профилактика и лечение активного туберкулёза любой локализации.
Противопоказания
Гиперчувствительность, эпилепсия, тяжёлые психозы, склонность к судорогам, острая печёночная и почечная недостаточность.
Нежелательные лекарственные реакции
Гепатотоксичность (вплоть до гепатита), встречается чаще у «медленных инактиваторов» (профилактика: контроль активности трансаминаз 2 раза в течение первого месяца, затем ежемесячно). Полинейропатии, неврит или атрофия зрительного нерва, тремор, генерализованные судороги, нарушения чувствительности и др. (профилактика: приём пиридоксина в дозе 60-100 мг/сут). Гинекомастия, дисменорея, «кушингоид», гипергликемия. Аллергические реакции. Боли в животе.
При острой передозировке - тошнота, рвота, нарушение зрения и слуха, угнетение дыхания, ступор, кома, судороги.
Лекарственные взаимодействия
Фармакокинетическое. Антациды уменьшают всасывание изониазида в пищеварительном тракте.
При сочетании со стрептомицином возникает замедление выведения обоих препаратов с мочой (следует соблюдать максимально возможные интервалы).
Фармакодинамическое. При сочетании с циклосерином, этионамидом, рядом антиретровирусных ЛС повышается риск нейротоксичности.
При сочетании с рифампицином и алкоголем повышается риск гепатотоксичности.
Применение в особых ситуациях
Беременность. Проходит через плаценту. Возможно возникновение миеломенингоцеле и гипоспадии, геморрагий, задержки психомоторного развития плода. Применять с осторожностью, назначать пиридоксин.
Лактация. Проникает в грудное молоко, достигая концентраций, сопоставимых с таковыми в плазме крови. Возможно развитие гепатита и периферических невритов у ребёнка. Применять с осторожностью. Детям рекомендуют назначение пиридоксина.
Педиатрия. У новорождённых вследствие незрелости ферментов печени возможно увеличение T1/2 изониазида. Применять с осторожностью.
Нарушение функций почек. Риск токсичности повышен при тяжёлой почечной недостаточности (клиренс креатинина менее 10 мл/мин). Применять с осторожностью.
Нарушение функции печени. Возрастает риск гепатотоксичности. Применять с осторожностью.
РИФАМПИЦИН
Полусинтетическое производное природного рифамицина SV с широким спектром активности. Быстрое развитие устойчивости ограничивает показания к применению рифампицина туберкулёзом, атипичными микобактериозами и некоторыми другими инфекциями, при которых неэффективно лечение альтернативными антимикробными ЛС.
Фармакодинамика
Рифампицин оказывает бактерицидный эффект за счёт ингибирования ДНК зависимой РНК-полимеразы. Чувствительны M. tuberculosis, M. leprae, атипичные микобактерии (кроме M. fortuitum), грамположительные кокки, Я. influenzae (в том числе устойчивые к ампициллину и хлорамфениколу), Я. ducreyi, B. pertussis, B. anthracis, листерии, легионеллы, риккетсии.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 95%, снижается в присутствии пищи. Высокие концентрации в мокроте, слюне, назальном секрете, лёгких, плевральном и перитонеальном экссудатах, почках, печени, СМЖ. Проникает в клетки. Проходит через плаценту и проникает в грудное молоко.
Метаболизируется в печени при участии цитохрома P-450 с образованием активного метаболита. Выводится из организма с жёлчью и мочой, причём с увеличением дозы доля почечной экскреции возрастает. T1/2 - 1-4 ч.
Показания
Лечение как впервые выявленного, так и рецидивов туберкулёза. Профилактика и лечение атипичных микобактериозов у ВИЧ-инфицированных пациентов (в сочетании с азитромицином, ципрофлоксацином и др.). Лепра (в сочетании с клофазимином8, дапсоном, этионамидом и др.). Инфекции, вызванные MRSA (в сочетании с ванкомицином и др.). Легионеллёз (в сочетании с макролидами). Санация носителей менингококка. Профилактика инфекций, вызванных Я. influenzae типа B.
Противопоказания
Гиперчувствительность, тяжёлые заболевания печени и почек.
Нежелательные лекарственные реакции
Понижение аппетита, тошнота, рвота, диарея. Повышение активности трансаминаз и уровня билирубина в крови; редко - лекарственный гепатит (факторы риска: алкоголизм, заболевания печени). Аллергические реакции (перекрёстные с рифабутином). Гриппоподобный синдром (чаще при нерегулярном приёме). Тромбоцитопеническая пурпура, нейтропения.
Лекарственные взаимодействия
Фармакокинетическое. Рифампицин - сильный индуктор цитохрома P-450. Ускоряет метаболизм, снижает концентрации в крови и ослабляет действие непрямых антикоагулянтов, оральных контрацептивов, глюкокортикоидов, оральных противодиабетических ЛС, хинидина, циклоспорина, хлорамфеникола, доксициклина, кетоконазола, итраконазола и др.
Пиразинамид снижает концентрацию рифампицина в плазме крови.
Фармакодинамическое. Антагонизм при сочетании с оксациллином и циклосерином.
Применение в особых ситуациях
Беременность, лактация. Применять с осторожностью.
Педиатрия. У новорождённых и недоношенных используют только по жизненным показаниям в связи с возрастной незрелостью ферментных систем печени.
Гериатрия. У лиц пожилого возраста применять с осторожностью в связи с возможными возрастными изменениями функции печени.
Нарушение функции печени. С осторожностью применять при указаниях на заболевания печени в анамнезе. Противопоказан при тяжёлых нарушениях функции печени.
Алкоголизм. Возрастает риск гепатотоксичности.
РИФАБУТИН
Производное природного рифамицина S. По многим свойствам сходен с рифампицином.
Отличия:
-
более слабо индуцирует цитохром P450, поэтому лекарственные взаимодействия менее вероятны;
-
активен в отношении некоторых рифампицино-резистентных штаммов M. tuberculosis;
-
более активен против атипичных микобактерий (M. avium-intracellulare, M. fortuitum, M. kansasii, M. marinum, M. xenopi и др.);
-
более длительный T1/2 - 35-45 ч, что позволяет назначать рифабутин через день;
-
флуконазол и кларитромицин ингибируют метаболизм рифабутина и повышают его концентрацию в крови.
Показания
Лечение туберкулёза у пациентов, которые получают ЛС, имеет высокий риск неблагоприятных взаимодействий с рифампицином (особенно антиретровирусные). Туберкулёз различной локализации, вызванный рифампицинорезистентными, но чувствительными к рифабутину, штаммами. Лечение инфекций, вызванных M. avium-intracellulare и другими атипичными микобактериями. Профилактика атипичных микобактериозов при ВИЧ-инфекции.
Противопоказания
Гиперчувствительность, тяжёлые заболевания печени, беременность, кормление грудью, возраст до 14 лет.
Применение в особых ситуациях
Гериатрия. Учитывать возможные возрастные изменения функции печени и связанный с этим риск кумуляции и повышенной гепатотоксичности.
ПИРАЗИНАМИД
Фармакодинамика
Оказывает слабое бактерицидное действие на M. tuberculosis. Выраженное «стерилизующее» действие, особенно внутри макрофагов и в очагах свежего воспаления. Действует на медленно размножающиеся микобактерии, имеющие как вне-, так и внутриклеточную локализацию. Точный механизм действия не установлен.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 80-90%. Быстро проникает во все ткани и биологические жидкости организма.
Метаболизируется преимущественно в печени. Большая часть метаболитов (70%) выводится с мочой. T1/2 - 9-12 ч, при почечной недостаточности удлиняется.
Показания
Лечение туберкулёза в комбинации с другими противотуберкулёзными препаратами.
Противопоказания
Гиперчувствительность, тяжёлые заболевания почек и печени, подагра, тяжёлые нарушения функции пищеварительного тракта, гипотиреоз, психозы.
Нежелательные лекарственные реакции
Тошнота, рвота. Гиперурикемия с артралгией и миалгией (в отличие от подагры поражаются как крупные, так и мелкие суставы). Повышение активности трансаминаз, дозозависимая гепатотоксичность. Тромбоцитопения, сидеробластная анемия. Лекарственная лихорадка. Дизурия.
Лекарственные взаимодействия
Фармакодинамическое. Усиление эффекта при сочетании с изониазидом, рифампицином, фторхинолонами.
Применение в особых ситуациях
Беременность, лактация. Использовать с осторожностью.
Нарушения функций почек и печени. Противопоказан при тяжёлых заболеваниях почек и печени.
ЭТАМБУТОЛ
Фармакодинамика
Оказывает бактериостатическое действие, связанное с ингибированием ферментов, участвующих в синтезе клеточной стенки микобактерий. Активен только в отношении размножающихся микроорганизмов. Чувствительны M. tuberculosis и ряд атипичных микобактерий (M. kansasii, M. avium, M. xenopi).
Фармакокинетика
Хорошо всасывается в пищеварительном тракте, биодоступность - 75-80%. Проникает в большинство тканей и биологических жидкостей организма, включая СМЖ. Внутриклеточная концентрация в 2 раза выше внеклеточной. Депонируясь в эритроцитах, длительно циркулирует в крови. Выводится преимущественно почками в неизменённой форме (около 50%) и в виде метаболитов (8-15%). Часть этамбутола выводится через пищеварительный тракт в неизменённом виде. T1/2 - 3-4 ч, может удлиняться при почечной недостаточности.
Показания
Впервые выявленный туберкулёз или рецидив. Особенно показан при предполагаемой первичной резистентности к другим противотуберкулёзным препаратам.
Противопоказания
Гиперчувствительность, неврит зрительного нерва, катаракта, диабетическая ретинопатия, воспалительные заболевания глаз, возраст до 2 лет.
Нежелательные лекарственные реакции
Головокружение, ретробульбарный неврит, периферические полиневропатии, парестезии, депрессия, тошнота, рвота, аллергические реакции.
Лекарственные взаимодействия
Фармакодинамическое. При сочетании с производными гидразида изоникотиновой кислоты замедляет развитие устойчивости к ним M. tuberculosis. Антагонизм с этионамидом.
Применение в особых ситуациях
Беременность, лактация. Использовать с осторожностью.
Педиатрия. Не назначать детям до 2 лет ввиду невозможности адекватного контроля зрения.
Гериатрия. В связи с возрастными изменениями функций почек может потребоваться коррекция дозы.
Нарушение функций почек. При почечной недостаточности требуется коррекция дозы.
Противотуберкулёзные препараты II ряда
ЦИКЛОСЕРИН
Фармакодинамика
За счёт конкурентного антагонизма с D-аланином ингибирует ферменты, ответственные за его синтез в микробной клетке. В зависимости от концентрации может проявлять как бактериостатический, так и бактерицидный эффект. Клиническое значение имеет активность в отношении M. tuberculosis и некоторых атипичных микобактерий.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте, биодоступность - 70-90%. При повторных приёмах возможна кумуляция. Хорошо проникает в ткани и жидкости организма. Терапевтические уровни отмечают в мокроте, слизистой оболочке бронхиального дерева, лёгочной ткани, плевральной и брюшной полостях, лимфатических узлах. Проходит через ГЭБ, плаценту и проникает в грудное молоко. Частично метаболизируется в печени. Выводится почками, преимущественно в активной форме. T1/2 - около 10 ч, при почечной недостаточности увеличивается.
Показания
Лекарственно-устойчивый туберкулёз (лёгочный и внелёгочный) - на всех стадиях и при всех формах заболевания. Атипичные микобактериозы, вызываемые M. avium-intracellulare, M. xenopi и др.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, почечная недостаточность, психозы, эпилепсия, органические заболевания ЦНС, наркомания, алкоголизм.
Нежелательные лекарственные реакции
Нейротоксичность (до 75% всех НЛР могут отмечаться у 30% пациентов): головная боль, головокружение, дезориентация, сонливость, раздражительность, в тяжёлых случаях - нарушение зрения, депрессия, психоз, эпилептические судороги (профилактика: суточная дозе не более 1,0 г, терапевтический лекарственный мониторинг, концентрация в крови не более 25-30 мг/л, применение пиридоксина; меры помощи: назначение седативных и противосудорожных ЛС). Тошнота, потеря аппетита, диарея, запор. Реакция бактериолиза: гипертермия, увеличение количества мокроты, повышение скорости оседания эритроцитов (СОЭ), лейкоцитоз.
Лекарственные взаимодействия
Фармакодинамическое. Риск нейротоксичности возрастает при сочетании с изониазидом и/или этионамидом (профилактика: пиридоксин, глутаминовая кислота), а также с другими нейротоксичными ЛС, кофеином, алкоголем.
Применение в особых ситуациях
Педиатрия. Использовать с осторожностью.
Гериатрия. В связи с возможными возрастными изменениями функций почек увеличивается риск кумуляции и токсичности циклосерина. Может потребоваться коррекция дозы.
ЭТИОНАМИД, ПРОТИОНАМИД
Фармакодинамика
За счёт антагонизма с никотиновой кислотой блокируют синтез миколевых кислот и нарушают синтез белка. Оказывают бактериостатическое действие. Активны в отношении M. tuberculosis, в более высоких концентрациях - M. leprae и некоторых атипичных микобактерий. Действуют на быстро и медленно размножающиеся микроорганизмы, имеющие как вне-, так и внутриклеточную локализацию.
Фармакокинетика
Хорошо всасываются в пищеварительном тракте. Распределяются во все ткани и жидкости организма, включая СМЖ. Проникают в полости и инкапсулированные образования. Метаболизируются в печени, метаболиты выводятся почками. T1/2 - 2-3 ч.
Показания
Лечение туберкулёза при устойчивости к другим противотуберкулёзным препаратам.
Противопоказания
Гиперчувствительность, острый гастрит, язвенная болезнь желудка и двенадцатиперстной кишки, язвенный колит, цирроз и другие заболевания печени, беременность, возраст до 14 лет.
Нежелательные лекарственные реакции
Анорексия, тошнота, неприятный вкус во рту, отрыжка с неприятным запахом, саливация, рвота. Аллергические реакции. Сонливость, депрессия. Фотосенсибилизация. Гепатотоксичность вплоть до гепатита.
Протионамид переносится несколько лучше этионамида.
Профилактика НЛР: сочетать с пиридоксином или препаратами висмута.
Лекарственные взаимодействия
Фармакодинамическое. При сочетании с изониазидом и рифампицином повышается риск гепатотоксичности, с циклосерином - риск судорог. При сочетании с аминосалициловой кислотой возможны эндокринные нарушения (гипотиреоз, гинекомастия, импотенция).
Применение в особых ситуациях
Лактация. Применять с осторожностью.
Педиатрия. Не рекомендуют назначать детям до 14 лет, более старшим - с осторожностью.
АМИНОСАЛИЦИЛОВАЯ КИСЛОТА
Фармакодинамика
Активность в отношении M. tuberculosis обусловлена антагонизмом с парааминобензойной кислотой, являющейся фактором их роста. Аминосалициловая кислота действует преимущественно на внеклеточные микобактерии, пребывающие в состоянии активного размножения.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Метаболизируется в печени и частично - в желудке. Выводится с мочой. T1/2 - 30 мин.
Показания
Лечение туберкулёза при непереносимости других противотуберкулёзных препаратов или множественной устойчивости микобактерий.
Противопоказания
Гиперчувствительность, тяжёлая патология почек и печени, язвенная болезнь желудка и двенадцатиперстной кишки, неконтролируемая сердечная недостаточность, беременность, кормление грудью, гипотиреоз.
Нежелательные лекарственные реакции
Тошнота, рвота, диарея, боль в животе (за счёт сильного раздражающего эффекта). Аллергические реакции. Повышение активности трансаминаз, нарушение синтеза протромбина. Гипокалиемия, агранулоцитоз, гипотиреоз, кристаллурия.
Лекарственные взаимодействия
Фармакокинетическое. Повышает концентрацию изониазида в крови (конкуренция за пути метаболизма).
Нарушает всасывание рифампицина, эритромицина, линкомицина (интервалы между приёмами не менее 8 ч).
Нарушает усвоение витамина B12, риск развития анемии при тяжёлом туберкулёзе.
Фармакодинамическое. При сочетании с капреомицином возрастает риск электролитных нарушений.
При сочетании с этионамидом или протионамидом возможны эндокринные нарушения (гипотиреоз, гинекомастия, импотенция).
КАПРЕОМИЦИН
Фармакодинамика
Подавляет синтез белков, нарушая рибосомальную функцию микробной клетки. Активен в отношении M. tuberculosis, M. bovis, M. kansasii и M. avium. На микобактерии, расположенные внеклеточно, действует бактериостатически, а локализующиеся внутриклеточно - бактерицидно.
Фармакокинетика
Плохо всасывается в пищеварительном тракте, вводится внутримышечно. Не проходит через ГЭБ. Проникает через плаценту. Не метаболизируется, выводится почками в активной форме. T1/2 - 4-6 ч.
Показания
Лечение туберкулёза при устойчивости к противотуберкулёзным препаратам I ряда или их плохой переносимости (см. табл. 20-21).
Противопоказания
Гиперчувствительность, беременность, кормление грудью, детский возраст.
Нежелательные лекарственные реакции
Почечная недостаточность. Снижение в крови концентрации калия, железа, кальция, фосфора. Ототоксичность (звон в ушах, ослабление слуха), головокружение, нервно-мышечная блокада, аллергические реакции. Боль в месте инъекции, инфильтраты, стерильные абсцессы.
Таблица 20-21. Дозирование противотуберкулёзных препаратов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Изониазид |
Внутрь 4-6 мг/(кг х сут) в 1 приём; при туберкулёзном менингите - 10 мг/(кгх сут); парентерально 0,2-0,3 г в сут в 1 введение |
Внутрь и парентерально 10-15 мг/(кгх сут) (до 0,3 г в сут) в 1-2 введения |
Рифампицин |
Внутрь 10-20 мг/(кгх сут) (до 0,6 г в сут) в 1 приём за 1 ч до еды; |
Внутрь (за 1 ч до еды) и в/в 10-20 мг/(кгх сут) (до 0,6 г в сут) в 1 введение |
Рифабутин |
Внутрь при туберкулёзе 0,15-0,3 г в сут в 1 приём; при атипичных микобактериозах - 0,45-0,6 г в сут |
— |
Пиразинамид |
Внутрь 1,5-2,0 г в сут в 1 приём ежедневно или 2,0-2,5 г в сут 3 раза в нед |
Внутрь 20-40 мг/(кгх сут) в 1 приём |
Этамбутол |
Внутрь 15-20 мг/(кг х сут) в 1 приём ежедневно или 30 мг/(кгх сут) 3 раза в нед |
Внутрь 15-25 мг/(кгх сут) (до 2,5 г в сут) в 1 приём |
Циклосерин |
Внутрь 0,25 г каждые 12 ч в течение 2 нед, далее 10-20 мг/(кгх сут) в 2 приёма |
Внутрь 10-20 мг/(кгх сут) (до 1 г в сут) в 2 приёма |
Этионамид, протионамид |
Внутрь 15-20 мг/(кгх сут) (до 1 г в сут) в 1-3 приёма |
Внутрь 15-20 мг/(кгх сут) (до 1 г в сут) в 1-3 приёма |
Аминосалициловая кислота |
Внутрь 10-12 г в сут в 3-4 приёма |
Внутрь 200-300 мг/(кгх сут) (до 12 г в сут) в 2-3 приёма |
Капреомицин |
В/м 15-30 мг/(кгх сут) (до 1 г в сут) в 1 введение |
В/м 15-30 мг/(кгх сут) (до 1 г в сут) в 1 введение |
Лекарственные взаимодействия
Фармакодинамическое. Нефротоксичность усиливается при сочетании с аминогликозидами и полимиксинами, ототоксичность - при сочетании с аминогликозидами, полимиксинами, петлевыми диуретиками, риск электролитных нарушений - при сочетании с аминосалициловой кислотой.
Применение в особых ситуациях
Гериатрия. В связи с возможными возрастными изменениями функций почек может потребоваться коррекция дозы.
Нарушение функций почек. При почечной недостаточности возрастает риск нефротоксичности. Необходима коррекция дозы.
Заболевания ЦНС. У пациентов с миастенией и паркинсонизмом возрастает риск развития нервно-мышечной блокады.
Комбинированные противотуберкулёзные препараты
Комбинированные противотуберкулёзные препараты - различные сочетания препаратов I ряда: рифампицина, изониазида, пиразинамида, этамбутола. Их использование наиболее оправдано при лечении в амбулаторных условиях и у пациентов, которые высказывают опасение или недоверие к приёму большого числа таблеток. При назначении комбинированных противотуберкулёзных препаратов следует помнить об особенностях НЛР каждого из компонентов и возможности их суммации. Следует с осторожностью применять у пациентов с патологией печени, подагрой, сахарным диабетом, лицам пожилого возраста. В процессе лечения необходим контроль функции печени, уровня мочевой кислоты в крови, зрения.
ПРОТИВОГРИБКОВЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Активностью в отношении микроскопических грибов (микромицетов) обладают ЛС как природного происхождения, так и полученные путём химического синтеза. Их разделяют на несколько групп, отличных по структуре, спектру действия, фармакокинетике и клиническому применению (табл. 20-22, 20-23).
Таблица 20-22. Классификация противогрибковых лекарственных средств
| Группы | Препараты |
|---|---|
Полиены |
Нистатин |
Натамицин |
|
Амфотерицин В |
|
Азолы |
|
Для системного применения |
Кетоконазол |
Флуконазол |
|
Итраконазол |
|
Вориконазол |
|
Для местного применения |
Клотримазол, миконазол, бифоназол и др. |
Эхинокандины |
Каспофунгин |
Аллиламины |
Тербинафин |
Нафтифин |
|
Гризеофульвин |
|
Прочие |
Аморолфин |
Циклопирокс |
|
Полиены
Полиены - природные противогрибковые ЛС. Нистатин и натамицин применяют местно и внутрь, амфотерицин В - внутривенно. Амфотерицин B липосомальный и липидный комплекс амфотерицина В - современные липидные формы с улучшенной переносимостью, поскольку они обеспечивают высвобождение активного вещества только при соприкосновении с клетками гриба и относительную интактность по отношению к нормальным тканям.
Фармакодинамика
В зависимости от концентрации оказывают фунгистатическое или фунгицидное действие, обусловленное связыванием с эргостеролом цитоплазматической мембраны грибов, что ведёт к нарушению её целостности и гибели клетки.
К амфотерицину В чувствительны Candida spp., аспергиллы, криптококки, возбудители эндемичных микозов и некоторые другие грибы. Нистатин и натамицин действуют преимущественно на Candida spp.
Полиены активны также в отношении некоторых простейших - трихомонад (натамицин), лейшманий и амёб (амфотерицин В).
Фармакокинетика
Полиены практически не всасываются в пищеварительном тракте и при местном применении. Амфотерицин В при внутривенном введении распределяется во многие органы и ткани (лёгкие, печень, почки, надпочечники, мышцы и др.), плевральную, перитонеальную, синовиальную и внутриглазную жидкость. Плохо проходит через ГЭБ. Медленно экскретируется почками. - 24-48 ч, при длительном применении может увеличиваться до 2 нед за счёт кумуляции в тканях.
Липидные формы амфотерицина В создают более высокие концентрации в крови, чем стандартный препарат, а также в тканях ЦНС. Практически не проникают в ткань почек (поэтому менее нефротоксичны). - 6-18 ч.
Показания
Нистатин, натамицин
Кандидоз кожи, полости рта и глотки, кишечника. Кандидозный вульвовагинит.
Натамицин
Кандидозный баланопостит. Tрихомонадный вульвовагинит.
Амфотерицин В
Tяжёлые формы инвазивных микозов (кандидоз, аспергиллёз, криптококкоз, мукормикоз, фузариоз, эндемичные микозы и др.). Эмпирическая антифунгальная терапия. Лейшманиоз.
Липидные формы амфотерицина В
Tяжёлые формы инвазивных микозов у пациентов с почечной недостаточностью, при неэффективности стандартного препарата (возможность применения более высоких доз), при его нефротоксичности или некупируемых премедикацией выраженных реакциях на внутривенную инфузию.
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Нистатин, натамицин
Боль в животе, тошнота, рвота, диарея, аллергические реакции, раздражение кожи и слизистых оболочек.
Амфотерицин В
Инфузионные реакции: лихорадка, озноб, тошнота, рвота, головная боль, гипотензия. Боль в месте инфузии, флебит, тромбофлебит. Олигоурия или полиурия, гиперкреатининемия. Гепатотоксичность. Гипокалиемия, гипомагниемия. Анемия, реже лейкопения или тромбоцитопения. Боль в животе, анорексия, тошнота, рвота, диарея. Головная боль, головокружение, парезы, нарушение чувствительности, тремор, судороги. Аллергические реакции.
Липидные формы реже вызывают анемию, лихорадку, озноб, гипотензию, менее нефротоксичны.
Лекарственные взаимодействия
Фармакодинамическое. При сочетании с метотрексатом, хлорамфениколом и другими ЛС, угнетающими гемопоэз, возрастает риск анемии и других цитопений.
При сочетании с аминогликозидами, ванкомицином, циклоспорином повышается риск тяжёлых нарушений функций почек.
При сочетании с тиазидными или петлевыми диуретиками, глюкокортикоидами повышается риск гипокалиемии, гипомагниемии.
За счёт электролитных нарушений амфотерицин В повышает токсичность сердечных гликозидов.
Применение в особых ситуациях
Беременность, лактация. Применять с осторожностью.
Педиатрия. При кандидозе полости рта у детей до 5 лет предпочтительна суспензия натамицина, так как защёчное применение таблеток может быть затруднительно.
Гериатрия. В связи с возможным снижением функций почек у лиц пожилого возраста повышен риск нефротоксичности амфотерицина В.
Нарушение функций почек. Предпочтительны липидные формы амфотерицина В.
Нарушение функции печени. Более высокий риск гепатотоксичности амфотерицина В. Применять с осторожностью.
Азолы
Фармакодинамика
Азолы обладают преимущественно фунгистатическим эффектом за счёт ингибирования 14α-деметилазы, катализирующей биосинтез эргостерола - основного структурного компонента грибковой мембраны.
К итраконазолу чувствительны Candida spp., аспергиллы, криптококки, дерматомицеты, гистоплазмы, кокцидиоиды и ряд других грибов. Кетоконазол, в отличие от итраконазола, не действует на аспергиллы.
Флуконазол активен преимущественно в отношении Candida spp., криптококков, кокцидиоида, дерматомицетов.
Вориконазол - против всех видов Candida и Aspergillus, включая штаммы, устойчивые к «ранним» азолам. К нему чувствительны также криптококки, грибы рода Fusarium, дерматомицеты, возбудители эндемичных микозов.
Азолы, используемые местно, активны преимущественно в отношении Candida spp., дерматомицетов, Malassezia furfur, некоторых грамположительных кокков и коринебактерий.
Фармакокинетика
Хорошо всасываются в пищеварительном тракте. Биодоступность вориконазола - 96 (натощак), флуконазола - 90, кетоконазола - 75%. Биодоступность итраконазола, назначаемого в виде капсул, выше при приёме с пищей (90-100%), а в виде раствора - натощак (90-100%). Степень связывания с белками плазмы флуконазола - 11, вориконазола - 55, кетоконазола и итраконазола - около 99%.
Флуконазол, вориконазол и кетоконазол создают высокие концентрации в различных органах, тканях и средах. Флуконазол проникает через ГЭБ и гематоофтальмический барьер. Уровни флуконазола в СМЖ составляют 52-85% концентрации в плазме, вориконазола - около 50%. Кетоконазол плохо проходит через ГЭБ и создаёт очень низкие концентрации в СМЖ. Концентрация флуконазола в моче высокая, вориконазола и кетоконазола - низкая.
Итраконазол в связи с высокой липофильностью распределяется преимущественно в органы и ткани с высоким содержанием жира: печень, почки, большой сальник. Накапливается в коже, ногтевых пластинках, лёгких, где его концентрации почти в 7 раз выше, чем в плазме. В экссудате уровни итраконазола в 3,5 раза превышают плазменные. Практически не проникает в водные среды: слюну, внутриглазную жидкость, СМЖ, низкие концентрации в моче.
Кетоконазол, итраконазол и вориконазол метаболизируются в печени при участии цитохрома P450, экскретируются преимущественно из пищеварительного тракта. Итраконазол частично выделяется с секретом сальных и потовых желёз кожи. Флуконазол выводят почки преимущественно в активной форме. T1/2 кетоконазола и вориконазола - 6-10 ч, итраконазола - 20-45 ч, при почечной недостаточности не изменяется. T1/2 флуконазола - 30 ч, при почечной недостаточности может возрастать до 3-4 сут.
Азолы для местного применения создают высокие и достаточно стабильные концентрации в эпидермисе и нижележащих поражённых слоях кожи. Системная абсорбция через кожу минимальна и не имеет клинического значения. При интравагинальном применении всасывание составляет 3-10%.
Показания
Кетоконазол
Кандидоз кожи, пищевода, кандидозная паронихия, вульвовагинит. Отрубевидный лишай. Дерматомикозы, себорейная экзема (местно).
Флуконазол
Инвазивный кандидоз. Кандидоз кожи, слизистых, пищевода, мочевыводящих путей, кандидозная паронихия, онихомикоз, вульвовагинит. Криптококкоз. Дерматофитозы. Отрубевидный лишай. Споротрихоз. Сцедоспориоз. Трихоспороз. Бластомикоз, кокцидиоидоз, паракокцидиоидоз. Эмпирическая антифунгальная терапия.
Итраконазол
Дерматофитозы. Отрубевидный лишай. Кандидоз пищевода, кожи и слизистых оболочек, ногтей, кандидозная паронихия, вульвовагинит. Криптококкоз. Аспергиллёз. Сцедоспориоз. Феогифомикозы. Хромомикоз. Споротрихоз. Эндемичные микозы.
Вориконазол
Аспергиллёз. Инвазивный кандидоз. Кандидоз пищевода. Фузариоз. Сцедоспориоз. Другие инвазивные микозы при неэффективности или плохой переносимости других антимикотиков.
Азолы для местного применения
Кандидоз кожи, полости рта и глотки, кандидозный вульвовагинит. Дерматофитозы (при ограниченных поражениях). Отрубевидный лишай. Эритразма.
Противопоказания
Гиперчувствительность, беременность, кормление грудью (системно), тяжёлые нарушения функции печени (кетоконазол, итраконазол), сердечная недостаточность (итраконазол), возраст до 16 лет (итраконазол), до 2 лет (вориконазол).
Нежелательные лекарственные реакции
Боль в животе, нарушение аппетита, тошнота, рвота. Головная боль, головокружение, сонливость, нарушения зрения, парестезии, тремор. Аллергические реакции. Тромбоцитопения, агранулоцитоз. Повышение активности трансаминаз, холестатическая желтуха.
Дополнительно для итраконазола: застойная сердечная недостаточность, артериальная гипертензия, гипокалиемия, отёки.
Дополнительно для кетоконазола: гепатотоксичность вплоть до развития гепатита, нарушение выработки тестостерона и кортикостероидов, сопровождаемое у мужчин гинекомастией, олигоспермией, импотенцией, у женщин - нарушением менструального цикла.
Дополнительно для вориконазола: нарушения зрения, фотофобия, фотосенсибилизация.
При интравагинальном применении: зуд, жжение, гиперемия и отёк слизистой оболочки, выделения из влагалища, учащение мочеиспускания.
Лекарственные взаимодействия
Фармакокинетическое. Антациды, сукральфат и антисекреторные ЛС уменьшают биодоступность кетоконазола и итраконазола.
Кетоконазол, итраконазол, вориконазол и в меньшей степени флуконазол ингибируют цитохром P450 и нарушают метаболизм в печени многих ЛС: пероральных антидиабетических, непрямых антикоагулянтов, циклоспорина, дигоксина, теофиллина, что может привести к повышению их концентрации в крови и токсическим эффектам. Необходим клинический контроль, мониторинг концентраций ЛС с возможной коррекцией их дозировки. Нельзя сочетать с терфенадином 8, астемизолом8, цизапридом8, хинидином, пимозидом8 (удлинение интервала Q-T, тяжёлые нарушения ритма), ловастатином и симвастатином (рабдомиолиз). Индукторы цитохрома P450 (рифампицин, рифабутин, изониазид и др.) усиливают метаболизм азолов в печени и понижают их концентрации в плазме. Такие сочетания не рекомендуются.
Ингибиторы цитохрома P450 (циметидин, эритромицин и др.) нарушают метаболизм кетоконазола и итраконазола и повышают их концентрации в крови. Возможно повышение риска кардиотоксичности итраконазола.
При приёме алкоголя на фоне лечения кетоконазолом возможна дисульфирамоподобная реакция.
Применение в особых ситуациях
Беременность. Системное применение не рекомендовано. Интравагинальное не рекомендуют в I триместре, в других - не более 7 дней. Наружно следует использовать с осторожностью.
Гериатрия. У пожилых лиц в связи с возрастными изменениями функций почек возможно нарушение экскреции флуконазола, может потребоваться коррекция режима дозирования.
Нарушение функций почек. При почечной недостаточности нарушается экскреция флуконазола, что может сопровождать его кумуляция и токсические эффекты. Требуется коррекция режима его дозирования и периодический контроль клиренса креатинина.
Нарушение функции печени. Кетоконазол и итраконазол противопоказаны при тяжёлых нарушениях функции печени. У пациентов с лёгкой/умеренной печёночной недостаточностью поддерживающую дозу вориконазола следует уменьшить в 2 раза. Необходим регулярный клинико-лабораторный контроль.
Сердечная недостаточность. Итраконазол не следует использовать у пациентов с нарушением сердечной функции.
Эхинокандины
Единственный зарегистированый в России представитель группы эхинокандинов - каспофунгин.
Фармакодинамика
Каспофунгин блокирует синтез 1,3-β-D-глюкана - важного структурнофункционального компонента клеточной стенки грибов. Клиническое значение имеет активность в отношении Aspergillus spp. (включая резистентные к амфотерицину В) и Candida spp. (включая резистентные к азолам).
Фармакокинетика
Плохо всасывается в пищеварительном тракте, вводится внутривенно. Имеет высокую степень связывания с белками плазмы - 97%. Создаёт высокие концентрации в почках, печени, селезёнке и лёгких, более низкие - в головном мозге. Метаболизируется в печени без участия цитохрома P450. T1/2 - 9-11 ч.
Показания
Инвазивный кандидоз. Кандидоз пищевода. Инвазивный аспергиллёз при неэффективности других антимикотиков или их плохой переносимости. Эмпирическая терапия при фебрильной нейтропении.
Противопоказания
Гиперчувствительность, беременность, кормление грудью.
Нежелательные лекарственные реакции
Лихорадка, флебит, головные боли, аллергические рекции; повышение активности трансаминаз, ЩФ.
Лекарственные взаимодействия
Фармакокинетическое. Рифампицин, дексаметазон и карбамазепин повышают, а циметидин снижает клиренс каспофунгина, что может потребовать коррекции его дозы.
Применение в особых ситуациях
Педиатрия. Отсутствуют данные о безопасности у лиц моложе 18 лет. В этих возрастных группах применять только по жизненным показаниям.
Гериатрия. У пациентов старше 65 лет применять с осторожностью.
Нарушение функции печени. При умеренной печёночной недостаточности поддерживающую дозу следует уменьшить.
Аллиламины
К аллиламинам относят тербинафин, применяемый внутрь и местно, и нафтифин, предназначенный только для местного использования.
Фармакодинамика
Аллиламины блокируют ранние стадии биосинтеза эргостерола, ингибируя фермент скваленэпоксидазу. Обладают преимущественно фунгицидным действием. Клиническое значение имеет активность в отношении дерматомицетов (Trichophyton, Microsporum и Epidermophyton spp.), возбудителей хромомикоза, споротрикса, M. furfur, Candida spp.
Фармакокинетика
Tербинафин хорошо всасывается в пищеварительном тракте. Биодоступность - 80%, практически не зависит от пищи. Почти полностью (на 99%) связывается с белками плазмы. За счёт высокой липофильности распределяется во многие ткани. Выделяясь через кожу, с секретами сальных и потовых желёз, создаёт высокие концентрации в роговом слое эпидермиса, ногтевых пластинках, волосяных фолликулах, волосах. Метаболизируется в печени при участии цитохрома P450, выводится почками. T1/2 - 11-17 ч, возрастает при почечной и печёночной недостаточности. При местном применении абсорбция тербинафина и нафтифина около 5%.
Показания
Дерматофитозы, онихомикоз, хромомикоз, споротрихоз. Местно - при кандидозе кожи, отрубевидном лишае.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, возраст до 2 лет.
Нежелательные лекарственные реакции
Боль в животе, нарушение аппетита, тошнота, рвота, диарея, изменение вкуса. Головная боль, головокружение, аллергические реакции, нейтропения, панцитопения, повышение активности трансаминаз, холестатическая желтуха, печёночная недостаточность, артралгия, миалгия.
При местном применении - зуд, жжение, гиперемия и сухость кожи.
Лекарственные взаимодействия
Фармакокинетическое. Индукторы цитохрома P450 (рифампицин и др.) усиливают метаболизм тербинафина и увеличивают его клиренс. Ингибиторы цитохрома P450 (циметидин и др.) блокируют метаболизм тербинафина и снижают его клиренс. Может возникнуть необходимость коррекции дозы тербинафина.
Применение в особых ситуациях
Гериатрия. У пожилых людей в связи с возрастными изменениями функций почек возможно нарушение экскреции тербинафина, может потребоваться коррекция дозы.
Нарушение функций почек. Необходим контроль клиренса креатинина. При почечной недостаточности требуется коррекция режима дозирования тербинафина.
Нарушение функции печени. Повышение риска гепатотоксичности тербинафина. Необходим адекватный клинико-лабораторный контроль.
Гризеофульвин
Один из ранних природных антимикотиков, продуцируется грибом рода Penicillium.
Фармакодинамика
Обладает фунгистатическим эффектом, который обусловлен ингибированием митотической активности грибковых клеток в метафазе и нарушением синтеза ДНК. Чувствительны только дерматомицеты.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 79-90%, больше при приёме с жирной пищей. Максимальная концентрация в крови отмечается через 4 ч. Избирательно накапливается в «прокератиновых» клетках кожи, волос, ногтей. Tолько незначительная часть распределяется в другие ткани. Метаболизируется в печени при участии цитохрома P450. Выводится с калом (36% в активной форме) и мочой (менее 1%). T1/2 - 15-20 ч.
Показания
Микозы кожи, вызванные дерматомицетами, микроспория, трихофития волосистой части головы, онихомикоз.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, нарушения функции печени, системная красная волчанка.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота, диарея. Головная боль, головокружение, бессонница, периферические невриты. Аллергические реакции, фотодерматит. Гранулоцитопения, лейкопения. Повышение активности трансаминаз, желтуха, гепатит. Кандидоз полости рта, волчаночноподобный синдром.
Лекарственные взаимодействия
Фармакокинетическое. Индукторы цитохрома P450 (барбитураты, рифампицин и др.) усиливают метаболизм гризеофульвина и ослабляют его эффект.
Гризеофульвин индуцирует цитохром P450, поэтому может усиливать метаболизм и, следовательно, ослаблять действие непрямых антикоагулянтов, пероральных антидиабетических ЛС, теофиллина, оральных контрацептивов. Необходим строгий клинический и лабораторный контроль, может потребоваться изменение доз ЛС.
Гризеофульвин усиливает действие алкоголя.
Применение в особых ситуациях
Гериатрия. У пожилых лиц в связи с возрастными изменениями функции печени повышен риск гепатотоксичности. Необходим строгий клинико-лабораторный контроль.
Аморолфин
Синтетический антимикотик для местного применения в виде лака для ногтей, производное морфолина.
Таблица 20-23. Режимы дозирования противогрибковых препаратов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Амфотерицин В |
В/в тест-доза 1 мг в 20 мл 5% глюкозы в течение 1 ч; лечебная доза - 0,3-1,5 мг/(кгх сут) |
В/в тест-доза 1 мг в 20 мл 5% глюкозы в течение 1 ч; лечебная доза - 0,3-1,5 мг/(кгх сут) |
Амфотерицин В липосомальный |
В/в 1-5 мг/(кгх сут) |
В/в 1-5 мг/(кгх сут) |
Липидный комплекс амфотерицина В |
В/в 1-5 мг/(кгх сут) |
В/в 1-5 мг/(кгх сут) |
Нистатин |
Внутрь от 500 тыс до1 млн ЕД каждые 6 ч; при кандидозе полости рта и глотки рассасывать по 1 таблетке каждые 6-8 ч после еды; интравагинально по 1-2 таблетке на ночь; местно мазь наносят на поражённые участки кожи 2 раза в сут |
Внутрь 125-250 тыс. ЕД каждые 6 ч; |
Итраконазол |
Внутрь 0,1-0,6 г каждые 12-24 ч; при кандидозном вульвовагините - 0,2 г каждые 12 ч один день или 0,2 г/сут в течение 3 дней |
— |
Флуконазол |
Внутрь 0,1-0,6 г/сут в 1 приём, при споротрихозе и псевдоаллешериозе - до 0,8-1,2 г/сут; при кандидозном онихомикозе и паронихии - 0,15 г 1 раз в нед.; при отрубевидном лишае - 0,4 г однократно; при кандидозном вульвовагините - 0,15 г однократно; В/в 0,1-0,6 г/сут в 1 введение; при споротрихозе и псевдоаллешериозе - до 0,8-1,2 г/сут |
Внутрь и в/в при кандидозе кожи и слизистых оболочек - 1-2 мг/(кг х сут) в 1 введение; при инвазивном кандидозе и криптококкозе - 6-12 мг/(кгх сут) в 1 введение |
Кетоконазол |
Внутрь 0,2-0,4 г/сут в 2 приёма; интравагинально по 1 супп. на ночь; |
— |
Вориконазол |
Внутрь доза насыщения при массе тела менее 40 кг - 0,4 г/сут в 2 приёма, при массе более 40 кг - 0,8 г/сут в 2 приёма; поддерживающая доза при массе менее 40 кг - 0,2-0,3 г/сут в 2 приёма, при массе более 40 кг - 0,4-0,6 г/сут в 2 приёма; в/в доза насыщения - 6 мг/кг каждые 12 ч, поддерживающая доза - 4 мг/кг каждые 12 ч |
Старше 2 лет - внутрь и в/в 6 мг/кг каждые 12 ч в первые сут, далее 4 мг/кг каждые 12 ч |
Каспофунгин |
В/в 70 мг в первые сут, далее 50 мг каждые 24 ч |
— |
Тербинафин |
Внутрь 0,25 г/сут в 1 приём; |
Старше 2 лет - внутрь при массе тела менее 20 кг - 62,5 мг/сут, 20-40 кг - 0,125 г/сут, более 40 кг - 0,25 г/сут в 1 приём; |
Гризеофульвин |
Внутрь 0,25-0,5 г каждые 12 ч |
Внутрь 10 мг/(кгх сут) в 1-2 приёма |
Фармакодинамика
В зависимости от концентрации может оказывать как фунгистатическое, так и фунгицидное действие, обусловленное нарушением структуры цитоплазматической мембраны клетки грибов. Чувствительны дерматомицеты, Candida spp., Malassezia spp., криптококки и ряд других грибов.
Фармакокинетика
Хорошо проникает в ногтевую пластинку и ногтевое ложе. Системная абсорбция незначительна и не имеет клинического значения.
Показания
Онихомикоз, вызванный дерматомицетами, дрожжевыми и плесневыми грибами (если поражено не более 1/3 ногтевой пластинки), профилактика онихомикоза.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, возраст до 6 лет.
Нежелательные лекарственные реакции
Жжение, зуд или раздражение кожи около ногтя.
Лекарственные взаимодействия
Системные антимикотики усиливают эффект аморолфина.
Циклопирокс
Синтетический антимикотик для местного применения.
Фармакодинамика
Механизм действия точно не установлен. Клиническое значение имеет активность в отношении дерматомицетов, Candida spp., M. furfur и некоторых других грибов.
Фармакокинетика
Быстро проникает в различные слои кожи и её придатки, создавая высокие локальные концентрации, в 20-30 раз превышающие минимальную подавляющую концентрацию для основных возбудителей поверхностных микозов. При нанесении на обширные участки может незначительно всасываться (в крови обнаруживают 1,3% дозы), на 94-97% связывается с белками плазмы, выводится почками. Т1/2 - 1,7 ч.
Показания
Дерматомикозы. Онихомикоз (если поражено не более 1/3 ногтевой пластинки). Грибковый вагинит и вульвовагинит. Профилактика грибковых инфекций стоп.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, возраст до 6 лет.
Нежелательные лекарственные реакции
Жжение, зуд, раздражение, шелушение или гиперемия кожи.
Лекарственные взаимодействия
Системные антимикотики усиливают эффект циклопирокса.
ПРОТИВОВИРУСНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Противогерпетические препараты
К основным противогерпетическим препаратам, эффективность которых доказана в рандомизированных клинических исследованиях, относят аналоги нуклеозидов - ацикловир, валацикловир, пенцикловир и фамцикловир. Причём валацикловир и фамцикловир исходно неактивные соединения, которые в организме человека превращаются в ацикловир и пенцикловир соответственно.
Фармакодинамика
Противовирусное действие оказывают активные метаболиты ацикловира и пенцикловира - ацикловира трифосфат и пенцикловира трифосфат соответственно, которые образуются в клетках, поражённых вирусом герпеса. Ингибируя вирусную ДНК-полимеразу, они блокируют синтез вирусной ДНК. Пенцикловир имеет значительно более длительный внутриклеточный T1/2 (7-20 ч), чем ацикловир (менее 1 ч). Наиболее чувствительны вирусы простого герпеса I и II типа. Вирус varicella-zoster в 20 раз менее чувствителен. Как правило, у вируса простого герпеса отмечают перекрёстную резистентность ко всем аналогам нуклеозидов.
Фармакокинетика
Биодоступность ацикловира - 15-30%. Биодоступность валацикловира - 54%. В процессе всасывания в пищеварительном тракте и в печени он превращается в ацикловир. Пенцикловир применяют только наружно, так как при приёме внутрь он имеет очень низкую биодоступность (5%). Биодоступность фамцикловира - 70-80%, в пищеварительном тракте он превращается в пенцикловир.
Ацикловир и пенцикловир хорошо распределяются в организме. Проникают в слюну, внутриглазную жидкость, вагинальный секрет, жидкость герпетических пузырьков. Ацикловир проходит через ГЭБ. При местном применении незначительно всасываются через кожу и слизистые оболочки.
Как ацикловир, так и пенцикловир экскретируются преимущественно почками на 60-90% в неизменённом виде. Препараты имеют сходный - 2-3 ч, у детей младшего возраста - до 4 ч. При почечной недостаточности значительно возрастает.
Показания
Инфекции, вызванные вирусом простого герпеса I и II типа: кожи и слизистых оболочек, офтальмогерпес (только ацикловир), генитальный герпес, энцефалит, неонатальный герпес (табл. 20-24).
Инфекции, вызванные вирусом varicella-zoster опоясывающий лишай, ветряная оспа и др.
Профилактика цитомегаловирусной инфекции после трансплантации почек (ацикловир, валацикловир).
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Жжение при нанесении на слизистые оболочки. Боль или дискомфорт в животе, тошнота, рвота, диарея. Головная боль, головокружение. Заторможённость, тремор, судороги, галлюцинации, бред, экстрапирамидные расстройства; обструктивная нефропатия, проявляющаяся тошнотой, рвотой, болью в пояснице, азотемией (чаще при внутривенном введении ацикловира).
Лекарственные взаимодействия
Фармакокинетическое. При сочетании валацикловира с циметидином увеличивается концентрация ацикловира в крови.
Фармакодинамическое. При сочетании ацикловира с аминогликозидами или другими нефротоксичными ЛС возрастает риск осложнений со стороны почек и
ЦНС.
Таблица 20-24. Режимы дозирования противогерпетических препаратов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Ацикловир |
Внутрь 0,2 г 5 раз в сут или 0,4 г каждые 8 ч, при иммунодефиците - 0,4 г 5 раз в сут; при супрессивной терапии генитального герпеса - 0,2-0,4 г каждые 8-12 ч; при герпесе varicella-zoster - 0,8 г 5 раз в сут; для профилактики рецидивов вируса простого герпеса при иммунодефиците - 0,2 г каждые 6 ч, после трасплантации - 0,4 г 5 раз в сут; для профилактики и супрессивной терапии Herpes zoster при иммунодефиците после трансплантации - 0,4-0,8 г каждые 6 ч; |
Внутрь 0,2 г 5 раз в сут или 0,4 г каждые 8 ч; при ветряной оспе - 20 мг/кг (не более 0,8 г) каждые 6 ч; в/в 0,25 г/м2; при сниженном иммунитете, герпетическом энцефалите, ветряной оспе, опоясывающем герпесе - 0,5 г/м2; при неонатальном герпесе - 1,5-3 г/м2 в сут в 3 введения; местно крем или мазь (5%) наносят на поражённые участки кожи; глазную мазь (3%) закладывают в нижний конъюнктивальный мешок 5-6 раз в сут |
Валацикловир |
Внутрь при слизисто-кожном герпесе 0,5-1 г каждые 12 ч; при опоясывающем герпесе - 1 г каждые 8 ч; при первичном эпизоде генитального герпеса - 1 г каждые 12 ч; при рецидивах генитального герпеса - 0,5 г каждые 12 ч; при длительной супрессивной терапии рецидивирующего генитального герпеса - 0,5 г каждые 24 ч; для профилактики цитомегаловирусной инфекции после трансплантации - 2 г каждые 6 ч |
— |
Пенцикловир |
Крем наносят на поражённые участки каждые 2 ч (в дневное время) в течение 4 дней |
— |
Фамцикловир |
Внутрь при слизисто-кожном и генитальном герпесе 0,25 г каждые 8 ч (при первичном эпизоде) и 0,125 г каждые 12 ч (при рецидивах); при слизисто-кожном герпесе у пациентов с иммунодефицитом - 0,5 г каждые 12 ч; при супрессивной терапии генитального герпеса - 0,25-0,5 г каждые 12 ч; при опоясывающем лишае - 0,5 г каждые 8 ч |
— |
Применение в особых ситуациях
Беременность, лактация. Применять с осторожностью.
Педиатрия. Основной препарат для применения в педиатрии - ацикловир, так как он наиболее хорошо изучен у детей.
Гериатрия. Учитывая возрастное снижение функций почек, может потребоваться коррекция режима дозирования.
Нарушение функций почек. Необходима коррекция дозы. У пациентов, на гемодиализе, валацикловир применяют в дозе, рекомендуемой при клиренсе креатинина менее 15 мл/мин, причём препарат лучше принимать после сеанса гемодиализа.
Нарушение функции печени. При печёночной недостаточности дозу фамцикловира следует уменьшить.
Противоцитомегаловирусные препараты
Данная группа включает ганцикловир и валганцикловир. Ганцикловир по структуре и механизму действия близок к ацикловиру, но значительно более токсичен. Валганцикловир - пролекарство для приёма внутрь, в организме превращается в ганцикловир.
Фармакодинамика
В клетках, поражённых цитомегаловирусом, ганцикловир превращается в активную форму - ганцикловира трифосфат, который ингибирует вирусную ДНКполимеразу.
Фармакокинетика
Ганцикловир обычно вводят внутривенно, реже per os. Плазменный T1/2 составляет 3,5 ч, внутриклеточный - 12 ч. При приёме внутрь биодоступность низкая - 8-9%, T1/2 - 5 ч. Валганцикловир хорошо всасывается в пищеварительном тракте, в кишечнике и печени превращается в ганцикловир. Биодоступность ганцикловира в этом случае составляет 61%, несколько выше при приёме с пищей. Практически не метаболизируется, выводится почками в активной форме.
Показания
Цитомегаловирусный ретинит у пациентов с иммунодефицитом (включая СПИД). Профилактика цитомегаловирусной инфекции после трансплантации внутренних органов (табл. 20-25).
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Нейтропения, анемия, тромбоцитопения. Диарея, анорексия, рвота. Невропатия. Флебит, катетер-ассоциированные инфекции (профилактика: вводить медленно, не менее чем за 1 ч). Лихорадка, озноб, потливость, зуд, вторичная бактериальная инфекция.
Лекарственные взаимодействия
Фармакокинетическое. Циклоспорин и амфотерицин В повышают концентрацию ганцикловира в крови. Ганцикловир, в свою очередь, повышает концентрацию циклоспорина.
Фармакодинамическое. Не сочетаются с имипенемом ввиду повышения риска судорог.
Применение в особых ситуациях
Беременность. Применять только в том случае, если польза превышает потенциальный риск.
Лактация. Следует прекратить кормление грудью.
Педиатрия. Использовать ганцикловир у детей только в том случае, если польза превышает потенциальный риск. Валганцикловир противопоказан до 12 лет.
Гериатрия. Применять с осторожностью в связи с возможным снижением функций почек и наличием сопутствующих заболеваний.
Нарушение функций почек. Следует проводить коррекцию дозы.
Таблица 20-25. Режимы дозирования противоцитомегаловирусных препаратов
| Препарат | Режимы дозирования Взрослые и дети, дозы |
|---|---|
Ганцикловир |
В/в |
Валганцикловир |
Взрослые и дети старше 12 лет |
Противогриппозные препараты
Активностью против вирусов гриппа обладают блокаторы М2 -каналов - амантадин, римантадин, ингибиторы нейроаминидазы - осельтамивир, занамивир, а также арбидол*.
БЛОКАТОРЫ М2 -КАНАЛОВ
Фармакодинамика
Блокаторы М2 -каналов, блокируя ионные М2 -каналы вируса гриппа А, нарушают его способность проникать в клетки и высвобождать рибонуклеопротеид, ингибируя тем самым важнейшую стадию репликации вирусов. В процессе применения возможно развитие резистентности, частота которой к 5-му дню лечения может достигать 30%.
Фармакокинетика
Практически полностью всасываются в пищеварительном тракте. Пища не влияет на биодоступность (около 100%). Связывание с белками плазмы крови амантадина - 67, римантадина - 40%. Высокие концентрации создаются в тканях и секретах, которые первично контактируют с вирусом (слизь носовых ходов, слюна, слёзная жидкость). Проходят через ГЭБ, плаценту. Амантадин проникает в грудное молоко. Римантадин примерно на 75% метаболизируется в печени, выводится почками в основном в виде неактивных метаболитов. Амантадин почти не метаболизируется, выводится почками в активной форме. T1/2 амантадина - 11-15 ч, у пожилых - до 24-29 ч, при почечной недостаточности - до 7-10 сут. T1/2 римантадина - 1-1,5 сут, при тяжёлой почечной недостаточности - до 2-2,5 сут.
Показания
Лечение гриппа, вызванного вирусом А (начало не позднее 24 ч от появления первых симптомов). Профилактика гриппа при эпидемии, вызванной вирусом А.
Противопоказания
Гиперчувствительность, кормление грудью, возраст до 1 года, эпилепсия, тяжёлая почечная и печёночная недостаточность.
Нежелательные лекарственные реакции
Боль в животе, сухость во рту, нарушение аппетита, тошнота. Нейротоксичность (чаще амантадин): сонливость, бессонница, головная боль, головокружение, нарушения зрения, раздражительность, нарушение концентрации внимания, утомляемость, парестезии, тремор и др.
Лекарственные взаимодействия
Фармакокинетическое. Адсорбенты, вяжущие и обволакивающие средства уменьшают всасывание римантадина.
Циметидин ингибирует метаболизм римантадина и может повышать его концентрацию в крови.
Тиазиды, триамтерен, хинин, хинидин, ко-тримоксазол тормозят почечную экскрецию амантадина и могут повышать его токсичность.
Фармакодинамическое. Ослабляют действие противоэпилептических ЛС.
Нейротоксичность амантадина усиливается при сочетании с антихолинергическими и антигистаминными ЛС, антидепрессантами, производными фенотиазина, алкоголем.
Амантадин усиливает действие леводопы и психостимуляторов.
Применение в особых ситуациях
Беременность. Назначение допускается только при крайней необходимости.
Гериатрия. У лиц старше 65 лет увеличивается риск развития НЛР со стороны пищеварительного тракта и ЦНС, особенно при использовании амантадина. Необходимо учитывать возможное возрастное понижение функций почек, в связи с которым может потребоваться коррекция дозы.
Нарушение функции печени. Поскольку римантадин метаболизируется в печени, у пациентов с выраженными нарушениями её функции дозу следует уменьшить.
Заболевания ЦНС. У пациентов с эпилепсией и другими заболеваниями, характеризуемыми повышенной судорожной готовностью, возрастает риск развития тремора и судорог, особенно при применении амантадина. Предпочтителен римантадин.
ИНГИБИТОРЫ НЕЙРОАМИНИДАЗЫ
Фармакодинамика
При ингибировании нейроаминидазы нарушается способность вирусов А и В проникать в здоровые клетки, тормозится выход вирионов из инфицированной клетки и уменьшается их устойчивость к инактивирующему действию слизистого секрета дыхательных путей, вследствие чего приостанавливается дальнейшее распространение вируса в организме.
Фармакокинетика
Осельтамивир хорошо всасывается в пищеварительном тракте. В кишечнике и печени превращается в активный метаболит - осельтамивира карбоксилат. Биодоступность - 75%, не зависит от пищи. Метаболит создаёт высокие концентрации в основных очагах гриппозной инфекции - слизистой носа, среднем ухе, трахее, бронхах, лёгких. Экскретируется преимущественно с мочой. - 6-10 ч, при почечной - до 18 ч.
Показания
Лечение гриппа, вызванного вирусами А и В (начало не позднее 24 ч от появления первых симптомов). Профилактика гриппа во время эпидемий.
Противопоказания
Гиперчувствительность, тяжёлая почечная недостаточность.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота, диарея. Головная боль, головокружение, бессонница, общая слабость, нарушение сознания. Заложенность носа, боль в горле, кашель.
Применение в особых ситуациях
Беременность, лактация. Назначать только при крайней необходимости.
Педиатрия. Осельтамивир можно применять для лечения гриппа у детей старше 1 года, для профилактики - у детей старше 13 лет.
Гериатрия. Возможно возрастное снижение функций почек, может потребоваться коррекция дозы.
Нарушение функций почек. Возможна кумуляция с повышением риска токсичности. Необходима коррекция дозы с учётом степени снижения функции почек. При клиренсе креатинина менее 10 мл/мин осельтамивир противопоказан.
АРБИДОЛ*
Фармакодинамика
Механизм противовирусного действия связан с ингибированием слияния липидной оболочки вируса с клеточными мембранами. Активен против вирусов А и В. Обладает также интерферониндуцирующими и иммуномодулирующими свойствами, усиливает фагоцитоз.
Фармакокинетика
Изучена недостаточно. Хорошо всасывается в пищеварительном тракте. Частично метаболизируется в печени. Около 40% препарата выводится из организма в активной форме, преимущественно со стулом. T1/2 - 17 ч.
Показания
Лечение и профилактика гриппа, вызванного вирусами А и В (табл. 20-26).
Противопоказания
Аллергическая реакция на арбидол*, возраст до 2 лет.
Нежелательные лекарственные реакции
Аллергические реакции: сыпь, крапивница и др.
Применение в особых ситуациях
Беременность, лактация. Применять только при крайней необходимости.
Таблица 20-26. Режимы дозирования противогриппозных препаратов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Амантадин |
0,1 г каждые 12 ч, старше 65 лет - не более 0,1 г/сут |
Старше 1 года - 5 мг/(кгх сут) (не более 0,15 г/сут) в 2 приёма |
Римантадин |
0,1 г каждые 12 ч |
1-10 лет - 5 мг/(кгх сут) (не более 0,15 г/сут) в 2 приёма, старше 10 лет - 0,1 г каждые 12 ч |
Осельтамивир |
0,075 г каждые 12 ч |
Старше 12 лет - 0,075 г каждые 12 ч |
Арбидол* |
Для лечения - 0,2 г каждые 6 ч; для профилактики - 0,2 г/сут |
2-6 лет: для лечения - 0,05 г каждые 6 ч, для профилактики - 0,05 г/сут; 6-12 лет: для лечения 0,1 г каждые 6 ч, для профилактики - 0,1 г/сут; старше 12 лет - как у взрослых |
Противовирусные препараты расширенного спектра
РИБАВИРИН
Фармакодинамика
Предполагают, что рибавирин вызывает уменьшение внутриклеточного пула гуанозина трифосфата, понижает тем самым синтез нуклеиновых кислот вирусов. Клиническое значение имеет активность против респираторно-синцитиального вируса, вирусов, вызывающих лихорадку Ласса, геморрагическую лихорадку с почечным синдромом и гепатит С.
Фармакокинетика
Биодоступность при приёме внутрь - 45%. При ингаляционном введении высокие концентрации отмечают в секретах ДП и значительно более низкие - в плазме. Не связывается с белками плазмы. Накапливается в эритроцитах. Проникает через ГЭБ. Метаболизируется в печени, экскретируется преимущественно с мочой. T1/2 - от 27-36 ч до 6 сут.
Показания
Респираторно-синцитиальная вирусная инфекция: тяжёлый бронхиолит и пневмония у новорождённых и детей раннего возраста, относимых к группе риска по летальному исходу (врождённый порок сердца, иммунодефицит, бронхолёгочная дисплазия), на фоне тяжёлого муковисцидоза или лёгочной гипертензии. Гепатит С (в сочетании с интерфероном альфа). Лихорадка Ласса. Геморрагическая лихорадка с почечным синдромом.
Противопоказания
Гиперчувствительность, тяжёлая печёночная и/или почечная недостаточность, анемия, гемоглобинопатия, тяжёлая сердечная недостаточность, беременность, кормление грудью.
Нежелательные лекарственные реакции
Анемия и другие цитопении, гемолитическая анемия. Астенический синдром, головная боль, бессонница, ощущение усталости, раздражительность. Сыпь, раздражение кожи, конъюнктивит. Пневмоторакс, диспноэ, бронхоспазм, отёк лёгких, синдром гиповентиляции. Гипотензия, брадикардия, асистолия. Анорексия, тошнота, металлический привкус во рту, боль в животе, метеоризм. Гипербилирубинемия.
Лекарственные взаимодействия
Фармакокинетическое. Препараты, содержащие магний и алюминий, а также симетикон уменьшают биодоступность рибавирина при приёме внутрь.
Фармакодинамическое. Антагонизм с зидовудином (подавляет фосфорилирование зидовудина).
ЛАМИВУДИН
Аналог нуклеозида цитидина.
Фармакодинамика
В клетках, поражённых вирусом, превращается в ламивудин трифосфат, который ингибирует ДНК-полимеразу вируса гепатита В и обратную транскриптазу ВИЧ.
Фармакокинетика
Хорошо всасыватся в пищеварительном тракте. Биодоступрность - 80-90%, существенно не зависит от пищи. Связывание с белками плазмы - 36%. Распределяется во многие ткани и секреты, проходит через ГЭБ, плаценту. Частично метаболизируется, выводится преимущественно почками (около 70%) в неизменённом виде. T1/2 у взрослых - 2-11 ч, у детей - около 2 ч, при почечной недостаточности возрастает.
Показания
Хронический гепатит В, лечение и профилактика ВИЧ-инфекции.
Противопоказания
Гиперчувствительность, беременность, кормление грудью.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота, диарея. Повышение активности трансаминаз, гепатомегалия со стеатозом. Утомляемость, головная боль, головокружение, слабость, бессонница, периферическая нейропатия, парестезии (чаще у детей). Нейтропения, анемия. Кашель, инфекции дыхательных путей. Аллергические реакции.
Лекарственные взаимодействия
Фармакокинетическое. Повышает концентрацию в крови и пролонгирует эффект зидовудина.
Ко-тримоксазол повышает концентрацию ламивудина в плазме за счёт ингибирования почечной экскреции.
Фармакодинамическое. При сочетании с зидовудином замедляет появление зидовудино-устойчивых штаммов ВИЧ у пациентов, которые ранее не получали антиретровирусную терапию.
При сочетании с диданозином, пентамидином, сульфаниламидами, алкоголем повышается риск развития панкреатита.
При сочетании с изониазидом и ставудином повышается риск периферической невропатии.
Применение в особых ситуациях
Гериатрия. В связи с возможным возрастным снижением функций почек может потребоваться коррекция дозы.
Нарушение функций почек. При почечной недостаточности возможна кумуляция и повышенный риск токсических эффектов. Tребуется коррекция режима дозирования.
Панкреатит. При наличии в анамнезе панкреатита назначать с осторожностью. Tребуется тщательный клинико-лабораторный контроль.
Периферические невропатии. Использовать с осторожностью, под строгим клиническим контролем.
Интерфероны
Интерфероны - биологически активные белки, синтезируемые клеткой в процессе защитной реакции. Различают альфа-, бета- и гамма-интерферон. В качестве противовирусных ЛС чаще всего используют рекомбинантный альфа-интерферон. В последние годы разработаны пегилированные интерфероны (пег-интерфероны), получаемые путём присоединения полиэтиленгликоля. Пег-интерфероны обладают более длительным и улучшенной клинической эффективностью.
Фармакодинамика
Интерфероны блокируют синтез вирусных белков, подавляя репликацию вирусов. Они индуцируют клеточную резистентность к вирусным инфекциям, модулируют ответную реакцию иммунной системы, направленную на нейтрализацию вирусов или уничтожение инфицированных ими клеток. Основное клиническое значение имеет активность в отношении вирусов гепатита В, С и D.
Фармакокинетика
Интерфероны разрушаются в пищеварительном тракте, поэтому их применяют только парентерально. При внутримышечном и подкожном введении биодоступность составляет около 80%. Отмечены низкие концентрации интерферонов в секретах ДП, тканях глаза, ЦНС. Быстро инактивируются в почках, меньше - в печени. - 2-4 ч. Фармакокинетика пег-интерферонов изучена несколько меньше. Максимальная концентрация в крови достигается в течение 15-44 ч, причём она в 10 раз выше, чем у обычного альфа-интерферона. T1/2 - 40 ч.
Показания
Хронический гепатит В, острый гепатит С, хронический гепатит С (монотерапия или в сочетании с рибавирином), хронический гепатит D (табл. 20-27).
Противопоказания
Гиперчувствительность. Психоз (на момент лечения или в анамнезе). Tяжёлая депрессия. Нейтропения или тромбоцитопения. Декомпенсированные заболевания сердечно-сосудистой системы. Декомпенсированный цирроз печени. Неконтролируемые судороги. Tрансплантация органов (кроме печени). Беременность.
Нежелательные лекарственные реакции
Ранние. Гриппоподобный синдром (профилактика: приём парацетамола перед введением альфа-интерферона).
Поздние. Анемия, тромбоцитопения, агранулоцитоз. Сонливость, заторможённость, депрессия, парестезии, онемение кожи конечностей, зуд, тремор. Аритмия, транзиторная кардиомиопатия, артериальная гипотензия, инфаркт миокарда. Кашель, одышка, отёк лёгких, пневмония, остановка дыхания. Аутоиммунный тиреоидит. Сыпь. Потеря аппетита, тошнота, рвота, изменение вкуса, сухость во рту, похудение, диарея, боль в животе. Повышение активности трансаминаз, ЩФ, гипербилирубинемия.
Лекарственные взаимодействия
Фармакокинетическое. Альфа-интерферон ингибирует цитохром P450, поэтому может нарушать метаболизм многих ЛС, повышая их концентрацию в крови. Следует с особой осторожностью применять одновременно с альфа-интерфероном наркотические, снотворные и седативные препараты, а также ЛС, обладающие нейро-, гемато- и кардиотоксичностью.
Применение в особых ситуациях
Лактация. Вопрос о прекращении кормления грудью или отмене интерферонов должен решаться в зависимости от важности лечения для матери.
Педиатрия. Эффективность и безопасность у детей окончательно не установлены. Альфа-интерферон не рекомендуют назначать детям до 1 года. Пегинтерферон у детей не применяют.
Нарушение функций почек. При клиренсе креатинина менее 50 мл/мин необходимо уменьшение дозы альфа-интерферона в 2 раза.
Таблица 20-27. Режимы дозирования противовирусных препаратов расширенного спектра
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Рибавирин |
Внутрь при гепатите С 0,6 г каждые 12 ч; в/в при лихорадке Ласса и геморрагической лихорадке первая доза 2,0 г, затем 1,0 г каждые 6 ч в течение 4 дней и далее 0,5 г каждые 8 ч в течение 6 дней |
Ингаляционно (через небулайзер) при респираторно-синцитиальной вирусной инфекции 20 мг/мл в сут (6,0 г в 300 мл стерильной воды) в течение 18 ч |
Ламивудин |
Внутрь при хроническом гепатите В 0,1 г/сут; при ВИЧ-инфекции - 0,15 г каждые 12 ч |
Внутрь при хроническом гепатите В (у детей старше 2 лет) 3 мг/кг (не более 0,1 г) каждые 24 ч; при ВИЧ-инфекции до 1 мес: 2 мг/кг каждые 12 ч; от 1 мес до 12 лет: 4 мг/кг каждые 12 ч (не более 0,3 г/сут) |
Интерферон альфа-2 рекомбинантный человеческий |
Подкожно или в/м 3-10 млн МЕ 3 раза в нед. |
Старше 1 года: 3-6 млн МЕ/м2 поверхности тела 3 раза в нед |
Пегилированный интерферон |
Подкожно пег-интерферон альфа-2b - 1 мгк/кг (монотерапия) или 1,5 мгк/кг (в комбинации с рибавирином) раз в нед; пег-интерферон альфа-2а - 180 мкг раз в нед |
Антиретровирусные препараты |
Антиретровирусные препараты применяют для терапии и профилактики ВИЧ-инфекции. Существует четыре класса антиретровирусных препаратов:
Основной принцип лечения больных ВИЧ-инфекцией - пожизненное применение антиретровирусных препаратов. Все они - высокотоксичные ЛС. Для большинства антиретровирусных препаратов, особенно ингибиторов протеазы ВИЧ, характерны потенциально опасные лекарственные взаимодействия. Неправильное применение антиретровирусных препаратов приводит к быстрому развитию резистентности. В настоящее время применяют несколько вариантов высокоактивной антиретровирусной терапии:
-
2 нуклеозидных ингибитора обратной транскриптазы ВИЧ + 1 или 2 ингибитора протеазы ВИЧ;
-
2 нуклеозидных ингибитора обратной транскриптазы ВИЧ + 1 ненуклеозидный ингибитор обратной транскриптазы ВИЧ;
-
нуклеозидный ингибитор обратной транскриптазы ВИЧ + ненуклеозидный ингибитор обратной транскриптазы ВИЧ + ингибитор протеазы ВИЧ.
В качестве стартового режима рекомендуют 2 нуклеозидных ингибитора обратной транскриптазы ВИЧ + ингибиторы протеазы ВИЧ или 2 нуклеозидных ингибитора обратной транскриптазы ВИЧ + ненуклеозидный ингибитор обратной транскриптазы ВИЧ.
Нуклеозидные ингибиторы обратной транскриптазы вируса иммунодефицита человека
Группа нуклеозидных ингибиторов обратной транскриптазы ВИЧ включает зидовудин, фосфазид, ставудин, диданозин, абакавир, ламивудин, комбинированные препараты ламивудин + зидовудин и ламивудин + зидовудин + абакавир.
Фармакодинамика
В основе структуры нуклеозидных ингибиторов обратной транскриптазы ВИЧ лежит один из аналогов природного нуклеозида (тимидина, аденина, цитидина или гуанина), что обусловливает способность их метаболитов (трифосфатов) блокировать обратную транскриптазу ВИЧ и избирательно ингибировать репликацию вирусной ДНК. Ненуклеозидные ингибиторы обратной транскриптазы ВИЧ-активны в инфицированных ВИЧ T-лимфоцитах и макрофагах, ингибируют ранние стадии жизненного цикла вируса.
ЗИДОВУДИН
Аналог тимидина. Первый появившийся в клинике антиретровирусный препарат.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 65%, несколько уменьшается в присутствии пищи. Связывание с белками плазмы - 30-38%. Проникает через ГЭБ, плаценту, в семенную жидкость. Метаболизируется в печени при участии цитохрома P450, выводится почками. Плазменный T1/2 - 1,1 ч, клеточный - 3,3 ч.
Противопоказания
Гиперчувствительность, лейкопения (число нейтрофилов менее 0,75х109/л), анемия (концентрация гемоглобина менее 70 г/л), возраст до 3 мес.
Нежелательные лекарственные реакции
Tошнота, рвота, боль в животе, диарея, анорексия, метеоризм. Повышение активности трансаминаз, стеатоз. Анемия, нейтропения, лейкопения, тромбоцитопения. Головная боль, бессонница, астенический синдром, сонливость, депрессия, периферические невропатии. Боль в сердце. Кашель.
Лекарственные взаимодействия
Фармакокинетическое. Ингибиторы цитохрома P450 (циметидин и др.) повышают концентрацию зидовудина в плазме.
Фармакодинамическое. Не сочетать с фосфазидом и ставудином (конкуренция за фермент тимидинкиназу).
При сочетании с парацетамолом повышается риск нейтропении, а с рибавирином - риск анемии.
ЛС, обладающие нефротоксическим действием и подавляющие функцию костного мозга (амфотерицин В, ганцикловир, винкристин, винбластин), увеличивают риск токсических эффектов зидовудина.
Не рекомендуют сочетать зидовудин с рибавирином.
Применение в особых ситуациях
Лактация. Проникает в грудное молоко и достигает концентрации, близкой к сывороточному уровню. Матерям с ВИЧ-инфекцией кормление грудью не рекомендуют.
Нарушение функций почек. При клиренсе креатинина менее 20 мл/мин требуется коррекция дозы.
Нарушение функции печени. Возможна кумуляция препарата и повышение риска токсичности, необходимо уменьшение дозы.
ФОСФАЗИД
Один из метаболитов зидовудина. Зарегистрирован только в России.
Фармакокинетика
Биодоступность - 20%. Распределяется во многие органы и ткани. Проникает через ГЭБ, концентрация в СМЖ составляет 15-64% уровня в плазме крови. Проходит через плаценту. Метаболизируется в печени, экскретируется почками. T/2 - 2,5 ч.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, уровень гемоглобина ниже 50 г/л, лейтропения (менее 0,5х109/л), тромбоцитопения (менее 25х109/л).
Нежелательные лекарственные реакции
Tошнота, рвота, диарея, анорексия. Головная боль, бессонница, слабость. Анемия, гранулоцитопения. Миалгия. Сыпь, зуд.
СТАВУДИН
Как и зидовудин, аналог тимидина.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 86%, не зависит от пищи. Связывание с белками плазмы - 30-38%. Проходит через ГЭБ. Метаболизируется в печени, выводится почками. Плазменный - 1,2 ч, клеточный - 3,5 ч.
Противопоказания
Гиперчувствительность, периферическая невропатия, кормление грудью, возраст до 3 мес, печёночная недостаточность, тяжёлая почечная недостаточность (клиренс креатинина менее 15 мл/мин).
Нежелательные лекарственные реакции
Тошнота, рвота, анорексия, боль в животе. Анемия. Нарушение сна, астенический синдром, головная боль, периферические невропатии. Кашель. Сыпь, лихорадка. Артралгия, миалгия.
Лекарственные взаимодействия
Фармакодинамическое. При сочетании с хлорамфениколом, цисплатином, диданозином, этамбутолом, этионамидом, изониазидом, препаратами лития, метронидазолом, нитрофурантоином, фенитоином, винкристином повышается риск периферической полинейропатии.
Антагонизм с зидовудином.
При сочетании с диданозином усиление антиретровирусного эффекта.
Применение в особых ситуациях
Беременность. Данные о прохождении через плаценту и возможности уменьшения риска трансплацентарной передачи вируса отсутствуют. Применять только в крайнем случае.
Нарушение функций почек. Tребуется коррекция дозы. При клиренсе креатинина менее 15 мл/мин противопоказан.
Нарушение функции печени. Может провоцировать обострение хронических заболеваний печени.
ДИДАНОЗИН
Аналог аденина.
Фармакокинетика
Биодоступность - 42%, уменьшается в присутствии пищи. Связывание с белками плазмы менее 5%. Распределяется во многие ткани и органы. Проникает через ГЭБ, уровень в СМЖ достигает 20% концентрации в плазме. Данные о метаболизме не установлены. Выводится почками. Плазменный T1/2 - 1,5 ч, клеточный - 8-24 ч.
Противопоказания
Гиперчувствительность, кормление грудью.
Нежелательные лекарственные реакции
Тошнота, рвота, сухость во рту, боль в животе, анорексия, метеоризм, диарея. Анемия, гранулоцитопения, лейкопения, тромбоцитопения. Нарушение сна, астенический синдром, головная боль, тревога, бессонница, эпилептические припадки, периферическая невропатия. Сыпь, зуд, алопеция. Миалгия, рабдомиолиз. Нарушение функции печени, стеатоз, гепатит. Острая почечная недостаточность. Анафилактоидные реакции. Озноб, артралгия. Гипертрофия околоушной слюнной железы. Панкреатит.
Лекарственные взаимодействия
Фармакокинетическое. Нарушает всасывание кетоконазола, итраконазола, фторхинолонов, тетрациклинов (необходимы интервалы между приёмами не менее 2 ч).
Фармакодинамическое. При сочетании с алкоголем, азатиоприном, эстрогенами, фуросемидом, метилдопой, нитрофурантоином, сульфаниламидами, тетрациклином, тиазидами, вальпроевой кислотой повышается риск панкреатита.
При сочетании с хлорамфениколом, цисплатином, этамбутолом, этионамидом, изониазидом, препаратами лития, метронидазолом, нитрофурантоином, фенитоином, винкристином, ставудином повышается риск периферической полинейропатии.
Применение в особых ситуациях
Беременность. Проходит через плаценту. Данные об уменьшении риска трансплацентарной передачи вируса отсутствуют. Применять только при крайней необходимости.
Нарушение функций почек. Повышение токсичности препарата. При клиренсе креатинина менее 50 мл/мин необходима коррекция дозы.
АБАКАВИР
Аналог гуанина.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 85%, не зависит от пищи. Связывание с белками плазмы - 50%. Распределяется во многие ткани и органы. Проходит через ГЭБ, уровень в СМЖ достигает 27-33% концентрации в плазме. Более 80% абакавира метаболизируется в печени, экскретируется почками. Плазменный - 1,54 ч, клеточный - 3,3 ч.
Противопоказания
Гиперчувствительность, возраст до 3 мес, беременность, кормление грудью, патология печени.
Нежелательные лекарственные реакции
Сыпь, крапивница. Tошнота, рвота, диарея, боль в животе. Сонливость, быстрая утомляемость, головная боль, парестезия. Повышение активности трансаминаз, гепатомегалия, жировая дистрофия (чаще у женщин). Лактатацидоз. Лихорадка. Лимфаденопатия. Конъюнктивит. Гипотензия. Панкреатит. Миалгия. Артралгия.
Лекарственные взаимодействия
Фармакокинетическое. Алкоголь повышает концентрацию абакавира в плазме на 40%.
Фармакодинамическое. Усиление противовирусного эффекта при сочетании с диданозином, ламивудином и ставудином.
Применение в особых ситуациях
Нарушение функций почек. При тяжёлой почечной недостаточности требуется коррекция дозы.
Ненуклеозидные ингибиторы обратной транскриптазы вируса иммунодефицита человека
Представители группы ненуклеозидных ингибиторов обратной транскриптазы ВИЧ - невирапин и эфавиренз (табл. 20-28).
НЕВИРАПИН
Фармакодинамика
Вызывает деструкцию каталитического участка обратной транскриптазы ВИЧ-1. Блокирует активность РНК- и ДНК-зависимой полимеразы. Активен в остро инфицированных ВИЧ T-лимфоцитах, ингибирует ранние стадии жизненного цикла вируса.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 93%, не зависит от пищи. Связывание с белками плазмы - 60%. Обладает высокой липофильностью. Проникает через ГЭБ, уровень в СМЖ достигает 45% концентрации в плазме. Проходит через плаценту, накапливается в грудном молоке. Метаболизируется в печени при участии цитохрома P450, выводится преимущественно почками. T1/2 - 20-45 ч.
Противопоказания
Гиперчувствительность, кормление грудью.
Нежелательные лекарственные реакции
Аллергические реакции. Tошнота, стоматит. Головная боль, утомляемость, сонливость. Гранулоцитопения. Гепатит (факторы риска: хронический вирусный гепатит, алкоголизм).
Лекарственные взаимодействия
Фармакокинетическое. Снижает концентрации в плазме эстрогенсодержащих контрацептивов и кетоконазола.
Индукторы цитохрома P450 (рифампицин и др.) снижают, а ингибиторы (циметидин и др.) повышают концентрацию невирапина в плазме.
Применение в особых ситуациях
Беременность. Проникает через плаценту. Данные об уменьшении риска трансплацентарной передачи вируса отсутствуют. Применять с осторожностью.
Педиатрия. Гранулоцитопению у детей встречают чаще, чем у взрослых.
Нарушение функции печени. При повышении активности трансаминаз более чем в 5 раз по сравнению с верхней границей нормы препарат временно отменяют, назначают снова, когда активность ферментов уменьшится ниже данного порога.
ЭФАВИРЕНЗ
Фармакодинамика
Селективно ингибирует обратную транскриптазу ВИЧ-1. Препятствует транскрипции вирусной РНК на комплементарной цепочке ДНК и её встраиванию в геном человека. Активен в остро инфицированных ВИЧ T-лимфоцитах, ингибирует ранние стадии жизненного цикла вируса.
Фармакокинетика
Биодоступность - 40-45%, уменьшается при приёме пищи (особенно жирной). Практически полностью связывается с белками плазмы. Плохо проникает через ГЭБ. Метаболизируется в печени при участии цитохрома P450, выводится почками и органами пищеварения. T1/2 - 40-75 ч.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, печёночная и/или почечная недостаточность, активный вирусный гепатит, алкоголизм, наркомания, энцефалопатия, возраст до 3 лет, масса тела менее 13 кг.
Нежелательные лекарственные реакции
Аллергические реакции. Головокружение, головная боль, бессонница, сонливость, утомляемость, снижение концентрации внимания, невралгии, парестезия. Гематурия, образование конкрементов. Тошнота, диарея. Гепатит, гипербилирубинемия, повышение активности трансаминаз. Панкреатит, повышение активности амилазы.
Лекарственные взаимодействия
Фармакокинетическое. Индуцируя цитохром P450, эфавиренз усиливает метаболизм и снижает концентрации в крови фенобарбитала, фенитоина, карбамазепина, кларитромицина, индинавира, саквинавира, ампренавира.
Рифампицин понижает уровень эфавиренза в плазме на 25%, концентрация рифампицина при этом не изменяется.
Рифабутин не влияет на концентрацию в плазме эфавиренза, однако уровень рифабутина при этом уменьшается на 35%.
Ингибиторы протеазы ВИЧ
К ингибиторам протеазы ВИЧ относят ампренавир, атазанавир, дарунавир, индинавир, нелфинавир8, ритонавир, саквинавир и комбинированный препарат лопинавир + ритонавир (табл. 20-28).
Фармакодинамика
Протеаза ВИЧ - фермент, катализирующий расщепление вирусных полипротеинов, необходимых для созревания вируса, способного к инфицированию. Блокируя активный центр фермента, ингибиторы протеазы ВИЧ нарушают образование белков вирусного капсида, подавляют репликацию ВИЧ-1 и ВИЧ-2, в том числе при резистентности к нуклеозидным и ненуклеозидным ингибиторам обратной транскриптазы ВИЧ.
САКВИНАВИР
Первый представитель группы ингибиторов протеазы ВИЧ, применяемый с 1995 г.
Фармакокинетика
Всасывание в пищеварительном тракте - 30%, но биодоступность - всего 4% вследствие пресистемного метаболизма. Пища (особенно жирная) существенно повышает биодоступность. Связывание с белками плазмы - 98%. Хорошо распределяется, но не проникает через ГЭБ. Метаболизируется в печени при участии цитохрома P450, выводится в основном с калом. - 1-2 ч, удлиняется при систематическом приёме.
Противопоказания
Гиперчувствительность, почечная недостаточность, кормление грудью, возраст до 16 лет и старше 60 лет.
Нежелательные лекарственные реакции
Диарея, боль в животе, тошнота, изъязвление слизистой полости рта, фарингит. Гемолитическая анемия. Дислипидемия, гипергликемия (иногда сахарный диабет 2-го типа). Головная боль, спутанность сознания, атаксия, головокружение, астенический синдром, судороги, периферические невропатии. Аллергические рекции. Артралгия, миалгия, остеопороз.
Лекарственные взаимодействия
Фармакокинетическое. Саквинавир может повышать концентрации в плазме многих ЛС, тормозя их метаболизм в печени (нифедипин, верапамил, дилтиазем, клиндамицин, хинидин, препараты спорыньи, циклоспорин, фентанил и др.). Нельзя сочетать с терфенадином 8, астемизолом8 или цизапридом8 (высокий риск потенциально фатальной аритмии). Не рекомендуют сочетать с эфавирензом, так как его концентрация в плазме снижается при этом на 60%.
Индинавир повышает концентрацию саквинавира в плазме в 4-7 раз, ритонавира - в 20 раз. Невирапин понижает концентрацию саквинавира на 25%.
При сочетании с нелфинавиром8 концентрация саквинавира повышается в 3-5 раз, нелфинавира8 - на 20%, при сочетании с ампренавиром концентрация саквинавира уменьшается на 19%, ампренавира - на 32%.
Кетоконазол, флуконазол и итраконазол увеличивают концентрацию в плазме саквинавира.
Индукторы цитохрома P450 (рифампицин, фенитоин и др.) уменьшают концентрацию в плазме саквинавира, уменьшая его эффективность.
Применение в особых ситуациях
Беременность. Данные о прохождении через плаценту и уменьшении риска трансплацентарной передачи вируса отсутствуют. Применять с осторожностью.
АМПРЕНАВИР
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 89%, несколько снижается под влиянием пищи. Связывание с белками плазмы - 90%. Плохо проходит через ГЭБ. Метаболизируется в печени при участии цитохрома P450, выводится преимущественно с калом. T1/2 - 7-10,5 ч, при нарушении функции печени может увеличиваться.
Противопоказания
Гиперчувствительность, возраст до 4 лет, беременность, кормление грудью.
Нежелательные лекарственные реакции
Tошнота, рвота, метеоризм, диарея. Дислипидемия, гипергликемия (иногда сахарный диабет 2-го типа). Головная боль, утомляемость. Аллергические реакции. Парестезия слизистой полости рта. Остеопороз.
За счёт пропиленгликоля (в растворе - 55, в капсуле - 5%): эпилептические припадки, ступор, тахикардия, лактатацидоз, почечная недостаточность, гемолиз.
Лекарственные взаимодействия
Фармакокинетическое. Угнетает метаболизм терфенадина 8, цизаприда8, астемизола8, пимозида8 (повышение риска тяжёлых нарушений сердечного ритма), эритромицина, итраконазола, бензодиазепинов, блокаторов медленных кальциевых каналов, статинов, клозапина, карбамазепина, циметидина, лоратадина, варфарина и других ЛС, повышая их концентрации в плазме. Ненуклеозидные ингибиторы обратной транскриптазы ВИЧ, рифампицин и зверобой снижают концентрации ампренавира в плазме (такие сочетания не использовать).
Антациды и диданозин нарушают всасывание ампренавира в пищеварительном тракте.
Циметидин и ритонавир могут повышать концентрацию ампренавира в плазме.
Фармакодинамическое. Синергизм с нуклеозидными ингибиторами обратной транскриптазы ВИЧ (диданозин, зидовудин, абакавир) и ингибиторами протеазы ВИЧ (саквинавир, индинавир, ритонавир, нелфинавир8).
Не следует сочетать раствор ампренавира с дисульфирамом, метронидазолом и препаратами, содержащими этиловый спирт или пропиленгликоль.
Применение в особых ситуациях
Нарушение функций почек. Ампренавир в виде раствора для приёма внутрь противопоказан при почечной недостаточности.
Нарушение функции печени. Необходимо уменьшение дозы.
АТАЗАНАВИР
Фармакокинетика
Быстро всасывается в пищеварительном тракте. Пища улучшает биодоступность и фармакокинетическую стабильность. Связывание с белками плазмы - 86%. Проникает в СМЖ и семенную жидкость. Метаболизируется в печени при участии цитохрома P450, выводится преимущественно из пищеварительного тракта (около 80%) и почками. T1/2 - 6,5-7,9 ч.
Противопоказания
Гиперчувствительность, тяжёлая печёночная недостаточность, кормление грудью, возраст до 18 лет.
Нежелательные лекарственные реакции
Диспепсия, желтуха, анорексия или повышение аппетита, гастрит, панкреатит, афтозный стоматит. Общая слабость, головная боль, бессонница, амнезия, спутанность сознания, беспокойство, депрессия. Аллергические реакции. Алопеция. Гипербилирубинемия, повышение активности амилазы, липазы, креатинин фосфокиназы, АЛТ, АСТ. Нейтропения. Артралгия, миалгия, миопатия. Боль в груди. Лихорадка. Гинекомастия. Гипергликемия.
Лекарственные взаимодействия
Фармакокинетическое. Антациды и антисекреторные ЛС снижают всасывание атазанавира в пищеварительном тракте.
Кетоконазол, итраконазол и ритонавир повышают концентрацию атазанавира в крови.
Атазанавир увеличивает концентрацию в крови макролидов, пероральных контрацептивов, рифабутина, циклоспорина, такролимуса, ингибиторов фосфодиэстеразы-5, варфарина, амиодарона, лидокаина, хинидина, дилтиазема.
Применение в особых ситуациях
Беременность. Данные о прохождении через плаценту и уменьшении риска трансплацентарной передачи вируса отсутствуют. Применять с осторожностью.
Гериатрия. Эффективность и безопасность у лиц старше 65 лет не изучена. Применять с осторожностью.
ИНДИНАВИР
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 65%, значительно уменьшается в присутствии пищи. Связывание с белками плазмы - 60%. Умеренно проникает через ГЭБ. Метаболизируется в печени при участии цитохрома P450, выводится почками. T1/2 - 1,5-2 ч.
Противопоказания
Гиперчувствительность, беременность, кормление грудью, детский возраст.
Нежелательные лекарственные реакции
Изжога, метеоризм, боль в животе, диарея, нарушение вкуса, сухость во рту, афтозный стоматит. Дислипидемия, гипергликемия (иногда сахарный диабет 2-го типа). Астенический синдром, головокружение, головная боль, нарушения чувствительности, сонливость, депрессия, парестезия, тремор, периферическая полиневропатия. Кашель, дыхательные расстройства, инфекции дыхательных путей. Артралгия, миалгия, судороги или ригидность мышц конечностей, остеопороз. Холестатический гепатит, гипербилирубинемия, холецистит. Дизурия, никтурия, образование конкрементов, гематурия, протеинурия, повышение уровня креатинина. Сухость кожи, зуд, дерматит, паронихия и вросшие ногти на стопах, алопеция, потливость. Гемолитическая анемия, тромбоцитопения, спонтанные кровотечения. Сухость слизистой глаз. Лимфаденопатия. Лихорадка.
Лекарственные взаимодействия
Фармакокинетическое. Ингибируя цитохром P450, индинавир повышает концентрацию в плазме рифабутина. Нельзя сочетать с терфенадином 8, астемизолом8 или цизапридом8 (высокий риск потенциально фатальной аритмии). Кетоконазол увеличивает концентрацию индинавира в плазме крови.
Рифампицин значительно снижает концентрацию индинавира в плазме (сочетать не рекомендуют).
Фармакодинамическое. Усиливает эффект ингибиторов обратной транскриптазы.
НЕЛФИНАВИР8
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 78%, пища её повышает. Практически полностью связывается с белками плазмы. Плохо проходит через ГЭБ. Метаболизируется в печени при участии цитохрома P450, выводится преимущественно с калом. T1/2 - 3,5-5 ч.
Противопоказания
Гиперчувствительность, кормление грудью, возраст до 2 лет, печёночная недостаточность, гемофилия.
Нежелательные лекарственные реакции
Диарея, метеоризм, тошнота, боль в животе. Кожная сыпь. Остеопороз, гемартроз при гемофилии. Астенический синдром. Нейтропения, лимфоцитоз, гипокоагуляция (возможны кровотечения, спонтанная подкожная гематома). Дислипидемия, гипергликемия (иногда сахарный диабет 2-го типа), повышение активности трансаминаз и креатинкиназы.
Лекарственные взаимодействия
Фармакокинетическое. Значительно повышает концентрацию саквинавира и индинавира в плазме (не сочетать!).
Не рекомендуют сочетать с терфенадином 8, астемизолом8, цизапридом8, триазоламом8, мидазоламом, рифампицином, симвастатином, ловастатином. Ритонавир и индинавир повышают концентрацию нелфинавира8 в плазме и удлиняют его T1/2.
Индукторы цитохрома P450 (рифампицин, фенобарбитал и др.) могут уменьшать концентрацию нелфинавира8 в плазме.
Применение в особых ситуациях
Беременность. Адекватных исследований безопасности не проводилось. Применять с осторожностью.
Нарушение функции печени. Применять с осторожностью.
ЛОПИНАВИР + РИТОНАВИР
Более активный компонент данной комбинации - лопинавир. Добавление ритонавира ингибирует метаболизм лопинавира в печени и повышает его концентрацию в плазме.
Фармакокинетика
Биодоступность лопинавира в комбинации с ритонавиром точно не установлена. Известно, что она повышается при приёме во время еды. Для лопинавира характерен пресистемный метаболизм в печени при участии цитохрома P-450 (преимущественно изофермента CYP3A). Ритонавир, являясь мощным ингибитором CYP3A, препятствует инактивации лопинавира, что обеспечивает повышение его концентрации в плазме.
Противопоказания
Гиперчувствительность к лопинавиру или ритонавиру, кормление грудью, возраст до 2 лет.
Нежелательные лекарственные реакции
Диарея, тошнота, рвота, боль в животе. Головная боль, головокружение, астения, нарушения сна, возбуждение, амнезия, беспокойство, атаксия, нарушения ориентации, депрессия, энцефалопатия, периферические невриты, тремор. Нарушения зрения и слуха. Анемия, лейкопения, лимфаденопатия. Синдром Кушинга, гипотиреоз. Авитаминозы. Дегидратация. Нарушение толерантности к глюкозе, лактацидоз, ожирение, периферические отёки, снижение массы тела. Гипертензия, тахикардия, тромбофлебит, васкулит, удлинение интервала P-Q. Бронхит, одышка, отёк лёгких, синусит. Акне, алопеция, сухость кожи, эксфолиативный дерматит, фурункулёз, макулопапулёзная сыпь, изменения структуры ногтей, кожный зуд. Артралгия, артроз, миалгия. Нарушения мочеиспускания и эякуляции, гинекомастия, мужской гипогонадизм. Боль в спине, в груди. Гриппоподобный синдром.
Лекарственные взаимодействия
Фармакокинетическое. Лопинавир + ритонавир увеличивает в плазме концентрации ингибиторов протеазы ВИЧ (индинавир, нелфинавир8, саквинавир), статинов (ловастатин, симвастатин), антиаритмических ЛС (бепридил8, лидокаин, хинидин), силденафила, циклоспорина и многих других препаратов.
Зверобой и рифампицин снижают концентрацию лопинавира в плазме, что может привести к снижению терапевтического эффекта и развитию резистентности.
Лопинавир + ритонавир снижает концентрации зидовудина и абакавира в плазме.
Диданозин следует принимать за 1 ч до или через 2 ч после приёма лопинавира + ритонавира.
Применение в особых ситуациях
Беременность. Применять с осторожностью.
Нарушение функций почек. Фармакокинетика лопинавира + ритонавира при почечной недостаточности не изучена. Применять с осторожностью.
Нарушение функции печени. Лопинавир и ритонавир метаболизируются в печени, поэтому при печёночной недостаточности возможно повышение их концентрации в плазме (опыт применения у данной категории больных отсутствует).
ДАРУНАВИР
Ингибитор протеазы ВИЧ II поколения. Активен против штаммов ВИЧ, резистентных к другим ингибиторам протеазы ВИЧ. Применяют только в комбинации с ритонавиром, что способствует повышению концентрации дарунавира в плазме.
Фармакокинетика
Клиническое значение имеет фармакокинетика дарунавира, назначаемого вместе с ритонавиром. Биодоступность - 37%, увеличивается при приёме во время еды. Связывание с белками плазмы - 95%. Метаболизируется при участии цитохрома P450 (преимущественно CYP3A). Ритонавир ингибирует CYP3A и повышает концентрацию дарунавира в 14 раз. Около 80% дарунавира выводится почками и 14% - из пищеварительного тракта. T1/2 - 15 ч.
Противопоказания
Гиперчувствительность, возраст до 18 лет, кормление грудью.
Нежелательные лекарственные реакции
Диарея, тошнота, метеоризм, боль в животе, сухость во рту, диспепсия, запор. Инфаркт миокарда, тахикардия, гипертензия. Периферическая невропатия, парестезии, нарушения памяти, сонливость, преходящие нарушения мозгового кровообращения, состояние оглушённости, дезориентация, раздражительность, головная боль, беспокойство, астения. Артралгии, боли в конечностях, остеопения, остеопороз. Одышка, кашель, икота. Фолликулит, периферические отёки, липоатрофия, ночная потливость, аллергический дерматит, экзема, токсические поражения кожи, алопеция, гипергидроз, многоформная эритема, синдром Стивенса- Джонсона. Острая почечная недостаточность, мочекаменная болезнь, полиурия. Дислипидемия, гипонатриемия, полидипсия, гинекомастия. Повышение активности трансаминаз. Лихорадка, озноб.
Лекарственные взаимодействия
Фармакокинетическое. Дарунавир и ритонавир повышают концентрацию в плазме ненуклеозидных ингибиторов обратной транскриптазы ВИЧ (эфавиренз, невирапин), ингибиторов протеазы ВИЧ (индинавир, лопинавир), антиаритмических ЛС (бепридил8, амиодарон, лидокаин, хинидин), антидепрессантов (тразодон), антибиотиков (кларитромицин, рифабутин), противогрибковых ЛС (кетоконазол, итраконазол), антагонистов кальция (фелодипин, нифидепин, никардипин8), глюкокортикоидов (флутиказон, дексаметазон), статинов (аторвастатин, правастатин), ингибиторов фосфодиэстеразы-5, иммунодепрессантов (циклоспорин, такролимус).
Дарунавир и ритонавир снижают концентрацию вориконазола, сертралина, эстрадиола, варфарина.
Концентрация дарунавира снижается при сочетании с саквинавиром, рифабутином, дексаметазоном, повышается при сочетании с кетоконазолом и итраконазолом.
Применение в особых ситуациях
Беременность. Данные о прохождении через плаценту и уменьшении риска трансплацентарной передачи вируса отсутствуют. Применять с осторожностью.
Гериатрия. Эффективность и безопасность у лиц старше 65 лет не изучена. Применять с осторожностью.
Ингибиторы слияния
К ингибиторам слияния - новой группе антиретровирусных препаратов - относят энфувиртид. Его применяют для комбинированной терапии ВИЧ-инфекции, вызванной резистентными штаммами.
Фармакодинамика
Специфически связываясь с гликопротеидом gp41 ВИЧ-1 вне клетки и нарушая его структуру, блокируют проникновение вируса внутрь CD4+ клеток. Благодаря действию на различные ферменты-мишени перекрёстная резистентность с нуклеозидными ингибиторами обратной транскриптазы ВИЧ, ненуклеозидными ингибиторами обратной транскриптазы ВИЧ и ингибиторами протеазы ВИЧ отсутствует.
ЭНФУВИРТИД
Фармакокинетика
Являясь пептидом, разрушается в пищеварительном тракте. При подкожном введении биодоступность составляет 60-100% (зависит от дозы). Связывание с белками плазмы - 92%. Подвергается катаболизму до аминокислот, входящих в его состав, с последующей их утилизацией в организме. - 3-4 ч.
Противопоказания
Гиперчувствительность, кормление грудью, возраст до 6 лет.
Нежелательные лекарственные реакции
Боль в месте инъекции, уплотнение, эритема, узел, киста, зуд. Головная боль, периферическая невропатия, головокружение, нарушение вкуса, бессонница, депрессия, тревога, раздражительность, гипестезия, нарушение концентрации внимания, тремор. Кашель, боль в горле. Зуд и сухость кожи, повышенная потливость, себорейная экзема, эритема, акне. Миалгия, артралгия, боль в спине, боли в конечностях, мышечные спазмы. Конкременты в почках, гематурия. Tошнота, боль в животе, запор, диарея, панкреатит. Аллергические реакции. Лихорадка, озноб, дрожь, гипотензия. Респираторный дистресс-синдром. Гломерулонефрит. Гриппоподобный синдром. Лимфоаденопатия. Оральный кандидоз, простой герпес, папиллома кожи, грипп, синусит, фолликулит, отит, пневмония.
Лекарственные взаимодействия
Фармацевтическое. Не следует смешивать с другими ЛС, за исключением прилагаемого растворителя.
Фармакодинамическое. При сочетании нуклеозидных и ненуклеозидных ингибиторов обратной транскриптазы ВИЧ и ингибиторов протеазы ВИЧ отмечают усиление противовирусного эффекта (аддитивное либо синергидное действие).
Применение в особых ситуациях
Беременность. Адекватных исследований безопасности препарата не проводилось. Применения во время беременности следует избегать, если только потенциальные преимущества для матери не превышают возможный риск для плода.
Педиатрия. Эффективность и безопасность энфувиртида у детей до 6 лет не изучалась.
Нарушение функций почек, печени. Фармакокинетика энфувиртида при почечной и печёночной недостаточности не изучена.
Таблица 20-28. Режимы дозирования антиретровирусных препаратов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Зидовудин |
Терапия ВИЧ-инфекции: внутрь 0,6 г/сут в 2-3 приёма; профилактика перинатальной ВИЧ-инфекции: беременные, инфицированные ВИЧ - 0,1 г 5 раз в сут внутрь до начала родов, во время родов - 2 мг/кг в/в в течение часа, затем в/в 1 мг/кг в час до отсечения пуповины |
Терапия ВИЧ-инфекции: от 6 нед до 12 лет: внутрь 160 мг/м2 каждые 8 ч (480 мг/м2 в сут); Профилактика перинатальной ВИЧ-инфекции: новорождённые - 2 мг/кг каждые 6 ч в течение первых 6 нед жизни |
Фосфазид |
Терапия ВИЧ-инфекции: внутрь 0,6-1,2 г/сут в 2 приёма; профилактика профессионального заражения ВИЧ - 0,6 г каждые 12 ч в течение 4 нед (начинать не позднее чем через 3 сут после возможного инфицирования) |
Терапия ВИЧ-инфекции: |
Ставудин |
Внутрь при массе тела более 60 кг - 40 мг каждые 12 ч; менее 60 кг - 30 мг каждые 12 ч |
Внутрь при массе тела более 30 кг - 15 мг каждые 12 ч; менее 30 кг - 1 мг/кг каждые 12 ч |
Диданозин |
Внутрь при массе тела менее 50 кг - 0,125 г (таблетки) и 0,167 г (порошок); 50-74 кг - 0,2 г и 0,25 г (соответственно); более 75 кг - 0,3 г и 0,375 г, каждые 12 ч. Капсулы - 1 раз/сут: при массе более 60 кг - 0,4 г; менее 60 кг - 0,25 г |
Внутрь 120 мг/м2 каждые 12 ч |
Абакавир |
Внутрь 0,3 г каждые 12 ч |
Старше 3 мес - внутрь 8 мг/кг каждые 12 ч (не более 0,6 г/сут). |
Невирапин |
Терапия ВИЧ-инфекции: |
Терапия ВИЧ-инфекции: от 2 мес до 8 лет - внутрь 4 мг/(кгхсут) в 1 приём в течение 2 нед, далее 7 мг/кг каждые 12 ч; |
Эфавиренз |
Внутрь 0,6 г 1 раз в сут |
Старше 3 лет: при массе тела 13-15 кг - внутрь 0,2 г/сут; 15-20 кг - 0,25 г/сут; 20-25 кг - 0,3 г/сут; 25-32 кг - 0,35 г/сут; 32-40 кг - 0,4 г/сут |
Ампренавир |
Внутрь 1,2 г (капсулы) или 1,4 г (раствор) каждые 12 ч |
Старше 4 лет: капсулы - внутрь 20 мг/кг каждые 12 ч или 15 мг/кг каждые 8 ч; раствор - 22,5 мг/кг каждые 12 ч или 17 мг/кг каждые 8 ч |
Атазанавир |
Внутрь 0,4 г 1 раз в сут |
— |
Дарунавир |
Внутрь 0,6 г каждые 12 ч |
— |
Индинавир |
Внутрь 0,8 г каждые 8 ч |
— |
Лопинавир/ ритонавир |
Внутрь 400/100 мг (3 капсулы или 5 мл раствора) каждые 12 ч |
Старше 2 лет в зависимости от площади поверхности тела: более 1,3 м2 - внутрь 3 капсулы 2 раза в сут, менее 1,3 м2 - 230/57,5 мг/м2 раствора 2 раза в сут |
Нелфинавир8 |
Внутрь 0,75 г каждые 8 ч или 1,25 г 2 раза в сут |
Внутрь 20-30 мг/кг каждые 8 ч |
Саквинавир |
Внутрь твёрдые капсулы - 1,0 г + 0,1 г ритонавира каждые 12 ч, мягкие капсулы - 1,2 г каждые 8 ч или 1,0 г + 0,1 г ритонавира каждые 12 ч |
— |
Энфувиртид |
Подкожно 90 мг каждые 12 ч |
Старше 6 лет - подкожно 2 мг/кг каждые 12 ч (не более 90 мг каждые 12 ч) |
АНТИПРОТОЗОЙНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА
Класс антипротозойных средств включает различные по химической структуре соединения, применяемые при инфекциях, вызванных одноклеточными простейшими: малярийными плазмодиями, лямблиями, амёбами, токсоплазмами и др. (табл. 20-29). Согласно международной систематизации антипротозойных ЛС противомалярийные препараты как наиболее многочисленные выделены в отдельную группу.
Противомалярийные препараты
В основу классификации противомалярийных ЛС положены их различия по химической структуре.
Таблица 20-29. Классификация противомалярийных препаратов
| Группы | Препараты |
|---|---|
Хинолины |
Хлорохин |
Бигуаниды |
Прогуанил |
Диаминопиримидины |
Пириметамин |
Фенантренметанолы |
Галофантрин* |
Терпенлактоны |
Артемизинин* и его производные |
Сульфаниламиды |
Сульфадоксин |
Тетрациклины |
Тетрациклин |
Линкозамиды |
Клиндамицин |
Свойства сульфаниламидов, тетрациклинов и линкозамидов описаны в разделе «Антибактериальные лекарственные средства», поэтому в этой главе не рассматриваются.
При малярии, вызванной Plasmodium malariae, радикальное излечение достигается применением хлорохина. При малярии, вызванной P. vivax или P. ovale, в целях профилактики отдалённых рецидивов необходимо добавлять тканевой шизонтоцид примахин. В связи с быстрым развитием лекарственной резистентности (хлорохинорезистентности, в некоторых эндемичных очагах - полирезистентности) у возбудителя тропической малярии, вызываемой P. falciparum, используют мефлохин, производные артемизининаP и потенциально токсичные препараты хинина или комбинации хинина либо пириметамина с сульфаниламидами и тетрациклинами, либо галофантринP . Для профилактики P. vivax- и P. ovale-малярии применяют хлорохин, P. falciparum-малярии - мефлохин и доксициклин.
Хинолины
ХЛОРОХИН
В течение многих лет применялся наиболее широко. Сейчас используют ограниченно в связи с развитием резистентности P. falciparum во многих эндемичных очагах тропической малярии.
Фармакодинамика
Протозоацидный эффект связан с блокированием синтеза нуклеиновых кислот. Активен против эритроцитарных форм (шизонтов) P. vivax, P. ovale, P. malariae - гематошизонтоцидное действие. У P. falciparum чувствительность сохраняется только в отдельных регионах. Чувствительны также патогенные амёбы.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 85-90%, не зависит от пищи. Связывание с белками плазмы - 50-65%. Высокие концентрации создаются в печени, почках, селезёнке, лёгких. Накапливается в эритроцитах, особенно поражённых плазмодием (уровни в 100-300 раз выше, чем в нормальных). Проникает через плаценту, в грудное молоко. Частично метаболизируется в печени. Медленно экскретируется с мочой, на 50% в активной форме. При понижении рН мочи экскреция усиливается. при кратковременном приёме - 4-9 сут.
Показания
Малярия, вызванная P. vivax, P. ovale, P. malariae, а также чувствительными к хлорохину P. falciparum (лечение и профилактика). Внекишечный амёбиаз.
Противопоказания
Гиперчувствительность, эпилепсия, псориаз, ретинопатия, нарушения зрения.
Нежелательные лекарственные реакции
Боль в животе, анорексия, тошнота, рвота, диарея. Головная боль, головокружение, усталость, заторможённость, нарушения сна, зрения, слуха. Кожная сыпь, зуд, обострение псориаза и экземы. Депигментация волос. Цитопении, гемолитическая анемия при дефиците глюкозо-6-фосфат-дегидрогеназы в эритроцитах. Кератопатии и ретинопатии, возможна деструкция сетчатки (профилактика: избегать прямой инсоляции, осмотры офтальмологом).
При острой передозировке сильная головная боль, головокружение, боль в животе, резкая слабость, гипотензия, аритмия, внезапная потеря зрения, дыхательные расстройства, судороги, возможна остановка дыхания.
Лекарственные взаимодействия
Фармакокинетическое. Уменьшает всасывание ампициллина в пищеварительном тракте (необходимы интервалы не менее 2 ч).
Может повышать концентрацию в крови дигоксина и циклоспорина (необходим мониторинг).
Антациды и адсорбенты уменьшают всасывание хлорохина в пищеварительном тракте (необходимы интервалы не менее 4 ч).
Циметидин нарушает метаболизм хлорохина в печени, повышая его концентрацию в крови и риск токсичности.
Фармакодинамическое. При сочетании с мефлохином повышается риск судорог.
Применение в особых ситуациях
Беременность. Применять с осторожностью.
Лактация. При назначении кормящим женщинам следует сопоставлять возможные пользу и риск для ребёнка.
Педиатрия. Повышенный риск токсичности у детей. Применять крайне осторожно, особенно парентерально.
Гериатрия. Применять с осторожностью.
Нарушение функций почек, печени. Возможно нарушение элиминации хлорохина и повышение его концентрации в крови, повышен риск токсичности.
Заболевания ЦНС. При заболеваниях с понижением судорожного порога использовать крайне осторожно. При эпилепсии применять не рекомендуется.
ХИНИН
Алкалоид коры хинного дерева, первый эффективный противомалярийный препарат.
Фармакодинамика
Гематошизонтоцидный эффект в отношении всех видов плазмодия, включая P. falciparum, резистентные к хлорохину. Предполагается, что он может быть связан с нарушением функции лизосом и блокированием синтеза нуклеиновых кислот. Действие развивается быстро, особенно при парентеральном введении. Оказывает также слабое аналгезирующее и жаропонижающее действие.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 80%, не зависит от пищи. Связывание с белками плазмы - 85-90%. Распределяется во многие ткани и среды. Во время приступа малярии концентрация в плазме крови значительно выше, чем в эритроцитах. Плохо проходит через ГЭБ. Проникает через плаценту и в грудное молоко. Метаболизируется в печени, экскретируется почками (быстрее при кислой реакции мочи). - у взрослых 16-18 ч, у детей - 12 ч.
Показания
Хинин - препарат первого ряда при лечении полирезистентной тропической малярии. Иногда используется в сочетании с пириметамином/сульфадоксином.
Противопоказания
Гиперчувствительность, заболевания среднего и внутреннего уха, дефицит глюкозо-6-фосфат-дегидрогеназы.
Нежелательные лекарственные реакции
Цинхонизм (от лат. cinchona - «хинное дерево») - токсическое состояние, проявляющееся головной болью, головокружением, тошнотой, расстройством зрения, шумом в ушах и др. Эритема, крапивница. Усиление сократимости миометрия, маточные кровотечения. Tромбоцитопения, агранулоцитоз, гемолитическая анемия (при дефиците глюкозо-6-фосфат-дегидрогеназы). Гипогликемия. Боль в сердце, аритмия, блокада, понижение сократимости миокарда, гипотензия. Гипопротромбинемия, гепатит. Курареподобное действие. При внутримышечном введении резкая болезненность, возможен абсцесс, некроз ткани. Лекарственная лихорадка.
Острая передозировка (см. «Хлорохин»).
Лекарственные взаимодействия
Фармакокинетическое. Может повышать концентрацию в крови дигоксина за счёт замедления его элиминации. Антациды, содержащие алюминий, уменьшают всасывание хинина. Циметидин нарушает метаболизм хинина в печени, повышая его концентрацию в крови и риск токсичности.
Фармакодинамическое. Усиливает действие непрямых антикоагулянтов, нарушая синтез протромбина и других факторов свёртывания в печени (строгий лабораторный контроль, возможная коррекция дозы антикоагулянтов).
При сочетании с хинидином повышается риск удлинения интервала Q-T и развития аритмий.
При сочетании с мефлохином повышается риск кардиотоксичности (удлинение интервала Q-T, аритмии) и развития судорог (мефлохин назначают не ранее чем через 12 ч после последней дозы хинина).
Применение в особых ситуациях
Беременность. При лечении тропической малярии повышен риск развития гипогликемии. За счёт утерокинетического эффекта может провоцировать аборты и преждевременные роды. Однако опасность для жизни беременной и плода при тяжёлой тропической малярии может превалировать над риском токсичности хинина. Применять с крайней осторожностью.
Лактация. При использовании кормящими женщинами следует сопоставлять возможные пользу и риск.
Педиатрия. При лечении тропической малярии у детей повышен риск гипогликемии.
Гериатрия. Учитывая возрастное понижение функции печени и почек, а также наличие сопутствующих заболеваний у лиц пожилого возраста, применять с осторожностью.
Нарушение функций почек, печени. Возможно нарушение элиминации хинина, повышение его концентрации и риска токсичности.
Заболевания сердца. При нарушениях ритма в анамнезе или врождённом удлинении интервала Q-T повышен риск тяжёлой аритмии и блокады.
МЕФЛОХИН
Фармакодинамика
Гематошизонтоцидный эффект в отношении всех видов малярийного плазмодия, включая P. falciparum, резистентных к хлорохину, и некоторых полирезистентных штаммов. Механизм действия точно не установлен.
Фармакокинетика
Практически полностью всасывается в пищеварительном тракте. Биодоступность - около 100%, не зависит от пищи. Связывание с белками плазмы - 98%. Распределятся во многие ткани и среды, накапливается в эритроцитах. Проходит через ГЭБ. Метаболизируется в печени, экскретируется преимущественно с калом. Часть препарата подвергается энтерогепатической циркуляции. Обладает кумулятивными свойствами. T1/2 - 2-4 нед.
Показания
Лечение тропической малярии, вызванной хлорохино-устойчивыми штаммами P. falciparum. Химиопрофилактика малярии.
Противопоказания
Гиперчувствительность, тяжёлые неврологические и психические заболевания, тяжёлые нарушения функции печени, возраст до 2 лет, масса тела менее 15 кг. I триместр беременности.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота, диарея. Общая слабость, головная боль, головокружение, беспокойство, бессонница, депрессия, судороги, психозы, шум в ушах. Зрительные расстройства (нарушение объёмного зрения). Брадикардия, аритмия, блокада. Tромбоцитопения, лейкопения. Повышение активности трансаминаз. Кожная сыпь, зуд, алопеция. Артралгия, миалгия.
Лекарственные взаимодействия
Фармакокинетическое. Уменьшает концентрацию в крови вальпроевой кислоты (может потребоваться её мониторинг и коррекция дозы).
Фармакодинамическое. Нельзя сочетать с хинином или хинидином, а также применять менее чем через 12 ч после их отмены во избежание суммации токсических эффектов.
При сочетании с галофантрином* возрастает риск кардиотоксичности, с хлорохином - риск судорог.
Крайне опасно сочетать с ЛС, замедляющими проводимость в сердце (β-адреноблокаторы и др.).
Применение в особых ситуациях
Лактация. При назначении кормящим женщинам следует сопоставлять возможные пользу и риск.
Гериатрия. Учитывая возрастное понижение функции печени и наличие сопутствующих заболеваний у лиц пожилого возраста, применять с осторожностью.
Нарушение функции печени. При длительном применении необходим адекватный клинико-лабораторный контроль. При тяжёлых нарушениях функции мефлохин противопоказан.
Заболевания ЦНС. Повышен риск нейротоксичности. Применять с осторожностью. При тяжёлых неврологических и психических заболеваниях мефлохин противопоказан.
ПРИМАХИН
Фармакодинамика
Активен в отношении тканевых форм P. vivax и P. ovale (гистошизонтоцидный эффект), находящихся в печени, и половых форм P. falciparum. Механизм действия точно не установлен.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 96%, не зависит от пищи. Распределяется во многие ткани и среды. Метаболизируется в печени. Около 60% препарата превращается в активный метаболит - карбоксипримахин, концентрация которого в организме может значительно превышать уровень исходного вещества. Он усиливает и пролонгирует эффект примахина. Элиминируется почками. T1/2 примахина - 4-8 ч, активного метаболита - до 22-30 ч.
Показания
Радикальное излечение малярии, вызванной P. vivax и P. ovale (после завершения курса лечения хлорохином). Профилактика рецидивов P. vivax- и P. ovale-малярии у лиц, вернувшихся из эндемичных зон.
Противопоказания
Гиперчувствительность, тяжёлая патология кроветворения, тяжёлые нарушения функций почек, возраст до 3 лет, беременность.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота. Гемолитическая анемия (при дефиците глюкозо6-фосфат-дегидрогеназы), метгемоглобинемия, лейкопения.
Лекарственные взаимодействия
Фармакодинамическое. При сочетании с ЛС, обладающими гематотоксичностью (сульфаниламиды, хлорамфеникол и др.), значительно возрастает риск нарушений кроветворения.
Применение в особых ситуациях
Лактация. При назначении кормящим женщинам следует сопоставлять возможные пользу и риск.
Гериатрия. Учитывая возрастное снижение функций почек и возможное наличие сопутствующих заболеваний у лиц пожилого возраста, применять с осторожностью.
Нарушения функций почек. Возможно нарушение экскреции примахина и его активного метаболита, что повышает риск токсичности. Необходим адекватный клинико-лабораторный контроль. При тяжёлой почечной недостаточности примахин противопоказан.
Препараты других групп
ПРОГУАНИЛ
Фармакодинамика
Активный метаболит прогуанила циклогуанил ингибирует фермент дигидрофолат редуктазу, блокируя тем самым обмен фолиевой кислоты и синтез нуклеиновых кислот. Активен преимущественно в отношении тканевых форм всех видов плазмодия. Проявляет также споронтоцидное действие, нарушая цикл развития плазмодиев в теле комара.
Фармакокинетика
Хорошо всасывается в пищеварительном тракте. Биодоступность - 90%, не зависит от пищи. Связывание с белками плазмы - 75%. Метаболизируется в печени с частичным образованием активного метаболита - циклогуанила. У ряда лиц в силу генетических особенностей циклогуанил не образуется в достаточном количестве, что является причиной резистентности к прогуанилу. Экскретируется преимущественно почками - 60% в неизменённом виде, 30% - в виде циклогуанила. T1/2 - около 20 ч.
Показания
Химиопрофилактика малярии.
Противопоказания
Гиперчувствительность.
Нежелательные лекарственные реакции
Афтозный стоматит, диспепсия. Раздражение паренхимы почек, гематурия.
Применение в особых ситуациях
Беременность, лактация. Применять с осторожностью, сопоставляя возможные пользу и риск.
Гериатрия. Учитывая возрастное снижение функций почек и наличие сопутствующих заболеваний у лиц пожилого возраста, применять с осторожностью.
Нарушение функций почек. Возможно нарушение экскреции прогуанила и его активного метаболита, повышение риска токсичности. Применять с осторожностью.
Нарушение функции печени. Возможно нарушение образования циклогуанила и ослабление противомалярийного эффекта.
ПИРИМЕТАМИН
Близок по структуре и действию к триметоприму (см. «Ко-тримоксазол» в главе 20). При монотерапии быстро развивается резистентность, поэтому его используют в сочетании с другими ЛС, чаще всего с сульфаниламидами.
Фармакодинамика
Ингибируя фермент дигидрофолат редуктазу (значительно сильнее у простейших, чем у бактерий), нарушает обмен фолиевой кислоты. Активен против тканевых форм P. falciparum, в меньшей степени - P. vivax. Медленный гематошизонтоцидный эффект в отношении всех видов плазмодия, включая P. falciparum, резистентные к хлорохину. Чувствительны также токсоплазмы.
Фармакокинетика
Биодоступность - 95-100%, не зависит от пищи. Связывание с белками плазмы - 87%. Хорошо распределяется, накапливается в эритроцитах, почках, лёгких, печени, селезёнке. Проходит через ГЭБ, создавая концентрацию в СМЖ, равную 13-26% от плазменного уровня. Проникает через плаценту и в грудное молоко. Метаболизируется в печени. Медленно экскретируется почками, на 20-30% в активной форме. T1/2 - 4-6 сут.
Показания
Лечение хлорохинорезистентной тропической малярии в сочетании с сульфадоксином и хинином (комбинированный препарат пириметамин + сульфадоксин). Боксоплазмоз - в сочетании с сульфадимидином или сульфадиазином.
Противопоказания
Гиперчувствительность, I триместр беременности, кормление грудью, мегалобластная фолиево-дефицитная анемия.
Нежелательные лекарственные реакции
Мегалобластная фолиеводефицитная анемия, тромбоцитопения, лейкопения, агранулоцитоз. Кожная сыпь, многоформная эритема, синдром Стивенса-Джонсона. Атрофический глоссит, боль в животе, тошнота, рвота, диарея.
Острая передозировка: резкая боль в животе, повторная рвота, возбуждение, судороги, дыхательные расстройства, коллапс.
Применение в особых ситуациях
Беременность. Не рекомендуют в I триместре беременности. В других - с осторожностью.
Гериатрия. Учитывая возрастное снижение функций почек и возможные сопутствующие заболевания у лиц пожилого возраста, применять с осторожностью.
Нарушение функций почек, печени. Возможно нарушение элиминации пириметамина, повышение риска токсичности. Необходим адекватный клиниколабораторный контроль. Применять с осторожностью.
ГАЛОФАНТРИН
Фармакодинамика
Механизм противомалярийного эффекта точно не установлен. Чувствительны эритроцитарные формы P. falciparum (включая ряд штаммов, устойчивых к хлорохину и пириметамину + сульфадоксину) и P. vivax. Возможна перекрёстная резистентность к мефлохину.
Фармакокинетика
Биодоступность варьирует у разных людей, возрастает при приёме с пищей (особенно жирной). Около 20-30% введённой дозы метаболизируется с образованием активного метаболита - N-дезбутил-галофантрина. Элиминируется преимущественно с калом. галофантрина* - 1-2 сут, активного метаболита - до 6-10 сут.
Показания
Лечение тропической малярии при резистентности к хлорохину и другим препаратам.
Противопоказания
Гиперчувствительность, беременность, возраст до 1 года, заболевания сердца с предрасположенностью к удлинению интервала Q-T.
Нежелательные лекарственные реакции
Боль в животе, тошнота, рвота, диарея. Аллергические реакции. Замедление проводимости в сердце, удлинение интервалов P-R и Q-T с высоким риском фатальных аритмий (факторы риска: применение во время или сразу после еды, недостаточность витамина В1 , нарушения электролитного баланса, синдром врождённого удлинения Q-T) . Общая слабость, заторможённость, головная боль, судороги. Артралгии. Боль в груди. Кашель. Гипотензия.
Лекарственные взаимодействия
Фармакодинамическое. Не сочетать с хинином и мефлохином ввиду значительного повышения риска кардиотоксичности. Можно использовать не ранее чем через 3 нед после окончания приёма мефлохина.
Применение в особых ситуациях
Лактация. При назначении кормящим женщинам необходимо сопоставлять возможные пользу и риск.
Гериатрия. Учитывая возможные сопутствующие заболевания у лиц пожилого возраста, применять с осторожностью под строгим контролем.
Заболевания сердца. Возрастает риск кардиотоксичности. При заболеваниях с предрасположенностью к удлинению интервала Q-T галофантринP противопоказан.
АРТЕМИЗИНИНP И ЕГО ПРОИЗВОДНЫЕ
АртемизининP - экстракт травы Artemisia annua. В настоящее время чаще используют его полусинтетические производные - артеметерP , артесунатP и артеэтерP , имеющие более высокую противомалярийную активность.
Фармакодинамика
Предполагают, что противомалярийный эффект связан с активацией перекисного окисления и повреждением свободными радикалами клеточных мембран и внутриклеточных белков плазмодия. Чувствительны эритроцитарные формы всех видов плазмодия, включая полирезистентные P. falciparum.
Фармакокинетика
Изучена недостаточно. После введения в организм быстро гидролизуются с образованием активного метаболита - дигидроартемизинина. Артесунат* имеет более короткий T1/2 (около 1 ч), чем артеметер* (4-12 ч). T1/2 артеэтера* ещё более длительный.
Показания
Лечение малярии при резистентности к другим препаратам (иногда в сочетании с мефлохином, хинином, галофантрином*, пириметамином/сульфадоксином или доксициклином). Характерен быстрый эффект: купирование приступов в течение 1-3 сут.
Противопоказания
Гиперчувствительность, беременность.
Нежелательные лекарственные реакции
Боль в животе, диарея. Повышение активности трансаминаз. Tранзиторная ретикулоцитопения и нейтропения. Лекарственнная лихорадка. Брадикардия.
Применение в особых ситуациях
Лактация. При назначении кормящим женщинам необходимо сопоставлять возможные пользу и риск.
Педиатрия. Адекватные исследования безопасности не проводились. Применять с осторожностью.
Препараты, применяемые при других протозойных инфекциях
ПАРОМОМИЦИН
Природный антибиотик-аминогликозид, близкий по структуре к неомицину.
Фармакодинамика
Протозоацидный эффект паромомицина8 связан с нарушением синтеза белка рибосомами. Клиническое значение имеет действие на патогенные амёбы («просветный» амебицид, действующий только на паразитов, находящихся в просвете кишечника), криптоспоридии и лейшмании.
Фармакокинетика
Практически не всасывается в пищеварительном тракте, создаёт высокую концентрацию в просвете кишечника и полностью выводится с калом. Возможна абсорбция через повреждённую слизистую оболочку, а также при выраженных нарушениях моторно-эвакуаторной функции пищеварительного тракта. При наружном применении не всасывается.
Показания
Неинвазивный амёбиаз (бессимптомное носительство). Криптоспоридиоз. Кожный лейшманиоз (местно).
Противопоказания
Гиперчувствительность, тяжёлая почечная недостаточность, эрозивно-язвенные поражения пищеварительного тракта, непроходимость кишечника.
Нежелательные лекарственные реакции
Боль или дискомфорт в животе, тошнота, рвота, диарея. В случае абсорбции возможны нефротоксические, ототоксические и/или вестибулотоксические эффекты (см. «Аминогликозиды»).
Лекарственные взаимодействия
Не сочетать с ЛС, обладающими отоили нефротоксичностью.
Применение в особых ситуациях
Беременность, лактация. Адекватные данные о безопасности отсутствуют. Применять с осторожностью.
Гериатрия. Учитывая возможное возрастное понижение функций почек и слуха, применять с осторожностью.
Нарушение функций почек. Применять с осторожностью, контролируя функции почек. При тяжёлой почечной недостаточности противопоказан.
ЭМЕТИН И ДЕГИДРОЭМЕТИН
Эметин - алкалоид растения Ipecacuanha, дегидроэметин* - его полусинтетический аналог с несколько меньшей токсичностью.
Фармакодинамика
Активны в отношении патогенных амёб, являются тканевыми амебицидами, действующими на клетки паразита, локализующегося в стенке кишечника и печени. Эффект предположительно связан с дегенеративными изменениями в ядре и цитоплазме.
Фармакокинетика
Имеют низкую биодоступность при приёме внутрь. Хорошо всасываются при внутримышечном введении. Распределяются во многие органы и ткани, накапливаются в печени, лёгких, селезёнке, почках. Медленно экскретируются почками. Обладают кумулятивными свойствами. в среднем составляет около 5 сут.
Показания
Tяжёлые формы кишечного и внекишечного амёбиаза, включая абсцесс печени (при неэффективности или непереносимости нитроимидазолов). Иногда в сочетании с хлорохином.
Противопоказания
Гиперчувствительность, заболевания почек, сердца, скелетных мышц, беременность, кормление грудью, ранний детский возраст.
Нежелательные лекарственные реакции
Чаще отмечают при использовании эметина.
Tошнота, рвота, диарея (появление или усиление). Боль в сердце, тахикардия, изменения на ЭКГ (удлинение Q-T, инверсия зубца Т, депрессия ST, гипотензия), возможен острый дегенеративный миокардит с летальным исходом. Боль и ригидность в области инъекции (возможны абсцессы и некрозы). Генерализованная мышечная слабость, нарушения чувствительности. Экзематозная, эритематозная или уртикарная сыпь. Нефротоксичность. Повышение активности трансаминаз, токсический гепатит.
Лекарственные взаимодействия
Фармакодинамическое. Не сочетать с ЛС, обладающими кардиотоксичностью, нейротоксичностью или неблагоприятно влияющими на скелетную мускулатуру.
Применение в особых ситуациях
Педиатрия. Адекватные данные о безопасности отсутствуют. Не применять детям раннего возраста. В других возрастных группах использовать с осторожностью.
Гериатрия. Учитывая возрастное понижение функций печени и почек, сопутствующие заболевания у лиц пожилого возраста, применять с большой осторожностью.
ДИЛОКСАНИДА ФУРОАТ
Используют в качестве «просветного» амёбицида.
Фармакокинетика
Изучена недостаточно. Под влиянием эстераз кишечника гидролизуется с высвобождением активного дилоксанида, большая часть которого всасывается, метаболизируется в печени и экскретируется преимущественно с мочой. Неабсорбированный дилоксанид (около 10%) действует на амёб, находящихся в просвете кишечника. Выводится с калом.
Показания
Кишечный амёбиаз. Бессимптомное носительство амёб в кишечнике.
Противопоказания
Гиперчувствительность, беременность, возраст до 2 лет.
Нежелательные лекарственные реакции
Метеоризм, боль в животе, тошнота, рвота. Крапивница, кожный зуд.
Применение в особых ситуациях
Лактация. Адекватные данные о безопасности отсутствуют. Применять с осторожностью.
Педиатрия. Адекватные данные о безопасности отсутствуют. Применять с осторожностью у детей старше 2 лет.
ЭТОФАМИД
По структуре и клинико-фармакологическим характеристикам близок дилоксанида фуроату*. Используют в качестве «просветного» амёбицида.
МЕГЛЮМИНА АНТИМОНАТ
Органическое соединение пятивалентной сурьмы, препарат выбора при лечении лейшманиоза. Механизм противопротозойного эффекта точно не установлен.
Фармакокинетика
При парентеральном введении распределяется во многие ткани и среды организма, накапливается в коже, клетках ретикулоэндотелиальной системы. Элиминируется почками. при внутривенном введении - 2-30 ч, при внутримышечном - до 1 мес.
Показания
Лейшманиоз - висцеральный, кожно-слизистый, кожный.
Противопоказания
Гиперчувствительность, тяжёлые нарушения функций почек, печени, тяжёлые заболевания сердечно-сосудистой системы, туберкулёз легких, возраст до 2 лет.
Нежелательные лекарственные реакции
Анорексия, тошнота, рвота. Сыпь, лихорадка, артралгия, миалгия, кашель, пневмонит. Головная боль, головокружение, полиневрит. Нарушение функций почек, острая почечная недостаточность. Боль в сердце, удлинение Q-T, изменение зубца Т, нарушения ритма, миокардит. Повышение активности трансаминаз, амилазы, гепатит, панкреатит. Боль в месте введения.
Применение в особых ситуациях
Беременность, лактация. Адекватные данные о безопасности отсутствуют. Применять с осторожностью.
Педиатрия. Адекватные данные о безопасности отсутствуют. Не рекомендуют детям до 2 лет. В других возрастных группах применять с осторожностью.
Гериатрия. Учитывая возрастное понижение функций печени и почек, наличие сопутствующих заболеваний у лиц пожилого возраста, применять с осторожностью.
Нарушение функций почек, печени. Возрастает риск токсичности. Применять с осторожностью. При тяжёлых нарушениях функций противопоказан.
Противопротозойной активностью обладают также нитроимидазолы (метронидазол и др.) и производное нитрофурана фуразолидон, которые описаны в разделе «Антибактериальные лекарственные средства».
Таблица 20-30. Режимы дозирования противопротозойных препаратов
| Препарат | Взрослые, доза | Дети, доза |
|---|---|---|
Хлорохин |
Лечение малярии: |
Лечение малярии: |
Хинин |
I схема: 1-я доза - 15-20 мг/кг в/в в течение 4 ч, далее 7-10 мг/кг каждые 8-12 ч в/в с последующим переводом на приём внутрь; |
25 мг/ (кгх сут) в 3 введения каждые 8 ч, сначала в/в, затем внутрь |
Мефлохин |
Лечение малярии: |
Старше 2 лет: |
Примахин |
Внутрь 0,25 мг/(кгх сут) в течение от 3 сут до 3 нед или 0,75 мг/кг 1 раз в нед в течение 8 нед |
Старше 3 лет: как у взрослых |
Прогуанил |
Внутрь 0,2 г/сут |
Внутрь 3 мг/(кгх сут) |
Пириметамин |
Лечение токсоплазмоза в первые 2 дня - внутрь 75-100 мг (при энцефалите до 0,2 г), далее 50-75 г/сут |
Лечение токсоплазмоза в первые 2 дня - внутрь 2 мг/(кгх сут), далее 1 мг/(кгх сут) |
Пириметамин/ сульфадоксин |
Внутрь 3 таблетки однократно В/м 3 ампулы однократно |
До 4 лет - внутрь 1/2 таблетки, 5-8 лет - 1 таблетка, 9-15 лет - 2 таблетки однократно; в/м до 1 года - 1/4 ампулы, 1-4 лет - 1/4-3/4 ампулы, 5-8 лет - 3/4-1 ампула, 9-15 лет - 1-1,5 ампулы, однократно |
ГалофантринP |
Внутрь 8 мг/кг в два приёма через 6 ч |
Старше 1 года: внутрь 8 мг/кг три приёма через 6 ч |
АртеметерP |
В/м 1-я доза - 3,2 мг/кг, далее 1,6 мг/(кгх сут), в течение 7 дней |
— |
АртесунатP |
В/в 1-я доза - 4 мг/кг, далее 2 мг/(кгх сут) в течение 7 дней |
В/в в 1-е сут - 2 мг/кг каждые 12 ч, далее - 1 мг/кг каждые 12 ч в течение 7 дней |
Паромомицин8 |
Внутрь 25-30 мг/(кгх сут) в 3 приёма в течение 7-10 дней |
— |
Эметин |
В/м 1 мг/(кгхсут) (не более 60 мг) в 1 введение в течение 4-6 дней |
— |
ДегидроэметинP |
В/м 1 мг/(кгхсут) (не более 90 мг) в 1 введение в течение 4-6 дней |
— |
Дилоксанида фуроатP |
Внутрь 0,5 г каждые 6-8 ч в течение 10 дней |
Старше 2 лет: внутрь 20 мг/(кгхсут) в 3 приёма в течение 10 дней |
Этофамид8 |
Внутрь 20 мг/(кгхсут) в 2 приёма в течение 5-7 дней |
— |
Меглумина антимонат8 |
В/м 20 мг Sb/(кгхсут) в 1 введение в течение 10-15 дней |
— |
СПИСОК ЛИТЕРАТУРЫ
Практическое руководство по антиинфекционной химиотерапии / Под. общ. ред. Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова. - Смоленск: МАКМАХ, 2007.
Федеральное руководство по использованию лекарственных средств (формулярная система). -Вып. VIII. - М., 2007.
Bryskier A. Antimicrobial Agents. - Washington, DC: Publisher, 2005.
Finch R.G., Greenwood D., Norrby S.R. et al. Antibiotic and Chemotherapy. - Edinburgh etc.: Churchill Livingstone, 2003.
Mandell G.l., Bennett J.E., Dolin R. Principles and Practice of Infectious Diseases. - 6-th ed. - City: Publisher, 2005.
Neu H.C. et al. New Macrolides, Azalides, and Streptogramines in Clinical Practice. - New York, 1995.
Scolar E.M., Pratt W.B. The Antimicrobial Drugs. - 2-d ed. - Oxford: University Press, 2000. USP DI - Drug Information for the Health Care Professional. - New York: Micromedex, 2004.