Клиническая фармакология : национальное руководство / под ред. Ю. Б. Белоусова, В. Г. Кукеса, В. К. Лепахина, В. И. Петрова - Москва : ГЭОТАР-Медиа, 2014 |
Аннотация
Издание разработано и рекомендовано ведущими специалистами в области клинической фармакологии при участии специализированных научно-исследовательских учреждений, медицинских вузов.
В книгу вошли общие и частные вопросы клинической фармакологии, содержащие объединённую согласованную позицию ведущих отечественных специалистов из Москвы, Санкт-Петербурга, Волгограда, Воронежа, Смоленска, Ярославля, Казани, Ставрополя, Перми и других городов России. Имеется компакт-диск с дополнительными материалами к книге.
Руководство предназначено клиническим фармакологам, врачам-терапевтам, студентам старших курсов медицинских вузов, интернам, ординаторам, аспирантам.
Основные направления современного лекарственного лечения злокачественных опухолей:
Первые три метода относят к категории противоопухолевого лечения; последний - позволяет уменьшить тягостные симптомы заболевания.
Лекарственное лечение может быть:
Первичное (или индуктивное) лечение применяют при местнораспространённом неоперабельном опухолевом процессе. Критерии эффективности первичной терапии:
По степени выраженности лечебного эффекта принято различать:
Первичная терапия может быть излечивающей (для взрослых - болезнь Ходжкина, неходжкинские лимфомы, герминогенные опухоли и хориокарцинома; для детей - острый лимфобластный лейкоз, лимфома Беркитта, опухоль Вильмса, эмбриональная рабдомиосаркома) или паллиативной - с улучшением качества жизни, увеличением времени до прогрессирования и общей выживаемости для большинства солидных опухолей.
Неоадъювантное лечение проводят при операбельных опухолях до выполнения оперативного вмешательства. Критерии эффективности: частота лечебных эффектов (полная или частичная регрессия) и частота морфологически полной регрессии. При этом первичная опухоль выступает в качестве биологического маркёра чувствительности к лекарственному лечению отдалённых микрометастазов, которые к этому времени могут иметь большинство пациентов в связи с высокой вероятностью системного характера заболевания. Проведение неоадъювантной терапии позволяет:
-
выполнять органосохраняющие операции без ущерба для радикальности;
-
прогнозировать индивидуальную эффективность адъювантной лекарственной терапии (хороший эффект указывает на целесообразность аналогичного адъювантного лечения, отсутствие эффекта - на необходимость изменения схемы);
-
дифференцировать пациентов с частичным регрессом с точки зрения прогноза (гистологическая и молекулярно-генетическая оценка оставшихся опухолевых клеток);
-
достигать подавления микрометастазов при наличии системного характера заболевания.
Адъювантное лечение проводят после оперативного лечения (в том числе циторедуктивного) при отсутствии клинических проявлений отдалённых метастазов. Цель адъювантной терапии - снижение частоты системных рецидивов заболевания путём уничтожения отдалённых микрометастазов. При этом критериями эффективности лечения служат безрецидивная (от начала лечения до появления прогрессирования заболевания) и общая выживаемость.
Проведение лекарственной терапии на ранней стадии теоретически должно быть более эффективным в силу:
Паллиативное лечение проводят при наличии отдалённых метастазов. Критерии эффективности: частота лечебных эффектов, время до прогрессирования, время продолжительности эффекта, общая выживаемость.
Различия в подходах к терапии операбельного и распространённого рака определяет цель лечения: при операбельных опухолях - излечение, при распространённых - продление жизни и улучшение её качества.
Различия касаются также требований к ожидаемой токсичности химиотерапии и к удобству её проведения. Высокая токсичность допустима при операбельных опухолях и не может быть оправдана при лечении распространённых процессов. Удобство проведения лечения не имеет большого значения при операбельных формах рака (так как терапия занимает непродолжительное время) и выступает важным фактором при распространённых поражениях, требующих длительного применения противоопухолевых препаратов.
Выбор лекарственного лечения можно проводить:
Чаще всего при планировании лечения используют следующие молекулярно-генетические маркёры: рецепторы стероидных гормонов, гиперэкспрессия HER2, экспрессия CD20, гиперэкспрессия или мутация c-kit (CD117), мутации EGFR.
Изучение эффективности противоопухолевых препаратов предполагает проведение предклинической и клинической фазы исследования. Предклиническую фазу можно проводить in vitro и in vivo; в последнем случае оценивают противоопухолевую активность и токсичность препарата. Клиническая фаза, в свою очередь, подразделена на три фазы:
Химиотерапия - лечение злокачественных опухолей с помощью цитостатических препаратов - широко используемый метод лекарственной терапии. Л. Гудман и А. Джилман в 1942 г. первыми с успехом использовали эмбихинà при болезни Ходжкина и лимфоцитарной лимфоме. В настоящее время в арсенал цитостатиков входят десятки препаратов.
Классификация цитостатиков представлена ниже.
С учётом особенностей действия цитостатиков на клетку препараты классифицируют на циклоспецифичные (действующие на делящуюся клетку) и циклонеспецифичные (действующие на клетку независимо от того, делится она или нет). Циклоспецифичные препараты, в свою очередь, подразделяют на фазоспецифические (действующие на клетку в определённые фазы клеточного цикла) и фазонеспецифические.
Эффективность цитостатиков во многом зависит от особенностей их абсорбции, распределения, метаболизма и экскреции в организме (то есть от фармакокинетики). Фармакокинетические показатели существенно варьируют у разных больных. При этом абсорбция зависит от предшествующих операций, химио- и лучевой терапии, от тошноты и рвоты, от диеты, от применения других препаратов, а также от генетических различий обмена веществ и транспортных систем кишечника. На распределение оказывают влияние количество жировой ткани, наличие экстраваскулярных скоплений жидкости (асцит), гипоальбуминемия, одновременное применение нескольких препаратов. Функциональное состояние печени и нарушения печёночного кровотока (в том числе и возрастные) в большей степени определяют характеристики метаболизма. В качестве факторов, влияющих на экскрецию выступают: нарушение функции печени, почечная недостаточность, pH мочи, генетические различия путей элиминации препарата и одновременное применение других лекарственных средств.
Возраст больных, генетические и этнические особенности - наиболее значимые факторы, оказывающие влияние на фармакокинетику цитостатиков.
Важнейшие параметры, характеризующие фармакокинетику цитостатика - AUC (площадь под кривой - изменение концентрации препарата в плазме во времени) и время полувыведения (время, необходимое для снижения концентрации препарата в плазме в 2 раза - функция элиминации).
Химиотерапию можно применять системно или местно. Системная терапия предполагает пероральное, подкожное, внутримышечное или внутрисосудистое (внутривенное или внутриартериальное) введение. Внутрисосудистое введение осуществляют болюсно или путём длительных инфузий. Местная химиотерапия может быть применена в виде перфузий (полости, конечности, органа), инфузий (внутриартериально), внутриопухолевого и внутриполостного введения препарата (в мочевой пузырь, брюшную и плевральную полости, в спинномозговой канал), а также в виде мазей, присыпок и растворов для наружного применения.
В связи с экспоненциальной зависимостью между дозой и эффектом для большинства цитостатиков одним из основных принципов химиотерапии выступает использование максимальной дозы в минимальный промежуток времени. Стандартный интервал между циклами введения цитостатиков - 21 день, что соответствует времени восстановления костного мозга. Эффективность терапии оценивают после каждых 2 циклов лечения при условии отсутствия явных признаков прогрессирования. Общее количество циклов определяют индивидуально, однако, обычно после достижения максимального эффекта проводят ещё 2 цикла.
В связи с тем, что большинство цитостатиков обладают неспецифической активностью, их использование неизбежно сопровождают побочные эффекты. Побочные эффекты могут быть как местными, так и системными.
К локальным побочным эффектам могут быть отнесены тромбофлебиты и экстравазация; к системным - миелосупрессия (лейкопения, анемия, тромбоцитопения), желудочно-кишечные проявления (рвота, понос, запор), нейротоксичность (полиневриты, ототоксичность), гепато- и нефротоксичность, а также воздействие на репродуктивные органы (аменорея, стерильность).
Дозу цитостатиков при последующих циклах химиотерапии корригируют с учетом наличия и выраженности побочных токсических эффектов. При этом необходимо помнить, что снижение дозы на 20% сопровождает снижение ожидаемой эффективности лечения на 50%.
Гормонотерапия - метод лечения рака путём удаления источника гормонов, подавления их продукции или блокирования действия гормонов на органы-мишени. История метода берёт начало с работ Битсона, который в 1896 г. с успехом применил овариэктомию для лечения больных раком молочной железы.
Удаление источника гормонов предполагает выполнение овариэктомии, орхиэктомии, адреналэктомии или гипофизэктомии.
Блокирование продукции гормонов может быть достигнуто применением ингибиторов ароматазы или ингибиторов рилизинг-гормонов гипофиза.
Конкуренция с эндогенными гормонами на уровне органа-мишени лежит в основе действия антиандрогенов, антиэстрогенов, глюкокортикоидов, прогестинов, эстрогенов и андрогенов.
Гормонотерапию чаще всего применяют при раке молочной железы, раке предстательной железы и раке эндометрия.
Как правило, гормонотерапию проводят непрерывно до появления признаков прогрессирования. Необходимо учитывать, что в ряде случаев при использовании аналогов рилизинг-гормонов, тамоксифена, андрогенов и прогестинов в первые 2 нед лечения можно наблюдать усиление болевого синдрома в области метастазов, гиперемию и отёчность при кожных поражениях. Это может быть проявлением, так называемой, flare-реакции, которая постепенно исчезает при продолжении лечения в ближайшие 3-4 нед и расценивается как косвенный признак эффективности последующей гормонотерапии.
Гормонотерапию, как правило, переносят удовлетворительно; различные побочные эффекты развиваются при длительном применении в зависимости от особенностей препарата или метода. Наиболее типичны феминизация или маскулинизация, остеопороз, гиперплазия эндометрия, гиперкальциемия, надпочечниковая недостаточность, тромбоэмболические осложнения.
Биотерапия - метод лечения рака путём активизации естественных защитных механизмов или введения естественных полимерных молекул (цитокины, факторы роста). Впервые Бух в 1868 г. сообщил о регрессе опухоли на фоне рожистого воспаления и с успехом индуцировал его у другого пациента, страдающего раком. Биотерапия подразделяется на активную иммунотерапию, пассивную иммунотерапию и применение, так называемых, непрямых методов.
Активную иммунотерапию классифицируют на неспецифическую (интерферон альфа-2, интерферон гамма, интерлейкин-1,2) и специфическую (вакцинотерапия).
Пассивная иммунотерапия предусматривает применение антител (ритуксимаб, трастузумаб, бевацизумаб, цетуксимаб и т.п.) или клеток (опухольинфильтрирующие лимфоциты, лимфокинактивированные киллеры).
Непрямые методы биотерапии предполагают воздействие посредством ингибиторов сигнальной трансдукции.
Показания для неспецифической активной иммунотерапии с использованием интерферона альфа, интерлейкина-2 - метастатический рак почки и диссеминированная меланома.
Вакцинотерапия до настоящего времени выступает экспериментальным методом лечения и может использоваться только в клинических исследованиях.
Применение моноклональных антител и ингибиторов сигнальной трансдукции относят к наиболее активно развивающимся способам лекарственного лечения злокачественных опухолей. Особенность их использования - необходимость подтверждения наличия соответствующей мишени в опухоли или организме пациента (HER2, EGFR, c-Kit).
Как правило, биотерапию проводят до прогрессирования опухоли или в течение ограниченного периода времени (1-2 г.) в случае адъювантного лечения.
Для биотерапии характерны как острые, так и хронические побочные эффекты; наиболее часто отмечают лихорадку, гриппоподобный синдром, местные реакции, обострение аутоиммунных заболеваний.
Применение молекулярно-генетического анализа для выбора противоопухолевой терапии
Введение
В настоящее время основанием для назначения большинства противоопухолевых препаратов считают статистическую вероятность получения положительного эффекта. Если при применении современных комбинаций цитостатиков на начальных этапах лечения относительно химиочувствительных опухолей (например, РМЖ) вероятность достигает 80%, то во многих ситуациях (например, при лечении карцином толстой кишки 5-фторурацилом) регресс новообразования наблюдают менее чем у 20% пациентов. Недостатки вероятностного подхода при выборе терапии особенно очевидны именно в онкологии.
-
Врачи других специальностей, как правило, имеют достаточный резерв времени на оптимизацию лечения (например, подбор антигипертензивных схем занимает несколько месяцев), однако при лекарственной терапии новообразований подобной возможности зачастую нет. Любая неудачная попытка противоопухолевого воздействия сопровождается продолжением роста опухоли, что подразумевает возрастание риска нарушения функций жизненно важных органов.
-
Противоопухолевые препараты обладают весьма низким терапевтическим индексом, поэтому их применение почти всегда сопровождается тяжёлыми (зачастую угрожающими жизни) побочными эффектами. Следовательно, сознательный отказ от назначения заведомо неэффективного лечения во многих ситуациях можно рассматривать как оптимальное терапевтическое решение.
-
Большинство современных онкологических препаратов обладает чрезвычайно высокой стоимостью: подсчитано, что расходы на лечение одного пациента составляют несколько (десятков) тысяч долларов в месяц. Предполагают, что разработка маркёров химиочувствительности новообразований поможет уменьшить затраты на лечение за счёт более обоснованного использования дорогостоящих препаратов.
При оценке вероятности положительного эффекта лечения онкологического заболевания, как правило, можно полагаться только на отдельные фенотипические характеристики (гистологический тип опухоли, степень её дифференцировки, общее состояние пациента и др.). Предполагают, что идентификация молекулярных маркёров химиочувствительности и химиорезистентности позволит существенно улучшить результаты противоопухолевой терапии.
Исследования, проводимые в данном направлении, ставят две задачи:
В первом случае объект изучения - унаследованные генные полиморфизмы, во втором - приобретённые мутационные и экспрессионные события, произошедшие непосредственно в опухолевой ткани (рис. 8-1, табл. 8-1).
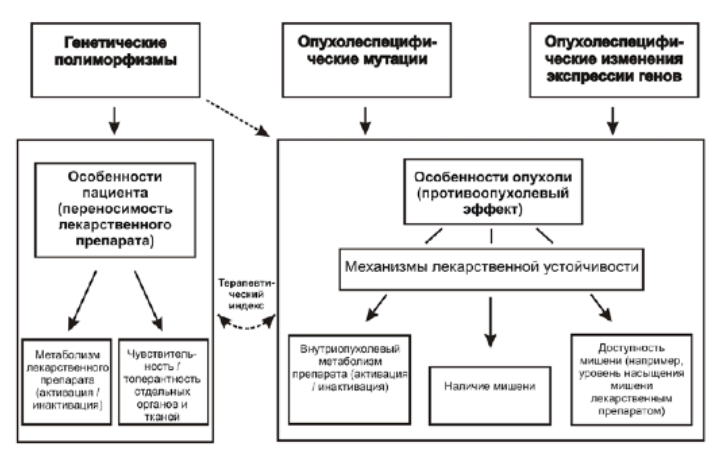
Рис. 8-1. Молекулярные маркёры ответа на противоопухолевую терапию.
Таблица 8-1. Молекулярные маркёры эффективности и токсичности противоопухолевой терапии
| Препарат | Прогнозирование токсичности | Прогнозирование противоопухолевого эффекта | Литература |
|---|---|---|---|
Цитостатические препараты |
|||
Меркаптопурин |
TPMT (полиморфизм) |
Marsh and McLeod, 2004; Dervieux et al., 2005 |
|
Иринотекан |
UGT1A1 (полиморфизм) |
Innocenti and Ratain, 2004; Innocenti et al., 2006 |
|
Метотрексат |
MTHFR (полиморфизм) |
Toffoli et al., 2000; Ulrich et al., 2001; Chiusolo et al., 2002; Toffoli et al., 2003 |
|
Фторурацил и его производные |
DPD (DPYD) (полиморфизм) |
TS (TYMS) и MTHFR (полиморфизм); TS, DPD, TS, OPRT (экспрессия) |
Aschele et al., 2002; Omura, 2003; Watters and McLeod, 2003; Ciccolini et al., 2004; Formentini et al., 2004; van Kuilenburg, 2004; Kawakami et al., 2005; Marsh, 2005; Robert et al., 2005; Stohlmacher, 2005; Ochiai et al., 2006 |
Препараты платины |
Фермент ERCC1 (экспрессия) |
Rosell et al., 2005 |
|
Алкилирующие вещества |
MGMT (экспрессия) |
Robert et al., 2004; Liu and Gerson, 2006 |
|
Антрациклины |
TOP2A (амплификация или гиперэкспрессия) |
Coon et al., 2002; Di Leo et al., 2002a; MacGrogan et al., 2003; Park et al., 2003; Knoop et al., 2005; Tanner et al., 2006 |
|
Препараты, взаимодействующие с микротрубочками |
class III b-tubulin, t, thioredoxin (экспрессия) |
Rouzier et al., 2005; Seve et al., 2005; Ferrandina et al., 2006; Kim et al., 2006; Urano et al., 2006 |
|
Таргетные препараты |
|||
Антиэстрогеновые препараты |
ER, PR экспрессия; HER2, cyclin D1 амплификация или гиперэкспрессия |
Di Leo et al., 2002; Pusztai et al., 2004 |
|
Ритуксимаб |
CD20 экспрессия |
Doan and Massarotti, 2005 |
|
Трастузумаб |
HER2 амплификация или гиперэкспрессия |
Ross et al., 2003 |
|
Иматиниб |
BCR-ABL транслокация, KIT мутация |
Druker, 2004; Guilhot, 2004 |
|
Гефитиниб и эрлотиниб |
EGFR мутация |
Giaccone and Rodrigues, 2005; Imyanitov et al., 2005; Chan et al., 2006 |
|
Цетуксимаб |
EGFR амплификация |
Moroni et al., 2005; Lievre et al., 2006 |
|
Примечание: DPD - дигидропиримидин-дегидрогеназа; EGFR - эпидермальный фактор роста; MGMT - 6-O-метилгуанин-ДНК-метилтрансфераза; MTHFR - метилен-тетрагидрофолат-редуктаза; TOP2A - топоизомеразы II-a; TPMT - тиопурин-метилтрансфераза; TS - тимидилат-синтаза; UGT1A1 - уридин-дифосфат-глюкуронозил-трансфераза 1A1
Фармакогенетика противоопухолевых препаратов
Полиморфизм гена тиопурин-метилтрансферазы и переносимость меркаптопурина
Меркаптопурин принадлежит к семейству тиопуриновых антиметаболитов. Его применяют преимущественно для лечения острого лимфобластного лейкоза у детей. Производный препарат - азатиоприн используют для иммуносупрессии у пациентов, перенёсших трансплантацию органов и тканей, а также при тяжёлых аутоиммунных заболеваниях. Оба препарата инактивируются ферментом тиопурин-метилтрансферазой (TPMT). Для активности TPMT характерна большая популяционная вариабельность. Порядка у 90% людей активность фермента нормальная; у примерно 10% - активность TPMT значительно снижена; а у 0,3% населения она полностью отсутствует. Инактивирующие полиморфизмы гена TPMT - причина всех нарушений продукции и активности фермента. Более 90% неактивных аллелей TPMT обусловлены тремя генными полиморфизмами. Эти аллели обозначают как TPMT*2 (нуклеотидная замена G238C; на уровне белка проявляется как Ala18Pro), TPMT*3A (нуклеотидные замены G460A и A719G; аминокислотные замены Ala154Thr и Tyr240Cys) и TMPT*3C (нуклеотидная замена A719G; аминокислотная замена Tyr240Cys). Присутствие вариантных аминокислот делает белок TPMT более чувствительным к деградации посредством убиквитилирования.
Таким образом, три достаточно простых ПЦР-теста позволяют с высокой степенью надёжности предсказать переносимость меркаптопурина. При назначении обычных доз препарата гетерозиготные носители вариантных аллелей могут страдать от серьёзных побочных действий. Эти эффекты могут представлять угрозу для жизни, если лечение проводят у гомозиготных носителей мутаций. Для предупреждения подобных осложнений перед применением меркаптопурина рекомендуют проводить молекулярный анализ TPMT. При выявлении гомозиготного носительства инактивирующих мутаций дозу препарата необходимо понизить в 10-15 раз. У гетерозиготных носителей вариантных аллелей TPMT наблюдают больший эффект лечения меркаптопурином. Подобные наблюдения позволяют поставить вопрос о целесообразности увеличения дозы меркаптопурина у пациентов с нормальным генотипом.
Фармакогенетика иринотекана
Иринотекан - полусинтетический аналог растительного алкалоида камптотецина. Механизм его противоопухолевого эффекта основан на ингибировании топоизомеразы I. Биологические эффекты иринотекана зависят от концентрации его активного метаболита - 7-этил-10-гидроксикамптотецина (SN-38). Физиологическую инактивацию SN-38 осуществляет фермент уридин-дифосфат-глюкуронозил-трансфераза 1A1 (UGT1A1) посредством глюкуронидации. Один из полиморфизмов фермента UGT1A1 основан на вариабельности количества TA повторов в промоторной области гена. Большинство людей гомозиготны по аллелю (TA)6, ассоциированному с нормальной экспрессией UGT1A1. Некоторые индивидуумы гетеро- или гомозиготны по варианту (TA)7 (UGT1A1*28), который характеризует сниженная транскрипция гена. В то время как аллель UGT1A1*28 характерен преимущественно для представителей европеоидной расы, у людей монголоидной расы низкоактивный вариант UGT1A1 связан с полиморфизмом G211A (Gly71Arg). Поскольку UGT1A1 "отвечает" за конъюгацию билирубина, дефицит данного фермента может быть с ассоциирован с гипербилирубинемией (синдром Жильбера).
Большинство исследователей сходятся во мненнии, что присутствие вариантных аллелей гена, кодирущего UGT1A1, сопряжено с повышенной токсичностью иринотекана. Воспроизводимость подобных наблюдений привела к тому, что тест на полиморфизм UGT1A1 получил поддержку управления пищевых продуктов и лекарств США (FDA). Гомозиготным по аллелю UGT1A1*28 пациентам рекомендуют понижение начальной дозировки препарата. В то же время, многие специалисты обсуждают целесообразность увеличения дозы иринотекана у носителей нормального генотипа UGT1A1.
Полиморфизм генов метаболизма фторпиримидинов
Механизм противоопухолевого действия 5-фторурацила основан на угнетении фермента тимидилат-синтазы (TS). Активный метаболит фторурацила - 5-фтор-2’-дезоксиуридин-монофосфат (FdUMP), взаимодействует с TS в присутствии ко-фактора - 5,10-метилен-тетрагидрофолата (CH2FH4). Концентрацию CH2FH4 регулирует фермент метилен-тетрагидрофолат-редуктаза (MTHFR), который конвертирует CH2FH4 в 5-метилтетрагидрофолат (CH3FH4).
Наиболее драматические последствия применения фторурацила могут быть связаны с полиморфизмом гена, кодирующего дигидропиримидин-дегидрогеназу (DPD). Примерно 95% людей обладают нормальной активностью фермента DPD. Ещё у 3-5% функция фермента снижена, а у 0,1% - отсутствует полностью. Полный дефицит DPD может быть ассоциирован с церебральной дисфункцией. Пониженная активность DPD не сопровождается какими-либо клиническими проявлениями. Однако при лечении фторурацилом у таких пациентов могут развиваться тяжелейшие токсические реакции. Многие случаи дефицита DPD можно объяснить инактивирующей мутацией в соответствующем гене. Мутации в гене DPD (в отличие от TPMT) могут располагаться в любой его части. Поэтому для проведения соответствующего молекулярного анализа необходимо полное секвенирование гена. Несмотря на то, что применение стандартных дозировок фторурацила при врождённом дефекте DPD может привести к летальному исходу, рутинный скрининг подобных аномалий пока не включён в стандарты клинической онкологии. Единственный фактор, ограничивающий внедрение данного молекулярного теста - высокая стоимость секвенирования ДНК.
Определённый интерес вызывают полиморфизмы, обнаруженные в гене фермента TS. Наиболее хорошо изучен 28-ми нуклеотидный повтор, расположенный в 5’-нетранслируемой области данного гена. Этот повтор состоит или из двух (аллель TSER*2), или из трёх (аллель TSER*3) фрагментов. Аллель TSER*3 характеризует более интенсивная экспрессия гена за счёт присутствия дополнительного сайта связывания для фактора транскрипции USF-1. Однако, этот эффект может нивелироваться другим полиморфизмом (G>C), который расположен внутри сайта распознавания USF-1. Геном некоторых пациентов содержит 6-ти нуклеотидную делецию внутри 3’-нетранслируемой последовательности гена. Эта делеция ассоциирована с пониженной экспрессией TS. Считают, что гомозиготность по низкоактивным аллелям TS ассоциирована с наибольшей эффективностью лечения фторпиримидинами. Однако присутствие хотя бы одного высокоактивного варианта гена может быть причиной потенциальной неэффективности подобного лечения. Поскольку полиморфизм гена TS влияет не только на опухолевую, но и на системную восприимчивость к воздействию фторпиримидинов, присутствие низкоэкспрессируемых аллелей гена TS зачастую сопряжено с повышенным риском возникновения побочных реакций на применение фторурацила. Следует отметить, что представление о предиктивной значимости гена TS разделяют далеко не все исследователи.
Полиморфизм C677T (Ala222Val) гена, кодирующего MTHFR, фенотипически выражается в пониженной активности фермента. Это приводит к снижению концентрации CH3FH4, и, как следствие, к усиленному связыванию TS 5-фтор-2’-дезоксиуридин-монофосфатом. Таким образом, у носителей валинового аллеля наблюдают тенденцию к возрастанию эффективности лечения фторурацилом.
Молекулярные маркёры химиочувствительности опухолей
Индивидуализация назначения фторпиримидинов
К настоящему моменту лучше всего изучены молекулярные маркёры ответа опухоли на лечение фторпиримидинами. Во множестве работ продемонстрирована взаимосвязь между повышенным содержанием фермента TS и резистентностью новообразования к фторурацилу. Однако в данном контексте уместно сделать несколько комментариев.
-
Уровень экспрессии TS может различаться в первичной неоплазме и метастазах. Следовательно, при планировании лечения распространённых форм опухолей желательно проводить анализ тканей, полученных непосредственно из метастатических очагов. Однако подобное требование сопряжено с необходимостью проведения дополнительных инвазивных вмешательств.
-
Уровень экспрессии TS может возрастать уже в процессе самого лечения фторпиримидинами.
-
Активация транскрипции гена TS может быть одним из механизмов приобретённой резистентности к фторурацилу.
-
Предиктивная значимость статуса TS зависит от множества обстоятельств клинического характера. Напимер, при метастатическом распространении онкологического процесса у пациентов с пониженным содержанием TS наблюдают возрастание положительного эффекта лечения фторпиримидинами, тогда как у пациентов, которые получают адъювантное лечение теми же препаратами, отмечают обратную закономерность. Подобное противоречие принято объяснять фундаментальными биологическими различиями между сформировавшимся макроскопическим очагом метастазы и единичными опухолевыми клетками. Избыток TS может быть компенсирован локальной доставкой цитостатика. В частности, при метастазах печени, экспрессирующих значительное количество TS, рекомендуют внутрипечёночную артериальную инфузию фторурацила.
-
От назначения фторпиримидинов в качестве монотерапии или в комбинации с другими цитостатиками зависит предиктивная значимость TS.
Данные, демонстрирующие корреляцию между низким содержанием фермента DPD и чувствительностью опухоли к лечению фторпиримидинами, имеют хорошую воспроизводимость. Экспрессия DPD может понижаться в процессе злокачественной трансформации, что создаёт определённое "терапевтическое окно" для действия фторурацила и его производных. Вопрос о предиктивной значимости уровня тимидин-фосфорилазы - комплексная проблема. Этот фермент не только участвует в метаболизме азотистых оснований ДНК, но и способствует процессам сосудообразования. Его экспрессия повышена в большинстве опухолей, причём высокая степень гиперэкспрессии тимидин-фосфорилазы коррелирует с плохим прогнозом для пациента. Однако повышение содержания тимидин-фосфорилазы в опухолевой ткани создаёт определённые преимущества для применения пероральных предшественников фторурацила (капецитабина и доксифлюридинаÃ), поскольку их активация происходит посредством упомянутого фермента. Таким образом, высокая внутриопухолевая активность тимидин-фосфорилазы может с одной стороны способствовать прогрессии онкологического заболевания, а с другой - избирательности действия пероральных форм фторпиримидинов. Помимо тимидин-фосфорилазы, в активации фторпиримидинов участвует фермент оротат-фософорибозил-трансфераза. Его внутриопухолевая активация также ассоциирована с хорошим лечебным эффектом фторурацила. Комплексность метаболизма фторурацила позволяет предположить, что положительный эффект применения фторурацила зависит не столько от активности какого-либо ключевого фермента, сколько от комбинации функциональных характеристик нескольких ферментативных каскадов.
Недавно стали известны результаты первого проспективного исследования, в котором выбор терапии первой линии при раке толстой кишки был основан на молекулярном анализе опухоли. Пациентам с низкой экспрессией TS и DPD назначали фторпиримидины, в то время как при повышении уровня одного из этих ферментов применяли комбинацию оксалиплатина и иринотекана. Частота объективного ответа в первой группе составила 35%, что примерно в 2 раза выше показателей, получаемых при обычном неселективном использовании фторурацила.
Гены репарации ДНК как маркёры ответа опухоли на производные платины и алкилирующие агенты
Основной механизм устранения дефектов ДНК, возникающих в результате воздействия производных платины - эксцизионная репарация. Ключевую роль в данном процессе отводят ферменту ERCC1. Многочисленные исследования демонстрируют взаимосвязь между низким уровнем экспрессии ERCC1 и ответом опухоли на цисплатин, карбоплатин или оксалиплатин. Подобная закономерность была отмечена для целого ряда карцином, включая новообразования пищевода, яичников, желудка, толстой кишки, лёгкого и др. Предварительные результаты проспективного клинического исследования указывают на целесообразность определения уровня ERCC1 для выбора между комбинациями доцетаксела с цисплатином и доцетаксела с гемцитабином при планировании лечения метастатического рака лёгкого.
Сходные рассуждения применимы в отношении фермента 6-O-метилгуанин-ДНК-метилтрансферазы (MGMT), котрый участвует в репарации алкилированной ДНК. Высокий уровень MGMT сопряжён с резистентностью опухоли к воздействию алкилирующих агентов (циклофосфамида, дакарбазина, темозоломида, производных нитрозомочевины), тогда как низкая активность фермента увеличивает вероятность ответа опухоли на лечение.
Чувствительность опухолей к препаратам антрациклинового ряда
Опубликовано много работ, посвящённых анализу молекулярных маркёров ответа опухоли на соединения группы антрациклинов. Все подобные работы посвящены лечению РМЖ, в то время как другие разновидности новообразований практически не изучали в данном контексте. Классический пример молекулярного предиктора чувствительности к антрациклинам - амплификация или гиперэкспрессия онкогена HER2. Биологический смысл подобной закономерности остаётся предметом для дискуссий. Наиболее вероятно объяснение, в соответствии с которым амплификация HER2 отражает увеличение числа копий соседнего гена - гена топоизомеразы II-a (TOP2A). TOP2A - основная молекулярная мишень антрациклинов. Таким образом, представляется вполне логичным предположение о предпочтительном ответе на лечение антрациклинами опухолей, чей патогенез предусматривает активацию TOP2A. TOP2A амплифицируется в новообразованиях молочной железы несколько реже, чем онкоген HER2, однако увеличение числа копий TOP2A в отсутствие активации HER2 выявляют довольно редко. Многочисленные исследования подтверждают взаимосвязь между амплификацией TOP2A и эффектом антрациклинов как при лечении метастатической формы заболевания, так и при адъювантной терапии. Аналогичные наблюдения опубликованы для другого ингибитора топоизомеразы - этопозида.
Молекулярные предикторы эффективности ингибиторов микротрубочек
В ряде исследований отмечают ассоциацию между гиперэкспрессией b-тубулина класса III и резистентностью опухолей к препаратам, воздействующим на микротрубочки. Клинические результаты согласуются с данными лабораторных экспериментов in vitro. Установлено, что увеличенное содержание b-тубулина класса III в опухолевой ткани оказывает негативное влияние на результаты лечения паклитакселом новообразований яичника и лёгкого. Сходная закономерность обнаружена для лечения опухолей молочной железы и желудка при помощи доцетаксела. Эффективность винорельбинаà при лечении немелкоклеточного рака лёгкого также выше, если опухоль содержит низкое количество b-тубулина класса III. Другой механизм резистентности карцином к лечению таксанами - увеличение содержания белка tau. Вероятно этот белок разрушает взаимодействие микротрубочек с доцетакселом или паклитакселом. Гиперэкспрессия фермента тиоредоксина также может быть негативным предиктором эффективности таксанов. Эти сведения были получены при изучении экспрессионных портретов опухолей молочной железы и впоследствии подтверждены иммуногистохимическими исследованиями патоморфологических препаратов.
Предиктивные маркёры применения таргетных препаратов
Многие таргетные препараты можно применять только при наличии в опухолевой ткани "мишени" для их действия.
-
Антиэстрогеновые препараты используют, если опухоль содержит достаточное количество рецепторов эстрогенов или прогестерона.
-
Трастузумаб применяют исключительно при амплификации или гиперэкспрессии онкогена HER2.
-
Ритуксимаб используют только для лечения лимфом, экспрессирующих антиген CD20.
-
Иматиниб включают в схему лечения при обнаружении химеры BCR-ABL или гиперэкспрессии онкогена KIT.
Однако использование других таргетных препаратов (например, новых ингибиторов ангиогенеза) пока не сопряжено с молекулярным анализом опухолевой ткани.
В большинстве случаев участие молекулярной мишени в патогенезе заболевания определяет предиктивное значение лабораторного теста. Классический пример - статус гормональных рецепторов при РМЖ. Многолетний опыт клинической практики показывает, что наибольший положительный эффект антиэстрогеновой терапии наблюдают при экспрессии опухолью и ER, и PR. Эффект трастузумаба в значительной степени зависит от уровня гиперэкспрессии онкогена HER2. Максимальный эффект лечения достигают при амплификации данного онкогена, поскольку это молекулярное событие сопряжено с наиболее стойкой активацией соответствующего рецептора. Предиктивная значимость статуса молекулы-мишени при назначении цетуксимаба остаётся под вопросом. Отбор пациентов на клинические испытания цетуксимаба ограничивался в основном теми больными, опухоли которых экспрессировали большое количество молекулярной мишени данного препарата - рецептора эпидермального фактора роста (EGFR). Однако дальнейший анализ результатов показал, что ответ опухоли на лечение не зависит от уровня EGFR и нередко его наблюдают даже в EGFR-негативных опухолях. Есть достаточно воспроизводимые данные, указывающие на предиктивную значимость не столько экспрессии EGFR, сколько его амплификации. Причины подобных противоречий остаются непонятными. Наиболее вероятное объяснение ("техническое") основывают на субъективности и недостаточной воспроизводимости иммуногистохимических методов оценки экспрессии EGFR.
Много вопросов возникло при использовании низкомолекулярного ингибитора тирозинкиназной активности EGFR - препарата гефитиниб. Первоначально предполагали, что внедрение данного препарата кардинально изменит стандарты лечения новообразований лёгкого. Это предположение было основано на сведениях о частой гиперэкспрессии EGFR в немелкоклеточных опухолях данной локализации. Первые клинические испытания (IDEAL: Iressa Dose Evaluation in Advanced Lung Cancer) проводили у пациентов с раком лёгкого (опухоли развили резистентность на фоне нескольких предшествующих линий химиотерапии). Полученные данные продемонстрировали обнадёживающие результаты: в подобной бесперспективной ситуации противоопухолевый эффект наблюдали у 9-19% пациентов, что существенно превышало возможности альтернативных методов лечения. По аналогии с исключительно успешными испытаниями герцептина на больных с опухолями молочной железы, ожидалось, что гефитиниб повысит эффективность лечения новообразований лёгкого при комбинированном применении с цитостатическими препаратами. Однако, масштабные клинические испытания фазы III (INTACT: Iressa Non-Small Cell Lung Cancer Trial Assessing Combination Treatment) полностью опровергли подобные надежды (выяснили, что эффект гефитиниба не отличался от такового при назначении плацебо). Хотя результаты программы INTACT часто цитировали как пример неудачи в разработке нового противоопухолевого препарата, не оставалось никаких сомнений, что в отдельных достаточно редких случаях гефитиниб демонстрировал чётко выраженный эффект. Загадка данного препарата была раскрыта в середине 2004 г., когда три исследовательских коллектива независимо друг от друга установили, что ответ опухолей лёгкого на применение препарата ассоциирован с присутствием небольшой мутации, расположенной внутри гена EGFR, в опухолевой ДНК. Сходная закономерность была установлена и для другого тирозинкиназного ингибитора EGFR - эрлотиниба.
Мутации EGFR, ассоциированные с высокой чувствительностью опухоли к гефитинибу, достаточно редки (выявляют в 10% опухолей лёгкого у лиц европеоидной расы, и в 25% - у выходцев из стран Азии). Последняя закономерность объясняет неожиданные разногласия в результатах первых клинических испытаний, которые показали большую эффективность гефитиниба в Японии, чем в США. Мутации EGFR проявляют выраженную гистологическую специфичность - их выявляют исключительно в аденокарциномах лёгкого (особенно в бронхиолоальвеолярных карциномах). В опухолях других локализаций данные повреждения структуры EGFR практически не обнаруживают. Спектр сенситизирующих мутаций EGFR достаточно консервативен, что позволяет рутинно использовать соответствующий тест в условиях клиники. Для выявления мутации можно применять относительно доступный метод аллель-специфической полимеразной цепной реакции (ПЦР). В качестве источника ДНК допустимо использовать не только свежеудалённую опухоль, но и архивный гистологический материал. Использование данного теста в НИИ онкологии им. проф. Петрова Н.Н. подтвердило основные закономерности, установленные в первых работах. Существенно, что практически во всех случаях при наличии мутации EGFR происходило быстрое симптоматическое улучшение после применения гефитиниба с последующим объективным ответом опухоли на длительное лечение данным препаратом.
В литературе часто цитируют работы, посвящённые клиническим испытаниям эрлотиниба, в которых была продемонстрирована решающая роль амплификации гена EGFR в формировании чувствительности к тирозинкиназным ингибиторам соответствующего рецептора.
-
Возрастание копийности гена EGFR в большинстве случаев сочетается с присутствием сенситизирующей мутации.
-
В работе Тсао (2005) учитывали не только консервативные изменения нуклеотидной последовательности, ассоциированные с чувствительностью к гефитинибу и эрлотинибу, но и все остальные, вероятно клинически-индифферентные генетические повреждения.
Идентификация мутаций, сенситизирующих новообразования лёгкого к действию ингибиторов тирозинкиназ, может принципиально изменить стратегию разработки новых таргетных препаратов. Длительное время в качестве предпочтительных опухолевых мишеней рассматривали молекулы, которые экспрессируются в больших количествах на клетках опухоли по сравнению с нормальными тканями. Развитию такого подхода отчасти способствовал значительный прогресс в области разработки методов систематического изучения экспрессии генов, в частности так называемых микрочиповых технологий, которые позволяют получить индивидуальный РНК-профиль практически для каждой опухоли. Клинический опыт первых лет XXI в. показывает, что мутированные онкобелки могут оказаться более предпочтительными мишенями по сравнению с молекулами, которые в процессе канцерогенеза претерпевают только изменения в степени экспрессии. В качестве примера (помимо ингибиторов EGFR) можно привести препарат иматиниб, действие которого также ассоциировано с мутантной тирозинкиназой. Не исключено, что "история" с гефитинибом повлияет на направление фундаментальных исследований в онкологии. Если до раньще многие коллективы учёных делали акцент на сопоставлении транскрипционных портретов опухолей и нормальных тканей, то в настоящее время всё больше внимания уделяют работам по систематическому поиску интрагенных мутаций. Однако выполнение подобных проектов сопряжено с методическими трудностями, поскольку технологии обнаружения новых мутаций пока отстают от поставленных задач.
Помимо статуса мишени как таковой, ответ на лечение таргетными препаратами может быть опосредован другими молекулярными характеристиками опухоли. Например, гиперэкспрессия онкогена HER2 ассоциирована с пониженным эффектом антиэстрогеновой терапии даже в тех новообразованиях молочной железы, которые имеют высокую представленность рецепторов эстрогенов и прогестерона. Один из наиболее явных примеров индивидуальных различий в ответе на таргетные препараты в зависимости от статуса молекул-модификаторов был продемонстрирован совсем недавно. На некоторые опухоли молочной железы тамоксифен производит парадоксальный эффект - до 15% ER-позитивных новообразований реагируют на назначение тамоксифена не замедлением роста, а ускоренным делением трансформированных клеток. В исследовании Jirstrom (2005) было показано, что негативный эффект тамоксифена на течение РМЖ строго коррелирует с наличием амплификации онкогена cyclin D1. Данное открытие может привести к коренному пересмотру стандартов назначения упомянутого препарата. Не вызывает сомнения, что пациентки с увеличенной копийностью гена cyclin D1 должны получать в качестве гормональной терапии антиэстрогеновые препараты альтернативного механизма действия (например, ингибиторы ароматазы) или полностью воздерживаться от применения антагонистов эстрогенового сигнального каскада.
Заключение
Индивидуализация противоопухолевой терапии на основе молекулярных маркёров - не панацея. Низкая эффективность лекарственного лечения опухолей связана не столько с проблемой выбора соответствующих препаратов, сколько с трудностями в разработке истинно селективных агентов. В отличие от ситуации с антибактериальной терапией (существуют значительные биохимические отличия между клетками микро- и макроорганизма), при поиске мишеней для лечения опухолей возникают большие трудности, поскольку злокачественные новообразования практически по всем ключевым параметрам сохраняют молекулярные характеристики нормальных тканей. Однако первые попытки применения молекулярных тестов в химиотерапии опухолей уже показали перспективность подобного подхода как для улучшения результатов лечения, так и для повышения экономической эффективности использования дорогостоящих лекарственных препаратов.
Литература
Adlard J.W., Richman S.D., Seymour M.T., Quirke P. Prediction of the response of colorectal cancer to systemic therapy // Lancet Oncol. - 2002. - Vol. 3. - P. 75-82.
Aschele C., Lonardi S., Monfardini S. Thymidylate Synthase expression as a predictor of clinical response to fluoropyrimidine-based chemotherapy in advanced colorectal cancer // Cancer Treat Rev. - 2002. - Vol. 28. - P. 27-47.
Beutler E., Gelbart T., Demina A. Racial variability in the UDP-glucuronosyltransferase 1 (UGT1A1) promoter: a balanced polymorphism for regulation of bilirubin metabolism // Proc Natl Acad Sci U S A. - 1998. - Vol. 95. - P. 8170-8174.
Braybrooke J.P., Levitt N.C., Joel S. et al. Pharmacokinetic study of cisplatin and infusional etoposide phosphate in advanced breast cancer with correlation of response to topoisomerase II alpha expression // Clin Cancer Res. - 2003. - Vol. 9. - P. 4682-4688.
Burton, A. What went wrong with Iressa // Lancet Oncol. - 2002. - Vol. 3. - P. 708.
Cappuzzo F., Varella-Garcia M., Shigematsu H. et al. Increased HER2 gene copy number is associated with response to gefitinib therapy in epidermal growth factor receptor-positive non-small-cell lung cancer patients // J Clin Oncol. - 2005. - Vol. 23. - P. 5007-5018.
Chabner B.A., Roberts T.G. Timeline: Chemotherapy and the war on cancer // Nat Rev Cancer. - 2005. - Vol. 5. - P. 65-72.
Chan S.K., Gullick W.J., Hill M.E. Mutations of the epidermal growth factor receptor in non-small cell lung cancer - search and destroy. Eur J Cancer. - 2006. - Vol. 42. - P. 17-23.
Chiusolo P., Reddiconto G., Casorelli I. et al. Preponderance of methylenetetrahydrofolate reductase C677T homozygosity among leukemia patients intolerant to methotrexate // Ann Oncol. - 2002. - Vol. 13. - P. 1915-1918.
Chung K.Y., Shia J., Kemeny N.E. et al. Cetuximab shows activity in colorectal cancer patients with tumors that do not express the epidermal growth factor receptor by immunohistochemistry // J Clin Onco. - 2005. - Vol. 23. - P. 1803-1810.
Ciardiello F., De Vita F., Orditura M., Tortora G. The role of EGFR inhibitors in nonsmall cell lung cancer // Curr. Opin. Oncol. - 2004. - Vol. 16. - P. 130-135.
Ciccolini J., Evrard A., Cuq P. Thymidine phosphorylase and fluoropyrimidines efficacy: a Jekyll and Hyde story // Curr Med Chem Anticancer Agents. - 2004. - Vol. 4. - P. 71-81.
Cohen V., Panet-Raymond V., Sabbaghian N. et al. Methylenetetrahydrofolate reductase polymorphism in advanced colorectal cancer:a novel genomic predictor of clinical response to fluoropyrimidine-based chemotherapy // Clin Cancer Res. - 2003. - Vol. 9. - P. 1611-1615.
Coon J.S., Marcus E., Gupta-Burt S. et al. Amplification and overexpression of topoisomerase IIalpha predict response to anthracycline-based therapy in locally advanced breast cancer // Clin Cancer Res. - 2002. - Vol. 8. - P. 1061-1067.
Dabholkar M., Vionnet J., Bostick-Bruton F. et al. Messenger RNA levels of XPAC and ERCC1 in ovarian cancer tissue correlate with response to platinum-based chemotherapy // J Clin Invest. - 1994. - Vol. 94. - P. 703-708.
De Laurentiis M., Arpino G., Massarelli E. et al. A meta-analysis on the interaction between HER-2 expression and response to endocrine treatment in advanced breast cancer // Clin Cancer Res. - 2005. - Vol. 11. - P. 4741-4748.
Dervieux T., Meshkin B., Neri B. Pharmacogenetic testing: proofs of principle and pharmacoeconomic implications // Mutat Res. - 2005. - Vol. 573. - P. 180-194.
Desai A.A., Innocenti F., Ratain M.J. Pharmacogenomics: road to anticancer therapeutics nirvana? // Oncogene. - 2003. - Vol. 22. - P. 6621-6628.
Di Leo A., Gancberg D., Larsimont D. et al. HER-2 amplification and topoisomerase IIalpha gene aberrations as predictive markers in node-positive breast cancer patients randomly treated either with an anthracycline-based therapy or with cyclophosphamide, methotrexate, and 5-fluorouracil // Clin Cancer Res. - 2002. - Vol. 8. - P. 1107-1116.
Di Leo A., Cardoso F., Durbecq V. et al. Predictive molecular markers in the adjuvant therapy of breast cancer: state of the art in the year 2002 // Int J Clin Oncol. - 2002. - Vol. 7. - P. 245-253.
Doan T., Massarotti E. Rituximab // Drugs Today (Barc). - 2005. - Vol. 41. - P. 785-797.
Dotor E., Cuatrecases M., Martinez-Iniesta M. et al. Tumor thymidylate synthase 1494del6 genotype as a prognostic factor in colorectal cancer patients receiving fluorouracil-based adjuvant treatment // J Clin Oncol. - 2006. - Vol. 24. - P. 1603-1611.
Druker B.J. Imatinib as a paradigm of targeted therapies // Adv Cancer Res. - 2004. - Vol. 91. - P. 1-30.
Duffy M.J. Predictive markers in breast and other cancers: a review // Clin Chem. - 2005. - Vol. 51. - P. 494-503.
Etienne M.C., Chazal M., Laurent-Puig P. et al. Prognostic value of tumoral thymidylate synthase and p53 in metastatic colorectal cancer patients receiving fluorouracil-based chemotherapy: phenotypic and genotypic analyses // J Clin Oncol. - 2002. - Vol. 20. - P. 2832-2843.
Ferrandina G., Zannoni G.F., Martinelli E. et al. Class III beta-tubulin overexpression is a marker of poor clinical outcome in advanced ovarian cancer patients // Clin Cancer Res. - 2006. - Vol. 12. - P. 2774-2779.
Formentini A., Henne-Bruns D., Kornmann M. Thymidylate synthase expression and prognosis of patients with gastrointestinal cancers receiving adjuvant chemotherapy: a review // Langenbecks Arch Surg. - 2004. - Vol. 389. - P. 405-413.
Giaccone G., Rodriguez J.A. EGFR inhibitors: what have we learned from the treatment of lung cancer? // Nat Clin Pract Oncol. - 2005. - Vol. 2. - P. 554-561.
Gonen M., Hummer A., Zervoudakis A. et al. Thymidylate synthase expression in hepatic tumors is a predictor of survival and progression in patients with resectable metastatic colorectal cancer // J Clin Oncol. - 2003. - Vol. 21. - P. 406-412.
Guilhot F. Indications for imatinib mesylate therapy and clinical management // Oncologist. - 2004. - Vol. 9. - P. 271-281.
Hasegawa S., Miyoshi Y., Egawa C. et al. Prediction of response to docetaxel by quantitative analysis of class I and III beta-tubulin isotype mRNA expression in human breast cancers // Clin Cancer Res. - 2003. - Vol. 9. - P. 2992-2997.
Heinrich M.C., Corless C.L., Demetri G.D. et al. Kinase mutations and imatinib response in patients with metastatic gastrointestinal stromal tumor // J Clin Oncol. - 2003. - Vol. 21. - P. 4342-4349.
Imyanitov E.N., Kuligina E.S., Belogubova E.V. et al. Mechanisms of lung cancer // Drug Discov. Today: Dis. Mech. - 2005. - Vol. 2. - P. 213-223.
Ichikawa W., Uetake H., Shirota Y. et al. Both gene expression for orotate phosphoribosyltransferase and its ratio to dihydropyrimidine dehydrogenase influence outcome following fluoropyrimidine-based chemotherapy for metastatic colorectal cancer // Br J Cancer. - 2003. - Vol. 89. - P. 1486-1492.
Ichikawa W., Takahashi T., Suto K. et al. Thymidylate synthase predictive power is overcome by irinotecan combination therapy with S-1 for gastric cancer // Br J Cancer. - 2004. - Vol. 91. - P. 1245-1250.
Innocenti F., Ratain M.J. Update on pharmacogenetics in cancer chemotherapy // Eur J Cancer. - 2002. - Vol. 38. - P. 639-644.
Innocenti F, Ratain M.J. "Irinogenetics" and UGT1A: from genotypes to haplotypes // Clin Pharmacol Ther. - 2004. - Vol. 75. - P. 495-500.
Innocenti F., Undevia S.D., Iyer L. et al. Genetic variants in the UDP-glucuronosyltransferase 1A1 gene predict the risk of severe neutropenia of irinotecan // J Clin Oncol. - 2004. - Vol. 22. - P. 382-388.
Innocenti F., Vokes E.E., Ratain M.J. Irinogenetics: what is the right star? J Clin Oncol. - 2006. - Vol. 24. - P. 2221-2224.
Iwao-Koizumi K., Matoba R., Ueno N. et al. Prediction of docetaxel response in human breast cancer by gene expression profiling // J Clin Oncol. - 2005. - Vol. 23. - P. 422-431.
Jakobsen A., Nielsen J.N., Gyldenkerne N., Lindeberg J. Thymidylate synthase and methylenetetrahydrofolate reductase gene polymorphism in normal tissue as predictors of fluorouracil sensitivity // J Clin Oncol. - 2005. - Vol. 23. - P. 1365-1369.
Jirstrom K., Stendahl M., Ryden L. et al. Adverse effect of adjuvant tamoxifen in premenopausal breast cancer with cyclin D1 gene amplification // Cancer Res. - 2005. - Vol. 65. - P. 8009-8016.
Joshi M.B., Shirota Y., Danenberg K.D. et al. High gene expression of TS1, GSTP1, and ERCC1 are risk factors for survival in patients treated with trimodality therapy for esophageal cancer // Clin Cancer Res. - 2005. - Vol. 11. - P. 2215-2221.
Kamath K., Wilson L., Cabral F., Jordan M.A. BetaIII-tubulin induces paclitaxel resistance in association with reduced effects on microtubule dynamic instability // J Biol Chem. - 2005. - Vol. 280. - P. 12902-12907.
Kawakami K., Graziano F., Watanabe G. et al. Prognostic role of thymidylate synthase polymorphisms in gastric cancer patients treated with surgery and adjuvant chemotherapy // Clin Cancer Res. - 2005. - Vol. 11. - P. 3778-3783.
Kaye F.J. A curious link between epidermal growth factor receptor amplification and survival: effect of "allele dilution" on gefitinib sensitivity // J. Natl. Cancer Inst. - 2005. - Vol. 97. - P. 621-623.
Kidd E.A., Yu J., Li X. et al. Variance in the expression of 5-Fluorouracil pathway genes in colorectal cancer // Clin Cancer Res. - 2005. - Vol. 11. - P. 2612-2619.
Kim S.J., Miyoshi Y., Taguchi T. High thioredoxin expression is associated with resistance to docetaxel in primary breast cancer // Clin Cancer Res. - 2005. - Vol. 11. - P. 8425-8430.
Knoop A.S., Knudsen H., Balslev E. et al. Retrospective analysis of topoisomerase IIa amplifications and deletions as predictive markers in primary breast cancer patients randomly assigned to cyclophosphamide, methotrexate, and fluorouracil or cyclophosphamide, epirubicin, and fluorouracil: Danish Breast Cancer Cooperative Group // J Clin Oncol. - 2005. - Vol. 23. - P. 7483-7490.
Lecomte T., Ferraz J.M., Zinzindohoue F. et al. Thymidylate synthase gene polymorphism predicts toxicity in colorectal cancer patients receiving 5-fluorouracil-based chemotherapy // Clin Cancer Res. - 2004. - Vol. 10. - P. 5880-5888.
Leo A., Cardoso F., Durbecq V. et al. Predictive molecular markers in the adjuvant therapy of breast cancer: state of the art in the year 2002 // Int J Clin Oncol. - 2002. - Vol. 7. - P. 245-253.
Libra M., Navolanic P.M., Talamini R. Thymidylate synthetase mRNA levels are increased in liver metastases of colorectal cancer patients resistant to fluoropyrimidine-based chemotherapy // BMC Cancer. - 2004. - Vol. 4. - P. 11.
Lievre A., Bachet J.B., Le Corre D. et al. KRAS mutation status is predictive of response to cetuximab therapy in colorectal cancer // Cancer Res. - 2006. - Vol. 66. - P. 3992-3995.
Liu L., Gerson S.L. Targeted modulation of MGMT: clinical implications // Clin Cancer Res. - 2006. - Vol. 12. - P. 328-331.
Longley D.B., Harkin D.P., Johnston P.G. 5-fluorouracil: mechanisms of action and clinical strategies // Nat Rev Cancer. - 2003. - Vol. 3. - P. 330-338.
Lord R.V., Brabender J., Gandara D. Low ERCC1 expression correlates with prolonged survival after cisplatin plus gemcitabine chemotherapy in non-small cell lung cancer // Clin Cancer Res. - 2002. - Vol. 8. - P. 2286-2291.
Lynch T.J., Bell D.W., Sordella R. et al. Activating mutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer to gefitinib // N. Engl. J. Med. - 2004. - Vol. 350. - P. 2129-2139.
Ma S., Egyhazi S., Ueno T. et al. O6-methylguanine-DNA-methyltransferase expression and gene polymorphisms in relation to chemotherapeutic response in metastatic melanoma // Br J Cancer. - 2003. - Vol. 89. - P. 1517-1523.
MacGrogan G., Rudolph P., Mascarel Id. I et al. DNA topoisomerase IIalpha expression and the response to primary chemotherapy in breast cancer // Br J Cancer. - 2003. - Vol. 89. - P. 666-671.
Mandola M.V., Stoehlmacher J., Muller-Weeks S. et al. A novel single nucleotide polymorphism within the 5' tandem repeat polymorphism of the thymidylate synthase gene abolishes USF-1 binding and alters transcriptional activity // Cancer Res. - 2003. - Vol. 63. - P. 2898-2904.
Mandola M.V., Stoehlmacher J., Zhang W. et al. A 6 bp polymorphism in the thymidylate synthase gene causes message instability and is associated with decreased intratumoral TS mRNA levels // Pharmacogenetics. - 2004. - Vol. 14. - P. 319-327.
Marcuello E., Altes A., Menoyo A. et al. UGT1A1 gene variations and irinotecan treatment in patients with metastatic colorectal cancer // Br J Cancer. - 2004. - Vol. 91. - P. 678-682.
Marcuello E., Altes A., Del Rio E. et al. Single nucleotide polymorphism in the 5' tandem repeat sequences of thymidylate synthase gene predicts for response to fluorouracil-based chemotherapy in advanced colorectal cancer patients // Int J Cancer. - 2004. - Vol. 112. - P. 733-737.
Marsh S., McLeod H.L. Cancer pharmacogenetics // Br J Cancer. - 2004. - Vol. 90. - P. 8-11.
Marsh S. Thymidylate synthase pharmacogenetics // Invest New Drugs. - 2005. - Vol. 23. - P. 533-537.
Massacesi C., Terrazzino S., Marcucci F. et al. Uridine diphosphate glucuronosyl transferase 1A1 promoter polymorphism predicts the risk of gastrointestinal toxicity and fatigue induced by irinotecan-based chemotherapy // Cancer. - 2006. - Vol. 106. - P. 1007-1016.
McLeod H.L., Yu J. Cancer pharmacogenomics: SNPs, chips, and the individual patient // Cancer Invest. - 2003. - Vol. 21. - P. 630-640.
Metzger R., Leichman C.G., Danenberg K.D. et al. ERCC1 mRNA levels complement thymidylate synthase mRNA levels in predicting response and survival for gastric cancer patients receiving combination cisplatin and fluorouracil chemotherapy // J Clin Oncol. - 1998. - Vol. 16. - P. 309-316.
Molina R., Barak V., Van Dalen A. et al. Tumor markers in breast cancer- European Group on Tumor Markers recommendations // Tumour Biol. - 2005. - Vol. 26. - P. 281-293.
Monaghan G., Ryan M., Seddon R. et al. Genetic variation in bilirubin UPD-glucuronosyltransferase gene promoter and Gilbert’s syndrome // Lancet. - 1996. - Vol. 347. - P. 578-581.
Morganti M., Ciantelli M., Giglioni B. et al. Relationships between promoter polymorphisms in the thymidylate synthase gene and mRNA levels in colorectal cancers // Eur J Cancer. - 2005. - Vol. 41. - P. 2176-2183.
Moroni M., Veronese S., Benvenuti S. et al. Gene copy number for epidermal growth factor receptor (EGFR) and clinical response to antiEGFR treatment in colorectal cancer: a cohort study // Lancet Oncol. - 2005. - Vol. 6. - P. 279-286.
Mozzetti S., Ferlini C., Concolino P. et al. Class III beta-tubulin overexpression is a prominent mechanism of paclitaxel resistance in ovarian cancer patients // Clin Cancer Res. - 2005. - Vol. 11. - P. 298-305.
Ochiai T., Nishimura K., Noguchi H. et al. Prognostic impact of orotate phosphoribosyl transferase among 5-fluorouracil metabolic enzymes in resectable colorectal cancers treated by oral 5-fluorouracil-based adjuvant chemotherapy // Int J Cancer. - 2006. - Vol. 118. - P. 3084-3088.
Ohno T., Hiraga J., Ohashi H. et al. Loss of O6-methylguanine-DNA methyltransferase protein expression is a favorable prognostic marker in diffuse large B-cell lymphoma // Int J Hematol. - 2006. - Vol. 83. - P. 341-347.
Omura K. Clinical implications of dihydropyrimidine dehydrogenase (DPD) activity in 5-FU-based chemotherapy: mutations in the DPD gene, and DPD inhibitory fluoropyrimidines // Int J Clin Oncol. - 2003. - Vol. 8. - P. 132-138.
Paez J.G., Janne P.A., Lee J.C. et al. EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy // Science. - 2004. - Vol. 304. - P. 1497-1500.
Pao W., Miller V., Zakowski M. et al. EGF receptor gene mutations are common in lung cancers from "never smokers" and are associated with sensitivity of tumors to gefitinib and erlotinib // Proc. Natl. Acad. Sci. USA. - 2004. - Vol. 101. - P. 13306-13311.
Park K., Kim J., Lim S., Han S. Topoisomerase II-alpha (topoII) and HER2 amplification in breast cancers and response to preoperative doxorubicin chemotherapy // Eur J Cancer. - 2003. - Vol. 39. - P. 631-634.
Piccart-Gebhart M.J. Anthracyclines and the tailoring of treatment for early breast cancer // N Engl J Med. - 2006. - Vol. 354. - P. 2177-2179.
Pollack I.F., Hamilton R.L., Sobol R.W. et al. O6-methylguanine-DNA methyltransferase expression strongly correlates with outcome in childhood malignant gliomas: results from the CCG-945 Cohort // J Clin Oncol. - 2006. - Vol. 24. - P. 3431-3437.
Pusztai L., Rouzier R., Wagner P., Symmans W.F. Individualized chemotherapy treatment for breast cancer: is it necessary? Is it feasible? // Drug Resist Updat. - 2004. - Vol. 7. - P. 325-331.
Relling M.V., Hancock M.L., Boyett J.M. et al. Prognostic importance of 6-mercaptopurine dose intensity in acute lymphoblastic leukemia // Blood. - 1999. - Vol. 93. - P. 2817-23.
Robert J., Vekris A., Pourquier P., Bonnet J. Predicting drug response based on gene expression // Crit Rev Oncol Hematol. - 2004. - Vol. 51. - P. 205-227.
Robert J., Morvan V.L., Smith D. et al. Predicting drug response and toxicity based on gene polymorphisms // Crit Rev Oncol Hematol. - 2005. - Vol. 54. - P. 171-196.
Rosell R., Cobo M., Isla D. et al. Applications of genomics in NSCLC // Lung Cancer. - 2005. - Vol. 50. - P. 33-40.
Ross J.S., Fletcher J.A., Linette G.P. et al. The Her-2/neu gene and protein in breast cancer 2003: biomarker and target of therapy // Oncologist. - 2003. - Vol. 8. - P. 307-325.
Rouits E., Boisdron-Celle M., Dumont A. et al. Relevance of different UGT1A1 polymorphisms in irinotecan-induced toxicity: a molecular and clinical study of 75 patients // Clin Cancer Res. - 2004. - Vol. 10. - P. 5151-5159.
Rouzier R., Rajan R., Wagner P. et al. Microtubule-associated protein tau: a marker of paclitaxel sensitivity in breast cancer // Proc Natl Acad Sci U S A. - 2005. - Vol. 102. - P. 8315-8320.
Salonga D., Danenberg K.D., Johnson M. et al. Colorectal tumors responding to 5-fluorouracil have low gene expression levels of dihydropyrimidine dehydrogenase, thymidylate synthase, and thymidine phosphorylase // Clin Cancer Res. - 2000. - Vol. 6. - P. 1322-1327.
Seve P., Isaac S., Tredan O. et al. Expression of class III beta-tubulin is predictive of patient outcome in patients with non-small cell lung cancer receiving vinorelbine-based chemotherapy // Clin Cancer Res. - 2005. - Vol. 11. - P. 5481-5486.
Seve P., Mackey J., Isaac S. et al. Class III beta-tubulin expression in tumor cells predicts response and outcome in patients with non-small cell lung cancer receiving paclitaxel // Mol Cancer Ther. - 2005. - Vol. 4. - P. 2001-2007.
Shigematsu H., Lin L., Takahashi T. et al. Clinical and biological features associated with epidermal growth factor receptor gene mutations in lung cancers // J. Natl. Cancer Inst. - 2005. - Vol. 97 - P. 339-346.
Shirota Y., Stoehlmacher J., Brabender J. ERCC1 and thymidylate synthase mRNA levels predict survival for colorectal cancer patients receiving combination oxaliplatin and fluorouracil chemotherapy // J Clin Oncol. - 2001. - Vol. 19. - P. 4298-4304.
Smorenburg C.H., Peters G.J., Van Groeningen C.J. et al. Phase II study of tailored chemotherapy for advanced colorectal cancer with either 5-fluouracil and leucovorin or oxaliplatin and irinotecan based on the expression of thymidylate synthase and dihydropyrimidine dehydrogenase // Ann Oncol. - 2006. - Vol. 17. - P. 35-42.
Stohlmacher J. Pharmacogenetics in gastrointestinal tumors // Onkologie. - 2005. - Vol. 28. - P. 435-440.
Tai H.L., Fessing M.Y., Bonten E.J. et al. Enhanced proteasomal degradation of mutant human thiopurine S-methyltransferase (TPMT) in mammalian cells: mechanism for TPMT protein deficiency inherited by TPMT*2, TPMT*3A, TPMT*3B or TPMT*3C // Pharmacogenetics. - 1999. - Vol. 9. - P. 641-650.
Takano T., Ohe Y., Sakamoto H. et al. Epidermal growth factor receptor gene mutations and increased copy numbers predict gefitinib sensitivity in patients with recurrent non-small-cell lung cancer // J Clin Oncol. - 2005. - Vol. 23. - P. 6829-6837.
Toffoli G., Veronesi A., Boiocchi M., Crivellari D. MTHFR gene polymorphism and severe toxicity during adjuvant treatment of early breast cancer with cyclophosphamide, methotrexate, and fluorouracil (CMF) // Ann Oncol. - 2000. - Vol. 11. - P. 373-374.
Toffoli G., Russo A., Innocenti F. et al. Effect of methylenetetrahydrofolate reductase 677C-→T polymorphism on toxicity and homocysteine plasma level after chronic methotrexate treatment of ovarian cancer patients // Int J Cancer. - 2003. - Vol. 103. - P. 294-299.
Toi M., Atiqur Rahman M., Bando H., Chow L.W. Thymidine phosphorylase (platelet-derived endothelial-cell growth factor) in cancer biology and treatment // Lancet Oncol. - 2005. - Vol. 6. - P. 158-166.
Tanner M., Isola J., Wiklund T. et al. Topoisomerase IIalpha gene amplification predicts favorable treatment response to tailored and dose-escalated anthracycline-based adjuvant chemotherapy in HER-2/neu-amplified breast cancer: Scandinavian Breast Group Trial 9401 // J Clin Oncol. - 2006. - Vol. 24. - P. 2428-2436.
Tsao M.S., Sakurada A., Cutz J.C. et al. Erlotinib in lung cancer - molecular and clinical predictors of outcome // N. Engl. J. Med. -., 2005. - Vol. 353. - P. 133-144.
Tsuji T., Hidaka S., Sawai T. et al. Polymorphism in the thymidylate synthase promoter enhancer region is not an efficacious marker for tumor sensitivity to 5-fluorouracil-based oral adjuvant chemotherapy in colorectal cancer // Clin Cancer Res. - 2003. - Vol. 9. - P. 3700-3704.
Ulrich C.M., Bigler J., Velicer C.M. et al. Searching expressed sequence tag databases: discovery and confirmation of a common polymorphism in the thymidylate synthase gene // Cancer Epidemiol Biomarkers Prev. - 2000. - Vol. 9. - P. 1381-1385.
Ulrich C.M., Yasui Y., Storb R. et al. Pharmacogenetics of methotrexate: toxicity among marrow transplantation patients varies with the methylenetetrahydrofolate reductase C677T polymorphism // Blood. - 2001. - Vol. 98. - P. 231-234.
Urano N., Fujiwara Y., Doki Y. et al. Clinical significance of class III beta-tubulin expression and its predictive value for resistance to docetaxel-based chemotherapy in gastric cancer // Int J Oncol. - 2006. - Vol. 28. - P. 375-381.
Van Kuilenburg A.B. Dihydropyrimidine dehydrogenase and the efficacy and toxicity of 5-fluorouracil // Eur J Cancer. - 2004. - Vol. 40. - P. 939-950.
Vincenzi B., Cesa A.L., Santini D. et al. Predictive factors for response to chemotherapy in colorectal cancer patients // Crit Rev Oncol Hematol. - 2004. - Vol. 52. - P. 45-60.
Walgren R.A., Meucci M.A., McLeod H.L. Pharmacogenomic discovery approaches: will the real genes please stand up? // J Clin Oncol. - 2005. - Vol. 23. - P. 7342-7349.
Warnecke-Eberz U., Metzger R., Miyazono F et al. High specificity of quantitative excision repair cross-complementing 1 messenger RNA expression for prediction of minor histopathological response to neoadjuvant radiochemotherapy in esophageal cancer // Clin Cancer Res. - 2004. - Vol. 10. - P. 3794-3799.
Watters J.W., McLeod H.L. Cancer pharmacogenomics: current and future applications // Biochim Biophys Acta. - 2003. - Vol. 1603. - P. 99-111.
I. ЦИТОТОКСИЧЕСКИЕ СРЕДСТВА
Алкилирующие соединения
Производные хлорэтиламина
Ифосфамид (Ifosfamide)
Фармакологический/химический класс АТХ
N, 3-бис(2-хлорэтил)тетрагидро-2Н-1, 3, 2-оксазафосфорин-2-амин-2-оксид.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Ифосфамид - алкилирующее лекарственное средство из группы азотистого иприта. Активированные метаболиты ифосфамида связываются со многими внутриклеточными молекулярными структурами, включая нуклеиновые кислоты. Цитотоксическое действие обусловлено образованием поперечных сшивок между нитями ДНК и РНК, а также ингибированием синтеза белка.
Фармакокинетика
После внутривенного введения активное вещество (основное пролекарство) метаболизируется в фармакологически активный метаболит 4-гидрооксиифосфамид, в ограниченной степени проникающий через гематоэнцефалический барьер. Биотрансформация происходит в печени (включая начальную активацию и последующий распад). Период полувыведения 7-15 ч. Выводится почками 70-86% (61% дозы в неизменённом виде).
Показания к применению и дозирование
Герминогенные опухоли, рак яичников, рак лёгкого, саркомы мягких тканей, РМЖ, рак поджелудочной железы, РШМ, остеогенные саркомы, саркома Юинга, неходжкинские лимфомы.
Режим дозирования: препарат применяют только внутривенно по 3,5-5 г/м2 1 раз в 3 нед или по 1,2-2 г/м2 в течение 3-5 дней каждые 3 нед или по 10 г/м2 1 раз в 3-4 нед.
Побочные эффекты
Система кроветворения: лейкопения, нейтропения, анемия, тромбоцитопения.
Пищеварительная система: тошнота, рвота; анорексия; редко - стоматит, фарингит, нарушение функции печени в виде повышения активности АЛТ и АСТ и/или уровня билирубина в сыворотке.
Мочевыделительная система: геморрагический цистит; дизурия (частое мочеиспускание); нарушение функций почек (повышение уровня креатинина и мочевины в сыворотке, снижение клиренса креатинина); протеинурия; метаболический ацидоз.
Нервная система: дезориентация, спутанность сознания, галлюцинации, повышенная утомляемость, ажитация, энцефалопатия, головокружение, сенсорная или моторная полиневропатия.
Прочие: кардиотоксическое действие, иммуносупрессия, инфекционные осложнения, кашель и одышка, лихорадка, аллергические реакции.
Передозировка
Симптомы: более быстрое развитие и резкая выраженность основных побочных эффектов (наиболее опасный - геморрагический цистит).
Лечение симптоматическое, с обязательным использованием антидота - месны.
Противопоказания
Повышенная чувствительность к ифосфамиду, тяжёлое угнетение функции костного мозга, выраженные нарушения функций почек, обструкция мочевыводящих путей, цистит, беременность и кормление грудью.
С осторожностью лекарственное средство применяют при гипопротеинемии (гипоальбуминемии), нарушении электролитного баланса, иммуносупрессии, хронической печёночной недостаточности, ветряной оспе (в том числе при недавнем контакте с больными), герпетической инфекции, в пожилом возрасте.
Беременность
Применение препарата в период беременности противопоказано.
В период лечение ифосфамидом рекомендуют использовать противозачаточные средства.
Кормление грудью
Ифосфамид проникает в грудное молоко. Во время проведения химиотерапии грудное вскармливание не рекомендуют из-за возможного риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Лекарственные средства, оказывающие миелотоксическое, нейротоксическое и нефротоксическое действие, - усиление побочных эффектов ифосфамида.
Индукторы микросомальных ферментов печени - повышенное образование алкилирующих метаболитов ифосфамида.
Противодиабетические лекарственные средства - усиление гипогликемического эффекта.
Аллопуринол - усиление миелосупрессии.
Месна - снижение нефротоксичности.
Варфарин - снижение свёртываемости крови и увеличение риска кровотечения.
Резюме и дополнительные сведения
Больным, получающим ифосфамид, необходимо наблюдение врача, имеющего опыт проведения химиотерапии.
Дозу лекарственного средства подбирают с учётом индивидуальных особенностей больного, клинической эффективности ифосфамида, возникновения и выраженности побочных эффектов.
До назначения ифосфамида и в течение по крайней мере 72 ч после его применения с целью снижения риска развития геморрагического цистита необходимо обеспечить поступление адекватного количества жидкости в организм и поддерживать достаточный диурез. С целью профилактики геморрагического цистита также проводят одновременное введение месны. Кроме того, для предотвращения длительного контакта метаболитов ифосфамида (оказывающих раздражающее действие) со слизистой оболочкой мочевого пузыря больному следует чаще опорожнять мочевой пузырь.
В случае слабовыраженного раздражения слизистой оболочки мочевого пузыря (микрогематурия) необходимо скорректировать дозу месны. Несмотря на то что при одновременном применении месны риск развития геморрагического цистита значительно ниже, при первых признаках возникновения данного побочного эффекта применение ифосфамида следует прекратить.
Последующую дозу ифосфамида необходимо вводить только после прекращения микрогематурии (в поле зрения микроскопа с высоким разрешением >10 эритроцитов).
При выраженных побочных эффектах со стороны ЦНС применение ифосфамида необходимо прекратить.
При возникновении значительной лейкопении (в частности, гранулоцитопении) или тромбоцитопении применение ифосфамида следует отменить до восстановления числа лейкоцитов и тромбоцитов до допустимых значений.
Код АТХ
L01AA06
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования ифосфамида: Холоксанª /Holoxan/ (Германия).
Формы выпуска:
Упаковка и хранение
Хранить при температуре <40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе.
Мелфалан (Melphalan)
Фармакологический/химический класс АТХ
D, L-а-Амино-b-[пара-бис-(b -хлорэтил)-аминофенил] -пропионовой кислоты гидрохлорид.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Мелфалан - алкилирующий препарат группы азотистого иприта. Данное лекарственное средство циклонеспецифично, его относят к бифункциональным алкилирующим соединениям. Активность мелфалана связана с образованием нестабильного этилениммониевого иона, алкилирующего многие внутриклеточные молекулярные структуры, включая нуклеиновые кислоты. Цитотоксическое действие лекарственного средства обусловлено образованием поперечных сшивок между нитями ДНК, а также ингибированием синтеза белка, что приводит к нарушению деления клеток и их гибели. Мелфалан блокирует нормальный митоз в быстро пролиферирующих тканях.
Фармакологические эффекты
Иммунодепрессант.
Фармакокинетика
Абсорбция мелфалана из ЖКТ вариабельна. Биодоступность варьирует от 25% до 89%. Степень связывания с белками плазмы низкая (30% и менее). Мелфалан сохраняется в крови в активной форме около 6 ч, метаболизируется в печени с образованием моногидроксимелфалана и дигидроксимелфалана. Конечный период полувыведения около 90 мин.
Выводится почками - 50% (10-15% в неизменённом виде), через кишечник - 20-50%.
При гемодиализе не удаляется.
Показания к применению и дозирование
Рак яичников, РМЖ, рак яичка, миеломная болезнь, неходжкинские лимфомы, саркома Юинга, локализованная саркома мягких тканей конечностей, истинная полицитемия, нейробластома.
Режим дозирования устанавливают индивидуально в зависимости от показаний, состояния пациента и применяемой схемы противоопухолевой терапии.
При миеломной болезни - 150 мкг/кг в сутки в течение 4 дней; циклы повторяют с перерывами в 5-6 нед. Средняя продолжительность лечения - 12 мес.
При неходжкинских лимфомах мелфалан назначают в/в в дозе 140-240 мг/м2 (с последующей трансплантацией аутологичных стволовых клеток периферической крови).
Рак яичников - мелфалан принимают внутрь, 200 мкг/кг в сутки в течение 5 дней, с повторением курса каждые 5 нед.
Побочные эффекты
Система кроветворения: нейтропения (обычно бессимптомная, реже - фебрильная); тромбоцитопения; анемия.
Миелосупрессивное действие отмечают в течение 2-3 нед после начала лечения, хотя у некоторых больных развитие лейкопении возможно в течение 5 дней. Наиболее низкий уровень лейкоцитов и тромбоцитов наблюдают на 3-5 нед, нормализация показателей крови происходит к 4-8 нед.
Пищеварительная система: тошнота и рвота (дозозависимые); диарея; стоматит (язвы в полости рта или на губах), крайне редко - нарушение функций печени.
Дыхательная система: пневмонит, пневмосклероз.
Аллергические реакции: кожная сыпь, зуд, крапивница.
Прочие: гиперурикемия или нефропатия, связанная с повышенным образованием мочевой кислоты (боль в суставах, боль в нижней части спины или в боку, отёчность стоп или лодыжек). Данный побочный эффект наиболее часто возникает в начальном периоде лечения больных лейкозом или лимфомой вследствие быстрого распада клеток и увеличения концентрации мочевой кислоты в сыворотке крови.
Противопоказания
Повышенная чувствительность к мелфалану.
Следует соблюдать осторожность при назначении мелфалана больным, ранее получавшим цитотоксические препараты и лучевую терапию.
Риск и пользу от применения мелфалана необходимо сопоставлять при угнетении функции костного мозга; ветряной оспе (включая недавний контакт с больным) или опоясывающем герпесе; подагре или почечных конкрементах (ураты) в анамнезе (риск гиперурикемии).
Беременность
В I триместре рекомендуют избегать назначения противоопухолевых препаратов. Несмотря на небольшое количество информации об использовании данного лекарственного средства во время беременности необходимо помнить о его возможном мутагенном, тератогенном и канцерогенном действии. При назначении мелфалана во II и III триместрах следует оценить предполагаемую пользу для матери и потенциальный риск для плода.
Вредное действие на плод оказывают также неблагоприятные изменения в организме матери.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Хотя информации о проникновении противоопухолевых препаратов в грудное молоко очень мало, грудное вскармливание во время применения мелфалана не рекомендуют из-за существующего риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие). При необходимости применения мелфалана в период лактации грудное вскармливание необходимо прекратить.
Клинически значимые взаимодействия
Циклоспорин - описаны случаи развития тяжёлых нарушений функций почек.
Налидиксовая кислота - возможно развития тяжёлого некротического геморрагического колита. Цисплатин - снижение клиренса мелфалана за счёт нарушения функции почек.
Резюме и дополнительные сведения
Лечение мелфаланом проводят под тщательным наблюдением врачей, имеющих опыт применения подобных лекарственных средств. Учитывая побочные действия мелфалана и необходимость вспомогательной терапии, парентеральное применение следует проводить опытным специалистам в специализированном стационаре. Дозу лекарственного средства подбирают с учётом индивидуальных особенностей каждого больного на основании клинической эффективности и степени угнетения функции костного мозга. Необходимо помнить о неполном всасывании принимаемого внутрь мелфалана.
Не рекомендуют применение препарата у пациентов с ветряной оспой (в т.ч. недавно перенесённой или после контакта с заболевшими), опоясывающим герпесом или другими инфекционными заболеваниями. Не следует проводить вакцинацию пациентов, получавших мелфалан.
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии. Эти побочные эффекты могут быть необратимыми, как правило, они зависят от дозы лекарственного средства и продолжительности лечения. Из-за частого применения комбинации нескольких противоопухолевых препаратов прогнозирование степени нарушения функции яичек или яичников затруднительно (сложно оценить эффект каждого лекарственного средства в отдельности).
Как и другие алкилирующие средства, мелфалан может оказывать лейкозогенное действие. Имеются сообщения о развитии острого лейкоза после длительного лечения мелфаланом таких заболеваний, как амилоидоз, меланома, миеломная болезнь и рак яичников.
Развитие нефропатии, связанной с повышенным образованием мочевой кислоты (у больных лейкозом или лимфомой) можно предотвратить, обеспечив адекватное потребление жидкости и в ряде случаев назначив аллопуринол. При повышении концентрации мочевой кислоты в сыворотке крови необходимо применение средств, вызывающих подщелачивание мочи.
Во избежание возможного развития выраженной миелосупрессии и риска необратимой аплазии костного мозга в период лечения необходимо проводить регулярный контроль гематологических показателей. При выраженной лейкопении (особенно нейтропении) или тромбоцитопении лечение мелфаланом рекомендуют прекратить. В случае удовлетворительных результатов клинических и лабораторных исследований лечение можно возобновить с использованием редуцированной дозы мелфалана.
При развитии у больного тромбоцитопении в результате применения мелфалана необходимо соблюдать особые меры предосторожности:
-
регулярно осматривать места внутривенного введения препаратов, кожу и слизистые оболочки для определения признаков кровотечения или кровоизлияний;
-
ограничить частоту венепункций и отказаться от внутримышечных инъекций;
-
осторожно пользоваться зубной щёткой, нитью для чистки межзубных промежутков, зубочистками, безопасной бритвой и ножницами для стрижки ногтей;
-
избегать занятий контактными видами спорта или других ситуаций, при которых возможны кровоизлияния или травмы.
Больным с тромбоцитопенией могут потребоваться переливания тромбоконцентрата. Из-за риска желудочно-кишечных кровотечений данным пациентам необходимо избегать приёма аспирина и алкоголя.
При развитии лейкопении необходимо тщательное наблюдение за пациентами для определения признаков возникновения инфекции. Следует избегать контактов с больными бактериальными инфекциями. При возникновении фебрильной нейтропении эмпирически назначают антибиотики широкого спектра действия (до получения результатов бактериологических исследований и соответствующих диагностических тестов).
Код АТХ
L01AA03
Торговые наименования, формы выпуска и производители
Другие обычно используемые наименования L-PAM и phenylalanine mustard.
Используемые в России торговые наименования Melphalan: Алкеранª /Alkeran/ (Великобритания).
Формы выпуска:
Упаковка и хранение
Хранить при температуре <40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Держать в хорошо закрытой, светонепроницаемой упаковке.
Циклофосфамид (Cyclophosphamide)
Фармакологический/химический класс АТХ
N-бис-(b -Хлорэтил)-N -О-триметиленовый эфир диамида фосфорной кислоты.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия; иммунодепрессант.
Механизм действия
Циклофосфамид - алкилирующий препарат из группы азотистого иприта. Активированная форма циклофосфамида (фосфорамидное производное азотистого иприта) связывается со многими внутриклеточными молекулярными структурами, включая нуклеиновые кислоты. Цитотоксическое действие циклофосфамида обусловлено образованием поперечных сшивок между нитями ДНК и РНК, а также ингибированием синтеза белка.
Фармакологические эффекты
Циклофосфамид - сильный иммунодепрессант. Кроме того, он вызывает выраженное и длительное ингибирование активности холинэстеразы.
Фармакокинетика
Лекарственное средство хорошо всасывается после приёма внутрь (биодоступность >75%). Проникает через гематоэнцефалический барьер в ограниченной степени. Связывание с белками очень низкое (однако, для некоторых активных метаболитов - >60%).
Биотрансформация циклофосфамида происходит в печени (включая начальную активацию и последующий распад). Период полувыведения неизменённого препарата - 3-12 ч.
Максимальная концентрация метаболитов в плазме достигается через 2-3 ч после внутривенного введения. Выводится почками, 5-25% в неизменённом виде.
Выводится при диализе.
Показания к применению и дозирование
Лимфобластный (недифференцированный) лейкоз у детей (в том числе и в период ремиссии для увеличения её продолжительности); миело- и монобластный лейкозы; хронический миелолейкоз (обычно препарат неэффективен при остром бластном кризе) и хронический лимфолейкоз; рак яичников; РМЖ; нейробластома; ретинобластома; РШМ; рак тела матки; РМП; РПЖ; рак яичка; опухоль Вильмса; болезнь Ходжкина и неходжкинские лимфомы (включая лимфому нодулярного или диффузного типа, лимфому смешанно-клеточного варианта, гистиоцитарную лимфому, лимфому Беркитта); миеломная болезнь; грибовидный микоз; нефротический синдром (циклофосфамид применяют в качестве иммунодепрессанта для лечения устойчивого к стероидам или часто рецидивирующего чувствительного к стероидам незначительно выраженного нефротического синдрома); саркома Юинга, остеогенная саркома; саркомы мягких тканей; герминогенные опухоли яичника; отторжение трансплантата (циклофосфамид как иммунодепрессант применяют для предотвращения отторжения трансплантата при аллотрансплантации).
При длительном применении циклофосфамида для лечения неопухолевых заболеваний рекомендуют соблюдать осторожность из-за возможного канцерогенного действия.
Режим дозирования устанавливают в зависимости от показаний, состояния пациента, переносимости лечения и выбранной схемы противоопухолевой терапии. Лекарственное средство используют для парентерального введения (внутривенно, внутримышечно) и для приёма внутрь.
Схемы лечения:
Курсовая доза циклофосфамида при всех режимах лечения составляет 6-14 г.
Побочные эффекты
Наиболее частые побочные эффекты:
Регулярные менструации обычно возобновляются в течение нескольких месяцев после окончания лечения циклофосфамидом.
Через 7-12 дней после введения препарата обычно отмечают наиболее низкий уровень лейкоцитов. Восстановление количества лейкоцитов происходит через 17-21 день.
Побочные эффекты при применении высоких доз циклофосфамида и/или длительном лечении:
-
кардиотоксическое действие, включая острый миоперикардит - учащённое сердцебиение, повышенная температура или озноб, одышка;
-
геморрагический цистит - кровь в моче, болезненное мочеиспускание;
-
гиперурикемия и нефропатия, связанные с повышенным образованием мочевой кислоты;
-
негеморрагический цистит или нефротоксическое действие - боль в суставах, в нижней части спины или в боку, отёчность стоп или лодыжек;
-
пневмонит или интерстициальный пневмосклероз - кашель, одышка;
-
синдром, сходный с синдром неадекватной секреции антидиуретического гормона (АДГ) - головокружение, спутанность сознания или ажитация, необычная усталость или слабость.
Кардиотоксическое действие наиболее выражено при применении циклофосфамида в дозах 180-270 мг/кг в течение 4-6 дней. Описано несколько случаев тяжёлой застойной сердечной недостаточности (в том числе со смертельным исходом), развившейся в течение нескольких дней после введения первой дозы циклофосфамида; при гистопатологическом исследовании был диагностирован геморрагический миокардит. Развитие гемоперикарда - следствие геморрагического миокардита и некроза миокарда. Также сообщалось о развитии перикардита, не связанного с гемоперикардом.
Геморрагический цистит может развиться как в течение нескольких часов, так и спустя несколько недель после введения препарата. Считают, что его возникновение связано с метаболитами циклофосфамида (хлоруксусной кислотой, акролеином), выделяемыми с мочой. После отмены циклофосфамида геморрагический цистит проходит в течение нескольких дней. Возможно развитие фиброза мочевого пузыря (в том числе обширного), сопровождающегося циститом или без него. В ряде случаев в моче обнаруживают атипичные клетки эпителия слизистой оболочки мочевого пузыря. Сообщалось также о возникновении геморрагического уретрита и некроза почечных канальцев, проходивших после отмены циклофосфамида.
Гиперурикемия и нефропатия, связанные с повышенным образованием мочевой кислоты, наиболее часто возникают в начальном периоде лечения больных лейкозом или лимфомой. В результате быстрого распада клеток происходит увеличение концентрации мочевой кислоты в сыворотке крови.
Выпадение волос. После окончания лечения обычно происходит восстановление нормального роста волос, хотя волосы могут отличаться по цвету или структуре.
Потемнение кожи и ногтей на пальцах рук; потеря аппетита; тошнота или рвота (особенно при приёме препарата в высоких дозах).
Менее часто диагностируют анемию, тромбоцитопению (обычно бессимптомная, редко - кровотечения или кровоизлияния, чёрный дёгтеобразный стул, кровь в моче или кале, точечные красные пятна на коже), диарею, боль в желудке, приливы крови к лицу, покраснение лица, головную боль, повышенную потливость, микседему (отёчность губ), кожную сыпь, крапивницу или зуд.
Редкие побочные эффекты: анафилактическая реакция; чёрный дёгтеобразный стул; гепатит; гипергликемия; покраснение, отёчность или боль в месте инъекции; стоматит.
Противопоказания
Риск и пользу от применения циклофосфамида необходимо сопоставлять при адреналэктомии (возможно усиление токсических эффектов циклофосфамида, в связи с этим необходима корректировка доз как стероидов для заместительной терапии, так и циклофосфамида); угнетении функции костного мозга; ветряной оспе в настоящее время или недавно перенесённой (включая контакт с больным), опоясывающем герпесе (риск тяжёлого генерализованного заболевания); наличии в анамнезе подагры или почечных конкрементов (уратов) - риск гиперурикемии; нарушениях функций печени (возможно снижение эффекта циклофосфамида); нарушениях функций почек - уменьшение выведения циклофосфамида (снижение дозы обычно не требуется); поражении костного мозга опухолевыми клетками (больным с угнетением функции костного мозга, обусловленным инфильтрацией его опухолевыми клетками, рекомендуют снижение начальной дозы циклофосфамида на 1/3 или 1/2); повышенной чувствительности к циклофосфамиду.
Беременность
Циклофосфамид проникает через плаценту. Применение лекарственного средства приводит к рождению как здоровых детей, так и детей с пороками развития (отсутствие пальцев рук и/или пальцев ног, пороки развития сердца, грыжи). По-видимому, риск возикновения пороков более низкий во II и III триместрах беременности. Низкая масса тела при рождении также следствие действия противоопухолевых препаратов на плод. В I триместре рекомендуют избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Несмотря на небольшое количество информации об использовании циклофосфамида во время беременности необходимо помнить о его возможном мутагенном, тератогенном и канцерогенном действии.
Вредное действие на плод оказывают также неблагоприятные изменения в организме матери.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Циклофосфамид проникает в грудное молоко. Во время проведения химиотерапии грудное вскармливание рекомендуют прекратить из-за возможного риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Пробенецид или сульфинпиразон - при лечении гиперурикемии и подагры может потребоваться корректировка доз урикозурических противоподагрических средств, так как их применение увеличивает риск нефропатии, связанной с повышенным образованием мочевой кислоты.
Антикоагулянты для приёма внутрь - циклофосфамид повышает антикоагулянтную активность в результате снижения синтеза факторов свёртывания крови в печени и нарушения образования тромбоцитов, однако он может также снижать активность антикоагулянтов (механизм неизвестен).
Препараты, вызывающие патологические изменения показателей крови, - при одновременном или недавно проводившемся лечении данными лекарственными средствами лейкопеническое и/или тромбоцитопеническое действие циклофосфамида может усиливаться. При необходимости корректировку дозы циклофосфамида следует проводить на основании результатов анализа крови.
Другие лекарственные средства, вызывающие угнетение функции костного мозга, или лучевая терапия - возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких лекарственных средств, вызывающих угнетение функции костного мозга, а также лучевой терапии необходимо снижение дозы циклофосфамида.
Индукторы ферментов печени - вследствие индукции микросомального метаболизма происходит повышенное образование алкилирующих метаболитов циклофосфамида, снижается его период полувыведения и возрастает активность.
Другие иммунодепрессанты [азатиоприн, хлорамбуцил (хлорбутинª), глюкокортикоиды, циклоспорин, меркаптопурин] - повышается риск развития инфекции и вторичных опухолей.
Ловастатин - у больных, перенесших трансплантацию сердца, повышен риск возникновения острого некроза скелетных мышц и острой почечной недостаточности.
Суксаметония йодид (дитилинª) - циклофосфамид снижает в плазме активность псевдохолинэстеразы (фермента, метаболизирующего сукцинилхолин), усиливая тем самым блокаду сукцинилхолином нервно-мышечной передачи. Возможно сильное или длительное угнетение дыхания или его остановка (апноэ). Это не имеет существенной клинической значимости при проведении больному искусственной вентиляции лёгких. Однако, при одновременном или последовательном применении данных лекарственных средств рекомендуют соблюдать осторожность и тщательно наблюдать больных (особенно если существует вероятность неполного снятия блокады нервно-мышечной передачи после операции).
Резюме и дополнительные сведения
Больным, получающим циклофосфамид, необходимо тщательное наблюдение врача, имеющего опыт проведения химиотерапии или применения иммунодепрессантов.
Существует ряд схем и режимов применения циклофосфамида в комбинации с другими противоопухолевыми препаратами.
Дозу лекарственного средства необходимо подбирать с учётом индивидуальных особенностей каждого больного, клинической эффективности циклофосфамида, а также выраженности его токсического действия.
Развитие нефропатии, связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить обеспечив адекватную водную нагрузку и назначив аллопуринол.
С целью снижения риска развития геморрагического цистита перед назначением циклофосфамида и в течение, по крайней мере, 72 ч после его применения необходимо обеспечить поступление в организм адекватного количества жидкости для достижения достаточного диуреза. Кроме того, для предотвращения длительного контакта метаболитов (оказывающих раздражающее действие) со слизистой оболочкой мочевого пузыря больному следует принимать циклофосфамид утром (чтобы основная часть метаболитов выводилась из организма до сна) и чаще опорожнять мочевой пузырь. При первых признаках геморрагического цистита циклофосфамид необходимо отменить. Для профилактики геморрагического цистита при назначении циклофосфамида в высоких дозах целесообразно назначение месны. При возобновлении лечения следует помнить о возможных рецидивах данного осложнения.
При выраженной лейкопении (в частности, гранулоцитопении) или тромбоцитопении применение циклофосфамида следует отменить до восстановления показателей крови. Затем лечение можно возобновить, назначив циклофосфамид в редуцированной дозе.
При остром лейкозе циклофосфамид назначают несмотря на наличие тромбоцитопении (кровотечения). Возможно прекращение кровотечения и повышение числа тромбоцитов в процессе лечения. В ряде случаев необходимо переливание тромбоконцентрата.
При развитии у больного тромбоцитопении в результате применения циклофосфамида необходимо соблюдать особые меры предосторожности:
-
регулярно осматривать места внутривенного введения препаратов, кожу и слизистые оболочки для определения признаков кровотечения или кровоизлияний;
-
ограничить частоту венепункций и отказаться от внутримышечных инъекций;
-
осторожно пользоваться зубной щёткой, нитью для чистки межзубных промежутков, зубочистками, безопасной бритвой и ножницами для стрижки ногтей;
-
избегать занятий контактными видами спорта или других ситуаций, при которых возможны кровоизлияния или травмы.
Больным с тромбоцитопенией могут потребоваться переливания тромбоконцентрата. Из-за риска желудочно-кишечных кровотечений следует отказаться от приёма алкоголя и аспирина. Также необходимо избегать занятий контактными видами спорта или других ситуаций, при которых возможны кровоизлияния или травмы.
При развитии лейкопении необходимо тщательное наблюдение за больным для определения признаков возникновения инфекции. Следует избегать контактов с больными бактериальными инфекциями. При возникновении фебрильной нейтропении показано парентеральное применение антибиотиков широкого спектра действия (до получения результатов бактериологических исследований и соответствующих диагностических тестов).
При назначении циклофосфамида внутрь его следует принимать на пустой желудок; однако при наличии "желудочного расстройства" дозу можно разделить и принимать во время еды.
Фертильность. У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии. Эти эффекты могут быть необратимыми, как правило, они зависят от дозы препарата и продолжительности лечения. Прогнозирование степени нарушения функции яичек или яичников обычно осложняет применение комбинации нескольких противоопухолевых препаратов, что затрудняет оценку эффекта каждого из них в отдельности. Применение циклофосфамида до зачатия ребёнка у отца приводило к порокам развития сердца и конечностей плода.
У девочек, получавших циклофосфамид в препубертатном возрасте, вторичные половые признаки развиваются нормально, менструальные циклы проходят регулярно, и впоследствии наступает беременность. Однако имеются сообщения о фиброзе яичников и полном исчезновении половых клеток после длительного лечения циклофосфамидом в позднем препубертатном возрасте.
У мальчиков, получавших циклофосфамид в препубертатном возрасте, вторичные половые признаки обычно развиваются нормально, однако у них возможно возникновение олигоспермии или азооспермии, повышенной секреции ХГЧ и атрофии яичек. Азооспермия, как правило, обратима, хотя может сохраняться в течение нескольких лет после окончания лечения циклофосфамидом.
Канцерогенность. Отдалённые побочные эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли. Неизвестно, связано ли их развитие с мутагенным или иммунодепрессивным действием лекарственных средств. Влияние дозы и продолжительности лечения также неясно, но, вероятно, риск их возникновения повышается при длительном применении препаратов. Несмотря на то что информации по данному вопросу немного, имеющиеся данные позволяют предположить, что риск канцерогенного действия наиболее высок при использовании алкилирующих препаратов. В опытах на животных циклофосфамид оказывал сильное канцерогенное действие. Использование его у человека приводило к развитию миело- и лимфопролиферативных заболеваний, а также РМП (особенно у больных с развившимся во время лечения циклофосфамидом геморрагическим циститом) в течение нескольких лет после его применения. Отмечен случай рака почечной лоханки у больного, длительно получающего циклофосфамид по поводу церебрального васкулита.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Cyclophosphamide: Ледоксинаª /Ledoxina/ (Мексика), Циклофосфамид-Теваª /Cyclophosphamide-Teva/ (Израиль), Циклофосфанª /Cyclophosphan/ (РФ), Цитоксанª /Cytoxan/ (США), Эндоксанª /Endoxan/ (Германия)
Формы выпуска:
Упаковка и хранение
Хранить при температуре 2-25 °С. Держать в плотной упаковке.
Хлорамбуцил (Chlorambucil)
Фармакологический/химический класс АТХ
3-[пара-бис- b -Хлорэтил)-аминофенил] масляная кислота.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия; иммунодепрессант.
Механизм действия
Хлорамбуцил - бифункциональное алкилирующее соединение группы азотистого иприта. Хлорамбуцил - циклонеспецифичный препарат, хотя токсичен также для непролиферирующих клеток. Активность препарата связана с образованием нестабильного этилениммониевого иона, алкилирующего многие внутриклеточные молекулярные структуры, включая нуклеиновые кислоты. Цитотоксическое действие хлорамбуцила обусловлено образованием поперечных сшивок между нитями ДНК и РНК, а также ингибированием синтеза белка.
Фармакологические эффекты
Иммунодепрессант.
Фармакокинетика
Лекарственное средство быстро и полностью всасывается из ЖКТ. Связывание с белками очень высокое (99%). Биотрансформация полная и быстрая, осуществляется в печени. Основной метаболит - фенилацетатное производное иприта (производное аминофенилуксусной кислоты) - активное соединение, подвергающееся спонтанному распаду. Период полувыведения хлорамбуцила - около 1,5 ч, производного аминофенилуксусной кислоты - около 2,5 ч. Время достижения максимальной концентрации в плазме крови- 1 ч. Клинические эффекты обычно проявляются через 3-4 нед. Выводится почками, <1% в виде хлорамбуцила или фенилацетатного производного иприта. Не выводится при диализе.
Показания к применению и дозирование
Хронический лимфолейкоз, лимфогранулематоз, неходжкинские лимфомы, рак яичника, рак яичка, волосатоклеточный лейкоз, истинная полицитемия, нефротический синдром (хлорамбуцил применяли в качестве иммунодепрессанта в комбинации с преднизоном для лечения устойчивого к стероидам или незначительно выраженного часто рецидивирующего чувствительного к стероидам нефротического синдрома у детей и взрослых). Наиболее часто токсическое действие хлорамбуцила выражается в угнетении функции костного мозга, в связи с этим в ряде случаев необходимо снижение дозы препарата. Из-за возможных отдалённых токсических эффектов (бесплодие у мужчин, лейкоз) рекомендуют применять хлорамбуцил только у больных, не поддающихся лечению стероидами или обладающих их выраженной непереносимостью.
Режим дозирования для взрослых. При хроническом лимфолейкозе, лимфогранулематозе или неходжкинских лимфомах (начальное лечение или короткий курс): внутрь, 100-200 мкг/кг (0,1-0,2 мг/кг) в сутки или 3-6 мг/м2 однократно или в разделённых дозах. Общая доза на курс лечения 200-400 мг. При уменьшении количества лейкоцитов до 25-20x109/л больного переводят на поддерживающую терапию, назначая по 2-6 мг в нед в течение года и более.
После прерывистого двухнедельного курса лечения угнетение функции костного мозга обычно менее выражено. Начальную дозу 400 мкг/кг (0,4 мг/кг) или 12 мг/м2 увеличивают на 100 мкг/кг (0,1 мг/кг) или 3 мг/м2 каждые 2 нед до достижения эффективной или токсической дозы, затем по мере необходимости дозу корректируют.
Режим дозирования для детей. При лимфогранулематозе или неходжкинских лимфомах: внутрь, 100-200 мкг/кг (0,1-0,2 мг/кг) или 4,5 мг/м2 в сутки однократно или в разделённых дозах.
Побочные эффекты
Наиболее частые дозозависимые побочные эффекты:
При коротком курсе терапии лейкопения и тромбоцитопения могут отсутствовать до третьей недели лечения, обычно они сохраняются в течение 1-2 нед (иногда до 3-4 нед) после отмены хлорамбуцила. Снижение числа нейтрофилов, как правило, продолжается до 10 дней после последнего применения лекарственного средства. После однократного приёма хлорамбуцила в высокой дозе наиболее низкий уровень лейкоцитов и тромбоцитов отмечают через 7-14 дней, восстановление показателей крови происходит в течение 2-3 нед.
Считают, что при коротких прерывистых курсах лечения хлорамбуцилом угнетение функции костного мозга менее выражено, чем при непрерывном лечении, так как функции костного мозга восстанавливаются между циклами.
Менее часто диагностируют медикаментозную лихорадку; аллергические реакции (кожная сыпь, многоформная эритема, токсический эпидермальный некролиз); гиперурикемию или нефропатию (боль в суставах, боль в нижней части спины или в боку, отёчность стоп и лодыжек), наиболее часто возникающую в начальном периоде лечения больных лейкозом или лимфомой (результат быстрого распада клеток, приводящего к повышению концентрации мочевой кислоты в сыворотке крови); стоматит; гепатотоксическое действие, некроз или цирроз печени (желтушность склер или кожи); нейротоксическое действие (возбуждение, спутанность сознания, галлюцинации, мышечные подёргивания, судорожные припадки, сильная слабость или паралич, тремор, затруднение при ходьбе); нарушения менструального цикла, аменорею, азооспермию; после длительного применения хлорамбуцила - пневмосклероз (кашель или одышка), обычно обратимый после отмены лекарственного средства.
Сообщалось о редких случаях очаговых и/или генерализованных судорожных припадков у детей и взрослых при назначении хлорамбуцила в терапевтических суточных дозах, при использовании ударных доз лекарственного средства и его острой передозировке. Риск данных побочных эффектов повышается у детей с нефротическим синдромом (судорожные припадки наблюдают через 6-90 дней после начала лечения) и у больных, получающих препарат в ударных дозах. Нейротоксическое действие обычно обратимо при отмене хлорамбуцила.
Передозировка
Симптомы: обратимая панцитопения; нейротоксическое действие (атаксия, возбуждение и судорожные припадки).
Специфический антидот отсутствует.
Лечение: немедленная эвакуация содержимого желудка; поддерживающая симптоматическая терапия; мониторирование числа форменных элементов крови не менее 3 раз в нед в течение не менее 3 нед или до восстановления функции костного мозга.
Противопоказания
Риск и пользу от применения хлорамбуцила необходимо сопоставлять при угнетении функции костного мозга; ветряной оспе (включая недавний контакт с больным) или опоясывающем герпесе (риск тяжёлого генерализованного заболевания); наличии в анамнезе подагры или почечных конкрементов - уратов (риск гиперурикемии); травмах головы или судорожных расстройствах в анамнезе (повышенный риск судорог); повышенной чувствительности к хлорамбуцилу; инфильтрации костного мозга опухолевыми клетками; проведении ранее цитотоксической или лучевой терапии.
Беременность
Контролируемых исследований по применению хлорамбуцила в период беременности не проводилось. Несмотя на то, что сообщалось о ряде случаев благополучной беременности при применении хлорамбуцила, описаны два случая рождения детей без почки и мочеточника.
В I триместре обычно рекомендуют избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Несмотря на небольшое количество информации об использовании хлорамбуцила во время беременности необходимо помнить о его возможном мутагенном, тератогенном и канцерогенном действии.
Вредное действие на плод оказывают также неблагоприятные изменения в организме матери.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
В опытах на крысах получены данные о наличии врождённых пороков мочеполовой системы (отсутствие почки).
Кормление грудью
Данных о проникновении хлорамбуцила в грудное молоко нет. Во время проведения химиотерапии грудное вскармливание рекомендуют прекратить из-за возможного риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Аллопуринол; колхицин; сульфинпиразон - при лечении гиперурикемии и подагры может потребоваться корректировка доз урикозурических противоподагрических средств, так как их применение увеличивает риск нефропатии, связанной с повышенным образованием мочевой кислоты. Предпочтительное лекарственное средство для предотвращения или устранения вызванной применением хлорамбуцила гиперурикемии - аллопуринол.
Трициклические антидепрессанты и, возможно, структурно сходные с ними соединения (галоперидол, локсапин, мапротилин, молиндон, ингибиторы моноаминоксидазы: фуразолидон, прокарбазин и селегилин, фенотиазины, пимозид или тиоксантены) - вследствие применения данных лекарственных средств снижается судорожный порог и возрастает риск судорожных припадков.
Лекарственные средства, вызывающие патологические изменения показателей крови, - при одновременном или недавно проводившемся лечении данными препаратами лейкопеническое и/или тромбоцитопеническое действие хлорамбуцила может усиливаться. При необходимости корректировку дозы хлорамбуцила проводят на основании результатов анализа крови.
Другие лекарственные средства, вызывающие угнетение функции костного мозга, или лучевая терапия - возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких лекарственных средств, вызывающих угнетение функции костного мозга, а также лучевой терапии необходимо снижение дозы хлорамбуцила.
Другие иммунодепрессанты [азатиоприн, глюкокортикоиды, кортикотропин (АКТГ), циклофосфамид, циклоспорин, цитарабин, меркаптопурин] - повышается риск развития инфекции и вторичных опухолей.
Резюме и дополнительные сведения
Больным, получающим хлорамбуцил, необходимо тщательное наблюдение врача, имеющего опыт применения лекарственных средств алкилирующего действия. Существует ряд схем и режимов применения хлорамбуцила в отдельности или в комбинации с другими противоопухолевыми препаратами.
Дозу хлорамбуцила необходимо подбирать с учётом индивидуальных особенностей каждого больного, клинической эффективности и выраженности токсического действия лекарственного средства.
При приёме хлорамбуцила важно потребление достаточного количества жидкости и последующее усиление диуреза с целью обеспечения выведения мочевой кислоты. Развитие нефропатии, связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить путём адекватного потребления жидкости и назначением аллопуринола.
При возникновении симптомов токсического действия на лёгкие или выраженных кожных реакциях хлорамбуцил следует отменить.
Из-за риска усиления токсического действия на костный мозг не рекомендуют применение хлорамбуцила в течение 4-6 нед после проведения лучевой терапии или химиотерапии с использованием препаратов, вызывающих угнетение функции костного мозга.
Поскольку снижение числа нейтрофилов может продолжаться в течение 10 дней после последнего применения хлорамбуцила, необходимо помнить о риске развития панцитопении по мере приближения общей дозы к 6,5 мг/кг.
При резком снижении числа лейкоцитов (особенно гранулоцитов) требуется уменьшение дозы или отмена хлорамбуцила с последующим постоянным наблюдением до тех пор, пока их уровень не достигнет допустимых значений.
При развитии у больного тромбоцитопении в результате применения хлорамбуцила необходимо соблюдать особые меры предосторожности:
При развитии лейкопении необходимо тщательное наблюдение за больным для определения признаков возникновения инфекции. При фебрильной нейтропении показано парентеральное применение антибиотиков широкого спектра действия (до получения результатов бактериологических исследований и соответствующих диагностических тестов).
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии. Эти эффекты могут быть необратимыми, как правило, они зависят от дозы препарата и продолжительности лечения.
Имеются многочисленные сообщения о длительной (необратимой) азооспермии или необратимом бесплодии при продолжительном применении хлорамбуцила у мальчиков препубертатного и пубертатного возраста. У девочек пубертатного возраста и у взрослых женщин сообщалось о случаях аменореи. При патологоанатомическом исследовании яичников у женщин, получавших комбинированную терапию, включающую хлорамбуцил, диагностировали фиброз различной степени тяжести, васкулит и снижение числа примордиальных фолликулов.
Код АТХ
L01AA02
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Chlorambucil: Лейкеранª /Leukeran/ (Великобритания), Хлорбутинª /Chlorbutin/ (РФ).
Формы выпуска:
Упаковка и хранение
Хранить при температуре <40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Держать в хорошо закрытой, светонепроницаемой упаковке.
Производные этиленимина и этилендиамина
Алтретамин (Altretamine)
Фармакологический/химический класс АТХ
N, N, N', N', N'', N''-гексаметил -1, 3, 5-триазин-2, 4, 6-триамин.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Точный механизм действия алтретамина неизвестен. Хотя алтретамин сходен по химической структуре с алкилирующими препаратами, обнаружено, что in vitro он не обладает алкилирующей активностью. Существует ряд доказательств того, что алтретамин ингибирует синтез ДНК и РНК.
Фармакокинетика
После приёма внутрь лекарственное средство быстро и хорошо всасывается; однако из-за быстрого метаболизма в печени максимальные концентрации в плазме варьируют. В связи с высокой растворимостью в жирах алтретамин распределяется в тканях с высоким содержанием липидов (например, сальник и подкожная жировая клетчатка). Для проявления активности алтретамина необходимо его метаболическое превращение. Алтретамин подвергается быстрому и интенсивному деметилированию, катализируемому ферментами системы цитохрома Р-450. Максимальной концентрации в плазме достигает через 0,5-3 ч. Период полувыведения варьирует от 4,7 до 10,2 ч. Алтретамин выводится почками (в неизменённом виде <1%).
Показания к применению и дозирование
Рак яичников. Атретамин назначают в качестве монотерапии при лечении больных устойчивым к терапии или рецидивирующим раком яичников после применения препаратов первой линии (комбинации на основе препаратов платины).
Режим дозирования для взрослых. При раке яичников: внутрь, 260 мг/м2 в сутки в 4 разделённых дозах (после еды и перед сном) в течение 14 или 21 дня подряд 28-дневного цикла.
При возникновении сильной тошноты и рвоты, лейкопении, тромбоцитопении или нейротоксического действия рекомендуют воздержаться от приёма алтретамина в течение по крайней мере 14 дней, а затем возобновить лечение в дозе 200 мг/м2 в сутки.
Побочные эффекты
Наиболее частые побочные эффекты:
При прерывистом применении (например, по 8-12 мг/кг в сутки в течение 21 дня) наиболее низкие уровни лейкоцитов и тромбоцитов отмечают примерно через 3-4 нед с восстановлением через 6 нед; при непрерывном применении наиболее низкие уровни лейкоцитов и тромбоцитов в среднем - через 6-8 нед.
При ежедневном применении атретамина в высоких дозах частота нейротоксического действия выше, чем при прерывистом курсе лечения в умеренных дозах.
Редкие побочные эффекты: гепатотоксическое действие; кожная сыпь или зуд.
Противопоказания
Риск и пользу от применения атретамина необходимо сопоставлять при угнетении функции костного мозга; ветряной оспе (включая недавний контакт с больным) или опоясывающем герпесе (риск тяжёлого генерализованного заболевания); тяжёлом нарушении функций печени; нейротоксических побочных эффектах; нарушении функций почек; поражении костного мозга; повышенной чувствительности к алтретамину; проведении ранее цитотоксической или лучевой терапии.
Беременность
Исследований по применению алтретамина в период беременности не проводилось. Обычно рекомендуют избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Несмотря на небольшое количество информации об использовании противоопухолевых лекарственных средств во время беременности необходимо помнить об их возможном мутагенном, тератогенном и канцерогенном действии.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Данных о проникновении алтретамина и его метаболитов в грудное молоко нет. Во время проведения химиотерапии грудное вскармливание рекомендуют прекратить из-за возможного риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Лекарственные средства, вызывающие патологические изменения показателей крови, - при одновременном или недавно проводившемся лечении данными препаратами лейкопеническое и/или тромбоцитопеническое действие алтретамина может усиливаться. При необходимости корректировку дозы алтретамина проводят на основании результатов анализа крови.
Другие лекарственные средства, вызывающие угнетение функции костного мозга, или лучевая терапия - возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких лекарственных средств, вызывающих угнетение функции костного мозга, а также лучевой терапии необходимо снижение дозы алтретамина.
Циметидин - ингибирование циметидином ферментной системы цитохрома Р-450 вызывает снижение метаболизма алтретамина в печени, что приводит к замедлению его выведения и повышению концентрации в крови.
Ингибиторы моноаминоксидазы (МАО): фуразолидон, прокарбазин и селегилин - при одновременном применении возможна тяжёлая ортостатическая гипотензия.
Резюме и дополнительные сведения
Больным, получающим альтретамин, необходимо наблюдение врача, имеющего опыт проведения химиотерапии. Существует ряд схем и режимов применения алтретамина в отдельности или в комбинации с другими противоопухолевыми препаратами.
Дозу алтретамина необходимо подбирать с учётом индивидуальных особенностей каждого больного, клинической эффективности, выраженности неротоксического действия и степени угнетения функции костного мозга.
Следует временно воздержаться от применения алтретамина при:
Примерно через 14 дней терапию можно возобновить, редуцировав дозу алтретамина до 200 мг/м2 в сутки.
Если нейротоксичность лекарственного средства сохраняется даже после снижения дозы, применение алтретамина рекомендуют прекратить.
При развитии у больного тромбоцитопении в результате применения алтретамина необходимо соблюдать особые меры предосторожности:
-
регулярно осматривать места внутривенного введения препаратов, кожу и слизистые оболочки для определения признаков кровотечения или кровоизлияний;
-
ограничить частоту венепункций и отказаться от внутримышечных инъекций;
-
осторожно пользоваться зубной щёткой, нитью для чистки межзубных промежутков, зубочистками, безопасной бритвой и ножницами для стрижки ногтей;
-
избегать занятий контактными видами спорта или других ситуаций, при которых возможны кровоизлияния или травмы.
При развитии лейкопении необходимо тщательное наблюдение за больным для определения признаков возникновения инфекции. При фебрильной нейтропении показано эмпирическое назначение антибиотиков широкого спектра действия (до получения результатов бактериологических исследований и соответствующих диагностических тестов).
Код АТХ
Торговые наименования, формы выпуска и производители
Другое обычно используемое наименование - hexamethylmelamine (гексаметилмеламин).
Используемые в России торговые наименования Altretamine: Гексаленª /Hexalen/ (Израиль).
Формы выпуска:
Упаковка и хранение
Хранить при температуре <40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Держать в хорошо закрытой, светонепроницаемой упаковке.
Дополнительная маркировка: принимать после еды.
Тиотепа (Thiotepa)
Фармакологический/химический класс АТХ
N,N',N"-Три(этилен)-триамид тиофосфорной кислоты, или N,N',N"-Триэтилениминтиофосфамид.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Тиотепа - трифункциональный алкилирующий препарат группы азотистого иприта, обладающий циклонеспецифичной активностью. Активность лекарственного средства связана с образованием нестабильного этилениммониевого иона, алкилирующего многие внутриклеточные молекулярные структуры, включая нуклеиновые кислоты. Цитотоксическое действие лекарственного средства обусловлено образованием поперечных сшивок между нитями ДНК и РНК, а также ингибированием синтеза белка.
Фармакокинетика
При местном применении часть лекарственного средства подвергается системному всасыванию. Абсорбция через слизистую оболочку мочевого пузыря вариабельна - 10-100% (зависит от концентрации препарата, продолжительности его контакта со слизистой оболочкой мочевого пузыря), она повышается при обширном разрастании опухоли, воспалении слизистой оболочки, эндоскопических хирургических вмешательствах, лучевой терапии и при пузырно-мочеточниковом рефлюксе. Выводится почками (85%) в основном в виде метаболитов.
Показания к применению и дозирование
РМЖ, рак яичника, РМП, рак лёгкого, лимфогранулематоз, неходжкинские лимфомы. Экссудативный перикардит, плеврит и асцит при злокачественной опухоли (внутриполостные введения тиофосфамида для ликвидации выпота в различные серозные полости при диффузных или локализованных формах опухолей).
Режим дозирования для взрослых и подростков. При экссудативом перикардите, экссудативном перитоните, экссудативном плеврите, развившихся при злокачественной опухоли,: в полость вводят по 600-800 мкг/кг через 1-4 нед с поддерживающей дозой 70-800 мкг/кг. Дозу снижают при выраженном истощении или слабости, хронических заболеваниях сердечно-сосудистой системы или почек. Поддерживающую дозу подбирают на основании результата анализа крови и вводят 1 раз через 1-4 нед.
РМЖ, рак яичника, рак лёгкого, лимфогранулематоз, неходжкинские лимфомы: лекарственное средство вводят внутривенно, по 300-400 мкг (0,3-0,4 мг)/кг через 1-4 нед или по 200 мкг (0,2 мг) в течение 4-5 дней через 2-4 нед. Поддерживающую дозу подбирают на основании результата анализа крови.
РМП: лекарственное средство вводят в мочевой пузырь путём инстилляции с помощью катетера по 30-60 мг в 30-60 мл дистиллированной воды 1 раз в неделю в течение 4 нед; при необходимости курс можно повторять ежемесячно. Больному следует ограничить потребление жидкости в течение 8-12 ч перед каждым введением, попытаться воздержаться от мочеиспускания в течение 2 ч после введения лекарственного средства. Для обеспечения максимального контакта лекарственного средства со слизистой оболочкой мочевого пузыря больному необходимо менять положение каждые 15 мин.
Побочные эффекты
Наиболее частые побочные эффекты:
Менее часто диагностируют гиперурикемию или нефропатию, связанную с повышенным образованием мочевой кислоты (боль в суставах, боль в нижней части спины или в боку, отёчность стоп или лодыжек; боль в месте инъекции или инстилляции в мочевой пузырь).
Гиперурикемия или нефропатия, связанная с повышенным образованием мочевой кислоты, наиболее часто возникает в начальном периоде лечения больных лейкозом или лимфомой вследствие быстрого распада клеток и увеличения концентрации мочевой кислоты в сыворотке крови.
Редкие побочные эффекты: анафилаксия (кожная сыпь, бронхоспазм); нефротоксическое действие после инстилляции в мочевой пузырь (болезненное или затруднённое мочеиспускание); стоматит; головокружение; потеря аппетита; тошнота и рвота; выпадение волос.
Противопоказания
Риск и пользу от применения тиотепы необходимо сопоставлять при угнетении функции костного мозга; нарушении функций печени и почек (рекомендуют более низкие дозы и тщательное мониторирование клинико-биохимических показателей); ветряной оспе (включая недавний контакт с больным) или опоясывающем герпесе (риск тяжёлого генерализованного заболевания); наличии в анамнезе подагры или почечных конкрементов - уратов (риск гиперурикемии); повышенной чувствительности к тиотепе; проведении ранее цитотоксической или лучевой терапии.
Беременность
Тиотепа тератогенно влияет на плод, хотя сообщалось о случаях рождения здоровых детей. Назначение препарата в период беременности противопоказано.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Данных о проникновении тиотепы и её метаболитов в грудное молоко нет. Во время проведения химиотерапии грудное вскармливание рекомендуют прекратить из-за возможного риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Аллопуринол; колхицин; сульфинпиразон - при лечении гиперурикемии и подагры может потребоваться корректировка доз урикозурических противоподагрических средств, так как их применение увеличивает риск нефропатии, связанной с повышенным образованием мочевой кислоты. Предпочтительное лекарственное средство для предотвращения или устранения вызванной применением тиотепы гиперурикемии - аллопуринол.
Лекарственные средства, вызывающие патологические изменения показателей крови, - при одновременном или недавно проводившемся лечении данными препаратами лейкопеническое и/или тромбоцитопеническое действие может усиливаться. При необходимости корректировку дозы тиотепы проводят на основании результатов анализа крови.
Другие лекарственные средства, вызывающие угнетение функции костного мозга, или лучевая терапия - возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких лекарственных средств, вызывающих угнетение функции костного мозга, а также лучевой терапии необходимо снижение дозы тиотепы.
Суксаметония йодид (дитилинª) - тиотепа снижает в плазме активность псевдохолинэстеразы (фермента, метаболизирующего сукцинилхолин), усиливая тем самым блокаду сукцинилхолином нервно-мышечной передачи. У больных, получающих тиотепу, до применения дитилина рекомендуют определить активность псевдохолинэстеразы в плазме. Возможно сильное и длительное угнетение дыхания или его остановка (апноэ). Это не имеет существенной клинической значимости при проведении больному искусственной вентиляции лёгких. Однако при одновременном или последовательном применении этих препаратов рекомендуют соблюдать осторожность и тщательно наблюдать за больными (особенно если существует вероятность неполного снятия блокады нервно-мышечной передачи).
Урокиназа - может усиливать эффективность тиотепы при лечении РМП, действуя в качестве активатора плазминогена и увеличивая концентрацию лекарственного средства в опухолевой ткани.
Инактивированные вирусные вакцины - в связи с тем, что при лечении тиотепой происходит подавление естественных защитных механизмов, выработка антител в организме больного в ответ на введение вакцины может снижаться. Интервал между прекращением применения иммунодепрессантов и восстановлением способности больного реагировать на вакцину зависит от дозы и типа используемого иммунодепрессанта, основного заболевания и других факторов; по разным оценкам, этот интервал варьирует от 3 до 12 мес.
Резюме и дополнительные сведения
Больным, получающим тиотепу, необходимо наблюдение врача, имеющего опыт проведения химиотерапии.
Дозу тиотепы необходимо подбирать с учётом индивидуальных особенностей каждого больного, клинической эффективности, выраженности оксического действия лекарственного средства.
Развитие нефропатии, связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить обеспечив адекватное потребление жидкости и в ряде случаев назначив аллопуринол.
Тиотепу можно вводить внутривенно, внутриплеврально, внутрибрюшинно, в перикардиальную полость, в опухоль или путём инстилляции в мочевой пузырь.
Для предотвращения необратимого угнетения функции костного мозга при первых признаках значительного снижения числа лейкоцитов (в частности, гранулоцитов) или числа тромбоцитов лечение тиофосфамидом рекомендуют прекратить или уменьшить дозу лекарственного средства. Лечение можно возобновить при восстановлении числа лейкоцитов и тромбоцитов до допустимых значений.
Больным с тромбоцитопенией, развившейся в результате применения тиотепы, рекомендуют соблюдать особые меры предосторожности.
При развитии лейкопении необходимо тщательное наблюдение за больным для определения признаков возникновения инфекции. При фебрильной нейтропении показано эмпирическое назначение антибиотиков широкого спектра действия (до получения результатов бактериологических исследований и соответствующих диагностических тестов).
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии.
Отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, неясно, их развитие связано с мутагенным или иммунодепрессивным действием лекарственных средств.
Код АТХ
L01AC01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Thiotepa: Тиотепа-Тиоплексª /Thiotepa-Thioplex/ (Великобритания), Тиофосфамидª лиофилизированный/Thiphosphamide Lyophilized/ (РФ).
Форма выпуска:
Упаковка и хранение
Хранить при температуре 2-8 °С. Защищать от света.
Производные метансульфоновой кислоты
Бусульфан (Busulfan)
Фармакологический/химический класс АТХ
Бис-метилсульфоновый эфир бутандиола-1, 4.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Бусульфан - бифункциональное алкилирующее соединение группы алкилсульфонатов, циклонеспецифичный препарат. Механизм действия препарата неясен, считают, что он связан с алкилированием и образованием поперечных сшивок между нитями ДНК и подавлением роста миелоидных клеток.
Фармакокинетика
Бусульфан полностью всасывается из ЖКТ. После приёма внутрь меченного радиоактивным изотопом бусульфана, в крови его обнаруживают через 0,5-2 ч. Быстрая биотрансформация препарата происходит в печени. Период полувыведения около 2,5 ч. Клинический эффект развивается через 1-2 нед после начала лечения. Медленно выводится почками, практически полностью в виде метаболитов. Минимальное выведение лекарственного средства при диализе вероятно связано с плохой растворимостью бусульфана в воде и длительной задержкой метаболитов.
Показания к применению и дозирование
Хронический миелолейкоз (в фазе бластного криза препарат не эффективен); миелобластный лейкоз, эритремия, истинная полицитемия, эссенциальная тромбоцитемия, миелофиброз.
Режим дозирования устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии.
Режим дозирования для взрослых. При хроническом миелолейкозе: начальная доза - внутрь, 1,8 мг/м2 в сутки или 60 мкг (0,06 мг)/кг в сутки, до снижения уровня лейкоцитов <15x109/л. Обычный диапазон доз - 4-8 мг в сутки, он может варьировать от 1 до 12 мг. В стадии ремиссии лечение возобновляют, когда ежемесячно определяемое число лейкоцитов достигает 50x109/л.
Некоторые больные имеют необычно высокую чувствительность к бусульфану, в результате его применения у них развивается выраженое угнетение функции костного мозга, поэтому необходимо частое и тщательное мониторирование показателей крови.
Режим дозирования для детей. При хроническом миелолейкозе: начальная доза - внутрь, 60-120 мкг (0,06-0,12 мг)/кг в сутки или 1,8-4,6 мг/м2 в сутки.
Дозу бусульфана подбирают таким образом, чтобы снизить число лейкоцитов и поддерживать их уровень около 20x109/л.
Побочные эффекты
Бусульфан может вызывать дисплазию клеток в лёгочной ткани, лимфатических узлах, поджелудочной и щитовидной железе, надпочечниках, печени, костном мозге, мочевом пузыре, молочной железе и шейке матки.
Наиболее частые побочные эффекты:
Лейкопения обычно диагностируют через 10-15 дней после начала лечения (перед этим число лейкоцитов обычно кратковременно повышается), причём наиболее низкие показатели - примерно через 11-30 дней; число лейкоцитов может снижаться в течение 1 мес и более после отмены лекарственного средства, но обычно восстанавливается к 12-20 недели.
Угнетение функции костного мозга может быть выраженным и в дальнейшем прогрессировать, приводя к панцитопении. Восстановление числа форменных элементов крови до уровня нормы после отмены бусульфана при панцитопении происходит в течение 1 мес. Симптомы угнетения функции костного мозга могут указывать на трансформацию хронического миелолейкоза в острую бластную форму.
Менее часто диагностируют бронхолёгочную дисплазию с пневмосклерозом (повышенная температура, кашель, одышка); гиперурикемию или нефропатию, связанную с повышенным образованием мочевой кислоты, (боль в суставах, боль в нижней части спины или в боку, отёчность стоп и лодыжек); стоматит. Данные побочные эффекты возникают при длительном применении бусульфана или использовании его в высокой дозе.
Бронхолёгочную дисплазию с пневмосклерозом обычно диагностируют в период от 8 мес до 10 лет (в среднем через 4 года) после начала лечения. Она сопровождается уменьшением жизненной ёмкости лёгких и эластичности лёгочной ткани, часто заканчивается смертельным исходом в течение 6 мес после постановки диагноза. При гистологическом исследовании картина изменений сходна с таковыми после облучения лёгких. Для постановки диагноза необходимо исследование биоптатов лёгких.
Гиперурикемия или нефропатия, связанная с повышенным образованием мочевой кислоты, наиболее часто возникает в начальном периоде лечения больных лейкозом или лимфомой вследствие быстрого распада клеток и увеличения концентрации мочевой кислоты в сыворотке крови.
Редкие побочные эффекты: катаракта; аменорея или угнетение функции яичников; потемнение кожи (5-10%), спутанность сознания; диарея; гипотензия (головокружение); потеря аппетита; тошнота и рвота; необычная усталость или слабость; быстрое снижение массы тела.
Все вышеперечисленные неблагоприятные эффекты, включая потемнение кожи, развиваются при длительном лечении бусульфаном и могут быть сходными с симптомами недостаточности коры надпочечников, хотя у большинства больных угнетение функции коры надпочечников не отмечают. При отмене бусульфана симптомы иногда обратимы. Чувствительность надпочечников к экзогенному АКТГ обычно в пределах нормы, результаты теста на определение функции гипофиза с использованием метирапона показали уменьшение выведения 17-гидроксикортикостероидов с мочой у ряда больных с возвращением к нормальному уровню при прекращении применения бусульфана.
Передозировка
Симптомы: проявление острой дозолимитирующей токсичности бусульфана у человека - миелосупрессия. Основные симптомы хронической передозировки препарата: угнетение костномозгового кроветворения и панцитопения.
Лечение: антидот неизвестен. Возможно проведение диализа (существует одно сообщение об успешном выведении бусульфана путём диализа). При наличии признаков гематологической токсичности проводят соответствующую поддерживающую терапию.
Противопоказания
Риск и пользу от применения бусульфана необходимо сопоставлять при угнетении функции костного мозга; ветряной оспе (включая недавний контакт с больным) или опоясывающем герпесе (риск тяжёлого генерализованного заболевания); наличии в анамнезе подагры или почечных конкрементов - уратов (риск гиперурикемии); повышенной чувствительности к бусульфану; применении бусульфана в очень высоких дозах у больных с травмой головы или с судорожными расстройствами в анамнезе (иногда врачи применяют профилактическую противосудорожную терапию); проведении ранее цитотоксической или лучевой терапии; наличии симптомов мелофиброза.
Беременность
Контролируемых исследований по применению бусульфана в период беременности не проводилось. Сообщалось о нескольких случаях благоприятного исхода беременности. Существуют данные об одном случае наличия пороков развития у новорождённого, развившихся в результате проведения матери облучения и комбинированной химиотерапию (включающей бусульфан). Кроме того, сообщалось о рождении грудных детей с низкой массой тела, особенно после применения бусульфана во время III триместра беременности. Также есть данные об умеренно выраженной анемии и нейтропении у новорождённого, при назначении матери бусульфана, начиная с 8-й недели беременности до родов.
Обычно рекомендуют избегать применения противоопухолевых препаратов в течение беременности. Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Данных о проникновении бусульфана в грудное молоко нет. Препарат противопоказан к применению в период лактации (грудного вскармливания).
Клинически значимые взаимодействия
Аллопуринол; колхицин; сульфинпиразон - при лечении гиперурикемии и подагры может потребоваться корректировка доз урикозурических противоподагрических средств, так как их применение увеличивает риск нефропатии, связанной с повышенным образованием мочевой кислоты. Предпочтительное лекарственное средство для предотвращения или устранения вызванной применением тиотепы гиперурикемии - аллопуринол.
Лекарственные средства, вызывающие патологические изменения показателей крови, - при одновременном или недавно проводившемся лечении данными препаратами лейкопеническое и/или тромбоцитопеническое действие может усиливаться. При необходимости корректировку дозы бусульфана проводят на основании результатов анализа крови.
Другие лекарственные средства, вызывающие угнетение функции костного мозга, или лучевая терапия - возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких лекарственных средств, вызывающих угнетение функции костного мозга, а также лучевой терапии необходимо снижение дозы бусульфана.
При длительном лечении бусульфаном и тиогуанином 330 больных у 12 из них отмечено варикозное расширение вен пищевода, изменения показателей функциональных проб печени и признаки её узелковой регенеративной гиперплазии (при биопсии после терапии в течение 6-45 мес).
Резюме и дополнительные сведения
Бусульфан - цитотоксическое средство. Его следует применять только под контролем врачей, имеющих опыт терапии подобными лекарственными средствами.
При интактной наружной оболочке использование таблеток бусульфана безопасно. Таблетки не следует делить на части. При назначении бусульфана в таблетках необходимо выполнять рекомендации по применению цитотоксических препаратов.
Как правило, бусульфан не назначаютв комбинации с лучевой терапией или вскоре после неё.
Бусульфан следует отменить при наличии признаков его токсического действия на лёгкие. Если пациентам с возможным токсическим поражением лёгких необходима общая анестезия, то концентрацию вдыхаемого кислорода следует поддерживать на наиболее низком безопасном уровне. В послеоперационном периоде необходимо тщательно контролировать и поддерживать функцию внешнего дыхания.
Не рекомендуют проводить иммунизацию живыми вакцинами иммунокомпрометированных пациентов.
Бусульфан применяют при наличии нормальных показателей мочевой кислоты в крови и/или моче (нередко повышены у пациентов с хроническим миелолейкозом). Во время лечения бусульфаном необходима профилактика гиперурикемии и мочекислой нефропатии, включающая потребление достаточного количества жидкости и применение аллопуринола.
Следует помнить о канцерогенных свойствах бусульфана и соблюдать особую осторожность при назначении его для лечения истинной полицитемии и эссенциальной тромбоцитемии. При указанных заболеваниях не рекомендуют применять бусульфан у пациентов молодого возраста или при отсутствии симптомов. Если назначение бусульфана необходимо, то курсы терапии должны быть короткими.
При одновременном приёме бусульфана в стандартных дозах и итраконазола или метронидазола необходимо тщательно наблюдать пациента для своевременного выявления признаков токсичности бусульфана. Одновременный приём метронидазола и бусульфана в высоких дозах не рекомендуют. При применении бусульфана в режиме высокодозной терапии пациентам следует принимать противосудорожные препараты с профилактической целью, предпочтительнее назначать препараты бензодиазепинового ряда, а не фенитоин.
У пациентов, принимавших бусульфан, отмечались различные хромосомные аберрации. По заключению ВОЗ, существует причинно-следственная связь между применением бусульфана и развитием рака. У пациентов, длительно принимавших бусульфан, определяли распространённую эпителиальную дисплазию, причём некоторые изменения были сходны с предраковыми. У нескольких пациентов, получавших бусульфан, описаны случаи развития злокачественных опухолей.
Накапливаются данные о том, что бусульфан, как и другие алкилирующие средства, оказывает лейкозогенное действие. Хотя острый лейкоз, вероятно, - компонент естественного течения истинной полицитемии, длительная терапия алкилирующим средством может повысить риск его развития.
Во время лечения бусульфаном необходимо регулярно определять число форменных элементов крови во избежание выраженной миелосупрессии и необратимой аплазии костного мозга.
Код АТХ
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Busulfan: Миелосанª /Myelosan/ (РФ), Милеранª /Myleran/ (Великобритания)
Форма выпуска:
Упаковка и хранение
Хранить при температуре <40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Держать в хорошо закрытой, светонепроницаемой упаковке.
Производные триазена и гидразина
Дакарбазин (Dacarbazine)
Фармакологический/химический класс АТХ
5-(3, 3-Диметил-1-триазено)-имидазол-4-карбоксамид.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Взаимодействует с SH-группами. Ингибирует синтез пуриновых оснований и ДНК.
Фармакокинетика
Связывание с белками низкое. Проникает через гематоэнцефалический барьер в ограниченных количествах. Интенсивно метаболизируется в печени. Период полувыведения в начальной фазе - 19 мин, в конечной - 5 ч. При нарушениях функции почек и печени период полувыведения увеличивается. Выводится почками в неизменённом виде и в виде метаболитов (40%) в течение 6 ч.
Показания к применению и дозирование
Злокачественная меланома, лимфогранулематоз, саркомы мягких тканей. В качестве лекарственного средства второго ряда дакарбазин применяют при тестикулярных опухолях, злокачественных новообразованиях ЖКТ и нейробластоме.
Режим дозирования: дакарбазин вводят только внутривенно. Содержимое флакона растворяют в 10 или 20 мл стерильной воды для инъекций. Обычная доза 200-250 мг на 1 м2 в течение 5 дней. Циклы лечения повторяют с промежутками 21-28 дней.
Побочные эффекты
Система кроветворения: лейкопения, тромбоцитопения, анемия.
Пищеварительная система: анорексия, тошнота, рвота, диарея, стоматит; в отдельных случаях - нарушения функций печени, тромбоз печёночных вен, токсическая дистрофия печени.
Репродуктивная система: аменорея, азооспермия.
Дерматологические реакции: алопеция, кожная сыпь.
Прочие: гиперемия, гипестезия лица; в единичных случаях - нарушение функций почек.
Передозировка
После разового введения в высокой дозе возможно развитие гриппоподобного синдрома, сопровождающегося повышением температуры тела и миалгией.
Противопоказания
Беременность и Кормление грудью
Дакарбазин противопоказан при беременности. В случае необходимости его применения в период лактации грудное вскармливание следует прекратить.
Женщинам детородного возраста необходмо использовать надёжные методы контрацепции.
В экспериментальных исследованиях определено токсическое действие дакарбазина на плод.
Клинически значимые взаимодействия
Индукторы микросомальных ферментов печени (фенобарбитал, рифампицин, фенитоином) - возможно усиление метаболизма дакарбазина.
При одновременном применении с фенобарбиталом, азатиоприном или меркаптопурином усиливается токсическое действие дакарбазина.
Резюме и дополнительные сведения
Не рекомендуют применять дакарбазин у пациентов с ветряной оспой (в т.ч. недавно перенесённой и после контакта с заболевшими), с опоясывающим герпесом и другими острыми инфекционными заболеваниями.
С осторожностью назначают пациентам, ранее получавшим цитотоксические препараты или лучевую терапию.
Перед началом и в процессе лечения дакарбазином необходим контроль показателей периферической крови, уровня азота мочевины, креатинина, мочевой кислоты, активности трансаминаз печени, ЛДГ и концентрации билирубина в плазме крови.
На фоне терапии не рекомендуют проводить вакцинацию пациентов и членов их семей.
При проведении комбинированной противоопухолевой терапии дакарбазин применяют прежде всего в сочетании с блеомицином, цисплатином, фторурацилом, винкристином и преднизолоном.
В экспериментальных исследованиях установлено канцерогенное и мутагенное действие дакарбазина.
Код АТХ
L01AX04
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Dacarbazine: Дакарбазин Лахемаª/Dacarbazine Lachema (Словения)
Формы выпуска:
Прокарбазин (Procarbazine)
Фармакологический/химический класс АТХ
N-Изопропил-пара-(2-метилгидразино - метил)-бензамида гидрохлорид.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Прокарбазин - алкилирующий препарат, оказывающий слабое ингибирующее действие на моноаминоксидазу (МАО). Точный механизм противоопухолевого действия прокарбазина неизвестен, полагают, что он сходен с таковым у алкилирующих препаратов. Прокарбазин - S-фазовоспецифичное лекарственное средство. Считают, что он ингибирует синтез ДНК, РНК и белка.
Фармакологические эффекты
Ингибиторы МАО препятствуют инактивации тирамина моноаминоксидазами печени и ЖКТ. Циркулирующий тирамин высвобождает норадреналин из окончаний симпатических нервов и вызывает резкое повышение артериального давления.
Фармакокинетика
Лекарственное средство почти полностью всасывается из ЖКТ. Прокарбазин проникает через гематоэнцефалический барьер, биотрансформируется печени до активного метаболита.
Период полувыведения прокарбазина около 10 мин. Выводится почками - 70% (<5% в неизменённом виде) и через дыхательные пути (в виде метана и углерода диоксида).
Показания к применению и дозирование
Лимфогранулематоз; неходжкинские лимфомы (прокарбазин применяют в комбинации с другими препаратами для лечения III и IV стадий лимфогранулематоза и ряда неходжкинских лимфом), первичные опухоли мозга, рак лёгкого, миеломная болезнь, злокачественная тимома.
Режим дозирования для взрослых. При лимфогранулематозе: начальная доза - внутрь, 2-4 мг/кг (до 50 мг) в сутки в однократной или разделённых дозах в течение первой недели, а затем 4-6 мг/кг в сутки до возникновения лейкопении, тромбоцитопении или развития максимального терапевтического эффекта.
При возникновении гематологических осложнений препарат отменяют до прекращения токсического действия, при возобновлении лечения прокарбазин назначают в дозе 1-2 мг/кг (основание) в сутки.
Поддерживающая доза: внутрь, 1-2 мг/кг (основание) в сутки.
Режим дозирования для детей. При лимфогранулематозе: начальная доза - внутрь, 50 мг (основание) в сутки в течение первой недели, а затем 100 мг/м2 (до 50 мг) в сутки до возникновения лейкопении, тромбоцитопении или развития максимального терапевтического эффекта.
При возникновении гематологических осложнений препарат отменяют до прекращения токсического действия, при возобновлении лечения прокарбазин назначают в дозе 50 мг (основание) в сутки.
Поддерживающая доза: внутрь, 50 мг (основание) в сутки.
Побочные эффекты
Многие побочные эффекты противоопухолевой терапии - результат фармакологического действия лекарственного средства. Некоторые из них (например, лейкопению и тромбоцитопению) учитывают при индивидуальном подборе дозы лекарственного средства.
Неблагоприятные эффекты прокарбазина сходны с таковыми у ингибиторов МАО, за исключением токсического действия на кровь, лёгкие и ЖКТ. У больных с нарушением функций почек, печени или с угнетением функции костного мозга токсическое действие прокарбазина выражено более сильно.
Наиболее частые побочные эффекты:
Наиболее низкий уровень тромбоцитов отмечают примерно через 4 нед, после чего снижается число лейкоцитов; показатели крови полностью восстанавливаются примерно через 6 нед.
Менее часто диагностируют тошноту, рвоту, диарею, гепатотоксическое действие, анорексию, периферическую нейропатию (ощущение покалывания или онемения в пальцах рук или ног, неустойчивость или неловкость), стоматит, выпадение волос.
Редкие побочные эффекты: аллергические реакции, артериальная гипертензия, ортостатическая гипотензия.
Передозировка
При передозировке прокарбазина симптомы могут отсутствовать или быть минимальными в течение примерно 12 ч после его приёма, медленно развиваясь, они достигают максимума через 24-48 ч. В этот период необходимы немедленная госпитализация и тщательное наблюдение за больным.
Лечение:
-
в раннем периоде - индукция рвоты или промывание желудка (при защите дыхательных путей) с последующим введением взвеси активированного угля;
-
медленное внутривенное введение диазепама (сибазонаª) - при наличии симптомов стимуляции ЦНС;
-
внутривенное введение жидкостей и разбавленного сосудосуживающего средства (для лечения гипотензии и коллапса);
-
поддержка дыхания с помощью интубации и искусственной вентиляции лёгких с использованием при необходимости кислорода;
-
мониторирование температуры тела и активное лечение гипертермии жаропонижающими средствами;
-
внутривенное введение дантролена натрия в количестве 2,5 мг/кг в сутки в разделённых дозах с тщательным наблюдением за признаками гепатотоксического действия и возникновением плеврального или перикардиального выпота - при наличии симптомов гиперметаболического состояния (кома, дыхательная недостаточность, гиперпирексия, тахикардия, ригидность мышц, дрожание и гиперрефлексия);
Патофизиологические эффекты массивной передозировки могут сохраняться в течение нескольких дней. При небольшой передозировке выздоровление возможно через 3-4 дня.
Противопоказания
Хронический алкоголизм; застойная сердечная недостаточность; тяжёлые нарушения функции печени (прокарбазин может вызывать развитие печёночной прекомы); феохромоцитома (сосудосуживающие вещества, выделяемые такими опухолями, могут изменять артериальное давление во время лечения ингибиторами МАО); выраженные нарушения функций почек (из-за снижения почечного выведения возможно возникновение кумулятивных эффектов прокарбазина).
Риск и пользу от применения прокарбазина необходимо сопоставлять при угнетении функции костного мозга; аритмии; заболеваниях сердечно-сосудистой системы или коронарной недостаточности; сосудистых заболеваниях мозга; ветряной оспе, включая недавний контакт с больным или опоясывающем герпесе (риск тяжёлого генерализованного заболевания); сахарном диабете (прокарбазин может изменять потребность в инсулине или приёме пероральных гипогликемических средств); эпилепсии; гипертиреозе (чувствительность к сосудосуживающим аминам может повышаться); паркинсонизме (возможно обострение), повышенной чувствительности к прокарбазину. Следует также соблюдать осторожность при назначении прокарбазина больным, ранее получавшим цитотоксические лекарственные средства или лучевую терапию.
Беременность
Прокарбазин часто оказывает тератогенное действие у животных. Существуют сообщения о возникновении пороков развития у плода и преждевременных родах у женщин, при назначении прокарбазина в позднем периоде беременности.
В I триместре обычно рекомендуют избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Несмотря на небольшое количество информации об использовании противоопухолевых лекарственных средств во время беременности необходимо помнить об их возможном мутагенном, тератогенном и канцерогенном действии.
Вредное действие на плод оказывают также неблагоприятные изменения в организме матери.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Хотя информации о проникновении противоопухолевых лекарственных средств в грудное молоко очень мало, грудное вскармливание во время применения прокарбазина не рекомендуют из-за существующего риска для ребёнка (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Алкоголь - возможна реакция, сходная с таковой при использовании дисульфирама (тетурамª) - усиление угнетения ЦНС и ортостатическая гипотензия; кроме того, наличие тирамина в алкогольных напитках, особенно в пиве, вине может вызывать гипертензивные реакции.
Местноанестезирующие средства, содержащие эпинефрин (адреналинª) или кокаин - при одновременном применении с прокарбазином возможна выраженная артериальная гипертензия.
Средства для спинномозговой анестезии - усиление гипотензивных эффектов.
Антихолинергические средства или другие препараты с антихолинергической активностью, антигистаминные средства - возможно усиление антихолинергических эффектов в связи с вторичной антихолинергической активностью ингибиторов МАО; кроме того, ингибиторы МАО могут блокировать обезвреживание антихолинергических средств, что усиливает их действие.
Антикоагулянты (производные кумарина и индандиона) - усиление антикоагулянтной активности.
Противосудорожные средства - усиление угнетающего действия на ЦНС, а также изменение типа эпилептиформных припадков.
Пероральные противодиабетические средства или инсулин - прокарбазин может усиливать гипогликемические эффекты; во время или после такой комбинированной терапии требуется снижение дозы гипогликемического средства.
Антигипертензивные средства, диуретические средства и другие лекарственные средства, вызывающие гипотензию - усиление гипотензивного эффекта.
Лекарственные средства, вызывающие патологические изменения показателей крови, - при одновременном или недавно проводившемся лечении данными препаратами лейкопеническое и/или тромбоцитопеническое действие может усиливаться. При необходимости корректировку дозы прокарбазина проводят на основании результатов анализа крови.
Другие лекарственные средства, вызывающие угнетение функции костного мозга, или лучевая терапия - возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких лекарственных средств, вызывающих угнетение функции костного мозга, а также лучевой терапии необходимо снижение дозы прокарбазина.
Бромокриптин (парлоделª) - повышение концентрации пролактина в сыворотке крови и снижение эффектов бромокриптина, необходима корректировка дозы бромокриптина.
Буспирон - одновременное применение прокарбазина с ингибиторами МАО не рекомендуют в связи с возможным повышением артериального давления.
Кофеинсодержащие вещества - при одновременном потреблении избыточного количества кофеина, содержащегося в шоколаде, кофе, чае или тонизирующих напитках, возможно развитие опасных аритмий или тяжёлой гипертензии из-за симпатомиметических эффектов кофеина.
Средства, вызывающие угнетение ЦНС - усиление угнетения ЦНС и ортостатической гипотензии.
Одновременное применение с антигистаминными средствами не рекомендуют.
Флуоксетин - возможны спутанность сознания, ажитация, двигательное беспокойство и симптомы нарушения функций ЖКТ, периоды гиперпирексии, тяжёлые судороги и гипертонические кризы.
Гуанетидин или алкалоиды раувольфии - во время и в течение одной недели после терапии прокарбазином парентеральное применение данных лекарственных средств не рекомендуют из-за возможности резкого высвобождения накопившихся катехоламинов и гипертензивной реакции.
Галоперидол, локсапин, фенотиазины, пимозид или тиоксантены - увеличение продолжительности и усиление седативного, гипотензивного и антихолинергического эффектов данных лекарственных средств и прокарбазина.
Метилдопа - повышенная возбудимость, кроме того, имеются сообщения о возникновении головной боли, тяжёлой гипертензии и галлюцинаций.
Метилфенидат - усиление стимулирующего действия метилфенидата на ЦНС, приводящее к гипертоническому кризу. Метилфенидат не следует назначать во время или в течение 14 дней после использования прокарбазина.
Триптофан - при одновременном применении с ингибиторами МАО возможны гиперрефлексия, дрожание, гипервентиляция, гипертермия, маниакальное или гипоманиакальное состояния, дезориентация или спутанность сознания. При добавлении триптофана к уже применяемой схеме лечения ингибитором МАО, следует начинать с низких доз лекарственного средства и увеличивать дозу постепенно при тщательном мониторировании психического статуса и артериального давления.
Продукты питания и напитки, содержащие тирамин или другие амины с высокой сосудосуживающей активностью (например, выдержанный сыр, пиво, слабоалкогольное или безалкогольное пиво, красные и белые вина, ликёры; дрожжевые/белковые экстракты, фасоль или зелёные бобы, копчёное или маринованное мясо, ферментированное мясо и любые перезрелые фрукты, ферментированная колбаса: болонская, копчёная, салями), - внезапные и тяжёлые гипертензивные реакции, длящиеся в течение нескольких часов, легко поддающиеся лечению фентоламином. Тяжесть реакций зависит от дозы тирамина, скорости опорожнения желудка и длительности интервала между приёмом прокарбазина и потреблением тирамина. После прекращения применения прокарбазина необходимы ограничения в диете в течение, по крайней мере, ещё двух недель; другие тирамин- или аминсодержащие продукты питания с высокой сосудосуживающей активностью, такие как йогурт, сметана, сливочный сыр, прессованный творог, шоколад или соевый соус, при употреблении в свежем виде и в умеренном количестве не вызывают тяжёлых осложнений).
Резюме и дополнительные сведения
Больным, получающим прокарбазин, необходимо наблюдение врача, имеющего опыт проведения химиотерапии.
Существует ряд схем и режимов применения прокарбазина в отдельности или в комбинации с другими противоопухолевыми препаратами. Дозу прокарбазина необходимо подбирать с учётом индивидуальных особенностей каждого больного, клинической эффективности, выраженности оксического действия лекарственного средства.
Лечение прокарбазином рекомендуют немедленно прекратить при возникновении любого из следующих неблагоприятных эффектов: аллергической реакции, диареи, тромбоцитопении и склонности к кровотечению или кровоизлиянию, выраженной лейкопении, стоматита.
При удовлетворительных результатах клинического обследования и лабораторных исследований лечение можно возобновить, используя прокарбазин в редуцированной дозе.
В связи с риском повышенного токсического действия на костный мозг прокарбазин рекомендуют назначать спустя месяц после проведения лучевой терапии или химиотерапии с использованием препаратов, вызывающих угнетение функции костного мозга,.
При развитии у больного тромбоцитопении в результате применения прокарбазина необходимо соблюдать особые меры предосторожности:
-
регулярно осматривать места внутривенного введения препаратов, кожу и слизистые оболочки для определения признаков кровотечения или кровоизлияний;
-
ограничить частоту венепункций и отказаться от внутримышечных инъекций;
-
анализ мочи, рвотных масс, кала и секретов на скрытую кровь;
-
осторожно пользоваться зубной щёткой, нитью для чистки межзубных промежутков, зубочистками, безопасной бритвой и ножницами для стрижки ногтей;
-
избегать занятий контактными видами спорта или других ситуаций, при которых возможны кровоизлияния или травмы.
Больным с тромбоцитопенией могут потребоваться переливания тромбоконцентрата. Из-за риска желудочно-кишечных кровотечений им необходимо отказаться от приёма алкоголя и аспирина.
При развитии лейкопении необходимо тщательное наблюдение за пациентом для определения признаков возникновения инфекции. Следует избегать контактов с больными бактериальными инфекциями. При возникновении фебрильной нейтропении показано парентеральное применение антибиотиков широкого спектра действия (до получения результатов бактериологических исследований и соответствующих диагностических тестов).
Исследований по применению прокарбазина у детей не проведено. Однако специфических педиатрических проблем, ограничивающих применение этого препарата у детей, не отмечают.
Несмотря на то что соответствующих исследований с использованием прокарбазина у пожилых людей не проведено, вероятность увеличения частоты острых сосудистых нарушений (особенно при внезапных приступах артериальной гипертензии), повышенная чувствительность к гипотензивным эффектам и снижение активности метаболизма препятствуют применению ингибиторов МАО в качестве препаратов первого ряда у больных старше 60 лет. При назначении ингибитора МАО больным пожилого возраста, необходимо принимать во внимание наличие депрессии в анамнезе, способность больного выполнять инструкции врача и возможные взаимодействия лекарственных средств. Кроме того, у пожилых больных более вероятны возрастные нарушения функций почек, что может потребовать использования более низкой дозы или, в тяжёлых случаях, отказа от применения прокарбазина.
Код АТХ
L01XB01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Procarbazine: Натуланª /Natulan/ (Швеция).
Форма выпуска:
Упаковка и хранение
Хранить при температуре <40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Держать в хорошо закрытой, светонепроницаемой упаковке.
Темозоломид (Temozolomide)
Фармакологический/химический класс АТХ
3,4-Дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксамид.
Терапевтический класс АТХ
Противоопухолевый препарат, алкилирующее соединение.
Механизм действия
При попадании в системный кровоток темозоломид подвергается быстрому химическому превращению с образованием активного соединения - монометилтриазеноимидазолкарбоксамида. Считается, что цитотоксичность монометилтриазеноимидазолкарбоксамида обусловлена в первую очередь алкилированием гуанина в положении О6 и дополнительным алкилированием в положении N7. По-видимому, цитотоксические повреждения, возникающие вследствие этого, запускают механизм аберрантного восстановления метилового остатка.
Фармакокинетика
После приёма внутрь темозоломид быстро всасывается. Максимальная концентрация в плазме достигается в среднем через 0,5-1,5 ч (самое раннее - через 20 мин). Приём темозоломида вместе с пищей вызывает снижение максимальной концентрации на 33% и уменьшение AUC на 9%. После перорального приёма темозоломида, меченного 14С, средняя степень выведения изотопа 14С с калом в течение 7 дней составляла 0,8%, что свидетельствует о полном всасывании лекарственного средства.
Темозоломид быстро проникает через гемато-энцефалический барьер и попадает в спинномозговую жидкость. Связь с белками плазмы - 10-20%.
Период полувыведения из плазмы составляет около 1,8 ч. Выводится в основном почками. Через 24 ч после приёма внутрь темозоламида приблизительно 5-10% дозы определяют в неизменённом виде в моче; остальную часть - в виде 4-амино-5-имидазол-карбоксамида гидрохлорида или неидентифицированных полярных метаболитов. Клиренс и период полувыведения не зависят от дозы.
Фармакокинетика в особых клинических случаях
Клиренс препарата в плазме не зависит от возраста пациента, наличия нарушений функций почек или курения.
Фармакокинетический профиль препарата у больных с нарушением функций печени слабой или умеренной степени такой же, как у лиц с нормальной функцией печени.
У детей показатель AUC выше, чем у взрослых.
Максимальная переносимая доза у детей и взрослых одинакова - 1 г/м2 на один цикл лечения.
Показания к применению и дозирование
Злокачественная глиома (мультиформная глиобластома или анапластическая астроцитома) - при наличии рецидива или прогрессирования заболевания после стандартной терапии; метастатическая меланома (в качестве первой линии терапии).
Режим дозирования: темозоломид принимают внутрь, натощак, не менее, чем за 1 ч до приёма пищи. Назначенная доза должна быть принята с использованием минимально возможного числа капсул. Капсулы нельзя вскрывать или разжёвывать, их следует проглатывать целиком, запивая стаканом воды.
Взрослые и дети старше 3-х лет
Больным, ранее не подвергавшимся химиотерапии, темозоломид назначают в дозе 200 мг/м2 1 раз в сутки 5 дней подряд с последующим перерывом в течение 23 дней (общая продолжительность одного цикла лечения - 28 дней).
Для больных, ранее проходивших курс химиотерапии, начальная доза - 150 мг/м2 1 раз в сутки; во втором цикле доза может быть повышена до 200 мг/м2 в день при условии, что в первый день следующего цикла абсолютное число нейтрофилов не ниже 1,5x109/л, а число тромбоцитов не ниже 100x109/л. Длительность лечения составляет максимально 2 года. При возникновении признаков прогрессирования заболевания лечение темозоламидом следует прекратить.
Побочные эффекты
Перечисленные ниже побочные эффекты, отмеченные при приёме темозоломида, распределены по частоте возникновения в соответствии со следующей градацией:
Система кроветворения:
При лечении больных с глиомой и метастазирующей меланомой отмечены случаи тромбоцитопении и нейтропении III или IV степени у 19% и 17% при глиоме и у 20% и 22% при меланоме соответственно. Госпитализация больного или/и отмена темозоломида при этом потребовалась в 8% и 4% случаев при глиоме и в 3% и 1,3% при меланоме соответственно. Угнетение костного мозга диагностировали в течение первых нескольких циклов лечения, с максимумом между 21 и 28 днями; восстановление происходило, как правило, в течение 1-2 нед. Признаков кумулятивной миелосупрессии не отмечено.
Пищеварительная система:
Нервная система:
Дерматологические реакции:
Иммунная система:
Прочие:
Передозировка
При использовании лекарственного средства в дозах 500 мг/м2, 750 мг/м2, 1000 мг/м2 и 1250 мг/м2 (суммарная доза, полученная за 5-дневный цикл лечения) дозолимитирующей токсичностью была гематологическая токсичность (наиболее выражена при высоких дозах темозоломида). Описан случай передозировки темозоломида (приём 2 г в сутки в течение 5 дней) с развитием панцитопении, пирексии, полиорганной недостаточности, приведшей к смерти пациента. При приёме препарата более 5 дней (вплоть до 64 дней), в числе других побочных эффектов отмечают угнетение кроветворения, осложнённое или не осложнённое инфекцией, в некоторых случаях - длительное и выраженное, с фатальным исходом.
Лечение: антидот неизвестен. Рекомендуют проведение гематологического контроля и при необходимости - симптоматической терапии.
Противопоказания
Выраженная миелосупрессия; беременность; период лактации (грудного вскармливания); детский возраст до 3 лет; повышенная чувствительность к темозоломиду или другим компонентам препарата, а также к дакарбазину.
С осторожностью следует назначать препарат пациентам старше 70 лет.
Беременность
При проведении доклинических исследований на крысах и кроликах, получавших темозоломид в дозе 150 мг/м2, отмечено тератогенное и токсическое действие лекарственного средства на плод. В связи с этим темозоломид не рекомендуют назначать при беременности.
Мужчинам и женщинам детородного возраста во время лечения темозоломидом, и в течение 6 мес после его окончания необходимо использовать надёжные методы контрацепции.
Кормление грудью
Данных о проникновении темозоломида в грудное молоко нет. Препарат противопоказан к применению в период лактации (грудного вскармливания).
Из-за риска развития необратимого бесплодия на фоне лечения темозоломидом перед началом приёма лекарственного средства с пациентами мужского пола необходимо провести беседу о возможности криоконсервации спермы.
Клинически значимые взаимодействия
Приём темозоломида совместно с ранитидином не приводит к клинически значимому изменению степени всасывания темозоломида.
Дексаметазон, прохлорперазин, фенитоин, карбамазепин, ондансетрон, блокаторы Н2-рецепторов гистамина и фенобарбитал - клиренс темозоломида не изменяется.
Вальпроевая кислота - слабо выраженное, но статистически значимое снижение клиренса темозоломида.
Исследований воздействия темозоломида на метаболизм и выведение других препаратов, не проводилось. В связи с тем, что темозоломид не метаболизируется в печени и слабо связывается с белками, его действие на фармакокинетику других лекарственных средств маловероятно.
Применение темозоломида совместно с другими веществами, угнетающими функции костного мозга, увеличивает вероятность миелосупрессии.
Резюме и дополнительные сведения
Лечение темозоломидом необходимо осуществлять только под контролем врача, имеющего опыт проведения химиотерапии при опухолях головного мозга.
Начинать лечение темозоломидом можно только при абсолютном числе нейтрофилов ³1,5x109/л и тромбоцитов ³100x109/л. Полный клинический анализ крови необходимо выполнить на 22-й день (21-й день после приёма первой дозы), но не позднее 48 ч после этого дня; далее - еженедельно, пока абсолютное число нейтрофилов не станет >1,5x109/л, а число тромбоцитов >100x109/л. При абсолютном числе нейтрофилов <1x109/л или тромбоцитов <50x109/л в ходе любого цикла лечения, доза в следующем цикле должна быть снижена на одну ступень. Возможные дозы: 100 мг/м2, 150 мг/м2 и 200 мг/м2. Минимальная рекомендованная доза - 100 мг/м2.
Если на фоне лечения темозоломидом возникает тошнота или рвота в дальнейшем рекомендуют проводить противорвотную терапию. Противорвотные препараты принимают как до, так и после темозоломида. Если рвота развилась в первые 2 ч после приёма темозоломида, повторять приём препарата в тот же день не следует.
Фармакокинетические показатели темозоломида у лиц с нормальной функцией печени и у больных с нарушением функций печени слабой или умеренной степени тяжести сопоставимы. Данных о применении темозоломида у больных с выраженным нарушением функции печени (класс III по шкале Чайлда-Пью) или нарушением функции почек нет. На основании данных изучения фармакокинетических свойств темозоломида маловероятно, что даже при наличии выраженных нарушений функций печени или почек может потребоваться снижение дозы лекарственного средства. При назначении темозоломида таким больным, а также пожилым пациентам следует проявлять осторожность. У больных пожилого возраста (старше 70 лет) риск развития нейтропении и тромбоцитопении выше, чем у молодых пациентов.
При попадании содержимого капсулы (порошка) на кожу или слизистые оболочки необходимо промыть их большим количеством воды.
Использование в педиатрии
Клинического опыта применения темозоломида при мультиформной глиобластоме у детей до 3 лет и при злокачественной меланоме у детей до 18 лет нет. Существуют данные о применении темозоломида при глиоме у детей старше 3 лет.
Влияние на способность к вождению автотранспорта и управлению автомобилем
Побочные действия препарата, такие как сонливость и чувство усталости, могут отрицательно влиять на способность управления транспортными средствами или выполнения потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Код АТХ
L01AX03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Temozolomide: Темодалª/Temodal (ШЕРИНГ-ПЛАУ, Германия).
Формы выпуска:
Условия и сроки хранения:
Препарат следует хранить в недоступном для детей месте при температуре от 2° до 30°С.
Производные нитрозомочевины
Кармустин (Carmustine)
Фармакологический/химический класс АТХ
1,3-бис-(2-Хлорметил)-1-нитрозомочевина.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Кармустин - алкилирующий препарат группы нитрозомочевины. Кармустин и/или его метаболиты оказывают алкилирующее действие на основания и фосфатные группы ДНК, что приводит к разрывам и сшивкам её молекулы. Циклонеспецифичный препарат. Действие кармустина может быть также связано с модификацией белков.
Фармакокинетика
Препарат проникает через гематоэнцефалический барьер (из-за высокой растворимости в жирах и относительно низкой ионизации при физиологических значениях рН). Быстрая биотрансформация осуществляется в печени с образованием активных метаболитов.
Период полувыведения: биологический - примерно 15-30 мин; химический - около 5 мин. Метаболиты могут сохраняться в плазме крови в течение нескольких суток, что может обусловливать замедленное токсическое действие препарата на кровь.
Выведение: главным образом почками - 60-70% (менее 1% в неизменённом виде); предполагают наличие некоторой кишечно-печёночной циркуляции; через кишечник - 1%; через дыхательные пути - 10% (в виде диоксида углерода).
Показания к применению и дозирование
Кармустин применяют для паллиативного лечения как средство монотерапии или в комбинации в следующих случаях:
Обычная доза для взрослых и подростков: первичные опухоли мозга, рак печени, лимфогранулёматоз, неходжкинские лимфомы, миеломная болезнь или меланома - внутривенно, 150-200 мг/м2 однократно каждые 6-8 нед, или по 75-100 мг/м2 2 дня подряд каждые 6 нед или по 40 мг/м2 5 дней подряд каждые 6 нед. Дозу для повторного введения (не ранее чем через 6 нед) устанавливают с учётом количества лейкоцитов и тромбоцитов в крови.
Побочные эффекты
Примечание: для кармустина характерна отсроченная лейкопения и тромбоцитопения - проявляются примерно через 4-5 нед после начала лечения. Восстановление показателей крови обычно происходит к 6-7 нед лечения. Степень тяжести угнетения функции костного мозга варьирует и определяет дозу кармустина при последующем применении. Жжение в месте инъекции связано с быстрой внутривенной инфузией; случаи истинного тромбоза редки.
Примечание: нефротоксическое действие и почечную недостаточность обычно отмечают у больных, получивших высокие кумулятивные дозы препарата при длительном лечении, но иногда о таких эффектах сообщали и при применении препарата в более низких кумулятивных дозах.
Передозировка
Проявление острой дозолимитирующей токсичности кармустина у человека - миелосупрессия. Основное проявление хронической передозировки препарата - угнетение костномозгового кроветворения и панцитопения.
Антидот неизвестен. При наличии признаков гематологической токсичности проводят соответствующую поддерживающую терапию.
Противопоказания
Необходимо сопоставлять риск и пользу в следующих случаях:
Повышенная чувствительность к кармустину.
Следует также соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию, особенно при облучении области средостения, и у курящих больных из-за возможного повышенного риска токсического действия на лёгкие.
Беременность
Адекватных и строго контролируемых исследований безопасности применения кармустина при беременности у человека не проводили. Есть данные об эмбриотоксическом действии кармустина у человека.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
В дозах, эквивалентных дозе для человека, кармустин оказывает эмбриотоксическое и тератогенное действие у крыс и эмбриотоксическое действие у крыс и кроликов.
Кормление грудью
Проникает ли кармустин в грудное молоко, неизвестно. Хотя информации о проникновении противоопухолевых средств в грудное молоко очень мало, во время применения кармустина грудное вскармливание не рекомендуется из-за возможного риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны на основе их потенциальной клинической значимости.
-
Другие препараты, вызывающие угнетение функции костного мозга или лучевая терапия:
-
при одновременном или последовательном применении нескольких препаратов, вызывающих угнетение функции костного мозга, а также лучевой терапии может потребоваться снижение дозы.
-
Препараты, оказывающие гепатотоксическое или нефротоксическое действие:
-
при одновременном применении с кармустином возможно усиление гепато- или нефротоксического действия;
-
при первых признаках нарушения функции печени или почек применение одного из ЛС или обоих следует прекратить.
Резюме и дополнительные сведения
Больные, получающие кармустин, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии. Используют ряд схем и режимов применения кармустина в отдельности или в комбинации с другими противоопухолевыми препаратами.
Вследствие замедленного и кумулятивного угнетения функции костного мозга, связанного с применением кармустина, препарат следует назначать не чаще 1 раза в 6 нед.
Частоту и продолжительность тошноты и рвоты у некоторых больных можно снизить применением противорвотных средств перед введением кармустина.
Для предотвращения раздражающего действия препарата в месте инъекции растворы для внутривенной инфузии следует вводить в течение 1-2 ч. Кроме того, рекомендуется также до и после введения кармустина промывать систему для проведения инфузии 10 мл 0,9% раствора натрия хлорида для инъекций или 5% раствора декстрозы для инъекций.
У больных с развившейся в результате применения кармустина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности.
Больных с развившейся лейкопенией следует тщательно наблюдать для выявления признаков возникновения инфекции. Может потребоваться использование антибиотиков. У больных с фебрильной нейтропенией парентеральное применение антибиотиков широкого спектра действия необходимо начинать эмпирически, до получения результатов бактериологических исследований и соответствующих диагностических тестов.
Если при внутривенном введении раствора происходит образование инфильтрата, возможно местное повреждение тканей и рубцевание.
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии.
Возможные отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств. Влияние дозы и продолжительности лечения также неизвестно, но, вероятно, риск повышается при длительном применении. Хотя информация ограничена, имеющиеся данные позволяют предположить, что риск канцерогенного действия наиболее высок при использовании алкилирующих препаратов. При введении в дозах, близких к клиническим, кармустин оказывает канцерогенное действие у крыс и мышей, а его применение у человека сопровождалось развитием вторичных злокачественных опухолей, включая острый лейкоз.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Carmustine:
Форма выпуска: лиофилизированный порошок для инъекционных растворов во флаконах по 0,1 г в комплекте с растворителем (3 мл).
Хранить при температуре 2-8 °С, если производителем не указано иначе. При температуре 30,5-32,0 °С или выше происходит разложение и расплавление препарата с образованием масляной пленки на дне флакона; при этом флакон следует ликвидировать.
Примечание. Избегать попадания приготовленного раствора на кожу или в глаза, это может вызывать ожог или окрашивание кожи в коричневый цвет. При случайном попадании раствора на кожу или слизистую оболочку повреждённый участок следует немедленно и тщательно промыть водой с мылом.
Ломустин (Lomustine)
Фармакологический/химический класс АТХ
1-(2-Хлорэтил)-3-циклогексил-1-нитрозомочевина.
Терапевтический класс АТХ
Противоопухолевое средство алкилирующего действия.
Механизм действия
Ломустин - алкилирующий препарат группы нитрозомочевины. Ломустин (и/или его метаболиты) нарушает функции ДНК и РНК за счёт ингибирования синтеза ДНК путём подавления ключевых ферментативных процессов. Циклонеспецифичный препарат.
Фармакокинетика
После приёма внутрь ломустин хорошо и быстро всасывается из ЖКТ. Проникает через гематоэнцефалический барьер. Связывание с белками умеренное - около 50%. Быстро метаболизируется в печени с образованием активных метаболитов.
Период полувыведения: биологический - около 94 мин, химический - примерно 15 мин, метаболиты: длительный - 16-48 ч.
Выведение: почками (полностью в виде метаболитов), предполагают некоторую кишечно-печёночную циркуляцию, через кишечник (менее 5%), через дыхательные пути (10%).
Показания к применению и дозирование
-
Первичные опухоли мозга. Ломустин применяют для лечения как первичных, так и метастатических опухолей мозга у больных, уже получивших соответствующее хирургическое лечение и/или прошедших курс лучевой терапии.
-
Лимфогранулематоз. Ломустин применяют для лечения лимфогранулематоза в качестве терапии второй линии в комбинации с другими препаратами у больных с рецидивами в период начального лечения или при отсутствии эффекта в начальной терапии.
Обычная доза для взрослых и подростков: в монорежиме - внутрь, 100-130 мг/м2 однократно каждые 6 нед; в комбинации с другими препаратами ломустин применяют в более низкой дозе.
Примечание: У больных с угнетением функции костного мозга дозу снижают до 100 мг/м2, назначают однократно с повторением через 6 нед.
Побочные эффекты
Примечание: развитие лейкопении и тромбоцитопении отмечается примерно через 4 недели после приёма и сохраняется в течение 1-2 нед. Восстановление показателей периферической крови обычно происходит в течение 6-7 нед после приёма препарата. Степень тяжести угнетения функции костного мозга варьирует и определяет дозу ломустина при последующем приёме. Тошнота и рвота возникают через 3-6 ч после применения ЛС и обычно продолжаются менее 24 ч.
Примечание: токсическое действие на лёгкие отмечают при кумулятивных дозах 600-1240 мг или лечении в течение 6 мес и более.
Передозировка
Проявление острой дозолимитирующей токсичности ломустина у человека - миелосупрессия. Основное проявление хронической передозировки препарата - угнетение костномозгового кроветворения и панцитопения.
Антидот неизвестен. При наличии признаков гематологической токсичности проводят соответствующую поддерживающую терапию.
Противопоказания
Необходимо сопоставлять риск и пользу в следующих случаях:
Следует также соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Повышенная чувствительность к ломустину.
Беременность
Адекватных и строго контролируемых исследований безопасности в период беременности у человека не проведено. Рекомендуется избегать применения препарата в период беременности.
Как правило, в период лечения цитотоксическими препаратами рекомендуется применение противозачаточных средств.
Кормление грудью
Ломустин проникает в грудное молоко. Во время проведения химиотерапии грудное вскармливание следует прекратить из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
-
Другие препараты, вызывающие угнетение функции костного мозга или лучевая терапия:
-
Инактивированные и живые вирусные вакцины:
-
в связи с тем, что при лечении ломустином возможно подавление естественных защитных механизмов, выработка антител в организме больного в ответ на введение вакцины может снижаться;
-
при одновременном применении с живой вирусной вакциной возможны интенсификация процесса репликации вакцинного вируса, усиление его побочных/неблагоприятных эффектов и/или снижение выработки антител в организме больного в ответ на введение вакцины.
-
Примечание. Интервал между прекращением применения иммунодепрессантов и восстановлением способности больного реагировать на вакцину зависит от дозы и типа используемого иммунодепрессанта, основного заболевания и других факторов. По оценкам, этот интервал варьирует от 3 мес до 1 г; кроме того, иммунизацию пероральной вакциной против полиомиелита людей, находящихся в близком контакте с таким больным, особенно членов семьи, следует отсрочить.
Резюме и дополнительные сведения
Больные, получающие ломустин, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии.
Лечение ломустином продолжают, пока препарат оказывает терапевтическое действие. При отсутствии эффекта после 2 циклов терапии эффективность препарата маловероятна.
Частоту и продолжительность тошноты и рвоты у некоторых больных можно снизить назначением противорвотных средств до применения ломустина.
Вследствие замедленного и кумулятивного угнетения функции костного мозга, связанного с применением препарата, ломустин следует назначать не чаще 1 раза в 6 нед.
У больных с развившейся в результате применения ломустина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности.
Больных с развившейся лейкопенией следует тщательно наблюдать для выявления признаков возникновения инфекции. Может потребоваться использование антибиотиков. У больных с фебрильной нейтропенией парентеральное применение антибиотиков широкого спектра действия необходимо начинать эмпирически, до получения результатов бактериологических исследований и соответствующих диагностических тестов.
Возможные отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств. Влияние дозы и продолжительности лечения также неизвестно, но, вероятно, риск повышается при длительном применении. Хотя информация ограничена, имеющиеся данные позволяют предположить, что риск канцерогенного действия наиболее высок при использовании алкилирующих препаратов. Сообщалось, что длительное применение производных нитрозомочевины у человека, возможно, связано с развитием вторичных злокачественных заболеваний (острый лейкоз) и дисплазии костного мозга.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Lomustine:
Форма выпуска: таблетки по 0,04 г (40 мг) (№ 50); капсулы по 0,01; 0,04 и 0,1 г (№ 20).
Хранить при температуре ниже 40 °С, предпочтительно при 15-30 °С, в хорошо закрытой упаковке, если производителем не указано иначе.
Фотемустин (Fotemustine)
Фармакологический/химический класс АТХ
(±)-Диэтил-[1-[3-(2-хлорэтил)-3-нитрозоуреидо]этил]фосфонат.
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Цитостатический противоопухолевый препарат из группы производных нитрозомочевины с алкилирующим и карбамилирующим действием. Химическая структура ЛС включает биоизомер аланина (амино-1-этилфосфоновая кислота), который облегчает проникновение препарата в клетки и через гематоэнцефалический барьер.
Фармакокинетика
После внутривенного введения фармакокинетика фотемустина носит моно- или биэкспоненциальный характер с коротким периодом полувыведения. Связывание с белками плазмы невелико (25-30%).
Фотемустин проникает через гематоэнцефалический барьер.
Показания к применению и дозирование
Режим дозирования: фотемустин вводят внутривенно. Лечение больного можно начинать, если количество тромбоцитов ³100x109/л и гранулоцитов ³2x109/л (табл. 8-2).
Между началом индукционной терапии и началом поддерживающей терапии рекомендуется интервал 5 нед, между двумя циклами поддерживающей терапии - 3 нед.
Монотерапия: препарат вводят в дозе 100 мг/м2.
Индукционная терапия: 3 последовательных инъекции с интервалом в 1 нед (1, 8 и 15 день) и последующим перерывом в 4-5 нед.
Поддерживающая терапия: 1 инъекция в 3 нед.
В процессе лечения фотемустином необходимо контролировать количество тромбоцитов, лейкоцитов и гранулоцитов в крови. В случае развития гематологической токсичности доза мюстофоранаª может быть уменьшена, либо введение препарата следует отложить в соответствии со следующей схемой.
Таблица 8-2. Дозирование фотемустина в зависимости от данных общего анализа крови
| Количество клеток крови | % от предыдущей дозы |
|---|---|
Гранулоциты >2000/мкл и |
100% |
Гранулоциты >1500-2000/мкл и/или |
75% |
Гранулоциты >1000-1500/мкл и |
50% |
Гранулоциты ≤1000/мкл и/или |
отложить введение очередной дозы |
Побочные эффекты
Передозировка
Специфического антидота нет. В случае передозировки необходимо отменить препарат, назначить поддерживающую терапию и усилить контроль гематологических показателей.
Противопоказания
Препарат не следует назначать ранее чем через 3 нед после введения дакарбазина из-за риска развития респираторного дистресс-синдрома взрослых.
Беременность и кормление грудью
Фотемустин противопоказан к применению при беременности. При необходимости назначения ЛС в период лактации следует прекратить грудное вскармливание.
Клинически значимые взаимодействия
При одновременном применении (в один день) фотемустина и дакарбазина в высоких дозах отмечены отдельные случаи респираторного дистресс-синдрома взрослых. При необходимости применения комбинированной терапии этими препаратами следует точно соблюдать рекомендуемый режим дозирования.
Во время и после лечения (не менее 3 мес) фотемустином следует избегать вакцинации живыми и ослабленными вакцинами.
При одновременном применении фотемустина и фенитоина концентрация последнего в сыворотке крови может снижаться.
Резюме и дополнительные сведения
Способность препарата угнетать кроветворение усиливается, если одновременно или ранее применяли вещества, угнетающие гемопоэз. Не рекомендуется назначать препарат, если после предшествующего лечения химиотерапевтическими средствами прошло менее 4 нед (а в случае лечения препаратами нитрозомочевины - 6 нед).
Мужчины и женщины во время и не менее 6 мес после окончания терапии должны использовать надёжные методы контрацепции.
Следует избегать попадания препарата на кожу и слизистые оболочки. При случайном попадании на кожу и слизистые оболочки их следует тщательно промыть водой с мылом, при попадании в глаза - большим количеством воды. Следует избегать вдыхания препарата.
Во время приготовления раствора фотемустина рекомендуется работать в маске и латексных перчатках. Беременным женщинам запрещено работать с фотемустином.
При работе с фотемустином следует соблюдать необходимые правила использования и уничтожения цитотоксических препаратов.
Контроль лабораторных показателей:
Эффективность и безопасность применения фотемустина у детей не изучена.
Код АТХ
L01AD05
Торговые наименования, форма выпуска и производители
Используемые в России торговые наименования Fotemustine:
Форма выпуска: порошок для приготовления раствора для инфузий по 208 мг во флаконе.
Препарат следует хранить в защищенном от света месте при температуре 2-8°C. Срок годности - 2 г.
Готовый раствор следует использовать сразу же после приготовления.
Антиметаболиты
Антагонисты фолиевой кислоты
Пеметрексед (Pemetrexed)
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Пеметрексед - антифолат, ингибирующий ключевые в биосинтезе тимидиновых и пуриновых нуклеотидов фолат-зависимые ферменты: тимидилатсинтетазу, дигидрофолатредуктазу, глицинамидрибонуклеотидформилтрансферазу (ГАРФТ). Препарат поступает в клетки посредством белковых фолат-связывающих транспортных систем и переносчика восстановленных фолатов. Попав в клетку, быстро и эффективно с помощью фермента фолилполиглутаматсинтетазы превращается в полиглутаматные формы (более мощными ингибиторы тимидилатсинтетазы и ГАРФТ), которые задерживаются в клетках. Полиглутамация - процесс, зависимый от времени и концентрации, встречающийся в опухолевых клетках и, в меньшей степени, в нормальных тканях. У полиглутамированных метаболитов увеличен T1/2, поэтому препарат действует продолжительно.
Фармакологические эффекты
Фармакокинетика
Около 81% препарата связывается с белками плазмы крови. Пеметрексед незначительно метаболизируется печенью, 70-90% выводится почками в неизменённом виде в течение первых 24 ч. Общий плазменный клиренс пеметрекседа составляет 92 мл/мин, T1/2 составляет 3,5 ч (у пациентов с нормальной функцией почек).
При почечной недостаточности тяжёлой степени связывание с белками плазмы не изменяется.
Показания к применению и дозирование
Показания.
Препарат вводят внутривенно, капельно в течение 10 мин.
Злокачественная мезотелиома плевры
Комбинированная терапия с цисплатином: рекомендованная доза пеметрекседа - 500 мг/м2 (расчёт на площадь поверхности тела) в первый день каждого 21-дневного цикла. Цисплатин вводят в дозе 75 мг/м2 инфузионно в течение 2 ч на фоне гидратации (в соответствии с инструкцией по применению) приблизительно через 30 мин после пеметрекседа, в первый день каждого 21-дневного цикла.
Немелкоклеточный рак лёгкого
Рекомендованная доза пеметрекседа - 500 мг/м2 в первый день каждого 21-дневного цикла.
Для снижения частоты и выраженности кожных реакций за день до начала лечения пеметрекседом назначают дексаметазон в дозе 4 мг 2 раза в сутки.
Для уменьшения токсичности пеметрекседа назначают препараты фолиевой кислоты или мультивитамины, содержащие суточную дозу фолиевой кислоты. Фолиевую кислоту в суточной дозе (от 350 мкг до 1000 мкг, в среднем 400 мкг) следует назначать как минимум 5 дней в течение 7 дней перед первым введением пеметрекседа, и применение в таких дозах следует продолжать во время всего цикла лечения и в течение 21 дня после последнего введения пеметрекседа. В течение недели до начала терапии пациентам необходимо однократно ввести витамин В12 в дозе 1 мг, внутримышечно и затем повторять процедуру через каждые 3 цикла лечения. В последующем применять витамин В12 в той же дозе можно в день введения пеметрекседа.
Рекомендации по снижению дозы препарата
Дозу препарата перед повторными курсами корректируют с учётом минимальных пороговых значений гематологических показателей или на основе максимально выраженной негематологической токсичности в течение предыдущего цикла лечения.
При ухудшении состояния здоровья, обусловленного токсичностью препарата, лечение может быть отсрочено. По мере восстановления терапию следует продолжить в соответствии с рекомендациями, приведёнными в табл. 8-3.
В случае гематологической токсичности рекомендованная коррекция доз пеметрекседа и цисплатина представлена в табл. 8-3.
Таблица 8-3. Коррекция доз препаратов в случае гематологической токсичности
| Гематологическая токсичность | Коррекция дозы |
|---|---|
Минимальное содержание нейтрофилов 500 клеток/мкл и минимальное содержание тромбоцитов ≥50 000 клеток/мкл |
75% предыдущей дозы (оба препарата) |
Минимальное содержание тромбоцитов ≤50 000 клеток/мкл независимо от минимального содержания нейтрофилов |
50% предыдущей дозы (оба препарата) |
При развитии негематологической токсичности (исключая нейротоксичность) ≥III степени (за исключением повышения уровня трансаминаз III степени) введение пеметрекседа необходимо отложить до восстановления показателей, соответствующих уровню "до лечения". Далее терапию продолжают в соответствии с рекомендациями, приведёнными в табл. 8-4.
Таблица 8-4. Режим дозирования препаратов пеметрекседа (при монотерапии или при комбинированной терапии) и цисплатина.
| Негематологическая токсичностьa,b | Доза пеметрекседа | Доза цисплатина |
|---|---|---|
Любая токсичность IIIc или IV степени, за исключением воспаления слизистой оболочки |
75% предыдущей дозы |
75% предыдущей дозы |
Диарея, требующая госпитализации (независимо от степени), либо диарея III-IV степени |
75% предыдущей дозы |
75% предыдущей дозы |
Воспаление слизистой оболочки III или IV степени |
50% предыдущей дозы |
100% предыдущей дозы |
a NCI CTC (Критерий Общей Токсичности);
b исключая нейротоксичность;
с за исключением повышения уровня трансаминаз III степени.
В случае нейротоксичности рекомендованная коррекция доз пеметрекседа и цисплатина представлена в табл. 8-5. При нейротоксичности III или IV степени лечение отменяют.
Таблица 8-5. Коррекция доз препаратов в случае нейротоксичности
| Степень нейротоксичности | Доза пеметрекседа | Доза цисплатина |
|---|---|---|
0-I |
100% предыдущей дозы |
100% предыдущей дозы |
II |
100% предыдущей дозы |
50% предыдущей дозы |
Пеметрексед отменяют, если у пациента после двух снижений доз отмечены проявления гематологической и негематологической токсичности III-IV степени (за исключением повышения уровня трансаминаз III степени) или при наличии нейротоксичности III-IV степени.
Нет данных о риске побочных эффектов у пациентов от 65 лет и старше. Режим снижения доз соответствует общим рекомендациям.
У пациентов с нарушением функции почек при клиренсе креатинина (КК) не менее 45 мл/мин корректировать дозу и режим введения препарата не требуется. При КК менее 45 мл/мин применение пеметрекседа не рекомендуется (недостаточно данных о его влиянии на эту категорию пациентов).
Недостаточно данных об эффективности препарата у пациентов с нарушением функции печени при увеличении содержания билирубина более чем в 1,5 раза от верхней границы нормы (ВГН); повышении активности трансаминаз более чем в 3 раза от ВГН (при отсутствии метастазов в печени) или более чем в 5 раз от ВГН (при наличии метастазов в печени).
Побочные эффекты
Побочные эффекты, наблюдавшиеся при монотерапии пеметрекседом с добавлением фолиевой кислоты и витамина В12ª, изложены в соответствии со следующей частотой:
В скобках указана частота токсичности (в процентах) всех степеней/III-IV степени соответственно.
Со стороны системы кроветворения
Очень часто:
Часто - тромбоцитопения (7,0-8,3%/1,9-2,3%).
Со стороны пищеварительной системы
Очень часто:
Часто - запоры, боль в животе.
Дерматологические реакции
Очень часто - сыпь/шелушение (14-15,9%/0-0,2%).
Часто - кожный зуд, алопеция.
Редко - мультиформная эритема.
Со стороны периферической нервной системы
Часто - сенсорная или моторная невропатии.
Со стороны мочевыделительной системы
Часто - повышение уровня креатинина.
Со стороны сердечно-сосудистой системы
Редко - наджелудочковая тахикардия.
Прочие
Очень часто - повышенная утомляемость (34%/4,7-5,3%).
Часто - лихорадка, фебрильная нейтропения, аллергические реакции и присоединение вторичных инфекций без нейтропении.
Передозировка
Симптомы
Угнетение функции костного мозга, проявляющееся нейтропенией, тромбоцитопенией и анемией. Также могут развиться диарея, воспаление слизистых оболочек, сыпь и вторичная инфекция.
Лечение
Симптоматическое, включая немедленное применение лейковоринаª или тимидинаÃ.
Противопоказания
Беременность, лактация, повышенная чувствительность к пеметрекседу или вспомогательным веществам в составе препарата.
Резюме и дополнительные сведения
Препарат должен назначать врач, имеющий опыт применения противоопухолевых лекарственных средств.
Пеметрексед может угнетать костномозговое кроветворение, что проявляется нейтропенией, тромбоцитопенией и анемией (обычно вызывает миелодепрессию, что требует ограничения дозы).
Перед каждым введением пеметрекседа необходимо делать общий анализ крови с подсчётом лейкоцитарной формулы и количества тромбоцитов.
Для оценки функции почек и печени периодически берут кровь на биохимический анализ.
Перед началом лечения абсолютное количество нейтрофилов должно быть не меньше 1,5x109/л, а тромбоцитов - не менее100x109/л.
Назначение фолиевой кислоты и витамина В12ª снижает токсичность пеметрекседа, и уменьшает необходимость редукции дозы при гематологической и негематологической токсичности III-IV степени (нейтропения, фебрильная нейтропения и инфекция с нейтропенией III-IV степени).
Больным с клиническими проявлениями асцита и плеврита перед началом терапии пеметрекседом необходимо дренирование полостей.
Пеметрексед не рекомендуется применять у детей (нет данных о безопасности и эффективности).
Клинически значимые взаимодействия
Совместное применение с нефротоксичными препаратами и/или веществами, выводящимися почками, может снизить клиренс пеметрекседа.
Результаты исследований in vitro свидетельствуют, что пеметрексед минимально взаимодействует с препаратами, которые метаболизируются CYP3A, CYP2D6, CYP2C9, CYP1A2.
Фармакокинетика пеметрекседа не меняется при применении фолиевой кислоты внутрь, витамина В12ª внутримышечно и при комбинированном применении c цисплатином (in vitro наблюдали синергизм противоопухолевого действия).
У больных с нормальной функцией почек (КК ≥80 мл/мин) пеметрексед можно применять совместно с ибупрофеномª (по 400 мг 4 раза в сут), однако при почечной недостаточности лёгкой или средней степеней тяжести (КК 45-79 мл/мин) следует соблюдать осторожность.
У пациентов с почечной недостаточностью лёгкой и срёдней степеней тяжести не рекомендуют в течение двух дней перед введением пеметрекседа, в день введения и в течение двух дней после него применять нестероидные противовоспалительные средства (НПВС) с коротким периодом полувыведения (T1/2).
НПВС с большим T1/2 отменяют минимум за 5 дней до приёма пеметрекседа, в день приёма и в течение двух дней после него (нет данных о возможном взаимодействии между препаратами). Если требуется совместное назначение с НПВС, пациентам необходим строгий мониторинг токсичности (особенно миелосупрессии и токсичности со стороны ЖКТ).
Пеметрексед несовместим с раствором Рингера лактатаª и раствором Рингераª. Совместное назначение пеметрекседа с другими препаратами и растворами не исследовано и поэтому не рекомендуется.
Код АТХ
L01BA04
Торговые наименования, форма выпуска и производители
Используемые в России торговые наименования Pemetrexedi
Форма выпуска
Лиофилизат для приготовления раствора для инфузий, 500 мг во флаконе.
Условия и сроки хранения
Хранить в недоступном для детей месте при температуре от 15 до 25 °С. Готовый раствор хранить при температуре от 2 до 8 °C или от 15 до 25 °С не более 24 ч.
Метотрексат (Methotrexate)
Фармакологический/ химический класс АТХ
4-Амино-N 10-метилптероилглутаминовая кислота или (дезокси-4-амино-N метилфолиевая кислота).
Терапевтический класс АТХ
Противоопухолевое средство из группы антиметаболитов.
Механизм действия
Метотрексат - антиметаболит из группы аналогов фолиевой кислоты; S-фазоспецифичный препарат. В основе механизма действия лежит ингибирование синтеза пуриновых нуклеотидов, тимидилата и белка в результате относительно необратимого связывания с дигидрофолатредуктазой, что препятствует восстановлению дигидрофолата в активный тетрагидрофолат. Метотрексат в основном действует на быстро пролиферирующие клетки (злокачественные клетки, клетки костного мозга; клетки плода; сперматогонии; клетки слизистых оболочек полости рта, кишечника и мочевого пузыря).
Препарат также обладает слабовыраженной иммунодепрессивной активностью.
Фармакологические эффекты
Физико-химические свойства
Молекулярная масса - 454,44.
Фармакокинетика
Всасывание препарата вариабельно. Ограниченно (дозозависимо) проникает через гематоэнцефалический барьер, однако после интратекального введения в значительных количествах поступает в системный кровоток. Связывание с белками умеренное (примерно 50%), в основном с альбуминами. Биотрансформируется в печени, внутриклеточно, с образованием задерживающихся в клетках полиглутаматов.
Конечный T1/2:
Примечание
Существует широкая вариабельность скорости клиренса препарата: малые количества метотрексата и его метаболитов могут удерживаться тканями (почками, печенью) от нескольких недель до нескольких месяцев; наличие жидкости (асцит или выпот в плевральной полости при опухоли) будет также замедлять клиренс. При приёме внутрь концентрации препарата в сыворотке крови достигает максимума через 1-2 ч, а при внутримышечном введении - через 30-60 мин. В течение 24 ч после введения первой дозы 80-90% препарата выводиться почками в неизменённом виде и до 10% - с желчью. При повторном введении отмечают накопление полиглутаматов в тканях.
Показания к применению и дозирование
Показания
Дозирование
Хорионаденома или пузырный занос (в том числе деструирующий)
Внутрь 15-30 мг в сутки, в течение пяти дней. Повторные циклы с интервалом 1-2 нед. Обычно после нормализации концентрации ХГЧ в моче проводят ещё 1-2 цикла.
Лимфобластный лейкоз
Начальная доза - 3,3 мг/м2 в сутки, внутрь, в комбинации с преднизоном или другими препаратами. Поддерживающая доза - 30 мг/м2 в неделю, внутрь или внутривенно, по 2,5 мг/кг каждые 14 дней.
Лимфома
Внутрь всего 625 мкг/кг (по 2,5 мг/кг в сутки).
Грибовидный микоз
Внутрь по 2,5-10 мг в сутки в течение нескольких недель или месяцев.
Остеогенная саркома
Внутривенная инфузия (в течение 6 ч) в дозе 12 г/м2, с последующим введением лейковоринаª в качестве антидота каждые 6 ч в течение суток после инфузии метотрексата (до 10 введений, доза зависит от концентрации метотрексата в сыворотке крови).
Обычная доза для детей
Как противоопухолевое средство - внутримышечно, 20-40 мг/м2 раз в неделю.
Лейкозная инфильтрация мозговых оболочек (лечение до тех пор, пока число клеток в спинномозговой жидкости не достигнет нормального уровня):
Беременность
Противопоказан при беременности! Метотрексат способен стимулировать аборт; проходя через плаценту, оказывает неблагоприятное воздействие на плод.
В период лечения метотрексатом женщины детородного возраста должны использовать надёжные методы контрацепции.
кормление грудью
Препарат проникает в грудное молоко, поэтому при необходимости применения в период лактации следует прекратить грудное вскармливание из-за риска для детей (мутагенное и канцерогенное действие).
Побочные эффекты
Встречаются чаще:
Встречаются более часто:
Примечание
Гиперурикемия и нефропатия, связанные с повышенным образованием мочевой кислоты, чаще возникают в начальный период лечения больных лейкозом или лимфомой. В результате быстрого распада клеток концентрация мочевой кислоты в сыворотке крови повышается. При терапии высокими дозами симптомы, сходные с таковыми вышеописанной нефропатии, могут быть обусловлены повреждением почечных канальцев вследствие осаждения препарата или его метаболитов в моче.
Встречаются реже (в основном при длительном ежедневном применении):
Встречаются реже (в основном при интратекальном введении или длительном применении в высоких дозах):
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу.
-
Тошнота и рвота (потеря жидкости - обезвоживание - может привести к усилению токсического действия метотрексата).
-
Больным с нарушением функции почек (возможно нарушение выведения метотрексата и его накопление; риск токсического действия повышается) рекомендуют более низкую дозировку и тщательное мониторирование концентрации препарата в сыворотке крови;
-
Ветряная оспа (включая недавний контакт с больным) или опоясывающий герпес (риск развития тяжёлого генерализованного заболевания).
-
Подагра или почечные конкременты (ураты) в анамнезе (риск гиперурикемии).
-
Язвенная болезнь желудка и двенадцатиперстной кишки, язвенный колит.
Применение метотрексата у больных, ранее получавших цитотоксические препараты или лучевую терапию, даже в низких дозах может приводить к выраженной миелосупрессии и воспалению слизистых оболочек. Наряду с тщательным мониторированием концентрации препарата могут быть необходимы более высокие дозы и/или увеличение продолжительности применения кальция фолината (лейковоринаª).
Клинически значимые взаимодействия
Ацикловир для парентерального применения
Применять с осторожностью, одновременное введение метотрексата (интратекально) и ацикловира может вызвать неврологические нарушения.
Алкоголь или другие препараты, обладающие гепатотоксическим действием
При одновременном применении возможен риск гепатотоксического действия.
Аллопуринол, колхицин, пробенецидà или сульфинпиразон
Метотрексат вызвает повышение концентрации мочевой кислоты в крови, поэтому:
Предпочтительным препаратом для предотвращения или устранения гиперурикемии, связанной с использованием метотрексата, может быть аллопуринол.
Антикоагулянты - производные кумарина или индандиона
Метотрексат повышает антикоагулянтную активность этой группы препаратов и/или риск кровотечений, так как снижает синтез в печени факторов свёртывания крови и нарушает образование тромбоцитов.
Нестероидные противовоспалительные аналгезирующие средства
Не рекомендуется одновременное применение фенилбутазона (бутадионª) с метотрексатом, так как при этом возможно повышение риска агранулоцитоза или угнетения функции костного мозга. Кроме того, фенилбутазон может вытеснять метотрексат из участков связывания с белками, снижая его почечный клиренс, повышая концентрацию в плазме крови и увеличивая риск токсического действия, особенно при инфузионном введении высоких доз метотрексата.
Если одновременного применения двух препаратов избежать невозможно, рекомендуется особенно тщательное мониторирование концентрации метотрексата в плазме крови и усиленное наблюдение за больным для своевременного выявления признаков токсического действия и/или оценки адекватности выделительной функции почек.
Лечение фенилбутазоном следует прекратить за 7-12 дней до и в течение, по крайней мере, 12 ч после инфузионного введения метотрексата в высокой дозе.
Введение высоких доз путём инфузии больным, получающим дифлунисал или кетопрофен, приводило к выраженному токсическому действию метотрексата, иногда со смертельным исходом, возможно, вследствие длительного повышения концентрации метотрексата в плазме крови из-за уменьшения его выведения. Рекомендуется прекратить лечение НПВС за 24-48 ч (для дифлунисала) или за 12-24 ч (для кетопрофена) до и в течение, по крайней мере, 12 ч после инфузии метотрексата.
Введение индометацина следует прекратить за 24-48 ч до и в течение 12 ч после инфузии метотрексата.
Известны случаи выраженного токсического действия метотрексата, иногда со смертельным исходом, при его использовании в дозах от низких до умеренных у больных, принимающих диклофенак (ортофенª), индометацин, напроксен или фенилбутазон, поэтому требуется корректировать дозу, основываясь на данных мониторирования концентрации метотрексата в плазме крови и/или адекватности выделительной функции почек.
Аспарагиназа
При одновременном применении возможно блокирование действия метотрексата путём ингибирования репликации клеток (по-видимому, коррелирует со снижением концентрации аспарагина).
Препараты, вызывающие патологические изменения крови
Если препараты оказывают лейкопеническое и/или тромбоцитопеническое действие, они могут усиливать аналогичные эффекты метотрексата (при одновременном или недавнем применении). При необходимости дозу метотрексата корректируют, основываясь на результатах анализа крови.
Лучевая терапия или препараты, угнетающие функцию костного мозга
Возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких препаратов, а также лучевой терапии может потребоваться снижение дозы метотрексата.
Цитарабин
Применение цитарабина за 48 ч до или в течение 10 мин после начала терапии метотрексатом может повлечь синергический цитотоксический эффект.
Фолиевая кислота
Может препятствовать антифолиевому действию метотрексата.
Неомицин для приёма внутрь
Может снижать всасывание метотрексата для приёма внутрь.
ПробенецидÃ
При одновременном применении возможно уменьшение выведения метотрексата почками (нарастает концентрация препарата в плазме крови, вплоть до токсической), поэтому дозу метотрексата следует снизить и наблюдать за больным (для своевременного выявления признаков токсического действия) и/или мониторировать концентрацию метотрексата в плазме крови.
Салицилаты и другие слабые органические кислоты
Салицилаты могут повышать концентрацию метотрексата в плазме крови, подавляя его выведения почками или вытесняя из участков связывания с белками.
При одновременном применении следует наблюдать за больным для выявления признаков токсического действия и/или мониторировать концентрацию метотрексата в плазме крови. Кроме того, рекомендуют прекратить введение салицилатов за 24-48 ч до и в течение, по крайней мере, 12 ч после проведения инфузии метотрексата.
Сульфаниламиды
При одновременном применении помимо повышения риска гепатотоксического действия, сульфаниламиды способны вытеснять метотрексат из участков связывания с белками плазмы крови, в результате концентрация последнего в плазме возрастает, вплоть до токсической.
Резюме и дополнительные сведения
Больные, получающие метотрексат, должны наблюдаться у врача, имеющего опыт проведения противоопухолевой химиотерапии.
При интратекальном введении значительное количество метотрексата поступает в системный кровоток. Одновременное применение с метотрексатом системного действия приводит к превышению концентрации препарата в плазме крови до токсической и требует корректировки дозы.
Развитие нефропатии, связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить путём потребления адекватного количества жидкости и, в некоторых случаях, назначением аллопуринола. При повышении концентрации мочевой кислоты в сыворотке крови можно воспользоваться препаратами, вызывающими подщелачивание мочи.
При выраженном угнетении функции костного мозга метотрексат отменяют. Однако у некоторых больных острым лейкозом метотрексат можно применять несмотря на наличие тромбоцитопении и кровотечений. Иногда прекращение кровотечения и повышение числа тромбоцитов отмечают во время лечения, в остальных случаях целесообразно переливание тромбоцитарной массы.
У больных с развившейся в результате применения метотрексата тромбоцитопенией рекомендуют соблюдать особые меры предосторожности.
Больных с развившейся лейкопенией следует тщательно наблюдать для своевременной диагностики присоединившейся инфекции. Может возникнуть необходимость применения антибиотиков. Больным с фебрильной нейтропенией до получения результатов бактериологических исследований и соответствующих диагностических тестов назначают эмпирическую антибиотикотерапию препаратами широкого спектра действия (парентеральное введение).
При развитиии диареи или язвенного стоматита лечение метотрексатом прекращают из-за риска геморрагического энтерита и перфорации кишечника с летальным исходом.
При развитии клинической симптоматики поражения дыхательной системы (особенно сухой кашель без мокроты) лечение метотрексатом так же прекращают из-за риска возможно необратимого токсического действия на лёгкие.
Для предотвращения токсического воздействия высоких доз метотрексата на ЖКТ и гематологические показатели в качестве антидота применяют кальция фолинат (лейковоринª).
Не следует начинать терапию метотрексатом, если КК и уровень креатинина в сыворотке крови отличаются от значений нормы. При нарушении функций почек в период лечения метотрексат следует отменить, пока показатели функции почек не будут находиться в пределах допустимых значений. Кроме того, для предотвращения нефротоксического действия препарата и/или его метаболитов применяют подщелачивание мочи (при помощи гидрокарбоната натрия) и внутривенную гидратацию (1000 мг/м2 в течение 6 ч до начала инфузии метотрексата и 3000 мг/м2 в сут в течение двух дней после неё).
Лейковоринª применяют после введения метотрексата, чтобы не препятствовать противоопухолевому эффекту последнего. Первое введение лейковоринаª рекомендуется через 24 ч от начала инфузии метотрексата в высокой дозе. Продолжительность применения лейковоринаª варьирует в зависимости от дозы метотрексата и концентрации, достигаемой в плазме крови (включая скорость выведения). Больным с ацидурией, обезвоживанием, непроходимостью кишечника, выпотом в плевральной или брюшной полостях, нарушением функции почек могут потребоваться более высокая доза и/или более длительное применение лейковоринаª, поскольку метотрексат выводится медленно и увеличивается время снижения его концентрации в плазме крови до нетоксического уровня. Временные рамки терапии лейковориномª у этих больных определяют, основываясь на данных о концентрации метотрексата в плазме.
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии. Возможны отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, - хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств.
Исследования с применением метотрексата у пожилых людей не проводились. Из-за возможного снижения функций почек и печени и уменьшения запасов фолиевой кислоты у данной категории больных препарат следует применять с осторожностью. Может понадобиться корректировка дозы, главным образом на основании оценки функций почек.
Код АТХ
L01BA01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Methotrexate
Формы выпуска
Метотрексат для парентерального применения можно вводить внутримышечно, внутривенно (быстрая или непрерывная инфузия), интратекально, внутриартериально или в желудочки мозга.
Упаковка и хранение
Хранить в закрытой упаковке при температуре ниже 40 °С, предпочтительно при 15-30 °С, если производителем не указано иные условия. Защищать от света.
Антагонисты пуринов
Меркаптопурин (Mercaptopurine)
Фармакологический/химический класс АТХ
6-Меркаптопурин (моногидрат).
Терапевтический класс АТХ
Противоопухолевое средство. Иммунодепрессант.
Механизм действия
Меркаптопурин - антиметаболит; аналог пуриновых оснований (аденина, гуанина, гипоксантина), входящих в состав нуклеиновых кислот. Это S-фазоспецифичный препарат. Активируясь в тканях и включаясь в процессы превращения пуринов, меркаптопурин нарушает синтез нуклеотидов, что приводит к ингибированию синтеза ДНК в пролиферирующих клетках.
Фармакологические эффекты
Физико-химические свойства
Молекулярная масса - 170,19.
рКа - 7,6.
Фармококинетика
Всасывание вариабельно, препарат неполностью (до 50%) всасывается из ЖКТ, незначительное количество проникает через гематоэнцефалический барьер. Связывание с белками слабое (20%). Биотрансфармируется в печени (активация и катаболизм); распад происходит при участии ксантиноксидазы.
T1/2 препарата трёхфазный: 45 мин; 2,5 ч и 10 ч. 7-39% выводится почками в неизменённом виде. В процессе диализа удаляется полностью.
Показания к применению и дозирование
Показания
При использовании меркаптопурина для лечения неопухолевых заболеваний рекомендуется особая осторожность из-за возможного канцерогенного действия препарата при длительном применении.
Обычная доза для взрослых
Лимфобластный, миелобластный или миеломонобластный лейкоз.
-
Начальная доза - внутрь, 2,5 мг/кг или 80-100 мг/м2 в сутки, однократно или в разделённых дозах. При отсутствии клинического улучшения или снижении числа лейкоцитов после 4-недельного лечения можно попытаться увеличить дозу до 5 мг/кг в сутки.
-
Поддерживающая доза - внутрь, 1,5-2,5 мг/кг или 50-100 мг/м2 в сутки.
Обычная доза для детей
Лимфобластный, миелобластный или миеломонобластный лейкоз - внутрь, 2,5 мг/кг или 75 мг/м2 в сутки, однократно или в разделённых дозах.
Побочные эффекты
Чаще встречаются:
Реже встречаются:
Примечание
Гиперурикемия или нефропатия, связанные с повышенным образованием мочевой кислоты (результат быстрого распада клеток) чаще возникают в начальный период лечения больных лейкозом или лимфомой. Потеря аппетита, тошнота и/или рвота могут быть симптомами передозировки.
Встречаются редко:
Примечание
При использовании препарата в высоких дозах стоматит - обычное явление.
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу.
Следует соблюдать осторожность также у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Беременность
Препарат не рекомендован к применению. Вызывает патологические изменения у эмбрионов крыс; его применение у беременных сопровождалось повышенным риском выкидыша или преждевременных родов. Риск тератогенного действия у выжившего потомства не изучен.
В период лечения цитотоксическими препаратами женщинам следует использовать надёжные методы контрацепции.
Кормление грудью
Неизвестно, проникает ли меркаптопурин в грудное молоко, но грудное вскармливание на период лечения не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Аллопуринол, колхицин, пробенецидà или сульфинпиразон
При одновременном применении с аллопуринолом может значительно увеличиваться активность меркаптопурина и усиливаться его токсическое действие вследствие замедления метаболизма; рекомендуется тщательное наблюдение. Больным, получающим 300-600 мг аллопуринола в сутки, рекомендуется снизить дозу меркаптопурина до 1/3-1/4 обычной с целью уменьшения (или предотвращения) гиперурикемии или снижения метаболизма меркаптопурина. Кроме того, меркаптопурин может повышать концентрацию мочевой кислоты в крови, поэтому при лечении гиперурикемии и подагры может потребоваться корректировка дозы противоподагрических средств. Следует избегать одновременного применения урикозурических противоподагрических препаратов из-за риска нефропатии, связанной с повышенным образованием мочевой кислоты.
Антикоагулянты - производные кумарина или индандиона
Меркаптопурин может повышать антикоагулянтную активность и/или риск кровотечений (снижая синтез в печени факторов свёртывания крови и нарушая образование тромбоцитов), либо снижать антикоагулянтную активность посредством стимуляции синтеза или активации протромбина.
Препараты, вызывающие патологические изменения крови
Если препараты оказывают лейкопеническое и/или тромбоцитопеническое действие, они могут усиливать аналогичные эффекты меркаптопурина (при одновременном или недавнем применении). При необходимости дозу меркаптопурина корректируют, основываясь на результатах анализа крови.
Другие препараты, угнетающие функции костного мозга, или лучевая терапия
Возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении нескольких препаратов, а также лучевой терапии может потребоваться снижение дозы меркаптопурина.
Другие препараты, оказывающие гепатотоксическое действие
Следует избегать одновременного применения из-за значительного повышения риска гепатотоксического действия.
Другие иммунодепрессанты
Такие как глюкокортикоиды, а также азатиопринÃ, хлорамбуцил, кортикотропин, циклофосфамид, циклоспорин при одновременном с меркаптопурином применении могут повышать риск развития инфекции и вторичных опухолей.
Резюме и дополнительные сведения
Больные, получающие меркаптопурин, должны наблюдаться у врача, имеющего опыт проведения химиотерапии с использованием иммунодепрессантов и антиметаболитов.
Развитие нефропатии, связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить путём потребления адекватного количества жидкости. При повышении концентрации мочевой кислоты в сыворотке крови можно воспользоваться препаратами, вызывающими подщелачивание мочи. Аллопуринол следует назначать с осторожностью и только в тех случаях, когда концентрация мочевой кислоты резко превышает допустимые значения. Больным, получающим одновременно 300-600 мг аллопуринола в сутки, рекомендуется назначать 1/3-1/4 обычной дозы меркаптопурина с целью уменьшения (или предотвращения) гиперурикемии и замедления метаболизма последнего.
В связи с тем, что действие меркаптопурина может быть замедленным, при первых признаках выраженной лейкопении (в частности, гранулоцитопении) или тромбоцитопении, склонности к кровотечениям и кровоизлияниям или желтухи препарат следует немедленно отменить.
При остром лейкозе меркаптопурин можно применять, несмотря на наличие тромбоцитопении и кровотечений. Иногда прекращение кровотечения и повышение числа тромбоцитов отмечают во время лечения, в других случаях целесообразно переливание тромбоцитарной массы.
У больных с развившейся в результате применения меркаптопурина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности.
Больных с развившейся лейкопенией следует тщательно наблюдать для своевременной диагностики присоединившейся инфекции. Может возникнуть необходимость применения антибиотиков. Больным с фебрильной нейтропенией до получения результатов бактериологических исследований и соответствующих диагностических тестов назначают эмпирическую антибиотикотерапию препаратами широкого спектра действия (парентеральное введение).
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желёз, приводящее к аменорее или азооспермии Возможны отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, - хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств. Меркаптопурин вызывает хромосомные аберрации в клетках животных и человека и доминантно-летальные мутации у самцов мышей.
Код АТХ
L01BB02
Торговые наименования, формы выпуска и производители
Другое используемое наименование - 6-МР (6-МП).
Используемые в России торговые наименования Mercaptopurine
Форма выпуска
Таблетки по 0,05 г.
Упаковка и хранение
Хранить в хорошо закрытой упаковке при температуре ниже 40 °С, предпочтительно при 15-30 °С, если производителем не указаны иные условия.
Тиогуанин (Thioguanine)
Фармакологический/химический класс АТХ
2-Амино-6-меркаптопурин.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Тиогуанин - антиметаболит, аналогов пуринов и S-фазовоспецифичный препарат. Активируясь в тканях, способен ингибировать синтез ДНК и блокировать митотический процесс в опухолевой клетке. Препарат избирательно влияет на клетки костного мозга.
Фармакология
Физико-химические свойства
Молекулярная масса - 167,19 (безводный).
рКа - 8,1.
Фармакокинетика
Преперат частично (около 30% принятой дозы) всасывается из ЖКТ. В значительных количествах проникает через гематоэнцефалический барьер. Биотрансформируется в печени (активация и катаболизм). T1/2 составляет в среднем 80 мин (25-240 мин). Практически полностью выводится почками в виде метаболитов.
Показания к применению и дозирование
Показания
Обычная доза для взрослых и подростков
Лимфобластный, миелобластный лейкоз или хронический миелолейкоз.
-
Начальная доза - внутрь, 2 мг/кг или 75-100 мг/м2 раз в сутки. При отсутствии клинического улучшения и снижения числа лейкоцитов после 4-недельного лечения с использованием этой дозы можно попытаться с осторожностью! увеличить дозу до 3 мг/кг в сутки.
-
Поддерживающая доза - внутрь, 2-3 мг/кг или 100 мг/м2 в сутки.
Побочные эффекты
Чаще встречаются:
Реже встречаются:
Примечание
Гиперурикемия или нефропатия, связанная с повышенным образованием мочевой кислоты и увеличением её концентрации в сыворотке крови (результата быстрого распада клеток) чаще возникают в начальный период лечения больных лейкозом или лимфомой. Потерю аппетита, тошноту и/или рвоту чаще отмечают при передозировке.
Встречаются редко:
Противопоказания
При наличии следующих медицинских проблем, необходимо сопоставлять риск и пользу.
Следует соблюдать осторожность у больных, ранее (в течение 4-6 нед) получавших цитотоксические препараты или лучевую терапию.
Беременность
Противопоказан при беременности (тератогенное и эмбриотоксическое действие). Женщины детородного возраста в период применения тиогуанина и в течение последующих 6 мес должны применять надёжные методы контрацепции.
Кормление грудью
Неизвестно, проникает ли тиогуанин в грудное молоко, но грудное вскармливание на период лечения не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
При одновременном применении тиогуанина с бусульфаном возможно развитие варикозного расширения вен пищевода, узловатой регенеративной гиперплазии печени и симптомов портальной гипертензии.
При одновременном применении с урикозурическими препаратами повышается риск развития нефропатии.
Препараты, вызывающие патологические изменения крови
Если эти препараты дают лейкопенический и/или тромбоцитопенический эффект, они могут усиливать аналогичные эффекты тиогуанина (при одновременном или недавнем применении). При необходимости дозу тиогуанина корректируют, основываясь на результатах анализа крови.
Другие препараты, угнетающие функции костного мозга, или лучевая терапия
Возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении препаратов, а также лучевой терапии может потребоваться снижение дозы тиогуанина.
Резюме и дополнительные сведения
Больные, получающие тиогуанин, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии.
Развитие нефропатии, связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить путём потребления адекватного количества жидкости и, в некоторых случаях, назначением аллопуринола. При повышении концентрации мочевой кислоты в сыворотке крови можно применить вещества, вызывающие подщелачивание мочи.
При одновременном назначении больным аллопуринола с целью снижения образования мочевой кислоты тиогуанин можно продолжать принимать в обычной дозе (в отличие от меркаптопурина и азатиоприна), так как ксантиноксидаза не участвует в его метаболизме.
Если эффект от лечения меркаптопурином отсутствует, маловероятно, что применение тиогуанина будет эффективным.
В связи с тем, что действие тиогуанина может быть замедленным, при первых признаках выраженной лейкопении (особенно гранулоцитопении), тромбоцитопении, желтухи или склонности к кровотечениям или кровоизлияниям препарат следует немедленно отменить. При возвращении лабораторных показателей картины крови к допустимому уровню терапию можно возобновить, используя более низкую дозу препарата.
При остром лейкозе тиогуанин можно применять, несмотря на наличие тромбоцитопении или кровотечений. Иногда прекращение кровотечений и повышение числа тромбоцитов отмечают во время лечения, в других случаях может быть целесообразным переливание тромбоцитарной массы.
У больных с развившейся в результате применения тиогуанина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности.
Больных с развившейся лейкопенией следует тщательно наблюдать для своевременной диагностики присоединившейся инфекции. Может возникнуть необходимость применения антибиотиков. Больным с фебрильной нейтропенией до получения результатов бактериологических исследований и соответствующих диагностических тестов назначают эмпирическую антибиотикотерапию препаратами широкого спектра действия (парентеральное введение).
Возможны отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, - хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Thioguanine (Tioguanine)
Форма выпуска
Таблетки по 0,04 г (40 мг) в банках тёмного стекла по 50 шт. или в поливинилхлоридной плёнке.
Упаковка и хранение
Хранить в плотной упаковке при температуре ниже 40 °С, предпочтительно при 15-30 °С, если производителем не указаны иные условия.
Антагонисты пиримидинов
Фторурацил (Ftoruracil)
Фармакологический/химический класс АТХ
2, 4-Диоксо-5-фторпиримидин, или 5-фторурацил.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Фторурацил - антиметаболит, структурный аналог пиримидина; считается S-фазоспецифичным препаратом. Превращаясь в тканях в активный метаболит, препарат ингибирует синтез ДНК (угнетает активность тимидилатсинтетазы) и РНК (внедряется в структуру нуклеиновой кислоты).
Фармакология
Физико-химические свойства
Молекулярная масса - 130,08.
рКа - 8,0 и 13,0.
Фармакокинетика
Проходит через гематоэнцефалический барьер, активные метаболиты локализуются в клетке. Биотрансформация в тканях быстрая (в течение часа) по сложному пути превращений с образованием активного метаболита - фторуридинмонофосфата. Катаболическое расщепление происходит в печени.
При внутривенном введении T1/2 в начальной фазе составляет 10-20 мин (для фторурацила). В конечной фазе T1/2 длительный, примерно 20 ч, из-за депонирования в тканях (метаболиты).
Выводится в основном через дыхательные пути (60-80% в виде диоксида углерода, CO2), а также почками (примерно 7-20% в неизменённом виде, из них 90% - в течение первого часа).
Показания к применению и дозирование
Препарат показан при раке:
Режим дозирования
Обычная доза для взрослых и подростков
Рак толстой и прямой кишки, РМЖ, рак желудка, рак поджелудочной железы, РМП или рак яичников.
-
внутривенно, 500-1000 мг/м2 в сутки в течение 5 дней (1 раз в 4 нед);
-
200-400 мг/м2 в сутки в виде длительной внутривенной инфузии;
-
1000 мг/м2 в сутки в течение 4 дней в виде длительной инфузии (1 раз в 3-4 нед);
-
425 мг/м2 в сутки с предварительным введением лейковорина внутривенно по 20 мг/м2 в течение 5 дней (1 раз в 4 нед).
Примечание
Дозы препарата рассчитывают, исходя из истинной массы тела. Однако, у тучных больных и пациентов с приростом массы тела вследствие задержки жидкости в организме (например, отёки, асцит) истинную массу оценивают без учёта жировой ткани ("сухая" масса тела).
Побочные эффекты
Неблагоприятные эффекты, связанные с длительной внутривенной катетеризацией:
Чаще встречаются:
Примечание
Воспаление слизистой оболочки пищевода и глотки может привести к отторжению струпа и изъязвлению.
Лейкопения обычно возникает через 9-14 дней после введения препарата; примерно через 4 нед число лейкоцитов восстанавливается. Расстройство ЖКТ обычно возникает на 4-й день лечения и проходит через 2-3 дня после отмены препарата. Слабость отмечают сразу после введения препарата и в следующие 12-36 ч.
Реже встречаются:
Встречаются редко:
Примечание
Ишемия миокарда развивается в течение нескольких часов после введения препарата (чаще повторного).
Синдром ладонно-подошвенной эритродизестезии начинается с ощущения покалывания в ладонях и стопах и может усиливаться в течение следующих нескольких дней (до появления боли при держании предметов или ходьбе). Отмечают симметричное припухание ладоней и подошв и эритему с болезненностью в дистальных фалангах пальцев, что иногда сопровождается десквамацией эпителия. Симптомы постепенно проходят в течение 5-7 дней после отмены фторурацила. Для лечения данного синдрома можно назначить 100-150 мг пиридоксина в сутки, внутрь.
Противопоказания
С особой осторожностью применяют при наличии:
Рекомендуется снижать дозу больным, ранее получавшим цитотоксические препараты (алкилирующие средства) или лучевую терапию (особенно облучение органов таза в высоких дозах).
Беременность
Противопоказан при беременности. В период лечения женщины детородного возраста должны применять надёжные методы контрацепции. В экспериментальных исследованиях установлено тератогенное и эмбриотоксическое действие фторурацила.
Кормление грудью
Неизвестно, проникает ли фторурацил в грудное молоко, но грудное вскармливание во время проведения химиотерапии не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
При одновременном применении с другими препаратами, вызывающими миелодепрессию возможно аддитивное угнетение функции костного мозга. С интерфероном альфа-2b возможно уменьшение клиренса фторурацила и увеличение его начальной концентрации в плазме.
У пациентов с КРР при одновременном применении с метронидазолом возможно повышение токсичности фторурацила.
Фторурацил способен ингибировать цитотоксическое действие паклитаксела.
На фоне терапии циметидином возможно повышение концентрации фторурацила в плазме крови.
При одновременном применении с аллопуринолом, метотрексатом возможно изменение противоопухолевого действия; с кальция фолинатом - возможно усиление противоопухолевого и токсического действия фторурацила, особенно на ЖКТ.
Резюме и дополнительные сведения
Больные, получающие фторурацил, должны проходить лечение в стационаре (по крайней мере, во время первого цикла) и наблюдаться у врача, имеющего опыт проведения химиотерапии.
При подборе следующей после начальной дозы учитывают индивидуальные особенности больного и гематологические показатели после предыдущего применения препарата.
Фторурацил рекомендуется только для парентерального применения, его не следует вводить интратекально из-за опасности нейротоксического действия. Медленная внутривенная инфузия в течение 2-24 ч, по-видимому, оказывает менее выраженное токсическое действие, хотя быстрые инъекции (в течение 1-2 мин) могут быть терапевтически более эффективными. При внутриартериальном введении рекомендуется использовать соответствующий инфузионный насос для обеспечения постоянной скорости инфузии.
Фторурацил - крайне токсичный препарат; его следует немедленно отменить при первых признаках следующих осложнений:
При изменении выраженности побочных эффектов лечение можно возобновить в редуцированной дозе.
Код АТХ
L01BC02
Торговые наименования, формы выпуска и производители
Другое используемое наименование - 5-FU (5-ФУ).
Используемые в России торговые наименования Fluorouracil
Форма выпуска
5%-й раствор в ампулах по 5 мл (250 мг), 10 ампул в упаковке.
Упаковка и хранение
Хранить при температуре ниже 40 °С, предпочтительно при 15-30 °С, если производителем не указаны иные условия. Защищать от света. Не допускать замораживания.
Цитарабин (Cytarabine)
Фармакологический/химический класс АТХ
4-амино-1-бета-D-арабинофуранозил-пиримидинон
Терапевтический класс АТХ
Противоопухолевый препарат. Иммунодепрессант.
Механизм действия
Цитарабин - антиметаболит, аналог пиримидина; S-фазоспецифичный препарат. В результате фосфорилирования превращается в арабинозилцитозинтрифосфат (Ара-ЦТФ), который конкурентно ингибирует ДНК-полимеразу, что ведёт к торможению синтеза ДНК. Имеются данные, что цитарабин способен также встраиваться в молекулы ДНК и РНК. Возможное развитие резистентности к цитарабину связано с:
Цитотоксический эффект достигается при создании постоянных высоких внутриклеточных концентраций Ара-ЦТФ.
Фармакологические эффекты
Физико-химические свойства
Молекулярная масса - 243,22.
рКа - 4,35 в 60% водном этаноле (C2H5OH).
Фармакокинетика
При непрерывной внутривенной инфузии цитарабина в обычной дозе (100-200 мг/м2 поверхности тела) в крови достигаются концентрации 0,04-0,6 мкмоль/л. При подкожном введении концентрация в плазме достигает максимума в течение 20-60 мин. Цитарабин лишь в умеренных количествах проникает через гематоэнцефалический барьер, хотя после непрерывной инфузии в спинномозговой жидкости достигается концентрация, составляющая 10-40% плазменной. Связывание с белками плазмы слабое - около 15%. После внутривенного введения цитарабин под действием цитидиндезаминазы быстро и практически полностью биотрансформируется в печени и в других тканях в неактивный урацил-метаболит (Ара-У). Незначительная часть препарата подвергается внутриклеточному фосфорилированию под действием киназ, с образованием активного метаболита Ара-ЦТФ.
Концентрация препарата в плазме снижается двухфазно: T1/2 в a-фазе (начальной) составляет 10 мин, в b-фазе (конечной) - примерно 1-3 ч.
Из спинномозговой жидкости цитарабин выводится медленно из-за минимальной активности дезаминазы в ЦНС (T1/2 составляет 2-11 ч). Около 4-10% дозы выводится почками в неизменном виде; в первые 24 ч 71-96% введённого препарата обнаруживается в моче в виде Ара-У.
Показания к применению и дозирование
Показания
Высокие дозы показаны при:
Схема и метод применения цитарабина варьируют при использовании разных режимов химиотерапии. Цитарабин можно вводить внутривенно струйно или капельно, подкожно, внутримышечно, а также интратекально. Средняя суточная доза - 100-200 мг/м2; для пациентов пожилого возраста или с пониженными резервами кроветворения - 50-70 мг/м2.
Для индукции ремиссии при острых лейкозах в комбинации с другими противоопухолевыми препаратами назначают по 100 мг/м2 в сутки в виде непрерывной внутривенной инфузии в течение 7 дней или 100 мг/м2 внутривенно каждые 12 ч (7 дней подряд). Всего проводят 4-7 циклов терапии. Интервалы между циклами - не менее 14 дней.
При высокодозной терапии для лечения лейкозов с плохим прогнозом, а также рефрактерных лейкозов и рецидивов цитарабин назначают в дозе 2-3 г/м2 в виде внутривенной инфузии продолжительностью 1-3 ч (с 12-часовым интервалом) в течение 2-6 дней в виде монотерапии или в комбинации с другими противоопухолевыми препаратами.
При интратекальном введении при остром лейкозе доза препарата составляет 5-75 мг/м2. Частота введения может колебаться от 1 раза в сутки в течение 4 дней до 1 раза в 4 дня. Чаще назначают по 30 мг/м2 каждые 4 дня до нормализации гематологических показателей, далее следует ещё одно дополнительное введение.
При почечной и печёночной недостаточности нет необходимости снижать дозу препарата. Если проводится высокодозная терапия, то при выборе дозы следует принимать во внимание повышенный риск осложнений со стороны ЦНС.
Побочные эффекты
Побочные эффекты зависят от дозы, способа введения и длительности терапии.
Со стороны системы кроветворения
Снижение числа лейкоцитов носит двухфазный характер.
К 5-ому дню терапии падает число тромбоцитов, минимум отмечают между 12-15 днями. В последующие 10 дней количества тромбоцитов быстро достигает исходного уровня. Степень тяжести этих реакций зависит от дозы и схемы введения.
Со стороны пищеварительной системы
Чаще встречаются:
Тошнота и рвота чаще возникают вслед за быстрым внутривенным введением. При высокодозной терапии (2-3 г/м2) изъязвления ЖКТ могут носить тяжёлый характер, возможно развитие некротического колита, некрозов тонкой кишки, кистозного пневматоза кишечника, приводящего к перитониту.
Со стороны печени и поджелудочной железы
Чаще отмечают нарушение функции печени и желтуху. При терапии высокими дозами - нарушение функции печени с гипербилирубинемией, сепсис, абсцесс печени. Есть сообщения об отдельных случаях развития тромбоза печёночных вен (синдром Бадда-Киари), а также панкреатита при высокодозной терапии в комбинации с другими противоопухолевыми препаратами.
Со стороны нервной системы
Препарат обладает нейротоксичностью, возможно появление головной боли, головокружений. Нарушения со стороны ЦНС возникают чаще при проведении высокодозной терапии и носят обратимый характер. Преимущественно это расстройства функции головного мозга и мозжечка:
Сообщалось о случаях развития периферической моторной и сенсорной нейропатии и позднего прогрессирующего восходящего паралича. Иногда после интратекального введения возникали тошнота, рвота, головокружение, лихорадка, возможно связанные с проведением спинномозговой пункции. Также может проявляться кумулятивная нейротоксичность, особенно при коротких интервалах между введениями препарата. Были описаны отдельные случаи некротизирующей лейкоэнцефалопатии, параплегии и слепоты после интратекального введения.
Со стороны органов чувств
Чаще возникают конъюнктивит (фотофобия, жжение в глазах, выраженное слезотечение) и кератит. При высокодозной терапии - обратимый язвенный кератит, геморрагический конъюнктивит, расстройства зрения.
Со стороны костно-мышечной системы
При высокодозной терапии развиваются миалгии и/или артралгии в области шеи и нижних конечностей.
Со стороны дыхательной системы
Чаще отмечают:
Со стороны сердечно-сосудистой системы
Кардиомиопатия (в том числе фатальная при использовании цитарабина в высоких дозах в комбинации с циклофосфамидом), перикардит, транзиторная аритмия.
Со стороны мочевыделительной системы
Нарушение функции почек, задержка мочи, гиперурикемия или уратная нефропатия.
Дерматологические реакции
Чаще возникают:
Редко - тяжёлая кожная сыпь, приводящая к десквамации эпителия.
Аллергические реакции
Крапивница, анафилаксия, отёк.
Местные реакции
Воспаление подкожно-жировой клетчатки в месте инъекции.
Инфекционные осложнения
Вирусные, бактериальные, грибковые, паразитарные или вызванные сапрофитной флорой инфекции любой локализации (в том числе сепсис), обычно лёгкой или средней степеней тяжести, но могут быть тяжёлыми и иногда фатальными (их развитие обусловлено снижением иммунитета).
Прочие
Лихорадка, тромбофлебит; в отдельных случаях - синдром неадекватной выработки АДГ.
Через 6-12 ч после введения препарата может развиться цитарабиновый синдром (лихорадка; боли в мышцах, костях, иногда в области грудной клетки; пятнисто-папулёзная сыпь, конъюнктивит, общее недомогание). Для лечения этого осложнения применяют глюкокортикоиды.
Передозировка
Симптомы
Хроническая передозировка может привести к тяжёлому угнетению функции костного мозга, что сопровождается массивным кровотечением, развитием опасных для жизни инфекций, а также тяжёлым проявлениям нейротоксического действия препарата.
Лечение
Поскольку для цитарабина нет эффективных антидотов, вводить препарат следует с осторожностью. При передозировке показана вспомогательная терапия (гемотрансфузия, антибиотикотерапия). В случае тяжёлой передозировки, возникшей во время интратекального введения, следует провести повторные люмбальные пункции для обеспечения дренажа спинномозговой жидкости. Возможно нейрохирургическое вмешательство с вентрикулолюмбальной перфузией.
Цитарабин может выводиться при гемодиализе, однако нет данных об эффективности гемодиализа при передозировке.
Противопоказания
Цитарабин противопоказан в период беременности и грудного вскармливания, а также при повышенной чувствительности к препарату и его компонентам.
С осторожностью следует назначать препарат при:
Беременность
Препарат противопоказан. Во время терапии цитарабином, а также в течение 6 мес после неё женщины и мужчины детородного возраста должны применять надёжные методы контрацепции.
Кормление грудью
Неизвестно, проникает ли цитарабин в грудное молоко, но грудное вскармливание во время проведения химиотерапии не рекомендуется из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны в соответствии с их потенциальной клинической значимостью.
При одновременном применении цитарабин усиливает цитостатическую и иммуносупрессивную активность других противоопухолевых препаратов и лучевой терапии.
Проводят полихимиотерапию (ПХТ) с включением цитарабина.
Отмечают обратимое снижение равновесной плазменной концентрации дигоксина за счёт уменьшения его всасывания в кишечнике (токсическое воздействие на слизистую оболочку кишечника) и экскреции с мочой. В качестве альтернативы у таких больных применяют дигитоксин, равновесная плазменная концентрация которого не меняется.
Проведенные in vitro исследования взаимодействия между гентамицином и цитарабином выявили существование антагонизма, вследствие чего возможно снижение чувствительности штаммов Klebsiella pneumoniae к гентамицину.
При одновременном применении цитарабина и фторцитозинаà возможно снижение эффективности последнего.
Иммунодепрессанты (азатиоприн, хлорамбуцил, глюкокортикоиды, циклофосфамид, циклоспорин, меркаптопурин, такролимус) при одновременном с цитарабином применении повышают риск развития инфекционных осложнений.
При одновременном применении с убитыми вирусными вакцинами цитарабин снижает выработку антител.
При одновременном применении с живыми вирусными вакцинами возможно снижение образования антител, потенцирование репликации вируса, усиление побочных эффектов за счёт подавления цитарабином нормальных механизмов иммунной защиты.
Нельзя смешивать цитарабин в одном шприце или капельнице с другими препаратами. Фармацевтически несовместим с гепарином натрия, инсулином, метотрексатом, 5-фторурациломª, оксациллином, бензилпенициллином, метилпреднизолоном.
Код АТХ
L01BC01
Торговые наименования, формы выпуска и производители
Другие обычно используемые наименования - ага-С (ара-Ц) и cytosine arabinoside (цитозинарабинозид).
Используемые в России торговые наименования Cytarabine
Форма выпуска
Раствор для инъекций прозрачный бесцветный, во флаконах по 100 мг/5 мл; 500 мг/10 мл; 1 г/20 мл.
Упаковка и хранение
Хранить при температуре ниже 40 °С, предпочтительно при 15-30 °С, если производителем не указаны иные услвия.
Гемцитабин (Gemcitabine)
Фармакологический/химический класс АТХ
2´-2´-Дифторцитидин.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Гемцитабин - антиметаболит из группы аналогов пиримидина (дезоксицитидин). Проявляет циклоспецифичность, действуя на клетки в фазах S и G1/S периода деления.
Внутриклеточный метаболизм под действием нуклеозидкиназ с образованием двух активных метаболитов: дифосфатных и трифосфатных нуклеозидов.
Дифосфатные нуклеозиды ингибируют рибонуклеотидредуктазу - единственный катализатор реакций, приводящих к образованию дезоксинуклеозидтрифосфатов, необходимых для синтеза ДНК.
Трифосфатные нуклеозиды активно конкурируют с дезоксицитидинтрифосфатом за встраивание в молекулы ДНК и РНК. После встраивания внутриклеточных метаболитов гемцитабина в цепь ДНК, к её растущим нитям добавляется ещё один дополнительный нуклеотид, что приводит к полному ингибированию дальнейшего синтеза и запрограммированной гибели клетки, известной как апоптоз.
Другие эффекты
Гемцитабин - сильное радиосенсибилизирующее средство. В опытах in vitro препарат оказывал значительное радиосенсибилизирующее действие даже в концентрациях более низких, чем цитотоксические.
Фармакологические эффекты
Физико-химические свойства
Молекулярная масса гемцитабина гидрохлорида - 299,66.
рН - 2,7-3,3 (после растворения).
рКа - 3,6.
Практически не растворим в этаноле или полярных органических растворителях; растворим в воде.
Фармакокинетика
Объём распределения препарата существенно зависит от продолжительности инфузии и пола больного. При кратковременной инфузии (<70 мин) объём распределения 50 л/м2 указывает, что гемцитабин не проникает в ткани в больших количествах.
При длительной инфузии (70-285 мин) объём распределения 370 л/м2 свидетельствует о медленном достижении равновесия в тканях. У женщин клиренс препарата примерно на 25% ниже, чем у мужчин. Связывание с белками очень слабое (<10%). В результате внутриклеточного метаболизма с участием нуклеозидкиназ образуется два активных метаболита (гемцитабина дифосфат и гемцитабина трифосфат), а дезаминирование гемцитабина ведёт образованию неактивного метаболита урацила. 92-98% однократной дозы меченного радиоактивным изотопом гемцитабина (доза 1000 мг/м2, введённая в течение 30 мин пяти больным) выводится почками в течение недели, главным образом в виде неактивного метаболита урацила (примерно 89% выделенной дозы) и неизменённого гемцитабина (менее 10% выделенной дозы). Почечная недостаточность лёгкой или средней степеней тяжести (скорость клубочковой фильтрации от 30 до 80 мл/мин) не оказывает заметного влияния на фармакокинетику гемцитабина.
Показания к применению и дозирование
Показания
Обычная доза для взрослых
Рак поджелудочной железы: внутривенная инфузия (в течение 30 мин), 1000 мг/м2 раз в неделю 6-8 введений с последующим недельным перерывом. Каждый следующий цикл терапии включает введение препарата 1 раз в неделю в течение трёх недель с последующим недельным перерывом.
Немелкоклеточный рак лёгкого: внутривенная инфузия (в течение 30 мин), 1000 мг/м2 раз в неделю в течение трёх недель с последующим недельным перерывом.
При применении в составе комбинированной терапии: рекомендованная доза - 1250 мг/м2 в 1-й и 8-й дни каждого 21-дневного цикла или 1000 мг/м2 в 1-й, 8-й и 15-й дни каждого 28-дневного цикла. Цисплатин вводят в дозе 80 мг/м2 в 1-й день цикла после инфузии гемцитабина на фоне гипергидратации.
РМЖ: в виде монотерапии при прогрессировании заболевания (после терапии первой линии, включавшей антрациклины), рекомендованная доза - 1000-1200 мг/м2 в 1-й, 8-й и 15-й дни каждого 28-дневного цикла.
При РМП (местнораспространённом, метастатическом и поверхностном):
-
в виде монотерапии; рекомендованная доза - 1250 мг/м2 в 1-й, 8-й и 15-й дни каждого 28-дневного цикла;
-
в составе комбинированной терапии; рекомендованная доза - 1000 мг/м2 в 1-й, 8-й и 15-й дни в сочетании с цисплатином, который вводят в дозе 80 мг/м2 сразу после инфузии гемцитабина в 1-й день каждого 28-дневного цикла.
Для внутрипузырного введения рекомендованная доза препарата - 2000 мг. При получении раствора для инстилляций препарат растворяют в 100 или 50 мл 0,9% раствора натрия хлорида до концентрации от 20 до 40 мг/мл (Концентрация раствора не должна превышать 40 мг/мл.). Экспозиция препарата составляет 60 мин. Вводят один раз в неделю в течение шести недель.
При эпителиальном раке яичников (местнораспространённом или метастатическом):
-
в виде монотерапии; рекомендованная доза препарата - 800-1250 мг/м2 в 1-й, 8-й и 15-й дни каждого 28-дневного цикла;
-
в составе комбинированной терапии; рекомендованная доза - 1000 мг/м2 в 1-й и 8-й дни в сочетании с карбоплатином в дозе AUC 4-5, который вводят сразу после инфузии гемцитабина в 1-й день каждого 21-дневного цикла.
Перед каждым введением гемцитабина необходимо контролировать количество тромбоцитов, лейкоцитов и гранулоцитов. При признаках угнетения функции костного мозга необходимо приостановить лечение или скорректировать дозу.
Если абсолютное число гранулоцитов и тромбоцитов перед введением каждой дозы составляет 0,6-1x109/л и 50-99x109/л соответственно, то дозу гемцитабина следует снизить на 25%.
Если менее 0,5x109/л и 50x109/л соответственно, препарат отменяют до восстановления числа гранулоцитов и тромбоцитов.
Побочные эффекты
Побочные реакции перечислены соответствии со следующей градацией: очень часто (>10%); часто (>1%,<10%); иногда (>0,1%, <1%); редко (>0,01%, <0,1%); крайне редко (<0,01%).
Со стороны системы кроветворения
Часто: лейкопения, тромбоцитопения, анемия.
Очень редко: тромбоцитоз.
Со стороны пищеварительной системы
Очень часто: тошнота, рвота, повышение уровня печёночных трансаминаз, щелочной фосфатазы.
Часто: анорексия, диарея, запор, стоматит, повышение уровня билирубина.
Со стороны мочевыделительной системы
Очень часто: лёгкая протеинурия и гематурия.
Редко: почечная недостаточность, клинические признаки и симптомы, схожие с гемолитико-уремическим синдромом (снижение уровня гемоглобина, тромбоцитопения, повышение уровней билирубина, креатинина, мочевины и/или лактатдегидрогеназы в сыворотке крови).
Дерматологические реакции
Часто: сыпь, зуд, алопеция.
Со стороны дыхательной системы
Очень часто: одышка.
Часто: кашель, ринит.
Иногда: бронхоспазм, интерстициальная пневмония, отёк лёгкого.
Редко: острый респираторный дистресс-синдром.
Со стороны сердечно-сосудистой системы
Редко: снижение АД, инфаркт миокарда, сердечная недостаточность, аритмии.
Со стороны ЦНС
Часто: головная боль, сонливость, бессонница.
Прочие
Очень часто: гриппоподобный синдром, периферические отёки.
Часто: повышение температуры тела, озноб, астения, боли в спине, миалгия.
Иногда: отёчность лица.
Очень редко: анафилактические реакции.
Передозировка
Симптомы острой и хронической передозировки
Лечение
Антидот не известен. Клинически допустимая токсичность наблюдалась при введении однократных доз вплоть до 5,7 г/м2 внутривенно в течение 30 мин каждые 2 нед. В случае подозрения на передозировку необходим постоянный врачебный контроль, включая мониторинг показателей крови. При необходимости проводят симптоматическое лечение.
Противопоказания
Гемцитабин противопоказан во время беременности, грудного вскармливания и при повышенной чувствительности к препарату или его компонентам.
С осторожностью назначают препарат при нарушении функции печени и/или почек, угнетении костномозгового кроветворения (в том числе на фоне сопутствующей лучевой или химиотерапии), острых инфекционных заболеваниях вирусной, грибковой или бактериальной этиологий.
Беременность
Препарат противопоказан. Обычно избегают применения противоопухолевых средств во время беременности, учитывая возможное мутагенное, тератогенное и канцерогенное действие данных препаратов. Женщинам и мужчинам во время лечения гемцитабином и, как минимум, в течение 6 мес после терапии следует использовать надёжные способы контрацепции.
Кормление грудью
Неизвестно, проникает ли гемцитабин в грудное молоко, но грудное вскармливание во время проведения химиотерапии не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное, тератогенное и канцерогенное действие).
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны в соответствии с их потенциальной клинической значимостью.
Препараты, угнетающие функцию костного мозга или лучевая терапия:
Возможно аддитивное угнетение функции костного мозга. При одновременном или последовательном применении препаратов, а также лучевой терапии может потребоваться снижение дозы гемцитабина.
Гемцитабин - сильное радиосенсибилизирующее средство. В зависимости от участка облучения одновременное применение гемцитабина может вызывать тяжёлый, угрожающий жизни эзофагит или пневмонию. Сочетанное использование гемцитабина и лучевой терапии приводило к тяжёлому стоматиту и поражению глотки.
Резюме и дополнительные сведения
Больные, получающие гемцитабин, должны наблюдаться у врача, имеющего опыт проведения химиотерапии рака.
Гемцитабин следует вводить только путем внутривенной инфузии.
Перед началом лечения абсолютное количество гранулоцитов должно быть не менее 1,5x109/л, тромбоцитов - не менее 100x109/л.
Для выявления негематологической токсичности необходимо проводить регулярное обследование больного и оценку функции печени и почек. В зависимости от степени токсичности дозу можно снижать в ходе каждого цикла или с началом нового цикла ступенчато. Решение об отсрочке очередного введения препарата должно базироваться на клинической оценке врачом динамики токсичности.
Увеличение длительности инфузии и частоты введений приводит к возрастанию токсичности.
При возникновении первых признаков гемолитико-уремического синдрома гемцитабин следует отменить.
У больных раком лёгкого или с метастазами в лёгких повышен риск возникновения побочных эффектов со стороны дыхательной системы. При появлении первых признаков пневмонита или появлении инфильтратов в лёгких гемцитабин следует отменить.
При применении гемцитабина чаще раза в неделю или проведении инфузии длительностью более 60 мин неблагоприятные эффекты могут отмечаться чаще и быть более выраженными.
В случае подтверждения или при подозрении на пневмонит, вызванный гемцитабином, лечение следует немедленно прекратить.
У больных с развившейся в результате применения гемцитабина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности.
Больных с развившейся лейкопенией следует тщательно наблюдать для своевременной диагностики присоединившейся инфекции. Может возникнуть необходимость применения антибиотиков. Больным с фебрильной нейтропенией до получения результатов бактериологических исследований и соответствующих диагностических тестов назначают эмпирическую антибиотикотерапию препаратами широкого спектра действия (парентеральное введение).
Код АТХ
L01BC05
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Gemcitabine
Формы выпуска
Лиофилизат для приготовления раствора для инфузий:
Упаковка и хранение
Хранить при температуре 20-25 °С, если производителем не указаны иные условия.
Не хранить в холодном месте!
Флударабин (Fludarabine)
Фармакологический/химический класс АТХ
9-β-D-[Арабинофуранозил-2-фтораденин 5´-(дигидрофосфат)].
Терапевтический класс АТХ
Противоопухолевое средство. Иммунодепрессант.
Механизм действия
Активное вещество препарата - фторированный нуклеотидный аналог противовирусного средства видарабина, 9-β-D-арабинофуранозиладенина (ара-А), относительно устойчивого к действию аденозиндезаминазы.
Флударабина фосфатª быстро дефосфорилируется до 2-фтор-ара-А, который захватывается клетками и затем внутриклеточно фосфорилируется дезоксицитидинкиназой до активного трифосфата - 2-фтор-ара-АТФ. Этот метаболит ингибирует рибонуклеотидную редуктазу, ДНК-полимеразу (a,d и u), ДНК-праймазу, ДНК-лигазу, угнетая синтез ДНК. Кроме того, частично ингибируется РНК-полимераза II с последующим снижением белкового синтеза.
К настоящему времени некоторые аспекты действия 2-фтор-ара-АТФ остаются неясными, однако, предполагают, что его ингибирующее влияние на синтез нуклеиновых кислот и белка способствует угнетению клеточного роста (в основном за счёт торможения синтеза ДНК). Исследования in vitro показали, что воздействие 2-фтор-ара-А на лимфоциты больных хроническим лимфолейкозом активируют механизм фрагментации ДНК и апоптоза.
Флударабин оказывает иммунодепрессивное действие, ингибируя созревание лимфоцитов.
Фармакологические эффекты
Молекулярная масса - 365,21.
Фармакокинетика
Фармакокинетика 2-фтор-ара-А исследовалась после внутривенного введения в виде болюсной инъекции, кратковременной или длительной инфузии, а также после приёма внутрь флударабина фосфатаª. Исследования с 2-фтор-ара-А продемонстрировали одинаковую фармакокинетическую картину у больных хроническим лимфолейкозом и низкозлокачественными неходжкинскими лимфомами. Нет чёткой корреляции между фармакокинетикой 2-фтор-ара-А и лечебным эффектом препарата у онкологических больных, но частота нейтропении и изменения гематокрита указывают на дозозависимый характер цитотоксичности.
После приёма внутрь максимальная концентрация 2-фтор-ара-А в плазме достигается через 1-2 ч и составляет примерно 20-30% уровня, определяемого к концу внутривенной инфузии. Будучи водорастворимым предшественником флударабина (2-фтор-ара-А), в организме человека 2-фтор-ара-АМФ быстро и полностью дефосфорилируется до нуклеозида 2-фтор-ара-А. Другой метаболит - 2-фтор-ара-гипоксантин обнаруживается в человеческом организме в минимальных количествах.
Фармакокинетические процессы после достижения максимальной концентрации описываются трёхфазной моделью с Т1/2 в a-фазе - около 5 мин, в b-фазе - 1-2 ч и в терминальной фазе - около 20 ч.
После внутривенного введения и приёма внутрь флударабина фосфатаª концентрации 2-фтор-ара-А в плазме и AUC увеличиваются в линейной зависимости от дозы, тогда как T1/2, плазменный клиренс и уровни распределения остаются постоянными вне зависимости от дозы и носят линейный характер.
2-фтор-ара-А выводится преимущественно почками (от 40 до 60% дозы, введённой внутривенно).
У лиц со сниженной функцией почек уменьшен общий клиренс препарата, поэтому дозу необходимо снижать.
Показания к применению и дозирование
Флударабин применяют для лечения больных хроническим В-клеточным лимфолейкозом в случае неэффективности по крайней мере одной стандартной схемы терапии (включающей алкилирующий препарат) или прогрессирования заболевания во время лечения.
Рекомендуемая доза для взрослых
Внутривенно инфузионно (в течение примерно 30 мин), 25 мг/м2 в сутки, ежедневно в течение 5 дней через каждые 28 дней.
Примечание
Доза необходимо снизить или отсрочить её введение, если проявляется токсическое действие препарата на кровь и другие системы и органы. Пациентам с нарушениями функций почек и КК от 30 до 70 мл/мин дозу препарата уменьшают на 50%. При этом необходим постоянный гематологический контроль для оценки токсичности. При КК менее 30 мл/мин флударабин противопоказан.
Побочные эффекты
Частота побочных эффектов (типичные ≥1%; редкие <1%, ≥0,1%) определена на основании клинических исследований.
Со стороны организма в целом
Типичные явления: лихорадка, ознобы, присоединение инфекции, недомогание, слабость, утомляемость.
Со стороны системы кроветворения
Типичные явления: нейтропения, тромбоцитопения, анемия. Наибольшее снижение уровня нейтрофилов наблюдают на 13-е сут от начала лечения, тромбоцитов - на 16-е сут. Миелосупрессия может быть выраженной и носить кумулятивный характер. Длительный эффект флударабина в виде снижения числа Т-лимфоцитов может привести к увеличению частоты оппортунистических инфекций (включая реактивацию латентной вирусной инфекции), например прогрессирующей мультифокальной лейкоэнцефалопатии.
Со стороны обмена веществ
Типичное явление- синдром лизиса опухоли, включающий гиперурикемию, гиперфосфатемию, гипокальциемию, метаболический ацидоз, гиперкалиемию, гематурию, уратную кристаллурию и нарушение функции почек. Первыми признаками синдрома могут быть острая боль в поясничной области и гематурия.
Со стороны ЦНС и периферической нервной системы
Типичные явления: периферическая невропатия, нарушения зрения.
Редко: коматозное или возбуждённое состояние, спутанность сознания.
Очень редко: неврит зрительного нерва, зрительная невропатия, слепота.
Со стороны дыхательной системы
Типичные явления: пневмонии.
Редко: лёгочные инфильтраты, пневмониты, фиброзы, сопровождающиеся одышкой и кашлем.
Со стороны пищеварительной системы
Типичные явления: тошнота, рвота, анорексия, диарея, стоматит.
Редко: изменение активности ферментов печени и поджелудочной железы, кровотечения из ЖКТ.
Со стороны сердечно-сосудистой системы
Очень редко: сердечная недостаточность, аритмии.
Со стороны мочеполовой системы
Очень редко: геморрагический цистит.
Дерматологические реакции
Типичные: кожная сыпь.
Очень редко: синдром Стивенса-Джонсона, синдром Лайелла.
Прочие
Вне зависимости от наличия аутоиммунных процессов в анамнезе и результатов пробы Кумбса были описаны угрожающие жизни, в некоторых случаях смертельные аутоиммунные реакции (аутоиммунная гемолитическая анемия, аутоиммунная тромбоцитопения, трмобоцитопеническая пурпура, пузырчатка, синдром Эванса) во время и по окончании лечения.
Передозировка
Симптомы
Лечение
При необходимости проводят симптоматическую терапию. Специфического антидота нет.
Противопоказания
Флударабин противопоказан при выраженных нарушениях выделительной функции почек (КК менее 30 мл/мин); декомпенсированной гемолитической анемии; в период беременности и лактация; при повышенной чувствительности к препарату или его компонентам.
Беременность
Препарат противопоказан. В экспериментальных исследованиях установлено эмбриотоксическое и тератогенное действие препарата. Доклинические данные показали проникновение флударабина фосфатаª и/или метаболитов через фетоплацентарный барьер (у крыс).
Женщинам детородного возраста и мужчинам во время лечения флударабином и, как минимум, в течение 6 мес после терапии следует использовать надёжные способы контрацепции.
Кормление грудью
Неизвестно, проникает ли флударабин в грудное молоко, но грудное вскармливание во время проведения химиотерапии не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное, тератогенное и канцерогенное действие).
Резюме и дополнительные сведения
При применении флударабина пациенты должны тщательно наблюдаться для раннего выявления симптомов нейротоксичности. В период лечения следует тщательно контролировать гематологические показатели для ранней диагностики анемии, нейтропении и тромбоцитопении.
Ослабленным пациентам, пациентам с выраженными нарушениями кроветворения (тромбоцитопения, анемия, гранулоцитопения), с иммунодефицитом или с оппортунистическими инфекциями флударабин назначают с осторожностью после тщательной оценки соотношения риск/польза.
Данные о безопасности препарата у пациентов с нарушениями функции печени отсутствуют. Этой категории пациентов препарат назначают с осторожностью и только, когда вероятность успешного результата превосходит потенциальный риск.
Синдром лизиса опухоли наблюдался у больных с большой опухолевой массой. Так как препарат может оказать лечебный эффект уже на первой неделе терапии, следует соблюдать осторожность при лечении больных с риском развития данного осложнения.
У большинства больных с гемолитической анемией развивался повторный гемолитический процесс после возобновления лечения флударабином. Больные, получающие препарат, должны тщательно наблюдаться на предмет появления признаков гемолитической анемии (снижение уровня гемоглобина и положительная проба Кумбса). При развитии гемолиза терапию следует прекратить, и при необходимости начать трансфузию облучённой крови и ведение глюкокортикидов.
Пациентам пожилого возраста (старше 75 лет) препарат следует назначать с осторожностью, в связи с недостаточностью клинических данных о его безопасности.
У детей безопасность и эффективность применения препарата не установлены.
Код АТХ
L01BB05
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Fludarabine
Формы выпуска
Таблетки, покрытые оболочкой по 10 мг.
Лиофилизированный порошок для приготовления раствора для инъекций во флаконах по 50 мг.
Упаковка и хранение
Хранить при температуре 2-8 СС, если производителем не указаны иные условия.
Капецитабин (Capecitabine)
Фармакологический/химический класс АТХ
Пентил-1-(5-деокси-β-D-рибофуранозил)-5-фтор-1,2-дигидро-2-оксо-4пиримидинкарбамат.
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Капецитабин - производное фторпиримидина карбамата; цитостатик для приёма внутрь. Активируясь в опухолевой ткани, оказывает на неё селективное цитотоксическое влияние. in vitro капецитабин не обладает цитотоксическим эффектом. In vivo в опухолевой ткани под действием опухолевого ангиогенного фактора - тимидинфосфорилазы - превращается в 5-фторурацил (5-ФУ), который подвергается дальнейшему метаболизму. После перорального назначения капецитабина больным раком толстой кишки концентрация 5-ФУ в ткани опухоли была выше, чем в прилежащих здоровых тканях в 3,2 раза (благодаря последовательной тканевой трансформации). Соотношение концентраций 5-ФУ в ткани опухоли и плазме - 21,4, соотношение его концентрации в здоровых тканях и в плазме - 8,9. Активность тимидинфосфорилазы в первичной раковой опухоли толстой кишки так же в 4 раза выше, чем в прилежащих здоровых тканях.
В ткани опухолей человека, таких как РМЖ, рак желудка, толстой кишки, РШМ и рак яичников, содержится больше тимидинфосфорилазы, способной превращать 5'-ДФУР (5'-дезокси-5-фторуридин) в 5-ФУ, чем в соответствующих здоровых тканях.
Как здоровые, так и опухолевые клетки метаболизируют 5-ФУ в 5-фтор-2-дезоксиуридина монофосфат (ФдУМФ) и 5-фторуридина трифосфат (ФУТФ). Эти метаболиты повреждают клетки посредством двух различных механизмов. Во-первых, ФдУМФ и фолатный кофактор N5-10-метилентетрагидрофолат связываются с тимидилатсинтазой с образованием ковалентно связанного третичного комплекса. Это связывание подавляет образование тимидилата из урацила. Тимидилат - необходимый предшественник тимидина трифосфата, крайне важного для синтеза ДНК вещества (его недостаток может привести к угнетению клеточного деления). Во-вторых, в процессе синтеза РНК транскрипционные ферменты ядра могут ошибочно включить в нее ФУТФ вместо уридина трифосфата, что нарушает образование РНК и синтез белка.
Фармакокинетика
После приёма внутрь капецитабин быстро и полностью абсорбируется из ЖКТ и метаболизируется в печени под воздействием карбоксилэстеразы до 5'-ДФЦТ, который затем трансформируется в 5'-ДФУР под действием цитидиндезаминазы, находящейся в основном в печени и опухолевых тканях. Дальнейшая трансформация до активного цитотоксического метаболита 5-ФУ происходит, преимущественно, в ткани опухоли под действием опухолевого ангиогенного фактора - тимидинфосфорилазы.
Одновременный приём пищи уменьшает скорость всасывания, однако незначительно влияет на величину AUC 5'-ДФУР и следующего метаболита, 5-ФУ. Концентрация капецитабина в плазме достигает максимума через 1,5 ч, а его метаболитов - через 2 ч после приёма препарата.
Капецитабин, 5'-ДФЦТ, 5'-ДФУР и 5-ФУ связываются с белками (главным образом, с альбумином), на 54%, 10%, 62% и 10% соответственно.
Метаболиты капецитабина становятся цитотоксичными только после превращения в 5-ФУ и его анаболиты. Далее 5-ФУ катаболизируется под воздействием дигидропиримидиндегидрогеназы, активность которой ограничивает скорость реакции с образованием неактивных метаболитов - дигидро-5-фторурацила, 5-фторуреидопропионовой кислоты (ФУПК) и a-фтор-b-аланина (ФБАЛ).
T1/2 капецитабина, 5'-ДФЦТ, 5'-ДФУР, 5-ФУ и ФБАЛ составляет, 0,85; 1,11; 0,66; 0,76 и 3,23 ч соответственно. Фармакокинетические параметры капецитабина, 5'-ДФЦТ и 5'-ДФУР на 1-й и 14-й день одинаковы. AUC 5-ФУ увеличивается к 14-ому дню на 30-35%, и больше не растёт (22 день). В диапазоне терапевтических доз фармакокинетические параметры капецитабина и его метаболитов, за исключением 5-ФУ, носят дозозависимый характер.
Препарат выводится с мочой - 95,5% и с калом - 2,6%. Основной метаболит в моче - ФБАЛ, на который приходится 57% принятой дозы. Около 3% принятой дозы выводится с мочой в неизменённом виде.
Пол, наличие или отсутствие метастазов в печени до начала лечения, индекс общего состояния пациента, концентрация общего билирубина, сывороточного альбумина, активность АЛТ и АСТ у больных раком толстой кишки не оказывали влияния на фармакокинетику 5'-ДФУР, 5-ФУ и ФБАЛ.
У пациентов с лёгкой и умеренной степенью нарушений функции печени, обусловленной метастазами, клинически значимого изменения фармакокинетики капецитабина не происходит. Данных о фармакокинетике препарата у больных с тяжёлым нарушением функции печени нет.
При различной степени (от лёгкой до тяжёлой) почечной недостаточности фармакокинетика неизменённого препарата и 5-ФУ не зависит от клиренса креатинина. Последний влияет только на величину AUC 5'-ДФУР (увеличение AUC на 35% при снижении КК на 50%) и ФБАЛ (увеличение AUC на 114% при снижении КК на 50%).
Возраст на фармакокинетику 5'-ДФУР и 5-ФУ не влияет. AUC ФБАЛ увеличивалась у пациентов в возрасте 65 лет и старше (увеличение возраста на 20% сопровождалось увеличением AUC ФБАЛ на 15%), что, вероятно, обусловлено изменением функций почек.
Показания к применению и дозирование
Показания
-
Комбинированная терапия с доцетакселом местнораспространённого или метастатического РМЖ, при неэффективности химиотерапии, включающей препарат антрациклинового ряда.
-
Монотерапия местнораспространённого или метастатического РМЖ, при неэффективности химиотерапии таксанами или препаратами антрациклинового ряда, или при наличии противопоказаний к терапии антрациклинами.
Режимы дозирования
Препарат принимают внутрь, запивая водой, не позже чем через 30 мин после еды.
Стандартный режим дозирования: при проведении монотерапии препарат назначают в дозе 2500 мг/м2 в сутки (по 1250 мг/м2 2 раза в сутки, утром и вечером), в течение двух недель с последующим недельным перерывом.
При комбинированной терапии назначают по 1250 мг/м2 2 раза в сутки в течение двух недель с последующим недельным перерывом в сочетании с доцетакселом в дозе 75 мг/м2 раз в 3 нед.
Явления токсичности можно устранить симптоматической терапией, прервав лечение или уменьшив дозу. При токсичности I степени корректировать дозу не следует. При токсичности II и III степеней препарат следует отменить. После того как выраженность нежелательных явлений уменьшится до I степени приём можно возобновить в полной дозе. При повторном развитии токсичности II и III степени дозу препарата уменьшают на 20%.
При развитии признаков токсичности IV степени лечение либо прекращают, либо прерывают до купирования или уменьшения симптоматики (до I степени), после приём возобновляют - 50% прежней дозы.
Следует немедленно прекратить приём капецитабина при возникновении токсичности тяжёлой или средней степеней тяжести. Если было пропущено несколько приёмов, то эти дозы не восполняют, а продолжают запланированные циклы терапии. Если дозу пришлось снизить, увеличивать её впоследствии нельзя.
При наличии метастазов в печени, лёгких или умеренных нарушений функции печени изменять начальную дозу не требуется, но этих больных следует тщательно наблюдать. Нет данных о влиянии препарата на пациентов с тяжёлой печёночной недостаточностью.
У больных с исходной почечной недостаточностью средней степени тяжести (КК 30-50 мл/мин) рекомендуется уменьшить начальную дозу до 75% стандартной, у больных с почечной недостаточностью лёгкой степени тяжести (КК 51-80 мл/мин) коррекция начальной дозы не требуется.
Коррекции начальной дозы у пациентов пожилого возраста не требуется, но им рекомендуется тщательный мониторинг состояния (у больных старше 80 лет токсичность III и IV степени развивалась чаще, чем у более молодых). У пациентов старше 60 лет, которые будут получать комбинацию капецитабина с доцетакселом, рекомендуется снизить начальную дозу капецитабина до 75%.
Побочное действие
Наиболее частые побочные эффекты (≥10%):
Со стороны пищеварительной системы
Чаще встречаются:
Менее чем в 5% случаев:
Описаны случаи печёночной недостаточности и холестатического гепатита; их причинная связь с применением капецитабина не установлена.
Дерматологические реакции
Чаще встречаются:
Менее чем в 5% случаев:
Cо стороны организма в целом
Повышенная утомляемость;
Менее чем в 5% случаев:
Со стороны ЦНС и периферической нервной системы
Чаще встречаются:
Менее чем в 5% случаев:
Со стороны органов чувств
Со стороны дыхательной системы:
Со стороны костно-мышечной системы:
Артралгии, миалгии.
Со стороны сердечно-сосудистой системы
Чаще всего: отёки нижних конечностей.
Менее чем в 5% случаев:
Со стороны системы кроветворения
Чаще всего: анемия, нейтропения.
Менее чем в 5% случаев - панцитопения.
Передозировка
Симптомы
Тошнота, рвота, диарея, воспаление слизистых оболочек, кровотечения из ЖКТ, а также угнетение функции костного мозга.
Лечение
Антидот отсутствует. Проводят симптоматическую терапию.
Противопоказания
С осторожностью следует назначать препарат при ИБС, почечной или печёночной недостаточности, одновременно с пероральными антикоагулянтами кумаринового ряда, а также пациентам старше 60 лет.
Беременность
Препарат противопоказан. Обычно избегают применения противоопухолевых средств во время беременности, учитывая возможное мутагенное, тератогенное и канцерогенное действие данных препаратов. Женщинам и мужчинам во время лечения гемцитабином и, как минимум, в течение 6 мес после терапии следует использовать надёжные способы контрацепции.
Кормление грудью
Неизвестно, проникает ли капецитабин в грудное молоко, но грудное вскармливание во время проведения химиотерапии не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное, тератогенное и канцерогенное действие).
Клинически значимые взаимодействия
Капецитабин усиливает эффекты непрямых антикоагулянтов, что может приводить к нарушению показателей свёртывания и кровотечениям через несколько дней или месяцев от начала терапии (а в одном случае - через месяц после её завершения).
Увеличивает AUC варфарина на 57% и МНО на 91%.
Необходимо соблюдать осторожность при назначении капецитабина с другими препаратами, метаболизирующимися изоферментом 2С9 системы цитохрома Р450, так как исследования по их взаимодействию не проводились.
Капецитабин увеличивает концентрацию фенитоина в плазме, предположительно, подавляя активность изофермента CYP2C9. У больных, принимающих оба препарата, рекомендуется регулярно контролировать концентрацию фенитоина в плазме крови.
Антациды, содержащие гидроксиды алюминия и магния, немного повышают концентрации капецитабина и его метаболита - 5'-ДФЦТ - в плазме (на остальные метаболиты не влияют).
Кальция фолинат (лейковорин) не влияет на фармакокинетику капецитабина и его метаболитов.
Соривудин и его аналоги потенциально усиливают токсичность фторпиримидинов из-за подавления активности дигидропиримидиндегидрогеназы.
Резюме и дополнительные сведения
Терапию капецитабином проводят под тщательным контролем врача, имеющего опыт проведения химиотерапии.
Большинство нежелательных явлений обратимы и не требуют полной отмены препарата, хотя может возникнуть необходимость коррекции дозы или временной отмены препарата.
Спектр кардиотоксичности при лечении капецитабином аналогичен таковому других фторпиримидинов и включает инфаркт миокарда, стенокардию, аритмии, остановку сердца, сердечную недостаточность и изменения на ЭКГ. Эти нежелательные явления более характерны для больных ИБС.
В редких случаях отмечают тяжёлые явления токсичности, ассоциированные с 5-ФУ - стоматит, диарею, нейтропению и нейротоксичность, - обусловленные недостаточной активностью дигидропиримидиндегидрогеназы. Нельзя исключить связь между сниженной активностью дигидропиримидиндегидрогеназы и более выраженной, потенциально летальной токсичностью 5-ФУ.
У больных с почечной недостаточностью средней степени тяжести (КК 30-50 мл/мин) при лечении капецитабином, как и при терапия 5-ФУ, частота нежелательных явлений III и IV степеней тяжести выше.
Лечение капецитабином может вызвать диарею. При монотерапии капецитабином диарея II-IV степеней тяжести длится, в среднем, 4-5 дней. Больных с тяжёлой диареей следует госпитализировать, и в случае дегидратации возместить потери жидкости и электролитов. При появлении диареи II, III и IV степеней приём капецитабина следует прервать до исчезновения или уменьшения её интенсивности (до I степени). При диарее III и IV степеней лечение возобновляют в редуцированной дозе. По показаниям, как можно раньше рекомендуется назначать стандартные противодиарейные препараты (например, лоперамид).
У пациентов 80 лет и старше часто развивались обратимые желудочно-кишечные расстройства III и IV степеней, такие как диарея, тошнота и стоматит. У пациентов старше 60 лет, получавших комбинированную терапию капецитабином и доцетакселом отмечено увеличение частоты нежелательных явлений III и IV степеней тяжести.
Проявление кожной токсичности - развитие ладонно-подошвенного синдрома I-III степени тяжести (пальмарно-плантарная эритродизестезия). При возникновении ладонно-подошвенного синдрома II или III степеней применение капецитабина нужно прервать до исчезновения симптомов или их уменьшения до I степени; при рецидиве синдрома III степени тяжести дозу капецитабина нужно уменьшить на 20%.
Если в связи с лечением отмечена гипербилирубинемия, более чем в 3 раза превышающая верхнюю границу нормы, или повышение активности печёночных аминотрансфераз (АЛТ, АСТ), более чем в 2,5 раза превышающее верхнюю границу нормы, применение капецитабина следует прервать. Его можно возобновить при снижении уровня билирубина и активности печёночных трансаминаз ниже указанных пределов. При заболеваниях печени неметастатического характера терапию проводят под тщательным наблюдением. Фармакокинетика при заболеваниях печени, не обусловленных метастазами в печень, а также при тяжёлой печёночной недостаточности не изучена.
У больных, одновременно принимающих капецитабин и пероральные антикоагулянты (производные кумарина), необходимо тщательно мониторировать показатели свёртываемости крови (протромбиновое время) и подбирать дозу антикоагулянта.
Безопасность и эффективность применения капецитабина у детей и подростков в возрасте до 18 лет не изучались.
Код АТХ
L01BC06
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Сapecitabine
Форма выпуска
Таблетки, покрытые оболочкой по 0,15 г (60 шт. в упаковке) и 0,5 г (120 шт. в упаковке).
Упаковка и хранение
Хранить при температуре до 30 °С, если производителем не указаны иные условия.
Ралтитрексид (Raltitrexed)
Фармакологический/химический класс АТХ
N-[5-[[(3-Дигидро-2-метил-4-оксо-6-хиназолинил)-метил]метиламино]-2-теноил]-L-глютаминовая кислота.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Ралтитрексид - аналог фолата, прямой специфический ингибитор тимидилатсинтетазы - ключевого фермента синтеза тимидинтрифосфата (нуклеотид, необходимый для синтеза ДНК). Ингибирование тимидилатсинтетазы ведёт к фрагментации ДНК и гибели клетки. Препарат с помощью восстановленного переносчика фолатов транспортируется в клетку, где подвергается полиглютатимированию посредством фермента фолилполиглютаматсинтетазы. Полиглютатимирование ралтитрексида усиливает его ингибирующую активность по отношению к тимидилатсинтетазе и увеличивает продолжительность этого действия, что потенциально может усилить противоопухолевую активность препарата, а также его токсичность из-за задержки в нормальных тканях.
Фармакологические эффекты
После внутривенного введения в дозе 3 мг/м2 кривая "концентрация-время" имеет трёхфазный характер:
При повторных введениях с трёхнедельным интервалом не отмечалось клинически значимой кумуляции ралтитрексида в плазме у пациентов с нормальной функцией почек.
Ралтитрексид выводится преимущественно почками в неизменённом виде (приблизительно 40-50%), около 15% выводится с калом. Плазменный клиренс препарата - 51,6 мл/мин; почечный клиренс - 25,1 мл/мин. T1/2 для второй фазы - 1,79 ч.
Предполагается, что часть дозы удерживается в тканях, вероятно, в виде полиглютамата. Следовые количества радиоактивной метки выявлялись в эритроцитах на 29-й день исследования.
Фармакокинетика не зависит от пола и возраста.
Фармакокинетика препарата у детей не изучалась.
Лёгкие и умеренные нарушения функции печени приводят к небольшому снижению клиренса ралтитрексида (менее чем на 25%).
Лёгкие и умеренно выраженные нарушения функции почек (КК 25-65 мл/мин) приводят к значительному снижению (примерно на 50%) клиренса ралтитрексида.
Показания к применению и дозирование
Паллиативное лечение распространённых форм рака толстой и прямой кишки.
Ралтитрексид вводят внутривенно (15-минутная инфузия).
Рекомендованная доза для взрослых 3 мг/м2 поверхности тела, раз в 21 день. Доза свыше 3 мг/м2 может привести к угрожающей жизни токсичности.
В зависимости от степени токсичности (желудочно-кишечной и/или гематологической), предыдущей дозы препарата, для повторных введений рекомендуется следующий алгоритм:
-
уменьшение дозы на 25% при III степени гематологической (нейтропения или тромбоцитопения) и/или II степени желудочно-кишечной (диарея или воспаление слизистой) токсичности;
-
уменьшение дозы на 50% при IV степени гематологической (нейтропения или тромбоцитопения) или III степени желудочно-кишечной (диарея или воспаление слизистой) токсичности;
-
прекращение лечения при развитии IV степени желудочно-кишечной токсичности (диарея или воспаление слизистой оболочки) или в случае сочетания III степени желудочно-кишечной с IV степенью гематологической токсичности.
Если доза была однажды уменьшена, все последующие введения препарата проводят в этой уменьшенной дозе.
У пациентов с нарушениями функции почек при уровне КК ниже или равном 65 мл/мин необходимо изначально уменьшить дозу ралтитрексида на 25-50%, а в дальнейшем постоянно контролировать этот показатель.
У пациентов пожилого возраста применяют с осторожностью, хотя коррекции режима дозирования не требуется. Препарат не рекомендован к применению у детей, поскольку его безопасность и эффективность у этой группы пациентов не изучалась.
Побочное действие
Со стороны пищеварительной системы
Чаще всего отмечались тошнота (57%) и рвота (35%) а также:
Обычно эти явления носят лёгкий или умеренный характер (I-II степени по шкале ВОЗ). Однако, возможно развитие тяжёлой диареи в сочетании с гематологическими нарушениями, особенно с лейкопенией.
Со стороны системы кроветворения
Чаще наблюдают лейкопению, нейтропению, анемию и тромбоцитопению. Угнетение костномозгового кроветворения обычно отмечают в первые 2 нед после введения препарата. Возможно развитие нейтропении и тромбоцитопении (IV степень по шкале ВОЗ), которые могут быть тяжёлыми и угрожающими жизни, особенно в сочетании с токсическими явлениями со стороны ЖКТ.
Со стороны костно-мышечной системы - артралгия.
Со стороны ЦНС - повышение мышечного тонуса (обычно в виде судорог), головная боль.
Со стороны органа зрения - конъюнктивит.
Дерматологические реакции
Чаще всего:
Прочие
Часто: астения, лихорадка, гриппоподобный синдром.
Реже: боли в животе, болевой синдром других локализаций, присоединение вторичной инфекции, поверхностная флегмона, сепсис, снижение массы тела, дегидратация, периферические отёки.
Передозировка
Симптомы
Ожидаемые проявления передозировки - усиление угнетения костномозгового кроветворения и выраженности симптомов диспепсии.
Лечение
Антидота с доказанной клинической эффективностью не существует. По некоторым данным, лейковоринª уменьшает токсическое действие препарата. При передозировке как можно раньше рекомендуется начать внутривенное введение фолината кальция в дозе 25 мг/м2 каждые 6 ч до разрешения симптомов.
В случае возникновения токсичности применяют стандартную поддерживающее и симптоматическую терапию.
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу:
Нельзя применять при беременности и лактации.
Не рекомендуется использовать у детей.
Беременность
Препарат противопоказан. Мужчинам и женщинам детородного возраста в период лечения ралтитрексидом и как минимум в течение 6 мес после прекращения терапии следует использовать надёжные методы контрацепции.
Кормление грудью
Неизвестно, проникает ли ралтитрексид в грудное молоко, но грудное вскармливание во время проведения химиотерапии не рекомендуется из-за риска для детей (неблагоприятные эффекты, мутагенное, тератогенное и канцерогенное действие).
Клинически значимые взаимодействия
Фолиниевая кислота, фолиевая кислота и витаминные препараты, их содержащие, снижают эффективность ралтитрексида, поэтому их не следует использовать одновременно.
Клинически значимого взаимодействия ралтитрексида с НПВС или варфарином не выявлено.
Препарат не следует смешивать в шприцах с другими лекарственными средствами.
Резюме и дополнительные сведения
Терапию ралтитрексидом проводят под тщательным контролем врача, имеющего опыт проведения химиотерапии. Необходимо внимательно наблюдать за пациентами с подавленной функцией костного мозга, плохим общим состоянием или после радиотерапии.
Пациенты с прогрессированием после предшествующего лечения (с включением 5-ФУ) распространённым опухолевым процессом могут также оказаться нечувствительными к действию ралтитрексида.
Перед каждым введением препарата необходим контроль картины периферической крови (включая формулу крови и тромбоциты), активности печёночных трансаминаз, содержания билирубина и креатинина в сыворотке крови.
Препарат можно вводить только при следующих показателях крови:
Повторные введения препарата возможны только при исчезновении всех признаков токсичности (в особенности желудочно-кишечной и гематологической).
Пациентам, у которых развились признаки желудочно-кишечной токсичности, необходимо контролировать картину периферической крови (включая формулу крови и тромбоциты) не реже раза в неделю для выявления гематологической токсичности.
В случае развития IV степени желудочно-кишечной токсичности (диарея или воспаление слизистой) или в случае сочетания III степени желудочно-кишечной с IV степенью гематологической токсичности лечение ралтитрексидом следует прекратить и немедленно начать стандартную поддерживающую терапию, включающую внутривенное введение жидкости и терапевтические мероприятия для поддержания костномозгового кроветворения. Возможно внутривенное введение фолиниевой кислоты (лейковоринаª) в дозе 25 мг/м2 каждые 6 ч до исчезновения симптоматики. Дальнейшее применение ралтитрексида у таких пациентов не рекомендуется.
Некоторые побочные эффекты ралтитрексида, такие как недомогание или астения, могут отрицательно влиять на способность к управлению автомобилем и выполненению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Код АТХ
L01BA03
Торговые наименования, формы выпуска и производители
Используемые в России торговые непатентованное наименование ралтитрексида
Формы выпуска
Лиофилизированный порошок для приготовления раствора для внутривенных инфузий во флаконах по 2 мг на 5 мл.
Условия и сроки хранения
Лиофилизированный порошок для инфузий следует хранить в защищённом от света, недоступном для детей месте при температуре не выше 25 °С. Срок годности 3 года.
Растворённый препарат следует хранить при температуре от 2до 8 °С не более 24 ч.
Тегафур (Tegafur)
Фармакологический/химический класс АТХ
5-Фтор-1(тетрагидро-2-Фурaнил)-2,4 (1Н,3Н)-пиримидиндион (в виде натриевой соли).
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Действие обусловленно нарушением синтеза ДНК и РНК. Образующийся в результате гидролиза фторурацил ингибирует фермент тимидилатсинтетазу и синтез ДНК; внедряется в структуру РНК вместо урацила, делая её дефектной, и ингибирует клеточную пролиферацию.
В клетках опухоли превращается в 5-фтор-дезоксиуридин-5-монофосфат (фосфорилируется в трифосфат и включается в структуру РНК), и флоксуридина монофосфат, который ингибирует тимидилатсинтетазу. Менее токсичен и лучше переносится пациентами, чем 5-ФУ.
Фармакокинетика
При приёме внутрь тегафур быстро абсорбируется из ЖКТ и обнаруживается в крови, по крайней мере, в течение 24 ч после однократного применения. Максимальная концентрация в плазме достигается в течение 4-6 ч после введения. Биодоступность практически полная.
Обладает высокой липофильностью (в 200 раз выше, чем фторурацил), оставаясь при этом водорастворимым соединением. Высокая липофильность обеспечивает быстрое прохождение через биологические мембраны, распределение в организме и проникновение через гематоэнцефалический барьер.
Метаболизируется в печени с образованием фармакологически активного 5-ФУ (концентрация значительно ниже, но более стабильная). Биоактивация происходит не только в печени, но и в опухолевой ткани, отличающейся повышенным содержанием цитозольных гидролитических ферментов.
Показания к применению и дозирование
Препарат показан при раке желудка, толстой и прямой кишки; РМЖ; кожной лимфоме.
Применяют внутрь. Суточная доза составляет 800-1000 мг/м2 поверхности тела (20-30 мг/кг массы тела) в 2-4 приёма, но не более 2 г в сутки. Интервал между курсами составляет 4 нед. Доза тегафура может быть уменьшена у пациентов пожилого возраста и у ослабленных больных.
Побочные эффекты
Со стороны системы кроветворения - лейкопения, тромбоцитопения, анемия.
Со стороны пищеварительной системы
Чаще всего:
Редко:
Со стороны ЦНС:
Со стороны сердечно-сосудистой системы:
Со стороны органов чувств:
Дерматологические реакции
Прочие
Передозировка
Симптомы
Усиление токсических эффектов со стороны ЖКТ и ЦНС, угнетение гемопоэза.
Лечение
Контроль функции кроветворения в течение не менее чем 4 нед, при необходимости проводят симптоматическую терапию. Специфический антидот неизвестен.
Противопоказания
Препарат противопоказан при:
С осторожностью следует применять у пациентов с нарушением кроветворения, функций печени и почек, метаболизма глюкозы; при язвенной болезни желудка и двенадцатиперстной кишки, склонностью к кровотечениям, с инфекционными заболеваниями (ветряная оспа, герпес и другие инфекции).
Беременность
Препарат противопоказан.
Кормление грудью
При необходимости назначения препарата грудное вскармливание следует прекратить.
Резюме и дополнительные сведения
При необходимости назначения тегафура пациентам с нарушениями кроветворения, функций печени и почек, метаболизма глюкозы, с язвенной болезнью желудка и двенадцатиперстной кишки, склонностью к геморрагиям, с инфекционными заболеваниями следует учитывать потенциальный риск развития тяжёлых побочных реакций. В период лечения следует регулярно контролировать картину периферической крови, функциональное состояние печени и почек. При длительном применении препарата побочное действие усиливается.
Головокружение, тошнота и рвота уменьшаются при фракционировании суточной дозы.
При развитии серьёзных побочных эффектов препарат следует отменить.
Тегафур угнетает репродуктивную функцию.
Безопасность применения у детей не установлена.
Клинически значимые взаимодействия
При одновременном применении тегафур способен усиливать действие фенитоина.
Тегафур повышает эффективность других химиотерапевтических средств и лучевой терапии (усиливается также и побочное действие).
Токсичность тегафура повышается при одновременном применении с ингибиторами микросомального окисления в печени.
КОД АТХ
L01BC03
Торговые наименования, формы выпуска, производители
Используемые в России торговые непатентованное наименование Tegafura
Форма выпуска
Капсулы по 400 мг (100 шт. в упаковке).
Условия и сроки хранения
Препарат следует хранить в недоступном для детей, тёмном месте, при температуре не выше 25 °С. Срок годности 4 года.
Синтетические противоопухолевые препараты разных химических групп
Комплексные соединения платины
Цисплатин (Cisplatin)
Фармакологичеких/химический класс АТХ
Цис-Диаминдихлорплатина (II)
Терапевтичекий класс АТХ
Системное, противоопухолевое действие.
Механизм действия
Цисплатин сходен с алкилирующими препаратами. Хотя точный механизм его действия неизвестен, полагают, что оно подобно действию бифункциональных алкилирующих препаратов, которое заключается в возможном образовании поперечных сшивок и нарушении функции ДНК, а также некотором действии на РНК. Цисплатин - циклонеспецифичным препаратом.
Возможен его иммуностимулирующий эффект.
Фармакокинетика
Препарат плохо проходит через гематоэнцефалический барьер. Связывание с белками (в виде метаболитов) очень высокое - более 90%. Биотрансформация происходит путём быстрого неферментативного превращения в неактивные метаболиты.
Период полувыведения: в начальной фазе составляет 25-49 мин; в конечной при нормальной выделительной функции - 58-73 ч, а при анурии до 240 ч.
Выведение: почками (27-43% через 5 дней); платину можно обнаружить в тканях в течение 4 мес и более после введения. При проведении диализа цисплатин удаляется из крови, но только в течение 3 ч после введения.
Длительность действия препарата: ингибирование ДНК сохраняется в течение нескольких дней после введения.
Показания к применению и дозирование
Обычная доза для взрослых и подростков: вводят раствор цисплатина препарат внутривенно; при монохимиотерапии - по 20 мг/м2 в сутки в течение 5 дней или по 100-120 мг/м2 каждые 3 нед. Больным, ранее получавшим в больших дозах лучевую терапию или химиотерапию, рекомендуют меньшую из доз указанного диапазона.
Общая доза для одного цикла цисплатина (вводимая в виде однократной инфузии в сутки или в виде непрерывной инфузии в течение нескольких дней, с повторением каждые 3 нед) не должна превышать 120 мг/м2. Использование более высоких доз в течение одного цикла может приводить к потенциально смертельной передозировке.
Одно из наиболее грозных осложнений терапии цисплатином - нефротоксичность, сопровождается повреждением почечных канальцев, что проявляется повышением уровня креатинина, мочевины и мочевой кислоты в сыворотке крови и/или снижением клиренса креатинина. Нефротоксичность носит кумулятивный характер и относится к основным токсическим факторам, ограничивающим дозу препарата.
С целью стимуляции диуреза и для максимального уменьшения нефротоксического действия проводят плановую гидратацию.
-
Перед введением цисплатина внутривенно капельно в течение 2-4 ч вводят 1,5-2 л 0,9% раствора хлорида натрия или 5% раствора декстрозы.
-
Затем внутривенно капельно в течение 60 мин вводят цисплатин, разведённый в 500 мл 0,9% раствора хлорида натрия.
-
После завершения инфузии проводят постгидратацию в объёме 1-1,5 л 0,9% раствора хлорида натрия или 5% раствора декстрозы.
-
Для усиления диуреза в течение последних 30 мин предварительной гидратации или по её окончании можно ввести внутривенно капельно раствор маннита для инъекций. Обильное потребление жидкости и поддержание диуреза необходимо соблюдать в течение 24 ч.
Цисплатин относится к группе высокоэметогенных препаратов. Тошноту и рвоту, которые обычно начинаются в течение первого часа терапии и продолжаются в течение 24 ч и более, наблюдают более чем у 70% больных. Эти побочные эффекты лишь частично устраняются при применении стандартных противорвотных ЛС.
Побочные эффекты
Многие побочные эффекты противоопухолевой терапии - неизбежное проявление фармакологического действия препарата. Некоторые из них (например, лейкопению и тромбоцитопению) используют в качестве параметров при индивидуальном подборе дозы. Побочные эффекты более выражены при дозах цисплатина, превышающих 50 мг/м2.
Сообщалось о редких случаях токсического действия на сосуды при использовании цисплатина в комбинации с другими противоопухолевыми препаратами, хотя неизвестно, было ли токсическое действие связано с применением цисплатина или с другими факторами. Описанные случаи токсического действия на сосуды включали инфаркт миокарда, нарушение мозгового кровообращения, тромботическую микроангиопатию, церебральный артериит и синдром Рейно.
Следующие побочные/неблагоприятные эффекты отобраны на основе их потенциальной клинической значимости:
-
Более часто и при повторном введении:
-
Выраженная тошнота и рвота. Тошнота и рвота обычно начинаются через 1-4 ч после введения дозы, и рвота может продолжаться в течение 24 ч. Тошнота и анорексия могут сохраняться в течение 1 нед. Установлено, что для профилактики сильной тошноты и рвоты можно использовать антагонисты серотонина (например, ондансетрон), метоклопрамид внутривенно в высоких дозах и кортикостероиды.
-
Анемия, связанная с угнетением функции костного мозга: обычно бессимптомная; более выражена при более высоких дозах.
-
Нефротоксическое действие, часто в форме острой почечной недостаточности, которая может обнаруживаться на начальных стадиях только при проведении функциональных почечных тестов. Изменения лабораторных показателей выявляются в течение второй недели после введения дозы. Нефротоксическое действие дозозависимо возникает следствие накопления препарата; обычно оно обратимо, но при высоких дозах или при повторных циклах лечения может становиться необратимым и иногда приводит к смертельному исходу.
-
Гипокальциемия и гипомагниемия могут развиваться в связи с нефротоксическим действием. В редких случаях возможны тетания, связанная с гипокальциемией, дрожание или судорожные припадки как результат гипомагниемии
-
Гиперурикемия или нефропатия, связанная с повышенным образованием мочевой кислоты (максимальные концентрации мочевой кислоты отмечают через 3-5 дней после введения дозы ЛС.
-
Ототоксическое действие: потеря равновесия, звон в ушах, нарушение слуха. Ототоксическое действие может быть более сильным у детей и может быть необратимым. Ототоксический эффект - следствие накопления препарата; потеря слуха начинается с высоких частот (выше тонов речи) и может быть односторонней или двусторонней.
-
-
Примечание: экстравазат может в редких случаях оказывать местное токсическое действие на мягкие ткани, тяжесть которого зависит от концентрации раствора. При инфузии растворов с концентрацией цисплатина выше 500 мкг/мл (0,5 мг/мл) могут возникать целлюлит, фиброз и некроз тканей. Нейротоксическое действие, обычно проявляющееся периферической нейропатией, может возникать после однократной дозы или длительного лечения (4-7 мес) и может быть тяжёлым и необратимым. Признаки и симптомы нейропатии обычно развиваются во время лечения, но в редких случаях могут появляться через 3-8 нед после введения последней дозы и могут усиливаться даже после отмены цисплатина.
Примечание: ретробулъбарный неврит, отёк диска зрительного нерва или корковая слепота обычно обратимы после отмены препарата. При офтальмоскопии, как правило, обнаруживают только неравномерную пигментацию сетчатки в области пятна.
Передозировка
В случае передозировки отмечают усиление описанных побочных симптомов. Для лечения: необходим тщательный контроль состояния пациента, в том числе гематологических показателей; проводят симптоматическую терапию; антидот неизвестен.
Противопоказания
Необходимо сопоставлять риск и пользу в следующих случаях:
Следует также соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Беременность
Цисплатин может оказывать токсическое действие на органы мочеполовой системы плода.
Первый триместр: обычно рекомендуют избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Хотя информация ограниченна из-за относительно малого числа случаев использования противоопухолевых средств во время беременности, необходимо учитывать возможное мутагенное, тератогенное и канцерогенное действие данных ЛС. Другие факторы, оказывающие вредное действие на плод, включают неблагоприятные реакции, отмечаемые у взрослых.
Как правило, в период лечения цитотоксическими препаратами рекомендуется применение противозачаточных средств.
Кормление грудью
Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограниченна, во время проведения химиотерапии грудное вскармливание не рекомендуется из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны на основе их потенциальной клинической значимости. Комбинации, содержащие любое из перечисленных веществ, в зависимости от имеющегося количества, могут также взаимодействовать с данным ЛС.
Цисплатин может повышать концентрацию мочевой кислоты в крови; при лечении гиперурикемии и подагры может потребоваться корректировка доз противоподагрических средств; применение урикозурических противоподагрических препаратов может увеличивать риск нефропатии, связанной с повышенным образованием мочевой кислоты, поэтому предпочтительным препаратом для предотвращения или устранения связанной с использованием цисплатина гиперурикемии может быть аллопуринол.
Одновременное применение с цисплатином может маскировать симптомы ототоксического действия, такие как шум в ушах или головокружение.
Вызываемое цисплатином нарушение функции почек может приводить к токсическому действию блеомицина даже при низких дозах; в связи с частым применением комбинации этих двух препаратов рекомендуется осторожность.
Лейкопеническое и/или тромбоцитопеническое действие цисплатина может усиливаться при одновременном или недавно проводившемся лечении, если эти препараты дают такой же эффект; корректировку дозы цисплатина при необходимости следует проводить на основании результатов анализа крови.
При одновременном применении возможно усиление суммарных эффектов этих препаратов и лучевой терапии; рекомендуется снижение дозы.
Одновременного и/или последовательного применения следует избегать, так как возможно повышение вероятности нефро- и ототоксического действия, особенно при уже имеющемся нарушении функции почек.
Резюме и дополнительные сведения
Цисплатин следует вводить в соответствующих условиях под наблюдением врача или медицинской сестры, имеющих опыт проведения химиотерапии рака. Рекомендуется также, чтобы при каждом введении цисплатина были наготове оборудование и лекарственные средства, необходимые для устранения возможной анафилактической реакции (включая адреналин, кислород, антигистаминные средства и кортикостероиды для внутривенного введения).
Используют ряд схем и режимов применения цисплатина в отдельности или в комбинации с другими противоопухолевыми препаратами.
Цисплатин рекомендуется вводить вместе с интенсивной парентеральной инфузией для повышения содержания жидкости в организме; это необходимо для поддержания диуреза и ослабления нефро- и ототоксического действия, что не всегда достигается.
Рекомендуют предварительное интенсивное внутривенное введение жидкости с последующим обильным потреблением жидкости и поддержанием диуреза в течение 24 ч. Для обеспечения интенсивного диуреза, не сопровождающегося избыточным обезвоживанием и потерей солей, можно также использовать маннитол (маннит) и фуросемид.
Цисплатин вводили также путём непрерывной внутривенной инфузии в течение 24-120 ч. Данный способ введения ослабляет тошноту и рвоту, но не нефро- или ототоксическое действие. Развитие нефропатии связанной с повышенным образованием мочевой кислоты, у больных лейкозом или лимфомой можно предотвратить путём адекватного потребления жидкости и, в некоторых случаях, применением аллопуринола. При повышении концентрации мочевой кислоты в сыворотке крови может быть необходимо подщелачивание мочи.
Для снижения риска кумулятивного нефротоксического действия последующие циклы лечения цисплатином рекомендуется проводить не чаще 1 раза в 3-4 нед.
Очередние дозы цисплатина нельзя вводить до нормализации показателей функции почек (уровень азота мочевины в крови, клиренс креатинина и уровень креатинина в сыворотке крови). Введение последующих доз цисплатина также не рекомендуется до тех пор, пока уровень тромбоцитов не достигнет, по крайней мере, 100x109/л, а нейтрофилов - по крайней мере, 1,5x109/л или пока не будет подтверждено, что острота слуха находится в пределах нормы. Ототоксическое действие цисплатина может быть более сильным у детей.
При появлении первых признаков нейротоксического действия, которое может быть необратимым, лечение цисплатином следует прекратить.
У больных с развившейся в результате применения цисплатина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности. Эти меры могут включать чрезвычайную осторожность при выполнении инвазивных процедур:
-
кожи и слизистых оболочек для выявления признаков кровотечений или кровоизлияний,
-
ограничение частоты венопункций и отказ от внутримышечных инъекций,
-
анализ мочи, рвотных масс, кала и секретов на скрытую кровь,
-
осторожность при применении зубных щеток, нитей для чистки межзубных промежутков, зубочисток, безопасных бритв и ножниц для стрижки ногтей,
-
соблюдение осторожности для предотвращения падений или других травм.
Таким больным следует избегать употребления алкоголя и приёма аспиринаª из-за риска желудочно-кишечных кровотечений. Могут потребоваться переливания тромбоцитов.
Больных с развившейся лейкопенией следует тщательно наблюдать для выявления признаков возникновения инфекции. Может потребоваться использование антибиотиков. У больных с фебрильной нейтропенией парентеральное применение антибиотиков широкого спектра действия необходимо начинать эмпирически, до получения результатов бактериологических исследований и соответствующих диагностических тестов.
Информация о зависимости эффекта цисплатина от возраста у пожилых людей отсутствует. Однако у пожилых больных более вероятны возрастные нарушения функции почек, что может потребовать снижения дозы у больных, получающих цисплатин.
Возможные отдалённые эффекты многих противоопухолевых препаратов - вторичные злокачественные опухоли, хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств. Влияние дозы и продолжительности лечения также неизвестно, но, вероятно, риск повышается при длительном применении. Хотя информация ограничена, имеющиеся данные позволяют предположить, что риск канцерогенного действия наиболее высок при использовании алкилирующих препаратов.
Сообщалось о редких случаях развития острого лейкоза у больных, которых лечили цисплатином, обычно в комбинации с другими препаратами, обладающими способностью вызывать лейкоз.
Код АТХ
L01XA01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Cisplatin:
Форма выпуска: концентрированный раствор для приготовления инфузий во флаконах тёмного стекла по 10 мг/20 мл, 25 мг/50 мл, 50 мг/100 мл. По одному флакону в картонной коробке.
Хранить при температуре 15-25 °С, если производителем не указано иначе. Не допускать замораживания.
Карбоплатин (Carboplatin)
Фармакологичеких/химический класс АТХ
цис-Диамино (1,1-циклобутандикарбоксилат) платина.
Терапевтичекий класс АТХ
Системное, противоопухолевое cредство, содержащее платину
Механизм действия
Карбоплатин сходен с алкилирующими препаратами. Хотя точный механизм его действия неизвестен, полагают, что оно подобно действию бифункциональных алкилирующих препаратов, которое заключается в возможном образовании поперечных сшивок и нарушении функции ДНК, что приводит к подавлению биосинтеза нуклеиновых кислот и гибели клеток. Карбоплатин - циклонеспецифичный препарат.
Физико-химические свойства
Молекулярная масса - 371,25.
Фармакокинетика
Связывание с белками очень низкое. Однако платина, образующаяся из карбоплатина, необратимо связывается с белками плазмы крови и медленно выводится с минимальным периодом полувыведения 5 дней. Метаболизируется путём гидролиза в растворе (гидратация) с более низкой скоростью, чем цисплатин, до активных соединений, которые взаимодействуют с ДНК.
Период полувыведения: начальная фаза - 1,1-2,0 ч, конечная фаза - 2,6-5,9 ч. Выводится почками, 71% в течение 24 ч при значениях клиренса креатинина 60 мл/мин и выше.
Показания к применению и дозирование
Карбоплатин применяют как в виде монотерапии, так и в сочетании с другими противоопухолевыми препаратами. Режим дозирования устанавливают индивидуально, в зависимости от показаний, стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии.
Препарат вводят в дозе 300-400 мг/м2 внутривенно в течение 60 мин или в виде 24 часовой инфузии, однократно каждые 3-4 нед (в 1-й день).
Примечание: больным с клиренсом креатинина 41-59 мл/мин рекомендуется начальная доза препарата 250 мг/м2, больным с клиренсом креатинина 16-40 мл/мин - 200 мг/м2. Определить исходную дозу препарата в миллиграммах можно по формуле Кальверта, описывающей зависимость значения скорости гломерулярной фильтрпации (СГФ в мл/мин) и желаемой концентрации препарата от времени [AUC в мг/(мл x мин)]:
Общая доза (мг) = AUC x (СГФ+25).
Больным пожилого возраста могут требоваться более низкие дозы.
Побочные эффекты
Многие побочные эффекты противоопухолевой терапии - неизбежное проявление фармакологического действия препарата. Некоторые из них (например, лейкопению и тромбоцитопению) используют в качестве параметров при индивидуальном подборе дозы.
В редких случаях карбоплатин оказывает слабое нефротоксическое действие, которое может обнаруживаться на начальных стадиях только при проведении функциональных почечных тестов.
Следующие побочные/неблагоприятные эффекты отобраны на основе их потенциальной клинической значимости.
Примечание: анемия может быть следствием накопления препарата; часто требуются переливания крови. При лейкопении и тромбоцитопении: наиболее низкий уровень лейкоцитов и тромбоцитов отмечают через 14 дней, он обычно восстанавливается к 21-му дню после введения дозы. Лейкопения и тромбоцитопения дозозависимы и возникают вследствие накопления препарата; у небольшой части больных (менее 10%) эти эффекты непрогнозируемы. Астения бывает менее часто и может быть связана с анемией. Тошноту и рвоту отмечают примерно у 65% больных; тяжёлые формы выявляют примерно у трети больных. Только тошноту отмечают примерно у 10-15% больных. Обычно тошнота и рвота возникают через 6-12 ч после введения препарата, рвота может продолжаться в течение 24 ч.
Примечание: аллергическую реакцию обычно отмечают в течение нескольких минут после введения препарата. Нейротоксическое действие может быть следствием накопления препарата. При ототоксическом действии потеря слуха обычно начинается с высоких частот (выше тонов речи) и может быть односторонней или двусторонней.
Передозировка
В случае передозировки происходит усиление описанных побочных симптомов. Для лечения необходим тщательный контроль состояния пациента, в том числе гематологических показателей; проводят симптоматическую терапию. Антидот неизвестен.
Противопоказания
Включённые медицинские проблемы/противопоказания отобраны на основе их потенциальной клинической значимости.
Необходимо сопоставлять риск и пользу в следующих случаях:
Больным с нарушением функции почек рекомендуются более низкие дозы карбоплатина и тщательный контроль картины крови между циклами терапии.
Повышенная чувствительность к карбоплатину.
Следует также соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Беременность
Карбоплатин оказывает эмбриотоксическое и тератогенное действие у крыс.
Первый триместр: желательно избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Хотя информация ограниченна из-за относительно малого числа случаев использования противоопухолевых средств во время беременности, необходимо учитывать возможное мутагенное, тератогенное и канцерогенное действие данных препаратов.
Другие факторы, оказывающие вредное действие на плод, включают неблагоприятные реакции, отмечаемые у взрослых.
Как правило, в период лечения цитотоксическими препаратами рекомендуется применение противозачаточных средств.
Кормление грудью
Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограничена, во время применения карбоплатина грудное вскармливание не рекомендуют из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие). Проникает ли карбоплатин в грудное молоко, неизвестно.
Клинически значимые взаимодействия
Больные, обладающие повышенной чувствительностью к цисплатину и другим содержащим платину соединениям, могут иметь повышенную чувствительность и к карбоплатину.
Взаимодействие ЛС и/или связанные с ним проблемы отобраны на основе их потенциальной клинической значимости: комбинации, содержащие любое из перечисленных веществ, в зависимости от имеющегося количества, могут также взаимодействовать с данным препаратом.
Лейкопеническое и/или тромбоцитопеническое действие карбоплатина может усиливаться при одновременном или недавно проводившемся лечении, если эти препараты дают такой же эффект. Корректировку дозы карбоплатина при необходимости следует проводить на основании результатов анализа крови.
При одновременном применении возможно усиление суммарных эффектов этих препаратов и лучевой терапии, рекомендуется снижение дозы.
У больных, которых ранее лечили цисплатином, частота вызываемых карбоплатином нейротоксических или ототоксических эффектов повышена; применение карбоплатина усиливает вызванное ранее цисплатином нейротоксическое (примерно у 30% таких больных) или ототоксическое действие.
При одновременном и/или последовательном применении возможно повышение вероятности нефро- и ототоксического действия.
Резюме и дополнительные сведения
Больные, получающие карбоплатин, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии рака. Рекомендуется также, чтобы при каждом введении карбоплатина на готове были оборудование и лекарственные средства, необходимые для устранения возможной анафилактической реакции (включая адреналин, кислород, антигистаминные средства и адренокортикоиды для внутритвенного введения).
Дозу необходимо корректировать на основании клинического эффекта и появления или степени тяжести токсического действия с учётом индивидуальных особенностей каждого больного.
Карбоплатин можно применять в комбинации с другими препаратами в различных схемах. В результате этого возможно изменение частоты и/или тяжести побочных эффектов и использование различных доз (обычно сниженных).
Карбоплатин рекомендуется вводить путём внутривенной инфузии, обычно в течение 60 мин. Введения жидкости до или после применения карбоплатина, а также форсированного диуреза не требуется.
Карбоплатин вводят, также, путём непрерывной внутривенной инфузии в течение более 24 ч или путём деления общей дозы на 6 последовательных суточных доз. Данный способ введения ослабляет тошноту и рвоту, но не нефро- или ототоксическое действие.
Циклы лечения карбоплатином рекомендуется проводить не чаще 1 раза в 3-4 нед для полного восстановления функции костного мозга.
Последующие дозы карбоплатина не рекомендуется вводить до тех пор, пока уровень тромбоцитов не достигнет, по крайней мере, 100x109/л, а нейтрофилов - по крайней мере 1,5x109/л.
У больных с развившейся в результате применения карбоплатина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности. Эти меры могут включать:
-
чрезвычайную осторожность при выполнении инвазивных процедур;
-
регулярный осмотр мест внутривенного введения препаратов, кожи и слизистых оболочек для выявления признаков кровотечений или кровоизлияний;
-
ограничение частоты венопункций и отказ от внутримышечных инъекций;
-
анализ мочи, рвотных масс, кала и секретов на скрытую кровь;
-
осторожность при применении зубных щеток, нитей для чистки межзубных промежутков, зубочисток, безопасных бритв и ножниц для стрижки ногтей;
-
соблюдение осторожности для предотвращения падений или других травм.
Таким больным следует избегать употребления алкоголя и приёма аспирина из-за риска желудочно-кишечных кровотечений. Могут потребоваться переливания тромбоцитов.
Больных с развившейся лейкопенией следует тщательно наблюдать для выявления признаков возникновения инфекции. Может потребоваться использование антибиотиков. У больных с фебрильной нейтропенией парентеральное применение антибиотиков широкого спектра действия необходимо начинать эмпирически, до получения результатов бактериологических исследований и соответствующих диагностических тестов.
У больных, получающих противоопухолевую терапию, особенно с использованием алкилирующих препаратов, возможно угнетение функции половых желез, приводящее к аменорее или азооспермии. Как правило, эти эффекты зависят от дозы и продолжительности лечения и могут быть необратимыми. Прогнозирование степени нарушения функции яичек или яичников осложняется обычным применением комбинаций нескольких противоопухолевых препаратов, что затрудняет оценку эффекта каждого из них в отдельности.
Информация о зависимости эффекта карбоплатина от возраста у детей отсутствует.
У больных старше 65 лет частота периферического нейротоксического действия повышена, а токсическое действие на костный мозг может быть более тяжёлым. Кроме того, у пожилых больных более вероятны возрастные нарушения функции почек, что может требовать снижения дозы и тщательного контроля картины крови у больных, получающих карбоплатин.
Код АТХ
L01XA2
Торговые наименования, формы выпуска и производителя
Используемые в России торговые наименования Carboplatin:
Формы выпуска: раствор для инфузий концентрированный во флаконах по 50 мг/5 мл, 150 мг/15 мл, 450 мг/45 мл; по одному флакону в картонной коробке.
Хранить при температуре 15-30 °С, если производителем не указано иначе. Защищать от света. Не допускать замораживания.
Несовместимость: не использовать иглы, системы для внутривенного введения или оборудование, содержащие алюминий, так как карбоплатин несовместим с алюминием.
Оксалиплатин (Оxaliplatin)
Фармакологичеких/химический класс АТХ
[(1R,2R)-1,2-Циклогександиамин-N,N´][оксалато(2)-О,О´]платина.
Терапевтичекий класс АТХ
Противоопухолевый препарат, производное платины.
Механизм действия
Биотрансформированные, водные производные оксалиплатина взаимодействуя с ДНК путём образования меж- и внутритяжевых мостиков подавляют синтез ДНК, что ведёт к цитотоксичности и противоопухолевому эффекту.
Фармакокинетика
Препарат относится к новому классу производных платины, в котором атом платины образует комплекс с оксалатом и 1,2-диаминоциклогексаном. Он также проявляет активность in vitro и in vivo на различных моделях опухолей, устойчивых к цисплатину.
In vivo оксалиплатин подвергается активной биотрансформации и не выявляется в плазме уже к концу двухчасового введения в дозе 85 мг/м2. При этом 15% выведенной платины находится в крови, а остальные 85% быстро распределяются по тканям или выводятся с мочой. Платина связывается с альбумином плазмы и выводится с мочой в течение 48 ч. К пятому дню около 54% всей дозы обнаруживают в моче и менее 3% - в кале.
При почечной недостаточности наблюдают значительное снижение клиренса оксалиплатина с 17,6±2,18 л/час до 9,95±1,91 л/час. Влияние тяжёлой почечной недостаточности на клиренс платины ещё не изучено.
Показания к применению и дозирование
Оксалиплатин применяют только у взрослых. Препарат вводят внутривенно капельно в виде 2-6 часовых инфузий. Гипергидратация при применении оксалиплатина не требуется. Если оксалиплатин применяется в комбинации с 5-фторурацилом, инфузия оксалиплатина должно предшествовать введению 5-фторурацила.
Рекомендованная доза составляет 85 мг/м2 1 раз в 2 нед в качестве монотерапии или в комбинации с 5-фторурацилом. В адьювантном режиме рекомендовано проведение 12 циклов химиотерапии (6 мес).
Повторные введения оксалиплатина производят только при количестве нейтрофилов >1,5x109/л и тромбоцитов >50x109/л
В случае гематологических нарушений (количество нейтрофилов <1,5x109/л и/или тромбоцитов <50x109/л) назначение следующего цикла откладывается до восстановления лабораторных показателей.
Доза оксалиплатина при последующих введениях должна быть снижена с 85 мг/м2 до 65 мг/м2 в дополнение к обычному снижению дозы 5-фторурацила в случае их комбинированного применения при
Больным, у которых в ходе инфузии или в течение нескольких часов после двухчасовой инфузии развивается острая гортанно-глоточная парестезия, следующую инфузию оксалиплатина следует проводить в течение 6 часов.
При симптомах нейтротоксичности, вызывающих боль, продолжительностью более, чем 7 дней или при парестезии без функциональных нарушений, сохраняющейся до следующего цикла, последующая доза оксалиплатина должна быть снижена на 25%. При парестезии с функциональными нарушениями, сохраняющейся до следующего цикла, оксалиплатин должен быть отменён. При уменьшении выраженности симптомов нейротоксичности после отмены оксалиплатина, можно рассмотреть вопрос о возобновлении лечения.
Больные с почечной недостаточностью: данных по применению препарата у больных с тяжёлой степенью нарушения функции почек нет. В связи с ограниченностью данных в отношении безопасности и переносимости препарата у больных с умеренной степенью нарушения функции почек, перед применением оксалиплатина следует взвесить отношение риска и пользы для больного. Терапия данной категории больных может быть начата с рекомендованной дозы, под тщательным контролем функции почек. При лёгкой степени нарушения функции почек коррекции дозы оксалипалтина не требуется.
Больные с недостаточностью функции печени: изменения дозировки у больных со слабой или умеренной формой недостаточности функции печени не требуется. Данных по применению оксалиплатина у больных с тяжёлыми нарушениями нет.
Побочные эффекты
Примечание: нейротоксичность дозолимитирующий фактор. Часто симптомы сенсорной нейропатии провоцирует холод. Длительность этих симптомов, которые обычно купируются в промежутках между циклами, увеличивается в зависимости от суммарной дозы оксалиплатина. Функциональные нарушения в виде затруднения выполнения точных движений возможные последствия сенсорного повреждения. Риск функциональных нарушений при суммарной дозе около 850 мг (10 циклов) составляет приблизительно 10%, достигая 20% в случае суммарной дозы 1020 мг (12 циклов). После прекращения лечения в большинстве случаев степень тяжести неврологических симптомов уменьшается или полностью купируется.
У 3% больных через 3 года после окончания лечения наблюдали устойчивые локальные парестезии умеренной интенсивности. На фоне терапии оксалиплатином отмечены острые нейросенсорные проявления, которые возникали в течение нескольких часов после введения препарата и чаще провоцировались холодом. Они характеризовались преходящей парестезией, дизетезией или гипостезией, редко (1-2%) - острым синдромом гортанно-глоточной дизестезии: чувство дисфагии или одышки без объективных признаков респираторного дистресс-синдрома, или же спазмом гортани или бронхоспазмом. Также наблюдали такие проявления как спазм мышц челюсти, дизестезия языка, дизартрия. Обычно все эти симптомы быстро купировали как без применения медикаментозной терапии, так и при введении антигистаминных и бронхолитических препаратов. Увеличение продолжительности инфузии при последующих циклах терапии оксалиплатином позволяет уменьшить частоту этого синдрома.
Передозировка
В случае передозировки происходит усиление описанных побочных симптомов. Для лечения: необходим тщательный контроль состояния пациента, в том числе гематологических показателей; проводят симптоматическую терапию. Антидот неизвестен.
Противопоказания
Включенные медицинские проблемы/противопоказания отобраны на основе их потенциальной клинической значимости.
Необходимо сопоставлять риск и пользу в следующих случаях:
-
миелосупрессия (число нейтрофилов <2x109/л и/или тромбицитов <100x109/л) до начала лечения;
-
периферическая сенсорная нейропатия с функциональными нарушениями до начала первого цикла лечения;
-
выраженное нарушение функции почек (клиренс креатинина <30 мл/мин);
-
повышенная чувствительность к оксалиплатину или другим составным частям препарата;
Следует также соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Беременность
Первый триместр: желательно избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии, когда это возможно, особенно в течение первого триместра беременности. Хотя информация ограниченна из-за относительно малого числа случаев использования противоопухолевых средств во время беременности, необходимо учитывать возможное мутагенное, тератогенное и канцерогенное действие данных препаратов.
Другие факторы, оказывающие вредное действие на плод, включают неблагоприятные реакции, отмечаемые у взрослых.
Как правило, в период лечения цитотоксическими препаратами рекомендуется применение противозачаточных средств.
Кормление грудью
Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограниченна, во время применения оксалиплатина грудное вскармливание не рекомендуется из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие). Проникает ли оксалиплатин в грудное молоко, неизвестно.
Клинически значимые взаимодействия
Существенного изменения связывания оксалиплатина с белками плазмы крови при одновременном применении с эритромицином, салицилатами, гранисетроном, паклитакселом, натрия вальпроатом не отмечалось.
Препарат не совместим с щелочными растворами или растворами, содержащие хлориды. При взаимодействии с алюминием возможно образование осадка и снижение активности оксалиплатина.
В комбинации с 5-фторурацилом оказывает синергическое цитотоксическое действие.
Резюме и дополнительные сведения
Больные, получающие оксалиплатин, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии рака.
Оксалиплатин рекомендуется вводить путём внутривенной инфузии, обычно в течение 2-6 часов. Введения жидкости до или после применения оксалиплатина, а также форсированного диуреза не требуется.
Дозу необходимо корректировать на основании клинического эффекта и появления или степени тяжести токсического действия с учётом индивидуальных особенностей каждого больного.
Оксалиплатин можно применять в комбинации с другими препаратами в различных схемах. В результате этого возможно изменение частоты и/или тяжести побочных эффектов и использование различных доз (обычно сниженных).
Еженедельно, а также перед каждым введением препарата следует проводить исследование периферической крови, показателей функции печени и почек. Последующие дозы оксалиплатина не рекомендуется вводить до тех пор, пока уровень тромбоцитов не достигнет, по крайней мере - 75x109/л, а нейтрофилов, по крайней мере - 1,5x109/л.
В ходе лечения следует проводить неврологическое обследование. При появлении респираторных симптомов: сухой кашель, диспноэ, хрипы или выявление лёгочной инфильтрации при рентгенологическом исследовании, лечение оксалиплатином следует приостановить для исключения развития интерстициального пневмонита.
Диареей и рвотой могут быть обусловлены такие симптомы как
В случае реакции на оксалиплатин, подобной анафилактической, инфузию следует немедленно прекратить и назначить соответствующую симптоматическую терапию. Дальнейшее лечение оксалиплатином в случае развития аллергических реакций противопоказано.
У больных с развившейся в результате применения оксалиплатина тромбоцитопенией рекомендуется соблюдать особые меры предосторожности. Эти меры могут включать
-
чрезвычайную осторожность при выполнении инвазивных процедур;
-
регулярный осмотр мест внутривенного введения препаратов, кожи и слизистых оболочек для выявления признаков кровотечений или кровоизлияний;
-
ограничение частоты венопункций и отказ от внутримышечных инъекций;
-
анализ мочи, рвотных масс, кала и секретов на скрытую кровь;
-
осторожность при применении зубных щеток, нитей для чистки межзубных промежутков, зубочисток, безопасных бритв и ножниц для стрижки ногтей;
-
профилактику запора и соблюдение осторожности для предотвращения падений или других травм.
Таким больным следует избегать употребления алкоголя и приёма аспирина из-за риска желудочно-кишечных кровотечений. Могут потребоваться переливания тромбоцитов.
Больных с развившейся лейкопенией следует тщательно наблюдать для выявления признаков возникновения инфекции. Может потребоваться использование антибиотиков. У больных с фебрильной нейтропенией парентеральное применение антибиотиков широкого спектра действия необходимо начинать эмпирически, до получения результатов бактериологических исследований и соответствующих диагностических тестов.
У больных старше 65 лет частота периферического нейротоксического действия повышена, а токсическое действие на костный мозг может быть более тяжёлым.
Не растворять и не разбавлять 0,9% раствором натрия хлорида и не смешивать с другими солевыми (щелочными) растворами или растворами, содержащими хлориды.
Раствор оксалиплатина не следует смешивать в одной и той же инфузионой системе с другими препаратами в особенности с 5-фторурацилом и кальция фолинатом. Препарат нельзя вводить неразбавленным.
Код АТХ
L01XA03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Охаliptatin:
Элоксатинà /Еloxatin/(Sanofi-Aventis).
Формы выпуска: лиофилизированый порошок для инъекционных растворов во флаконах по 0,05 и 0,1 г. по одному флакону в картонной коробке.
Хранить при температуре 15-30 °С, если производителем не указано иначе. Защищать от света. Не допускать замораживания.
Несовместимость: не использовать иглы, системы для внутривенного введения или оборудование, содержащие алюминий, так как оксалиплатин несовместим с алюминием.
Антибиотики
Актиномицины
Дактиномицин (Dactinomycin)
Фармакологический/химический класс АТХ
Акриноцинил-ди-(L-треонил-D-валинил-L-пролинилсаркозил-N-метил-L-валинил)-лактон.
Основной компонент смеси актиномицинов, продуцируемой Streptomyces parvullus.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Вследствие высокой токсичности дактиномицин в качестве противомикробного средства не применяется, относится к циклонеспецифичным препаратам. Противоопухолевая активность дактиномицина обусловлена способностью связываться с ДНК (встраивается между парами оснований) и ингибировать ДНК-зависимый синтез РНК.
Оказывает ингибирующее влияние на топоизомеразу II.
Обладает антибактериальным эффектом в отношении грамположительных и грамотрицательных бактерий и противогрибковым действием. Имеет иммунодепрессивную активность.
В исследованиях на самках крыс, кроликов и хомяков установлено эмбриотоксическое действие. В тестах in vitro и in vivo (фибробласты и лейкоциты человека, клетки HELA) проявляет мутагенные свойства, в опытах на мышах и крысах канцерогенное действие.
Фармакокинетика
Не метаболизируется, накапливается в ядерных клетках, не проходит через гематоэнцефалический барьер, проникает через плаценту. В значительной степени связывается с белками тканей. Период полувыведения из плазмы 36 ч. Медленно выводится из организма с жёлчью (30% дозы в течение 1 нед), калом (50% в неизменённом виде) и с мочой (10% в неизменённом виде).
Показания к применению и режим дозирования
Способ применения и дозы
Внутривенно, предварительно развести стерильной водой для инъекций (без консервантов). Для инфузии приготовленный раствор дополнительно разбавить 5% раствором глюкозы или 0,9% раствором натрия хлорида. Максимальная суточная доза для взрослых и детей - 15 мкг/кг или по 400-600 мкг/м2 поверхности тела в течение 5 дней. Альтернативный цикл для детей - общая доза 2,5 мг/м2 за 1 нед. Повторный цикл, как для детей, так и для взрослых может быть проведён не ранее чем через 3 нед (при условии исчезновения всех признаков токсических эффектов).
При опухоли Вильмса используют комбинацию низких доз дактиномицина и лучевой терапии, возможно применение комбинированной терапии с винкристином (в течение 7 циклов, продолжительность поддерживающей терапии 15 мес) вместе с хирургическим лечением и лучевой терапией.
При рабдомиосаркоме рекомендуются следующие комбинации: винкристин и дактиномицин; винкристин, дактиномицин и циклофосфамид (VAC-терапия).
При метастатической хориокарциноме применяют последовательно дактиномицин и метотрексат, при неметастатической - дактиномицин и метотрексат (вместе и раздельно) в сочетании с хирургическим вмешательством или без него.
При метастатической карциноме яичек назначают циклами по 0,5 мг/сут 5 дней подряд каждые 6-8 нед в течение 4 мес и более.
При саркоме Юинга используют последовательное назначение дактиномицина 45 мкг/м2 и циклофосфамида 1200 мг/м2 совместно с лучевой терапией в течение 18 нед.
При гроздевидной саркоме дактиномицин назначают в комбинации с лучевой терапией.
Противопоказания
Гиперчувствительность, угнетение функции костного мозга, ветряная оспа, опоясывающий герпес, нарушения функции печени, возраст до 6-12 мес.
Ограничения к применению: подагра или почечные конкременты в анамнезе (риск гиперурикемии), предшествующая цитотоксическая или лучевая терапия, беременность, кормление грудью.
Беременность и грудное вскармливание
Не рекомендуется применение препарата во время беременности из-за потенциального риска для плода (дактиномицин проникает через плаценту, оказывает мутагенное, тератогенное и канцерогенное действие). На период лечения следует прекратить грудное вскармливание.
Побочные эффекты
Сердечно-сосудистая система и кровь (кроветворение, гемостаз): анемия (вплоть до апластической), лейкопения, тромбоцитопения, панцитопения, агранулоцитоз и ретикулопения, необычные кровотечения или кровоизлияния.
Мочеполовая система: гиперурикемия, нефропатия (связанная с повышенным образованием мочевой кислоты).
Кожные покровы: алопеция (начинается через 7-10 дней после введения), акне, рецидив эритемы или усиление пигментации участков кожи, ранее подвергавшихся облучению.
Аллергические реакции: кожная сыпь, анафилаксия.
Прочие: необычная усталость, лихорадка, миалгии, гипокальциемия, экстравазат, целлюлит, флебит в месте введения, некроз мягких тканей (при попадании под кожу).
Клинически значимые взаимодействия
Другие противоопухолевые препараты и лучевая терапия потенцируют эффект дактиномицина. Может усиливать кардиотоксическое действие доксорубицина, ослаблять эффект витамина К.
Резюме и дополнитедьные сведения
Дактиномицин следует применять под строгим контролем показателей крови. Угнетение функции костного мозга наблюдается примерно через 7-10 дней после начала лечения с наиболее низким уровнем форменных элементов крови через 3 нед. При заметном уменьшении числа тромбоцитов и лейкоцитов лечение прекращают до восстановления функции костного мозга. Следует систематически определять активность печёночных ферментов, уровень билирубина, проводить общий анализ мочи. При расчёте дозы для пациентов, страдающих ожирением или отёками, необходимо учитывать идеальную массу тела. В ходе лечения рекомендуется избегать контакта с инфекционными больными, использовать адекватные меры контрацепции и соблюдать осторожность при использовании зубных щёток, нитей или зубочисток. Появление необычных кровотечений или кровоизлияний, чёрного дегтеобразного кала, крови в моче, кале или точечных красных пятен на коже, а также признаков инфекции требуют немедленной консультации врача. В период лечения не рекомендуется проведение вакцинации вирусными вакцинами (при введении на фоне лечения живых вирусных вакцин возможно усиление процесса репликации вакцинного вируса и усиление его побочных эффектов, инактивированных вакцин - уменьшение выработки противовирусных антител). Тошноту и рвоту, которые развиваются в течение первых часов после введения, можно купировать противорвотными средствами. В случае попадания дактиномицина под кожу или в ткани необходимо прервать инфузию, разъединить систему для внутривенного введения, но оставить канюлю/иглу на месте. После извлечения через канюлю/иглу излившегося препарата, её можно удалить. Конечности следует придать возвышенное положение и наложить холодный компресс на 45 мин. При приготовлении раствора следует избегать вдыхания порошка и паров, контакта с кожей и слизистыми оболочками (особенно глазами). В случае попадания препарата в глаза следует немедленно промыть их большим количеством воды и проконсультироваться с офтальмологом. При попадании на кожу необходимо промыть загрязнённую поверхность большим количеством воды в течение 15 мин. Если препарат вводят непосредственно в вену без инфузионной системы, должна применяться "двухигольная" методика: развести и извлечь расчётную дозу из флакона с помощью одной стерильной иглы, а вводить препарат другой. Следует помнить, что при совместном проведении лучевой терапии увеличивается риск развития токсических реакций со стороны ЖКТ и угнетения костного мозга. С особой осторожностью назначают во время двухмесячной терапии правосторонней опухоли Вильмса, так как при этом отмечается гепатомегалия и повышение активности ACT.
Применение дактиномицина должно проводиться с соблюдением установленных мер предосторожности при приготовлении и разбавлении инъекционных растворов (в стерильном боксе с использованием одноразовых хирургических перчаток и масок), необходимо уничтожение игл, шприцев, флаконов, ампул и остатка неиспользованного препарата. Для профилактики гиперурикемии возможно назначение аллопуринола. Дактиномицин искажает результаты биологических проб, используемых для определения эффективности антибактериальных препаратов.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска - раствор для инъекций (Solutio Dactinomycini pro injectionibus) по 1 мл (в реополиглюкине) с содержанием 0,5 мг препарата.
Условия хранения
В защищённом от света месте при температуре не выше +10 °С.
Митомицин (Mitomycin)
Фармакологический/химический класс АТХ
Противоопухолевый антибиотик, выделенный из Streptomyces caespitosus.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
В качестве противомикробного средства митомицин не применяют из-за токсического действия. Митомицин - циклонеспецифичный препарат, хотя наиболее активен в фазах G и S. После ферментативной активации в тканях действует как бифункциональный или трифункциональный алкилирующий препарат. Митомицин вызывает образование поперечных сшивок между нитями ДНК, ингибирует синтез ДНК, в меньшей степени РНК и белка.
Обладает некоторой иммунодепрессивной активностью.
Фармакокинетика
Не проходит через гематоэнцефалический барьер. Трансформация происходит преимущественно в печени; а также в других тканях, включая почки. Период полувыведения: начальная фаза - 5-15 мин., конечная фаза - 50 мин.
Выводиться почками (10 % в неизменённом виде); небольшие количества выводятся с жёлчью и калом.
Показания к применению и дозирование
Рак желудка, рак поджелудочной железы, рак толстой и прямой кишки, РМЖ, рак головы и шеи, рак жёлчных протоков, рак легкого, РШМ, толстой кишки, некоторые опухоли головы и шеи, РМП, хронический миелолейкоз.
Препарат вводят внутривенно 10-20 мг/м2 1 раз каждые 6-8 нед.
Побочные эффекты
Система кроветворения: лейкопения, тромбоцитопения, возможен гемолитикоуремический синдром
Дыхательная система: пневмопатия.
Мочевыделительная система: нефротоксическое действие.
ЖКТ: стоматит, рвота, тошнота, анорексия.
Аллергические реакции: кожные реакции замедленного типа.
Прочие: ощущение онемения или покалывания в пальцах рук и ног; багровые полосы на ногтях, выпадение волос, тромбофлебит.
Противопоказания
Угнетение функции костного мозга, ветряная оспа, включая недавний контакт с больным, опоясывающий герпес, нарушения свёртывающей системы крови, функции почек; повышенная чувствительность к митомицину.
Следует соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Беременность и грудное вскармливание
Применение препарата в период беременности противопоказано из-за возможного мутагенного, тератогенного и канцерогенного действия. Целесообразна контрацепция.
Грудное вскармливание во время применения митомицина не рекомендуется из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
При применении с препаратами, вызывающими угнетение функции костного мозга возможно аддитивное угнетение функции костного мозга.
При одновременном применении с доксорубицином возможно усиление токсического действия.
Резюме и дополнительные сведения
Больные, получающие митомицин, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии.
Используется ряд схем и режимов применения митомицина в комбинации с другими противоопухолевыми препаратами. Митомицин вводят внутривенно (через внутривенный катетер). Из-за риска сильного изъязвления и некроза в месте внутривенного введения необходимо принимать меры предосторожности для предотвращения образования экстравазата. При возникновении экстравазата, на что указывает ощущение местного жжения или острая боль (эти ощущения могут отсутствовать), введение препарата следует немедленно прекратить, а затем возобновить в другую вену до введения полной дозы. Может потребоваться хирургическое иссечение повреждённого участка.
Вводить митомицин внутримышечно и подкожно нельзя. Для лечения некоторых опухолей митомицин вводится внутриартериально (например, в печёночную артерию).
Код АТХ
L01DC03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Флаконы по 5 мг, 20 мг, 40 мг (кристаллы сине-фиолетового цвета, растворимые в воде).
Упаковка и хранение
Хранить при температуре ниже +4 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Защищать от света.
Флеомицины
Блеомицин (Bleomycin)
Фармакологический/химический класс АТХ
Смесь гликопептидных антибиотиков (А2, В2 и другие фракции), выделенных из штамма Streptomyces verticillus (в виде гидрохлорида или сульфата).
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Подавляет синтез нуклеиновых кислот, преимущественно ДНК, и белка. Взаимодействие с ДНК сопровождается индукцией лабильности её молекулы, разрывом одной или обеих цепочек с последующим образованием свободных радикалов. Фрагментация ДНК - следствие окисления комплекса ДНК-блеомицин-Fe (II) и причина хромосомных аберраций. Активен в отношении клеток, находящихся как в митотическом цикле, так и вне его, проявляет большую активность в фазе G2. Этот эффект дозозависим, наиболее эффективная схема применения - постоянное введение низких доз повторными инъекциями или продолжительными инфузиями. Относительно мало угнетает костномозговое кроветворение, не оказывает существенного иммуносупрессивного влияния. Оказывает токсическое действие на лёгкие (наиболее ранние признаки - уменьшение диффузионной способности, незначительные хрипы, при рентгеноскопии выявляется пневмонит, характеризующийся неспецифическими пятнами затемнений, обычно в нижних полях лёгких, наиболее сильное проявление - фиброз лёгких, вплоть до смертельного исхода). Высоко эффективен на ранних стадиях опухолевого процесса. Метастазы злокачественных опухолей значительно менее чувствительны к действию препарата. Улучшение состояния при лимфогранулематозе и опухолях яичка наступает через 2 нед, плоскоклеточных карциномах через 3 нед. При интраплевральном введении больным со злокачественным плевральным выпотом проявляет склерозирующие свойства, при инстилляции через торакальный зонд в дозах до 100 мл/сут (без предварительного интраплеврального или системного введения, лучевой терапии) вызывает позитивную динамику клеточного состава плеврального выпота, улучшает статус больных. Длительная инстилляция (в течение 30 дней) снижает частоту рецидивов плеврального выпота на 64%.
В высоких дозах у мышей вызывает хромосомные аберрации в клетках костного мозга и сперматогониях.
Фармакокинетика
При парентеральном введении накапливается главным образом в опухолевых клетках кожи и лёгких, в меньшей степени в почках, брюшине, лимфатических узлах, совсем незначительно - в гемопоэтической ткани. Связывание с белками крови очень низкое (1%). Биотрансформация, по данным экспериментов на животных, осуществляется путём расщепления блеомицина ферментами в тканях. Различие в активности тканевых ферментов (высокая в печени, почках, в костном мозге и лимфатических узлах, низкая в коже и лёгких) определяет токсическое действие и противоопухолевый эффект. При клиренсе креатинина более 35 мл/мин период полувыведения из плазмы составляет около 115 мин, менее 35 мл/мин - экспоненциально возрастает в соответствии со снижением клиренса креатинина. У больных с нормальной функцией почек 60-70% дозы выводится с мочой в неизменённом виде. При умеренно выраженной почечной недостаточности почками экскретируется менее 20% дозы.
Показания к применению и режим дозирования
Плоскоклеточный рак кожи, опухоли головы и шеи (включая слизистые оболочки полости рта, надгортанную область, гортань, миндалины, рото- и носоглотку, придаточные пазухи), рак полового члена, вульвы, шейки матки, лёгкого, щитовидной железы, пищевода, герминогенные опухоли яичка и яичника, в т. ч. эмбрионально-клеточная, хорио- и тератокарцинома I и II стадии (преимущественно в комбинации, в том числе с винбластином), злокачественные лимфомы (ходжкинская, неходжкинская), ретикулосаркома, глиома; плевральный выпот, сопровождающий злокачественные опухоли.
Способ применения - внутривенно, внутримышечно, внутриартериально, подкожно, в полость.
Внутривенно медленно в течение 5-10 мин в дозе15-30 мг (в 5-20 мл 0,9% раствора натрия хлорида или 5% раствора глюкозы), что соответствует 15-30 ME, внутримышечно и подкожно - 15-30 мг (в 1-5 мл стерильной воды для инъекций, 0,9% раствора натрия хлорида или 5% раствора глюкозы), внутриартериально - 5-15 мг (в 5-20 мл оптимального растворителя).
Взрослым вводят обычно в дозе 15 мг через день или 30 мг 2 раза в нед. Кумулятивная доза не более 5-6 мг/кг (до 300-400 мг). Повторные циклы проводят с осторожностью, снижая разовую и общую дозу, интервал между курсами 1,5-2 мес. Поддерживающая терапия - 15 мг 1 раз в 7-10 дней. Людям старческого возраста 15 мг 2 раза в нед (на курс не более 200 мг/м2), детям дозу снижают в соответствии с массой тела.
Для внутриплеврального введения 45-60 мг блеомицина разводят в 20 мл 0,9% раствора хлорида натрия, вводят после эвакуации максимально возможного количества плевральной жидкости.
Противопоказания
Гиперчувствительность, лёгочная недостаточность с выраженным нарушением дыхания, фиброз лёгких, тяжёлые заболевания сердечно-сосудистой системы, почечная недостаточность, беременность, грудное вскармливание.
Ограничения к применению: нарушение функции лёгких, печени, выраженное нарушение функции почек, заболевания периферических сосудов, предшествующая химио- или лучевая терапия, детский возраст.
Беременность и грудное вскармливание
Применение препарата противопоказано при беременности. На время лечения следует прекратить грудное вскармливание. Возможно проявление мутагенного и канцерогенного действия (в период беременности также и тератогенного), развитие неблагоприятных эффектов (аналогичных побочным действиям у взрослых) у плода и новорождённого.
Побочные эффекты
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): церебральный артериит, инсульт, инфаркт миокарда, тромботическая микроангиопатия, синдром Рейно, ангиалгия, кровотечение.
Дыхательная система: снижение диффузионной способности лёгких, хрипы, пневмонит, прогрессирующий до лёгочного фиброза, кашель и одышка у 10-40% больных обычно через 4-10 нед после начала лечения и до 1 мес после его прекращения.
ЖКТ: тошнота, рвота, потеря аппетита, диарея, редко гепатотоксическое действие (изменение показателей функциональных проб печени) стоматит, в том числе ангулярный, обусловленный токсическим действием на слизистые оболочки.
Мочеполовая система: нефротоксическое действие (изменение показателей функции почек), олигурия, болезненное мочеиспускание, поллакиурия, вульвит.
Кожные покровы: токсическое действие на кожу (у 25-50% больных развивается обычно через 2-4 нед после начала лечения) и слизистые оболочки, потемнение или утолщение кожи, зуд, кожная сыпь, появление окрашенных шишек на кончиках пальцев, локтевых суставах или ладонях, покраснение и болезненность кожи, покраснение кончиков пальцев, тёмные полосы на коже, опухание пальцев, изменение и ломкость ногтей, обратимое выпадение волос.
Аллергические реакции: зуд, крапивница и другие, вплоть до анафилактического шока, идиосинкразическая реакция (артериальная гипотензия, спутанность сознания, повышенная температура тела, озноб, стерторозное дыхание).
Прочие: снижение массы тела (при длительном применении), повышение температуры тела и озноб (у 20-60% больных, развиваются обычно через 3-6 ч после применения, продолжаются 4-12 ч и возникают менее часто при непрерывном введении), флебит и тромбоз (при превышении скорости в/в введения); при интраплевральном введении - локальная боль, боль в области опухолевых поражений; инфекционные заболевания (при длительном применении), гиперестезия дистальных (ногтевых) фаланг, конъюнктивит.
Клинически значимые заимодействия
Усиливает пневмотоксическое действие общей анестезии (сенсибилизирует ткань лёгких к кислороду). Другие противоопухолевые средства или лучевая терапия усиливают токсическое действие и аддитивно угнетают функцию костного мозга. Цисплатин замедляет клиренс и усиливает токсическое действие (даже при низких дозах). Винкристин усиливает действие (останавливает клеточный цикл в фазе митоза и повышает чувствительность клеток к действию блеомицина).
Резюме и дополнительные сведения
Лечение необходимо проводить под контролем врача, имеющего опыт проведения противоопухолевой терапии. С осторожностью назначают при заболеваниях лёгких, в т.ч. в анамнезе, нарушениях функции печени и почек, сердечно-сосудистых заболеваниях, ветряной оспе (высокий риск летального исхода), больным старше 60 лет (повышен риск токсического действия на лёгкие, вероятны возрастные нарушения функции почек), курящим больным (более вероятно токсическое действие на лёгкие), детям (повышен риск побочного действия и отрицательного действия на функцию половых желез), при хирургических вмешательствах (включая стоматологические). Новорождённым, недоношенным и детям раннего возраста назначение возможно только по жизненным показаниям, под постоянным наблюдением. Большой осторожности требует применение после предшествующего лечения цитотоксическими препаратами и лучевой терапии, особенно в области грудной клетки, головы и шеи. Необходимо соблюдать осторожность при комбинированной терапии (каждый препарат принимают в назначенное время). В период лечения необходимо проведение печёночных и почечных проб. С появлением пневмонии, при возникновении кожных изменений препарат отменяют; повышение температуры тела через 4-5 ч после парентерального введения требует редукции дозы. Женщинам детородного возраста рекомендуется использование контрацептивов. Токсическое действие на лёгкие зависит от возраста пациента и дозы, наиболее часто выявляется у больных старше 70 лет и у больных, получающих дозу выше 400 мг (400 ME). В некоторых случаях токсическое действие на лёгкие отмечалось при дозах 20-60 мг. Пневмотоксичность может быть необратимой. Токсическое действие развивается при более низких дозах у больных, которые получали другие противоопухолевые препараты или лучевую терапию грудной клетки (у облучённых больных летальность может составлять 10%). При введении низких доз возможен также аллергический пневмонит.
Введение блеомицина путём непрерывной внутривенной инфузии в течение 24 ч оказывает менее выраженное токсическое действие на лёгкие, снижает идиосинкразическую реакцию, в отличие от прерывистого введения препарата, хотя токсическое действие на слизистые оболочки и кожу может быть повышено.
Для раннего выявления побочных эффектов в период лечения необходимо: измерение температуры тела каждые 3 ч после введения препарата, осмотр кожи и видимых слизистых оболочек не реже 2 раз в нед, аускультация лёгких, рентгенография лёгких 1 раз в 2 нед, анализ крови и мочи не реже 1 раза в нед, исследование функции лёгких, в т.ч. диффузионной способности лёгких по углерода оксиду при одиночном дыхании и форсированной жизненной ёмкости лёгких. Лечение необходимо прекратить при первых признаках нарушения функции лёгких (форсированная жизненная ёмкость менее 75%). Лечение идиосинкразической реакции симптоматическое (увеличение потребления жидкости, введение сосудосуживающих средств, антигистаминных препаратов и глюкокортикоидов).
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: блеомицетина гидрохлоридª для инъекций (Вleomycetini hydrochloridum pro injectionibus) по 0,005 г в ампулах или флаконах вместимостью 5 мл.
Условия хранения
В защищённом от света месте при температуре не выше +10 °С.
Антрациклины
Доксорубицин (Doxorubicin)
Фармакологический/химический класс АТХ
(SS-цис)-10-[(З-Амто-2,3,6-тридезокси-альфа-L-ликсогексо-пиранозил)окси]-7,8,9,10-тетрагидро-6,8,11-тригидрокси-8-(гидроксиацетил)-1-метокси-5,12-нафтацендион.
Антибиотик антрациклинового ряда, выделенный из культуры Streptomyces peuceticus var. caesius.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Подавляет синтез ДНК и РНК: интеркалирует в двойную спираль ДНК между парами азотистых оснований (нарушается матрица и изменяется пространственная структура) и вызывает расщепление ДНК вследствие образования свободных радикалов. Помимо этого противоопухолевое действие обусловлено изменением клеточных функций в результате связывания с липидами клеточных мембран и взаимодействием с топоизомеразой II. Обладает высокой противоопухолевой и противолейкозной активностью при низкой избирательности действия.
Угнетает кроветворение, оказывает иммуносупрессивное и кардиотоксическое действие. Может вызывать отдаленные эффекты в виде развития вторичных злокачественных опухолей (риск повышается при длительном применении). Оказывает канцерогенное действие у животных и потенциально канцерогенен для человека. Влияет на половую функцию, но у человека это действие слабее, чем действие, выявляемое в опытах на мышах. В экспериментах на животных проявляет эмбриотоксический и тератогенный эффект.
Фармакокинетика
После внутривенного введения быстро распределяется в плазме и тканях, обнаруживаясь в печени, лёгких, сердце и почках через 30 с. Объём распределения (при стабильной концентрации) - более 20-30 л/кг, период полувыведения фазы распределения около 5 мин. Максимальная концентрация в крови уменьшается на 50% в первые 30 мин после инъекции, но значимый уровень сохраняется до 20 ч. Уменьшение концентрации доксорубицина в плазме имеет трёхфазный характер: начальный период полувыведения - 10 мин, второй фазы - 1-3 ч, окончательный около 30-40 ч. Не проникает через гематоэнцефалический барьер и не достигает измеряемых концентраций в ЦНС; может проходить через плаценту у человека. В течение 1 ч биотрансформируется в печени с образованием активного метаболита доксорубицинола. Частичное восстановление ферментами печени сопровождается формированием свободных радикалов, способствующих кардиотоксичности. Экскретируется в неизмененном виде и в виде метаболитов с жёлчью (40-50%) и мочой (5-12%) в течение 5 дней. Период полувыведения фазы выведения - 20-48 ч. Нарушение функции печени приводит к замедлению выведения и кумуляции в плазме и тканях.
Показания к применению и режим дозирования
Острый лимфобластный и миелобластный лейкоз; злокачественная лимфома ходжкинского и неходжкинского типа, РМЖ, РМП, рак лёгкого (особенно мелкоклеточный), щитовидной железы, яичников, остеогенная саркома, саркома мягких тканей, саркома Юинга, нейробластома; опухоль Вильмса.
Способ применения и дозы: внутривенно медленно (в течение не менее 2-5 мин), в 0,9% растворе натрия хлорида или воды для инъекций (концентрация 2 мг/мл), 60-75 мг/м2 1 раз в 3-4 нед или 20-30 мг/м2 в течение 3 дней каждые 3-4 нед, или 30 мг/м2 поверхности тела 1 раз в 1-й, 8-й и 15-й дни курса. Перерыв между циклами - 3-4 нед.
Внутрипузырно - 30-50 мг 1 раз в нед с интервалом от 1 нед до 1 мес.
При комбинированной терапии - 25-50 мг /м2 каждые 3-4 нед.
Кумулятивная доза не должна превышать 500-550 мг/м2.
При числе лейкоцитов менее 3,3-3,5x109/л и тромбоцитов менее 100-149x109/л дозу уменьшают на 50 и 75% соответственно. При уровне билирубина 12-30 мг/мл и выше 30 мг/л дозу уменьшают на 50 и 75% соответственно.
Противопоказания
Гиперчувствительность к гидроксибензоатам, выраженное угнетение функции костного мозга вследствие приёма других химиотерапевтических препаратов или лучевой терапии, предшествующее лечение антрациклинами в предельных суммарных дозах, лейкопения, тромбоцитопения, анемия, тяжёлые нарушения функции печени и почек, острый гепатит, билирубинемия, тяжёлые заболевания сердца (миокардит, выраженные нарушения ритма, острая фаза инфаркта миокарда), язвенная болезнь желудка и двенадцатиперстной кишки, кровотечение, туберкулёз, цистит, беременность, грудное вскармливание.
Ограничения к применению: возраст до 2 лет и после 70 лет (возможно повышение частоты кардиотоксического действия), органические поражения сердца (риск развития кардиотоксического действия при низких дозах).
Беременность и грудное вскармливание
Применение препарата противопоказано при беременности. На время лечения следует прекратить грудное вскармливание.
Побочные действия
Сердечно-сосудистая система и кровь (кроветворение, гемостаз): при общей суммарной дозе более 550 мг/м2 развивается застойная сердечная недостаточность (одышка, отёчность стоп и лодыжек, учащённое или неритмичное сердцебиение), которая в зависимости от дозы или продолжительности лечения может развиться через несколько недель после прекращения терапии (требует немедленного прекращения лечения, так как возможно развитие необратимой и летальной кардиомиопатии), острая предсердная и желудочковая аритмия (преимущественно в первые часы после введения), редко, в течение нескольких дней или недель после введения - токсический миокардит или синдром перикардита-миокардита (тахикардия, сердечная недостаточность, перикардит), тромбоцитопения, лейкопения, достигающая пика через 10-15 дней после начала лечения (картина крови восстанавливается обычно на 21-й день после прекращения введения), флебосклероз (при введении в малые вены или повторном введении в одну и ту же вену), прилив крови к лицу и гиперемия по ходу вены (при слишком быстром введении).
ЖКТ: тошнота, рвота, стоматит или эзофагит (могут возникнуть через 5-10 дней, особенно при введении в течение трёх последовательных дней, и привести к развитию тяжёлых инфекций), изъязвление в ЖКТ, анорексия, диарея.
Мочеполовая система: гиперурикемия, нефропатия (связана с повышенным образованием мочевой кислоты), красноватая окраска мочи (исчезает в течение 48 ч). При внутрипузырном введении - жжение в мочевом пузыре и уретре, расстройство мочеиспускания (болезненность, затрудненность и т.д.), гематурия.
Кожные покровы: алопеция (полная и обратимая), потемнение подошв, ладоней и ногтей, рецидив лучевой эритемы.
Аллергические реакции: кожная сыпь, зуд, повышенная температура тела, озноб, анафилаксия.
Прочие: экстравазат, целлюлит, некроз (при попадании в окружающие ткани), редко конъюнктивит, слезотечение.
Передозировка
Усиление токсических эффектов (воспаление слизистых оболочек, лейкопения, тромбоцитопения).
Лечение - антибиотикотерапия, переливание эритроцитарной массы, симптоматическое лечение.
Клинически значимые взаимодействия
Несовместим с растворами гепарина натрия, дексаметазона, фторурацила, гидрокортизона, натрия сукцината, аминофиллина, цефалотина (возможно образование осадка). Стрептозоцин увеличивает период полувыведения из плазмы доксорубицина. Усиливает токсическое действие других противоопухолевых средств (обострение геморрагического цистита, вызванного циклофосфамидом, повышение гепатотоксического действия 6-меркаптопурина и др.) и лучевой терапии на функцию костного мозга, миокард, слизистые оболочки, кожу и печень. Ослабляет действие инактивированных и живых вирусных вакцин. Может усиливать побочные эффекты живых вирусных вакцин.
Резюме и дополнительные сведения
Во время лечения необходим строгий контроль показателей крови (не реже 1 раза в неделю), деятельности сердца и печени (угнетение костномозгового кроветворения и кардиотоксичность являются дозолимитирующими факторами). Повторный курс можно начинать только после полной ликвидации признаков гематологической токсичности.
С осторожностью применяют у больных с недостаточным резервом костного мозга, обусловленным возрастом, предшествующим применением цитотоксических средств или лучевой терапии.
Стоматологические вмешательства следует по возможности завершить до начала терапии или отложить до нормализации картины крови (возможно повышение риска микробных инфекций, замедление процессов заживления, кровоточивость десен). При малейших признаках попадания под кожу вливание следует немедленно прекратить и выбрать для инъекции другую вену. Не следует применять ранее чем через 1 мес после предшествующей химиотерапии. Повышение концентрации мочевой кислоты в крови и риск развития нефропатии может потребовать корректировки доз урикозурических противоподагрических средств. В процессе лечения необходимо достаточное потребление жидкости с последующим усилением диуреза для обеспечения выведения мочевой кислоты.
Применение должно производиться специально обученным медицинским персоналом с соблюдением установленных мер предосторожности при приготовлении, разбавлении инъекционных растворов (в стерильном боксе с использованием одноразовых хирургических перчаток и масок) и уничтожении игл, шприцев, флаконов, ампул и остатка неиспользованного препарата. Не следует смешивать в одном шприце с другими противоопухолевыми препаратами.
Код АТХ
L01DB01
Торговые наименования, форма выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: 1 флакон с 5 и 25 мл концентрата для приготовления инфузионного раствора содержит доксорубицина гидрохлоридаª 10-50 мг соответственно, в изотоническом растворе натрия хлорида; в коробке 1 флакон.
Условия хранения
Хранить при температуре 2-8 °С.
Пегилированный липосомальный доксорубицин
Фармакологический/химический класс АТХ
(SS-цис)-10-[(З-Амто-2,3,6-тридезокси-альфа-L-ликсогексо-пиранозил)окси]-7,8,9,10-тетрагидро-6,8,11-тригидрокси-8-(гидроксиацетил)-1-метокси-5,12-нафтацендион.
Цитотоксический антрациклиновый антибиотик, выделенный из культуры Streptomyces peuceticus var. caesius.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Точный механизм противоопухолевого действия липосомального доксорубицина не известен. Полагают, что цитотоксический эффект обусловлен его способностью ингибировать синтез ДНК, РНК и белков путём внедрения липосомального доксорубицина между соседними парами оснований двойной спирали ДНК, что препятствует разворачиванию спирали для последующей репликации.
Пегилированная липосомальная форма доксорубицина длительно циркулирует в крови и обеспечивает более высокую концентрацию препарата в опухолевой ткани, чем в нормальных тканях. Липосомы содержат поверхностносвязанные гидрофильные полимеры метоксиполиэтиленгликоля. Линейные группы метоксиполиэтиленгликоля создают выступающую над поверхностью липосом защитную оболочку, что защищает липосомы от распознавания фагоцитарной системой и удлиняет время циркуляции препарата в кровотоке. Пегилированные липосомы содержат матрицу, способную удерживать доксорубицин внутри липосом во время циркуляции в кровотоке. Малый размер пегилированных липосом позволяет им проникать через дефекты кровеносных сосудов опухоли.
Фармакокинетика
При внутривенном введении концентрация пегилированного липосомального доксорубицина существенно выше, чем при введении эквивалентных доз традиционного (непегилированного нелипосомального) доксорубицина. Фармакокинетический профиль доксорубицина указывает на то, что его клиренс из плазмы крови определяется липосомным носителем. Доксорубицин становится доступным только после выхода липосом из сосудистого русла и проникновения их в ткани. В низких дозах (10-20 мг/м2) препарат демонстрирует линейную фармакокинетику, в более высоких дозах (20-60 мг/м2) нелинейную.
При введении препарата в дозе 10-60 мг/м2 клиренс доксорубицина составляет в среднем 0,03 л/ч/м2 (0,008-0,152 л/ч/м2), период полувыведениия 73,9 ч (24-231 ч).
Фармакокинетика в особых клинических случаях
Фармакокинетические показатели при нарушении функции печени и гипербилирубинемии незначительно отличаются от фармакокинетических параметров нормальной концентрации общего билирубина.
Почечная недостаточность (клиренс креатинина 30-156 мл/мин) не оказывает влияния на фармакокинетические параметры. Нет данных по фармакокинетике препарата у пациентов с клиренсом креатинина менее 30 мл/мин.
Возраст пациентов (21-75 лет) не оказывает существенного влияния на фармакокинетические показатели препарата.
Показания к применению и режим дозирования
Метастатический РМЖ при наличии показаний к терапии антрациклинами, даже в случае повышенного риска кардиологических осложнений и при неэффективности терапии таксанами; распространённый рак яичников при неэффективности химиотерапии препаратами платины.
Режим дозирования: препарат вводят внутривенно капельно (после разведения 5% раствором декстрозы) по 50 мг/м2 1 раз в 4 нед.
Препарат нельзя вводить внутривенно струйно или в неразведённом виде.
При расчётной дозе менее 90 мг концентрат разводят в 250 мл 5% раствора декстрозы для инфузий; при дозе 90 мг и более - в 500 мл.
Первое введение осуществляют со скоростью не более 1 мг/мин для того, чтобы снизить риск развития инфузионных реакций. При отсутствии реакций последующие инфузии можно проводить в течение 60 мин.
Введение препарата больным, у которых отмечались инфузионные реакции на предыдущее введение, следует модифицировать следующим образом: 5% расчётной дозы вводят медленно в течение 15 мин. При отсутствии реакций введение продолжают с удвоенной скоростью в течение ещё 15 мин. При хорошей переносимости инфузию продолжают в течение последующего часа (общее время введения 90 мин).
Модификация режима дозирования
Степени токсичности, приведённые в таблицах, основаны на шкале токсичности National Cancer Institute.
Таблица 8-6. Модификация режима дозирования в связи с развитием ладонно-подошвенного синдрома
Степень токсичности после предыдущего введения препарата |
Количество недель, прошедших после предыдущего введения |
||
4 нед |
5 нед |
6 нед |
|
(плановое очередное введение) |
(с учётом задержки в связи с токсичностью) |
||
1 степень (умеренная эритема, отёк или десквамация, не влияющие на повседневную деятельность) |
Вводить следующую дозу, за исключением пациентов, у которых ранее отмечалась III-IV степень токсичности (в этом случае отложить лечение на 1 нед) |
Вводить следующую дозу за исключением пациентов, у которых ранее отмечалась III-IV степень токсичности (в этом случае отложить лечение на 1 нед) |
Уменьшить дозу на 25%; вернуться к 4-недельному интервалу между введениями |
2 степень (эритема, десквамация, отёк, влияющие на повседневную физическую активность, но не ограничивающие её; маленькие волдыри или изъязвления <2 см в диаметре) |
Отложить лечение на 1 нед |
Отложить лечение на 1 нед |
Уменьшить дозу на 25%; вернуться к 4-недельному интервалу между введениями |
3 степень (волдыри, изъязвления, отёки, мешающие ходьбе или повседневной деятельности, пациент не может носить обычную одежду и обувь) |
Отложить лечение на 1 нед |
Отложить лечение на 1 нед |
Отменить препарат |
4 степень (диффузные или локальные процессы, приводящие к инфекционным осложнениям, постельному режиму или госпитализации) |
Отложить лечение на 1 нед |
Отложить лечение на 1 нед |
Отменить препарат |
Таблица 8-7. Модификация режима дозирования в связи с развитием стоматита (модификация рекомендованного 4-недельного курса терапии)
Степень токсичности после предыдущего введения препарата |
Количество недель, прошедших после предыдущего введения |
||
4 нед |
5 нед |
6 нед |
|
(плановое очередное введение) |
(с учетом задержки в связи с токсичностью) |
||
1 степень (безболезненные язвы, эритема или слабо выраженная болезненность) |
Вводить следующую дозу, за исключением пациентов, у которых ранее отмечалась III-IV степень токсичности (в этом случае отложить лечение на 1 нед) |
Вводить следующую дозу за исключением пациентов, у которых ранее отмечалась III-IV степень токсичности (в этом случае отложить лечение на 1 нед) |
Уменьшить дозу на 25%; вернуться к 4-недельному интервалу между введениями или отменить по индивидуальному решению врача |
2 степень (болезненные эритемы, отёки или язвы, но пациент может есть) |
Отложить лечение на 1 нед |
Отложить лечение на 1 нед |
Уменьшить дозу на 25%; вернуться к 4-недельному интервалу между введениями или отменить по индивидуальному решению врача |
3 степень (болезненные эритемы, отёки или язвы, пациент не может есть) |
Отложить лечение на 1 нед |
Отложить лечение на 1 нед |
Отменить препарат |
4 степень (состояние требует парентерального или энтерального питания) |
Отложить лечение на 1 нед |
Отложить лечение на 1 нед |
Отменить препарат |
Таблица 8-8. Модификация режима дозирования в связи с развитием гематологической токсичности
| Нейтрофилы | Тромбоциты | Изменение режима дозирования |
|---|---|---|
I cтепень |
||
1,5-1,9x109/л |
75-150x109/л |
Продолжение терапии без уменьшения дозы |
II cтепень |
||
1,0-1,5x109/л |
50-75x109/л |
При восстановлении числа нейтрофилов до 1,5x109/л и более и тромбоцитов до 75x109/л и более продолжить лечение без уменьшения дозы |
III cтепень |
||
0,5-1,0x109/л |
25-50x109/л |
При восстановлении числа нейтрофилов до 1,5x109/л и более и тромбоцитов до 75x109/л и более продолжить лечение без уменьшения дозы |
IV cтепень |
||
Менее 0,5x109/л |
Менее 25x109/л |
При восстановлении числа нейтрофилов до 1,5x109/л и более и тромбоцитов до 75x109/л и более продолжить лечение, уменьшив дозу на 25%, или продолжить лечение в той же дозе с одновременным добавлением цитокинов |
Пациентам с нарушением функции печени при содержании билирубина в сыворотке крови от 1,2 до 3,0 мг/дл расчётную дозу снижают на 25%. Если содержание билирубина превышает 3 мг/дл, расчётную дозу снижают на 50%. Если пациент хорошо перенёс введение этой дозы (без гипербилирубинемии или повышения активности печёночных ферментов в сыворотке крови), то следующую дозу повышают до предыдущего уровня (т.е. при снижении дозы на 25% её повышают до полной дозы, при снижении дозы на 50% повышают до 75% полной дозы). При хорошей переносимости в последующих циклах дозу можно повысить до полной дозы. Препарат можно назначать пациентам с метастазами в печень с сопутствующей гипербилирубинемией и повышением активности печёночных ферментов, до 4 раз превышающих верхнюю границу нормы. Перед введением препарата следует провести клинико-лабораторное исследование функции печени, включая определение активности АЛТ, АСТ, щелочной фосфатазы, билирубина.
Пациентам с нарушением функции почек коррекции режима дозирования не требуется.
Правила приготовления и введения раствора для инфузий
Нельзя использовать препарат с признаками преципитации или наличием взвешенных частиц.
При использовании препарата необходимо соблюдать правила работы с противоопухолевыми препаратами.
Необходимо применение перчаток. В случае попадания липосомального доксорубицина на кожу или слизистые оболочки следует немедленно промыть этот участок водой с мылом.
Сначала следует определить дозу липосомального доксорубицина необходимую для введения. Требуемый объём препарата набирается в стерильный шприц. Все манипуляции следует проводить со строгим соблюдением правил асептики (препарат не содержит консервантов и бактериостатических добавок).
Рекомендуется вводить препарат через боковой порт инфузионной системы, через которую вводят 5% раствор декстрозы для достижения большего разведения и минимизации риска тромбоза и экстравазации. Инфузию можно проводить в периферическую вену.
Липосомальный доксорубицин нельзя вводить внутримышечно или подкожно.
Побочные эффекты
Побочные эффекты перечислены в соответствии со следующей градацией:
Тяжёлые побочные реакции (серьёзные и жизнеугрожающие) составляют от 0 до 5% от числа нежелательных явлений каждого вида, и лишь в некоторых случаях их частота выше (при лейкопении - 6,8%, стоматите - 7,4%, нейтропении - 8,5%, ладонно-подошвенном синдроме - 19%).
Система кроветворения: лейкопения, нейтропения, тромбоцитопения, анемия. Гематологическая токсичность часто возникает у больных раком яичников. У больных РМЖ часто отмечается анемия, лейкопения, нейтропения, тромбоцитопения.
Сердечно-сосудистая система: нечасто боль в груди, периферические отёки, тахикардия, приливы, кардиотоксическое действие (клинически значимое изменение фракции выброса левого желудочка, в редких случаях ассоциированное с симптомами застойной сердечной недостаточности); редко - понижение АД. Частота и выраженность симптомов кардиотоксичности при терапии липосомальным доксорубицином ниже, чем при терапии в сопоставимых дозах традиционным доксорубицином.
ЖКТ: часто боль в животе, анорексия, запор, диарея, мукозит, стоматит, тошнота, рвота; нечасто дегидратация, сухость во рту, диспепсия, дисфагия, эзофагит, гастрит, гингивит, язвы в полости рта, извращение вкуса; редко метеоризм, боль в полости рта.
Дерматологические реакции: часто ладонно-подошвенный синдром (эритродизестезия), алопеция, кожная сыпь, эритема; нечасто сухость кожи, дерматит, эксфолиативный дерматит, макулопапуллёзная сыпь, везикулобуллёзная сыпь, поражение ногтей, нарушение пигментации кожи, кожные язвы, зуд кожи; редко акне, буллёзная сыпь, чешуйчатость кожи, крапивница.
Нервная система: часто парестезии; нечасто головокружение, сонливость, беспокойство; редко невропатия, депрессия, повышение тонуса гладких мышц.
Костно-мышечная система: нечасто миалгия; редко оссалгия.
Орган зрения: нечасто конъюнктивит; редко слезотечение.
Инфузионные реакции в основном наблюдаются во время первой инфузии: аллергические реакции, анафилактоидные реакции, приступ удушья, отёк лица, повышение или понижение АД, крапивница, боль в спине, боль в грудной клетке, озноб, лихорадка, тахикардия, диспепсия, тошнота, головокружение, затруднение дыхания, фарингит, кожная сыпь, зуд кожи, повышенное потоотделение, а также реакции в месте инъекции и реакции в результате взаимодействия с другими лекарственными средствами. Временная остановка инфузии обычно приводит к купированию этих реакций без дополнительного лечения. При последующих введениях липосомального доксорубицина инфузионные реакции возобновляются редко.
Местные реакции: при попадании препарата под кожу редко развивается некроз окружающих тканей.
Клинически значимые изменения данных лабораторных исследований: нечасто повышение активности ACT, общего билирубина в сыворотке крови, повышение уровня сывороточного креатинина; редко повышение активности АЛТ в сыворотке крови.
Прочие: часто астения, лихорадка, фарингит, повышенная утомляемость, слабость; нечасто аллергические реакции, головная боль, недомогание, снижение массы тела, опоясывающий лишай, кандидоз полости рта, повышенное потоотделение, инфекция мочевыводящих путей; редко анафилактические реакции, кахексия, фолликулит, простой герпес, сепсис, инфекция верхних отделов дыхательных путей, дизурия, вагинит, генитальный кандидоз.
Противопоказания
Возраст до 18 лет, беременность, период лактации, повышенная чувствительность к какому-либо из компонентов препарата.
С осторожностью следует применять препарат при недостаточности кровообращения, предшествующем применении других антрациклинов, совместном назначении с препаратами, обладающими цитотоксическим (особенно миелотоксическим) действием, подагре (в т.ч. в анамнезе), уратном нефроуролитиазе (в том числе в анамнезе), заболеваниях сердца (кардиотоксическое действие может отмечаться при более низких суммарных дозах), печёночной недостаточности.
Угнетение костномозгового кроветворения (в том числе инфильтрация костного мозга опухолевыми клетками, предшествующая химио- или лучевая терапия), паразитарные и инфекционные заболевания вирусной, грибковой или бактериальной природы (в настоящее время или недавно перенесённые) повышают риск развития тяжёлого генерализованного заболевания.
Передозировка
Тяжёлая миелосупрессия (преимущественно лейкопения и тромбоцитопения), токсические эффекты со стороны ЖКТ (мукозит).
Лечение острой передозировки у пациентов с тяжёлой миелосупрессией должно проводиться в стационаре и включать антибиотикотерапию, переливание гранулоцитов и тромбоцитов, симптоматическую терапию мукозита.
Беременность и грудное вскармливание
Препарат противопоказан к применению при беременности и в период грудного вскармливания.
Мужчины и женщины детородного возраста во время лечения, а также в течение 6 мес после его отмены должны использовать надёжные методы контрацепции.
Резюме и дополнительные сведения
Липосомальный доксорубицин должен применяться под наблюдением врача, имеющего опыт проведения цитостатической терапии. Поскольку препарат обладает особенными фармакокинетическими свойствами, не следует проводить чередующиеся циклы терапии липосомальным и традиционным доксорубицином.
Увеличение частоты развития застойной сердечной недостаточности возможно при суммарной дозе доксорубицина, превышающей 450 мг/м2, или в меньшей дозе при наличии факторов риска со стороны сердечно-сосудистой системы (предшествующая лучевая терапия на область средостения или терапия в сочетании с циклофосфамидом).
Всем пациентам, получающим терапию липосомальным доксорубицином, рекомендуется проводить ЭКГ-контроль. Преходящие изменения на ЭКГ, такие как уплощение зубца Т, снижение сегмента ST и клинически малозначимые нарушения ритма не являются обязательными показаниями к отмене препарата. Специфическое проявление кардиотоксического действия -снижение вольтажа комплекса QRS. При возникновении такого изменения, следует рассмотреть возможность проведения биопсии миокарда как наиболее специфического теста для диагностики повреждения сердечной мышцы, вызванного антрациклинами.
Методы измерения фракции выброса левого желудочка такие как ЭхоКГ и более предпочтительное MUGA-сканирование (многовходная артериография), относятся к специфичным методам контроля состояния функции сердца по сравнению с ЭКГ. Именно эти методы следует использовать перед началом и во время проведения терапии липосомальным доксорубицином. Измерение фракции выброса левого желудочка обязательно при каждом последующем введении препарата при суммарной дозе препарата превышающей 450 мг/м2.
При подозрении на кардиомиопатию, т.е. при снижении фракции выброса левого желудочка по сравнению с этим показателем до начала лечения и при прогностически значимом снижении данного показателя (менее 45%) следует провести биопсию миокарда.
Перечисленные методы исследования для выявления возможного отрицательного воздействия терапии антрациклинами на сердечную деятельность рекомендуется применять в следующей последовательности:
Если по результатам обследования можно предположить повреждение миокарда, связанное с терапией липосомальным доксорубицином, следует провести тщательную оценку соотношения предполагаемой пользы от продолжения применения препарата и риска развития кардиотоксичности.
Застойная сердечная недостаточность вследствие кардиомиопатии может развиться неожиданно, без предшествующих изменений на ЭКГ, а также может появиться через несколько недель после прекращения терапии.
Пациентам с кардиологическими заболеваниями, требующими соответствующей терапии, назначение липосомального доксорубицина возможно только в случае, когда польза от применения препарата превышает риск для пациента.
При расчёте кумулятивной дозы липосомального доксорубицина следует принимать в расчёт любое предшествующее или сопутствующее назначение кардиотоксических препаратов (другие антрациклины/антрахиноны или фторурацил).
Во время терапии липосомальным доксорубицином следует регулярно и, как минимум, перед каждым введением препарата контролировать картину периферической крови с обязательным подсчётом числа клеток.
Стойкая выраженная миелосупрессия может привести к развитию суперинфекции или кровотечению.
У пациентов, получавших комбинированную химиотерапию, включающую липосомальный доксорубицин (как и при применении других ДНК-связывающих противоопухолевых препаратов) отмечались случаи развития вторичного острого миелобластного лейкоза и миелодиспластического синдрома, в связи с чем рекомендуется таким пациентам периодически проводить контроль гематологических показателей.
Инфузионные реакции возникают, как правило, во время первой инфузий. Временная остановка инфузий обычно приводит к разрешению симптоматики без дополнительного лечения. Тем не менее, при введении препарата должны быть подготовлены лекарственные средства, предназначенные для купирования инфузионных реакций (эпинефрин, антигистаминные средства, глюкокортикоиды и другие препараты для оказания неотложной медицинской помощи).
При появлении симптомов инфузионной реакции, следует немедленно прекратить инфузию и провести симптоматическую терапию (антигистаминные препараты и глюкокортикоиды короткого действия).
Возобновление инфузий возможно после полного купирования всех симптомов с уменьшением скорости введения препарата. Инфузионные реакции редко повторяются после проведения первого цикла терапии.
Ладонно-подошвенный синдром появляется после 2-3 циклов терапии. У большинства пациентов симптомы проходят через 1-2 нед. Для профилактики и лечения этого синдрома применяют пиридоксин в дозе 50-150 мг/сут. Другие методы лечения и профилактики ладонно-подошвенного синдрома начинают через 4-7 дней после введения препарата.
Для профилактики этого синдрома следует содержать руки и ноги в прохладном состоянии (ванночки для кистей, стоп и ванны для тела с пониженной температурой воды, плавание в прохладной воде); также следует избегать излишнего воздействия тёплой и горячей воды, стараться не носить плотно облегающие носки, перчатки, тесную обувь, чтобы не нарушать кровообращение в ногах и руках. Проявления этого осложнения можно значительно уменьшить за счёт увеличения интервала между введениями на 1-2 нед или за счёт снижения дозы. Однако эти реакции могут быть выраженными и потребовать прекращения терапии.
При появлении симптомов экстравазального попадания препарата (жжение, покраснение) немедленно прекращают инфузию и обкладывают льдом место введения на 30 мин. Введение препарата продолжают в другую вену.
При назначении препарата больным сахарным диабетом следует учитывать, что препарат содержит сахарозу, и что препарат вводят вместе с 5% раствором декстрозы.
Клинически значимые взаимодействия
При совместном применении липосомального доксорубицина с циклофосфамидом или таксанами у больных с солидными опухолями (включая рак яичников и РМЖ) увеличения токсичности не выявлено. Тем не менее, препарат может усиливать токсическое действие других противоопухолевых препаратов.
Гепатотоксичные лекарственные средства, ухудшая функцию печени, могут приводить к повышению токсичности липосомального доксорубицина.
При одновременном приёме с живыми вирусными вакцинами возможна интенсификация процесса репликации вакцинного вируса, усиление его побочных эффектов и снижение выработки антител в организме больного в ответ на введение вакцины, поэтому интервал между прекращением применения препарата и вакцинацией варьируется от 3 мес до 1 года.
Липосомальный доксорубицин нельзя смешивать с другими растворами, кроме 5% раствора декстрозы для инфузии.
Присутствие в инфузионном растворе бактериостатических добавок, таких как бензиловый спирт, может вызвать преципитацию препарата.
Код АТХ
L01DB01
Торговые наименования, форма выпуска и производители
Концентрат для приготовления раствора для внутривенног введения 20 мг/10 мл и 50 мг/25 мл.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре от +2 до +8 °С; не замораживать.
Антрацендионы
Митоксантрон (Mitoxantrone)
Фармакологический/химический класс АТХ
1,4-Дигидрокси-5,8-бис[2-[((2-гидроксиэтил)амино)-этил]-аминo]антрахинон.
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Синтетическое противоопухолевое средство, сходное по химической структуре с противоопухолевыми антрациклиновыми антибиотиками.
Механизм противоопухолевого действия окончательно неяснен. По-видимому, митоксантрон нарушает матричную активность ДНК, образуя с ней комплекс (внедряется между слоями пар оснований ДНК); ингибирует фермент топоизомеразу II. Действие митоксантрона не зависит от фазы клеточного цикла.
Фармакокинетика
Быстро и интенсивно распределяется в организме, наиболее высокие концентрации достигаются в щитовидной железе, печени, сердце и эритроцитах. Связывание с белками плазмы около 78%. Биотрансформируется в печени. Выводится с жёлчью (около 25%) и почками (6-11%, из которых 65% в неизменённом виде). Большая часть дозы активно захватывается и связывается в тканях, откуда постепенно высвобождается. Период полувыведения из плазмы составляет 5,8 дня.
Показания к применению и режим дозирования
РМЖ, неходжкинские лимфомы, острый нелимфобластный лейкоз у взрослых, рак печени.
Режим дозирования: внутривенно капельно в течение 5-30 мин по 12-14 мг/м2 1 раз в 3 нед при солидных опухолях и по 10-12 мг/м2 ежедневно в течение 5 дней каждые 3 нед при остром нелимфобластном лейкозе. Максимальная суммарная доза 200 мг/м2.
При интраплевральной инстилляции рекомендуемая разовая доза составляет 20-30 мг.
Побочные эффекты
Система кроветворения: лейкопения, тромбоцитопения; эритроцитопения.
ЖКТ: тошнота, рвота, диарея, стоматит, боли в животе, запор, анорексия; нарушение функции печени.
Сердечно-сосудистая система: понижение фракции выброса желудочков, хроническая сердечная недостаточность, тахикардия, аритмии.
Прочие: аменорея, алопеция, лихорадка, аллергические реакции, общая слабость, нарушение функции почек.
Местные реакции: флебит, при экстравазации некроз.
Противопоказания
Беременность, повышенная чувствительность к митоксантрону.
Беременность и грудное вскармливание
Митоксантрон противопоказан к применению при беременности. При необходимости применения в период лактации грудное вскармливание следует прекратить.
В период использования митоксантрона и минимум 3 мес после его отмены женщины детородного возраста должны применять надёжные методы контрацепции.
В экспериментальных исследованиях установлено эмбриотоксическое действие митоксантрона.
Резюме и дополнительные сведения
С осторожностью применяют митоксантрон у пациентов с заболеваниями сердца, предшествующим облучением средостения, угнетением кроветворения, выраженными нарушениями функции печени или почек, бронхиальной астмой.
Не рекомендуют применять митоксантрон у пациентов с ветряной оспой (в т.ч. недавно перенесённой или после контакта с заболевшими), опоясывающим герпесом и другими острыми инфекционными заболеваниями.
В процессе лечения необходим систематический контроль картины периферической крови, лабораторных показателей функции печени, а также деятельности сердца (ЭКГ, ЭхоКГ и ангиографическое определение ударного объёма сердца).
Угнетение кроветворения, вызываемое митоксантроном, обычно развивается в течение 10 дней, регенерация - к 21 дню.
Не рекомендуют проводить вакцинацию пациентов и членов их семей.
На фоне применения митоксантрона через 1-2 дня возможно транзиторное зеленоватое окрашивание мочи (и иногда склер).
Клинически значимые взаимодействия
При одновременном применении с противоопухолевыми средствами возможно усиление миелотоксичности, а также кардиотоксичности.
При одновременном применении с цитарабином, цисплатином, циклофосфамидом, фторурацилом, метотрексатом, винкристином, дакарбазином взаимно усиливается действие митоксантрона и указанных противоопухолевых средств.
Код АТХ
L01DB07
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: раствор во флаконах по 10 мг/5 мл; 20 мг/10 мл; 25 мг/12,5 мл; 30 мг/15 мл.
Условия и сроки хранения
Препарат следует хранить в защищённом от света, недоступном для детей месте при температуре от +5 до +25 °С; не замораживать.
Цитостатики растительного происхождения
Алкалоиды барвинка розового
Винбластин (Vinblastine)
Фармакологический/химический класс АТХ
Алкалоид, содержащийся в растении барвинок розовый (Vinca rosea L.), а также в растении катарантус розовый (Catharanthus roseus L.).
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Механизм действия связан с блокадой тубулина и остановкой деления клетки в метафазе.
Фармакокинетика
В незначительной степени проникает через гематоэнцефалический барьер. Связывание с белками плазмы составляет около 75%. Биотрансформируется в печени с образованием активных метаболитов. Выводится преимущественно с желчью, частично почками.
Показания к применению и дозирование
Лимфогранулематоз, неходжкинские лимфомы, герминогенные опухоли яичка и яичников, хорионкарцинома (резистентная к применению других химиотерапевтических препаратов), саркома Капоши, рак почки, РМП, нейробластома, рак носоглотки, рак лёгкого, РМЖ.
Режим дозирования
Начальная доза: внутривенно, 100 мкг/кг 1 раз в неделю с увеличением последующих еженедельных доз на 50 мкг/кг, пока число лейкоцитов не снизится до 3x109/л, либо не будет достигнута максимальная доза 500 мкг/кг.
Поддерживающая доза: внутривенно, в дозе на 50 мкг/кг, 1 раз в 7-14 дней, или 10 мг 1-2 раза в месяц.
У больных при уровне билирубина в сыворотке крови выше 51,3 мкмоль/л необходимо снижение дозы на 50%.
Побочные эффекты
Со стороны ЦНС и периферической нервной системы: невропатия, невриты периферических нервов, головная боль, депрессия, судороги.
Со стороны системы кроветворения: лейкопения, гранулоцитопения, тромбоцитопения, анемия.
Со стороны пищеварительной системы: анорексия, тошнота, рвота, боли в животе, паралитическая непроходимость кишечника, запор, диарея, язвенный стоматит, геморрагический энтероколит.
Со стороны сердечно-сосудистой системы: повышение АД, развитие инфаркта миокарда, нарушения мозгового кровообращения, усиление симптоматики болезни Рейно.
Со стороны дыхательной системы: острая дыхательная недостаточность, бронхоспазм.
Со стороны репродуктивной системы: азооспермия, аменорея.
Прочие: алопеция, боли в костях.
Противопоказания
Выраженная лейкопения, беременность, повышенная чувствительность к винбластину.
Беременность
Винбластин противопоказан к применению при беременности.
При применении у женщин детородного возраста рекомендуют использовать надёжные методы контрацепции.
В экспериментальных исследованиях установлен тератогенный эффект винбластина.
Кормление грудью
Проникает ли препарат в грудное молоко - неизвестно. В случае необходимости применения в период лактации следует прекратить грудное вскармливание.
Резюме и дополнительные сведения
С осторожностью применяют винбластин у пациентов с ветряной оспой (в том числе недавно перенесённой или после контакта с заболевшими), опоясывающим герпесом, другими острыми инфекционными заболеваниями, подагрой, нефролитиазом (в том числе в анамнезе). У пациентов с нарушением функции печени повышен риск возникновения токсических эффектов винбластина.
С осторожностью применяют на фоне лечения препаратами, угнетающими активность изоферментов CYP3A.
Максимальная депрессия кроветворения (в первую очередь снижение количества лейкоцитов в периферической крови) достигается через 510 дней после прекращения применения винбластина. Нормализацию количества лейкоцитов в периферической крови отмечают через 7-14 дней. Развитие тромбоцитопении (менее 200 000/мкл) наиболее вероятно у пациентов, получавших предшествующую противоопухолевую или лучевую терапию. Нормализацию числа тромбоцитов отмечают, как правило, через несколько дней после отмены винбластина.
Риск развития лейкопении при применении винбластина повышен у больных с кахексией и язвенными поражениями кожи, поэтому пациентам с вышеуказанными состояниями его назначать не рекомендуют. У пациентов с метастазами в костный мозг выраженное снижение числа лейкоцитов и тромбоцитов было отмечено после применения винбластина в средних дозах. В этих случаях дальнейшее применение винбластина не показано.
В процессе терапии следует контролировать активность трансаминаз печени и ЛДГ, уровень билирубина и концентрацию мочевой кислоты в плазме крови.
В период лечения не рекомендуют проведение вакцинации пациентов и членов их семей.
При случайном попадании в глаза может возникнуть сильное воспаление.
Клинически значимые взаимодействия
При одновременном применении с ингибиторами активности изоферментов CYP3A возможно более раннее появление и/или усугубление тяжести побочных эффектов винбластина.
При одновременном применении с винбластином возможно снижение концентрации фенитоина в плазме крови и уменьшение его противосудорожной активности, по-видимому, за счёт уменьшения абсорбции, повышения скорости метаболизма и элиминации фенитоина.
При одновременном применении винбластина в высоких дозах с интерфероном альфа возможна тяжёлая миелодепрессия.
Код АТХ
L01CA01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Vinblastine:
Велбеª /Velbeª/ (Франция),
Винбластинª /Vinblastineª/ (Венгрия),
Винбластин-Teeaª /Vinblastine-Tevaª/ (Израиль),
Розевинª /Rosevinª/ (РФ),
Цитобластпин водныйª/Cytoblastine Aqueousª/ (Индия).
Форма выпуска: в лиофилизированном виде (пористая масса белого или белого со слегка желтоватым оттенком цвета) в ампулах и флаконах по 0,005 г (5 мг).
Хранение
В защищённом от света месте при температуре не выше +10 °С.
Винорелбин (Vinorelbine)
Фармакологический/химический класс АТХ
3´,4´-Дидегидро-4´-дезокси-8´-норвинкалейкобластин.
Терапевтический класс АТХ
Противоопухолевый препарат из группы винкаалкалоидов (алкалоид барвинка розового, получаемый полусинтетическим путём).
Механизм действия
Препарат блокирует митоз клеток на стадии метафазы G2-M, вызывая гибель клеток во время интерфазы или при последующем митозе. На молекулярном уровне влияет на динамическое равновесие тубулина в аппарате микротрубочек клетки. Винорелбин подавляет полимеризацию тубулина, связываясь преимущественно с митотическими микротрубочками, а в более высоких концентрациях оказывает также влияние на аксональные микротрубочки.
Фармакокинетика
После приёма внутрь быстро абсорбируется из ЖКТ. Максимальная концентрация винорелбина достигается через 1,5-3 ч. Абсолютная биодоступность в среднем составляет 40%. Приём пищи не влияет на степень всасывания. Связывание с белками плазмы составляет 13,5%. Интенсивно связывается с клетками крови, особенно с тромбоцитами (78%). Хорошо проникает в ткани и задерживается в них длительное время. Высокие концентрации винорелбина определяются в селезёнке, печени, почках, лёгких и вилочковой железе, умеренные - в сердце и мышцах, минимальные - в жировой ткани и костном мозге. Концентрация в лёгких в 300 раз превышает концентрацию в плазме. Не проникает через гематоэнцефалический барьер. Биотрансформируется в печени, главным образом под действием изофермента CYP3A4 с образованием ряда метаболитов; основной, определяемый в крови, - диацетилвинорелбин, который сохраняет противоопухолевую активность. Выводится преимущественно с желчью. Средний период полувыведения составляет 40 ч (27,7-43,6 ч). Фармакокинетические параметры винорелбина (вводимого в дозе 20 мг/м2 еженедельно) не зависят от возраста пациентов и не меняются при умеренной или тяжёлой печёночной недостаточности.
Показания к применению и дозирование
Немелкоклеточный рак лёгкого; РМЖ; РПЖ, резистентный к гормонотерапии (в комбинации с малыми дозами глюкокортикостероидов для приёма внутрь).
Винорелбин применяют как в виде монотерапии, так и в комбинации с другими противоопухолевыми препаратами.
Концентрат винорелбина вводят строго внутривенно в виде 6-10-минутной инфузии.
Капсулы принимают внутрь целиком, запивая водой не разжёвывая и не рассасывая их во рту.
В режиме монотерапии обычная доза препарата для внутривенного введения составляет 25-30 мг/м2 поверхности тела один раз в неделю. Винорелбин разводят в 0,9% растворе натрия хлорида или 5% растворе декстрозы до концентрации 1,0-2,0 мг/мл (в среднем в 50 мл). После введения препарата вену следует промыть, введя дополнительно не менее 250 мл 0.9% раствора натрия хлорида или 5% раствора декстрозы.
Для пациентов с площадью поверхности тела 2 м2 и более разовая доза винорелбина для внутривенного введения не должна превышать 60 мг.
Рекомендуемая разовая начальная доза винорелбина для приёма внутрь составляет 60 мг/м2 поверхности тела один раз в неделю. После третьего приёма дозу рекомендуют увеличить до 80 мг/м2. Увеличение дозы с 60 мг/м2 до 80 мг/м2 может быть осуществлено, если на протяжении трёх недель приёма винорелбина не отмечено нейтропении IV степени (менее 0,5x109/л), или был один эпизод нейтропении III степени (менее 1x109/мкл, но не ниже 0,5x109/л), и количество нейтрофилов перед очередным приёмом не ниже 1,5x109/л.
Если при приёме винорелбина в дозе 80 мг/м2 отмечена нейтропения IV степени (менее 0,5x109/л) или 2 случая нейтропении III степени (менее 1,0x109/л, но более 0,5x109/л), в последующие 3 приёма необходимо снизить дозу винорелбина с 80 до 60 мг/м2 в неделю.
Если число нейтрофилов не снижалось менее 0,5x109/л, или не наблюдали более одного снижения числа нейтрофилов в диапазоне от 0,5x109/л до 1,0x109/л в течение трёх недель приём винорелбина в дозе 60 мг/м2, можно снова увеличить дозу препарата с 60 до 80 мг/м2 в неделю.
Для пациентов с площадью поверхности тела 2 м2 и более общая разовая доза винорелбина для приёма внутрь не должна превышать 120 мг в неделю при назначении препарата в дозе 60 мг/м2 и 160 мг в неделю при дозе 80 мг/м2.
Применение винорелбина внутрь в дозах 60 мг/м2 и 80 мг/м2 соответствует внутривенному введению препарата в дозах 25 мг/м2 и 30 мг/м2 соответственно.
При ПХТ доза и частота введения винорелбина (как при в/в введении, так и при приёме внутрь) зависят от схемы химиотерапии.
При снижении числа нейтрофилов менее 1,5x109л или тромбоцитов менее 75x109/л (при в/в введении) или менее 100x109/л (при приёме внутрь) очередное введение или приём внутрь винорелбина откладывают на 1 неделю. Если из-за гематологической токсичности пришлось воздержаться от трёх еженедельных введений или приёмов препарата, применение винорелбина рекомендуют прекратить.
Пациентам с тяжёлой печеночной недостаточностью винорелбин следует назначать с осторожностью, в дозе, сниженной на 30%.
Безопасность и эффективность применения винорелбина у детей не изучена.
Специальной коррекции режима дозирования винорелбина у лиц пожилого возраста не требуется.
Побочные эффекты
Использовали следующие критерии оценки частоты встречаемости нежелательных явлений: понятие "очень часто" употребляли в случае, если нежелательные явления отмечаются более, чем у 10% пациентов; понятие "часто" - у 1-10%; понятие "иногда" - у 0,1-1,0%; понятие "редко" - у 0,01-0,10% пациентов; "крайне редко" - менее чем у 0,01%.
Со стороны системы кроветворения: очень часто - нейтропения, анемия, тромбоцитопения, присоединение вторичных инфекций на фоне угнетения костномозгового кроветворения; часто - лихорадка (38 °С) на фоне нейтропении; иногда - сепсис, септицемия; крайне редко - осложнённая септицемия, в некоторых случаях приводящая к летальному исходу. Наименьшее число нейтрофилов наблюдается на 7-10 день от начала терапии, восстановление происходит в последующие 5-7 дней. Кумулирования гематотоксичности не отмечено.
Со стороны иммунной системы: редко - анафилактический шок или ангионевротический отёк.
Со стороны периферической нервной системы: очень часто - парестезии, гиперестезии, снижение или выпадение глубоких сухожильных рефлексов; часто - слабость в ногах; иногда - тяжёлые парестезии с сенсорными и моторными симптомами, как правило, обратимого характера.
Со стороны сердечно-сосудистой системы: иногда - повышение или снижение АД, приливы жара и похолодание конечностей; редко - ИБС (стенокардия, инфаркт миокарда), выраженная гипотония, коллапс; крайне редко - тахикардия, сердцебиение и нарушение сердечного ритма.
Со стороны дыхательной системы: иногда - одышка, бронхоспазм; редко - интерстициальная пневмония (при комбинированной терапии с митомицином), острый респираторный дистресс-синдром.
Со стороны пищеварительной системы: очень часто - тошнота, рвота, стоматит, запор, диарея, преходящее повышение функциональных проб печени (АЛТ, ACT); редко - панкреатит, повышение уровня билирубина, парез кишечника.
Дерматологические реакции: часто - алопеция; редко - кожные высыпания.
Местные реакции: часто - боль/жжение или покраснение в месте инъекции, изменение окраски вены, флебит; при экстравазации - целлюлит; возможно - некроз окружающих тканей.
Прочие: часто - повышенная утомляемость, миалгии, артралгии, лихорадка, боли различной локализации, включая боль в грудной клетке, боль в нижней челюсти и в области опухолевых образований; редко - гипонатриемия; очень редко - геморрагический цистит и синдром неадекватной секреции АДГ.
Передозировка
Симптомы: подавление функции костного мозга, нейротоксические реакции.
Лечение: при необходимости проводят симптоматическую терапию, переливание крови, антибиотики широкого спектра действия. Специфического антидота нет.
Противопоказания
Количество нейтрофилов менее 1,5x109/л; количество тромбоцитов менее 75x109/л (для в/в введения) и менее100x109/л (для приёма внутрь).
Инфекционные заболевания во время начала терапии или перенесённые в течение последних двух недель.
Выраженная недостаточность функции печени, не связанная с опухолевым процессом.
Потребность в постоянной оксигенотерапии у пациентов с опухолью лёгкого.
Заболевания и состояния, приводящие к снижению всасывания из ЖКТ (для приёма внутрь).
Беременность и грудное вскармливание.
Повышенная чувствительность к препарату и к другим винкаалкалоидам.
С осторожностью назначают при дыхательной недостаточности, угнетении костномозгового кроветворения (в том числе после предыдущей химио- или лучевой терапии), запорах или явлениях кишечной непроходимости в анамнезе, нейропатии в анамнезе.
Беременность
Винорелбин противопоказан к применению при беременности.
Кормление грудью
При необходимости применения препарата в период лактации следует решить вопрос о прекращении грудного вскармливания.
Резюме и дополнительные сведения
При выраженном нарушении функции печени дозу винорелбина следует снизить на 30%.
При нарушении функции почек необходимо контролировать состояние больного.
При появлении признаков нейротоксичности 2 степени и более применение винорелбина следует прекратить.
При появлении одышки, кашля или гипоксии неясной этиологии следует обследовать больного для исключения лёгочной токсичности.
При экстравазации инфузию препарата следует немедленно прекратить, оставшуюся дозу вводят в другую вену.
В случае появления тошноты или рвоты после приёма капсул винорелбина повторно ту же дозу принимать не следует.
Во время и в течение, по крайней мере, трёх месяцев после прекращения терапии, необходимо использовать надёжные методы контрацепции.
При попадании действующего вещества в ротовую полость рекомендуют прополоскать рот водой или любым солевым раствором.
При попадании винорелбина в глаза их следует обильно и тщательно промыть водой.
Поскольку в состав препарата входит сорбитол, его не следует использовать у больных с наследственной непереносимостью фруктозы.
Контроль лабораторных показателей
Лечение препаратом проводят под строгим гематологическим контролем, определяя число лейкоцитов, гранулоцитов и уровень гемоглобина перед каждым очередным применением. При снижении числа нейтрофилов менее 1,5x109/л и/или тромбоцитов менее 75x109/мкл (для в/в введения) или менее 100x109/мкл (для приёма внутрь) применение очередной дозы препарата откладывают до нормализации показателей, одновременно осуществляют контроль состояния больного.
Клинически значимые взаимодействия
При совместном применении с другими цитостатиками возможно взаимное усугубление побочных эффектов, в первую очередь миелосупрессии.
При совместном применении с митомицином С возможно развитие острой дыхательной недостаточности.
При применении совместно с паклитакселом повышается риск нейротоксичности.
Применение на фоне лучевой терапии приводит к радиосенсибилизации. Применение винорелбина после лучевой терапии может привести к повторному появлению лучевых реакций.
Одновременное применение препарата с индукторами и ингибиторами изоферментов цитохрома P 450 может привести к изменению фармакокинетики винорелбина.
Код АТХ
L01CA04
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Vinorelbine:
Навельбинª /Navelbineª/ (Франция)
Форма выпуска: 1% раствор во флаконах по 1 и 5 мл.
Условия и сроки хранения
Концентрат для приготовления раствора для инфузий следует хранить в защищённом от света и недоступном для детей месте при температуре 2-8 °С. Капсулы следует хранить в недоступном для детей месте при температуре 2-8 °С.
После дополнительного разведения концентрата его физическая и химическая стабильность сохраняется в течение восьми дней при комнатной температуре (20°±5 °С) или в холодильнике (при температуре 2-8 °С).
Винкристин (Vincristine)
Фармакологический/химический класс АТХ
Алкалоид, содержащийся в растении барвинок розовый (Vinca rosea L.).
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Блокирует митоз путём остановки клеток в метафазе и, кроме того, может нарушать метаболизм аминокислот; винкристин - циклоспецифичный препарат в отношении клеток, находящихся в фазе М.
Фармакокинетика
Проникает через гематоэнцефалический барьер в незначительных количествах. Связывается с белками плазмы - около 75%. Биотрансформируется в печени. Выводится преимущественно в виде метаболитов, с желчью (около 67%) и почками (около 12%).
Показания к применению и режим дозирования
Острый лейкоз, лимфогранулематоз, неходжкинские лимфомы, миеломная болезнь, саркома Юинга, саркома мягких тканей, остеогенная саркома, нейробластома, саркома Капоши, саркома матки, РМЖ, мелкоклеточный рак лёгких, меланома, эпителиома, рак почечной лоханки и мочеточников, РМП, опухоль Вильмса, РШМ, герминогенная опухоль яичка и яичников, хорионкарцинома матки, эпендимома, менингиома, плеврит опухолевой этиологии, злокачественные опухоли половых органов у девочек.
Режим дозирования: устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии.
Препарат вводят внутривенно в дозе 1,4 мг/м2 (не более 2 мг) в неделю.
У больных при уровне билирубина в сыворотке крови выше 51,3 мкмоль/л рекомендуют снижение дозы на 50%.
Побочные эффеты
Со стороны системы кроветворения: лейкопения, анемия, тромбоцитопения.
Со стороны ЦНС и периферической нервной системы: нейропатия, невриты периферических нервов, головная боль, судороги, атаксия, депрессия, диплопия, птоз, галлюцинации, нарушения сна.
Со стороны мочевыделительной системы: полиурия, дизурия, атония мочевого пузыря, отёки, острая мочекислая нефропатия.
Со стороны пищеварительной системы: рвота, диарея, стоматит, запор, анорексия, паралитический илеус (особенно часто у детей).
Прочие: алопеция (проходящая после окончания лечения), артериальная гипотензия, отёки.
Передозировка
Симптомы: подавление функции костного мозга, нейротоксические реакции.
Лечение: специфического антидота нет; при необходимости проводят симптоматическую терапию:
Противопоказания
Заболевания центральной и периферической нервной системы, выраженная лейкопения, беременность.
Беременность и лактация
Винкристин противопоказан к применению при беременности. При необходимости применения в период лактации следует прекратить грудное вскармливание.
Женщины детородного возраста, получающие винкристин, должны применять надёжные методы контрацепции.
В экспериментальных исследованиях установлено тератогенное и эмбриотоксическое действие винкристина.
Резюме и дополнительные сведения
Не рекомендуют применять винкристин у пациентов с ветряной оспой (в том числе недавно перенесённой или после контакта с больными), с опоясывающим герпесом, другими острыми инфекционными заболеваниями.
Следует соблюдать осторожность при применении винкристина при подагре (в том числе в анамнезе) и нефролитиазе, а также у пациентов, ранее получавших цитотоксическую или лучевую терапию.
Частота побочных эффектов винкристина связана с суммарной дозой и длительностью терапии.
При одновременном проведении лучевой терапии на область спинного мозга возможно усиление нейротоксического действия винкристина.
Риск возникновения нейротоксических эффектов выше у пациентов пожилого возраста и лиц с неврологическими заболеваниями в анамнезе. При развитии периферических невритов следует прекратить введение винкристина.
В процессе лечения необходимо контролировать показатели периферической крови, активность печёночных трансаминаз и ЛДГ, концентрации мочевой кислоты и билирубина в плазме крови.
В период лечения не рекомендуют проведение вакцинации пациентов и членов их семей.
С осторожностью назначают препарат при одновременном применении лекарственных средств, ингибирующих изоферменты CYP3A.
В экспериментальных исследованиях установлено канцерогенное и мутагенное действие винкристина.
Клинически значимые взаимодействия
При одновременном применении винкристин усиливает нейротоксические эффекты других препаратов.
При одновременном применении винкристин ослабляет действие противоподагрических препаратов. При одновременном применении с урикозурическими средствами повышается риск развития нефропатии.
Введение винкристина до применения блеомицина повышает противоопухолевый эффект терапии.
Одновременное применение с митомицином С может вызывать угнетение дыхания, бронхоспазм, особенно у предрасположенных пациентов.
При одновременном применении винкристина и итраконазола возможно более раннее и более тяжёлое развитие нейротоксического эффекта.
Код АТХ
L01CA02
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Vincristine:
Винкристинª /Vincristineª/ (Венгрия, Франция),
Винкристин ликвид-Рихтерª/Vincristine liquid-Richterª/ (Венгрия),
Винкристин-Теваª /Vincristine-Tevaª/ (Израиль),
Винкристина сульфатª /Vincristine Sulfateª/ (Австрия, США),
Онковинª /Oncovinª/ (Франция),
Цитокристинª /Cytocristinª/ (Индия),
Цитомидª /Citomidª/ (Мексика).
Форма выпуска: во флаконах, содержащих по 0,5 мг лиофилизированного винкристина сульфата, с приложением растворителя в ампулах по 10 мл.
Подофиллотоксины
Этопозид (Etoposide)
Фармакологический/химический класс АТХ
4'-Деметилпиподофиллотоксин 9-[4,6-O-R)-этилиден]-b-D-гликопиранозид.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Полусинтетическое производное подофиллотоксина. Механизм действия связан с ингибированием топоизомеразы II. Угнетает митоз, блокирует клетки в S-G2-интерфазе клеточного цикла, в более высоких дозах действует в G2-фазе. Цитотоксическое действие в отношении нормальных здоровых клеток наблюдается только при применении этопозида в высоких дозах.
Фармакокинетика
При приёме внутрь этопозид всасывается из ЖКТ. Биодоступность в среднем составляет 50%. Распределение в спинномозговой жидкости низкое и вариабельное; концентрация в нормальной лёгочной ткани выше, чем при наличии метастазов в лёгких; определяется близкий уровень концентраций в тканях первичных опухолей и в нормальных тканях миометрия.
Отмечена прямая корреляция между коэффициентом связывания этопозида и уровнем альбумина в плазме крови здоровых людей и пациентов с раковыми заболеваниями. Метаболизируется в печени.
Конечный период полувыведения в среднем составляет 7 ч. Выводится почками (44-60%), с фекалиями (до 16%), с желчью (6% и менее).
Показания к применению и режим дозирования
Герминогенные опухоли (опухоли яичка, хориокарцинома), рак яичников, мелкоклеточный и немелкоклеточный рак лёгкого, лимфогранулематоз, неходжкинские лимфомы, рак желудка (для монотерапии и в составе комбинированной терапии), саркома Юинга, саркома Капоши, нейробластома, РМЖ, острый нелимфобластный лейкоз, мезотелиома.
Режим дозирования: устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии.
Вводят внутривенно капельно по 50-100 мг/м2 поверхности кожи с 1-го по 5-й день лечения; повторные курсы проводят с интервалами 3 нед.
Рекомендуют сочетание этопозида с цисплатином, доксорубицином (адриамициномª), циклофосфамидом (циклофосфаномª).
Побочные эффекты
Со стороны системы кроветворения: лейкопения, анемия; реже - тромбоцитопения.
Со стороны пищеварительной системы: тошнота, рвота; редко - анорексия, мукозиты, диарея; при применении в высоких дозах - токсические реакции со стороны печени.
Со стороны ЦНС и периферической нервной системы: сонливость, повышенная утомляемость; поражение периферической нервной системы.
Со стороны обмена веществ: гиперурикемия; при применении высоких доз - метаболический ацидоз.
Со стороны сердечно-сосудистой системы: тахикардия, артериальная гипотензия.
Со стороны репродуктивной системы: азооспермия, аменорея.
Аллергические реакции: озноб, лихорадка, бронхоспазм.
Дерматологические реакции: алопеция.
Противопоказания
Выраженная миелодепрессия, выраженные нарушения функции печени и почек, беременность, детский возраст до 2 лет, повышенная чувствительность к подофиллину или его производным.
Беременность и кормление грудью
Этопозид противопоказан при беременности. При необходимости применения в период лактации следует прекратить грудное вскармливание.
Во время лечения и в течение 3 мес после его окончания пациенткам детородного возраста необходимо применять эффективные методы контрацепции.
В экспериментальных исследованиях установлено, что этопозид оказывает тератогенное и эмбриотоксическое действие.
Резюме и дополнительные сведения
С осторожностью применяют у пациентов с предшествующей лучевой или химиотерапией, с ветряной оспой, опоясывающим герпесом, при инфекционных поражениях слизистых оболочек, при нарушениях сердечного ритма, при повышенном риске развития инфаркта миокарда, нарушении функции печени, заболеваниях нервной системы (эпилепсия), хроническом алкоголизме, у детей старше 2 лет.
При нарушении функции почек дозу уменьшают в соответствии со значениями клиренса креатинина.
Перед началом и на фоне проводимой терапии следует контролировать картину периферической крови.
Не рекомендуют проводить вакцинацию пациентов и членов их семей.
В экспериментальных исследованиях установлено, что этопозид оказывает мутагенное действие.
Влияние на способность к вождению автотранспорта и управлению механизмами.
Во время лечения следует воздерживаться от занятий, требующих повышенного внимания и быстрых психомоторных реакций.
Клинически значимые взаимодействия
При одновременном применении с другими препаратами, вызывающими миелодепрессию возможно аддитивное угнетение функции костного мозга.
При одновременном применении с цисплатином возможно уменьшение клиренса этопозида и увеличение его токсичности.
Циклоспорин в высоких дозах может уменьшать клиренс этопозида и увеличивать продолжительность его действия, при этом возможно усиление лейкопении.
Код АТХ
L01CB01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Etoposide:
Вепезидª /Vepesidª/ (Германия, Италия, США),
Ластетª /Lastetª/ (Япония),
Фитозидª /Fytosidª/ (Индия),
Этозидª /Etosidª/ (Индия),
Этопозидª /Etoposideª/ (Израиль, Франция),
Этопозид-Эбевеª /Etoposide-Ebeweª/ (Австрия),
Этопосª /Etoposª/ (Мексика).
Раствор для инфузий концентрированный по 50 мг/2,5 мл, 100 мг/5 мл, 200 мг/10 мл, 400 мг/20 мл во флаконе.
Капсулы по 50 мг и 100 мг.
Упаковка и хранение
Хранить при температуре 2-8 °С, в плотно закрытой упаковке, если производителем не указано иначе.
Терпеноиды тисового дерева
Доцетаксел (Docetaxel)
Фармакологический/химический класс АТХ
Сложное органическое соединение (C43H53NO14), имеющее элементы структурного сходства с паклитакселом. Оба соединения - производные бензолпропаноевой кислоты и содержат в молекуле группу фенилизосерина.
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Противоопухолевый цитостатический препарат растительного происхождения из группы таксанов. Активное вещество препарата - доцетаксел - накапливает тубулин в микротрубочках, препятствует их распаду, что приводит к нарушению фазы митоза и межфазных процессов в опухолевых клетках. Доцетаксел долго сохраняется в клетках, где достигаются его высокие концентрации. Доцетаксел активен в отношении некоторых (но не всех) клеток, продуцирующих в избыточном количестве P-гликопротеин, который кодируется геном множественной лекарственной резистентности.
In vivo доцетаксел имеет широкий спектр активности в отношении опухолей мышей и перевиваемых опухолевых клеток человека.
Фармакокинетика
Фармакокинетика доцетаксела дозозависима. После однократного внутривенного введения препарата в дозе 100 мг/м2 средняя максимальная концентрация в плазме равна 3,7 мкг/мл. Связывание с белками плазмы составляет более 95%.
Доцетаксел метаболизируется в нижних отделах ЖКТ.
В течение 7 дней доцетаксел выводится с мочой и калом после окисления тертбутиловой эфирной группы с участием цитохрома Р450. Выведение с мочой составляет 6% радиоактивной дозы, с калом - 75%. Примерно 80% радиоактивного препарата, выводимого с калом, обнаруживают в течение 48 ч в виде основного неактивного метаболита и трёх менее значимых неактивных метаболитов и, в очень незначительном количестве, в неизменённом виде.
Фармакокинетика доцетаксела не зависит от возраста и пола пациента.
Клиренс доцетаксела не меняется у больных с лёгкой или умеренной задержкой жидкости (данных о клиренсе препарата у пациентов с выраженной задержкой жидкости нет).
Показания к применению и дозирование
РМЖ как препарат 1-й линии химиотерапевтического лечения; или в качестве терапии 2-й линии в монорежиме, при неэффективности предшествующего лечения, включавшего в себя антрациклины или алкилирующие средства; метастатический РМЖ с опухолевой экспрессией HER2 в комбинации с трастузумабом, в случае отсутствия предшествующей химиотерапии.
Неоперабельный, местно-распространённый или метастатический немелкоклеточный рак лёгкого (в комбинации с цисплатином или карбоплатином) в качестве терапии 1-й линии или в монотерапии в качестве терапии 2-й линии при неэффективности химиотерапии, основанной на препаратах платины.
Метастатический рак яичников при неэффективности предшествующей терапии 1-й линии (терапия 2-й линии).
Метастатический плоскоклеточный рак головы и шеи при неэффективности предшествующей терапии (терапия 2-ой линии).
Метастатический, гормонорезистентный РПЖ (в комбинации с преднизолоном).
Для предупреждения реакций повышенной чувствительности, а также с целью уменьшения задержки жидкости всем больным до введения доцетаксела необходимо проводить премедикацию кортикостероидами, например дексаметазоном в дозе 16 мг/сут (по 8 мг 2 раза/сут) внутрь, в течение трёх дней, начиная за один день до введения препарата.
У больных РПЖ, получающих сопутствующее лечение преднизолоном, проводят премедикацию дексаметазоном в дозе 8 мг за 12, 3 и 1 ч до начала введения доцетаксела.
Доцетаксел вводят в виде одночасовой внутривенной инфузии каждые три недели.
РМЖ. При адъювантной терапии больных с операбельной формой РМЖ рекомендуемая доза доцетаксела составляет 75 мг/м2 через 1 час после введения доксорубицина (50 мг/м2) и циклофосфамида (500 мг/м2) каждые три недели. Всего 6 циклов терапии.
При монотерапии доцетаксел вводят в дозе 100 мг/м2 каждые 3 недели. При комбинации с доксорубицином (50 мг/м2) или капецитабином (1250 мг/м2 внутрь 2 раза/сут в течение 2 недель с последующим недельным перерывом) доцетаксел вводят в дозе 75 мг/м2 каждые три недели.
При комбинации с трастузумабом рекомендованная доза доцетаксела составляет 100 мг/м2 каждые три недели.
При немелкоклеточном раке лёгкого доцетаксел вводят в дозе 100 мг/м2 при монотерапии и 75 мг/м2 в комбинации с препаратами платины каждые три недели.
При метастатическом раке яичников и плоскоклеточном раке тканей головы и шеи доцетаксел вводят в дозе 100 мг/м2 каждые три недели.
При метастатическом гормонорезистентном РПЖ доцетаксел вводят в дозе 75 мг/м2 1 раз в три недели. Преднизолон назначают внутрь по 5 мг 2 раза/сут длительно на весь период курсового лечения.
Доцетаксел вводят при количестве нейтрофилов ³1,5x109/л. При падении числа нейтрофилов <0,5x109/л, которое наблюдали более недели, или развитии фебрильной нейтропении, или развитии выраженных кожных реакций, или выраженной периферической нейропатии во время терапии доцетакселом дозу этого препарата для следующих введений следует снизить со 100 до 75 мг/м2 и/или с 75 до 60 мг/м2. Если подобные осложнения возникают и при применении доцетаксела в дозе 60 мг/м2, лечение следует прекратить.
Пациентки с операбельной формой РМЖ, получающие адъювантную терапию, при развитии фебрильной нейтропении должны получать гранулоцитарный колониестимулирующий фактор (Г-КСФ) на всех последующих циклах. При сохранении фебрильной нейтропении необходимо уменьшить дозу доцетаксела до 60 мг/м2 и продолжить приём Г-КСФ. Если Г-КСФ не используют, то дозу доцетаксела нужно снизить с 75 до 60 мг/м2. У пациентов со стоматитом 3 или 4 степени необходимо снижение дозы до 60 мг/м2.
При первом появлении токсичности 2 степени, которая сохраняется до времени проведения очередного цикла лечения, лечения может быть отложено до снижения токсичности до 0-1 степени, при этом во время следующего цикла лечения вводят 100% первоначальной дозы доцетаксела.
У пациентов с повторным развитием токсичности 2 степени или первым эпизодом токсичности 3 степени в любое время цикла терапии, лечение откладывают до снижения токсичности до 0-1 степени, затем применение доцетаксела возобновляют в дозе 55 мг/м2.
При любых последующих проявлениях токсичности или появлении любых видов токсичности 4 степени введение доцетаксела должно быть прекращено.
При комбинированной терапии немелкоклеточного рака лёгкого для пациентов, которые первоначально получают доцетаксел в дозе 75 мг/м2 в комбинации с цисплатином, у которых количество тромбоцитов в предыдущем цикле лечения снижалось до <2,5x109/л, или у пациентов, у которых развилась фебрильная нейтропения, или у пациентов с серьёзными проявлениями негематологической токсичности дозу доцетаксела в следующем цикле необходимо снизить до 65 мг/м2.
Для пациентов с нарушениями функции печени при уровне АЛТ или АСТ, превышающем более чем в 1,5 раза ВГН, или уровне ЩФ, превышающем более чем в 2,5 раза ВГН, рекомендуемая доза составляет 75 мг/м2. У больных с повышенным уровнем билирубина и/или повышенной активностью АЛТ и АСТ (>3,5 ВГН) в сочетании с повышением уровня ЩФ (>6 ВГН) применять доцетаксел не следует.
В настоящее время отсутствуют данные относительно применения доцетаксела в комбинации с другими лекарственными препаратами у больных с нарушениями функции печени.
Безопасность и эффективность доцетаксела у детей изучена недостаточно.
С учётом анализа фармакокинетических данных какие-либо специальные инструкции по применению доцетаксела у пожилых пациентов отсутствуют. При комбинации с капецитабином у пациентов старше 60 лет рекомендуется снижение стартовой дозы капецитабина.
Побочное действие
Со стороны системы кроветворения: наиболее часто - обратимая нейтропения (у пациентов не получивших Г-КСФ), в ряде случаев развитие фебрильной нейтропении. Число нейтрофилов снижается до минимальных значений в среднем через 7 дней (у пациентов, получавших ранее химиотерапию, этот период может быть короче), средняя длительность выраженной нейтропении (<0,5x109/л) также составляет 7 дней. Возможно развитие тромбоцитопении и анемии. Редко возникают кровотечения, в основном обусловленные тромбоцитопенией.
Аллергические реакции: умеренно выраженные реакции повышенной чувствительности обычно возникают в течение нескольких минут после начала инфузии (приливы, сыпь, зуд, чувство стеснения в груди, боль в спине, одышка, лекарственная лихорадка, озноб). Крайне редко - синдром Лайелла, синдром Стивенса-Джонсона. Возможно развитие тяжёлых реакций (артериальная гипотензия, бронхоспазм, генерализованная сыпь и эритема), которые исчезали после прекращения инфузии и назначения адекватной терапии.
Дерматологические реакции: алопеция, лёгкие и умеренно выраженные кожные реакции. Редко встречались выраженные реакции: сыпь, сопровождающаяся зудом, или ограниченная эритема кожи ладоней и стоп с отёком и последующей десквамацией (в некоторых случаях может потребоваться прерывание или прекращение терапии) (реже - отёк рук, лица и груди), гипо- или гиперпигментация ногтей, онихолизис.
Задержка жидкости: описаны случаи развития периферических отёков, плеврального или перикардиального выпота, асцита, увеличения массы тела. Периферические отёки обычно появляются на нижних конечностях, а затем могут стать генерализованными. Частота и выраженность задержки жидкости увеличиваются при повторном введении препарата. Однако в некоторых случаях отёки возникали во время первых курсов терапии. Задержка жидкости не сопровождалась острыми эпизодами олигурии или артериальной гипотензии. В редких случаях сообщали о развитии дегидратации и отёка лёгких.
Со стороны пищеварительной системы: тошнота, рвота, диарея, анорексия, запор, стоматит, нарушение вкуса, эзофагит, боли в эпигастрии; колит, включая ишемический, энтероколит, перфорация желудка или кишечника; редко - желудочно-кишечные кровотечения, кишечная непроходимость. У больных, получающих монотерапию доцетакселом в дозе 100 мг/м2, повышение сывороточной активности ACT, AJIT, ЩФ и концентрации билирубина в сыворотке крови более, чем в 2,5 раза превышающее ВГН, отмечается менее, чем в 5% случаев. Крайне редко отмечали случаи развития гепатита (летальный исход был у пациентов с заболеваниями печени в анамнезе).
Со стороны периферической нервной системы: периферическая нейропатия в виде легко или умеренно выраженных парестезии, гиперестезии, дизестезии или боли, включая жжение. Двигательные нарушения характеризуются слабостью. В случае возникновения этих симптомов необходима коррекция дозы. Если симптомы сохраняются, то лечение следует прекратить. Очень редко отмечают развитие судорог и преходящей потери сознания.
Со стороны органа зрения: редко - развитие слезотечения в сочетании с конъюнктивитом (или без него), преходящие визуальные расстройства (вспышки света в глазах, появление скотом), обычно возникающие во время введения препарата и сочетающиеся с развитием реакций гиперчувствительности, которые обычно исчезают после прекращения инфузии; очень редко, главным образом у пациентов, получающих одновременно другие противоопухолевые препараты, возможно развитие окклюзии слезного канала, приводящей к чрезмерному слезотечению.
Со стороны сердечно-сосудистой системы: нарушения сердечного ритма (синусовая тахикардия, мерцательная аритмия), нестабильная стенокардия, сердечная недостаточность, артериальная гипо- или гипертензия. Редко отмечали случаи венозной тромбоэмболии и инфаркта миокарда.
Со стороны дыхательной системы: очень редко - острый респираторный дистресс-синдром и интерстициальная пневмония, лёгочный фиброз и усиление реакции на облучение.
Со стороны костно-мышечной системы: артралгия, миалгия, мышечная слабость.
Местные реакции: умеренно-выраженные - гиперпигментация, воспаление, покраснение, сухость кожи, флебит, кровоизлияние, отёк вен.
Прочие: астения, одышка, генерализованные или локальные боли, включая боли в грудной клетке, не связанные с заболеваниями сердца или лёгких.
При применении доцетаксела в комбинации с капецитабином наблюдали более частое развитие нежелательных явлений со стороны пищеварительной системы, ладонно-подошвенного синдрома (гиперемия кожи конечностей / ладоней и стоп / с последующим отёком и десквамацией), дегидратации, слезотечения, артралгии, тяжёлые тромбоцитопении и анемии, гипербилирубинемии, но более редкое развитие тяжёлой нейтропении, алопеции, нарушений со стороны ногтей, астении, миалгии, отёков нижних конечностей.
У пациентов в возрасте старше 60 лет, получавших комбинированную терапию доцетакселом и капецитабином, по сравнению с пациентами более молодого возраста отмечается более частое развитие токсичности 3-4 степени.
У больных получавших комбинированной лечение доцетакселом и трастузумабом была выявлена большая частота побочных явлений и более частое развитие токсичности 4 степени, по сравнению с монотерапией доцетакселом. Были выявлены случаи развития сердечной недостаточности, особенно при дополнении терапии антрациклинами (доксорубицина или эпирубицина).
Противопоказания
Реакции повышенной чувствительности на доцетаксел или другие компоненты препарата в анамнезе; выраженные нарушения функции печени; исходное число нейтрофилов <1,5x109/л; беременность; грудное вскармливание.
Беременность
Доцетаксел противопоказан к применению при беременности.
Пациенты детородного возраста должны избегать зачатия во время применения препарата и как минимум в течение трёх месяцев после его отмены.
Кормление грудью
Доцетаксел противопоказан к применению в период лактации (грудного вскармливания).
Резюме и дополнительные сведения
Лечение доцетакселом проводят только при участии опытного специалиста по противоопухолевой химиотерапии в условиях специализированного стационара или отделения.
При развитии выраженной нейтропении (<5x109/л в течение 7 дней и более) во время курса терапии доцетакселом рекомендуют снизить дозу препарата при последующих курсах или использовать адекватные симптоматические меры.
С целью выявления реакций повышенной чувствительности больных следует тщательно наблюдать, особенно во время первой и второй инфузий. Развитие реакций повышенной чувствительности возможно на первых минутах инфузии доцетаксела. Лёгкие проявления гиперчувствительности (покраснение лица, локализованные кожные реакции) не требуют прерывания терапии. Однако тяжёлые реакции повышенной чувствительности (артериальная гипотензия, бронхоспазм, генерализованная сыпь, эритема) требуют немедленного прекращения введения препарата и проведения соответствующих лечебных мероприятий. Повторное назначение доцетаксела не разрешается.
У больных, получающих монотерапию доцетакселом в дозе 100 мг/м2 и имеющих высокую активность АЛТ и/или АСТ, более чем в 1,5 раза превышающих ВГН, в сочетании с повышенным уровнем ЩФ более чем в 2,5 раза выше ВГН, крайне высок риск развития тяжёлых побочных эффектов: сепсис, желудочно-кишечные кровотечения, фебрильная нейтропения, инфекции, тромбоцитопения, стоматит, астения. В связи с этим у таких больных с повышенными показателями функции печени рекомендуемая доза доцетаксела составляет 75 мг/м2; функциональные пробы печени нужно определять до начала проведения терапии и перед каждым последующим циклом терапии доцетакселом. У больных с повышенным уровнем билирубина и/или повышенной активностью АЛТ и АСТ (>3,5 ВГН) в сочетании с повышением уровня ЩФ (>6 ВГН) доцетаксел назначать не рекомендуют. В настоящий момент отсутствуют данные относительно применения доцетаксела в комбинации с другими препаратами у больных с нарушениями функции печени.
В связи с возможностью развития отёчного синдрома необходимо наблюдать за пациентами с асцитом, выпотом в плевральную полость или перикард. При появлении отёков показано ограничение соли и питьевого режима и назначение диуретиков.
Необходим систематический контроль картины периферической крови с целью своевременного выявления миелотоксичности.
Безопасность и эффективность применения доцетаксела у детей изучены недостаточно. Имеется ограниченный опыт применения доцетаксела у детей.
Передозировка
Симптомы: подавление функции костного мозга, периферическая невропатия, стоматит.
Лечение: специфического антидота нет. Назначают Г-КСФ. При необходимости проводят симптоматическую терапию.
Клинически значимые взаимодействия
Исследования in vitro показали, что биотрансформация препарата может измениться при одновременном применении веществ, индуцирующих, ингибирующих или метаболизирующихся изоферментом CYP3A (циклоспорин, кетоконазол, эритромицин). В связи с этим необходимо соблюдать осторожность при одновременном назначении с подобными препаратами, учитывая возможность взаимодействия.
In vitro лекарственные средства, характеризующиеся высоким связыванием с белками (такие как эритромицин, дифенгидрамин, пропранолол, пропафенон, фенитоин, сульфаметоксазол), не влияли на связывание доцетаксела с белками.
Дексаметазон не влияет на степень связывания доцетаксела с белками плазмы.
Доцетаксел не влияет на связывание дигитоксина с белками плазмы.
При использовании доцетаксела в комбинации с доксорубицином клиренс доцетаксела увеличивается при сохранении его эффективности. При этом клиренс доксорубицина и уровень доксорубицинола (метаболита доксорубицина) в плазме не меняется.
Клиренс карбоплатина при комбинированной терапии с доцетакселом увеличивается на 50% по сравнению с монотерапией карбоплатином.
Не выявлено влияния доцетаксела на фармакокинетику (Cmax, AUC) главного метаболита капецитабина (5DFUR) и влияния капецитабина на фармакокинетику (Cmax, AUC) доцетаксела.
Код ATX
L01CD02
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Taxotere®:
Docetaxelª (Aventis Pharma)
Концентрат для инфузий во флаконах, содержащего 20 мг/0,5 мл и 80 мг/2 мл доцетаксела в комплекте с растворителем.
Условия и сроки хранения
Препарат следует хранить при температуре 2-25 °С, в защищённом от света месте. Предварительно смешанный раствор доцетаксела рекомендуют использовать сразу после приготовления. Раствор для инфузии следует использовать в течение 4 ч (включая часовую инфузию) при комнатной температуре и в обычных условиях освещённости.
Паклитаксел (Paclitaxel)
Фармакологический/химический класс АТХ
Вещество природного происхождения (C47H51NO14) - дитерпеноид со сложным "таксановым" трициклическим ядром.
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Связан с влиянием на процесс деления клетки. Паклитаксел относят к классу препаратов, действующих на микротрубочки, стимулирует сборку микротрубочек из димеров тубулина и стабилизирует микротрубочки за счёт подавления деполимеризации, что приводит к подавлению нормального процесса динамической реорганизации сети микротрубочек, который важен для клеточных функций на этапе митоза и интерфазы клеточного цикла. Кроме того, паклитаксел индуцирует образование аномальных скоплений или "связок" микротрубочек на протяжении клеточного цикла и вызывает образование множественных звёзд микротрубочек во время митоза.
Другие эффекты
Паклитаксел усиливает цитотоксические эффекты ионизирующей радиации in vitro.
Молекулярная масса - 853,9.
Фармакокинетика
После внутривенного введения концентрация паклитаксела в плазме крови уменьшается в соответствии с двухфазной кинетикой. Фармакокинетику паклитаксела изучали после в/в введения препарата в дозах 135 мг/м2 и 175 мг/м2 в течение 3 и 24 ч. При проведении инфузии более 3 ч фармакокинетика паклитаксела с повышением дозы приобретает нелинейный характер. При увеличении дозы препарата на 30% (от 135 мг/м2 до 175 мг/м2) значения Cmax и AUC увеличивались на 75% и 81% соответственно.
При повторных курсах терапии не было получено указаний на кумуляцию паклитаксела.
Связывание с белками очень высокое и составляет 89-98%.
Метаболизм паклитаксела у человека не исследован до конца. Паклитаксел метаболизируется при участии изоферментов CYP2C8 и CYP3A4.
Биотрансформация, вероятно, происходит в печени с образованием гидроксилированных метаболитов.
Выведение: процессы выведения полностью не изучены; период полувыведения паклитаксела составляет 3,0-52,7 ч, а средние значения общего клиренса - от 11,6 до 24 л/(час´м2); общий клиренс несколько уменьшается при более высоких концентрациях паклитаксела в плазме. Выводится преимущественно с желчью. Средние значения общего выведения неизменённого паклитаксела с мочой варьируют от 1,3 до 12,6% введённой дозы, что указывает на интенсивный внепочечный клиренс. Уменьшение концентрации в плазме крови двухфазное; начальное быстрое снижение отражает распределение препарата в периферических отделах и его значительное выведение. Более поздняя фаза частично обусловлена относительно медленным высвобождением препарата из периферических отделов.
Изменение метаболизма паклитаксела при нарушениях функции почек или печени при трёхчасовой инфузии формально не исследовали. Фармакокинетические параметры, полученные у одного больного, при трёхчасовом введении препарата таксолª (паклитаксел) в дозе 135 мг/м2 во время диализа, были в пределах интервала, определённого для больных, не находящихся на диализе.
Показания к применению и дозирование
Рак яичников: терапия 1-й линии в комбинации с карбоплатином у больных с распространённым метастатическим процессом или остаточной опухолью (более 1 см) после проведения хирургического лечения; терапия 2-й линии у больных с распространённым метастатическим раком яичников после стандартной терапии, не приведшей к положительному результату.
РМЖ: адъювантная терапия у больных с наличием метастазов в лимфатических узлах после проведения стандартного комбинированного лечения; терапия 1-й линии метастатического рака и при прогрессировании заболевания после адъювантной терапии с применением препаратов антрациклинового ряда; терапия 2-й линии при прогрессировании заболевания после комбинированной химиотерапии с применением противоопухолевых антибиотиков антрациклинового ряда.
Немелкоклеточный рак лёгкого: в качестве терапии 1-й линии в комбинации с карбоплатином или для монотерапии немелкоклеточного рака лёгкого у больных, которым не планируют хирургическое лечение и/или лучевую терапию с возможностью излечения.
Саркома Капоши: в качестве терапии 2-й линии саркомы Капоши, развившейся у больных СПИДом.
Для предупреждения тяжёлых реакций повышенной чувствительности всем больным до введения препарата паклитаксел следует провести премедикацию. Премедикация может включать дексаметазон (или его эквивалент) в дозе 20 мг внутрь приблизительно за 12 ч и 6 ч до введения препарата паклитаксел, дифенгидрамин (или эквивалент) в дозе 50 мг в/в за 30-60 мин, циметидин в дозе 300 мг в/в или ранитидин в дозе 50 мг в/в за 30-60 мин до введения препарата паклитаксел.
Рак яичников: больным, которым ранее не проводили химиотерапию (1-я линия), рекомендуемая доза препарата паклитаксел составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч или 135 мг/м2 в виде в/в инфузии в течение 24 ч с последующим введением карбоплатина (АUС5); интервал между циклами лечения должен составлять 3 нед; больным, которым ранее проводили химиотерапию (2-я линия), рекомендуемая доза препарата паклитаксел составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые три недели.
РМЖ: адъювантное лечение РМЖ проводят после стандартной комбинированной терапии. Рекомендуемая доза препарата паклитаксел составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч. Проводят 4 цикла с интервалом 3 нед; при терапии 1-й линии метастатического рака и при прогрессировании заболевания после адъювантной терапии рекомендуемая доза препарата паклитаксел составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 нед; при терапии 2-й линии для лечения больных с метастатическим заболеванием молочной железы после комбинированной химиотерапии, не давшей положительного результата, паклитаксел следует вводить в дозе 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 нед.
Немелкоклеточный рак лёгких: в режиме комбинированной терапии рекомендуемая доза препарата таксолª составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч с последующим введением карбоплатина (AUC5) каждые 3 нед; в режиме монотерапии рекомендуемая доза препарата паклитаксела составляет 175 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 нед.
У больных с солидными опухолями введение препарата не следует повторять если содержание нейтрофилов составляет менее 1,5x109/л, а содержание тромбоцитов менее 100x109/л. Больным с нейтропенией IV степени: содержание нейтрофилов менее 0,5x109/л в течение 7 дней или более длительного времени или с тяжёлой формой периферической нейропатии в ходе последующих курсов дозу следует снизить на 20%.
Если паклитаксел применяют в комбинации с карбоплатином, сначала следует вводить паклитаксел, а затем карбоплатин.
Саркома Капоши у больных СПИДом: при терапии 2-й линии рекомендуемая доза препарата таксолª составляет 135 мг/м2 в виде в/в инфузии в течение 3 ч каждые 3 нед или 100 мг/м2 в/в капельно в течение 3 ч каждые 2 нед. В зависимости от иммуносупрессии, наблюдаемой у больных с развивающейся формой СПИДа, рекомендуется: уменьшить дозу дексаметазона для приёма внутрь (одного из трёх компонентов премедикации) до 10 мг; вводить паклитаксел только при содержании нейтрофилов не менее 1,0x109/л; больным с тяжёлой нейтропенией: менее 0,5x109/л в течение недели или более, при последующих циклах необходимо уменьшить дозу препарата паклитаксел на 20%; по клиническим показаниям одновременно применять гемопоэтический фактор роста (G-CSF).
Побочное эффекты
Примечание: нейтропения - основной эффект, ограничивающий дозу.
Следующие побочные/неблагоприятные эффекты отобраны на основе их потенциальной клинической значимости.
Встречаются более часто: анемия: обычно бессимптомная; реакция гиперчувствительности: прилив крови к лицу, кожная сыпь или зуд, одышка; редко: сильная одышка, выраженная кожная реакция; лейкопения или нейтропения; тромбоцитопения: обычно бессимптомная; артралгии или миалгии: боль в суставах или мышцах, особенно рук или ног; диарея; тошнота и рвота; периферическая нейропатия с лёгкой парестезией: ощущение онемения, жжения или покалывания в кистях или стопах; выпадение волос.
Примечание: частота и тяжесть анемии, по-видимому, повышаются с увеличением длительности лечения паклитакселом.
При правильной премедикации реакции гиперчувствительности обычно выражены слабо: прилив крови к лицу, кожная сыпь, одышка. Однако даже при условии премедикации могут возникать тяжёлые реакции: гипотензия, требующая лечения, одышка, требующая назначения бронхорасширяющих средств, отёк Квинке или генерализованная крапивница, боль в грудной клетке, в этих случаях необходимы немедленное прекращение применения паклитаксела и активное симптоматическое лечение. Тяжёлые симптомы обычно возникают в первые 10 мин инфузии паклитаксела, после введения первой или второй дозы. Как правило, больным, у которых развивалась тяжёлая реакция гиперчувствительности, повторно вводить паклитаксел не рекомендуют.
Тяжёлая нейтропения: число нейтрофилов меньше 0,5x109/л распространённая, но лишь в редких случаях сохраняется более 7 дней. Наиболее низкий уровень нейтрофилов обычно отмечают примерно на 11-й день лечения паклитакселом; как правило, нейтропения быстро проходит с восстановлением числа нейтрофилов к 15-21-му дню. Как кумулятивная реакция нейтропения не зарегистрирована. Наиболее распространённые инфекции, связанные с нейтропенией, - инфекции мочевых путей, органов дыхания.
При развитии тромбоцитопении наиболее низкий уровень тромбоцитов обычно отмечают примерно на 8-9-й день лечения паклитакселом.
Примечание: артралгия или миалгия обычно начинается через 2-3 дня после лечения и проходит в течение 5 дней. Боль обычно купируется аналгезирующими средствами, но иногда может быть достаточно сильной и требовать применения наркотических анальгетиков.
Частота и тяжесть периферической нейропатии дозозависимы; при обычных дозах сенсорная невропатия отмечается в области кистей и стоп. Отмена паклитаксела необходима только в редких случаях. Симптомы обычно появляются после многократного применения препарата и ослабевают или проходят в течение нескольких месяцев после прекращения использования паклитаксела. Высокие дозы (выше 250 мг/м2) могут вызывать ограничивающие дозу двигательные и вегетативные нарушения, особенно у больных с ранее перенесённой невропатией, они начинаются через 24-72 ч после лечения.
Примечание: полное выпадение волос, включая волосы на коже черепа, брови, ресницы и лобковые волосы, отмечается почти у всех больных между 14-м и 21-м днём, обратимо после окончания терапии.
Встречаются менее часто: действие на сердечно-сосудистую систему, включая брадикардию, гипотензию или изменения ЭКГ: обычно бессимптомные; повышенная активность печёночных ферментов в сыворотке крови: бессимптомная.
Примечание: действие на сердечно-сосудистую систему включало также тяжёлую предсердно-желудочковую блокаду, иногда приводящую к блокаде III степени, требующей применения электрокардиостимулятора. Отмечали атипичные боли в грудной клетке и инфаркт миокарда, а также преходящую желудочковую тахикардию, хотя точная связь с применением паклитаксела не установлена.
Встречаются редко: образование экстравазата с флебитом или целлюлитом: боль и покраснение в месте введения; стоматит.
Передозировка
Симптомы: угнетение функции костного мозга, периферическая невропатия, мукозиты.
Лечение: проводят симптоматическую терапию. Специфический антидот паклитаксела неизвестен.
Противопоказания
Включенные медицинские проблемы/противопоказания отобраны на основе их потенциальной клинической значимости.
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу: угнетение функции костного мозга: будет усиливаться; при исходном числе нейтрофилов меньше 1,5x109/л применять паклитаксел не рекомендуется, а последующие дозы нельзя вводить до тех пор, пока число нейтрофилов не восстановится до уровня выше 1,5x109/л и число тромбоцитов до уровня выше 100x109/л или до исходных величин.
Нарушения сердечной деятельности, включая: стенокардию, нарушения проводимости сердца, застойную сердечную недостаточность в анамнезе или инфаркт миокарда в последние 6 мес: способность больного переносить побочные сердечно-сосудистые эффекты паклитаксела может быть снижена.
Ветряная оспа, включая недавний контакт с больным или опоясывающий герпес: риск тяжёлого генерализованного заболевания. Другие инфекции.
Повышенная чувствительность к паклитакселу и другим компонентам препарата (особенно к полиоксиэтилированному касторовому маслу).
Следует также соблюдать осторожность у больных, ранее получавших цитотоксические препараты или лучевую терапию.
Беременность; грудное вскармливание.
Беременность
Адекватных и строго контролируемых исследований у женщин не проведено. Первый триместр: обычно рекомендуется избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии, когда это возможно, особенно в течение первого триместра беременности. Хотя информация ограничена из-за относительно малого числа случаев использования противоопухолевых средств во время беременности, необходимо учитывать возможное мутагенное, тератогенное и канцерогенное действие данных препаратов. Другие факторы, оказывающие вредное действие на плод, включают неблагоприятные реакции, отмечаемые у взрослых.
Как правило, в период лечения цитотоксическими препаратами рекомендуется применение противозачаточных средств.
При внутривенном введении самкам кроликов в дозе 3 мг/кг (33 мг/м2) во время органогенеза паклитаксел оказывал токсическое действие на самок и эмбрион или плод. У крыс и кроликов паклитаксел вызывал выкидыши, снижал число жёлтых тел, частоту имплантации и число живых плодов, повышал частоту резорбции плода и гибели эмбрионов или плодов. Значительных внешних изменений, изменений мягких тканей или скелета не выявлено.
Кормление грудью
Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограничена, во время проведения химиотерапии грудное вскармливание не рекомендуется из-за возможного риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие). Проникает ли паклитаксел в грудное молоко - неизвестно.
Резюме и дополнительные сведения
Больные, получающие паклитаксел, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии.
Рекомендуется, чтобы больные, получающие паклитаксел, находились под наблюдением непрерывно в течение, по крайней мере, первых 30 мин инфузии и через частые интервалы времени после неё. Необходимо, чтобы во время каждого введения паклитаксела были наготове оборудование и препараты, включая адреналинª (эпинефрин) и кислород, требующиеся для устранения возможной анафилактической реакции.
До введения путём внутривенной инфузии концентрат паклитаксела для приготовления раствора для инъекций необходимо разбавить.
Паклитаксел следует вводить через систему со встроенным мембранным фильтром с размером пор не более 0,22 мкм. Приготовленные растворы стабильны в течение не более 27 ч (включая время подготовки и вливания) при комнатной температуре (приблизительно 25 °С) и при комнатном освещении. Приготовленные растворы могут опалесцировать из-за присутствующей в составе лекарственной формы основы-носителя, причём после фильтрования опалесценция раствора сохраняется. Разбавленные растворы не следует хранить в холодильнике.
С целью профилактики тяжёлых реакций гиперчувствительности у всех больных рекомендуют проводить премедикацию кортикостероидами (например, дексаметазоном), дифенгидрамином (димедролª) и блокаторами Н2-рецепторов (такими как циметидин или ранитидин).
При слабовыраженных реакциях гиперчувствительности: прилив крови к лицу, кожные реакции, одышка, гипотензия, тахикардия прекращать терапию паклитакселом необязательно. Однако при сильных реакциях: гипотензия, требующая лечения, одышка, требующая применения бронхорасширяющих средств, отёк Квинке или генерализованная крапивница необходимы немедленная отмена паклитаксела и активная симптоматическая терапия. Как правило, больным, у которых была тяжёлая реакция гиперчувствительности к паклитакселу, препарат не следует вводить повторно. Однако у больных с объективно подтверждённой реакцией опухоли и без альтернатив лечению паклитакселом опытный врач может попытаться провести повторное лечение с соблюдением чрезвычайных мер осторожности и энергичной премедикацией.
При возникновении тяжёлой периферической нейропатии последующую дозу паклитаксела необходимо снизить на 20%.
На фоне применения паклитаксела показан регулярный контроль АД, ЧСС и частоты дыхания (особенно на протяжении первого часа инфузии). При появлении тяжёлых нарушений АВ-проводимости в ходе лечения препаратом паклитаксел необходимо назначить соответствующее лечение, а при последующем введении препарата следует проводить непрерывный мониторинг функции сердца.
Если во время курса лечения паклитакселом развивается тяжёлая нейтропения: число нейтрофилов меньше 0,5x109/л в течение 7 дней или более продолжительного времени, дозу паклитаксела для следующих курсов неоходимо снизить на 20%.
Больных с развившейся лейкопенией следует наблюдать для выявления признаков возникновения инфекции. У больных с фебрильной нейтропенией парентеральное применение антибиотиков широкого спектра действия необходимо начинать эмпирически, до получения результатов бактериологических исследований и соответствующих диагностических тестов.
У больных с развившейся в результате применения паклитаксела тромбоцитопенией нужно соблюдать особые меры предосторожности.
Исследований паклитаксела на канцерогенность не проведено, возможными отдалёнными эффектами многих противоопухолевых препаратов могут быть вторичные злокачественные опухоли, хотя неясно, связано ли их развитие с мутагенным или иммунодепрессивным действием этих средств. Влияние дозы и продолжительности лечения также неизвестно, но, вероятно, риск повышается при длительном применении. Информация о зависимости эффекта паклитаксела от возраста у детей отсутствует, хотя сообщали о фазе I клинических испытаний в этой группе. Безопасность и эффективность не определены.
В одном ретроспективном исследовании, в котором изучали зависимость эффекта паклитаксела от возраста у пожилых людей, отличий оказываемого действия при использованной дозе не обнаружено.
Контроль лабораторных показателей: в ходе лечения препаратом необходимо регулярно определять содержание форменных элементов крови через короткие промежутки времени.
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны на основе их потенциальной клинической значимости.
Примечание: комбинации, содержащие любое из перечисленных веществ, в зависимости от имеющегося количества, могут также взаимодействовать с данным препаратом.
Препараты, вызывающие патологические изменения крови: лейкопеническое и/или тромбоцитопеническое действие паклитаксела может усиливаться при одновременном или недавно проведённом лечении, если эти препараты дают такой же эффект; корректировку дозы паклитаксела при необходимости следует проводить на основании результатов анализа крови.
Другие препараты, вызывающие угнетение функции костного мозга, или лучевая терапия: возможно аддитивное угнетение функции костного мозга; при одновременном или последовательном применении нескольких препаратов, вызывающих угнетение костного мозга, а также лучевой терапии может потребоваться снижение дозы, тяжесть вызываемой паклитакселом нейтропении может быть связана со степенью миелотоксического действия предшествовавшей терапии. В фазе I одного клинического испытания обнаружено, что применение цисплатина до паклитаксела чаще, чем использование цисплатина после паклитаксела, снижало клиренс последнего примерно на 25%, что привело к более выраженной миелосупрессии.
Премедикация циметидином не влияет на клиренс паклитаксела.
Метаболизм паклитаксела in vitro подавляется кетоконазолом, верапамилом, диазепамом, хинидином, дексаметазоном, циклоспорином, тенипозидом, этопозидом, винкристином. Однако использованные в экспериментальных исследованиях концентрации превышали обнаруживаемые in vivo после введения препарата в средних терапевтических дозах.
Тестостерон, 17a-этинилэстрадиол, ретиноевая кислотаª (изотретиноин) и кверцетинª, специфический ингибитор CYP2C8, также подавляли образование 6a-гидроксипаклитаксела in vitro. В результате взаимодействия с субстратами, индукторами или ингибиторами CYP2C8 и/или CYP3A4 фармакокинетика паклитаксела in vivo также может меняться.
При применении таксолаª в комбинации с доксорубицином отмечали побочные эффекты, связанные с последовательностью введения этих препаратов. При введении таксолаª перед введением доксорубицина (таксолª вводили в течение 24 ч, доксорубицин в течение 48 ч) наблюдали более выраженную нейтропению и случаи стоматита. При применении таксолаª в комбинации с доксорубицином возможно повышение содержания доксорубицина (и его активного метаболита доксорубицинола) в сыворотке. Однако при струйном введении доксорубицина и введении препарата таксолª в течение 3 ч каких-либо изменений характера токсических эффектов, связанных с последовательностью введения препаратов, не отмечали.
Код АТХ
L01CD01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Paclitaxel:
Паклитаксел-Эбевеª /Paclitaxel-Ebeweª/ (Австрия),
Таксолª /Taxolª/ (Италия, США),
Ютаксанª /Yewtaxanª/ (Норвегия).
Форма выпуска: 0,6% концентрат для инфузий во флаконах по 5, 17 и 35 мл.
Условия и сроки хранения
Препарат следует хранить в защищённом от света месте при температуре 15-30 °С. При хранении невскрытых флаконов в холодильнике препарат может выпасть в осадок, который вновь растворяется при согревании до комнатной температуры при незначительном помешивании (или без него). Качество препарата при этом не ухудшается. Если препарат во флаконе остаётся мутным или наблюдается нерастворимый осадок, препарат следует выбросить. Замораживание не влияет на качество препарата.
Полусинтетические аналоги камптотецина
Иринотекан (Irinotecan)
Фармакологический/химический класс АТХ
(+)-7-Этиловый эфир 10-оксикамптодецин-10-(1,4´-бипиперидин)-1´-карбоновой кислоты (гидрохлорид).
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Противоопухолевый препарат растительного происхождения. Иринотекан - полусинтетическое производное камптотецина, специфический ингибитор клеточного фермента топоизомеразы I. В тканях препарат метаболизируется с образованием активного метаболита 7-этил-10-гидроксикамптотецина (SN-38), который превосходит по своей активности иринотекан. Иринотекан и метаболит SN-38 стабилизируют комплекс топоизомеразы I с ДНК, что препятствует её репликации.
В опытах in vivo было показано, что иринотекан также активен в отношении опухолей, экспрессирующих Р-гликопротеин множественной лекарственной резистентности (винкристин- и доксорубицин-резистентные лейкемии Р388).
Фармакокинетика
Фармакокинетика иринотекана и метаболита SN-38 была изучена при 30-минутной в/в инфузии препарата в дозе 100-750 мг/м2. Фармакокинетический профиль иринотекана не зависел от дозы. Иринотекан метаболизируется в печени под действием фермента карбоксиэстеразы с образованием активного метаболита SN-38.
Распределение в плазме двух- или трёхфазное. Средний период полувыведения в первую фазу трёхфазной модели составляет 12 мин, во вторую фазу - 2,5 ч, в третью фазу - 14,2 ч. Максимальная концентрация иринотекана и SN-38 достигалась к концу в/в инфузии в рекомендованной для монотерапии дозе 350 мг/м2. Связывание с белками плазмы крови составляет приблизительно 65% для иринотекана, 95% - для метаболита SN-38. Выведение: с мочой в течение 24 ч выводится 19,9% в виде неизменённого иринотекана и 0,25% в виде метаболита SN-38.
Фармакокинетические исследования подтвердили отсутствие влияния 5-фторурацила и кальция фолината на фармакокинетику иринотекана.
Показания к применению и дозирование
Лечение местно-распространённого или метастатического рака толстой и прямой кишки: в комбинации с 5-фторурацилом и кальция фолинатом у больных, ранее не получавших химиотерапию; у больных с прогрессированием болезни после общепринятого лечения; РШМ; рак желудка; рак лёгкого.
Препарат назначают только взрослым. Препарат вводят в виде в/в инфузии продолжительностью не менее 30 мин и не более 90 мин.
При лечении КРР иринотекан применяют как в виде монотерапии, так и в комбинации с 5-фторурацилом и кальцием фолинатом. В режиме монотерапии иринотекан применяют в дозе 350 мг/м2 каждые 3 недели.
В составе комбинированной терапии с продолжительной инфузией 5-фторурацила и кальция фолината иринотекан назначают еженедельно в дозе 80 мг/м2; 1 раз в 2 нед - 180 мг/м2; при введении в комбинации с болюсом 5-фторурацила и кальция фолината еженедельно - 125 мг/м2.
Введение иринотекана не следует проводить до тех пор, пока количество нейтрофилов в периферической крови не превысит 1,5x109/л, и пока не будут полностью купированы такие осложнения терапии как тошнота, рвота и диарея. Введение препарата до разрешения всех побочных эффектов можно отложить на 1-2 нед.
В случае, если на фоне лечения развивается выраженное угнетение костно-мозгового кроветворения (количество нейтрофилов менее 0,5x109/л, и/или количество лейкоцитов менее 1,0x109/л, и/или количество тромбоцитов менее 100x109/л), или фебрильная нейтропения: количество нейтрофилов 1,0x109/л и менее в сочетании с лихорадкой более 38 °С, или инфекционные осложнения, или тяжёлая диарея, или другая негематологическая токсичность 3-4 степени, последующие дозы иринотекана или при необходимости 5-фторурацила снижают на 15-20%.
Лечение препаратом иринотекан можно продолжать до появления объективных признаков прогрессирования опухолевого заболевания или развития недопустимых токсических проявлений.
У пациентов с нарушениями функции печени при уровне билирубина в сыворотке крови, превышающем верхнюю границу нормы не более чем в 1,5 раза, в связи с повышенным риском развития выраженной нейтропении следует тщательно контролировать показатели крови у больного. При повышении уровня билирубина более чем в 1,5 раза - лечение иринотеканом следует прекратить.
У пациентов с нарушениями функции почек лечение иринотеканом проводить не следует, так как применение у данной категории пациентов не изучено.
Специальных инструкций по применению препарата иринотекан у больных пожилого возраста нет. С осторожностью следует подбирать дозу в каждом конкретном случае.
Безопасность и эффективность применения препарата иринотекан у детей недостаточно изучены.
Побочные эффекты
Многие побочные эффекты противоопухолевой терапии неизбежны и представляют проявление фармакологического действия препарата. Некоторые из них (например, лейкопению и тромбоцитопению) используют в качестве параметров при индивидуальном подборе дозы.
Следующие побочные/неблагоприятные эффекты отобраны на основе их потенциальной клинической значимости:
Со стороны системы кроветворения: нейтропения: обычно бессимптомная; менее часто - фебрильная нейтропения.
Анемия, связанная с угнетением функции костного мозга: обычно бессимптомная; необычная усталость или слабость; тромбоцитопения: обычно бессимптомная; менее часто - необычные кровотечения или кровоизлияния, чёрный дёгтеобразный стул, кровь в моче или кале, точечные красные пятна на коже.
Примечание: нейтропения обратима и не носит кумулятивный характер. Полное восстановление количества нейтрофилов и тромбоцитов отмечают к 21 дню от начала химиотерапии.
Со стороны пищеварительной системы: тошнота, рвота, диарея, боли в животе, анорексия, мукозиты, запор.
Примечание: диарея, возникающая более чем через 24 ч после введения (отсроченная диарея), - дозолимитирующий токсический эффект иринотекана, развитие отсроченной диареи в среднем отмечают на 4-7 сутки от начала терапии; при применении иринотекана при монотерапии приблизительно у 10% пациентов, применявших противорвотные средства, отмечали выраженную тошноту и рвоту.
Острый холинергический синдром: ранняя диарея, боли в животе, усиление потоотделения, конъюнктивит, ринит, снижение АД, вазодилатация, слёзотечение, слюнотечение, озноб, недомогание, головокружение, расстройство зрения, миоз, наблюдали у 9% пациентов, получающих иринотекан в качестве монотерапии (у 1,4% - в составе комбинированной терапии). Все симптомы купируются после введения атропина и с профилактической целью данным пациентам перед последующей инфузией иринотекана необходимо введение атропина.
Со стороны ЦНС и периферической нервной системы: непроизвольные мышечные подёргивания или судороги, парестезии, астения.
Аллергические реакции: редко - кожная сыпь, очень редко - анафилактический шок.
Прочие: развитие обезвоживания, обычно связанного с диареей или рвотой. Также отмечены очень редкие случаи развития почечной недостаточности, артериальной гипотензии, недостаточности кровообращения у пациентов, перенёсших эпизоды обезвоживания, связанные с диареей и/или рвотой. Редко отмечали локальные реакции в месте введения препарата.
Передозировка
Основные ожидаемые симптомы передозировки - нейтропения и диарея. При необходимости проводят симптоматическую терапию. Специфического антидота не существует.
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу: угнетение функции костного мозга; ветряная оспа, включая недавний контакт с больным или опоясывающий герпес: риск тяжёлого генерализованного заболевания, другие инфекции.
Хронические воспалительные заболевания кишечника и/или кишечная непроходимость, тяжёлое нарушение функции почек, подагра или почечные конкременты (ураты) в анамнезе: риск гиперурикемии; увеличение уровня билирубина в сыворотке крови в 3 раза выше верхней границы нормы. Повышенная чувствительность к препарату. Нельзя применять при беременности. Женщинам, получающим иринотекан, следует избегать грудного вскармливания.
Беременность
Препарат может оказывать токсическое действие на органы мочеполовой системы плода. Первый триместр: обычно рекомендуется избегать применения противоопухолевых препаратов, главным образом комбинированной химиотерапии. Хотя информация ограничена из-за относительно малого числа случаев использования противоопухолевых средств во время беременности, необходимо учитывать возможное мутагенное, тератогенное и канцерогенное действие данных препаратов.
Другие факторы, оказывающие вредное действие на плод, включают неблагоприятные реакции, отмечаемые у взрослых.
Как правило, в период лечения цитотоксическими препаратами рекомендуют применение противозачаточных средств.
Кормление грудью
Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограничена, во время проведения химиотерапии грудное вскармливание не рекомендуют из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Так как иринотекан обладает антихолинэстеразной активностью, возможно увеличение продолжительности нервно-мышечной блокады при одновременном применении с суксаметонием и антагонистическое взаимодействие в отношении нервно-мышечной блокады при сочетании с недеполяризующими миорелаксантами.
Фармацевтическое взаимодействие: иринотекан не следует смешивать с другими препаратами в одном флаконе.
Резюме и дополнительные сведения
Существуют данные об эффективности применения иринотекана при раке лёгкого, раке желудка.
Лечение препаратом следует проводить в специализированных химиотерапевтических отделениях и только под наблюдением врача, имеющего опыт работы с противоопухолевыми препаратами.
Препарат следует назначать с осторожностью пациентам, получавшим ранее лучевую терапию на область брюшной полости или таза, пациентам с общим состоянием по шкале ВОЗ³2, пациентам женского пола; во всех этих случаях повышается риск развития диареи.
Диарею, возникающую как следствие цитостатического действия препарата (отсроченная диарея), обычно отмечают не ранее 24 ч после введения иринотекана (у большинства больных в среднем на 4-7 день от начала терапии). При появлении первого эпизода жидкого стула необходимо назначение обильного питья, содержащего электролиты, и немедленное проведение противодиарейной терапии, включающей лоперамид в высоких дозах (4 мг на первый приём, затем по 2 мг каждые 2 ч). Терапию продолжают ещё в течение 12 ч вслед за последним эпизодом жидкого стула (но не более 48 ч из-за риска развития пареза кишечника). Если диарею расценивают как тяжёлую (более 6 эпизодов жидкого стула в течение суток или тяжёлые тенезмы), а также, если она сопровождается рвотой или лихорадкой, больной должен быть срочно госпитализирован для проведения комплексного лечения, включающего антибиотики широкого спектра действия. При умеренной или слабовыраженной диарее (менее 6 эпизодов жидкого стула в течение суток и умеренные тенезмы), которая не купируется в течение первых 48 ч, начинают приём внутрь антибиотиков широкого спектра действия, при этом больного госпитализируют. При одновременном возникновении диареи и тяжёлой нейтропении (количество лейкоцитов менее 0,5x109/л) в дополнение к антидиарейной терапии с профилактической целью назначают парентерально антибиотики широкого спектра действия.
Пациент должен быть информирован о возможности развития у него диареи. Пациенты должны сразу информировать своего врача о возникновении диареи (чтобы немедленно начать противодиарейную терапию).
При неадекватном лечении диареи может развиться состояние, угрожающее жизни больного, особенно, если диарея развилась на фоне нейтропении.
Пациентам с фебрильной нейтропенией: температура тела ³38 °С и количество нейтрофилов £1,0x109/л) следует немедленно начать антибиотикотерапию в условиях стационара.
При развитии острого холинергического синдрома при отсутствии противопоказаний показано п/к введение атропина в дозе 0,25 мг. Следует соблюдать осторожность при применении препарата у пациентов с бронхиальной астмой. Пациентам, имеющим в анамнезе указания на развитие острого холинергического синдрома, перед последующим назначением иринотекана рекомендовано профилактическое назначение атропина в стандартной дозе.
Учитывая, что иринотекан содержит сорбитол, препарат не назначают пациентам с наследственной непереносимостью фруктозы.
У пациентов, получающих иринотекан, необходимо еженедельно проводить развёрнутый клинический анализ крови и контролировать функцию печени.
Влияние на способность к вождению автотранспорта и управлению механизмами: пациентов необходимо предупредить о возможности появления во время лечения иринотеканом головокружения и зрительных расстройств, которые развиваются в течение 24 ч после введения препарата. При возникновении этих симптомов пациентам необходимо воздерживаться от управления автомобилем и другими механизмами.
Код АТХ
L01XX19
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Cаmpto:
Иринотеканª/Iriotecanª
Иритенª/ Iritenª (РФ)
Камптозарª/ Camptosarª (Израиль)
Форма выпуска: концентрат для приготовления раствора для инфузии во флаконах по 40 мг/2 мл и 100 мг/5 мл.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей и защищённом от света месте, при температуре не выше 25 °С. Срок годности 3 года.
Приготовленный раствор должен быть использован сразу после разведения.
Если разведение выполнено с соблюдением правил асептики (например, в установке ламинарного воздушного потока) раствор иринотекана может быть использован в случае хранения при комнатной температуре в течение 12 ч (включая время инфузии) и при температуре 2-8 °С - в течение 24 ч после вскрытия флакона с концентратом.
Топотекан (Topotecan)
Фармакологический/химический класс АТХ
(S)-10-[(Диметиламино)-метил]-4-этил-4,9-дигидрокси-1Н-пирано[3´,4´:6,7]индолизино[1,2-b]хинолин-3,14-(4Н,12Н)-диона гидрохлорид.
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Противоопухолевый препарат, ингибитор топоизомеразы I. Топоизомераза I - фермент, непосредственно участвующий в репликации ДНК. Топотекан связывается с комплексом топоизомераза I-ДНК и предотвращает повторное сшивание нитей ДНК. Цитотоксичность топотекана обусловлена повреждением удвоенной нити ДНК, образующейся в процессе её синтеза. При этом ферменты, участвующие в репликации, взаимодействуют с тройным комплексом, сформированным топотеканом, топоизомеразой I и ДНК.
Фармакокинетика
При в/в введении топотекана взрослым в дозах 1,0-1,5 мг/м2 в виде 30-минутной ежедневной инфузии в течение 5 дней AUC увеличивалась пропорционально увеличению дозы. Связывание топотекана с белками плазмы - 35%. Распределение между клетками крови и плазмой достаточно однородно. Топотекан подвергается метаболизму путём гидролиза лактонового кольца с образованием карболовой кислоты в виде открытого кольца.
В исследованиях in vitro топотекан не ингибировал человеческие изоферменты CYP1A2, CYP2A6, CYP2C8/9, CYP2C19, CYP2D6, CYP2E или CYP4A системы цитохрома Р 450, а также не ингибировал человеческие цитозольные ферменты дигидропиримидин оксидазу или ксантин оксидазу.
Клиренс топотекана - 64 л/ч, что составляет приблизительно 2/3 печёночного кровотока. Период полувыведения составляет 2-3 ч. Около 20-60% дозы выводится с мочой в неизменённом виде и в виде метаболитов.
У пациентов с печёночной недостаточностью, по сравнению с контрольной группой пациентов, плазменный клиренс был пониженным приблизительно до 67%. Период полувыведения топотекана увеличивался приблизительно на 30%. Общий плазменный клиренс у пациентов с печёночной недостаточностью был меньше лишь на 10% по сравнению с контрольной группой пациентов.
У пациентов с почечной недостаточностью (клиренс креатинина 41-60 мл/мин) плазменный клиренс уменьшился приблизительно на 67% по сравнению с контрольной группой пациентов. Vd был слегка пониженным, и, таким образом, T1/2 увеличился только на 14%. У пациентов с умеренной почечной недостаточностью плазменный клиренс топотекана сократился до уровня, который составлял 34% значения этого параметра у пациентов контрольной группы, период полувыведения увеличен с 1,9 ч до 4,9 ч.
Клиренс топотекана у детей при назначении его в виде 24-часовой непрерывной инфузии в дозе от 2 до 7,5 мг/м2 и в виде непрерывной 72-часовой инфузии в дозе от 0,75 до 1,95 мг/(м2´сут) подобен таковому у взрослых, получающих такие же дозы препарата.
Показания к применению и дозирование
Мелкоклеточный рак лёгкого; рак яичников; миелодиспластический синдром.
Для взрослых и пациентов пожилого возраста рекомендуемая начальная доза топотекана составляет 1,5 мг/м2 в/в в виде инфузии в течение не менее 30 мин ежедневно в течение 5 дней с интервалом в 21 день перед началом каждого цикла. Рекомендуется провести не менее 2 циклов терапии, поскольку период развития терапевтического эффекта у больных раком яичника составляет 8,0-11,7 нед, а у пациентов с мелкоклеточным раком лёгкого - 6,1 нед. Перед назначением первого цикла терапии топотеканом у пациентов исходный уровень нейтрофилов должен быть >1,5x109/л, тромбоцитов - >100x109/л и уровень гемоглобина ³9 г/дл.
Топотекан не назначают повторно, пока количество нейтрофилов не превысит 1,0x109/л, тромбоцитов - 100x109/л, а уровень гемоглобина - 9 г/дл (в том числе после переливания крови если это необходимо).
Пациентам с нейтропенией IV степени (количество нейтрофилов менее 0,5x109/л) в течение 7 дней или более или при фебрильной нейтропении, а также пациентам, лечение которых было отсрочено из-за нейтропении, препарат следует назначать в редуцированной дозе: 1,25 мг/(м2´сут), при необходимости постепенно снижая её до 1 мг/(м2´сут). При последующих циклах, начиная с 6-го дня цикла (первого дня после завершения применения топотекана), можно назначать профилактически колониестимулирующие факторы, чтобы поддержать интенсивность дозы. Если нейтропения не поддаётся коррекции при применении колониестимулирующего фактора, дозу препарата следует уменьшить.
Аналогичную коррекцию дозы проводят при уменьшении количества тромбоцитов менее 25x109/л.
Топотекан следует отменить, если при применении в дозе 1 мг/м2 требуется её дальнейшее снижение для предотвращения развития побочных эффектов.
При нарушениях функции почек для пациентов с КК³40 мл/мин коррекции дозы не требуется. Рекомендуемая доза для пациентов с КК 20-39 мл/мин составляет 750 мкг/(м2´сут). Для рекомендаций относительно дозы препарата для пациентов с КК<20 мл/мин существующих данных недостаточно.
Для пациентов с нарушениями функции печени (билирубин плазмы от 1,5 до 10 мг/дл) специального подбора дозы не требуется. При применении топотекана в дозе 1,5 мг/м2 в течение 5 дней каждые 3 нед наблюдали небольшое снижение клиренса топотекана.
Побочные эффекты
Со стороны системы кроветворения (обратимые, имеют дозозависимый характер): выраженная нейтропения (около 80%), сопровождающаяся лихорадкой или инфекцией (около 20%); сепсис (около 4%), выраженная тромбоцитопения (около 27%), умеренная и выраженная анемия (около 36%), кровоточивость, кровотечение (в том числе скрытое, обусловленное тромбоцитопенией). У пациентов с мелкоклеточным раком лёгкого и карциномой яичника нейтропения и тромбоцитопения появлялись в пределах 2 нед терапии, и в большинстве случаев эти осложнения длились не более 7 дней. В 11% терапевтических курсов нейтропения продолжалась более 7 дней.
При проведении длительной терапии не было разницы в частоте гематологической токсичности в течение первых 6 циклов лечения по сравнению с последующими.
Со стороны пищеварительной системы: тошнота, рвота, диарея, запор, стоматит, анорексия, боли в животе, гипербилирубинемия.
Со стороны ЦНС и периферической нервной системы: головная боль, парестезии.
Аллергические реакции: кожная сыпь, ангионевротический отёк, зуд, дерматит; редко - анафилактические реакции.
Дерматологические реакции: алопеция.
Со стороны организма в целом: усталость, недомогание, астения, лихорадка, боли различной локализации.
Местные реакции: гематома или гиперемия кожи в месте введения препарата.
При проведении длительной терапии не выявлено разницы в частоте негематологической токсичности при первых 6 циклах лечения по сравнению с последующими.
Передозировка
Симптомы: нарастающее угнетение функции костного мозга, лихорадка, кровотечения и стоматит.
Лечение: антидот топотекана неизвестен. Лечение cимптоматическое: при необходимости переливание компонентов крови, антибактериальная терапия.
Противопоказания
Выраженное угнетение функции костного мозга до назначения препарата (нейтропения <1,5x109/л и/или тромбоцитопения <100x109/л); беременность; грудное вскармливание; детский возраст (опыт применения отсутствует); повышенная чувствительность к компонентам препарата.
Беременность
Топотекан может оказывать эмбриотоксическое и фетотоксическое действие. Оказывает тератогенное действие, поэтому применение препарата при беременности противопоказано.
Женщины детородного возраста в период приёма топотекана должны использовать надёжные средства контрацепции.
Грудное вскармливание
Несмотря на то, что неизвестно, выделяется ли топотекан с грудным молоком, грудное вскармливание при применении топотекана следует прекратить.
Резюме и дополнительные сведения
Топотекан следует применять под руководством врача, имеющего опыт работы с цитотоксическими препаратами. Топотекан не рекомендуется применять в монорежиме в качестве первой линии терапии.
При развитии нейтропении на фоне применения топотекана необходимо установить тщательное наблюдение за пациентом для своевременной диагностики развития инфекции.
При развитии тромбоцитопении необходима крайняя осторожность при выполнении инвазивных процедур, следует проводить регулярный осмотр кожных покровов и слизистых оболочек, а также выделений (для выявления признаков кровоточивости).
Характер взаимодействия топотекана с препаратами платины зависит от последовательности назначения платины, а именно, назначают ли препараты платины в 1-й или в 5-й день применения топотекана. Если цисплатин или карбоплатин назначают в 1-й день, то необходимо использовать уменьшенные дозы каждого препарата по сравнению с дозами при назначении соединений платины в 5-й день.
Ниже приведены дозы и схемы сочетанного применения топотекана и препаратов платины, которые назначали пациентам в качестве терапии первой линии:
-
цисплатин в 1-й день в дозе 50 мг/м2 и топотекан в дозе 0.75 мг/м2 с 1-го по 5-й день;
-
цисплатин в 5-й день в дозе 50 мг/м2 и топотекан в дозе 1.25 мг/м2 с 1-го по 5-й день;
-
карбоплатин в 1-й день: AUC 5 (формула Калверта); топотекан в дозе 0.5 мг/м2 с 1-го по 5-й день;
-
карбоплатин в 5-й день: AUC 5; топотекан в дозе 1,0 мг/м2 с 1-го по 5-й день.
При работе с топотеканом следует строго соблюдать соответствующие правила обращения с противоопухолевыми препаратами: персонал должен быть обучен правилам приготовления растворов; не допускать беременных сотрудниц к работе с препаратом; при приготовлении растворов следует пользоваться защитной одеждой (в том числе маской, защитными очками, защитными перчатками); все предметы, использованные при работе с препаратом, относятся к категории предметов высокого риска, их следует помещать в мешки для высокотемпературной переработки, пролитый раствор должен быть смыт большим количеством воды; при случайном попадании препарата на кожу или в глаза необходимо немедленно промыть их обильным количеством воды.
В процессе терапии топотеканом необходимо регулярно контролировать развёрнутую картину периферической крови, включая уровень гемоглобина и гематокрита, количество лейкоцитов и тромбоцитов.
На фоне терапии топотеканом необходимо воздерживаться от управления автомобилем, работы с механизмами, а также других занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, если у пациента сохраняются утомляемость и слабость.
Клинически значимые взаимодействия
При одновременном применении топотекана с другими цитотоксическими средствами, вызывающими миелодепрессию, возможно усиление угнетающего действия на костный мозг.
Топотекан не ингибирует ферменты цитохрома Р 450. Совместное применение с ондансетроном, гранисетроном, морфином или кортикостероидами не оказывает существенного влияния на фармакокинетические параметры топотекана.
Код АТХ
L01XX17
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования HYCAMTIN:
Топотеканª/Topotecanª (Glaxo Smith Kline)
Форма выпуска: лиофилизированный порошок для приготовления раствора для инфузий во флаконах по 0,004 г (4 мг).
Условия и сроки хранения
Препарат следует хранить в недоступном для детей, защищённом от света месте при температуре не выше 30 °С. Срок годности - 3 года.
Приготовленный раствор следует хранить при температуре 5-30 °С не более 24 ч.
ГОРМОНАЛЬНЫЕ И АНТИГОРМОНАЛЬНЫЕ СРЕДСТВА
Гормональные средства и их синтетические аналоги
Андрогены
Тестостерон (Testosteroni propionas)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(17бета)-17-гидроксиандрост-4-ен-3-он.
Терапевтический класс АТХ
Противоопухолевое средство с андрогенной активностью.
Механизм действия
Андрогенный препарат, содержащий смесь разных эфиров тестостерона. Тестостерон необходим для формирования яичек, предстательной железы, семенных пузырьков и развития вторичных и третичных половых признаков. Участвует в формировании конституции тела и полового поведения, повышает либидо и потенцию, стимулирует сперматогенез, ослабляет негативные проявления мужского климакса. Тестостерон - антагонист женских половых гормонов эстрогенов. Вызывает торможение гонадотропной функции гипофиза и подавляет функцию молочных желёз у женщин. Во время лечения могут наблюдаться явления маскулинизации.
Тестостерон оказывает анаболическое действие: стимулирует синтез белка, усиливает фиксацию кальция в костях, увеличивает мышечную массу, стимулирует образование эритропоэтина в почках, повышает уровень гемоглобина в крови.
У здоровых мужчин введение экзогенного тестостерона угнетает выделение собственного (эндогенного) гормона путём торможения секреции ЛГ. В высоких дозах препарат подавляет сперматогенез, влияя на обратное торможение секреции ФСГ.
У мужчин с функциональной недостаточностью гипофиза тестостерон устраняет симптомы гипогонадизма. Если импотенция вызвана не гипогонадизмом, то лечение не приносит результатов.
Входящие в состав препарата эфиры тестостерона обладают различной скоростью всасывания и выведения, что обеспечивает быстрое развитие эффекта и длительное действие (до 4 нед) после однократного введения: тестостерона пропионат действует в течение первых суток, действие тестостерона фенилпропионата и изокапроната начинается через 24 ч после инъекции и продолжается до 2 нед. Активность тестостерона капроната возрастает в период, когда влияние тестостерона изокапроната и фенилпропионата прекращается.
Фармакокинетика
С белками плазмы (со специфической фракцией глобулинов) связывается около 98%. Метаболизируется в печени с образованием различных 17-кетостероидов, которые после соединения с глюкуроновой или серной кислотой выделяются с мочой. Выводится почками в виде метаболитов (около 90%), через кишечник в несвязанном виде (6%). Период полувыведения тестостерона - 10-100 мин.
Показания к применению и режим дозирования
Рак молочной железы; рак яичников.
Режим дозирования: препарат вводят внутримышечно глубоко в ягодичную мышцу.
Дозы устанавливают индивидуально в зависимости от показаний и реакции больного на лечение. При раке молочной железы и яичников - по 1-2 мл каждый 7-14 день в течение длительного времени.
Побочные эффекты
Признаки поражения эндокринной системы: у женщин - дисменорея, торможение секреции гонадотропина, маскулинизация, гирсутизм.
Признаки поражения половой системы: нарушение либидо.
Дерматологические реакции: угри, облысение по мужскому типу.
Признаки поражения пищеварительной системы: тошнота, нарушение функции печени, печёночная пурпура, опухолевые заболевания печени, холестатическая желтуха, повышение активности печёночных трансаминаз.
Признаки поражения свёртывающей системы крови: торможение активности плазменных факторов свёртывания крови II, V, VII и X, кровотечение у больных, принимающих противосвёртывающие препараты внутрь, полицитемия.
Признаки поражения ЦНС и периферической нервной системы: головные боли, страх, парестезии.
Признаки нарушения обмена веществ: повышение уровня холестерина в плазме крови.
Местные реакции: воспаление и боли в месте инъекции.
Противопоказания
Гиперкальциемия; гиперкальциурия; сердечная недостаточность; почечная и печёночная недостаточность; астения; беременность; грудное вскармливание; повышенная чувствительность к препарату.
Беременность и Кормление грудью
Препарат противопоказан к применению во время беременности.
При необходимости применения препарата в период лактации грудное вскармливание следует прекратить.
Резюме и дополнительные сведения
Препарат нельзя вводить внутривенно.
Андрогенная терапия при раке молочной железы может быть причиной гиперкальциемии, связанной со стимуляцией остеолиза. Данный процесс может усиливать метастазирование в кости. При лечении женщин следует контролировать концентрацию кальция в сыворотке крови.
При назначении андрогенных препаратов в высоких дозах следует контролировать уровень гемоглобина и гематокрит.
При появлении симптомов гепатита, развитии желтухи или изменении показателей функции печени следует отменить препарат и определить этиологию этих изменений. Следует контролировать состояние функции печени.
У пациентов с заболеваниями сердечно-сосудистой системы, печени или почек при развитии периферических отёков препарат следует отменить.
С осторожностью назначать андрогенную терапию пациентам с замедленным половым созреванием. У этой категории пациентов следует контролировать состояние костной системы каждые 6 мес.
Влияние на способность к вождению автотранспорта и управлению механизмами. Не обнаружено прямого влияния препарата на способность к управлению автотранспортом и работе с механизмами. Ухудшение концентрации внимания и уменьшение скорости психомоторных реакций возможно при развитии сердечной недостаточности.
Передозировка
Данные о передозировке препарата не предоставлены.
Клинически значимые взаимодействия
У пациентов, получающих антикоагулянты внутрь, при одновременном применении тестостерона, особенно в начале и при отмене терапии, требуется постоянный контроль показателей свёртывания крови.
У больных сахарным диабетом андрогенные препараты могут уменьшать уровень глюкозы в крови и потребность в инсулине.
При применении тестостерона с АКТГ или глюкокортикоидами повышается риск появления периферических отёков, особенно у пациентов с заболеваниями печени или сердечно-сосудистой системы.
Препараты, вызывающие индукцию микросомальных ферментов печени (в т.ч. рифампицин, карбамазепин, фенилбутазон, фенитоин, примидон, барбитураты, салицилаты), могут уменьшать эффекты тестостерона.
Код АТХ
G03BA03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: 1% или 5% раствор в масле в ампулах по 1 мл.
Условия и сроки хранения
Препарат следует хранить в защищённом от света месте при температуре 15-25 °C.
В случае появления в масляном растворе осадка в виде хлопьев следует поместить ампулу на несколько минут в теплую воду (37 °C).
Эстрогены
Фосфэстрол (Phosphoestrolum)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(E)-4,4’-(1,2-диэтил-1,2-этендил)бис[фенол]бис[дигидрофосфат] (в виде тетранатриевой соли).
Белый или белый с кремовым оттенком мелкокристаллический порошок. Легко растворим в воде, практически нерастворим в спирте.
Терапевтический класс АТХ
Противоопухолевое средство с эстрогенной активностью.
По структуре фосфэстрол - фосфорный эфир диэтилстильбэстрола.
Механизм действия
Фосфэстрол был синтезирован как эстрогенный препарат с избирательной противоопухолевой активностью, который неактивен во время циркуляции в крови. При проникновении в опухолевую ткань предстательной железы препарат дефосфорилируется с образованием диэтилстильбэстрола под влиянием кислой фосфатазы (активность которой повышена в опухолевых клетках). Диэтилстильбэстрол оказывает цитостатическое действие, угнетая аэробный гликолиз, митоз, рост и миграцию опухолевых клеток. Подавляет синтез андрогенов, препятствует реализации эффектов андрогенов.
По принципу построения фосфэстрол имеет, таким образом, сходство с циклофосфамидом.
Фармакокинетика
После приёма внутрь препарат быстро абсорбируется из ЖКТ. Метаболизируется в печени, большая часть секретируется с жёлчью в кишечник, откуда реабсорбируется (или выводится с калом); частично выделяется почками.
Показания к применению и режим дозирования
Применяют фосфэстрол для лечения рака предстательной железы (включая диссеминированную форму). Это специфическое средство действует на всех стадиях чувствительного к эстрогенным препаратам рака этой локализации. При эстрогенрезистентных формах опухоли фосфэстрол малоэффективен.
Фосфэстрол применяют внутривенно в виде 6% раствора и внутрь в виде таблеток.
Существуют разные схемы применения фосфэстрола. Обычно лечение начинают с ежедневного внутривенного введения по 1-2 г (4 ампулы по 0,3 г). Вводят медленно или капельно, разводя в 5% растворе глюкозы (при положении больного лёжа), в течение 10 дней, затем по 0,3 г (1 ампула в день) в течение 10-20 дней. В особых случаях применяют препарат ежедневно длительно.
Ослабленным больным, пациентам с сердечной недостаточностью, нарушениями функций печени и почек препарат начинают вводить в меньших дозах - 0,6 г (2 ампулы по 0,3 г) в день в течение 10 дней, затем по 0,3 г (1 ампула) в день.
Снижение дозы фосфэстрола следует проводить под контролем клинических и биохимических показателей, определяя уровень кислой фосфатазы в сыворотке крови.
При невозможности внутривенного введения фосфэстрол назначают внутрь в виде таблеток (до еды с небольшим количеством жидкости).
Принимают по 3-4 таблетки (по 0,1 г в таблетке) 3 раза в день. В случае развития диспепсических явлений, рекомендуют задерживать таблетки за щекой или под языком до полного рассасывания.
Для поддерживающей терапии назначают по 1-2 таблетки 3 раза в день, затем по 1 таблетке 2 раза в день (не меньше). Можно проводить поддерживающую терапию инъекциями фосфэстрола по 0,3 г: 4 раза на первой неделе, 3 - на второй, 2 - на третьей и 1 раз на четвёртой неделе (под контролем клинических и биохимических показателей).
Побочные эффекты
Больные обычно хорошо переносят лечение фосфэстролом. В начале лечения иногда возникают тошнота, рвота, ухудшение общего состояния, головная боль, головокружение, нарушение толерантности к глюкозе, гиперкальциемия. Эти явления проходят в процессе дальнейшего лечения. Возможно появление зуда и боли в области заднего прохода и половых органов, реже - лица и шеи. В этих случаях можно применять противогистаминные препараты. В процессе лечения могут возникнуть боли в области расположения метастатических узлов. Возможно также снижение свёртывания крови с геморрагическими явлениями. Могут наблюдаться явления феминизации (гинекомастия, геморрагии).
Противопоказания
Препарат противопоказан при пониженной свёртываемости крови, склонности к геморрагиям, при выраженных поражениях печени, инфаркте миокарда в анамнезе, недостаточности кровообращения, тромбоэмболии и тромбофлебитах.
Для предупреждения снижения свёртывания крови рекомендуется вводить в вену раствор кальция хлорида.
Клинически значимые взаимодействия
Растворы фосфэстрола нельзя смешивать с инфузионными растворами, содержащими соли кальция или магния.
Резюме и дополнительные сведения
Ослабленным больным, а также пациентам с нарушениями функции печени и почек, с сердечной недостаточностью необходима коррекция режима дозирования. С целью уменьшения частоты и выраженности побочных эффектов показано применение антигистаминных препаратов. В процессе лечения необходимо проводить контроль концентрации щелочной фосфатазы в сыворотке и исследование осадка мочи.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Формы выпуска: 6% раствор в ампулах по 5 мл; таблетки по 0,1 г в упаковке по 30 штук.
Полиэстрадиола фосфат (Polyestradiol phosphate)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(17бета)-эстра-1,3,5(10)триен-3,17-диола полимерный эфир с фосфорной кислотой.
Терапевтический класс АТХ
Противоопухолевое средство.
Фармакологическое действие
Представляет собой полимер, состоящий из 17b-эстрадиола и фосфорной кислоты. Оказывает влияние на гипоталамо-гипофизарную систему (по механизму обратной связи), что приводит к снижению продукции тестостерона и замедлению роста андрогензависимых опухолей предстательной железы. Препарат оказывает сильное и продолжительное эстрогенное влияние. По сравнению с эстрадиолом действует более длительно. Поскольку полиэстрадиола фосфат ингибирует кислую и щелочную фосфатазы, разрушение полимера фосфатазами происходит очень медленно, это обеспечивает продолжительную эстрогенную активность полиэстрадиола фосфата.
Показания к применению и режим дозирования
Паллиативное лечение рака предстательной железы.
В связи с пролонгированным действием, используется в целях поддерживающей терапии после применения фосфэстрола фосфата и других быстродействующих препаратов.
Вводят глубоко внутримышечно. При раке предстательной железы назначают по 80-160 мг 1 раз в месяц в течение 2-3 мес, затем дозу уменьшают до 40-80 мг в месяц.
Побочные эффекты
Признаки поражения пищеварительной системы: тошнота, рвота, холестаз, холестатическая желтуха.
Признаки поражения ЦНС: головная боль, мигрень, снижение умственной работоспособности, депрессия.
Признаки поражения эндокринной системы: снижение толерантности к глюкозе, гинекомастия, феминизация, атрофия яичек, снижение либидо и/или потенции.
Аллергические реакции: кожная сыпь, бронхообструктивный синдром, анафилактический шок.
Прочие: задержка натрия и воды; редко - тромбоэмболия, повышение АД.
Передозировка
Симптомы: возможно усиление побочных эффектов, особенно со стороны пищеварительной системы.
Лечение: специфический антидот отсутствует; проводят симптоматическую терапию. В течение 6 нед после передозировки следует контролировать картину крови и функциональное состояние печени.
Противопоказания
Тромбоэмболический синдром, активный тромбофлебит, синдром Дубина-Джонсона, серповидноклеточная анемия, тяжёлые нарушения функции печени, синдром Ротора, повышенная чувствительность к полиэстрадиола фосфату и эстрадиолу.
Резюме и дополнительные сведения
С особой осторожностью применяют при хронической сердечной недостаточности, хронической почечной недостаточности, артериальной гипертензии, эпилепсии, мигрени, нарушениях функции печени, порфирии, отосклерозе, нарушениях мозгового кровообращения, ИБС, при указаниях в анамнезе на тромбоэмболический синдром и тромбофлебит. В период лечения необходим систематический контроль АД, функционального состояния печени, у пациентов с сахарным диабетом - концентрации глюкозы в крови.
Перед планируемым оперативным вмешательством, связанным с повышенным риском тромбоэмболии, лечение полиэстрадиола фосфатом следует прекратить по крайней мере за 6 нед. Отмена терапии показана в следующих случаях: длительная иммобилизация, появление мигренеподобных головных болей, внезапное нарушение зрения (подозрение на тромбоз вен сетчатки), развитие тромбофлебита или тромбоэмболии, холестатического гепатита, повышение АД.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: выпускается в виде лиофилизированной белой пористой массы во флаконах по 40 или 80 мг в упаковке по 10 флаконов с приложением 10 ампул с растворителем (по 2 мл).
Растворение производят непосредственно перед инъекцией.
Условия хранения
В защищённом от света месте.
Эстрамустин
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(17бета)-эстра-1,3,5(10)-триен-3,17-диол-3-[бис(2-хлорэтил)карбамат] (в виде 17бета-динатрия фосфата).
Терапевтический класс АТХ
Противоопухолевый препарат
Фармакологическое действие
Эстрамустин (конъюгат эстрадиола и азотистого иприта) представляет собой противоопухолевый препарат с двойным механизмом действия. Установлено, что эстрон и эстрадиол (получающиеся в результате биотрансформации эстрамустина фосфата) обладают антигонадотропной активностью и вызывают снижение уровня тестостерона, сходное с таковым после хирургической кастрации.
В процессе дефосфорилирования эстрамустина фосфата образуется эстрамустин, который далее биотрансформируется в эстромустин. Эти метаболиты обладают антимитотическим действием, препятствуют образованию микротрубочек в метафазу и их разрушению в интерфазу митоза.
Фармакокинетика
После внутривенного введения неизменённый эстрамустина фосфат обнаруживается в плазме крови, однако он быстро биотрансформируется с образованием эстрамустина и далее - эстромустина, который является основным метаболитом, присутствующим в плазме. Связывание эстрамустина и эстромустина с белками плазмы высокое. Эстрамустин и эстромустин подвергаются дальнейшей биотрансформации с образованием эстрогенов - эстрадиола и эстрона. После введения препарата эстрамустин и эстромустин обнаруживаются в опухолевой ткани предстательной железы человека. Концентрации эстрамустина и эстромустина в опухолевой ткани выше, чем в плазме. Возможно, это объясняется тем, что эстрамустин и эстромустин поглощаются тканью предстательной железы за счет их связывания с особым белком, который был обнаружен в опухолевой ткани предстательной железы.
Эстрамустин и эстромустин выделяются с жёлчью и калом и не обнаруживаются в моче. Эстрадиол и эстрон подвергаются дальнейшему метаболизму и частично выделяются с мочой.
Показания к применению и режим дозирования
Поздние стадии рака предстательной железы, особенно при рефрактерности к гормональной терапии; первичная терапия рака предстательной железы при наличии прогностических факторов, указывающих на возможную низкую эффективность гормональной терапии.
Доза эстрамустина фосфата для приёма внутрь может составлять от 7 до 14 мг/кг массы тела в 2-3 приёма (4-8 капсул в сутки). Рекомендуемая начальная доза составляет 4-6 капсул в сутки для достижения дозы не менее 10 мг/кг массы тела.
Капсулы следует принимать не менее чем за 1 ч до еды или через 2 ч после еды, запивать водой.
Рекомендуемая доза эстрамустина фосфата в форме инъекций составляет 5 мг/кг массы тела (300-450 мг) ежедневно в течение 3 нед, затем по 300 мг 2 раза в неделю в качестве поддерживающей терапии. При отсутствии эффекта от проводимой в течение 4-6 нед терапии препарат следует отменить.
Побочные эффекты
Признаки поражения эндокринной системы: часто - гинекомастия, импотенция.
Признаки поражения пищеварительной системы: часто - тошнота, рвота (особенно в течение первых 2 нед лечения); возможно - диарея, нарушение функции печени.
Признаки поражения сердечно-сосудистой системы: задержка жидкости, ИБС (включая инфаркт миокарда), застойная сердечная недостаточность, тромбоэмболия, артериальная гипертензия.
Признаки поражения системы кроветворения: редко - анемия, лейкопения и тромбоцитопения.
Признаки поражения ЦНС: редко - мышечная слабость, депрессия, головная боль, спутанность сознания, летаргия.
Аллергические реакции: кожная сыпь, ангионевротический отёк (отёк Квинке и отёк гортани). Во многих случаях пациенты одновременно с эстрамустином получали ингибиторы АПФ.
Местные реакции: в месте внутривенного введения - флебит.
Противопоказания
Выраженные нарушения функции печени; заболевания сердечно-сосудистой системы, такие как ИБС, тромбоэмболия и осложнения, вызванные задержкой жидкости в организме; повышенная чувствительность к производным эстрадиола и/или азотистого иприта.
Резюме и дополнительные сведения
Больные, получающие лечение эстрамустином должны находиться под наблюдением врача, имеющего опыт применения противоопухолевых препаратов.
С осторожностью следует назначать эстрамустин пациентам с тромбофлебитом, тромбозом или тромбоэмболическими нарушениями в анамнезе (особенно связанных с применением эстрогенов); при атеросклерозе сосудов головного мозга или коронарной патологии.
Из-за возможного снижения толерантности к глюкозе пациенты с сахарным диабетом должны находиться под строгим наблюдением в процессе лечения эстрамустином.
У пациентов с артериальной гипертензией необходим систематический контроль АД.
При применении эстрамустина возможна задержка жидкости в организме, поэтому пациенты с эпилепсией, мигренью или нарушениями функции почек в случае задержки жидкости, требуют особого внимания.
С осторожностью назначают эстрамустин пациентам с метаболическими поражениями костной ткани, сопровождающимися гиперкальциемией, а также пациентам с почечной недостаточностью, т.к. препарат может оказывать влияние на метаболизм кальция или фосфора.
С осторожностью назначают препарат пациентам с нарушениями функции печени, т.к. он может недостаточно метаболизироваться у таких пациентов. Требуется регулярный контроль лабораторных показателей функции печени.
Известно, что эстрамустин мутагенен, поэтому при его применении пациенты детородного возраста должны использовать надежные методы контрацепции.
Поскольку некоторые эндокринные функции и функции печени подвержены влиянию эстрогеносодержащих препаратов, это может отразиться на соответствующих значениях лабораторных показателей.
При приготовлении раствора следует избегать контакта эстрамустина с кожей. Если это произошло, следует тщательно промыть место контакта холодной водой с мылом и уничтожить использованные при этом материалы путём сжигания.
Передозировка
Симптомы: возможно усиление побочных эффектов, особенно со стороны пищеварительной системы.
Лечение: проводят промывание желудка и симптоматическую терапию. В течение 6 нед после передозировки эстрамустина следует контролировать картину крови и функциональное состояние печени.
Клинически значимые взаимодействия
Клинические исследования показали, что эстрогены повышают как терапевтическую активность, так и токсичность трициклических антидепрессантов возможно путем ингибирования их метаболизма.
Нельзя принимать эстрамустин одновременно с лекарственными средствами, содержащими кальций, магний или алюминий (в т.ч. с антацидами), а также одновременно с употреблением молока, молочных продуктов, поскольку возможно значительное снижение всасывания эстрамустина из-за образования нерастворимых солей с поливалентными ионами металлов.
При одновременном применении эстрамустина и ингибиторов АПФ повышается вероятность развития ангионевротического отека.
Для приготовления инъекционного раствора эстрамустина не рекомендуют использовать физиологический раствор из-за выпадения осадка.
Код АТХ
L01XX11
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Условия и сроки хранения
Препарат в форме капсул следует хранить в недоступном для детей месте при температуре не выше 25 °C. Срок годности - 5 лет.
Лиофилизированный порошок следует хранить в недоступном для детей месте при температуре не выше 25 °C. Срок годности - 3 года. Приготовленный раствор для инфузий необходимо использовать в течение 12 ч при хранении при комнатной температуре и в течение 24 ч при хранении при температуре от 2 до 8 °C.
Гестагены
Медроксипрогестерон (Medroxyprogesterone acetate)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
17-гидрокси-6(-метилпрегн-4-ен-3,20-диона) ацетат.
По химической структуре близок к производным прогестерона.
Терапевтический класс АТХ
Прогестагенное, контрацептивное, противоопухолевое средство.
Механизм действия
По основному виду действия является прогестином (гестагеном). Как гестагенное средство имеет применение при нарушениях менструального цикла, дисфункциональных маточных кровотечениях. Однако, основное применение препарат нашел как противоопухолевое средство при гормоночувствительных злокачественных опухолях, особенно при раке молочной железы и раке матки (эндометрия). Эффект связан не только с гестагенной, но и с антиэстрогенной, антиандрогенной и антиагонадотропной активностью. Противоопухолевое действие препарата связано с антилютеинизирующим эффектом, реализующимся через гипофиз: ингибирует синтез гонадотропинов, предотвращает созревание фолликула и овуляцию, способствует истончению эндометрия. Возможно проявление андрогенного и анаболического эффектов.
Фармакокинетика
Связывание с белками плазмы очень высокое (90-95%). Период полувыведения составляет 30 ч. Метаболизируется в печени. Выводится преимущественно с мочой в виде метаболита.
Показания к применению и режим дозирования
Препарат можно применять в виде монотерапии или в сочетании с антиэстрогенами или цитостатиками.
В качестве противоопухолевого средства медроксипрогестерона ацетат применяют главным образом для дополнительной и/или паллиативной терапии рецидивов и/или метастазов рака эндометрия и почки; для терапии гормоночувствительного рака молочной железы у женщин в постменопаузе.
Препарат применяют внутрь или внутримышечно.
Препарат медроксипрогестерона провераª выпускают в двух видах: а) таблетки Провераª и б) суспензия депо-провераª (150 мг препарата в 1 мл).
Таблетки провераª назначают внутрь при раке эндометрия и почки от 200 до 600 мг в день, при раке молочной железы - от 400 до 1200 мг в день. Эффект отмечается обычно через 8-10 нед от начала лечения.
Суспензию депо-провераª вводят внутримышечно при раке эндометрия и почки по 400-1000 мг 1 раз в неделю. При улучшении состояния дозу уменьшают до 400 мг и вводят 1 раз в месяц.
При раке молочной железы вводят по 500 мг ежедневно в течение 28 дней, затем по 500 мг 2 раза в неделю до сохранения эффекта.
При прогрессировании заболевания терапию медроксипрогестерона ацетатом прекращают.
Побочные эффекты
Возможные побочные явления и противопоказания в основном такие же, как при применении других гестагенов.
Возможно: увеличение массы тела. В редких случаях: тромбофлебит, тромбоэмболия ветвей лёгочной артерии, туннельный синдром запястья, алопеция, тошнота и рвота; отёки; маточные кровотечения; одышка; гиперемия в месте опухоли; гипергликемия; сыпь.
При использовании суспензии возможны уплотнения и стерильные абсцессы в месте введения.
Противопоказания
Повышенная чувствительность к мегестролу; тромбофлебит, тромбоэмболический синдром или инсульт в анамнезе; заболевания печени; вагинальные кровотечения неуточнённой этиологии; беременность и кормление грудью.
Беременность
Препарат противопоказан в период беременности. На фоне терапии: показано применение дополнительного метода контрацепции.
Кормление грудью
Препарат противопоказан в период кормления грудью.
Клинически значимые взаимодействия
При одновременном применении с аминоглютетимидом возможно уменьшение концентрации мегестрола в плазме, по-видимому, вследствие индукции микросомальных ферментов печени.
Гризеофульвин, фенобарбитал, фенитоин, рифампицин могут повышать клиренс прогестагенов.
Под влиянием прогестагенов возможно изменение эффективности гипогликемических препаратов.
Прогестагены могут ингибировать метаболизм циклоспорина, что приводит к увеличению его концентрации в плазме и повышению риска токсичности.
Резюме и дополнительные сведения
Больные, получающие терапию медрокиспрогестероном должны находиться под наблюдением врача, имеющего опыт работы с противоопухолевыми препаратами.
При подозрении на развитие тромбофилических состояний (тромбоэмболия ветвей лёгочной артерии, тромбоз почечных сосудов) необходимо немедленно отменить препарат. Необходима осторожность при эпилепсии, мигрени, астме, сердечной и почечной недостаточности, учитывая возможную задержку жидкости. С осторожность назначают при сахарном диабете и депрессивных состояниях.
На фоне приёма препарата возможно снижение уровня стероидов в плазме и моче, гонадотропинов, факторов VII, VIII, IX,X.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Формы выпуска: таблетки по 100; 200; 250; 400 мг (0,1; 0,2; 0,25; 0,4 г); суспензия для приёма внутрь, содержащая 500 мг в 1 мл; суспензия для внутримышечных инъекций (Депо-провераª) во флаконах по 3, 3 мл (500 мг или 150 мг в 1 мл) и по 6, 7 мл (1000 мг).
Антигормональные препараты
Антиандрогены
Флутамид (Flutamide)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
2-метил-N-[4-нитро-3-(трифторметил)фенил]пропанамид.
Терапевтический класс АТХ
Антиандрогенный нестероидный препарат с противоопухолевой активностью.
Механизм действия
Антиандрогенный препарат нестероидной структуры, обладающий противоопухолевой активностью. Конкурентно блокирует взаимодействие андрогенов с их клеточными рецепторами.
Механизм действия связан с ингибированием захвата андрогена и/или ингибированием связывания андрогена в ядрах клеток тканей-мишеней. Его способность препятствовать действию тестостерона на клеточном уровне является дополнением к медикаментозной "кастрации", вызываемой агонистами гонадотропин-рилизинг-гормона (ГнРГ).
Органами-мишенями фармакологического действия флутамида являются предстательная железа и семенные пузырьки. Флутамид не обладает эстрогенной, антиэстрогенной, прогестагенной и антигестагенной активностью.
Физико-химические свойства
Молекулярная масса - 276,21.
Фармакокинетика
После приёма внутрь препарат быстро и полностью абсорбируется из желудочно-кишечного тракта. Связывание с белками очень высокое (94-96% для флутамида; 92-94% для альфа-гидроксилированного метаболита). Препарат интенсивно биотрансформируется в печени. Идентифицированы по крайней мере 6 метаболитов; основной метаболит, обнаруженный в плазме -биологически активное альфа-гидроксилированное производное (2-оксифлутамид). Максимальная его концентрация в плазме достигается через 2 ч. Период полувыведения для альфа-гидроксилированного метаболита составляет 6 часов. У больных пожилого возраста период полувыведения составляет 8 ч после однократного введения и 9,6 ч при стабильной концентрации. Из организма препарат выводится преимущественно с мочой. Приблизительно 4,2% выделяются с калом в течение 72 ч.
При проведении диализа: из-за высокой степени связывания с белками маловероятно, что флутамид в значительных количествах удаляется при гемодиализе или перитонеальном диализе.
Показания к применению и режим дозирования
Лечение метастатического рака предстательной железы: в начале лечения в комбинации с агонистами ГнРГ; в качестве дополнительного лечения больных, уже получающих терапию агонистами ГнРГ; у больных с хирургической кастрацией; при непереносимости или неэффективности других видов гормонотерапии.
Обычная доза для взрослых: рак предстательной железы - внутрь, по 250 мг каждые 8 ч. В случае достижения положительного эффекта препарат применяют до появления признаков прогрессирования опухолевого заболевания. В случае сочетанной терапии с агонистами ГнРГ оба препарата могут быть назначены одновременно, или приём флутамида начинают за 3 дня до первого приёма агониста ГнРГ.
Побочные эффекты
Признаки поражения эндокринной системы: часто (10% и более) - гинекомастия и/или боли в области грудных желез, иногда сопровождающиеся галактореей (эти явления исчезают при прекращении приёма или после снижения дозы); редко (менее 1%) - снижение либидо; при длительном лечении отмечено подавление сперматогенеза.
Признаки поражения пищеварительной системы: иногда (от 1% до 10%) - диарея, тошнота, рвота, повышение аппетита, транзиторное нарушение функции печени, гепатит; редко - анорексия, изжога, запор, диспепсия, желтуха в (т.ч. холестатическая), некроз печени, печёночная энцефалопатия, повышение активности трансаминаз.
Признаки поражения ЦНС: иногда - бессонница, утомляемость; редко - головная боль, головокружение, слабость, нарушение остроты зрения, тревога, депрессия.
Признаки поражения системы кроветворения: редко - тромбоцитопения; в отдельных случаях - гемолитическая анемия, макроцитарная анемия, метгемоглобинемия.
Дерматологические реакции: редко - подкожные кровоизлияния, зуд; в отдельных случаях - фотосенсибилизация (включая эритему, изъязвление кожи, эпидермальный некролиз).
Прочие: редко - повышение АД, жажда, боль в грудной клетке, отеки (пальцев, стоп, голеней), волчаночноподобный синдром, изменение окраски мочи от янтарной до желто-зеленой.
При применении в комбинации с агонистами ГнРГ:
Признаки поражения эндокринной системы: часто - приливы, снижение либидо, импотенция; иногда - гинекомастия.
Признаки поражения пищеварительной системы: часто - диарея, тошнота, рвота; иногда - отсутствие аппетита; редко - гепатит, холестатическая желтуха, печёночная недостаточность, некроз печени, печёночная энцефалопатия.
Признаки поражения системы кроветворения: иногда - анемия, лейкопения, тромбоцитопения.
Признаки поражения ЦНС и периферической нервной системы: иногда - симптомы нервно-мышечных расстройств (оцепенение, покалывание, боль или мышечная слабость в руках, кистях, ступнях, ногах), сонливость, депрессия, спутанность сознания, тревога, невроз.
Признаки поражения сердечно-сосудистой системы: иногда - артериальная гипертензия.
Признаки поражения дыхательной системы: редко - нарушения дыхания.
Дерматологические реакции: редко - фотосенсибилизация.
Прочие: иногда - отеки, затрудненное мочеиспускание; редко - метгемоглобинемия.
Передозировка
Симптомы: усугубление побочного действия.
Лечение: следует вызвать рвоту. Необходимо применять симптоматическую терапию при постоянном контроле жизненно важных функций организма.
Противопоказания
Выраженные нарушения функции печени.
Повышенная чувствительность к флутамиду и другим компонентам препарата.
С осторожностью следует применять флутамид у больных со сниженной функцией печени, при склонности к тромбозам и при сердечно-сосудистых заболеваниях, а также при состояниях, предрасполагающих к интоксикации анилином (один из метаболитов флутамида - метиланилиновое производное): дефицит глюкозо-6-фосфатдегидрогеназы, курение, гемоглобинопатия (метгемоглобин).
Резюме и дополнительные сведения
Больные, принимающие флутамид, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии рака.
Лечение флутамидом следует начинать одновременно с применением аналога гонадотропин релизинг гормонов.
Лечение флутамидом следует проводить под контролем активности печёночных ферментов (соответствующие лабораторные анализы следует проводить 1 раз в месяц в течение первых 4 мес и далее - регулярно).
В случае повышения активности печёночных ферментов в 2-3 раза по сравнению с верхним пределом нормальных значений и/или появления желтухи при отсутствии поражения печени применение флутамида следует прекратить.
Больные должны получить рекомендацию незамедлительно обратиться к врачу при появлении первых симптомов нарушения функции печени, таких как кожный зуд, потемнение мочи, тошнота, рвота, стойкая потеря аппетита, желтая окраска кожи или белков глаз, болезненные ощущения в правом подреберье, гриппоподобные симптомы.
Ввиду возможного усиления противосвёртывающего действия при одновременном применении антикоагулянтов непрямого действия и флутамида дозу антикоагулянта следует подбирать под контролем протромбинового времени.
Использование у людей пожилого возраста: период полувыведения увеличен, но меры предосторожности не требуются.
Клинически значимые взаимодействия
При одновременном применении флутамида и антикоагулянтов непрямого действия возможно усиление противосвёртывающего действия.
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки светло-желтого цвета, гладкие, круглые, двояковыпуклые по 250 мг 20 шт. - блистеры (5) - пачки картонные.
Код АТХ
L02BB01
Упаковка и хранение: Хранить при температуре ниже 40 °С, предпочтительно при 15-30 °С, в хорошо закрытой упаковке, если производитель не предписывает иначе.
Ципротерон (Cyproterone)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(1бета,2бета)-6-хлор-1,2-дигидро-17-гидрокси-3’Н-циклопропа[1,2]прегна-1,4,6-триен-3,20-дион.
Терапевтический класс АТХ
Антиандрогенный препарат.
Механизм действия
Антиандрогенный препарат для приёма внутрь. Тормозит воздействие мужских половых гормонов (андрогенов), в незначительных количествах вырабатываемых также и организмом женщины. Обладает гестагенным, антиандрогенным и антигонадотропным действием.
У мужчин на фоне приёма препарата наблюдается ослабление полового влечения и потенции, а также снижение функции семенников. Эти изменения после прекращения лечения исчезают. Препарат уменьшает или полностью устраняет влияние андрогенов на органы-мишени (в т.ч. на предстательную железу).
У женщин при приёме ципротерона ацетата уменьшается как патологически избыточный рост волос на лице и теле, так и вызываемое андрогенами выпадение волос на голове. Кроме того, снижается повышенная функция сальных желёз и тормозится на протяжении периода лечения функция яичников.
Фармакокинетика
После приёма препарата внутрь ципротерона ацетат полностью абсорбируется из желудочно-кишечного тракта. После приёма 10 мг Cmax достигается через 1,5 ч и составляет 75 нг/мл, после приёма 50 мг - 140 мг/мл. После приёма таблетки 100 мг Cmax достигается в среднем через 2,8±1,1 ч. Биодоступность составляет 88%. Связывание с белками плазмы очень высокое и составляет около 96%. Биотрансформируется препарат в печени путём гидроксилирования и конъюгации, основной метаболит, определяемый в плазме крови человека, - 15b-гидроксильное производное. Период полувыведения для таблеток 10 мг и 50 мг равен 43,9±12,8 ч, для 100 мг - 42,8±9,7 ч. Выводится с жёлчью и мочой преимущественно в виде метаболитов в соотношении 3:7.
Показание к применению и режим дозирования
Таблетки, содержащие 100 мг ципротерона ацетата:
У мужчин: метастатический или неоперабельный рак предстательной железы (без и после орхиэктомии, а также в сочетании с агонистами гонадотропин-рилизинг гормона (ГнРГ).
При лечении антиандрогенами при неоперабельном раке предстательной железы назначают препарат в дозе 100 мг 2-3 раза в сутки. Независимо от того, наблюдается улучшение состояния пациента или ремиссия заболевания, необходимо продолжать приём препарата в предписанной дозе.
С целью уменьшения повышенной продукции мужских половых гормонов в начале лечения агонистами ГнРГ в начале назначают препарат в дозе 100 мг 2 раза/сут в течение 5-7 дней, затем в последующие 3-4 нед - в той же дозе в комбинации с агонистом ГнРГ.
Таблетки андрокурª принимают внутрь после еды, запивая небольшим количеством жидкости.
Побочные эффекты
Признаки поражения опорно-двигательного аппарата: у мужчин редко - остеопороз.
Признаки поражения эндокринной системы: приём ципротерона в течение нескольких недель у мужчин ведет к снижению способности к оплодотворению (подавление сперматогенеза, обратимое снижение либидо и потенции), которая полностью восстанавливается через 3-4 мес после прекращения приёма препарата; в единичных случаях - гинекомастия, иногда в сочетании с повышением тактильной чувствительности сосков грудных желез. У женщин иногда - чувство напряжения в молочных железах, изменение массы тела.
Комбинированная терапия с ципротероном вызывает подавление овуляции и препятствует зачатию.
Признаки поражения ЦНС: при применении таблеток 100 мг в начале терапии возможны повышенная утомляемость, апатия, беспокойство, снижение способности к концентрации внимания.
Признаки поражения пищеварительной системы: при применении таблеток 100 мг в начале терапии возможны тошнота, боли в животе; в единичных случаях - нарушения функции печени.
Прочие: при применении таблеток 100 мг в начале терапии возможна сухость кожи; в единичных случаях при применении в высоких дозах - чувство нехватки воздуха.
Передозировка
Исследования острой токсичности ципротерона показали, что его можно отнести к веществам с очень низкой токсичностью.
При случайном приёме внутрь нескольких таблеток развития интоксикации ожидать не следует.
Противопоказания
Применение препарата противопоказано при заболеваниях печени, сопровождающихся развитием желтухи; постоянном зуде; синдроме Дубина-Джонсона; синдроме Ротора; имеющихся или ранее перенесённых опухолях печени (при карциноме предстательной железы - только в случаях, если опухоль не обусловлена метастазами); кахексии (за исключением пациентов с карциномой предстательной железы); тяжелых хронических депрессиях; предшествующих или существующих тромбоэмболических процессах; тяжелом диабете с сосудистыми осложнениями; серповидно-клеточной анемии. В период беременности и грудного вскармливания. Повышенная чувствительность к препарату.
Клинически значимые взаимодействия
При одновременном применении с ципротероном возможно изменение эффективности гипогликемических лекарственных средств и инсулина.
Антиандрогенное действие ципротерона ацетата усиливается при его совместном применении с агонистами ГнРГ, под действием ципротерона ацетата уменьшается первоначальное повышение выработки тестостерона агонистами ГнРГ.
Резюме и дополнительные сведения
У больных с карциномой предстательной железы и наличием тяжелого диабета с изменениями сосудов, серповидно-клеточной анемией или предшествовавшими тромбоэмболическими явлениями при решении вопроса о назначении препарата андрокурª необходимо индивидуально взвесить возможные пользу и риск развития негативных последствий лечения.
Пациенты перед началом терапии ципротероном должны пройти общемедицинское, а пациентки - дополнительно гинекологическое обследование для исключения беременности.
При одновременном употреблении алкоголя, оказывающего растормаживающее действие, у пациентов с патологически повышенным половым влечением может наблюдаться снижение эффекта терапии ципротероном.
В период лечения препаратом необходим тщательный контроль функции печени и картины периферической крови.
Пациенты, деятельность которых требует повышенного внимания, должны учитывать, что при приёме ципротерона может наблюдаться повышенная утомляемость, вялость, снижение способности к концентрации внимания.
Код АТХ
G03HA01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки по 0,05 г (50 мг) в упаковке по 50 штук.
Условия и сроки хранения
Специальных требований к условиям хранения нет. Срок годности - 5 лет.
Финастерид (Finasteride)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
N-трет-Бутил-3-оксо-4-аза-5альфа-андрост-1-ен-17бета-карбоксамид.
Терапевтический класс АТХ
Препарат для лечения доброкачественной гиперплазии предстательной железы
Фармакологическое действие
Антиандроген, синтетическое 4-азастероидное соединение. Конкурентный и специфический ингибитор 5-альфа-редуктазы - внутриклеточного фермента, который превращает тестостерон в активный андроген 5-дигидротестостерон (ДГТ). Рост ткани предстательной железы и развитие доброкачественной гиперплазии обусловлены превращениями тестостерона в дигидротестостерон в клетках предстательной железы. Под воздействием препарата происходит значительное снижение концентрации дигидротестостерона как в плазме, так и в ткани железы. Финастерид не связывается с андрогенными рецепторами.
Препарат угнетает стимулирующее действие дигидротестостерона на развитие аденомы предстательной железы, в результате уменьшается выраженность симптомов, связанных с аденомой предстательной железы.
Препарат не оказывает влияния на уровень липидов плазмы и уровень кортизола, эстрадиола, пролактина, ТТГ, тироксина.
Фармакокинетика
После приёма препарата внутрь финастерид быстро абсорбируется из желудочно-кишечного тракта. Биодоступность составляет около 80% и не зависит от приёма пищи. Максимальная концентрация в плазме достигается через 1-2 ч после однократного приёма препарата внутрь. Связывание с белками плазмы высокое (около 90%). Финастерид метаболизируется в печени и выводится в виде метаболитов почками (приблизительно 40%) и через кишечник (около 60%). Период полувыведения финастерида составляет около 6 ч., у пациентов старше 70 лет данный показатель может увеличиваться до 8 ч.
Показания к применению и режим дозирования
Лечение доброкачественной гиперплазии предстательной железы с целью: уменьшения размеров предстательной железы; увеличения максимальной скорости оттока мочи и уменьшения симптомов, связанных с гиперплазией; снижения риска возникновения острой задержки мочи и связанной с этим вероятности хирургического вмешательства.
Финастерид назначают по 5 мг 1 раз в сутки, независимо от приёма пищи.
Продолжительность терапии до оценки ее эффективности должна быть не менее 6 мес. Приблизительно у 50% больных исчезновение клинических симптомов происходило лишь при лечении в течение 12 мес.
Побочные эффекты
Признаки поражения эндокринной системы: 3-4% - гинекомастия, импотенция, снижение либидо, уменьшение объема эякулята (частота этих эффектов уменьшается в процессе лечения); в отдельных случаях - повышение уровня ЛГ, ФСГ и тестостерона приблизительно на 10%, однако эти показатели оставались в пределах нормальных величин.
Аллергические реакции: возможны ангионевротический отек губ, кожная сыпь.
Передозировка
Данные о передозировке препарата не предоставлены.
Противопоказания
Повышенная чувствительность к финастериду или другим компонентам препарата.
Клинически значимые взаимодействия
Данные о лекарственном взаимодействии препарата не предоставлены.
Резюме и дополнительные сведения
До начала терапии необходимо исключить заболевания с симптомами сходными с проявлениями доброкачественной гиперплазии предстательной железы, такие как рак предстательной железы, инфекционный простатит, стриктура уретры, гипотоничный мочевой пузырь и ряд изменений со стороны мочевыводящей системы, возникающих при некоторых заболеваниях нервной системы.
С осторожностью назначают препарат пациентам с нарушениями функции печени.
Поскольку при применении финастерида наблюдается снижение простатоспецифичного антигена, периодически в процессе терапии необходимо производить обследование пациентов для исключения у них рака предстательной железы.
Код ATX
G04CB01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки по 0,005 г (5 мг) (N. 10, 28, 30).
Условия и сроки хранения
Препарат следует хранить в недоступном для детей, защищенном от света месте, при температуре от 15 ° до 30 °С. Срок годности - 3 года.
Бикалутамид (Bicalutamide)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(±)-4-циано-альфа,альфа,альфа-трифтор-3-((n-фторфенил)сульфонил)-2-метил-м-лактотолуидид.
Терапевтический класс АТХ
Антиандрогенный нестероидный препарат с противоопухолевой активностью.
Механизм действия
Антиандрогенный нестероидный препарат. Представляет собой рацемическую смесь, причем антиандрогенной активностью обладает преимущественно ®-энантиомер. Бикалутамид связывается с андрогенными рецепторами и, не активируя при этом экспрессию генов, подавляет стимулирующее влияние андрогенов. В результате этого происходит регрессия новообразований предстательной железы. У некоторых пациентов прекращение приёма бикалутамида может привести к развитию клинического "синдрома отмены антиандрогенов". При применении бикалутамида в суточной дозе 150 мг ежедневно для лечения пациентов с местно-распространенным (ТЗ-Т4, любое N, М0 или любое Т, N+, М0) раком предстательной железы, в качестве гормональной терапии или в качестве адъювантной терапии, значительно снижается риск прогрессирования заболевания и метастазов в кости.
Фармакокинетика
После приёма внутрь быстро и полностью всасывается из желудочно-кишечного тракта. Одновременный приём пищи не влияет на абсорбцию. При ежедневном приёме бикалутамида концентрация ®-энантиомера в плазме увеличивается примерно в 10 раз вследствие длительного периода полувыведения, что позволяет принимать бикалутамид 1 раз в сутки. Связь с белками плазмы высокая (для рацемической смеси 96%, для ®-энантиомера 99,6%). Средняя концентрация ®-энантиомера в сперме мужчин, получавших бикалутамид 150 мг, составляет 4,9 мкг/мл. Препарат интенсивно метаболизируется в печени путем окисления и образования конъюгатов с глюкуроновой кислотой. Метаболиты выводятся с мочой и жёлчью примерно в равных соотношениях. На фармакокинетику ®-энантиомера не влияют возраст, нарушение функции почек, легкое и умеренное нарушение функции печени. У пациентов со средними и тяжелыми нарушениями функции печени может наблюдаться кумуляция бикалутамида в организме.
Показания к применению и режим дозирования
Таблетки 50 мг: распространённый рак предстательной железы (в комбинации с аналогом гонадотропин-рилизинг гормона (ГнРГ) или с хирургической кастрацией);
Таблетки 150 мг: местно-распространённый рак предстательной железы (Т3-Т4, N±, М0; Т1-Т2, N+, М0) в качестве монотерапии или адъювантной терапии в сочетании с радикальной простатэктомией или радиотерапией; местно-распространённый неметастатический рак предстательной железы в качестве монотерапии в случаях, когда хирургическая кастрация или другие медицинские вмешательства неприемлемы или неприменимы.
Бикалутамид назначают взрослым мужчинам (в т.ч. пожилого возраста) при распространённом раке предстательной железы в комбинации с аналогом ГнРГ или с хирургической кастрацией в дозе 50 мг 1 раз в сутки. Лечение необходимо начинать одновременно с началом приёма аналога ГнРГ или хирургической кастрацией.
При местно-распространенном раке предстательной железы бикалутамид назначают в дозе 150 мг 1 раз в сутки. При появлении признаков прогрессирования заболевания приём препарата следует прекратить.
Пациентам с нарушениями функции почек и с незначительными нарушениями функции печени коррекции дозы не требуется.
Побочные эффекты
Бикалутамид хорошо переносится большинством больных, и лишь в редких случаях его приходится отменять из-за вызванных им побочных эффектов.
Фармакологическое действие бикалутамида может обуславливать следующие побочные эффекты:
очень часто (³10%): гинекомастия (может сохраняться даже после прекращения терапии, особенно в случае приёма препарата в течение длительного времени), болезненность грудных желез, приливы жара;
часто (1-10%): диарея, тошнота, транзиторное повышение активности печёночных трансаминаз, холестаз и желтуха (описанные изменения функции печени редко оценивались как серьезные, носили транзиторный характер и полностью исчезали или уменьшались несмотря на продолжение терапии или же после ее прекращения), зуд, астения; при применении препарата в суточной дозе 150 мг - алопеция или восстановление роста волос, снижение полового влечения, сексуальные дисфункции, увеличение массы тела;
редко (0,1-1%): реакции повышенной чувствительности, включая ангионевротический отек и крапивницу, интерстициальные легочные заболевания; при применении препарата в суточной дозе 150 мг - боль в животе, депрессия, диспепсия, гематурия;
очень редко (0,01-0,1%): рвота, сухость кожи (при применении препарата в суточной дозе 150 мг сухость кожи наблюдается часто), печёночная недостаточность (причинно-следственная связь с приёмом бикалутамида не установлена).
При одновременном применении бикалутамида и аналогов ГнРГ могут наблюдаться также следующие побочные эффекты с частотой ³1% (причинно-следственная связь с приёмом препарата не установлена, некоторые из отмеченных эффектов часто возникают у пожилых больных без приёма бикалутамида):
Признаки поражения сердечно-сосудистой системы: сердечная недостаточность.
Признаки поражения пищеварительной системы: анорексия, сухость во рту, диспепсия, запор, метеоризм.
Признаки поражения ЦНС: головокружение, головная боль, бессонница, сонливость.
Признаки поражения дыхательной системы: одышка.
Признаки поражения мочеполовой системы: сексуальная дисфункция, никтурия.
Признаки поражения системы кроветворения: анемия.
Дерматологические реакции: алопеция, сыпь, усиление потоотделения, гирсутизм.
Признаки нарушения обмена веществ: сахарный диабет, гипергликемия, отеки, увеличение или уменьшение массы тела.
Прочие: боль в животе, боль в груди, боль в области таза, озноб.
Передозировка
Случаи передозировки у человека не описаны. Специфического антидота не существует, поэтому при необходимости проводят симптоматическую терапию. Диализ неэффективен, поскольку бикалутамид прочно связывается с белками и не выводится с мочой в неизмененном виде. Показана общая поддерживающая терапия и мониторинг жизненноважных функций организма.
Противопоказания
Противопоказан одновременный приём с терфенадином, астемизолом, цизапридом.
Повышенная чувствительность к бикалутамиду и другим компонентам препарата.
Бикалутамид не назначают женщинам и детям.
С осторожностью применяют касодексª у пациентов с нарушениями функции печени.
Резюме и дополнительные сведения
Учитывая возможность замедления выведения и кумуляции бикалутамида у больных с нарушением функции печени, целесообразно периодически оценивать функцию печени. Большинство изменений функции печени встречаются в течение первых 6 мес лечения бикалутамидом. В случае развития выраженных изменений функции печени приём препарата необходимо прекратить.
У пациентов с прогрессированием заболевания на фоне повышения уровни простатоспецифичного антигена (ПСА) необходимо рассмотреть вопрос о прекращении лечения бикалутамидом.
При назначении бикалутамида пациентам, получающим антикоагулянты кумаринового ряда, рекомендуется регулярно контролировать протромбиновое время.
Учитывая возможность ингибирования бикалутамидом активности цитохрома Р450 (CYP 3А4) следует проявлять осторожность при одновременном назначении бикалутамида с препаратами, преимущественно метабилизирующимися с участием CYP 3A4.
Пациентов с непереносимостью лактозы необходимо проинформировать о том, что каждая таблетка бикалутамида 50 мг содержит 61 мг, а 150 мг - 183 мг моногидрата лактозы соответственно.
Бикалутамид не влияет па способность пациентов управлять транспортными средствами или заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Клинически значимые взаимодействия
Нет данных о фармакодинамических или фармакокинетических взаимодействиях между бикалутамидом и аналогами ГнРГ.
В исследованиях in vitro показано, что ®-энантиомер бикалутамида является ингибитором CYP3A4, в меньшей степени CYP2C9, CYP2C19, CYP2D6. Потенциальной способности бикалутамида к взаимодействию с другими лекарственными средствами не обнаружено. Однако при использовании бикалутамида в течение 28 дней на фоне приёма мидазолама АUC мидазолама увеличивалась на 80%.
Противопоказано одновременное применение бикалутамида с такими препаратами как терфенадин, астемизол и цизаприд.
Следует соблюдать осторожность при назначении бикалутамида одновременно с циклоспорином или блокаторами кальциевых каналов. Возможно потребуется снижение дозы этих препаратов, особенно в случае потенцирования или развития нежелательных реакций. После начала использования или отмены бикалутамида рекомендуют проводить тщательный мониторинг концентрации циклоспорина в плазме крови и клинического состояния пациента.
Одновременное назначение бикалутамида и препаратов, угнетающих микросомальное окисление лекарственных средств (циметидин, кетоконазол), может привести к увеличению концентрации бикалутамида в плазме и, возможно, к увеличению частоты возникновения нежелательных реакций. Бикалутамид может вытеснять антикоагулянт кумаринового ряда варфарин из участков его связывания с белками.
Код ATX
L02BB03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки, покрытые оболочкой белого цвета, круглые, двояковыпуклые по 0,05 и 0,15 г (N. 28).
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 30 °C. Срок годности таблеток 50 мг - 5 лет, таблеток 150 мг - 4 года.
Антиэстрогены
Тамоксифен (Tamoxifen)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(Z)-2-[4-(1,2-дифенил-1-бутенил)фенокси]-N,N-диметилэтанамин (в виде цитрата).
Терапевтический класс АТХ
Противоопухолевое средство. Гормональный препарат, антиэстроген.
Физико-химические свойства
Молекулярная масса - 563,65. рКа - 8,85.
Механизм действия
Тамоксифен - нестероидные антиэстрогенный препарат, обладающий также слабыми эстрогенными свойствами. Точный механизм его противоопухолевого действия неизвестен, но может быть связан с антиэстрогенными эффектами; тамоксифен блокирует захват эстрадиола.
Другие эффекты
Тамоксифен может вызывать овуляцию у женщин с отсутствием последней, стимулируя высвобождение из гипоталамуса гонадотропин-рилизинг-гормона, который, в свою очередь, стимулирует высвобождение гонадотропных гормонов гипофиза. У мужчин с олигоспермией тамоксифен повышает концентрации ЛГ и ФСГ, тестостерона и эстрогенов в сыворотке крови. Тамоксифен и некоторые его метаболиты (N-десметилтамоксифен, 4-гидрокситамоксифен) являются сильными ингибиторами оксидаз смешанной функции системы цитохрома Р450 печени; однако клиническое значение этих эффектов не определено.
Фармакокинетика
Биотрансформация происходит в печени. Длительное сохранение в крови и выведение через кишечник объясняется кишечно-печёночной циркуляцией. Период полувыведения: фаза распределения от 7 до 14 ч; вторичные максимумы через 4 дня или более могут быть обусловлены кишечно-печёночной циркуляцией; фаза выведения может превышать 7 дней. Начало действия: объективно определяемая реакция обычно отмечается через 4-8 нед лечения, но у больных с метастазами в костях возможна и через несколько месяцев. Длительность действия: способность блокировать эстрогены может сохраняться в течение нескольких недель после однократной дозы. Выведение: основной путь - с жёлчью, через кишечник преимущественно в виде метаболитов; небольшое количество препарата выводится почками.
Показания к применению и режим дозирования
Рак молочной железы: тамоксифен применяют для адъювантной терапии рака молочной железы без или с поражением подмышечных лимфатических узлов у женщин в постменопаузе после хирургического лечения.
Тамоксифен применяют для лечения диссеминированного рака молочной железы у женщин и рака грудной железы у мужчин.
Рак почки, меланома (содержащая эстрогенные рецепторы), рак яичников, рак предстательной железы при резистентности к другим препаратам.
Примечание: оценка содержания рецепторов эстрогенов и прогестерона в опухолевой ткани может помочь в прогнозировании вероятности лечебных эффектов адъювантной терапии тамоксифеном при раке молочной железы с поражением или без поражения лимфатических узлов. Терапевтический эффект тамоксифена более вероятен у женщин, у которых опухоли содержат рецепторы стероидных гормонов.
Режим дозирования устанавливают индивидуально, в зависимости от показаний, состояния пациента и применяемой схемы противоопухолевой терапии.
Рак молочной железы: внутрь, по 20 мг в сутки, длительно; при раке почки: в высоких дозах: по 60 мг в сутки, длительно.
Побочные эффекты
Хотя информация ограничена, по-видимому, характер побочных эффектов у мужчин сходен с таковым у женщин.
Более частые (в 10-20% случаев)
Только у женщин: "приливы"; увеличение массы тела -следствие эстрогенного эффекта.
Менее частые
Как у женщин, так и у мужчин: головная боль; слабая тошнота и/или рвота; кожная сыпь или сухость кожи; временное местное обострение болезни (боль в костях).
Реакция "вспышки": временное местное обострение болезни может проявляться увеличением размеров имевшихся поражений у больных с поражением кожи и мягких тканей, иногда сопровождающимся выраженной эритемой пораженных участков и прилежащих областей и/или развитием новых очагов поражения, а также усиление и/или появление болей в костях или другое обострение болезни обычно отмечается вскоре после начала лечения, но обычно оно проходит через 1-2 нед при продолжении лечения тамоксифеном. В это время может потребоваться применение анальгезирующих средств.
Только у женщин: изменения менструального цикла; зуд половых органов; выделения из влагалища.
Только у мужчин: импотенция или снижение полового влечения.
Редкие
Как у женщин, так и у мужчин: спутанность сознания; гепатотоксическое действие; токсическое действие на органы зрения, включая ретинопатию, кератопатию, катаракту и ретробульбарный неврит; эмболия лёгочной артерии; тромбоз; слабость или сонливость.
Примечание: гепатотоксическое действие обычно проявляется повышением активности ферментов печени. Однако отмечались и более тяжелые эффекты, включая жировую инфильтрацию печени, холестаз и гепатит.
Токсическое действие на органы зрения может быть обратимым или необратимым после отмены тамоксифена. Необходимо проведение офтальмологического исследования до лечения тамоксифеном и периодически во время лечения для выявления субклинического токсического действия и решения вопроса об отмене тамоксифена на его ранних стадиях.
Только у женщин: гиперплазия эндометрия, полипы или рак тела матки.
Передозировка
Симптомы передозировки проявляются усилением антиэстрогенных ("приливы") или эстрогенных эффектов (вагинальные кровотечения).
Лечение: симптоматическое.
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу: катаракта или нарушения зрения; тромбофлебит; гиперлипидемия; лейкопения; тромбоцитопения. Повышенная чувствительность к тамоксифену.
Беременность
Хотя адекватных и строго контролируемых исследований у человека не проведено, сообщалось о случаях самопроизвольного аборта, пороков развития, гибели плода и влагалищного кровотечения. В связи с эстрогенным эффектом тамоксифена следует иметь в виду вероятность развития диэтилстильбэстролподобного синдрома у девочек, матери которых принимали тамоксифен во время беременности.
В период лечения тамоксифеном рекомендуется применение механического или негормонального противозачаточного средства.
Кормление грудью
Проникает ли тамоксифен в грудное молоко, неизвестно. Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограниченна, во время проведения химиотерапии грудное вскармливание не рекомендуется из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны на основе их потенциальной клинической значимости.
Комбинации, содержащие любое из перечисленных веществ, в зависимости от имеющегося количества, могут также взаимодействовать с данным препаратом.
Антацидные средства, циметидин, фамотидин или ранитидин: данные препараты повышают значение рН в желудке и, следовательно, могут вызывать преждевременное растворение и потерю защитного эффекта кишечнорастворимой оболочки; между применением антацидного средства и таблеток тамоксифена, покрытых кишечнорастворимой оболочкой, необходим интервал 1-2 ч; кроме того, следует учитывать вероятность того, что одновременное применение таких лекарственных форм тамоксифена с циметидином, фамотидином или ранитидином не будет обеспечивать более эффективную защиту слизистой оболочки желудка от раздражения или изъязвления, чем использование только блокаторов Н2-рецепторов);
При одновременном применении с антикоагулянтами производными кумарина повышается риск усиления антикоагуляторного действия; у пациентов, получающих тамоксифен, при применении варфарина возникает риск угрожающей клинической ситуации: пролонгирование протромбинового времени, гематурия, гематома;
При одновременном применении с цитостатиками возможно повышение риска тромбообразования; использование с митомицином повышает риск гемолитико-уремического синдрома;
Совместное применение с аллопуринолом потенцирует гепатотоксическое действие; с аминоглутетимидом - уменьшение концентрации тамоксифена в плазме, по-видимому, за счёт повышения его метаболизма;
У пациентов, получающих тамоксифен, возможно пролонгирование нервно-мышечной блокады, вызванной атракурия безилатом;
Возможно уменьшение концентрации тамоксифена в плазме крови, что обусловлено индукцией изофермента CYPЗA4 под действием рифампицина;
Эстрогены: могут снижать терапевтический эффект тамоксифена.
Резюме и дополнительные сведения
Больные, получающие тамоксифен, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии рака.
Если побочные эффекты выражены, дозу можно снизить без потери влияния на течение заболевания.
При появлении тяжелой гиперкальциемии тамоксифен следует отменить.
При появлении нарушений зрения рекомендуется провести офтальмологическое исследование и в случаях выявления ретинопатии или кератопатии рассмотреть возможность отмены тамоксифена.
Тамоксифен вызывает овуляцию, что повышает риск беременности у женщин.
Исследований зависимости эффекта тамоксифена от возраста у пожилых людей не проведено. Однако данный препарат широко применяют у пожилых больных, и специфических гериатрических проблем, которые ограничивали бы применение тамоксифена у больных пожилого возраста, не зарегистрировано и не предполагают.
Особенно важным в наблюдении за больными может быть следующее: определение концентрации кальция в сыворотке крови: рекомендуется у больных с метастазами в костях; определение концентрации холестерина в сыворотке крови; определение концентраций триглицеридов в сыворотке крови: могут быть рекомендованы периодически у больных с ранее отмечавшейся гиперлипидемией; клинические анализы крови: могут быть целесообразны периодически, хотя лейкопения и тромбоцитопения не были достоверно связаны с действием тамоксифена; гинекологическое обследование: рекомендуется регулярно у женщин, принимающих тамоксифен, для выявления возможного рака тела матки.
Код АТХ
L02BA01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Выпускается в виде цитрата.
Форма выпуска: таблетки, покрытые плёночной оболочкой по 0,01 г (10 мг); 0,02 г (20 мг); 0,04 г (40 мг).
Упаковка и хранение
Хранить при температуре ниже 40 °С, предпочтительно при 15-30 °С, в плотно закрытой упаковке, если производителем не указано иначе. Защищать от света.
Дополнительная маркировка
Глотать таблетки целиком.
Не принимать антацидные средства в течение 1-2 ч после приёма данного препарата.
Торемифен (Тоreмifеn)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
(Z)-2-[4-(4-хлор-1,2-дифенил-1-бутенил)фенокси]-N,N-диметилэтанамин (в виде цитрата).
Терапевтический класс АТХ
Антиэстрогенный препарат с противоопухолевым действием
Механизм действия
Противоопухолевый антиэстрогенный нестероидный препарат, производное трифенилэтилена. Торемифен специфически связывается с эстрогенными рецепторами, конкурируя с эстрадиолом, ингибирует вызванный эстрогенами синтез ДНК и репликацию клеток. В высоких дозах торемифен может оказывать противоопухолевый эффект, не связанный с эстрогенозависимым действием. У больных раком молочной железы противоопухолевое действие торемифена в основном связано с его антиэстрогенной активностью, хотя нельзя исключить и другие механизмы (регуляция экспрессии онкогена, секреции фактора роста, индукция апоптоза, влияние на кинетику клеточного цикла).
Фармакокинетика
После приёма внутрь торемифен полностью абсорбируется из желудочно-кишечного тракта. Максимальная концентрация в плазме достигается через 3 ч (2-5 ч). Приём пищи не оказывает влияния на полноту абсорбции. Связывание с белками плазмы (главным образом с альбумином) очень высокое - 99,5%. Торемифен метаболизируется в печени путем гидроксилирования и деметилирования при участии изофермента CYP3A4 с образованием активного метаболита - N-деметилторемифена. Средний период полувыведения N-деметилторемифена - 11 сут (4-20 сут). Выводится через кишечник, в основном в виде метаболитов; около 10% - почками.
Показания к применению и режим дозирования
Эстрогенозависимый рак молочной железы у женщин в постменопаузальном периоде. Назначают внутрь. Режим дозирования устанавливается индивидуально. В качестве стандартной дозы для первой линии гормонотерапии рекомендуется приём в дозе 60 мг ежедневно длительно. При назначении торемифена в качестве второй линии гормонального лечения доза препарата может быть увеличена до 240 мг/сут (по 120 мг 2 раза/сут). При появлении признаков прогрессирования заболевания приём препарата отменяют.
Побочные эффекты
Эффекты, обусловленные антиэстрогенным действием: наиболее часто - приступообразные ощущения жара (приливы), повышенная потливость, влагалищные кровотечения или выделения, повышенная утомляемость, тошнота, сыпь, зуд в области гениталий, задержка жидкости, головокружение, депрессия. Эти эффекты выражены обычно в легкой степени.
Признаки поражения эндокринной системы: редко - увеличение массы тела.
Признаки поражения пищеварительной системы: редко - анорексия, рвота, запор.
Признаки поражения ЦНС: редко - головная боль, бессонница, повышение уровня трансаминаз; в отдельных случаях - тяжелые нарушения функции печени (желтуха).
Признаки поражения органа зрения: редко - нарушение зрения, включая изменения роговицы, катаракту.
Признаки поражения сердечно-сосудистой системы: редко - тромбоз глубоких вен, эмболия легочной артерии.
Дерматологические реакции: редко - кожная сыпь, алопеция.
Прочие: редко - одышка.
У пациенток с метастазами в кости отмечались случаи развития гиперкальциемии в самом начале лечения.
Повышается риск изменений эндометрия, таких как гиперплазия, полипоз и рак. Это может быть вызвано фармакологическим свойством препарата - эстрогенной стимуляцией.
Противопоказания
Гиперплазия эндометрия (в т.ч. в анамнезе); тяжелая печёночная недостаточность; тромбоэмболия; беременность; грудное вскармливание.
Повышенная чувствительность к препарату.
С осторожностью назначают препарат при лейкопении, тромбоцитопении, гиперкальциемии.
Беременность
Торемифен противопоказан к применению при беременности. В период лечения торемифеном рекомендуется применение механического или негормонального противозачаточного средства.
Кормление грудью
Проникает ли торемифен в грудное молоко, неизвестно. Хотя информация о проникновении противоопухолевых препаратов в грудное молоко ограниченна, во время проведения химиотерапии грудное вскармливание не рекомендуется из-за риска для грудных детей (неблагоприятные эффекты, мутагенное и канцерогенное действие).
Резюме и дополнительные сведения
Перед началом лечения пациентка должна пройти обследование у гинеколога. Особое внимание следует уделить состоянию слизистой эндометрия. Затем гинекологические обследования необходимо повторять не менее 1 раза в год.
Пациентки, страдающие такими заболеваниями как артериальная гипертензия, сахарный диабет, имеющие высокий уровень индекса массы тела (>30) или получавшие длительную заместительную гормональную терапию, находятся в группе риска по возникновению рака эндометрия и поэтому нуждаются в тщательном мониторинге.
Торемифен не рекомендуется применять у пациенток, у которых в анамнезе были случаи тяжелой тромбоэмболической болезни.
Больные с декомпенсированной сердечной недостаточностью или тяжёлой стенокардией нуждаются в тщательном мониторинге.
Поскольку у больных с метастазами в костях в начале лечения препаратом может развиться гиперкальциемия, эти пациентки нуждаются в тщательном мониторинге.
Передозировка
Симптомы: при суточной дозе торемифена 680 мг наблюдались головокружение, головные боли, тошнота и/или рвота. Теоретически передозировка может проявляться усилением антиэстрогенных эффектов (приливы) или эстрогенных эффектов (вагинальные кровотечения).
Лечение: проведение симптоматической терапии.
Клинически значимые взаимодействия
Препараты, снижающие почечную экскрецию кальция (в т.ч. тиазидные диуретики), могут повышать риск возникновения гиперкальциемии.
Индукторы микросомального окисления (например, фенобарбитал, фенитоин или карбамазепин), могут ускорять метаболизм торемифена, снижая его концентрацию в сыворотке. В таких случаях суточную дозу следует удвоить.
Взаимодействие между антиэстрогенами и варфарином может привести к выраженному увеличению времени кровотечения (следует избегать одновременного применения торемифена и препаратов этой группы).
Теоретически метаболизм торемифена может замедляться под влиянием препаратов, ингибирующих изофермент CYP3A4, при участии которого осуществляется метаболизм торемифена. К таким препаратам относятся кетоконазол и другие подобные противогрибковые препараты, а также эритромицин, олеандомицин.
Код ATX
L02BA02
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки белого цвета, круглые, плоские, со скошенным краем по 0,02 г (20 мг) и 0,06 г (60 мг).
Условия и сроки хранения
Препарат следует хранить в сухом недоступном для детей месте при температуре от 15 ° до 25 °C. Срок годности - 5 лет.
Аналоги гонадотропин-релизинг гормона
Гозерелин (Goserelin)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
6-[0-(1,1-диметилэтил)-D-серин]-10-деглицинамидорилизинг фактора лютеинизирующего гормона (свиного) 2-(аминокарбонил)- гидразид.
Терапевтический класс АТХ
Аналог гонадотропин-рилизинг гормона - депо-форма. Противоопухолевое средство.
Механизм действия
Гозерелин является синтетическим аналогом гонадотропин-рилизинг-гормона (ГнРГ). Как и эндогенный ГнРГ, который образуется в гипоталамусе, гозерелин при начальном или прерывистом применении стимулирует высвобождение из передней доли гипофиза ЛГ и ФСГ, которые, в свою очередь, временно повышают концентрацию тестостерона и эстрогена у мужчин и женщин. Однако длительное использование гозерелина при лечении рака предстательной и молочной железы угнетает секрецию ЛГ и ФСГ, приводя в конце концов к снижению концентрации тестостерона или эстрогена и "лекарственной кастрации".
Показания к применению и режим дозирования
Рак предстательной железы; рак молочной железы.
Для взрослых мужчин и женщин: капсулу, содержащую гозерелина 3,6 мг вводят п/к в переднюю брюшную стенку каждые 4 нед; 10,8 мг - каждые 12 нед.
Физико-химические свойства
Молекулярная масса: гозерелин: 1269,43, гозерелина ацетат: 1328.
рКа - Гозерелин: 6,2.
Фармакокинетика
В первые 8 дней после введения всасывание более медленное, чем в течение остальной части 28-дневного периода между введениями препарата. Максимальной концентрации в сыворотке достигает к 12-15 дню. Препарат непрерывно высвобождается в течение 28-дневного периода. Связывание с белками плазмы низкое. Максимальная концентрация в сыворотке при дозе 3,6 мг составляет 2,5 нг/мл. Период полувыведения составляет 2-4 ч и несколько увеличивается при почечной недостаточности, но корректировки дозы не требуется. У больных с печёночной недостаточностью значительных изменений фармакокинетики не наблюдается. Кратковременное повышение концентрация тестостерона отмечается в течение 1-й недели лечения; снижение до уровня, отмечающегося после кастрации, происходит в течение 2-4 нед и сохраняется на протяжении всего периода терапии.
Побочные эффекты
Признаки поражения сердечно-сосудистой системы: возможны артериальная гипотензия или гипертензия (обычно транзиторные, исчезали либо в процессе терапии гозерелином, либо после её прекращения).
Признаки поражения ЦНС и периферической нервной системы: возможны неспецифические парестезии.
Признаки поражения опорно-двигательного аппарата: возможна артралгия.
Аллергические реакции: редко - реакции повышенной чувствительности, включая некоторые проявления анафилаксии.
Дерматологические реакции: возможна кожная сыпь.
У мужчин: возможны "приливы", потливость, снижение потенции (отмена терапии требуется редко), иногда - опухание и болезненность грудных желёз; в начале лечения у больных раком предстательной железы возможно временное усиление боли в костях. Применение аналогов рилизинг-гормона лютеинизирующего гормона может вызывать потерю минеральной плотности костной ткани.
У женщин: возможны "приливы", повышенная потливость, изменение либидо; иногда - головные боли, смена настроения, включая депрессию, сухость слизистой влагалища и изменение размера молочных желёз. На первоначальной стадии терапии больные раком молочной железы могут испытывать временное усиление признаков и симптомов заболевания.
Передозировка
Опыт передозировки препарата у людей ограничен. В случае непреднамеренного введения гозерелина с укороченным интервалом или в более высокой дозе не отмечалось клинически значимых нежелательных явлений.
Лечение: проведение симптоматической терапии.
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу: беременность и период кормления грудью; детский возраст.
Повышенная чувствительность к гозерелину или другим аналогам рилизинг-гормона лютеинизирующего гормона.
Беременность и кормление грудью
Препарат противопоказан к применению при беременности и в период лактации.
Клинически значимые взаимодействия
Лекарственное взаимодействие препарата гозерелин не описано.
Резюме и дополнительные сведения
Больные, получающие гозерелин, должны находиться под наблюдением врача, имеющего опыт проведения гормонотерапии рака. Препарат следует вводить с соблюдением правил асептики под наблюдением врача. Следует с осторожностью назначать гозерелин 10,8 мг мужчинам, подверженным особому риску развития непроходимости мочеточников или сдавливания спинного мозга. У этой категории пациентов следует проводить тщательный мониторинг в течение первого месяца терапии. В том случае, если наблюдаются или развиваются сдавливания спинного мозга или почечная недостаточность, обусловленная непроходимостью мочеточников, следует назначать стандартное для данных осложнений лечение.
Женщинам во время лечения и до восстановления менструаций следует применять негормональные методы контрацепции.
Применение аналогов рилизинг-гормона лютеинизирующего гормона у женщин может вызывать снижение минеральной плотности костной ткани. Результаты изучения гозерелина 3,6 мг показывают, что после окончания лечения происходит некоторое восстановление минеральной плотности костной ткани, отдельных данных об этом при применении гозерелина 10,8 мг в настоящее время не имеется.
Возобновление менструаций после окончания лечения гозерелином 10,8 мг у некоторых больных может происходить с задержкой.
Применение гозерелина может приводить к повышению цервикальной резистентности, необходимо соблюдать осторожность при дилатации шейки матки.
Не имеется данных о том, что гозерелин ухудшает способность к вождению автотранспорта и работе с механизмами.
Код АТХ
L02AE03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Выпускается в виде специального депо-аппарата - стержня-капсулы для подкожного введения пролонгированного действия цилиндрической формы, содержащего 3,6 или 10,8 мг гозерелина ацетата, включенного в полимерную биодеградируемую матрицу. Стержень находится в специальном шприце.
Ингибиторы ароматазы
Эксеместан (Exemestane)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
6-Метиленандроста-1,4-диен-3,17-дион.
Терапевтический класс АТХ
Противоопухолевый препарат. Ингибитор ароматазы.
Механизм действия
Эксеместан является необратимым стероидным ингибитором ароматазы III поколения, сходным по структуре с природным стероидом андростендионом.
У женщин в постменопаузе эстрогены продуцируются преимущественно путем превращения андрогенов в эстрогены под действием фермента ароматазы в периферических тканях. Блокирование образования эстрогенов путем ингибирования ароматазы является методом лечения гормонозависимого рака молочной железы у женщин в постменопаузе.
Механизм действия
Механизм действия препарата обусловлен необратимым связыванием с активным фрагментом фермента, что вызывает его инактивацию. У женщин в постменопаузе эксеместан достоверно снижает концентрацию эстрогенов в сыворотке уже начиная с дозы 5 мг; максимальное снижение (>90%) достигается при дозе 10-25 мг. У пациенток в постменопаузе с диагнозом рак молочной железы, получавших 25 мг препарата ежедневно, общий уровень ароматазы в организме снижался на 98%.
Эксеместан не обладает прогестагенной и эстрогенной активностью. Выявляется лишь незначительная андрогенная активность, преимущественно при применении в высоких дозах. В ходе испытаний с многократным введением в течение суток эксеместан не оказывал влияния на биосинтез кортизола и альдостерона в надпочечниках, что подтверждает избирательность действия данного препарата. В связи с этим отпадает необходимость в заместительной терапии глюкокортикоидами и минералкортикоидами.
Незначительное увеличение уровней ЛГ и ФСГ в сыворотке отмечается даже при низких дозах; этот эффект, однако, является ожидаемым для препаратов данной фармакологической группы; вероятно, он развивается по принципу обратной связи, на уровне гипофиза: снижение концентрации эстрогенов стимулирует секрецию гонадотропинов в гипофизе также и у женщин в постменопаузе.
Фармакокинетика
После приёма внутрь эксеместан быстро и экстенсивно абсорбируется из желудочно-кишечного тракта. При однократном приёме препарата в дозе 25 мг после приёма пищи максимальна концентрация составляет 18 нг/мл и достигается в течение 2 ч. Установлено, что пища улучшает абсорбцию: достигаемый при этом уровень эксеместана в плазме крови на 40% выше, чем после приёма препарата натощак. После достижения максимума уровень активного вещества в плазме снижается; при этом конечный период полувыведения составляет приблизительно 24 ч. Связывание эксеместана с белками плазмы составляет приблизительно 90%; при этом степень связывания не зависит от общей концентрации.
После повторных приёмов в дозе 25 мг/сут концентрация в плазме неизмененного препарата была сходна с таковой после однократного приёма.
После приёма внутрь однократной дозы меченного радиоактивным изотопом препарата было установлено, что выведение эксеместана и его метаболитов в основном завершалось в течение 1 нед, причём примерно равные части дозы выводились с мочой и с калом. Количество эксеместана, выводящегося с мочой в неизмененном виде, составляет менее 1% от введенной дозы. Эксеместан характеризуется высоким клиренсом, преимущественно за счет метаболизма. Процесс биотрансформации осуществляется путем окисления метиленовой группы в положении 6 при участии изофермента CYP3A4 и/или путем восстановления 17-кетогруппы при участии альдокеторедуктаз. В результате образуются многочисленные вторичные метаболиты, однако количество каждого из них очень невелико по сравнению с введенной дозой. В отношении ингибирования ароматазы эти метаболиты либо неактивны, либо менее активны, чем исходное соединение.
Показания к применению и режим дозирования
Лечение распространенного рака молочной железы у женщин в естественной или индуцированной постменопаузе с признаками прогрессирования заболевания на фоне антиэстрогенной терапии;
Третья линия терапии распространенного рака молочной железы у женщин в естественной или индуцированной постменопаузе, с признаками прогрессирования заболевания на фоне антиэстрогенной терапии, а также терапии либо нестероидными ингибиторами ароматазы, либо прогестинами.
Взрослым и пациенткам пожилого возраста эксеместан рекомендуется принимать по 25 мг 1 раз/сут ежедневно, предпочтительно после приёма пищи. Лечение следует продолжать до появления признаков прогрессирования опухолевого заболевания.
При печёночной или почечной недостаточности коррекции дозы не требуется.
Побочные эффекты
Побочные эффекты эксеместана выражены незначительно или умеренно.
Признаки поражения ЦНС: часто - утомляемость, головокружение; иногда - головная боль, бессонница, депрессия, астения.
Признаки поражения пищеварительной системы: часто - тошнота; иногда - боли в области живота, анорексия, запор, диспепсия; редко - увеличение показателей функциональных печёночных тестов в сыворотке, повышение уровня ЩФ. Четкая связь этих эффектов с приёмом эксеместана не установлена.
Признаки поражения эндокринной системы: часто - приступообразные ощущения жара (приливы).
Дерматологические реакции: иногда - кожная сыпь, алопеция.
Признаки поражения системы кроветворения: эпизоды снижения уровня лимфоцитов (у 20% пациенток); редко - тромбоцитопения, лейкопения.
Признаки нарушения обмена веществ: иногда - периферические отеки (отеки стоп, голеней).
Прочие: часто - усиление потоотделения.
Передозировка
Симптомы: не установлены. Данные по применению эксеместана в разовых дозах 600-800 мг свидетельствуют о хорошей переносимости этих доз. Однократная доза эксеместана, которая может вызывать появление опасных для жизни симптомов, не определена.
Лечение: специфические антидоты эксеместана неизвестны. При необходимости следует проводить симптоматическую терапию. Показаны общая вспомогательная терапия, а также регулярный контроль жизненно важных функций и тщательное наблюдение.
Противопоказания
Беременность; кормление грудью; повышенная чувствительность к компонентам препарата.
Беременность
Эксеместан противопоказан к применению при беременности.
Кормление грудью
При необходимости применения препарата в период лактации грудное вскармливание следует прекратить.
Клинически значимые взаимодействия
Препараты, содержащие эстрогены, при одновременном применении с эксеместаном полностью нивелируют его фармакологическое действие.
До настоящего времени не проводилось исследований взаимодействия эксеместана с другими лекарственными средствами. Результаты исследований in vitro показали, что эксеместан подвергается метаболизму под влиянием CYP3A4 и альдокеторедуктаз и не ингибирует ни один из главных изоферментов CYP. В ходе клинического фармакокинетического исследования было установлено, что специфическое ингибирование CYP3A4 кетоконазолом не вызывает достоверных изменений фармакокинетических параметров эксеместана. Однако нельзя исключить возможное снижение концентрации эксеместана в плазме под влиянием веществ, известных как индукторы CYP3A4.
Резюме и дополнительные сведения
Эксеместан не следует назначать женщинам с пременопаузным эндокринным статусом, поскольку оценка эффективности и безопасности препарата у этой группы больных не проводилась. В тех случаях, когда необходимость назначения препарата клинически обоснована, постменопаузный статус следует подтверждать определением уровня ЛГ, ФСГ и эстрадиола.
У пациенток с исходной лимфопенией повышен риск снижения количества лимфоцитов. Однако средний уровень лимфоцитов на протяжении достаточно длительного времени у этих пациенток достоверно не изменялся; также не отмечалось сопутствующего увеличения заболеваемости вирусными инфекциями.
Увеличение показателей функциональных печёночных тестов в сыворотке и повышение уровня ЩФ отмечались преимущественно у пациенток с метастазами в печень и в кости, а также при наличии других поражений печени.
Эксеместан не рекомендуется применять у детей.
Маловероятно, что эксеместан нарушает способность управлять автомобилем или работать с движущимися или точными механизмами. Однако при применении препарата отмечались такие симптомы, как сонливость, астения и головокружение. Пациенток следует предупредить, что при появлении таких явлений возможно уменьшение способности к концентрации внимания и снижение скорости психомоторных реакций.
Код ATX
L02BG06
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования exemestane:
Форма выпуска: таблетки, покрытые сахарной оболочкой, круглые, двояковыпуклые, белого цвета со слегка сероватым оттенком, содержащие 25 мг эксеместана.
Условия и сроки хранения
Препарат следует хранить при температуре не выше 30 °С в недоступном для детей месте. Срок годности - 3 года. Препарат не следует употреблять по истечении срока годности, указанного на упаковке
Анастрозол (Anastrozole)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
Альфа,альфа,альфа’,альфа’-тетраметил-5-(1Н-1,2,4-триазол-1илметил)-м-бензолдиацетонитрил.
Терапевтический класс АТХ
Противоопухолевый препарат. Ингибитор ароматазы.
Механизм действия
Высокоселективный нестероидный ингибитор ароматазы. Ароматаза - фермент, при помощи которого у женщин в постменопаузе андростендион в периферических тканях превращается в эстрон и далее в эстрадиол. Снижение уровня циркулирующего эстрадиола оказывает терапевтический эффект у больных раком молочной железы. В постменопаузе препарат в суточной дозе 1 мг вызывает снижение уровня эстрадиола на 80%. Анастрозол не обладает прогестагенной, андрогенной и эстрогенной активностью. Анастрозол в суточной дозе до 10 мг не оказывает эффекта на секрецию кортизола и альдостерона (следовательно, при применении препарата не требуется заместительного введения кортикостероидов).
Фармакокинетика
После приёма внутрь анастрозол быстро всасывается из ЖКТ. Максимальная концентрация в плазме достигается в течение 2 ч (натощак). Пища несколько уменьшает скорость, но не степень всасывания. Анастрозол связывается с белками плазмы на 40%. Приблизительно 90-95% от Сss достигается после 7 дней приёма препарата. Нет сведений о кумуляции препарата и зависимости фармакокинетических параметров анастрозола от времени и дозы. Анастрозол метаболизируется путем N-деалкилирования, гидроксилирования и глюкуронизации. Триазол, основной метаболит, определяемый в плазме и моче, не ингибирует ароматазу. Анастрозол выводится медленно, T1/2 - 40-50 ч. Анастрозол и его метаболиты выводятся, в основном, с мочой (менее 10% выведенной дозы - в неизмененном виде), в течение 72 ч после приёма препарата.
Определяемый клиренс анастрозола после перорального приёма у добровольцев со стабилизированным циррозом печени или нарушением функции почек не отличается от клиренса, определяемого у здоровых добровольцев. Фармакокинетика анастрозола не зависит от возраста у женщин в постменопаузе.
Показания к применению и режим дозирования
Адъювантная терапия раннего гормоноположительного рака молочной железы у женщин в постменопаузе; лечение распространенного рака молочной железы у женщин в постменопаузе.
Препарат назначают по 1 мг внутрь 1 раз в сутки, длительно.
Пациентам с легкими и умеренно выраженными нарушениями функции почек и печени не требуется коррекции дозы.
Побочное действие
Определение частоты побочных реакций: очень часто (>10%); часто (1-10%); редко (0,1-1%); очень редко (<0,1%).
Признаки поражения репродуктивной системы: очень часто - приливы; часто - сухость влагалища; редко - влагалищные кровотечения.
Признаки поражения пищеварительной системы: часто - тошнота, диарея; редко - анорексия, рвота, увеличение активности гамма-глутаминтрансферазы и щелочной фосфатазы.
Признаки поражения нервной системы: часто - головная боль; редко - сонливость.
Признаки нарушения обмена веществ: редко - гиперхолестеринемия. Приём препарата может вызывать снижение минеральной плотности костной ткани в связи со снижением уровня циркулирующего эстрадиола, тем самым, повышая риск возникновения остеопороза и переломов костей.
Дерматологические реакции: часто - истончение волос, кожная сыпь; очень редко - полиморфная эритема (синдром Стивенса-Джонсона).
Аллергические реакции: очень редко - аллергические реакции (в т.ч. ангионевротический отек, крапивница, анафилактический шок).
Прочие: часто - артралгия, астения.
Противопоказания
Почечная недостаточность тяжелой степени (клиренс креатинина менее 20 мл/мин); умеренная или выраженная печёночная недостаточность (безопасность и эффективность не установлены); детский возраст (безопасность и эффективность не установлены); беременность; лактация (грудное вскармливание); сопутствующая терапия тамоксифеном; повышенная чувствительность к анастрозолу и другим компонентам препарата. Препарат не назначают женщинам в пременопаузе.
Беременность
Препарат противопоказан к применению при беременности
Кормление грудью
Препарат противопоказан к применению в период лактации (грудного вскармливания).
Резюме и дополнительные сведения
У женщин с рецептороотрицательной опухолью эффективность анастрозола не была продемонстрирована, кроме тех случаев, когда имелся предшествующий положительный клинический ответ на тамоксифен.
В случае сомнений в гормональном статусе пациентки менопауза должна быть подтверждена определением половых гормонов в сыворотке крови.
В случае сохраняющегося маточного кровотечения на фоне приёма анастрозола необходима консультация и наблюдение гинеколога.
Препараты, содержащие эстрогены, не следует назначать одновременно с анастрозолом.
Снижая уровень циркулирующего эстрадиола, анастрозол может вызывать снижение минеральной плотности костной ткани. Данных об одновременном применении анастрозола и препаратов аналогов рилизинг-гормона лютеинизирующего гормона нет.
Неизвестно, улучшает ли анастрозол результаты лечения при совместном использовании с химиотерапией.
Эффективность и безопасность анастрозола и тамоксифена при их одновременном применении вне зависимости от статуса гормональных рецепторов сравнимы с таковыми при использовании одного тамоксифена. Точный механизм данного явления пока не известен.
В связи с сообщениями об астении и сонливости, связанными с приёмом анастрозола, рекомендуется при появлении этих симптомов соблюдать осторожность при управлении автомобилем или движущимися механизмами.
Передозировка
Описаны единичные клинические случаи передозировки препарата. Разовая доза анастрозола, при которой развиваются угрожающие жизни симптомы, не установлена.
Лечение: специфического антидота не существует. При необходимости проводят симптоматическую терапию: индуцирование рвоты (если больной в сознании), общая поддерживающая терапия, наблюдение за больным и контроль за функцией жизненно важных органов и систем. Возможно проведение диализа.
Клинически значимые взаимодействия
Клинические исследования по лекарственному взаимодействию с антипирином и циметидином указывают на то, что совместное введение анастрозола с другими препаратами вряд ли приведет к клинически значимому взаимодействию, обусловленному цитохромом P450.
Клинически значимое лекарственное взаимодействие при приёме анастрозола одновременно с другими часто назначаемыми препаратами отсутствует.
На данный момент нет сведений о применении анастрозола в комбинации с другими противоопухолевыми препаратами.
Препараты, содержащие эстрогены, а также тамоксифен не следует назначать одновременно с анастрозолом, т.к. они уменьшают фармакологическое действие последнего.
Код ATX
L02BG03
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Anastrozole:
Форма выпуска
Таблетки, покрытые оболочкой белого цвета, круглые, двояковыпуклые, содержащие анастрозол 1 мг.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре ниже 30 °C. Срок годности - 5 лет.
Летрозол (Letrozole)
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
4,4-(1Н-1,2,4-триазол-1-илметилен)дибензонитрил.
Терапевтический класс АТХ
Противоопухолевый препарат. Ингибитор ароматазы
Механизм действия
Противоопухолевый препарат. Оказывает антиэстрогенное действие, селективно ингибирует ароматазу (фермент синтеза эстрогенов) путем высокоспецифичного конкурентного связывания с субъединицей этого фермента - гемом цитохрома P450. Блокирует синтез эстрогенов как в периферической, так и в опухолевой тканях. У женщин в постменопаузе эстрогены образуются преимущественно при участии фермента ароматазы, который превращает синтезирующиеся в надпочечниках андрогены (в первую очередь, андростендион и тестостерон) в эстрон и эстрадиол.
Ежедневный приём летрозола в суточной дозе 0.1-5 мг приводит к снижению концентрации эстрадиола, эстрона и эстрона сульфата в плазме крови на 75-95% от исходного содержания. Супрессия синтеза эстрогенов поддерживается на протяжении лечения.
При применении летрозола в диапазоне доз от 0,1 до 5 мг нарушения синтеза стероидных гормонов в надпочечниках не наблюдается. Дополнительного назначения глюкокортикоидов и минералокортикоидов не требуется.
Блокада биосинтеза эстрогенов не приводит к накоплению андрогенов, являющихся предшественниками эстрогенов. На фоне приёма летрозола изменений концентраций ЛГ и ФСГ в плазме крови, изменений функции щитовидной железы, изменений липидного профиля, повышения частоты инфарктов миокарда и инсультов отмечено не было.
На фоне лечения летрозолом слабо повышается частота остеопороза (6,9% по сравнению с 5,5% на плацебо). Однако частота переломов костей у пациенток, получающих летрозол, не отличается от таковой у здоровых людей того же возраста.
Адъювантная терапия летрозолом ранних стадий рака молочной железы снижает риск рецидивов, увеличивает выживаемость без признаков заболевания в течение 5 лет, снижает риск развития вторичных опухолей. Продленная адъювантная терапия летрозолом снижает риск рецидивов на 42%.
Фармакокинетика
Летрозол быстро и полностью абсорбируется из желудочно-кишечного тракта (средняя величина биодоступности составляет 99,9%). Пища незначительно снижает скорость абсорбции. Среднее значение времени достижения максимальной концентрации летрозола в крови составляет 1 ч при приёме летрозола натощак и 2 ч - при приёме с пищей. Связывание летрозола с белками плазмы крови составляет приблизительно 60% (преимущественно с альбумином - 55%). Концентрация летрозола в эритроцитах составляет около 80% от его уровня в плазме крови. Летрозол в значительной степени подвергается метаболизму под действием изоферментов CYP3A4 и CYP2A6 с образованием фармакологически неактивного карбинолового соединения. Выводится преимущественно почками в виде метаболитов, в меньшей степени - через кишечник. Конечный период полувыведения составляет 48 ч. Выводится из плазмы посредством гемодиализа.
Фармакокинетические параметры летрозола не зависят от возраста пациента.
При почечной недостаточности фармакокинетические параметры не изменяются.
Показания к применению и режим дозирования
Ранние стадии рака молочной железы у женщин в постменопаузе после завершения стандартной адъювантной терапии тамоксифеном в качестве продленной адъювантной терапии; распространенные гормонозависимые формы рака молочной железы у женщин в постменопаузе (терапия первой линии); распространенные формы рака молочной железы у женщин в постменопаузе (естественной или вызванной искусственно), получавших предшествующую терапию антиэстрогенами.
Для взрослых рекомендуемая доза летрозола составляет 2,5 мг 1 раз в сутки, ежедневно длительно. В качестве продленной адъювантной терапии лечение должно продолжаться в течение 5 лет. При появлении признаков прогрессирования заболевания приём летрозола следует прекратить.
У пациенток пожилого возраста коррекции дозы летрозола не требуется. У пациенток с нарушениями функции печени и/или почек (КК ≥ 10 мл/мин) коррекции дозы препарата не требуется. Тем не менее, при тяжелых нарушениях функции печени пациентки должны находиться под постоянным наблюдением.
Таблетки принимают внутрь, независимо от приёма пищи.
Побочные эффекты
Частоту возникновения побочных эффектов оценивают следующим образом: возникающие "очень часто" - ³10%, "часто" - 1-10%, "иногда" - 0,1%-1%, "редко" - 0,01-0,1%, "очень редко" - <0,01%, включая отдельные сообщения.
Как правило, побочные реакции выражены слабо или умеренно и в основном связаны с подавлением синтеза эстрогенов.
Признаки поражения пищеварительной системы: часто - тошнота, рвота, диспепсия, запор, диарея; иногда - боли в животе, стоматит, сухость во рту, повышение активности печёночных ферментов.
Признаки поражения ЦНС и периферической нервной системы: часто - головная боль, головокружение, депрессия; иногда - тревога, нервозность, раздражительность, сонливость, бессонница, ухудшение памяти, дизестезия; парестезия, гипестезия, нарушения вкусового восприятия, эпизоды нарушения мозгового кровообращения.
Признаки поражения системы кроветворения: иногда - лейкопения.
Признаки поражения сердечно-сосудистой системы: иногда - ощущение сердцебиения, тахикардия, тромбофлебит поверхностных и глубоких вен, повышение АД, ИБС (стенокардия, инфаркт миокарда, сердечная недостаточность), тромбоэмболия; редко - эмболия легочной артерии, тромбоз артерий, инсульт.
Признаки поражения дыхательной системы: иногда - одышка.
Дерматологические реакции: часто - алопеция, повышенная потливость, кожная сыпь (включая эритематозную, макуло-папулёзную, везикулярную сыпь, псориазоподобные высыпания); иногда - кожный зуд, сухость кожи, крапивница.
Признаки поражения опорно-двигательного аппарата: очень часто - артралгия; часто - миалгия, боли в костях, остеопороз, переломы костей; иногда - артрит.
Признаки поражения органов чувств: иногда - катаракта, раздражение глаз, нарушение вкусовых ощущений.
Признаки поражения мочевыводящей системы: иногда - учащенное мочеиспускание, инфекции мочевыводящих путей.
Признаки поражения репродуктивной системы: иногда - вагинальные кровотечения, выделения из влагалища, сухость влагалища, боли в молочных железах.
Прочие: очень часто - приступообразные ощущения жара (приливы); часто - повышенная утомляемость, астения, недомогание, периферические отеки, увеличение массы тела, гиперхолестеринемия, анорексия, повышение аппетита; иногда - снижение массы тела, жажда, гипертермия, сухость слизистых оболочек, генерализованные отеки, боли в опухолевых узлах.
Передозировка
Имеются отдельные сообщения о случаях передозировки летрозола.
Лечение: какие-либо специфические методы лечения передозировки неизвестны. Показана симптоматическая и поддерживающая терапия. Летрозол выводится из плазмы при гемодиализе.
Противопоказания
Эндокринный статус, характерный для репродуктивного периода; беременность; период лактации (грудного вскармливания); детский и подростковый возраст до 18 лет; повышенная чувствительность к летрозолу или любому другому компоненту препарата.
Беременность
Препарат противопоказан к применению при беременности.
Кормление грудью
Препарат противопоказан к применению в период лактации (грудного вскармливания).
Резюме и дополнительные сведения
Нет данных о применении летрозола у пациентов с КК менее 10 мл/мин. Перед назначением летрозола таким пациенткам следует тщательно взвесить соотношение между потенциальным риском и ожидаемым эффектом лечения. Пациентки с тяжелыми нарушениями функции печени должны находиться под постоянным наблюдением.
Некоторые побочные эффекты препарата, такие как общая слабость и головокружение, могут влиять на способность выполнения потенциально опасных видов деятельности, требующих концентрации внимания и быстрых реакций. В этой связи следует соблюдать осторожность при управлении транспортными средствами и механизмами.
Клинически значимые взаимодействия
При одновременном назначении летрозола с циметидином и варфарином клинически значимых взаимодействий не наблюдается.
Клинического опыта по применению летрозола в комбинации с другими противоопухолевыми средствами в настоящее время не имеется.
Согласно результатам исследований in vitro летрозол подавляет активность изоферментов цитохрома Р450 - 2А6 и 2С19 (последнего - умеренно). При решении вопроса о значении этих данных для клиники необходимо учитывать, что изофермент CYP2A6 не играет существенной роли в метаболизме лекарственных препаратов. В экспериментах in vitro было показано, что летрозол, применяемый в концентрациях, в 100 раз превышающих равновесные значения в плазме, не обладает способностью существенно подавлять метаболизм диазепама (субстрата для CYP2С19). Таким образом, клинически значимые взаимодействия с изоферментом CYP2С19 маловероятны. Тем не менее, следует соблюдать осторожность при совместном применении летрозола и препаратов, метаболизирующихся преимущественно при участии вышеназванных изоферментов и имеющих узкий терапевтический индекс.
Код ATX
L02BG04
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки, покрытые плёнкой, содержащие 2,5 мг летрозола №30.
Условия и сроки хранения
Препарат следует хранить при температуре не выше 30 °C, в недоступном для детей месте, предохранять от воздействия влаги. Срок годности - 5 лет.
Ингибиторы биосинтеза гормонов коры надпочечников
Аминоглутетимид
ФАРМАКОЛОГИЧЕСКИЙ/ХИМИЧЕСКИЙ КЛАСС АТХ
3-(4-аминофенил)-3-этил-2,6-пиперидиндион.
Терапевтический класс АТХ
Средство, угнетающее функцию коры надпочечников; противоопухолевое.
Физико-химические свойства
Молекулярная масса - 232,28.
Механизм действия
Аминоглутетимид вызывает подавление функции коры надпочечников путем ингибирования ферментативного превращения холестерина в прегненолон, блокируя, таким образом, синтез стероидов в надпочечниках; эффективно угнетает синтез кортизола, в меньшей степени - синтез других стероидов (в т.ч. тестостерона, дигидротестостерона, андростендиона), может влиять также и на другие этапы синтеза и метаболизма этих стероидов. Отмечается компенсаторное увеличение секреции АКТГ гипофизом (за исключением больных с АКТГ-независимыми аденомами или карциномами), что делает необходимым применение глюкокортикоидов для поддержания эффекта аминоглутетимида. Кроме того, аминоглутетимид ингибирует образование эстрогенов из андрогенов в периферических тканях путем блокирования фермента ароматазы.
Другие эффекты
Индуктор микросомальных ферментов системы цитохрома Р-450 в печени.
Фармакокинетика
Из желудочно-кишечного тракта препарат всасывается быстро и полностью. Связывание с белками низкое (20-25%). Биотрансформация происходит в печени; основной метаболит - Af-ацетиламиноглутетимид; у некоторых больных возможна генетическая вариабельность скорости ацетилирования.
Период полувыведения составляет 12,5 ч; после длительного (2-32 нед) применения уменьшается до 7 ч, так как аминоглутетимид является индуктором ферментов печени, что приводит к увеличению скорости собственного метаболизма. Время достижения максимальной концентрации около 1,5 ч. Начало действия - угнетение функции коры надпочечников происходит через 3-5 дней; восстановление нормальной базальной секреции надпочечников и реакции на стресс обычно отмечается через 36-72 ч после отмены комбинированной терапии аминоглутетимидом и гидрокортизоном; для восстановления функции коры надпочечников после длительного лечения (например, в течение 1 года или более) может потребоваться более продолжительное время.
Выводится почками, 34-54% в неизмененном виде.
При проведении диализа: удаляется при гемодиализе.
Показания к применению и режим дозирования
Синдром Кушинга, включая, связанный с раком надпочечника и эктопическими опухолями, продуцирующими АКТГ, или гиперплазией надпочечников.
Рак молочной железы: лечение диссеминированной формы рака молочной железы у женщин в период постменопаузы.
Рак предстательной железы, не поддающегося гормональному или хирургическому лечению.
Обычная дозировка для взрослых
Как средство, угнетающее функцию коры надпочечников: начальная доза: внутрь, по 250 мг 2-3 раза в сутки в течение примерно 2 нед (для индукции метаболизма и максимального снижения побочного действия на ЦНС); поддерживающая доза: внутрь, по 250 мг 4 раза в сутки, предпочтительно каждые 6 ч.
Рак молочной железы или рак предстательной железы (лечение): начальная доза: внутрь, по 250 мг 2 или 3 раза в сутки в течение примерно 2 нед (для индукции метаболизма и максимального снижения побочного действия на ЦНС), в комбинации с гидрокортизоном в дозе 40 мг в сутки (по 10 мг утром и в 17.00, 20 мг перед сном); поддерживающая доза: внутрь, по 250 мг 4 раза в сутки, предпочтительно каждые 6 ч в комбинации с гидрокортизоном в дозе 40 мг в сутки (по 10 мг утром и в 17.00, 20 мг перед сном).
Побочные эффекты
Частота и степень тяжести большинства побочных эффектов снижаются после первых 2-6 нед лечения из-за увеличения скорости метаболизма лекарственного средства при длительном применении.
Частые
Дозозависимое действие на ЦНС: нарушение координации движений, головокружение, сонливость, апатия или непроизвольные движения глаз; потеря аппетита или тошнота; кореподобная кожная сыпь или зуд в области лица и/или в ладонях
Менее частые
Недостаточность функции коры надпочечников; лейкопения/нейтропения: обычно бессимптомные, редко - фебрильная температура; тромбоцитопения.
Редкие
Головная боль; ортостатическая или стабильная гипотензия; маскулинизация и гирсутизм у женщин; боль в мышцах; рвота
Возможна реакция гиперчувствительности; гипотиреоз и зоб (отмечаются при длительном применении, так как аминоглутетимид блокирует йодирование тирозина).
Передозировка
Лечение передозировки может включать в себя следующее: промывание желудка, симптоматическое, поддерживающее лечение. Внутривенное введение гидрокортизона при развитии глюкокортикоидной недостаточности. При появлении гиповолемии или гипотензии внутривенное введение норэпинефрина /норадреналин/ в сочетании с регидратацией. При тяжелой интоксикации проведение диализа.
Противопоказания
При наличии следующих медицинских проблем необходимо сопоставлять риск и пользу: ветряная оспа, включая недавний контакт с больным или опоясывающий герпес: риск тяжелого генерализованного заболевания; другие инфекции; нарушение функции печени: гипотиреоз: аминоглутетимид может снижать концентрацию тироксина в сыворотке крови; нарушение функции почек; повышенная чувствительность к аминоглутетимиду или глутетимиду.
Беременность
При необходимости применения данного препарата по жизненным показаниям или в случае тяжелых заболеваний, когда другие лекарственные средства не могут быть использованы или неэффективны, следует тщательно сопоставлять риск и пользу.
Аминоглутетимид проходит через плаценту и вызывает ложный гермафродитизм у грудных девочек, матери которых принимали сопутствующие противосудорожные средства.
Кормление грудью
Проникает ли аминоглутетимид в грудное молоко, неизвестно. Однако осложнений у человека не зарегистрировано.
Клинически значимые взаимодействия
Взаимодействие лекарственных средств и/или связанные с ним проблемы отобраны на основе их потенциальной клинической значимости. Комбинации, содержащие любое из перечисленных веществ, в зависимости от имеющегося количества, могут также взаимодействовать с данным препаратом.
Антикоагулянты - производные кумарина: аминоглутетимид увеличивает скорость метаболизма этих антикоагулянтов; корректировка дозы должна основываться на мониторировании времени свёртывания крови;
Минералокортикоиды: аминоглутетимид может изменять метаболизм минералокортикоидов; может потребоваться корректировка дозы;
АКТГ: аминоглутетимид может ингибировать реакцию надпочечников на АКТГ; это может снижать терапевтический эффект АКТГ;
Дексаметазон: аминоглутетимид увеличивает скорость метаболизма дексаметазона, что может приводить к двукратному снижению периода полувыведения дексаметазона; при необходимости назначения глюкокортикоидов больному, получающему аминоглутетимид, рекомендуется использовать гидрокортизон вместо дексаметазона;
Дигоксин или теофиллин: эффекты могут быть снижены из-за индукции аминоглутетимидом микросомальных ферментов в печени; рекомендуется соблюдать осторожность.
Резюме и дополнительные сведения
Больные, получающие аминоглутетимид, должны находиться под наблюдением врача, имеющего опыт проведения химиотерапии рака или в области клинической эндокринологии.
Дозу необходимо подбирать таким образом, чтобы обеспечить необходимый уровень подавления функции коры надпочечников.
Вследствие вызываемого аминоглутетимидом снижения образования альдостерона, что может приводить к гипонатриемии и ортостатической гипотензии, у 20-50% больных может быть необходимо проведение заместительной терапии минералкортикоидами.
Следует тщательно наблюдать больных в периоды стресса, такие как хирургическое вмешательство (включая хирургическую стоматологию), травмы или острые заболевания. Поскольку угнетение функции надпочечников может препятствовать нормальной реакции на стресс, возможно дополнительное назначение стероидов. После шока или тяжелой травмы применение аминоглутетимида рекомендуется сразу же временно прекратить.
При появлении побочного действия со стороны ЦНС рекомендуется снизить дозу.
Если кожная сыпь от слабовыраженной до умеренной степени тяжести не проходит в течение более 5-8 дней или в случае сильно выраженной сыпи применение аминоглутетимида рекомендуется отменить. При лечении кожной сыпи можно использовать дифенгидрамин. После исчезновения сыпи от слабовыраженной до умеренной степени тяжести лечение аминоглутетимидом можно возобновить с дозы 250 мг в сутки и постепенно увеличивать ее до терапевтической дозы.
Возможны тошнота и рвота; обычно ослабляются при продолжающемся лечении.
Соблюдать осторожность при появлении сонливости, головокружения или гипотензии, особенно при вождении автомобиля, управлении механизмами или выполнении других работ, требующих повышенного внимания.
Больные, обладающие повышенной чувствительностью к глутетимиду, могут иметь повышенную чувствительность и к аминоглутетимиду.
Исследований зависимости эффекта аминоглутетимида от возраста у детей не проведено. Однако существует невысокая вероятность того, что аминоглутетимид будет индуцировать преждевременное половое созревание у мальчиков и маскулинизацию и гирсутизм у девочек.
Исследований зависимости эффекта аминоглутетимида от возраста у пожилых людей не проведено. Однако люди пожилого возраста могут быть более чувствительны к действию препарата на центральную нервную систему (ЦНС) и при его использовании у них более вероятны случаи летаргии. Кроме этого, у пожилых больных более вероятны возрастные нарушения функции почек, что может потребовать соблюдения осторожности при приёме больными аминоглутетимида.
Для применения в качестве противоопухолевого средства
Подавление функции коры надпочечников аминоглутетимидом приводит к повышению секреции АКТГ гипофизом (за исключением больных АКТГ-независимыми аденомами или карциномами); поэтому для поддержания необходимого эффекта аминоглутетимида может потребоваться заместительная терапия глюкокортикоидами (обычно гидрокортизоном) с целью предотвращения гипертрофии коры надпочечников и возобновленного синтеза стероидов.
Заместительная терапия глюкокортикоидами обычно необходима у больных диссеминированным раком молочной железы.
В связи с быстрым восстановлением нормальной реактивной способности коры надпочечников после отмены аминоглутетимида и применения гидрокортизона постепенное снижение дозы обычно не требуется.
Код АТХ
L02BG01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования:
Форма выпуска: таблетки по 0,25 г.
Упаковка и хранение
Хранить при температуре ниже 40 °С, предпочтительно при 15-30 °С, если производителем не указано иначе. Держать в плотной упаковке. Защищать от света.
ИММУННЫЕ ПРЕПАРАТЫ
Таргетные (молекулярно-нацеленные) препараты
Ингибиторы поверхностных антигенов (моноклональные антитела)
Ритуксимаб (Мабтераª)
Терапевтический класс АТХ
Противоопухолевое средство, химерное моноклональное антитело мыши-человека.
Механизм действия
Специфически связывается с трансмембранным антигеном CD20. Антиген расположен на мембранах пре-В-лимфоцитов и зрелых В-лимфоцитов, отсутствует на стволовых и здоровых плазматических клетках, экспрессируется в 95% В-клеточных неходжкинских лимфом. Ритуксимаб связывается с антигеном CD20 на В-лимфоцитах и инициирует иммунологические реакции, опосредующие лизис В-клеток. Механизмы клеточного лизиса включают комплемент- и антителозависимую цитотоксичность.
Фармакокинетика
У больных, получающих препарат в дозах 125 мг/м2, 250 мг/м2 или 375 мг/м2 1 раз в неделю, концентрация антител в сыворотке крови возрастает по мере увеличения дозы. Ритуксимаб определяется в организме в течение 3-6 мес. У больных, получающих дозу 375 мг/м2, средний период полувыведения из плазмы составляет 68,1 ч, максимальная концентрация - 238,7 мкг/мл, средний плазменный клиренс - 0,0459 л/ч.
Показания к применению и дозирование
Рецидивирующие или устойчивые к химиотерапии В-клеточные CD20-позитивные неходжкинские лимфомы низкой степени злокачественности или фолликулярные.
В-крупноклеточные CD20-позитивные диффузные неходжкинские лимфомы (в составе комбинированной химиотерапии).
Режим дозирования устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии. При монотерапии разовая доза составляет 375 мг/м2 в виде внутривенной инфузии 1 раз в нед, на курс - 4 инфузии. За 30-60 мин до введения ритуксимаба рекомендуется проведение премедикации с использованием антигистаминного и анальгезирующего препаратов. При развитии реакции гиперчувствительности инфузию следует временно прервать. После купирования нежелательных явлений введение препарата возобновляют со скоростью, равной половине от предыдущей.
Побочные эффекты
Реакции, связанные с введением препарата: лихорадка и озноб, развивающиеся преимущественно при первом введении препарата в первые 2 ч. Возможны тошнота, рвота, крапивница, недомогание, головная боль, отёк языка, ангионевротический отёк глотки, гипотензия, одышка.
Со стороны системы кроветворения симптомы слабо выражены и обратимы, возможно развитие лимфаденопатии, тяжёлой нейтропении (1,8%), тромбоцитопении (1,8%), анемии (1,4%).
Со стороны процессов обмена веществ возможны гипергликемия, гипокальциемия, гиперурикемия, повышение активности лактатдегидрогеназы.
Центральная и периферическая нервная система: головокружение, тревога, депрессия, парестезии, бессонница, сонливость, невриты.
Сердечно-сосудистая система: брадикардия, тахикардия, артериальная гипертензия, редко вазодилатация, артериальная гипотония.
Дыхательная система: кашель, обострение бронхиальной астмы, псевдоларингит.
Пищеварительная система: тошнота, рвота, диарея, боли в животе, анорексия.
Дерматологические реакции: сухость кожи, ночная потливость.
Костно-мышечная система: миалгии, артралгии, боли в пояснице и грудной клетке, мышечный гипертонус, скованность мышц и суставов.
Мочевыделительная система: частое мочеиспускание, гематурия.
Со стороны биохимических показателей возможно транзиторное повышение активности трансаминаз или уровня билирубина (крайне редко).
Передозировка
Случаев передозировки ритуксимаба в клинических исследованиях не было. Действие препарата в дозе более 500 мг/м2 не изучено.
Противопоказания
Повышенная чувствительность к ритуксимабу или к мышиным белкам.
Беременность и грудное вскармливание
Влияние ритуксимаба на репродуктивную функцию не изучено. Неизвестно, выделяется ли препарат с грудным молоком. При применении препарата в период лактации следует прекратить грудное вскармливание.
Клинически значимые взаимодействия
В настоящее время данные о возможном лекарственном взаимодействии ритуксимаба отсутствуют. Переносимость одновременного или последовательного применения ритуксимаба и препаратов, которые могут уменьшить число здоровых В-клеток, точно не установлено. У пациентов получавших ритуксимаб в комбинации с химиотерапией по схеме СНОР потенцирования токсичности не наблюдалось.
Резюме и дополнительные сведения
Следует соблюдать осторожность при назначении препарата пациентам с заболеваниями лёгких (риск возникновения бронхоспазма), при уровне нейтрофилов менее 1,5x109/л и тромбоцитов менее 75x109/л. Во время всего периода терапии ритуксимабом необходимо систематически проводить полный клинический анализ периферической крови, функции печени. За 12 ч до введения ритуксимаба следует отменить антигипертензивные препараты. После введения белковых препаратов возможно развитие анафилактоидных реакций, поэтому при применении ритуксимаба всегда должны быть в наличии средства для немедленного купирования реакций гиперчувствительности (норадреналин, антигистаминные средства, кортикостероиды). Безопасность и эффективность у детей не установлены.
Код АТХ
L01XC02
Торговые наименования, формы выпуска и производители
мабтераª (F. HOFFMANN-LA ROCHE), раствор для инфузий, 10 мл и 50 мл во флаконах. 1 мл содержит 10 мг ритуксимаба.
Трастузумаб (Герцептинª)
Терапевтический класс АТХ
Противоопухолевое средство.
Механизм действия
Рекомбинантные гуманизированные моноклональные антитела, производные ДНК, которые селективно взаимодействуют с внеклеточным доменом белка, являющегося 2 подтипом рецептора к эпидермальному ростовому фактору человека (HER2). Антитела принадлежат к классу IgG. В 25-30% случаях первичного РМЖ имеется гиперэкспрессия HER2. Монотерапия трастузумабом, проводимая в качестве терапии второй и третьей линии у женщин с метастазирующим РМЖ, сопровождается объективным ответом в 15% и медианой выживаемости равной 13 мес.
Присоединение трастузумаба к комбинации химиотерапии антрациклиновыми антибиотиками и циклофосфамидом или паклитакселом в качестве первой линии у женщин с метастатическим РМЖ и гиперэкспрессией HER2 достоверно увеличивает медиану времени до прогрессирования (у больных, получавших антрациклиновые антибиотики, на 1,7 мес, паклитаксел - на 3,9 мес). Также отмечается увеличение частоты объективных ответов и медианы выживаемости.
Фармакокинетика
При введении препарата в виде внутривенных инфузий в дозе 10, 50, 100, 250 или 500 мг 1 раз в неделю фармакокинетика имела дозозависимый характер.
После введения нагрузочной дозы (4 мг/кг) и еженедельной поддерживающей терапии в дозе 2 мг/кг средний период полувыведения из плазмы равнялся 5,8 дням.
Показания к применению и дозирование
Лечение больных метастазирующим РМЖ с опухолевой гиперэкспрессией HER2:
Ú монотерапия, если пациентка уже получала одну или более схем химиотерапии по поводу метастатической стадии заболевания;
Ú комбинированная терапия (с паклитакселом) в случаях, если пациентка еще не получала химиотерапию по поводу метастатической стадии заболевания.
Режим дозирования
Тестирование на опухолевую экспрессию HER2 до начала лечения обязательно. Нагрузочная доза определяется из расчёта 4 мг/кг массы тела в виде 90-минутной внутривенной инфузии. Поддерживающая доза составляет 2 мг/кг массы тела в неделю. Если не было осложнений предшествующей инфузии, препарат можно вводить в виде 30-минутной инфузии.
Побочные эффекты
Реакции, связанные с введением препарата: лихорадка и озноб, развивающиеся при первом введении препарата.
Со стороны системы кроветворения: лейкопения, тромбоцитопения, анемия III степени (менее чем у 1% больных).
Со стороны процессов обмена веществ: отёки.
Центральная и периферическая нервная система: головокружение, тревога, депрессия, парестезии, бессонница, сонливость, невропатии.
Сердечно-сосудистая система: кардиотоксичность (признаки сердечной недостаточности: одышка, ортопноэ, усиление кашля, отёк легких, снижение фракции выброса), тахикардия, артериальная гипертензия, вазодилатация, артериальная гипотония, кардиомиопатия, сердечная недостаточность.
Дыхательная система: одышка, кашель, обострение бронхиальной астмы, плевральный выпот, фаринтит, ринит, синусит, редко дыхательная недостаточность.
Пищеварительная система: тошнота, рвота, диарея (у 27% больных), боли в животе, анорексия, гепатит, панкреатит (редко).
Дерматологические реакции: зуд, усиление потоотделения, сухость кожи, ночная потливость, поражение ногтей, алопеция, акне.
Костно-мышечная система: миалгии и артралгии, боли в костях.
Мочевыделительная система: инфекции мочевыводящих путей.
Аллергические реакции: анафилактоидные реакции (редко).
Со стороны биохимических показателей: транзиторное повышение активности трансаминаз или уровня билирубина (крайне редко).
Передозировка
Случаев передозировки трастузумаба в клинических исследованиях не было. Действие препарата в разовых дозах более 10 мг/кг не изучено.
Противопоказания
Повышенная чувствительность к трастузумабу или компонентам препарата.
Беременность и грудное вскармливание
Влияние трастузумаба на репродуктивную функцию или на плод не изучено. Неизвестно, выделяется ли препарат с грудным молоком. При применении препарата в период лактации следует прекратить грудное вскармливание.
Клинически значимые взаимодействия
Специальные исследования лекарственных взаимодействий трастузумаба у человека не проводились. В клинических исследованиях значимых взаимодействий с одновременно назначаемыми препаратами не отмечалось.
Разводить трастузумаб в 5% растворе глюкозы нельзя, поскольку он вызывает агрегацию белка. Препарат нельзя смешивать или разводить вместе с другими лекарственными препаратами.
Резюме и дополнительные сведения
Во время инфузии необходимо наблюдать больных на предмет появления лихорадки и других инфузионных симптомов. Следует соблюдать осторожность при назначении препарата пациентам с заболеваниями сердечно-сосудистой системы (сердечной недостаточностью, ИБС, артериальной гипертензией). Больные, которым планируется терапия трастузумабом, особенно те из них, которые ранее получали антрациклиновые антибиотики и циклофосфамид, должны пройти кардиологическое обследование (сбор анамнеза, физикальный осмотр, ЭКГ, ЭхоКГ или сканирование сердца). В ходе лечения необходимо мониторировать функцию сердца каждые 3 мес. При наличии стойкого снижения фракции выброса левого желудочка, даже в отсутствие клинических симптомов, целесообразно рассмотреть возможность прерывания терапии трастузумабом. При появлении симптомов сердечной недостаточности - назначение стандартной терапии. У больных с клинически значимыми симптомами сердечной недостаточности настоятельно рекомендуется прервать терапию трастузумабом.
Безопасность и эффективность препарата у детей не установлены.
Код АТХ
L01XC03
Торговые наименования, формы выпуска и производители
герцептинª (F. HOFFMANN-LA ROCHE), лиофилизированный порошок для приготовления концентрата для инфузий; во флаконах. 1 флакон содержит 440 мг трастузумаба.
Ингибиторы передачи митогенных сигналов (ингибиторы тирозинкиназы)
Иматиниб (Гливекª)
Терапевтический класс АТХ
Противоопухолевое средство, ингибитор тирозинкиназы.
Механизм действия
Эффективно ингибирует фермент Bcr-Abl-тирозинкиназу на клеточном уровне, in vitro и in vivo. Селективно подавляет пролиферацию и вызывает апоптоз клеточных линий, позитивных по Bcr-Abl, а также молодых лейкозных клеток при хроническом миелолейкозе с положительной филадельфийской хромосомой и при остром лимфобластном лейкозе. Кроме того, иматиниб - сильнодействующий ингибитор рецепторов тирозинкиназы для фактора роста тромбоцитов и фактора стволовых клеток, он также подавляет клеточные реакции, опосредуемые вышеуказанными факторами. In vitro ингибирует пролиферацию и индуцирует апоптоз клеток стромальных опухолей ЖКТ, экспрессирующих с-kit мутации.
Показания к применению и дозирование
Хронический миелолейкоз в фазе акселерации, бластного криза, а также в хронической фазе; терапия первой линии.
Лечение неоперабельных и метастатических злокачественных стромальных опухолей ЖКТ (GIST) у взрослых пациентов.
Режим дозирования
При хроническом миелолейкозе (ХМЛ) доза иматиниба зависит от фазы заболевания. В хроническую фазу доза составляет 400 мг/сут, в фазу акселерации и при бластном кризе 600 мг/сут. Препарат следует принимать 1 раз в сут, во время еды, запивая полным стаканом воды. Лечение продолжают до тех пор, пока сохраняется эффект. При условии отсутствия тяжёлых нежелательных явлений и тяжёлой нейтропении или тромбоцитопении, не связанных с основным заболеванием, возможно увеличение дозы иматиниба в следующих случаях:
Ú прогрессирование заболевания;
Ú отсутствие удовлетворительного гематологического ответа после как минимум 3 мес лечения;
Ú утрата достигнутого ранее гематологического ответа.
У больных с хронической фазой заболевания доза препарата может быть увеличена до 600 мг/сут, в фазе акселерации и при бластном кризе до 800 мг/сут (по 400 мг в 2 приёма).
В процессе терапии иматинибом требуется коррекция дозы в зависимости от динамики уровня нейтрофилов и тромбоцитов в периферической крови. При возникновении нейтропении или тромбоцитопении требуется временная отмена препарата или уменьшение его дозы, в зависимости от степени выраженности осложнений.
При хронической фазе ХМЛ и стромальных опухолях ЖКТ (начальная доза иматиниба 400 мг/сут) в случае снижения уровня нейтрофилов менее 1,0x109/л и уровня тромбоцитов менее 50x109/л рекомендуется отменить препарат до тех пор, пока число нейтрофилов не превысит 1,5x109/л, тромбоцитов 75x109/л, затем возобновить приём в исходной дозе. В случае повторного снижения числа нейтрофилов и тромбоцитов ниже указанного уровня, рекомендуется временно отменить препарат, при восстановлении уровня нейтрофилов и тромбоцитов возобновить приём иматиниба в дозе 300 мг/сутки.
Побочные эффекты
Наиболее частыми побочными эффектами являются тошнота, рвота, диарея, абдоминальные боли, астения, лихорадка, недомогание, миалгии, судороги мышц, периферические отёки преимущественно в периорбитальной области и нижних конечностей, которые хорошо поддаются терапии диуретиками.
Инфекционные осложнения: сепсис, пневмония, простой герпес, инфекции верхних дыхательных путей, гастроэнтерит.
Система кроветворения: часто нейтропения, тромбоцитопения, анемия, фебрильная нейтропения, панцитопения.
Со стороны обмена веществ: анорексия, редко гиперурикемия, гипокалиемия, гипонатриемия.
Центральная и периферическая нервная система: головная боль, головокружение, нарушение вкуса, парестезии, бессонница, иногда геморрагический инсульт, обмороки, сонливость, мигрень, депрессия, нарушение памяти, снижение либидо, спутанность сознания, отёк мозга, судороги.
Органы зрения: конъюнктивит, повышение слёзоотделения, иногда кровоизлияния в конъюнктиву, сухость конъюнктивы, отёчность век, макулярный отёк, глаукома.
Слуховые и вестибулярные нарушения: редко головокружение, шум в ушах.
Сердечно-сосудистая система: сердечная недостаточность, отёк легких, тахикардия, артериальная гипертензия, редко перикардит, тромбоэмболии.
Дыхательная система: диспноэ, плевральный выпот, кашель, редко интерстициальный фиброз, интерстициальная пневмония.
Пищеварительная система: часто тошнота, рвота, диарея, боли в животе, метеоризм, запор, редко - гипербилирубинемия, желтуха, гепатит, кровотечения, асцит, гастрит, язва желудка, колит, непроходимость кишечника, панкреатит.
Дерматологические реакции: периорбитальные отёки, дерматит, экзема, сыпь, отёчность лица, век, зуд, эритема, сухость кожи, алопеция, ночная потливость, петехии, повреждение ногтей, фотосенсибилизация, пурпура, хейлит, псориаз, гиперпигментация кожи, редко - везикулярная сыпь, ангионевротический отёк.
Костно-мышечная система: мышечные спазмы и судороги, миалгии и артралгии, припухание суставов, ишиалгии, скованность мышц и суставов.
Мочевыделительная система: почечная недостаточность, боли в области почек, частое мочеиспускание, гематурия.
Репродуктивная система: гинекомастия, увеличение молочных желёз, отёк мошонки, снижение потенции.
Со стороны биохимических показателей: повышение активности трансаминаз или уровня билирубина (менее 3% пациентов).
Передозировка
До настоящего времени о случаях передозировки иматиниба не сообщалось.
Противопоказания
Повышенная чувствительность к компонентам препарата.
Беременность и грудное вскармливание
Данных по применению иматиниба у беременных женщин нет. Не следует применять во время беременности, за исключением тех случаев, когда это жизненно необходимо. Неизвестно, выделяется ли иматиниб с грудным молоком. При применении препарата в период лактации следует прекратить грудное вскармливание.
Клинически значимые взаимодействия
Увеличение концентрации иматиниба в плазме возможно при одновременном применении с препаратами, ингибирующими изофермент CYP3A4 цитохрома Р450 (например, кетоконазол).
Резюме и дополнительные сведения
Для уменьшения риска возникновения нежелательных явлений рекомендуется принимать препарат во время еды, запивая достаточным количеством воды. Следует соблюдать осторожность при назначении препарата пациентам с нарушением функции печени. Почки не играют существенной роли в выведении метаболитов препарата. В клинических исследованиях у 5,4% пациентов с GIST были отмечены геморрагии ЖКТ, у 2,7% - в местах локализации метастазов опухоли (как внутрибрюшинные, так и внутрипечёночные).
Во время всего периода терапии иматинибом необходимо систематически проводить полный клинический анализ периферической крови, функции печени.
Торговые наименования, формы выпуска и производители
Гливекª (NOVARTIS PHARMA), капсулы от светло-жёлтого до оранжево-жёлтого цвета с маркировкой красного цвета "NVR SH". 1 капсула содержит 100 мг иматиниба мезилатаª.
Эрлотиниб (Тарцеваª)
Терапевтический класс АТХ
Противоопухолевое средство, ингибитор тирозинкиназы.
Механизм действия
Мощный ингибитор тирозинкиназы рецепторов эпидермального фактора роста человека HER1 и EGFR. Тирозинкиназа отвечает за процесс внутриклеточного фосфорилирования HER1/EGFR. Экспрессия HER1/EGFR наблюдается на поверхности как нормальных, так и раковых клеток. Ингибирование фосфотирозина EGFR тормозит рост линий опухолевых клеток и приводит к их гибели.
Фармакокинетика
Хорошо всасывается после приёма внутрь. Время достижения максимальной концентрации в плазме 4 ч, биодоступность эрлотиниба составляет 59%. Максимальная концентрация эрлотиниба Cmax в плазме 1,995 нг/мл. Равновесная концентрация достигается на 7-8 день. Связь с белками плазмы (альбумин и альфа-1 кислый гликопротеин) 95%. Эрлотиниб метаболизируется в печени при участии фермента CYP3А4, в меньшей степени CYP1А2 и лёгочной изоформы CYP1А1. In vitro 80‑95% эрлотиниба метаболизируется при участии CYP3А4.
Средний клиренс 4,47 л/ч. Не выявлено связи между клиренсом, возрастом, массой тела, полом и расой больного. Средний период полувыведения T1/2 36,2 ч. Метаболиты и следовые количества эрлотиниба выводятся, преимущественно, с каловыми массами (>90%), почками выводится небольшое количество введенной дозы.
Снижение клиренса эрлотиниба отмечено при повышении концентрации общего билирубина и альфа-1 кислого гликопротеина, a его повышение - у курильщиков. Эрлотиниб выводится через печень, в настоящее время нет данных о влиянии наличия метастазов в печени и нарушения функции печени на фармакокинетику эрлотиниба. Эрлотиниб и его метаболиты выводятся почками в незначительных количествах - менее 9% однократной дозы. Клинические исследования у больных с нарушением функции почек не проводились.
Показания к применению и дозирование
Местно-распространённый или метастатический немелкоклеточный рак лёгкого, прогрессирующий после одной или более схем химиотерапии.
Первая линия терапии местно-распространённого, неоперабельного или метастатического рака поджелудочной железы в комбинации с гемцитабином.
Режим дозирования
Внутрь, 1 раз в сут, не менее чем за час или через 2 ч после приёма пищи.
Немелкоклеточный рак лёгкого - по 150 мг ежедневно, длительно.
Рак поджелудочной железы - по 100 мг ежедневно, длительно в комбинации с гемцитабином.
При появлении признаков прогрессирования заболевания терапию эрлотинибом следует прекратить.
Побочные эффекты
Наиболее частые нежелательные явления независимо от причинной связи с препаратом: сыпь (69-75%) и диарея (48-54%), большинство из которых 1 и 2 степени тяжести и не требуют вмешательства. Сыпь и диарея III-VI степени тяжести наблюдались у 9% больных.
Побочные действия у больных, получавших эрлотиниб 150 мг в качестве монотерапии и по 100 мг или 150 мг в комбинации с гемцитабином:
-
ЖКТ - анорексия, диарея, рвота, стоматит, диспепсия, боли в животе; желудочно-кишечные кровотечения, некоторые из которых были связаны с одновременным применением варфарина или НПВС;
-
гепатобилиарная система - нарушения функции печени (включая повышение активности АЛТ, АСТ, уровня билирубина), в основном преходящие, лёгкой или умеренной степени тяжести или связанные с метастазами в печень;
-
орган зрения - конъюнктивит, сухой кератоконъюнктивит; кератит, выявлен случай перехода в язву роговицы;
-
дыхательная система - кашель, одышка, носовое кровотечение; интерстициальные заболевания лёгких (интерстициальная пневмония, облитерирующий бронхиолит, фиброз лёгких, острый респираторный дистресс-синдром и инфильтрация лёгких, включая случаи с фатальным исходом);
-
нервная система и психическая сфера - головная боль, невропатия, депрессия;
-
прочие - лихорадка, повышенная утомляемость, озноб, тяжёлые инфекции (с нейтропенией или без неё), пневмония, сепсис, фиброзное воспаление подкожной клетчатки, снижение массы тела.
Передозировка
Однократные дозы эрлотиниба до 160 мг внутрь переносятся хорошо. При приёме эрлотиниба в дозе выше рекомендованной могут наблюдаться тяжёлые нежелательные явления: диарея, кожные высыпания и возможно повышение активности печёночных трансаминаз. В случае подозрения на передозировку лечение приостанавливают и проводят симптоматическую терапию.
Противопоказания
Выраженная гиперчувствительность к эрлотинибу или к любому компоненту препарата.
Беременность и грудное всармливание
С осторожностью.
Клинически значимые взаимодействия
При применении препарата в комбинации с субстратами или модуляторами фермента CYP3А4 может потребоваться коррекция их дозы. Ингибиторы CYP3А4 (кетоконазол) снижают метаболизм эрлотиниба и увеличивают его концентрацию в плазме. В случае развития токсичности, необходимо снизить дозу эрлотиниба.
Индукторы CYP3А4 (рифампицин) увеличивают метаболизм эрлотиниба и значимо снижают его концентрацию в плазме. Индукция метаболизма с участием CYP3А4 при одновременном приёме рифампицина (600 мг внутрь 4 раза в сут в течение 7 дней) приводит к снижению медианы AUC эрлотиниба на 69%. Клиническое значение этого наблюдения неясно. При возможности необходимо предусмотреть альтернативный метод лечения без индукции активности CYP3А4. Варфарин, другие производные кумарина - отмечены повышение МНО и кровотечения, включая желудочно-кишечные кровотечения, некоторые из которых были связаны с одновременным введением варфарина. У больных, принимающих варфарин или другие производные кумарина необходимо регулярно контролировать протромбиновое время или МНО.
Резюме и дополнительные сведения
Интерстициальное заболевание лёгких (ИЗЛ), включая ИЗЛ с фатальным исходом, редко диагностировалось у больных с немелкоклеточным раком лёгкого, раком поджелудочной железы или другими солидными опухолями, получавших эрлотиниб. У пациентов с немелкоклеточным раком лёгкого, получавших плацебо или эрлотиниб частота серьёзных ИЗЛ составляла 0,8% в каждой группе. Частота случаев ИЗЛ у больных с раком поджелудочной железы получавших эрлотиниб и гемцитабин составила 2,5% по сравнению с 0,4% в группе, получавших гемцитабин и плацебо. Общая частота случаев ИЗЛ у больных, получавших эрлотиниб, включая применение в комбинации с химиотерапией, составляет 0,6%. ИЗЛ включают интерстициальную пневмонию, интерстициальное заболевание лёгких, облитерирующий бронхиолит, фиброз лёгких, острый респираторный дистресс-синдром и инфильтрацию лёгких. Большинство случаев ИЗЛ было связано с приёмом сопутствующей или ранее проводимой химиолучевой терапии, паренхиматозным заболеванием лёгких в анамнезе, метастатическим поражением лёгких или инфекцией. При развитии новых и прогрессировании лёгочных симптомов (одышка, кашель и лихорадка) приём эрлотиниба необходимо временно прекратить до выяснения причины. При возникновении тяжёлой или умеренной диареи необходимо назначить лоперамид. В некоторых случаях может потребоваться снижение дозы эрлотиниба. При тяжёлой или устойчивой диарее, тошноте, анорексии или рвоте с обезвоживанием эрлотиниб временно отменяют и проводят регидратацию. Во время лечения эрлотинибом и, как минимум в течение 2 нед после его окончания, следует применять надёжные методы контрацепции. Безопасность и эффективность эрлотиниба у больных в возрасте до 18 лет не изучались. При необходимости коррекции, дозу рекомендуется уменьшать постепенно на 50 мг.
Код АТХ
ЛС-001443
тарцеваª (F. HOFFMANN-LA ROCHE). Таблетки, покрытые плёночной оболочкой белого или белого с желтоватым оттенком цвета по 25 мг, 100 мг, 150 мг.
Гефитиниб (Ирессаª)
Терапевтический класс АТХ
Противоопухолевое средство, ингибитор тирозинкиназы.
Механизм действия
Селективный ингибитор тирозинкиназы рецепторов эпидермального фактора роста, гефитиниб тормозит рост опухолевых клеток, метастазирование и ангиогенез, а также ускоряет процессы апоптоза. Повышает противоопухолевую активность химиотерапевтических препаратов, лучевой и гормональной терапии.
Фармакокинетика
Относительно медленно всасывается после приёма внутрь. Время достижения максимальной концентрации в плазме достигает 3-7 ч, биодоступность гефитиниба составляет 59%, не зависит от приёма пищи. Равновесная концентрация достигается после приёма 7-8 доз.
Связь с белками плазмы (сывороточный альбумин и альфа-1 гликопротеин) составляет около 90%. Гефитиниб метаболизируется в печени при участии фермента CYP3А4, в меньшей степени CYP2D6.
Общий плазменный клиренс составляет 500 мл/мин. Не выявлено связи между клиренсом, возрастом, массой тела, полом и расой больного. Метаболиты и следовые количества гефитиниба выводятся, преимущественно с фекалиями (>90%), почками выводится не более 4% от количества введённой дозы.
Клинические исследования гефитиниба у больных с нарушением функции почек и печени (вследствие цирроза или гепатита) не проводились.
Показания к применению и дозирование
Местно-распространённый или метастатический немелкоклеточный рак лёгкого, рефрактерный к режимам химиотерапии, содержащим цисплатин или доцетаксел.
Режим дозирования
Внутрь по 250 мг 1 раз в сутки вне зависимости от приёма пищи. Таблетка может быть растворена в половине стакана питьевой воды. Раствор гефитиниба можно назначать через назогастральный зонд.
Не требуется коррекции дозы в зависимости от возраста, массы тела, этнической или половой принадлежности, функции почек, при умеренно выраженной печеночной недостаточности.
Побочные эффекты
Частые нежелательные явления, наблюдаемые более чем у 20% больных - угревая сыпь, зуд, диарея, сухость кожи. Обычно возникновение нежелательных реакций отмечается в течение первого месяца применения препарата. Характер их, как правило, обратимый. Примерно у 8% больных отмечались реакции III-IV степени тяжести, однако только у 1% больных лечение гефитинибом было завершено вследствие побочных реакций.
ЖКТ: анорексия, диарея, рвота, стоматит, дегидратация, редко - панкреатит, повышение активности трансаминаз печени.
Органы зрения: конъюнктивит, блефарит, обратимая эрозия роговицы, нарушение роста ресниц.
Дыхательная система: интерстициальная пневмония III-IV степени.
Кожа и её придатки: пустулёзная сыпь, алопеция, сухость кожи, зуд, изменение ногтей, редко - токсический эпидермальный некролиз и мультиформная эритема.
Прочие: повышенная утомляемость (астения).
Передозировка
Возможно увеличение тяжести и частоты нежелательных явлений (диареи, кожных высыпаний). Проводится симптоматическая терапия, антидота к гефитинибу не существует.
Противопоказания
Повышенная чувствительность к гефитинибу или к любому другому компоненту препарата, беременность, лактация, детский и подростковый возраст.
Беременность и грудное вскармливание
Противопоказано.
Клинически значимые взаимодействия
При применении препарата в комбинации с субстратами или модуляторами фермента CYP3А4 может потребоваться коррекция их дозы. Ингибиторы CYP3А4 (итраконазол) снижают метаболизм гефитиниба и увеличивают на 80% его концентрацию в плазме.
Индукторы CYP3А4 (рифампицин) увеличивают метаболизм гефитиниба и снижают на 83% его концентрацию в плазме.
Резюме и дополнительные сведения
Интерстициальное заболевание лёгких (ИЗЛ), включая ИЗЛ с фатальным исходом иногда диагностировалось у больных, получавших гефитиниб. При развитии новых и прогрессировании лёгочных симптомов (одышка, кашель и лихорадка) приём гефитиниба необходимо временно прекратить до выяснения причины. В случае развития ИЗЛ необходимо отменить препарат и провести необходимое лечение. При подтверждении ИЗЛ приём гефитиниба отменяют.
Во время лечения гефитинибом и как минимум в течение 3 мес после его окончания следует применять надёжные методы контрацепции.
Код АТХ
LO1XX31
Торговое наименование препарата, форма выпуска и производители
ирессаª (ASTRA ZENECA). Таблетки, покрытые оболочкой коричневого цвета по 250 мг.
Ингибиторы ангиогенеза
Бевацизумаб (Авастинª)
Терапевтический класс АТХ
Противоопухолевое средство, антитела моноклональные.
Механизм действия
Рекомбинантные гиперхимерные (гуманизированные) моноклональные антитела, которые селективно связываются с биологически активным фактором роста эндотелия сосудов (VEGF) и нейтрализуют его. Бевацизумаб ингибирует связывание фактора роста эндотелия сосудов с его рецепторами на поверхности эндотелиальных клеток, что приводит к снижению васкуляризации и угнетению роста опухоли. Введение бевацизумаба приводит к подавлению метастатического прогрессирования заболевания и снижению микрососудистой проницаемости при различных опухолях человека, включая рак ободочной кишки, молочной, поджелудочной, предстательной железы.
В комбинации с иринотеканом, фторурацилом и лейковорином в качестве первой линии терапии у больных с метастазирующим КРР статистически достоверно увеличивает общую выживаемость с 15,6 до 20,3 мес. Добавление бевацизумаба к режиму FOLFOX увеличивает период выживания без прогрессирования заболевания с 6,2 до 10,6 мес, общую частоту объективных ответов на лечение с 34,8 до 44,8% и медиану продолжительности ответа на лечение с 7,1 до 10,4 мес.
Фармакокинетика
При внутривенном введении препарата в диапазоне доз от 1 до 10 мг/кг в течение 90 мин его фармакокинетика имела линейный характер.
У пациентов с низким уровнем альбумина (менее 29 г/л) и высоким уровнем щелочной фосфатазы (более 484 Ед/л) клиренс бевацизумаба примерно на 20% выше, чем при нормальных показателях.
Показания к применению и дозирование
Метастатический КРР - первая линия терапии в комбинации с химиотерапией на основе производных фторпиримидинов.
Режим дозирования
Стандартный режим 5 мг/кг массы тела 1 раз в 14 дней в виде 90-минутной внутривенной инфузии. Начальную дозу препарата вводят после введения цитостатиков, если не было осложнений предшествующей инфузии, то препарат можно вводить в виде 30-60-минутной инфузии как до, так и после химиотерапии.
Побочные эффекты
Наиболее серьезные побочные эффекты: перфорация органов ЖКТ, кровоизлияния, артериальная тромбоэмболия.
Реакции, связанные с введением препарата: лихорадка и озноб, астения, абсцесс, вагинальные кровотечения.
Со стороны системы кроветворения: лейкопения, нейтропения, анемия.
Центральная и периферическая нервная система: возможны извращение вкуса, анорексия, обмороки, ишемия головного мозга.
Сердечно-сосудистая система: артериальная тромбоэмболия, инфаркт миокарда, инсульт, транзиторная ишемическая атака, тромбоз глубоких вен, хроническая сердечная недостаточность.
Дыхательная система: носовое кровотечение, одышка, ринит.
Пищеварительная система: боль в животе, тошнота, рвота, диарея (у 27% больных), запор, анорексия, ректальное кровотечение, стоматит, кровоточивость дёсен, перфорация органов ЖКТ.
Дерматологические реакции: сухость кожи, изменение цвета кожи, дерматит.
Со стороны биохимических показателей: протеинурия, гипергликемия, увеличение уровня щелочной фосфатазы, гиперкалиемия.
Передозировка
При назначении в максимальной дозе 20 мг/кг у некоторых больных отмечалась мигрень тяжёлой степени. При передозировке возможно усиление всех побочных эффектов. Антидота нет. Лечение симптоматическое.
Противопоказания
Повышенная чувствительность к бевацизумабу или к любому другому компоненту препарата, метастатическое поражение ЦНС, беременность и грудное вскармливание, детский возраст, почечная и печёночная недостаточность.
Беременность и грудное вскармливание
Мужчинам и женщинам детородного возраста во время лечения бевацизумабом и как минимум в течение 6 мес после окончания лечения необходимо использовать надёжные методы контрацепции. Вскармливание грудным молоком не рекомендуется как минимум в течение 6 мес после окончания терапии бевацизумабом.
Клинически значимые взаимодействия
Отмечается увеличение концентрации активного метаболита иринотекана SN38 на 33% при сочетании с бевацизумабом. У пациентов, получавших лечение комбинацией FOLFOX и бевацизумаб, отмечено небольшое увеличение частоты диареи и лейкопении. При развитии тяжелой диареи и лейкопении необходимо проведение коррекции дозы иринотекана согласно инструкции по его применению. Исследования лекарственного взаимодействия с другими цитостатиками не проводились. Существующие данные позволяют предположить, что бевацизумаб не влияет на фармакокинетику фторурацила, карбоплатина, паклитаксела и доксорубицина. При сочетанном назначении с варфарином увеличения частоты серьезных кровотечений не отмечено.
Резюме и дополнительные сведения
У пациентов с метастатическим КРР, получающих бевацизумаб в сочетании с химиотерапией, существует повышенный риск развития перфорации ЖКТ, в том числе с внутрибрюшинным воспалением и фатальным исходом. При развитии перфорации лечение бевацизумабом необходимо прекратить.
Бевацизумаб может негативно влиять на заживление ран, поэтому препарат не рекомендуется назначать в течение 28 сут после хирургического вмешательства или до полного заживления хирургической раны.
У больных, получавших бевацизумаб, наблюдалась повышенная частота возникновения артериальной гипертензии, а это основание для тщательного контроля артериального давления на протяжении всего курса лечения. Если не удаётся контролировать артериальную гипертензию или при развитии гипертонического криза лечение бевацизумабом необходимо прекратить.
Риск развития протеинурии повышен у больных с артериальной гипертензией в анамнезе. До начала и во время лечения необходимо контролировать уровень белка в моче. При развитии протеинурии 4 степени (нефротический синдром) лечение бевацизумабом необходимо прекратить.
У пациентов с метастатическим КРР повышен риск кровотечения из опухоли. При развитии кровотечения 3-4 степени лечение бевацизумабом прекращают. У больных с врожденным геморрагическим диатезом, приобретённой коагулопатией или получавших полную дозу антикоагулянтов по поводу тромбоэмболии перед назначением бевацизумаба следует соблюдать осторожность.
Терапия антрациклиновыми антибиотиками и лучевая терапия на область грудной клетки может способствовать развитию застойной сердечной недостаточности.
При назначении бевацизумаба пациентам старше 65 лет существует повышенный риск возникновения артериальной тромбоэмболии (включая развитие инсульта, транзиторной ишемической атаки, инфаркта миокарда) и лейкопении. Повышения частоты других осложнений у пожилых больных, получавших бевацизумаб, не отмечено. Безопасность и эффективность препарата у детей не установлены.
Код АТХ
L01XC07
Торговые наименования, формы выпуска и производители
авастинª (F. HOFFMANN-LA ROCHE). Концентрат для приготовления раствора для инфузий; во флаконах. 1 флакон содержит 100 мг или 400 мг бевацизумаба.
Модификаторы биологических реакций
Интерфероны
Интерферон-альфа
Фармакологический/химический класс АТХ
Интерфероны альфа-nl и -n3: природные альфа-интерфероны.
Рекомбинантные интерфероны альфа-2а и -2b: родственны природным альфа-интерферонам.
Терапевтический класс АТХ
Интерферон. Противоопухолевый, противовирусный и иммуномодулирующий препарат.
Механизм действия и фармакологические эффекты
Клетки продуцируют и секретируют интерфероны в ответ на вирусные инфекции или на воздействия различных синтетических и биологических индукторов; альфа-интерфероны продуцируют, главным образом, лейкоциты.
Интерфероны обладают противовирусной, антипролиферативной и иммуномодулирующей активностью.
Полагают, что противовирусное и антипролиферативное действие связано с изменениями синтеза РНК, ДНК и клеточных белков, включая онкогены. Точный механизм противоопухолевой активности не известен, но может быть связан с любым из этих трёх эффектов.
Противовирусное: ингибируют репликацию вирусов в инфицированных ими клетках, индуцируя в последних состояние резистентности к вирусным инфекциям и модулируя ответную реакцию иммунной системы, направленную на нейтрализацию вирусов или уничтожение инфицированных ими клеток.
Антипролиферативное: подавляют пролиферацию опухолевых клеток in vitro и рост некоторых ксенотрансплантатов опухолей человека у голых мышей. In vivo антипролиферативная активность интерферона альфа-2а изучалась на таких опухолях, как мукоидная карцинома молочной железы и аденокарцинома слепой и поперечноободочной кишки, а также предстательной железы. Степень антипролиферативной активности варьирует.
Иммуномодулирующее: повышают фагоцитарную активность макрофагов и усиливают специфическое цитотоксическое действие лимфоцитов на клетки-мишени.
Многие эффекты интерферона альфа-2а, в отличие от других подобных белков человека, частично или полностью исчезают при его испытании на животных. Тем не менее, у макак-резусов, которым предварительно вводили интерферон альфа-2а, индуцировалась значительная активность против вируса осповакцины.
Физико-химические свойства: рекомбинантный интерферон альфа-2а - синтетический препарат. Белковую цепь из 165 аминокислот синтезируют путём использования технологии рекомбинантной ДНК с участием полученной методами генетической инженерии Escherichia coli.
Фармакокинетика
После в/м или п/к введения биодоступность превышает 80%. После в/м введения интерферона альфа-2а в дозе 36 млн ME максимальная концентрация в сыворотке колебалась от 1500 до 2580 пг/мл (в среднем, 2020 пг/мл), а после п/к введения - от 1250 до 2320 пг/мл (в среднем, 1730 пг/мл) и достигалась, в среднем, через 3,8 ч и 7,3 ч соответственно.
Альфа-интерфероны полностью метаболизируются в почках: фильтруются через почечные клубочки и подвергаются быстрому протеолитическому расщеплению во время реабсорбции в канальцах. Печёночный метаболизм и выведение с жёлчью - менее важные пути элиминации.
У здоровых лиц период полувыведения интерферона альфа-2а после в/в инфузии 36 млн ME составляет 3,7-8,5 ч (в среднем, 5,1 ч), а общий клиренс - 2,14-3,62 мл/мин/кг (в среднем, 2,79 мл/мин/кг).
После однократного в/м введения интерферона альфа-2а пациентам с метастатическим раком и с хроническим гепатитом В фармакокинетические показатели аналогичны таковым у здоровых добровольцев.
Показания к применению и дозирование
-
Новообразования лимфатической системы и системы кроветворения: волосатоклеточный лейкоз; миеломная болезнь; кожная Т-клеточная лимфома; хронический миелолейкоз; тромбоцитоз при миелопролиферативных заболеваниях; неходжкинская лимфома низкой степени злокачественности.
-
Солидные опухоли: саркома Капоши у больных СПИД без оппортунистических инфекций в анамнезе; распространённый рак почки; диссеминированная форма меланомы.
Интерферон альфа-2а вводят п/к или в/м.
Волосатоклеточный лейкоз. Интерферон альфа-2а назначают в начальной дозе 3 млн МЕ/сут п/к или в/м в течение 16-24 нед. При непереносимости суточную дозу уменьшают до 1,5 млн МЕ и/или снижают кратность введения до 3 раз в неделю. Поддерживающая доза составляет 3 млн МЕ 3 раза в неделю п/к или в/м. При непереносимости дозу уменьшают до 1,5 млн МЕ 3 раза в неделю.
Миеломная болезнь. Препарат назначают по 3 млн МЕ 3 раза в неделю п/к или в/м. В зависимости от индивидуальной переносимости дозу можно еженедельно увеличивать до достижения максимально переносимой дозы (9-18 млн МЕ) 3 раза в неделю. Лечение по данной схеме можно продолжать неопределённо долго, если не выявляют прогрессирования болезни и не возникает непереносимость препарата.
Кожная Т-клеточная лимфома. Интерферон альфа-2а может оказывать эффект у больных с прогрессирующей формой заболевания, в том числе рефрактерных к традиционной терапии или не подходящих для её проведения. Больным в возрасте 18 лет и старше препарат вводят п/к или в/м в течение 12 нед, постепенно увеличивая суточную дозу до 18 млн МЕ. Рекомендуют увеличивать дозу по следующей схеме: 1-3 день - 3 млн МЕ/сут, 4-6 день - 9 млн МЕ/сут, 7-84 день - 18 млн МЕ/сут. Поддерживающее лечение проводят максимально переносимой пациентом дозой, но не превышающей 18 млн МЕ, в виде п/к или в/м инъекций 3 раза в неделю. У больных, положительно реагирующих на лечение, его надо продолжать не менее 12 мес, чтобы максимально увеличить вероятность достижения полной и длительной ремиссии.
Следует учитывать, что примерно у 40% больных с кожной Т-клеточной лимфомой не выявляют объективного противоопухолевого эффекта. Частичную ремиссию наблюдают обычно в пределах 3 мес лечения, полную - в пределах 6 мес, хотя иногда для достижения максимального эффекта необходимо 12 мес терапии.
Хронический миелолейкоз. Больным, положительным по филадельфийской хромосоме, показано лечение интерфероном альфа-2а в хронической стадии заболевания. Препарат приводит к гематологической ремиссии у 60% пациентов в хронической стадии хронического миелолейкоза, независимо от предшествующей терапии. У 2/3 из этих больных полная гематологическая ремиссия ещё сохраняется через 18 мес после начала лечения. В отличие от цитотоксической химиотерапии интерферон альфа-2а может привести к стабильной цитогенетической ремиссии длительностью более 40 мес.
Больным в возрасте 18 лет и старше препарат вводят п/к или в/м в течение 8-12 нед. Рекомендуют следующую схему постепенного увеличения дозы: 1-3 день - 3 млн МЕ/сут, 4-6 день - 6 млн МЕ/сут, 7-84 день - 9 млн МЕ/сут. При наличии клинического эффекта терапию следует продолжать до достижения полной гематологической ремиссии, но не более 18 мес. Всем пациентам с полной гематологической ремиссией необходимо продолжать лечение препаратом в дозе 9 млн МЕ (оптимальная доза) или 9 млн МЕ/сут 3 раза в неделю (минимальная доза), для того чтобы в более короткие сроки достичь цитогенетической ремиссии. Оптимальная продолжительность лечения хронического миелолейкоза интерфероном альфа-2а не установлена, хотя есть наблюдения цитогенетических ремиссий длительностью 2 года после начала лечения.
Тромбоцитоз, связанный с миелопролиферативными заболеваниями. Интерферон альфа-2а за несколько дней снижает число тромбоцитов, уменьшает частоту сопутствующих тромбогеморрагических осложнений. Тромбоцитоз часто сопровождает хронический миелолейкоз и служит основным признаком эссенциальной тромбоцитемии.
При тромбоцитозе на фоне хронического миелолейкоза рекомендуют следующую схему увеличения дозы: 1-3 день - 3 млн МЕ/сут, 4-6 день - 6 млн МЕ/сут, 7-84 день - 9 млн МЕ/сут.
Неходжкинская лимфома низкой степени злокачественности. Препарат назначают как поддерживающую терапию после стандартной химиотерапии (с лучевой терапией или без неё) в дозе 3 млн МЕ п/к 3 раза/нед в течение не менее 12 мес. Интерферон альфа-2а можно также назначать одновременно с традиционными схемами химиотерапии (например, с комбинацией циклофосфамида, преднизолона, винкристина и доксорубицина) по 6 млн МЕ/м2 поверхности тела п/к или в/м с 22-го по 26-й день каждого 28-дневного цикла.
Саркома Капоши на фоне СПИД. Оптимальный режим дозирования не установлен.
Вероятность того, что больные саркомой Капоши на фоне СПИД положительно отреагируют на терапию выше в том случае, если в анамнезе у них нет оппортунистических инфекций, симптомов группы В (снижение массы тела более 10%, температура выше 38°С при отсутствии известного очага инфекции, ночная потливость), а исходное число CD4+-лимфоцитов превышает 200/мкл.
Пациентам в возрасте 18 лет и старше препарат следует вводить п/к или в/м в течение 10-12 нед, постепенно доводя суточную дозу не менее чем до 18 млн МЕ/сут, а по возможности - до 36 млн МЕ. Рекомендуют следующую схему увеличения дозы: 1-3 день - 3 млн МЕ/сут, 4-6 день - 9 млн МЕ/сут, 7-9 день - 18 млн МЕ/сут, при переносимости увеличивая дозу на 10-84 день до 36 млн МЕ/сут.
Поддерживающая доза - максимально переносимая доза (но не более 36 млн МЕ) 3 раза в неделю в/м или п/к. Оптимальная продолжительность лечения саркомы Капоши на фоне СПИД не установлена. При наличии клинического эффекта лечение следует продолжать, по крайней мере, до исчезновения опухоли. После прекращения терапии интерфероном альфа-2а саркома Капоши часто рецидивирует.
Распространённые и метастатические формы рака почки. Наилучший терапевтический эффект наблюдают при назначении интерферона альфа-2а в высоких дозах (36 млн МЕ/сут) в качестве монотерапии или в умеренных дозах (18 млн МЕ 3 раза в неделю) в комбинации с винбластином.
При монотерапии интерферон альфа-2а назначают п/к или в/м в течение 8-12 нед, постепенно увеличивая дозу до 18 млн МЕ/сут, а по возможности - до 36 млн МЕ/сут. Дозу 36 млн МЕ/сут рекомендуют вводить в/м. Используют следующую схему увеличения дозы: 1-3 день - 3 млн МЕ/сут, 4-6 день - 9 млн МЕ/сут, 7-9 день - 18 млн МЕ/сут, при переносимости увеличивая дозу на 10-84 день до 36 млн МЕ/сут. Для поддерживающей терапии препарат вводят п/к или в/м 3 раза в неделю в максимальной дозе, переносимой больным, но не более 36 млн МЕ.
Продолжительность лечения составляет не менее 8 нед, предпочтительно - 12 нед. После этого врач должен решить, следует ли продолжать терапию (при наличии положительного эффекта) или прекратить её (при его отсутствии). Лечение проводилось до 16 мес подряд. Оптимальная продолжительность лечения распространённого рака почки интерфероном альфа-2а не установлена.
Меланома. Начальная доза интерферона альфа-2а составляет 18 млн МЕ п/к или в/м 3 раза в неделю в течение 8-12 нед. При применении в дозах менее 18 млн МЕ 3 раза/нед терапевтический эффект наблюдали реже. Поддерживающая доза - 18 млн МЕ (или в максимальной переносимой дозе) п/к или в/м 3 раза в неделю. Оптимальная продолжительность лечения не установлена.
Побочные эффекты
Со стороны организма в целом: часто - гриппоподобный синдром (вялость, повышение температуры, озноб, потеря аппетита, мышечные боли, головная боль, боли в суставах и усиление потоотделения). Приём парацетамола ослабляет или купирует данные острые побочные явления, а их выраженность в ходе лечения или при изменении дозы интерферона альфа-2а имеет тенденцию к уменьшению, хотя при продолжении терапии могут возникнуть сонливость, слабость и вялость.
Со стороны пищеварительной системы: часто - анорексия (примерно у 2/3 больных), тошнота (у 1/2 больных); возможны рвота, изменение вкусовых ощущений, сухость во рту, диарея, уменьшение массы тела, слабые или умеренные боли в животе; редко - запор, метеоризм, изжога, усиление перистальтики, обострение язвенной болезни, желудочно-кишечные кровотечения, повышение активности АЛТ, ЩФ, ЛДГ, увеличение уровня билирубина (коррекции дозы не требуют); изменение активности трансаминаз при гепатите В, что обычно свидетельствует об улучшении клинического состояния больного; в отдельных случаях - тяжёлое нарушение функции печени, печёночная недостаточность.
Со стороны центральной и периферической нервной системы: иногда - системное и несистемное головокружение, нарушение зрения, ухудшение психического состояния, забывчивость, депрессия, сонливость, спутанность сознания, нарушения поведения (нервозность, тревога), нарушения сна, парестезии, онемение конечностей, невропатия, зуд и тремор; редко - выраженная сонливость, судороги, кома, нарушения мозгового кровообращения, временная импотенция, ишемическая ретинопатия, а также суицидальное поведение (в последнем случае препарат следует отменить).
Со стороны сердечно-сосудистой системы: часто - транзиторная артериальная гипо- и гипертензия (примерно у 1/5 онкологических больных), отёки, цианоз, аритмии, ощущение сердцебиения, боли в грудной клетке; редко - небольшая одышка, отёк лёгких, застойная сердечная недостаточность, остановка сердца, инфаркт миокарда. У больных гепатитом В сердечно-сосудистые нарушения отмечают очень редко.
Со стороны дыхательной системы: редко - кашель, пневмония, остановка дыхания.
Со стороны мочевыделительной системы: редко - ухудшение функции почек, острая почечная недостаточность (главным образом, у онкологических больных с заболеваниями почек или при одновременном лечении нефротоксическими препаратами), протеинурия, увеличение содержания клеточных элементов в осадке мочи, повышение уровня азота, мочевины, креатинина и мочевой кислоты в сыворотке крови, электролитные нарушения, особенно при анорексии или обезвоживании.
Со стороны системы кроветворения: часто - транзиторная лейкопения (редко требующая снижения доз), у больных в состоянии миелосупрессии - тромбоцитопения, снижение уровня гемоглобина; возможна тромбоцитопения у пациентов без миелосупрессии; редко - уменьшение уровня гемоглобина и гематокрита. Возвращение тяжёлых гематологических нарушений к исходному уровню обычно отмечают через 7-10 дней после прекращения лечения препаратом.
Дерматологические реакции: часто (1/5 онкологических больных) - лёгкое или умеренное выпадение волос (обратимое после прекращения лечения); редко - обострение герпетических высыпаний на губах, сыпь, зуд, сухость кожи и слизистых оболочек, выделения из носа, носовые кровотечения, обострение или манифестация псориаза.
Прочие: редко - гипергликемия, реакции в месте инъекции, аутоиммунная патология (васкулит, артрит, гемолитическая анемия, нарушение функции щитовидной железы, волчаночноподобный синдром); в отдельных случаях - бессимптомная гипокальциемия.
У некоторых больных после введения препаратов, содержащих гомологичный белок, могут образовываться нейтрализующие активный белок антитела, поэтому вероятно, что у определённой части больных можно обнаружить антитела ко всем интерферонам (как природным, так и рекомбинантным). При некоторых заболеваниях (рак, системная красная волчанка, опоясывающий лишай) антитела к лейкоцитарному интерферону человека могут спонтанно возникать у больных, ранее никогда не получавших интерфероны.
При хранении лиофилизированного интерферона альфа-2а при температуре 4°С (рекомендуемые условия хранения) возрастания иммуногенности не происходит.
Передозировка
Случаи передозировки не известны. У лиц, имевших тяжёлые побочные реакции на проводимую терапию, прежнее состояние восстанавливалось через несколько дней после отмены препарата.
Симптомы: при повторном введении интерферона в высоких дозах могут возникнуть глубокая летаргия, вялость, прострация и кома. В клинических исследованиях кома регистрировалась у 0,4% онкологических больных.
Лечение: показано наблюдение и проведение поддерживающей терапии в условиях стационара.
Противопоказания
Тяжёлые заболевания сердца (в том числе в анамнезе); выраженные нарушения функции почек и печени; угнетение миелоидного ростка кроветворения; судороги и/или нарушения функции ЦНС; хронический гепатит с выраженной декомпенсацией или с циррозом печени; хронический гепатит у больных, получающих или недавно получавших терапию иммунодепрессантами, за исключением кратковременного лечения стероидами; больные с хроническим миелолейкозом, если больной имеет HLA-идентичного родственника и ему предстоит или возможна аллогенная трансплантация костного мозга в ближайшем будущем; повышенная чувствительность к рекомбинантному интерферону альфа-2a или любому другому компоненту препарата.
Беременность и кормление грудью
Применение препарата при беременности оправдано только в том случае, если польза от проводимой терапии превышает возможный риск для плода.
Хотя исследования на животных не дают указаний на тератогенность препарата, нельзя исключить возможность того, что его применение во время беременности может нанести вред плоду. В экспериментальных исследованиях на макаках-резус при введении на ранних и средних сроках беременности препарата в дозах, значительно превышающих рекомендуемые в клинической практике, было отмечено возрастание числа выкидышей.
Неизвестно, выделяется ли интерферон альфа-2а с грудным молоком. Вопрос о прекращении грудного вскармливания или об отмене препарата следует решать в зависимости от важности лечения для матери.
Бензиловый спирт, содержащийся в качестве наполнителя в готовом к применению растворе интерферона альфа-2а, может проникать через плаценту. При назначении препарата непосредственно перед родами или кесаревым сечением следует помнить о токсическом действии на недоношенных детей.
Мужчинам и женщинам детородного возраста, получающим интерферон альфа-2а, следует применять надёжные методы контрацепции.
Клинически значимые взаимодействия
Интерфероны альфа могут нарушать окислительные метаболические процессы, снижая активность микросомальных ферментов печени системы цитохрома Р450. Возможность такого воздействия необходимо учитывать при совместном применении интерферона альфа-2а и лекарственных средств, метаболизируемых данным путём. Описано снижение клиренса теофиллина после одновременного назначения интерферонов альфа.
Интерфероны могут усиливать нейротоксическое, гематотоксическое или кардиотоксическое действие препаратов, назначавшихся ранее или одновременно с ними. Взаимодействия можно наблюдать также с одновременно назначаемыми препаратами, действующими на ЦНС.
Резюме и дополнительные сведения
Интерферон альфа-2а следует применять под наблюдением врача, имеющего опыт лечения пациентов с онкологическими или вирусными заболеваниями. Пациенты должны быть проинформированы о преимуществах данной терапии и возможных побочных реакциях.
Указаний на прямое кардиотоксическое действие препарата нет, однако существует вероятность, что острые, самостоятельно исчезающие токсические эффекты (например, повышение температуры, озноб), часто сопровождающие лечение интерфероном альфа-2а, могут вызывать обострение сопутствующих заболеваний сердца.
При лёгком и умеренном нарушении функции почек, печени или костного мозга необходим их тщательный контроль.
С осторожностью назначают препарат пациентам с хроническим гепатитом и аутоиммунными заболеваниями в анамнезе. Пациентов, у которых при лечении интерфероном альфа-2а выявляют патологические изменения функциональных печёночных проб, нужно тщательно наблюдать и при необходимости препарат отменить.
Рекомендуют регулярное психоневрологическое обследование пациентов, получающих интерферон альфа-2а. В редких случаях у данных пациентов отмечались суицидальные попытки; при этом терапию следует прекратить.
С исключительной осторожностью необходимо применять интерферон альфа-2а у больных с тяжёлой миелосупрессией, так как препарат угнетает костномозговое кроветворение, вызывает падение числа лейкоцитов (особенно гранулоцитов), тромбоцитов и, реже, уровня гемоглобина. Это может приводить к повышенному риску развития инфекции или кровотечения. Следует внимательно следить за этими изменениями и проводить больным развёрнутые анализы крови до начала лечения и регулярно в его процессе.
У больных после трансплантации (например, почки или костного мозга) медикаментозная иммуносупрессия может быть менее эффективной, так как интерфероны оказывают стимулирующее воздействие на иммунную систему.
При наличии клинической симптоматики гипергликемии следует осуществлять контроль уровня глюкозы в плазме крови и соответствующее наблюдение. Больным с сахарным диабетом может быть необходима коррекция дозы сахароснижающих препаратов.
Эффективность, безопасность и оптимальные дозы интерферона альфа-2а для детей с хроническим миелолейкозом не установлены.
Новорождённые (особенно недоношенные) и дети до 2 лет. Назначать интерферон альфа-2а им не рекомендуют, поскольку он содержит бензиловый спирт в качестве консерванта, который может приводить к стойким нарушениям в нервно-психической сфере и полиорганной недостаточности.
В зависимости от режима дозирования и индивидуальной чувствительности больного интерферон альфа-2а может оказывать действие на скорость реакции, способность к потенциально опасным видам деятельности, включая вождение транспортных средств, работу с машинами и механизмами.
Код АТХ
L03AB04
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Interferon alpha:
Формы выпуска: раствор для инъекций прозрачный, слегка желтоватого цвета, для в/м и п/к введения, практически не содержащий частиц; не содержащий сывороточного альбумина человека: 3 млн МЕ/0,5 мл: шприц-тюбик 1 или 5 шт; 4,5 млн МЕ/1 мл: флакон 1 или 3 шт; 6 млн МЕ/1 мл: флакон 1 или 3 шт; 9 млн МЕ/1 мл: флакон 1 или 3 шт; 18 млн МЕ/1 мл: флакон 1 или 3 шт; 18 млн МЕ/3 мл: флакон 1 или 3 шт; 4,5 млн МЕ/0,5 мл: шприц-тюбик 1 или 5 шт; 6 млн МЕ/0,5 мл: шприц-тюбик 1 или 5 шт; 9 млн МЕ/0,5 мл: шприц-тюбик 1 или 5 шт; 3 млн МЕ/1 мл: флакон 1 или 3 шт; 18 млн МЕ/0,6 мл: картридж 1, 2, 3, 5 или 6 шт.
Условия и сроки хранения
Препарат следует хранить в защищённом от света, недоступном для детей месте, при температуре от 2 до 8°С; не замораживать. Срок годности - 2 года.
Шприц-ручка Роферон-Пенª со вставленным картриджем может храниться при комнатной температуре (до 25°С) в течение 30 дней.
Интерлейкины
Интерлейкин-2 (Interleukin-2)
Фармакологический/химический класс АТХ
Сходен с природными интерлейкинами, которых относят к лимфокинам - подгруппе гормоноподобных гликопротеиновых факторов роста, известных также как цитокины.
Терапевтический класс АТХ
Противоопухолевый, иммуномодулирующий препарат группы цитокинов.
Механизм действия и фармакологические эффекты
Алдеслейкин - рекомбинантный человеческий интерлейкин-2, белок с молекулярной массой около 15 600 дальтон, получаемый с помощью технологии рекомбинантной ДНК, с использованием штамма Еscherichia coli, содержащего модифицированный ген человеческого интерлейкина-2.
Ронколейкинª - рекомбинантный человеческий интерлейкин-2, получаемый с использованием штамма Saccharomyces cerevisiae, не имеет структурных отличий от природного интерлейкина-2.
Рекомбинантный человеческий интерлейкин-2 имеет ряд структурных отличий от природного интерлейкина-2 (не гликозилирован, не имеет концевого аланина, в 125-м аминокислотном положении цистеин замещён на серин), однако обладает аналогичной биологической активностью. Он стимулирует эндогенную иммунную защиту с выраженными лимфоцитозом, эозинофилией и тромбоцитопенией; активирует Т-лимфоциты и естественные киллерные клетки, участвующие в механизмах распознавания и уничтожения опухолевых клеток; способствует продукции антител В-клетками, стимулирует клеточную секрецию вторичных цитокинов (гамма-интерферон, фактор некроза опухоли (ФНО), интерлейкин-1, гранулоцитарно-макрофагальный колониестимулирующий фактор), стимулирует факторы комплемента, а также запускает механизмы высвобождения гормонов (АКТГ, кортизол). Действие интерлейкина-2 включает активацию клеточного иммунитета с выраженными лимфоцитозом, эозинофилией и тромбоцитопенией.
Точный механизм интерлейкин-2-опосредованной иммуностимуляции с противоопухолевым действием окончательно не выяснен.
Другие эффекты. Интерлейкин-2 вызывает "leak-синдром": в результате повышения проницаемости капилляров, приводящего к образованию экстравазата и способствующего снижению сосудистого сопротивления.
Сообщалось, что интерлейкин-2 обратимо снижает уровень холестерина, временно уменьшает концентрации тестостерона и дигидроэпиандростерона и повышает концентрацию эстрадиола в сыворотке крови. Кроме того, были сообщения, что он временно увеличивает секрецию АКТГ и выделение гидрокортизона надпочечниками.
Фармакокинетика
Абсолютная биодоступность составляет 35-47%. Около 87% интерлейкина-2 метаболизируется в почках до аминокислот (в клетках эпителия проксимальных извитых почечных канальцев).
Кривая периода полувыведения алдеслейкина в сыворотке при внутривенном струйном введении имеет биэкспоненциальный характер: в a-фазе он составляет 13 мин, в b-фазе - 85 мин.
При подкожном введении период полувыведения составляет 5,3 ч. Более длительное время полувыведения, по сравнению с внутривенным введением, объясняют продолжающейся абсорбцией препарата из подкожной клетчатки в месте введения в течение фазы элиминации из плазмы.
Препарат в основном выводится почками путём клубочковой фильтрации и канальцевой секреции, при этом большая часть дозы здесь же метаболизируется, в результате чего в моче отсутствует биологически активный интерлейкин-2. Вторичный путь выведения - рецептор-опосредованный захват клетками-мишенями. Активно этот процесс протекает при длительном курсе терапии. Между циклами, когда препарат не вводят, клиренс интерлейкина-2 восстанавливается до исходных значений.
Определяемая величина клиренса у человека в результате кратковременного (в течение 15 мин) и продолжительного 24-часового в/в введения приблизительно соответствует скорости клубочковой фильтрации.
Показания к применению и дозирование
Препарат предназначен для подкожного и внутривенного введения.
Режим дозирования при п/к введении. При п/к введении назначают 18 млн ME ежедневно в течение 5 дней, с последующим двухдневным перерывом. В течение последующих 3 нед - по 18 млн ME в 1-й и 2-й день каждой недели и по 9 млн ME в 3-й, 4-й и 5-й дни недели. После недельного перерыва повторяют аналогичный 4-недельный цикл.
Режим дозирования при в/в введении. Терапию проводят в виде индукционных и поддерживающих циклов.
Индукционный цикл терапии: назначают 18 млн МЕ/м2 в виде 24-часовой в/в инфузии в течение 5 дней, с последующим перерывом в 2-6 дней. В течение следующих 5 дней препарат вводят по аналогичной схеме с последующим 3-недельным перерывом. По его окончании назначают второй цикл индукционный терапии.
Поддерживающие циклы (18 млн МЕ/м2 в виде 24-часовой в/в инфузии в течение 5 дней) с 4-недельными интервалами рекомендуют проводить пациентам с положительной динамикой или стабилизацией опухолевого процесса.
Коррекция режима дозирования при п/к и в/в введении
При непереносимости препарата следует уменьшить его дозу или прекратить лечение до исчезновения токсических явлений.
Пациенты пожилого возраста. У них чаще возникают побочные эффекты интерлейкина-2, поэтому следует соблюдать осторожность при назначении препарата данной категории больных.
Дети. Безопасность и эффективность применения интерлейкина-2 у детей окончательно не установлена.
Правила приготовления инфузионного раствора
Содержимое флакона растворяют в 1,2 мл воды для инъекций. Струю воды направляют по стенке флакона, чтобы избежать пенообразования. Аккуратно перемешивают содержимое, выполняя круговые движения флаконом, до полного растворения лиофилизата. Запрещено встряхивать флакон.
Полученный раствор - бесцветная прозрачная жидкость с рН 7,5 (в пределах от 7,2 до 7,8).
Для получения инфузионного раствора суточную дозу приготовленного раствора интерлейкина-2 следует развести в 500 мл 5% раствора декстрозы, содержащем 0,1% человеческого альбумина. Полученный раствор вводят инфузионно в течение 24 ч.
Добавление человеческого альбумина, необходимого для сохранения биологической активности препарата, к раствору декстрозы следует проводить до разведения в нём раствора интерлейкина-2.
Перед введением восстановленный раствор должен быть доведён до комнатной температуры и визуально проверен на отсутствие механических включений и изменение цвета.
Приготовленный раствор не содержит консервантов и предназначен только для однократного применения. Любой неиспользованный раствор или вскрытый флакон должен быть утилизирован в соответствии с требованиями по обращению с биологически опасными препаратами.
При введении интерлейкина-2 не следует использовать инфузионные системы со встроенными фильтрами.
Побочные эффекты
Частота и тяжесть побочных реакций интерлейкина-2 зависят от дозировки и режима введения препарата. Необходимо отметить, что большинство побочных эффектов препарата обратимы и исчезают после 1-2-дневного перерыва.
Определение частоты перечисленных ниже побочных реакций: очень часто (³1/10), часто (от <1/10 до ³1/100), нечасто (от <1/100 до ³1/1000), редко (от <1/1000 до ³1/10 000), крайне редко (<1/10 000).
Таблица 8-9. Побочные эффекты интерлейкина-2
| Частота | В/в инфузии | П/к инъекции |
|---|---|---|
Со стороны сердечно-сосудистой системы |
||
Очень часто |
выраженное снижение АД, синусовая тахикардия |
снижение АД, боль в области сердца (в том числе стенокардия) |
Часто |
аритмия, повышение АД, флебит |
повышение АД, тахикардия |
Нечасто |
стенокардия напряжения, тромбозы, усиленное сердцебиение, преходящие изменения на ЭКГ, инфаркт миокарда, миокардит, кардиомиопатия |
аритмия, ишемия миокарда, инфаркт миокарда, цереброваскулярные нарушения |
Редко |
гипокинез стенки желудочков, тромбоэмболия |
сердечная недостаточность, флебит, тромбофлебит, тромбоэмболия легочной артерии |
Со стороны мочевыделительной системы |
||
Очень часто |
олигурия, увеличение содержания мочевины и креатинина в сыворотке крови |
- |
Часто |
гематурия |
олигурия, увеличение содержания мочевины и креатинина в сыворотке крови |
Нечасто |
почечная недостаточность |
гематурия, почечная недостаточность |
Со стороны дыхательной системы |
||
Очень часто |
одышка, кашель |
одышка, кашель |
Часто |
отёк лёгких, цианоз, гипоксия, инфекционные заболевания дыхательных путей, плеврит |
- |
Нечасто |
носовые кровотечения |
инфекционные заболевания дыхательных путей |
Редко |
респираторный дистресс-синдром |
отёк лёгких, выпот в плевральной полости |
Со стороны пищеварительной системы |
||
Очень часто |
тошнота, рвота, диарея, анорексия |
тошнота, рвота, диарея, анорексия, стоматит |
Часто |
дисфагия, диспепсия, запор, желудочно-кишечные кровотечения, гипербилирубинемия, повышение активности печёночных трансаминаз, щелочной фосфатазы |
запор, желудочно-кишечные кровотечения, повышение активности печёночных трансаминаз, щелочной фосфатазы и лактатдегидрогеназы |
Нечасто |
- |
хейлит, гастрит, гипербилирубинемия |
Редко |
гастрит, холецистит, обострение болезни Крона |
панкреатит, кишечная непроходимость |
Со стороны нервной системы |
||
Очень часто |
тревожность, спутанность сознания, сонливость, головокружение |
головокружение |
Часто |
нарушение психического статуса, включая возбуждение, парестезии, синкопальные явления, депрессия, галлюцинации |
нарушение психического статуса, включая раздражительность, тревожность, спутанность сознания, сонливость, центральные и периферические двигательные нарушения, парестезии, невропатии, бессонница |
Нечасто |
центральные и периферические моторные расстройства, паралич |
возбуждение, судороги, галлюцинации |
Редко |
судороги, летаргия, кома, поражение корковых структур |
- |
Со стороны кожи и слизистых оболочек |
||
Очень часто |
эритема/сыпь, зуд, шелушение кожи |
эритема/сыпь |
Часто |
конъюнктивит, воспаление слизистых оболочек, алопеция, носовые корки |
шелушение и зуд кожи, повышенное потоотделение |
Нечасто |
витилиго |
алопеция, воспаление слизистых оболочек |
Редко |
- |
конъюнктивит |
Со стороны системы кроветворения |
||
В процессе терапии у большинства пациентов выявляют лимфоцитопению и эозинофилию, с последующим компенсаторным лимфоцитозом через 24-48 ч после лечения. Вышеуказанные изменения относят не к побочным действиям, а к проявлениям противоопухолевого механизма интерлейкина-2. |
||
Очень часто |
анемия, тромбоцитопения |
- |
Часто |
лейкопения, нарушения свёртываемости крови |
анемия, тромбоцитопения, лейкопения |
Нечасто |
кровотечения |
кровотечения |
Местные реакции |
||
Очень часто |
- |
эритема/сыпь, боль, воспаление в месте инъекции |
Часто |
- |
уплотнение в месте инъекции |
Редко |
- |
некроз в месте инъекции |
Изменение лабораторных показателей |
||
Часто |
гипергликемия, гипокальциемия, гиперкалиемия |
гипергликемия |
Нечасто |
гипо- или гипертиреоидное состояние |
гипо- или гипертиреоидное состояние, гипо- или гиперкальциемия, гиперкалиемия |
Прочие |
||
Очень часто |
увеличение массы тела, отёки, лихорадка, озноб, недомогание, слабость, головная боль |
лихорадка, озноб, недомогание, головная боль, уменьшение массы тела |
Часто |
болевые ощущения, артралгия, миалгия, асцит |
артралгия, избыточная масса тела, отёки, дегидратация, миалгия, гипотермия |
Нечасто |
- |
миастения, реакции гиперчувствительности (включая отёк Квинке), потеря вкуса |
Редко |
реакции гиперчувствительности, анафилаксия, сахарный диабет |
анафилаксия |
Нарушения сердечного ритма (предсердная и желудочковая аритмия), стенокардия напряжения, инфаркт миокарда, дыхательная недостаточность, желудочно-кишечные кровотечения или ишемия, почечная недостаточность, отёки и нарушения психического статуса могут быть связаны с синдромом повышенной сосудистой проницаемости.
На фоне одновременного приёма с интерфероном альфа редко возникают следующие нежелательные эффекты: серповидный IgA гломерулонефрит, окулобульбарная миастения гравис, воспалительный артрит, тиреоидит, буллёзный пемфигоид, рабдомиолиз и синдром Стивенса-Джонсона.
Бактериальные инфекции или утяжеление их течения, включая септицемию, бактериальный эндокардит, септический тромбофлебит, перитонит и пневмонию, возникают чаще на фоне в/в введения.
Передозировка
Симптомы: возможно усиление проявлений описанных побочных эффектов. Все нежелательные проявления обратимы после прекращения применения препарата.
Лечение: при сохранении клинических симптомов передозировки показана симптоматическая терапия. Угрожающее жизни токсическое действие ослабевало при внутривенном введении дексаметазона; однако при этом возможна потеря терапевтической эффективности интерлейкина-2.
Противопоказания
Ослабленное общее состояние больного (статус больных по шкале ECOG ³2); декомпенсированные заболевания сердечно-сосудистой системы, в том числе в анамнезе; острые инфекционные заболевания, требующие проведения антибиотикотерапии; дыхательная недостаточность (показатель парциального давления кислорода менее 60 мм рт.ст. в покое); наличие метастатических очагов в ЦНС или эпилептические припадки в анамнезе (за исключением больных с положительной динамикой в лечении метастатических очагов в головном мозге: негативные результаты компьютерной томографии, стабильный неврологический статус); беременность и период кормления грудью (безопасность не определена); детский возраст (безопасность и эффективность не определены).
С осторожностью следует назначать препарат при угнетении костномозгового кроветворения (лейкопения менее 4*109/л, тромбоцитопения менее 100*109/л, анемия, гематокрит менее 30%), повышенном содержании билирубина и креатинина в сыворотке крови, аллотрансплантации органов в анамнезе, сопутствующей терапии кортикостероидами, аутоиммунных заболеваниях.
Беременность и кормление грудью
Безопасность применения препарата при беременности и в период грудного вскармливания не установлена, поэтому не следует назначать алдеслейкин в данные периоды.
Мужчинам и женщинам репродуктивного возраста во время терапии алдеслейкином и в течение 3-х месяцев после её окончания следует использовать надёжные методы контрацепции.
Клинически значимые взаимодействия
Одновременное назначение препаратов с нейротоксическим, гепатотоксическим, нефротоксическим, миелотоксическим или кардиотоксическим действием может приводить к усилению воздействия интерлейкина-2 на данные органы и системы.
При одновременном применении глюкокортикостероидов возможно уменьшение активности интерлейкина-2.
Антигипертензивные препараты, включая бета-адреноблокаторы, усиливают гипотензивное действие интерлейкина-2.
Применение рентгеноконтрастных средств по окончании курса терапии интерлейкином-2 может привести к возобновлению токсических явлений, отмеченных в процессе применения препарата. Чаще подобные состояния отмечают в течение 2 нед после введения последней дозы препарата, однако возможность их развития сохраняется в течение нескольких месяцев после окончания терапии.
У пациентов, получающих комбинированные режимы высоких доз интерлейкина-2 и противоопухолевых препаратов (в частности дакарбазина, цисплатина, тамоксифена и интерферона альфа), отмечались реакции гиперчувствительности.
При совместном применении интерлейкина-2 (в виде в/в инфузии) и интерферона альфа возможно увеличение риска развития тяжёлого рабдомиолиза и повреждения миокарда, включая инфаркт миокарда, миокардит и желудочковую гипокинезию.
При совместном применении интерлейкина-2 и интерферона альфа возможно обострение или проявление аутоиммунных и воспалительных заболеваний.
Нарушение процедуры приготовления раствора и его разведения может привести к уменьшению биологической активности препарата и/или образованию биологически неактивного протеина. В процессе приготовления раствора следует избегать применения бактериостатической воды для инъекций или 0,9% раствора натрия хлорида (данные растворы способствуют агрегации субстанции).
Не следует смешивать интерлейкин-2 с другими лекарственными веществами.
Резюме и дополнительные сведения
Терапию интерлейкином-2 необходимо проводить только под контролем врача соответствующей квалификации, имеющего опыт применения противоопухолевых лекарственных средств.
При в/в применении препарата пациента следует госпитализировать в специализированный стационар, имеющий отделение интенсивной терапии, с целью текущего контроля клинических и лабораторных показателей. П/к введение препарата может осуществлять квалифицированный медицинский персонал в амбулаторных условиях.
При появлении серьёзных сопутствующих реакций необходимо изменить режим дозирования. Важно отметить, что тяжёлые или угрожающие жизни побочные эффекты, как правило, но не во всех случаях, исчезают после 1-2-дневного перерыва терапии интерлейкином-2. Решение о возобновлении терапии препаратом принимают с учётом тяжести и характера возникших токсических реакций.
При использовании интерлейкина-2 выявляют обратимое повышение активности печёночных трансаминаз, увеличение содержания билирубина, мочевины и креатинина в сыворотке крови, поэтому следует тщательно контролировать состояние пациентов с почечной или печёночной недостаточностью.
Интерлейкин-2 оказывает влияние на почечный и печёночный метаболизм, а также на экскрецию сопутствующих лекарственных средств. Необходимо соблюдать осторожность при назначении других лекарственных препаратов, способных оказывать нефро- или гепатотоксическое действие.
К числу проявлений неблагоприятного действия препарата относят синдром повышенной сосудистой проницаемости, характеризуемый снижением сосудистого тонуса, выходом белков плазмы и жидкости во внесосудистое пространство. Следует учитывать, что частота возникновения и тяжесть течения данного осложнения выше при в/в введении препарата по сравнению с п/к инъекциями.
Для синдрома повышенной сосудистой проницаемости характерно снижение АД и перфузии органов (сообщалось и о случаях летального исхода). Данный синдром может возникать в ближайшие часы после начала терапии интерлейкином-2. При этом у некоторых пациентов возможно разрешение артериальной гипотензии без соответствующего лечения. При прочих условиях показано в/в введение инфузионных растворов, альбумина, а в некоторых случаях - терапия вазопрессорами (допамин) в низких дозах. При неэффективности лечения следует приостановить терапию интерлейкином-2.
Перед началом инфузионной терапии следует оценить возможность увеличения объёма внутрисосудистой жидкости в связи с риском развития вторичного отёка лёгких на фоне повышенной проницаемости капилляров.
Необходим регулярный контроль водного баланса и электролитного состава крови каждого пациента, поскольку применение интерлейкина-2 может быть причиной развития почечной недостаточности с явлениями олигурии.
Интерлейкин-2 стимулирует секреторные процессы в серозных оболочках, способствуя увеличению объёма выпота в серозных полостях. В связи с этим перед началом терапии необходимо принять меры по профилактике состояний, сопровождающихся увеличением количества выпота в серозных полостях, особенно той локализации, где это может привести к недостаточности жизненно-важных органов (например, выпот в полость перикарда).
Оценку функционального состояния лёгких обязательно проводят у пациентов с возникшими хрипами или одышкой. Купирование симптомов дыхательной недостаточности может потребовать применения методов респираторной поддержки с интубацией трахеи. Подобные случаи отмечены только у пациентов на фоне в/в введения препарата.
В процессе терапии интерлейкином-2 у пациентов могут быть отклонения в психическом статусе в виде раздражительности, спутанности сознания или депрессии. Указанные изменения носят обратимый характер, однако могут сохраняться на протяжении нескольких дней после отмены препарата. Интерлейкин-2 способен изменять реакцию пациента на психотропные лекарственные препараты.
При развитии летаргического состояния или сонливости следует прекратить применение интерлейкина-2, поскольку продолжение терапии может спровоцировать развитие глубокой комы.
Интерлейкин-2 может усиливать выраженность клинических симптомов у пациентов с диагностированным или нелеченным метастатическим процессом в ЦНС, поэтому перед началом терапии интерлейкином-2 всем пациентам рекомендуют провести полноценное диагностическое исследование с целью выявления метастазов в ЦНС и назначения адекватного лечения.
Интерлейкин-2 утяжеляет течение аутоиммунных заболеваний, приводя к возникновению осложнений, опасных для жизни. Поскольку не у всех пациентов с ассоциированным с интерлейкином-2 аутоиммунным феноменом были отмечены признаки предшествующих аутоиммунных расстройств, следует тщательно контролировать функцию щитовидной железы или других потенциально опасных в плане развития аутоиммунных заболеваний органов. У ряда пациентов с болезнью Крона отмечено обострение процесса на фоне применения интерлейкина-2, потребовавшее хирургического вмешательства.
Терапию интерлейкином-2 необходимо отложить до полного излечения существующих бактериальных инфекций, способных спровоцировать токсические эффекты препарата.
Применение интерлейкина-2 может привести к распространению или утяжелению бактериального инфекционного процесса, включая септицемию, бактериальный эндокардит, септический тромбофлебит, перитонит, пневмонию.
Подобные осложнения чаще возникают на фоне в/в введения препарата. Возбудителями инфекционных осложнений в большинстве случаев выступают Staphylococcus aureus или Staphylococcus epidermidis и лишь в некоторых случаях Escherichia coli.
Применение интерлейкина-2 может вызывать развитие анемии и тромбоцитопении. В связи с этим следует проводить периодический контроль гематологических показателей у всех пациентов, получающих препарат.
В дополнение к рутинным тестам пациентам с почечноклеточным раком перед началом терапии и затем с определённой периодичностью необходимо проводить следующие исследования: стандартное гематологическое исследование (включая дифференциальный подсчёт числа форменных элементов крови); биохимическое исследование крови (включая анализ электролитного состава, почечные и печёночные функциональные тесты); рентгенологическое исследование органов грудной клетки.
В качестве дополнения к комплексу обследования пациента перед началом терапии рекомендуют снять ЭКГ и провести стресс-тест (по показаниям), оценить физическое состояние больного, жизненные показатели, объективно оценить состояние коронарных сосудов, а также провести функциональные лёгочные тесты с определением газового состава артериальной крови для курящих пациентов или имеющих в анамнезе респираторные заболевания.
При п/к введении препарата часто возникают реакции в месте инъекций, вплоть до развития некрозов. Данный эффект может быть уменьшен при смене места инъекций.
В период лечения не следует заниматься потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (в том числе вождение автотранспортных средств и работы с машинами и механизмами).
Код АТХ
L03AC01
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования интерлейкина-2:
Форма выпуска: лиофилизат для приготовления раствора для п/к и в/в введения в виде аморфного порошка белого цвета по 18 млн МЕ.
Форма выпуска: лиофилизат для приготовления раствора для п/к и в/в введения в виде аморфного порошка белого цвета по 250 тыс. МЕ, 500 тыс. МЕ, 1 млн МЕ.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре от 2 до 8°C. Не замораживать!
Приготовленный раствор устойчив в течение 48 ч при хранении в холодильной камере и при комнатной температуре (от 2 до 30°С).
В связи с тем, что препарат не содержит консервантов, раствор необходимо использовать непосредственно после приготовления.
Колониестимулирующие факторы
Гранулоцитарные колониестимулирующие факторы
Ленограстим
Терапевтический класс АТХ
Рекомбинантный человеческий гликозилированный гранулоцитарный колониестимулирующий фактор, белок из группы цитокинов.
Механизм действия и фармакологические эффекты
Оказывает стимулирующее и дифференцирующее действие на клетки-предшественницы нейтрофильного ряда, что приводит к значительному увеличению числа активных нейтрофилов в периферической крови уже в течение первых 24 ч. Оказывает также стимулирующее действие на зрелые нейтрофилы, усиливая их способность к миграции и фагоцитозу.
Фармакокинетика
Фармакокинетические параметры ленограстима, как при внутривенном, так и при подкожном введении, -дозо- и времязависимы.
Всасывание и распределение: при назначении рекомендуемой дозы биодоступность составляет 30%.
Метаболизм: биотрансформируется до пептидов.
Выведение: период полувыведения составляет 3-4 часа. С мочой в неизменённом виде выводится не более 1% от введённной дозы.
Показания к применению и дозирование
Режим дозирования
Назначают в дозах из расчёта 150 мкг (19,2 млн МЕ)/м2 поверхности тела в сутки. Продолжительность зависит от основного лечения и терапии, получаемой пациентом, и составляет в среднем от 3 до 7 дней. Максимальная длительность непрерывного применения препарата не должна превышать 28 дней.
Химиотерапия. При проведении химиотерапии применяют на следующий день (через 24 ч) после окончания курса лечения и вводят подкожно ежедневно, до достижения стабильно нормального уровня нейтрофилов в периферической крови.
Трансплантация костного мозга. Препарат применяют в дозе 150 мкг (19,2 млн МЕ)/м2 поверхности тела (или 5 мкг/кг массы тела) в сутки. Введение препарата начинают на следующий день после трансплантации костного мозга или окончания химиотерапии. Вводят ежедневно подкожно или в виде 30-минутной внутривенной инфузии до восстановления нормального уровня нейтрофилов.
Мобилизация клеток-предшественниц гемопоэза. Препарат применяют в дозе 10 мкг/кг массы тела в сутки подкожно, ежедневно, в течение 4-6 дней.
У пожилых пациентов специальные исследования не проводились, особых рекомендаций по дозам не разработано.
Побочные эффекты
Наиболее часто - головная боль (у 30%), боль в костях (у 23%), боль в пояснице (у 17,5%), астения (у 11%), боли в животе (у 6%), преходящее повышение уровня АСТ или АЛТ, щелочной фосфатазы.
Развитие инфекционных осложнений, как правило, связано с режимом кондиционирования, а не с назначением ленограстима.
Передозировка
О случаях передозировки ленограстима сообщений нет.
Противопоказания
Повышенная чувствительность к ленограстиму или к другим компонентам препарата.
Беременность
Не рекомендуют применять у беременных.
Кормление грудью
Необходимо прекратить грудное вскармливание.
Клинически значимые взаимодействия
Взаимодействие ленограстима с другими лекарственными средствами не описано.
Резюме и дополнительные сведения
Доказана эффективность ленограстима при нейтропении, связанной с проведением химиотерапии, у больных ВИЧ-инфекцией.
При проведении цитостатической терапии первое введение ленограстима необходимо осуществлять не ранее, чем через 24 ч после введения последнего противоопухолевого препарата.
В период терапии ленограстимом необходим постоянный контроль клинического анализа крови с обязательным подсчётом количества нейтрофилов и тромбоцитов. В случае увеличения уровня лейкоцитов более 50х109/л, лечение должно быть приостановлено.
Код АТХ
L03AA10
Торговые наименования, формы выпуска и производители
ГРАНОЦИТ® (GRANOCYTE®)ª, компания AVENTIS PHARMA (Франция).
Форма выпуска: лиофилизированный порошок для инъекций (во флаконах по 1 мл). 1 флакон содержит 13,4 млн МЕ и 33,6 млн МЕ ленограстима.
Филграстим
Терапевтический класс АТХ
Рекомбинантный негликозилированный гранулоцитарный колониестимулирующий фактор.
Механизм действия и фармакологические эффекты
Филграстим, содержащий рекомбинантный гранулоцитарный колониестимулирующий фактор, оказывает выраженное стимулирующее и дифференцирующее действие на клетки-предшественницы нейтрофильного ряда, что приводит к значительному увеличению числа активных нейтрофилов в периферической крови уже в течение первых 24 ч. Функция нейтрофилов, образующихся при введении филграстима, нормальна или усилена, что было показано при исследовании хемотаксиса и фагоцитоза. После окончания лечения филграстимом выявляют снижение уровня нейтрофилов в периферической крови на 50% в течение 1-2 дней и до нормального уровня - в течение 1-7 дней.
Лечение филграстимом приводит к уменьшению частоты, тяжести и продолжительности нейтропении и фебрильной нейтропении у больных, получающих цитостатики, в том числе - миелоаблативную химиотерапию с трансплантацией костного мозга.
Фармакокинетика
Фармакокинетические параметры филграстима носят линейный характер, как при внутривенном, так и при подкожном введении.
Выведение: период полувыведения составляет около 3,5 ч.
Показания к применению и дозирование
-
Сокращение продолжительности нейтропении и частоты фебрильной нейтропении у больных, получающих цитостатики по поводу немиелоидных злокачественных заболеваний, а также сокращение нейтропении и её клинических последствий у больных, получающих миелоаблативную терапию с последующей трансплантацией костного мозга или периферических стволовых клеток-предшественниц гемопоэза.
-
Мобилизация аутологичных клеток-предшественниц гемопоэза в периферической крови.
-
Длительная терапия для увеличения числа нейтрофилов и снижения частоты и продолжительности инфекционных осложнений у детей и взрослых с тяжёлой врождённой, периодической или злокачественной нейтропенией (абсолютное число нейтрофилов менее 500/мм3).
Режим дозирования
Химиотерапия. При проведении химиотерапии применяют в дозе 0,5 млн ЕД/кг массы тела 1 раз в сутки подкожно, ежедневно, до достижения стабильно нормального уровня нейтрофилов в периферической крови.
Трансплантация костного мозга. Препарат применяют в начальной дозе 1 млн ЕД/кг массы тела в сутки в виде 30-минутной внутривенной инфузии до восстановления нормального уровня нейтрофилов. Отмену препарата производят после того, как число нейтрофилов превысит 1х109/л в течение 3 дней.
Мобилизации клеток-предшественниц гемопоэза. Препарат применяют в дозе 1 млн ЕД/кг массы тела в сутки, ежедневно, подкожно или внутривенно в течение 6 дней.
Побочные эффекты
Наиболее часто - боли в мышцах и костях (у 13%), купируемые анальгетиками, преходящее слабое или умеренное повышение уровня мочевой кислоты, активности ЛДГ, щелочной фосфатазы.
Редко - слабая или умеренная дизурия, преходящее снижение АД.
Передозировка
Эффекты передозировки филграстима не известны.
Противопоказания
Повышенная чувствительность к филграстиму или другим компонентам препарата.
Беременность
Не рекомендуют применять у беременных.
Кормление грудью
В связи с отсутствием сведений о проникновении филграстима в грудное молоко необходимо прекратить грудное вскармливание.
Клинически значимые взаимодействия
Взаимодействие филграстима с другими лекарственными средствами не описано. Возможное взаимодействие с другими гемопоэтическими факторами роста и цитокинами в клинических исследованиях не изучалось.
Резюме и дополнительные сведения
Эффективность и безопасность у детей и взрослых одинакова.
Препарат не совместим с солевыми растворами. Филграстим нельзя растворять в физиологическом растворе натрия хлорида. При необходимости препарат разводят 5%-ным раствором глюкозы.
При проведении цитостатической терапии первое введение филграстима следует осуществлять не ранее, чем через 24 ч после последнего введения цитостатиков.
В период терапии филграстимом необходим постоянный контроль клинического анализа крови с обязательным подсчётом числа нейтрофилов и тромбоцитов. В случае увеличения количества лейкоцитов более 50х109/л лечение должно быть приостановлено.
Код АТХ
L03AA02
Торговые наименования, формы выпуска и производители
Формы выпуска: раствор для инъекций (во флаконах по 1 мл и 1,6 мл, в шприц-тюбике по 0,5 мл, 1 мл, 1,6 мл). 1 флакон содержит 30 млн МЕ и 48 млн МЕ филграстима, 1 шприц-тюбик содержит 30 млн МЕ и 48 млн МЕ филграстима.
Форма выпуска: раствор для внутривенных и подкожных инъекций (во флаконах по 1 мл). 1 флакон содержит 30 млн МЕ филграстима.
Форма выпуска: раствор для инъекций (во флаконах по 1 мл). 1 флакон содержит 30 млн МЕ филграстима.
Форма выпуска: раствор для внутривенных и подкожных инъекций (во флаконах по 1 мл). 1 флакон содержит 150 мкг/мл и 300 мкг/мл филграстима.
Эритропоэтины
Эритропоэтинª(МНН - Эпоэтин)
Терапевтический класс АТХ
Рекомбинантный человеческий эритропоэтин.
Механизм действия и фармакологические эффекты
Оказывает стимулирующее действие на пролиферацию и дифференцировку эритроидных клеток в зрелые эритроциты. Он действует на ранних этапах эритропоэза, на уровне колониеобразующей эритроидной единицы, далее на уровне проэритробласта, эритробласта и ретикулоцита. Чувствительность этих клеток к эритропоэтину пропорциональна степени зрелости.
Фармакокинетика
Всасывание и распределение: после подкожного введения концентрация активного вещества в крови нарастает медленно. Максимальную концентрацию выявляют через 12-18 часов.
Выведение: период полувыведения составляет 5-6 ч.
Показания к применению и дозирование
Режим дозирования
При анемиях, связанных с химио- или радиотерапией опухолей, перед началом лечения рекомендуют провести определение уровня эндогенного эритропоэтина. При концентрации эритропоэтина ниже 200 мЕ/мл начальная доза составляет 150-450 МЕ/кг. Лечение продолжают в течение 3 нед после окончания химиотерапии.
Нормальный уровень эффективности - прирост гематокрита от 0,5% до 2% за 2 нед.
Побочные эффекты
Очень редко - головная боль, боли в суставах и костях, гриппоподобный синдром.
Со стороны системы кроветворения: очень редко - тромбоцитоз.
Аллергические реакции: очень редко - крапивница, кожный зуд.
Передозировка
О случаях передозировки эпоэтина не сообщалось.
Противопоказания
Повышенная чувствительность к компонентам препарата, неконтролируемая артериальная гипертензия.
Беременность и кормление грудью
Данные по безопасности не представлены.
Клинически значимые взаимодействия
Можно применять с другими лекарственными средствами.
Резюме и дополнительные сведения
Не рекомендуют применять у больных с резистентной артериальной гипертензией, при повышенной чувствительности к сывороточному альбумину, с осторожностью - при тромбоцитозах, эпилепсии.
Перед началом терапии - коррекция дефицита железа, фолиевой кислоты, витамина В12.
У больных с хронической почечной недостаточностью возможно развитие гиперкалиемии.
Код АТХ
В03ХA01
Торговые наименования, формы выпуска и производители
Форма выпуска: раствор для инъекций (в ампулах или флаконах по 1 мл). 1 мл содержит 1000 МЕ, 2000 МЕ, 4000 МЕ, 10 000 МЕ рекомбинантного эритропоэтина человека.
Форма выпуска: лиофилизированный порошок для инъекций (во флаконах). 1 флакон содержит 1000 МЕ, 2000 МЕ, 5000 МЕ эритропоэтина человека.
Форма выпуска: раствор для инъекций (во флаконах по 1 мл). 1 флакон содержит 2000 МЕ, 4000 МЕ эритропоэтина человека.
Форма выпуска: раствор для инъекций (в шприцах по 0,3 мл, 0,4 мл, 0,5 мл, 1 мл; во флаконах по 0,5 мл, 1 мл). 1 шприц содержит 3000 ЕД, 4000 ЕД, 10 000 ЕД эпоэтина альфа, 1 флакон содержит 1000 ЕД, 2000 ЕД, 4000 ЕД эпоэтина альфа.
ФЕРМЕНТНЫЕ ПРЕПАРАТЫ
Аспарагиназа (Asparaginase)
Фармакологический/химический класс АТХ
Аспарагиназа -фермент с высокой молекулярной массой, получаемый для производства коммерческого препарата из Escherichia coli.
Терапевтический класс АТХ
Противоопухолевый препарат.
Механизм действия
Аспарагиназа катализирует расщепление аспарагина, необходимого для жизнедеятельности клеток. Максимальное действие аспарагиназы по подавлению пролиферации отмечают в постмитотической G1-фазе клеточного цикла.
Полагают, что противоопухолевое действие препарата обусловлено снижением уровня аспарагина в лейкемических опухолевых клетках, не способных, в отличие от нормальных клеток, синтезировать собственный аспарагин вследствие отсутствия аспарагинсинтетазы. Это приводит к нарушению синтеза белка, а также ДНК и РНК.
Фармакокинетика
При внутривенном введении максимальную концентрацию в плазме крови отмечают в первые минуты, при внутримышечном введении - через 14-24 ч. Связывание с белками плазмы крови составляет 30%. Аспарагиназа проникает в ретикуло-эндотелиальную систему, где происходит её медленное расщепление до неактивных веществ. Период полувыведения при в/в введении составляет 14-22 ч, при в/м - 39-49 ч.
При ежедневном применении препарата удаётся поддерживать его достаточный уровень в крови, причем следы фермента можно обнаружить в плазме крови ещё в течение 10 сут после окончания курса лечения.
Путь выведения препарата не установлен. В моче препарат выявляют только в следовых количествах.
Показания к применению и дозирование
В составе комбинированной терапии для индукции ремиссии при остром лимфобластном лейкозе, а также для лечения лимфобластных неходжкинских лимфом (лимфо- и ретикулосаркомы). Не рекомендуют использовать препарат в составе схем поддерживающей терапии вследствие быстрого развития резистентности к нему.
Препарат вводят в/в струйно, в виде медленной в/в инфузии (не менее 30 мин) или в/м.
Первые введения препарата необходимо осуществлять под наблюдением врача, имеющего опыт проведения противоопухолевой химиотерапии.
Аспарагиназу используют как в монотерапии, так и в ряде схем в комбинации с другими цитостатиками, в связи с чем при подборе индивидуальной дозы следует руководствоваться данными медицинской литературы.
Препарат назначают взрослым и детям в дозе 6000-10 000 МЕ/м2 поверхности тела в/в или в/м через день или ежедневно до достижения общей дозы не более 400 000 ME.
При в/м введении в одно место следует вводить не более 2 мл раствора. При необходимости введения более высокой дозы одномоментно необходимо делать несколько инъекций.
Перед введением препарата рекомендуют проводить внутрикожную пробу, несмотря на то, что её результаты не полностью достоверны в прогнозировании аллергических реакций на аспарагиназу.
Данную пробу следует проводить до первого введения препарата и в тех случаях, когда между введениями проходит 1 неделя или более длительный срок. Для этого необходимо растворить препарат в воде для инъекций до достижения концентрации аспарагиназы 100 ME/мл. Внутрикожно вводят 0,1 мл (около 10 ME) полученного раствора и наблюдают за реакцией в течение 1 ч. Развитие гиперемии или папулы более 1 см в диаметре свидетельствует о положительной реакции, поэтому аспарагиназу использовать для лечения не следует. При в/в применении, кроме того, рекомендуют введение пробной дозы в/в (1000 ME в/в в виде кратковременной инфузии за 1 ч до лечения).
Приготовление раствора. Порошок в дозе 5000 МЕ растворяют в 2 мл, а в дозе 10 000 МЕ - в 4 мл воды для инъекций. Для того чтобы избежать образования пены, струю воды следует медленно вливать по внутренней стенке флакона, при растворении не взбалтывать, а вращать флакон. Приготовленный раствор может слабо опалесцировать. Для в/м введения приготовленный раствор разбавлять не нужно. Для продолжительной в/в инфузии после растворения, согласно инструкции, рассчитанное количество аспарагиназы должно быть разведено в 250-500 мл, а для в/в струйного введения - в 20-40 мл физиологического раствора или 5% раствора глюкозы.
Побочные эффекты
Аллергические реакции: в 20-35% случаев возможно развитие реакции гиперчувствительности (сыпь и/или волдыри); иногда - анафилактический шок с летальным исходом, дыхательная недостаточность. Риск анафилаксии возрастает при повторном применении препарата. Однако развитие анафилактического шока возможно и при первом введении.
Следует учитывать, что через 2-5 ч после введения препарата могут возникнуть лихорадочные реакции в виде повышения температуры тела и озноба. Обычно эти явления проходят самостоятельно. В редких случаях возможно жизнеугрожающее повышение температуры тела (гиперпирексия).
Со стороны пищеварительной системы: нарушения функции поджелудочной железы, острый панкреатит, редко - геморрагический панкреатит. В некоторых случаях отмечалось формирование псевдоцист (в течение 4 мес после окончания лечения), поэтому пациента необходимо наблюдать в течение 4 мес после последнего введения препарата с помощью соответствующих методик (например, УЗИ). В случае повышения активности амилазы в сыворотке крови применение препарата должно быть прекращено (это возможно и после окончания терапии аспарагиназой); нарушения функции печени (повышение активности сывороточных трансаминаз, щелочной фосфатазы (ЩФ), лактатдегидрогеназы (ЛДГ) и уровня сывороточного билирубина). В ходе лечения возможно снижение уровня сывороточного альбумина. В некоторых случаях отмечался холестаз; были сообщения об одном случае желтухи и одном случае некроза клеток печени; возможно также появление тошноты, рвоты и анорексии.
Со стороны обмена веществ: снижение толерантности к глюкозе, уровня инсулина; часто - гипергликемия, требующая применения инсулина; возможно развитие кетоацидоза.
Со стороны свёртывающей системы крови: снижение уровня фибриногена, факторов X и XI, антитромбина III, протеина С и плазминогена; тромбоэмболия; в отдельных случаях отмечено развитие гемолитической анемии.
Со стороны мочевыделительной системы: редко - нарушение функции почек. В основе повышения уровня азота в сыворотке крови, как правило, лежит преренальный метаболический дисбаланс. Может быть выявлена гиперурикемия.
Со стороны центральной нервной системы: её угнетение (летаргия, патологическая сонливость, спутанность сознания); в некоторых случаях отмечались судороги.
Со стороны эндокринной системы: у небольшого числа больных наблюдался транзиторный и вторичный гипотиреоз, а также снижение уровня тироксин-связывающего белка.
Дерматологические реакции: описан случай развития токсического эпидермального некролиза (синдром Лайелла).
Передозировка
Симптомы: анафилаксия, гипергликемия, нарушения свёртываемости крови.
Лечение: специфический антидот не известен. Проводят симптоматичскую терапию, при развитии гипергликемии - инсулинотерапию, при нарушениях свёртываемости крови возможно применение свежезамороженной плазмы.
Противопоказания
Панкреатит на момент начала лечения или в анамнезе; аллергические реакции в анамнезе, связанные с приёмом аспарагиназы; выраженные нарушения функций печени и почек; беременность; период лактации (грудного вскармливания).
Беременность и кормление грудью
Препарат противопоказан к применению при беременности и в период грудного вскармливания.
Клинически значимые взаимодействия
Терапия винкристином или преднизолоном непосредственно до или одновременно с аспарагиназой увеличивает риск токсичности последней (усиление гипергликемического действия аспарагиназы, повышение риска развития невропатий, нарушение эритропоэза).
Аспарагиназа в зависимости от дозировки и момента применения синергически или антагонистически взаимодействует с метотрексатом и цитарабином. Предварительное примененение метотрексата и цитарабина синергично усиливает эффект аспарагиназы. Если аспарагиназу вводят первой, то её эффект может быть ослаблен метотрексатом или цитарабином.
Аспарагиназа может усиливать токсичность других препаратов, влияя на функцию печени.
Применение урикозурических противоподагрических препаратов может увеличивать риск нефропатии, связанной с повышенным образованием мочевой кислоты.
Резюме и дополнительные сведения
В случае развития аллергических реакций введение препарата следует немедленно прекратить. Необходимо принятие соответствующих мер: введение антигистаминных препаратов, глюкокортикоидов и препаратов, стабилизирующих гемодинамику.
При значительном снижении содержания факторов свёртываемости крови, особенно фибриногена, в случае клинической предрасположенности к кровотечениям необходима заместительная терапия свежезамороженной плазмой.
Рекомендован регулярный контроль содержания глюкозы в крови и моче, показателей свёртываемости крови.
В период лечения препаратом следует избегать употребления алкоголя.
Влияние на способность к вождению автотранспорта и управлению механизмами: аспарагиназа может снижать психомоторную реакцию и, соответственно, способность к вождению автотранспорта и управлению механизмами, особенно при одновременном приёме алкоголя.
Код АТХ
L01XX02
Торговые наименования, формы выпуска и производители
Используемые в России торговые наименования Asparaginase:
L-аспарагиназа /L-asparaginase/ª (Латвия, РФ).
Формы выпуска: лиофилизированный порошок для приготовления инъекционного раствора по 5 тыс. и 10 тыс. МЕ во флаконе.
Условия и сроки хранения
Препарат следует хранить в защищённом от света, недоступном для детей месте при комнатной температуре. Срок годности - 2 года.
РАЗНЫЕ ПРЕПАРАТЫ
Бисфосфонаты
Клодроновая кислота
Терапевтический класс АТХ
Ингибитор костной резорбции при злокачественных новообразованиях и метастазах в кости, группа бисфосфонатов.
Механизм действия и фармакологические эффекты
Подавляет активность остеокластов, вызывает повреждение их структуры, уменьшение размеров и количества. При гиперкальциемических состояниях понижает уровень кальция в плазме крови, а у пациентов с нормальным содержанием кальция в плазме крови уменьшает выделение с мочой кальция и гидроксипролина.
Фармакокинетика
Всасывание: после приёма внутрь абсорбируется 2-5% введённой дозы.
Распределение: связывание с белками плазмы - менее 2%, высокое сродство к костной ткани.
Выведение: период полувыведения - 2 часа. Период полувыведения из костей - до нескольких лет. До 80% препарата выделяется с мочой.
Показания к применению и дозирование
Режим дозирования
При среднетяжёлой и тяжёлой гиперкальциемии (концентрация ионов кальция в плазме более 3 ммоль/л) и/или при сильных болях в костях препарат назначают в дозе 3-5 мг/кг в/в капельно в течение 3-5 часов. Курс лечения - 3-5 дней. Уменьшение уровня кальция происходит на вторые сутки от начала лечения, нормализация - на 4-е сут, боли в костях прекращаются через 1-2 дня;
При раке молочной железы в начале лечения в дозе 2,4-3,2 г/сут, после нормализации уровня кальция и/или уменьшении болей в костях - 1,6 г/сут;
При небольшом метастатическом поражении и умеренных болях в костях назначают внутрь в дозе 1,6-3,2 г/сут. Боли обычно уменьшаются в течение 1-2 недель, уровень кальция приходит к норме через 7-10 дней.
Продолжительность приёма - от нескольких месяцев до нескольких (2 и более) лет. Дозу 1600 мг принимают одномоментно утром. Большую дозу делят на 2 приёма. Препарат рекомендуют принимать утром натощак за 1-1,5 ч до завтрака и вечером перед сном минимум через 1-1,5 ч после ужина. Его необходимо запивать достаточным количеством воды.
Побочные эффекты
Со стороны обмена веществ: очень редко - гипокальциемия, протекающая бессимптомно, вторичный гиперпаратиреоидизм.
Со стороны пищеварительной системы: у 2-10% больных - тошнота, рвота, диарея (слабо выражены, имеют транзиторный характер), редко - повышение активности трансаминаз печени.
Со стороны мочевыделительной системы: острая почечная недостаточность (после инъекции большой дозы клодроновой кислоты).
Прочие: реакции гиперчувствительности.
Передозировка
При повышении концентрации клодроновой кислоты в инфузионном растворе возможно развитие гипокальциемии, протекающей бессимптомно. В таких случаях инфузионную терапию следует прервать, после этого концентрация кальция в плазме крови нормализуется в течение 4 дней.
Противопоказания
Повышенная чувствительность к препарату, одновременный приём других бисфосфонатов, выраженные нарушения функции почек.
Беременность и кормление грудью
Данные о влиянии на репродуктивную функцию и развитие плода отсутствуют.
Клинически значимые взаимодействия
При одновременном применении с аминогликозидами может возникнуть выраженная гипокальциемия.
При одновременном применении с нестероидными противовоспалительными средствами отмечались случаи нарушения функции почек.
Клодроновую кислоту нельзя применять внутрь одновременно с лекарственными препаратами, содержащими двухвалентные катионы (кальция, железа, марганца), из-за возможности образования связей клодроната с этими катионами со снижением его эффективности.
Код АТХ
М05ВА02
Торговые наименования, формы выпуска и производители
БОНЕФОС® (BONEFOS®)ª, компания LEIRAS.
Форма выпуска: концентрат для приготовления раствора для инфузий (в ампулах по 5 мл). 1 ампула (5 мл) содержит 300 мг клодроновой кислоты (в форме динатриевой соли).
Памидроновая кислота
Терапевтический класс АТХ
Ингибитор костной резорбции при злокачественных новообразованиях и метастазах в кости, группа бисфосфонатов.
Механизм действия и фармакологические эффекты
Подавляет активность остеокластов, вызывает повреждение их структуры, уменьшение размеров и количества. Взаимодействует с кристаллами гидроксиапатита костной ткани, тормозит их образование и растворение. Препятствует поступлению предшественников остеокластов в костную ткань и ингибирует их превращение в зрелые клетки.
При гиперкальциемических состояниях понижает уровень кальция в плазме крови. В комбинации со стандартной противоопухолевой терапией памидронат замедляет прогрессирование метастазов в костях, стабилизирует существующие изменения, способствует развитию остеосклероза.
Фармакокинетика
Всасывание: после внутривенного введения 60 мг памидроновой кислоты максимальная концентрация препарата в течение часа составляет около 10 нмоль/л.
Распределение: связывание с белками плазмы - менее 54%. Не подвергается биотрансформации.
Выведение: период полувыведения из плазмы - 0,8 ч. До 55% препарата выделяется с мочой в неизменённом виде.
Показания к применению и дозирование
Режим дозирования
Заранее приготовленный раствор памидроновой кислоты вводят только внутривенно капельно, медленно. Скорость инфузии не должна превышать 1 мг/мин. Длительность инфузии - 2 ч.
Гиперкальциемия (концентрация ионов кальция в плазме более 3 ммоль/л). Препарат назначают в дозе 90 мг при разведении в 500 мл инфузионного раствора. Длительность инфузии должна составлять не менее 4 ч.
Остеолиз, индуцированный злокачественными опухолями, с сопутствующей гиперкальциемией. Суммарная доза памидроната составляет от 30 до 90 мг, может быть введена как однократно, так и в виде нескольких последовательных инфузий. Максимальная курсовая доза - не более 90 мг.
Существенное снижение уровня кальция в крови отмечают через 24-48 ч, а нормализацию - через 3-7 дней после введения памидроновой кислоты.
Побочные эффекты
Со стороны обмена веществ: наиболее часто - бессимптомная гипокальциемия, лихорадка в течение первых 48 ч, гриппоподобный синдром, вторичный гиперпаратиреоидизм.
Со стороны пищеварительной системы: иногда тошнота, рвота, диарея, анорексия, диспепсия, запор, гастрит.
Со стороны мочевыделительной системы: гематурия, острая почечная недостаточность, которая может развиться после инъекции большой дозы препарата.
Со стороны опорно-двигательного аппарата: транзиторные оссалгии, миалгии, артралгии.
Со стороны ЦНС: иногда - головная боль, парестезии, дезориентация, сонливость, бессонница, зрительные галлюцинации (редко).
Прочие: местно - боль, гиперемия, отёк, флебит, тромбофлебит, редко - мышечные судороги. Реакции гиперчувствительности: зуд, сыпь (редко), редко - анафилактические реакции (бронхоспазм, одышка, отёк Квинке).
Передозировка
При повышении концентрации памидроновой кислоты в инфузионном растворе возможно развитие гипокальциемии, протекающей бессимптомно. В таких случаях инфузионную терапию следует прервать, показано внутривенное введение кальция глюконата.
Противопоказания
Повышенная чувствительность к препарату, одновременный приём других бисфосфонатов, выраженные нарушения функции почек.
Беременность и кормление грудью
Отсутствуют клинические данные о влиянии на репродуктивную функцию и развитие плода. Кормление грудью следует прекратить.
Клинически значимые взаимодействия
При одновременном применении с кальцитонином может возникнуть суммация действия, выражаемая в ускоренном снижении уровня кальция в плазме.
При одновременном применении с цитостатиками не отмечалось развитие нежелательных взаимодействий. Памидроновая кислота несовместима с инфузионными растворами, содержащими кальций.
Код АТХ
М05ВА03
Торговые наименования, формы выпуска и производители
АРЕДИЯ® (AREDIA®)ª, компания NOVARTIS PHARMA.
Форма выпуска: лиофилизированное сухое вещество для инфузий (во флаконах по 5 и 10 мл). 1 флакон содержит 15, 30, 60 или 90 мг памидроновой кислоты (в форме динатриевой соли).
Золедроновая кислота
Терапевтический класс АТХ
Ингибитор костной резорбции при злокачественных новообразованиях и метастазах в кости, группа бисфосфонатов.
Механизм действия
Ингибирует активность остеокластов, вызывает повреждение их структуры, уменьшение размеров и количества. Взаимодействует с кристаллами гидроксиапатита костной ткани, тормозит их образование и растворение, оказывает антиангиогенное действие. Препятствует поступлению предшественников остеокластов в костную ткань и ингибирует их созревание.
При гиперкальциемических состояниях понижает уровень кальция в плазме крови. В комбинации со стандартной противоопухолевой терапией замедляет прогрессирование метастазов в костях, стабилизирует существующие изменения, способствует развитию остеосклероза.
Фармакокинетика
Всасывание: после внутривенного введения 60 мг золедроновой кислоты максимальная концентрация препарата в течение часа составляет около 10 нмоль/л.
Распределение: связывание с белками плазмы - менее 54%. Не подвергается биотрансформации.
Выведение: период полувыведения из плазмы - 0,8 ч. До 55% препарата выделяется с мочой в неизменённом виде.
Показания к применению и дозирование
Режим дозирования
Раствор золедроновой кислоты вводят только внутривенно капельно, в течение 15 минут.
Гиперкальциемия (концентрация ионов кальция в плазме более 3 ммоль/л). Препарат назначают в дозе 4 мг при разведении препарата в 500 мл инфузионного раствора.
Остеолиз, индуцированный злокачественными опухолями, с сопутствующей гиперкальциемией. Суммарная доза золедроната составляет 4 мг, в виде нескольких последовательных инфузий с интервалом в 3-4 недели.
Нормализация уровня кальция - через 5-7 дней после введения золедроновой кислоты. Достигнутый эффект отмечают в течение 30 дней после введения 4 мг и в течение 40 дней после введения 8 мг золедроновой кислоты.
При слабом или умеренном нарушении функции почек нет необходимости в коррекции дозы золедроната.
Побочные эффекты
Со стороны обмена веществ: бессимптомная гипокальциемия, гипофосфатемия, повышение уровня креатинина и мочевины в сыворотке крови, иногда - гипомагниемия, гипокалиемия, гипернатриемия.
Со стороны организма в целом: лихорадка в течение первых 48 ч, гриппоподобный синдром, иногда - астения, периферические отёки, увеличение массы тела (редко).
Со стороны пищеварительной системы: тошнота, рвота, диарея, редко - повышение активности трансаминаз печени.
Со стороны мочевыделительной системы: острая почечная недостаточность, гематурия, протеинурия.
Реакции гиперчувствительности: редко - ангионевротический отёк, кожный зуд.
Передозировка
При развитии клинически значимой гипокальциемии - назначение кальция глюконата.
Противопоказания
Повышенная чувствительность к препарату, одновременный приём других бисфосфонатов, беременность, лактация.
Беременность и кормление грудью
Препарат противопоказан.
Клинически значимые взаимодействия
При одновременном применении с цитостатиками, диуретиками, антибиотиками, анальгетиками негативного лекарственного взаимодействия не отмечено.
Код АТХ
М05ВА05
Торговые наименования, формы выпуска и производители
ЗОМЕТА® (ZOMETA®)ª, компания NOVARTIS PHARMA AG.
Форма выпуска: порошок для приготовления раствора для инъекций (во флаконах). 1 флакон содержит 4 мг золедроновой кислоты.
Ибандроновая кислота
Терапевтический класс АТХ
Ингибитор костной резорбции при злокачественных новообразованиях и метастазах в кости, группа бисфосфонатов.
Механизм действия и фармакологические эффекты
Селективное действие на костную ткань основано на высокой аффинности к минеральным компонентам кости. Подавляет усиленную резорбцию костной ткани. При гиперкальциемических состояниях понижает уровень кальция в плазме крови.
Фармакокинетика
Распределение: связывание с белками плазмы не зависит от концентрации ибандроновой кислоты и достигает 99%. Не подвергается биотрансформации.
Выведение: период полувыведения из плазмы - 10-16 ч. До 60% препарата выделяется с мочой в неизменённом виде. Остальное количество препарата связывает костная ткань.
Показания к применению и дозирование
Гиперкальциемия при злокачественных опухолях, в том числе - при наличии метастазов в костях.
Режим дозирования
Доза зависит от степени тяжести гиперкальциемии и типа опухоли. Раствор ибандроновой кислоты вводят только внутривенно капельно, в течение 2 ч, в 500 мл изотонического раствора натрия хлорида или 5% раствора глюкозы.
Гиперкальциемия (концентрация ионов кальция в плазме более 3 ммоль/л). Препарат назначают в дозе 4 мг при разведении препарата в 500 мл инфузионного раствора. При уровне кальция менее 3 ммоль/л достаточно разовой дозы 2 мг.
Нормализация уровня кальция наступает через 5-7 дней после введения ибандроновой кислоты. Достигнутый эффект сохраняется в течение 18-20 дней после введения 4 мг и в течение 26 дней после введения 6 мг ибандроновой кислоты.
Побочные эффекты
Со стороны обмена веществ: иногда - бессимптомная гипокальциемия, гипофосфатемия.
Со стороны организма в целом: в течение первых 48 ч - гриппоподобный синдром, не требующий лечения. Симптомы исчезают в течение нескольких часов или дней самостоятельно.
Со стороны пищеварительной системы: иногда - тошнота, рвота, диарея.
Реакции гиперчувствительности - крайне редко.
Передозировка
Данные об острой передозировке отсутствуют. При развитии клинически значимой гипокальциемии показано назначение кальция глюконата.
Противопоказания
Повышенная чувствительность к препарату, тяжёлая почечная недостаточность (уровень креатинина 442 мкмоль/л).
Беременность и кормление грудью
Препарат не следует применять в период беременности и лактации.
Клинически значимые взаимодействия
При одновременном применении с цитостатиками, диуретиками, антибиотиками, анальгетиками негативного лекарственного взаимодействия не отмечено. Рекомендовано соблюдать осторожность при использовании одновременно с аминогликозидами.
Торговые наименования, формы выпуска и производители
БОНДРОНАТ® (BONDRONAT®)ª, компания F. HOFFMANN-LA ROCHE.
Форма выпуска: концентрат для инфузий (в ампулах по 1 мл). 1 ампула содержит 1 мг ибандроновой кислоты (в виде натрия моногидроибандроната).
ПРЕПАРАТЫ ДЛЯ СОПРОВОДИТЕЛЬНОЙ ТЕРАПИИ
К ним относят лекарственные средства, обеспечивающие переносимость противоопухолевых препаратов и улучшающие качество жизни больных в процессе лечения.
Противорвотные препараты
Апрепитант
Терапевтический класс АТХ
Противорвотное средство, антагонист нейрокининовых рецепторов.
Механизм действия и фармакологические эффекты
Селективный высокоаффинный антагонист рецепторов нейрокинина 1 (NK1) субстанции Р. Антагонисты NK1 рецепторов предупреждают развитие рвоты, вызванной химиотерапевтическими препаратами, за счёт центрального механизма действия. Апрепитант проникает в головной мозг и связывается с мозговыми рецепторами нейрокинина. Обладая выраженным длительным центральным действием, апрепитант ингибирует как острую, так и отсроченную рвоту, вызванную цисплатином и другими высокоэметогенными цитостатиками, а также усиливает противорвотный эффект ондансетрона и дексаметазона.
Фармакокинетика
Всасывание: средняя биодоступность при приёме внутрь составляет приблизительно 60-65%, среднюю максимальную концентрацию препарата в плазме выявляют через 4 ч после приёма препарата. Приём капсулы одновременно с приёмом пищи не влияет на биодоступность препарата. Фармакокинетика в диапазоне клинических доз - нелинейная.
Распределение: связывается с белками плазмы более чем на 95%. Проникает через гематоэнцефалический барьер.
Метаболизм: подвергается интенсивному метаболизму в печени под действием CYP3A4 и, значительно реже, - CYP1A2 и CYP2C19.
Выведение: элиминируется в виде метаболитов с калом (86%) и с мочой (5%).
Фармакокинетика у детей не изучалась. Нет необходимости в коррекции дозы у пожилых пациентов, у пациентов с лёгкой и умеренной печёночной недостаточностью, с тяжёлой почечной недостаточностью и у больных, находящихся на гемодиализе. Опыта применения апрепитанта у больных с тяжёлой печёночной недостаточностью нет. Также не требуют коррекции дозы препарата в зависимости от пола и расовой принадлежности.
Показания к применению и дозирование
В комбинации с другими противорвотными препаратами показан для предупреждения острой и отсроченной тошноты и рвоты, вызываемых высоко- и умеренноэметогенными противоопухолевыми препаратами.
Режим дозирования: капсулы апрепитанта принимают вне зависимости от приёма пищи, в течение 3 дней в комбинации с кортикостероидами и антагонистами 5НТ3-рецепторов. Рекомендуемая доза составляет 125 мг перорально за 1 час до приёма цитостатиков в 1-ый день и по 80 мг один раз в день утром во 2-ой и 3-й дни.
Побочные эффекты
Большинство побочных эффектов были лёгкими или умеренно выраженными. Наиболее часто - икота (4,6%), слабость/утомляемость (2,9%), повышение АЛТ (2,8%), запор (2,2%), головная боль (2,2%) и анорексия (2,0%). Кроме того, отмечались следующие осложнения со стороны различных органов и систем.
Со стороны системы кроветворения: редко - анемия, фебрильная нейтропения.
Со стороны обмена веществ: жажда, снижение или повышение массы тела.
Со стороны центральной и периферической нервной системы: часто - головная боль, головокружение; редко - нарушение сновидений, памяти, дезориентация, эйфория, тревожность.
Со стороны органов зрения: редко - конъюнктивит.
Слуховые и вестибулярные нарушения: редко - шум в ушах.
Со стороны сердечно-сосудистой системы: редко - брадикардия.
Со стороны дыхательной системы: редко - фарингит, чихание, кашель, першение в горле.
Со стороны пищеварительной системы: часто - анорексия, икота, запор, диарея, диспепсия, отрыжка; редко - тошнота, рефлюкс, извращение вкуса, дискомфорт в эпигастрии, боли в животе, вздутие живота, энтероколит, стоматит.
Дерматологические реакции: редко - сыпь, акне, фотосенсибилизация, потливость, зуд.
Со стороны костно-мышечной системы: редко - мышечные спазмы, миалгии.
Со стороны мочевыделительной системы: редко - полиурия, дизурия, поллакиурия.
Со стороны биохимических показателей: часто - повышение уровня АЛТ и АСТ, редко - повышение активности ЩФ, гипергликемия; микрогематурия.
Передозировка
Данные по применению высоких доз апрепитанта без химиотерапии (до 600 мг однократно или по 375 мг ежедневно в течение 42 дней) свидетельствуют о хорошей переносимости препарата. В случае передозировки терапию апрепитантом следует прекратить, за пациентом установить наблюдение. Антидота нет. При необходимости - симптоматическая терапия.
Противопоказания
Повышенная чувствительность к апрепитанту и любому другому компоненту препарата; одновременное назначение с пимозидом, терфенадином, астемизолом и цизапридом, тяжёлая печёночная недостаточность (более 9 балов по шкале Чайлд-Пью).
Беременность
Исследований у беременных не проводилось. Применять при беременности не рекомендуют.
Кормление грудью
Данных о выделении апрепитанта с грудным молоком нет, однако при назначении препарата следует завершить грудное вскармливание.
Клинически значимые взаимодействия
Апрепитант не следует применять одновременно с пимозидом, терфенадином, астемизолом и цизапридом, метаболизм которых происходит под действием CYP3A4. Апрепитант индуцирует метаболизм варфарина, поэтому необходимо мониторировать МНО на фоне приёма препарата (уровень МНО может снижаться до клинически значимого значения). Нет клинически значимого влияния на фармакокинетику антагонистов 5НТ3-рецепторов. Применение апрепитанта вместе с цитостатиками (этопозид, винорелбин, таксаны), метаболизм которых происходит через CYP3A4, коррекции их доз не требует.
Резюме и дополнительные сведения
С осторожностью следует применять препарат у пациентов, одновременно получающих варфарин и лекарственные препараты, метаболизм которых происходит через CYP3A4.
У больных, получающих варфарин, необходимо мониторировать уровень МНО в течение 2 нед при каждом цикле химиотерапии.
Эффективность гормональных контрацептивов может быть снижена в период приёма и в течение 28 дней после окончания приёма апрепитанта.
Код АТХ
А04АД12
Торговые наименования, формы выпуска и производители
ЭМЕНД (EMEND®)ª, компания Мерк Шарп и Доум Б.В. (Нидерланды).
Форма выпуска: капсулы, каждая капсула содержит апрепинант в дозе 80 мг или 125 мг.
Ондансетрон
Терапевтический класс АТХ
Противорвотное средство, селективный антагонист серотониновых 5НТ3-рецепторов
Механизм действия и Фармакологические эффекты
Оказывает выраженное противорвотное действие, механизм которого окончательно не установлен. ондансетрон блокирует пусковые механизмы рвотного рефлекса путём подавления высвобождения серотонина в тонкой кишке под влиянием цитостатиков или лучевой терапии. Подавление тошноты и рвоты, связанной с химио- или лучевой терапией, по-видимому, происходит благодаря антагонистическому действию ондансетрона на серотониновые рецепторы нейронов центральной и периферической нервной системы.
Фармакокинетика
Всасывание: абсолютная биодоступность при приёме внутрь составляет приблизительно 60%, среднюю максимальную концентрацию препарата в плазме выявляют через 1,5 часа после приёма. После внутримышечного введения максимальная концентрация достигается через 10 минут.
Распределение: связывается с белками плазмы на 70-75%.
Выведение: период полувыведения - 3 часа (как после приёма внутрь, так и после парентерального введения), у пожилых больных возрастает до 5 часов. Элиминируется в виде метаболитов с калом (около 90%) и в неизменённом виде с мочой (менее 5%).
Показания к применению и дозирование
Режим дозирования
Дозы ондансетрона могут варьировать в диапазоне 8-32 мг/сут в соответствии с указанными ниже критериями.
Взрослым при тошноте и рвоте, вызванных цитотоксической или лучевой терапией, назначают внутрь по 8 мг (в виде сиропа, таблеток, ректальных свечей, в/м или в/в медленно) за 1-2 ч до начала введения цитостатиков с последующим приёмом ещё 8 мг внутрь через 12 ч. При назначении высокоэметогенной химиотерапии рекомендуемая доза для приёма внутрь - 24 мг (одновременно с дексаметазоном в дозе 12 мг за 1-2 ч до начала химиотерапии). В течение последующих 5 дней - по 8 мг 2 раза в сутки.
У больных с умеренным и тяжёлым нарушением функции печени и почек клиренс препарата снижен, поэтому не рекомендуют назначение ондансетрона в дозах, превышающих 8 мг/сут.
Побочные эффекты
Большинство побочных эффектов были лёгкими или умеренно выраженными.
Со стороны центральной и периферической нервной системы: головная боль, судороги (преходящие).
Со стороны сердечно-сосудистой системы: приливы, боли в грудной клетке (редко), аритмии, брадикардия, артериальная гипотензия.
Со стороны пищеварительной системы: икота, запор, диарея, диспепсия, транзиторное повышение активности трансаминаз.
Аллергические реакции: редко - по типу гиперчувствительности немедленного типа (в том числе анафилаксия).
Местные реакции: редко - местные реакции в области инъекции, ощущение жжения в области ануса и прямой кишки после введения суппозитория.
Передозировка
Данные о передозировке ондансетрона ограничены. При подозрении на передозировку - симптоматическая терапия.
Противопоказания
Повышенная чувствительность к препарату.
Беременность
Исследований у беременных не проводилось. Применять при беременности не рекомендуют.
Кормление грудью
Данных о выделении препарата с грудным молоком нет, однако при назначении препарата необходимо завершить грудное вскармливание.
Клинически значимые взаимодействия
Изменение клиренса ондансетрона происходит при одновременном применении с индукторами или ингибиторами микросомальных ферментов печени - изоферментов цитохрома Р450 (барбитураты, карбамазепин, рифампицин, фенилбутазон, циметидин, аллопуринол).
Код АТХ
А04АА01
Торговые наименования, формы выпуска и производители
Формы выпуска: таблетки (по 4 мг и 8 мг), таблетки лингвальные (по 4 мг и 8 мг), сироп (по 50 мл во флаконе), раствор для инъекций (ампулы по 2 мл), суппозитории (по 16 мг).
Форма выпуска: раствор для инъекций (флаконы по 2 мл и 4 мл).
Формы выпуска: таблетки (по 4 мг и 8 мг), раствор для инъекций (ампулы по 2 мл и 4 мл).
Гранисетрон
Терапевтический класс АТХ
Противорвотное средство, селективный антагонист серотониновых 5НТ3-рецепторов
Механизм действия и фармакологические эффекты
Оказывает выраженное селективное блокирующее действие на рецепторы серотонина подтипа 3 (5НТ3). Гранисетрон блокирует пусковые механизмы рвотного рефлекса путём подавления высвобождения серотонина в тонкой кишке под влиянием цитостатиков или лучевой терапии. Подавление тошноты и рвоты, связанной с химио- или лучевой терапией, происходит благодаря антагонистическому действию гранисетрона на серотониновые рецепторы нейронов центральной и периферической нервной системы.
Фармакокинетика
Всасывание: быстрое и полное, биодоступность при пероральном приёме снижена до 60%.
Распределение: после 5-минутной инфузии гранисетрона в дозе 40 мкг/кг объём распределения был равен 2-3 л/кг. Связывается с белками плазмы в умеренной степени (65%).
Выведение: период полувыведения - 4-5 ч у здоровых добровольцев, 9-12 ч у больных раком (после парентерального введения), 6,5 ч (при приёме внутрь). Элиминируется в виде метаболитов с калом (около 85%) и в неизменённом виде с мочой (11-15%).
Показания к применению и дозирование
Режим дозирования
Внутрь взрослым при тошноте и рвоте, вызванных цитотоксической или лучевой терапией, назначают:
Курс профилактического лечения - до 5 дней.
Применение препарата у пожилых больных, а также у больных с умеренным и тяжёлым нарушением функции печени и почек корректировки дозы не требует.
Побочные эффекты
Большинство побочных эффектов были лёгкими или умеренно выраженными.
Со стороны центральной и периферической нервной системы: головная боль, астения, слабость, головокружение, бессонница, извращение вкуса, редко- тревога, беспокойство.
Со стороны сердечно-сосудистой системы: обмороки, боли в грудной клетке (редко), аритмии, брадикардия, артериальная гипотензия.
Со стороны пищеварительной системы: редко - анорексия, диспепсия, транзиторное повышение активности трансаминаз.
Аллергические реакции: редко - аллергические реакции немедленного типа (крапивница, кожная сыпь), анафилаксия, лихорадка.
Передозировка
Данные о передозировке гранисетрона ограничены. Специфического антидота не существует. При подозрении на передозировку - симптоматическая терапия.
Противопоказания
Повышенная чувствительность к препарату.
Беременность
Контролируемых исследований у беременных не проводилось. Применять при беременности не рекомендуют.
Кормление грудью
Данных о выделении препарата с грудным молоком нет, однако при назначении препарата необходимо завершить грудное вскармливание.
Клинически значимые взаимодействия
Не происходит изменения клиренса гранисетрона при одновременном применении с индукторами или ингибиторами микросомальных ферментов печени - изоферментов цитохрома Р450 (барбитураты, карбамазепин, рифампицин, фенилбутазон, циметидин, аллопуринол). Гранисетрон не влияет на активность ферментов подсемейства 3А4 системы цитохрома Р450.
Код АТХ
A04AA02
Торговые наименования, формы выпуска и производители
КИТРИЛ (KYTRIL®)ª, компания F. HOFFMANN-LA ROCHE.
Формы выпуска: таблетки (содержат гранисетрона гидрохлорид в дозе 1 мг), раствор для инъекций (ампулы по 1 мл и 3 мл, содержат гранисетрона гидрохлорид в дозе 1 мг или 3 мг).
Трописетрон
Терапевтический класс АТХ
Противорвотное средство, селективный антагонист серотониновых 5НТ3-рецепторов.
Механизм действия и фармакологические эффекты
Сильнодействующий и высокоселективный конкурентный антагонист рецепторов серотонина подтипа 3 (5НТ3). Трописетрон блокирует пусковые механизмы рвотного рефлекса путём подавления высвобождения серотонина в тонкой кишке под влиянием цитостатиков, лучевой терапии или в послеоперационном периоде. Трописетрон селективно блокирует возбуждение пресинаптических 5НТ3-рецепторов на периферических нейронах центральной и периферической нервной системы. Длительность действия составляет 24 ч, что позволяет применять его 1 раз в сутки.
Фармакокинетика
Всасывание: из желудочно-кишечного тракта быстрое и полное (более чем на 95%), биодоступность при пероральном приёме - около 60%. Максимальную концентрацию в плазме отмечают через 3 ч.
Распределение: связывается с белками плазмы (в основном с альфа1-гликопротеинами) на 71%. Метаболизм трописетрона происходит путём гидроксилирования в печени.
Выведение: период полувыведения - от 8 до 45 ч. Элиминируется в виде метаболитов с калом и мочой (соотношение содержания метаболитов в кале и моче составляет 1:5).
Показания к применению и дозирование:
Режим дозирования
Взрослым внутрь в виде капсул и внутривенно (по 5 мг за 1 ч до начала введения цитостатиков). В последующие 5 дней приём по 5 мг в сутки перорально.
С целью достижения максимального клинического эффекта рекомендуют дополнительное назначение дексаметазона.
У пожилых больных, а также у больных с умеренным и тяжёлым нарушением функции печени и почек нет необходимости в корректировке дозы.
Побочные эффекты
Большинство побочных эффектов были транзиторными, лёгкими или умеренно выраженными.
Со стороны центральной и периферической нервной системы: головная боль, астения, слабость, головокружение, бессонница, извращение вкуса, редко - тревога, беспокойство.
Со стороны сердечно-сосудистой системы: обмороки, боли в грудной клетке (редко), аритмии, брадикардия, артериальная гипотензия.
Со стороны пищеварительной системы: редко - анорексия, диспепсия, транзиторное повышение активности трансаминаз, диарея.
Аллергические реакции: редко - аллергические реакции немедленного типа (крапивница, бронхоспазм, кожная сыпь), анафилаксия, лихорадка.
Передозировка
Данные о передозировке трописетрона ограничены. При повторном применении очень высоких доз препарата наблюдались зрительные галлюцинации, повышение артериального давления. Специфического антидота не существует. При подозрении на передозировку - симптоматическая терапия.
Противопоказания
Повышенная чувствительность к препарату или любым другим компонентам препарата, беременность и кормление грудью.
Беременность
Контролируемых исследований у беременных не проводилось. Применять при беременности не рекомендуют.
Кормление грудью
Данных о выделении препарата с грудным молоком нет, однако при назначении препарата необходимо завершить грудное вскармливание.
Клинически значимые взаимодействия
При одновременном применении с индукторами микросомальных ферментов печени - изоферментов цитохрома Р450 (например, рифампицин, барбитураты) концентрация трописетрона в плазме снижается. Влияния ингибиторов ферментной системы цитохрома Р450 (например, циметидин, аллопуринол) на уровень трописетрона не выявлено.
Код АТХ
A04AA03
Торговые наименования, формы выпуска и производители
НАВОБАН (NAVOBAN®)ª, компания NOVARTIS.
Формы выпуска: капсулы (содержат трописетрона гидрохлорид в дозе 5 мг), раствор для инъекций (ампулы по 5 мл, содержат трописетрона гидрохлорид в дозе 5 мг).
Другие средства
Уромитексанª (МНН - месна, 2-меркаптоэтансульфонат натрия)
Терапевтический класс АТХ
Антидот акролеина, метаболита противоопухолевых средств из группы оксазафосфоринов.
Механизм действия
Метаболит ифосфамида и циклофосфамида акролеин оказывает раздражающее действие на слизистую оболочку мочевого пузыря. Защитные свойства месны обусловлены взаимодействием с двойной связью молекулы акролеина, что приводит к образованию стабильного тиоэфира. Уменьшение уротоксических эффектов не приводит к ослаблению противоопухолевого действия препаратов.
Фармакокинетика
Распределение: связывание с альбумином и иммуноглобулинами составляет 9,7%.
Выведение: пик выведения наступает через 2-3 часа после внутривенного введения месны. Период полувыведения составляет от 0,17 до 1,08 ч. Полностью выводится почками через 8 ч. Скорость выведения одинакова при приёме внутрь и внутривенном введении.
Показания к применению и дозирование
Локальная детоксикация урологических эффектов цитостатиков - производных оксазафосфоринов, в том числе в следующих случаях:
Режим дозирования
Вводят внутривенно струйно медленно, разовая доза составляет 20% от разовой дозы оксазафосфорина. Первую инъекцию препарата проводят одновременно с первым введением оксазафосфорина, вторую и третью - через 4 и 8 ч после введения цитостатика.
При непрерывной инфузии ифосфамида или циклофосфамида в течение 24 ч месну вводят в дозе 20% от дозы цитостатика в начале инфузии, затем - в дозе 100% от дозы цитостатика в виде 24-часовой инфузии и, по окончании введения цитостатика, продолжают введение данного препарата ещё в течение 6-12 ч в той же дозе.
Побочные эффекты
Со стороны пищеварительной системы возможны тошнота, рвота, диарея, а также гематурия, аллергические реакции на коже и слизистых оболочках (редко).
Передозировка
Токсического влияния на гемопоэз, функции печени и почек, ЦНС не отмечено. Антидот месны не известен.
Противопоказания
Повышенная чувствительность к препарату.
Беременность и кормление грудью
В экспериментальных исследованиях тератогенное и эмбриотоксическое действие месны не выявлено.
Клинически значимые взаимодействия
Не оказывает влияния на метаболизм и противоопухолевую активность доксорубицина, кармустина, цисплатина, метотрексата, винкристина, сердечных гликозидов.
Резюме и дополнительные сведения
Месна совместима в водных растворах с циклофосфамидом и ифосфамидом, препараты можно вводить в одном растворе. Не следует смешивать с цисплатином в одном инфузионном растворе из-за инактивации последнего.
Код АТХ
V03AF01
Торговые наименования, формы выпуска и производители
МЕСНА® (MESNA®)ª, компания ASTA MEDICA.
Форма выпуска: раствор для инъекций (в ампулах по 2 мл и 4 мл). 1 ампула содержит 100 и 200 мг препарата.
Дексразоксан
Терапевтический класс АТХ
Комплексообразующее соединение, аналог этилендиаминтетрауксусной кислоты.
Механизм действия и фармакологические эффекты
Оказывает кардиопротективное действие на фоне терапии антрациклиновыми антибиотиками. Механизм окончательно не установлен; предполагают, что дексразоксан в миокарде гидролизуется с образованием соединения, молекулы которого связывают ионы железа и меди и препятствует образованию комплекса антрациклин-железо, предотвращая, тем самым, образование кардиотоксичных свободных радикалов кислорода.
Фармакокинетика
Распределение: после внутривенного введения быстро распределяется в тканях, создавая высокие концентрации в печени и почках. Связывание с белками плазмы - менее 2%. Не проходит через гематоэнцефалический барьер.
Выведение: до 40% препарата выделяется с мочой. У больных с почечной недостаточностью выведение дексразоксана снижено.
Показания к применению и дозирование
Профилактика кардиомиопатии при проведении цитотоксической терапии антрациклинами у следующих групп больных:
Режим дозирования: лечение начинают одновременно с введением первой дозы цитостатика. Препарат вводят внутривенно в течение 20-30 мин, за 45-60 мин до введения антрациклинового антибиотика. Разовая доза превышает дозу антрациклинового антибиотика в 20 раз. Для обычной дозы доксорубицина (по 50 мг/м2 с интервалом в 21 день) доза дексразоксана должна составлять 1000 мг/м2.
Побочные эффекты
Возможны тошнота, рвота, снижение уровня гемоглобина, сывороточного железа, транзиторная лейкопения и тромбоцитопения, редко - изменение цвета ногтей, флебит в месте введения.
Противопоказания
Повышенная чувствительность к дексразоксану, беременность и кормление грудью.
Беременность и кормление грудью
Противопоказано.
Передозировка
Симптомы: тошнота, рвота, диарея, лейкопения, алопеция, кожные реакции. Лечение симптоматическое. Специфического антидота нет.
Клинически значимые взаимодействия
С осторожностью - при нарушении функции печени; при почечной недостаточности - снижение клиренса дексразоксана с увеличением гематотоксического действия.
Торговые наименования, формы выпуска и производители
КАРДИОКСАН® (CARDIOXAN®)ª, компания CHIRON.
Форма выпуска: лиофилизированное сухое вещество для инфузий (во флаконах). 1 флакон содержит 500 мг дексразоксана гидрохлорида.
Особенности химиотерапии при сопутствующих заболеваниях
Заболевания сердечно-сосудистой системы
С повышением продолжительности жизни увеличивается доля пожилых людей во всем мире, особенно в развитых странах, поэтому следует ожидать возрастания количества больных онкологическими заболеваниями среди пожилых. Разработанные за последние 30 лет диагностические и лечебные стратегии привели к колоссальному увеличению числа людей, перенесших злокачественное заболевание. Благодаря эффективности лечения детских онкологических заболеваний 5-летняя выживаемость увеличилась с 25% в 60-х гг. XX века до 75% в конце 90-х гг. XX века. По оценкам Национального института рака и Центра по контролю и профилактике заболеваний в США к 2003 г. зарегистрировано более 10 млн человек, перенёсших онкологическое заболевание. В Великобритании в настоящее время проживает более 30 000 людей, которые выздоровели от онкологического заболевания, а 1 из 715 ныне живущих молодых людей в детстве лечились от онкологического заболевания. По расчётам, 60% взрослых с впервые установленным диагнозом онкологического заболевания проживут 5 и более лет. Однако новообразование и лечение существенно сказываются на качестве жизни этих людей. У выживших значительно повышен риск заболеваемости и даже смертности из-за отсроченного результата перенесённого онкологического процесса и химиолучевого лечения.
Хорошо известно, что противоопухолевые препараты оказывают негативное влияние на различные органы и системы больных. Чаще токсическое воздействие отмечают в тканях, состоящих из быстро делящихся клеток (кроветворная ткань, ЖКТ). Побочные эффекты обычно спонтанно регрессируют без отдалённых последствий. Однако миокард состоит из клеток с ограниченным регенеративным потенциалом, поэтому сердце восприимчиво к необратимому побочному действию химиопрепаратов.
Антрациклиновая кардиотоксичность
Открытые в 60-х гг. XX века антрациклиновые антибиотики в настоящее время широко используют в качестве противоопухолевых препаратов. Они эффективны при лечении гемобластозов и солидных опухолей, как в детской практике, так и при лечении взрослых. Эффективность этих препаратов зависит от дозы: при уменьшении дозы снижается выживаемость пациентов и продолжительность ремиссии заболевания. Антрациклиновые антибиотики в дозах, оказывающих достаточное противоопухолевое действие обладают выраженной кардиотоксичностью у пациентов с онкологическими заболеваниями.
Этиология и патогенез
Факторами риска развития хронической и отсроченной антрациклиновой кардиотоксичности, по всей вероятности, служат кумулятивная доза антрациклинов, одновременное примененеие других химиотерапевтических препаратов (фторурацил, циклофосфамид, интерферон, блеомицин, цисплатин), облучение средостения, женский пол, пожилой или молодой возраст, артериальная гипертензия и предшествующие заболевания сердца. Возможно острая вирусная инфекция, увеличение гемодинамической нагрузки, избыточная масса тела, беременность, хирургическое вмешательство, злоупотребление наркотическими средствами - пусковые моменты развития отсроченной кардиомиопатии и сердечной недостаточности. Основным фактором риска развития повреждения миокарда считают кумулятивную дозу антрациклинов. Риск возрастает пропорционально общей кумулятивной дозе и не имеет линейной зависимости: по данным ряда авторов, риск развития антрациклиновой кардиотоксичности составляет 18% при суммарной дозе доксорубицина 700 мг/м2 поверхности тела и 3% и менее при дозе 400 мг/м2 поверхности тела. Однако, возможно, имеет значение индивидуальная чувствительность больного к антрациклиновым антибиотикам. Некоторые пациенты хорошо переносят приём препарата в дозах выше 1000 мг/м2 поверхности тела. Наряду с этим, иногда наблюдают снижение фракции выброса левого желудочка при ЭхоКГ в случаях назначения антрациклиновых антибиотиков в дозе менее 300 мг/м2 поверхности тела. Более того, в образцах, полученных при эндомиокардиальной биопсии, возможны гистопатологические изменения, характерные для антрациклин-индуцированой кардиотоксичности при применении антрациклиновых антибиотиков в дозе не превышающей 180 мг/м2 поверхности тела. Таким образом, вероятно, не существует безопасной дозы антрациклиновых антибиотиков.
Точные механизмы кардиотоксического действия антрациклиновых антибиотиков до конца не изучены. Было предложено несколько гипотез для объяснения токсического действия антрациклинов на миокард.
-
В исследованиях, проведённых in vivo и in vitro, показано, что антрациклиновые антибиотики действуют непосредственно на транскрипцию генов, связываясь с ядерными транскрипционными факторами и, таким образом специфически нарушают синтез белков кардиальных волокон.
-
Антрациклиновые антибиотики вызывают активацию кальциевых каналов, в результате чего возникает повреждение миоцитов из-за избытка кальция.
-
Другими возможными механизмами считают нарушение функций адренергических нервных волокон миокарда, обусловленное ухудшением регуляции миокардиальных a-адренергических рецепторов, освобождение вазоактивных аминов и провоспалительных цитокинов.
-
Антрациклиновые антибиотики индуцируют высвобождение фактора некроза опухолей (TNF-a) и интерлейкина-2 из моноцитов. Эти цитокины, воздействуя на соответствующие рецепторы кардиомиоцитов, могут оказывать цитотоксическое действие, приводя к кардиомиопатии.
-
Однако большинство исследователей считают основным звеном патогенеза антрациклин-индуцируемой кардиотоксичности воздействие на миокард свободных радикалов. В процессе метаболизма доксорубицина образуются свободные радикалы и перекись водорода. Эти высокотоксичные соединения взаимодействуют с нуклеиновыми кислотами, белками и липидами. Наиболее вероятной мишенью токсического влияния антрациклиновых антибиотиков служат мембраны митохондрий. Кардиолипин - основной компонент мембраны митохондрий, содержащий много полиненасыщенных жирных кислот. Антрациклиновые антибиотики, активируя процесс перекисного окисления липидов, способствуют повреждению митохондриальных мембран и инактивации основных ферментов дыхательной цепи в митохондриях.
Предполагают, что локализация поражения именно в сердце при системном введении антрациклиновых антибиотиков обусловлено низким уровнем каталазной активности в кардиомиоцитах. Каталаза - основной фермент необходимый для разрушения перекиси водорода, образуемой в результате пероксисомальных аэробных дегидрогеназных реакций. Активность каталазы наиболее высока в печени и эритроцитах. Её активность также сравнительно высока в почках, жировой ткани, лёгких и поджелудочной железе, а наиболее низка - в сердце и мозге. Было показано, что активность каталазы в кардиомиоцитах человека, мыши или крысы составляет примерно 2% от аналогичного показателя в печени.
Клиническая картина
Описано три типа антрациклиновой кардиотоксичности.
-
Острая, или ранняя кардиотоксичность ассоциирована с назначением сравнительно низкой кумулятивной дозы и может возникать даже после однократного введения препарата. Эта форма кардиотоксичности развивается редко. При этом возможны преходящие аритмии, синдром перикардита-миокардита и острая левожелудочковая недостаточность. На ЭКГ чаще обнаруживают неспецифические изменения сегмента ST и зубца Т, снижение вольтажа комплекса QRS и удлинение интервала Q-T. Самой частой формой нарушения ритма бывает синусовая тахикардия, однако иногда отмечают желудочковую, наджелудочковую и узловую тахикардию.
-
При использовании антрациклиновых антибиотиков возможно хроническое поражение сердца с развитием кардиомиопатии. Эта форма заболевания бывает самой распространённой и клинически наиболее важной. Хроническая кардиотоксичность формируется в течение первого года лечения и может приводить к необратимой застойной сердечной недостаточности и летальному исходу. На основании эмпирических данных считают, что предельная доза при терапии антрациклиновыми антибиотиками составляет 550 мг/м2 поверхности тела. В недавних исследованиях при помощи Эхо-КГ было отмечено практически полное восстановление сократительной способности миокарда, если терапия антрациклинами прекращается при появлении минимальных признаков кардиотоксичности. Однако и в этом случае не исключено снижение функционального резерва миокарда в будущем.
-
Поздняя кардиотоксичность, вызывающая отсроченную дисфункцию левого желудочка и аритмии, возникает спустя годы после окончания терапии после длительного бессимптомного периода. Выраженность ЭхоКГ признаков поражения возрастает при увеличении времени наблюдения за пациентами.
Диагностика
Для диагностики и контроля кардиотоксичности, индуцированной антрациклиновыми антибиотиками, необходим чувствительный и специфичный метод. Неоднократно пытались использовать для ранней диагностики миокардиального повреждения рутинные методы исследования (ЭКГ и определение концентрации кардиоспецифических маркеров), однако, они оказались весьма неспецифичными.
Наиболее чувствительным индикатором поражения сердца служит эндомиокардиальная биопсия. Тем не менее, её широко не используют, поскольку для точной оценки состояния миокарда необходимо повторное динамическое исследование, что весьма затруднительно, особенно в детской практике.
В последние годы благодаря доступности и возможности динамического контроля часто применяют неинвазивные методы оценки состояния миокарда [радионуклидную ангиокардиографию (РАКГ) и ЭхоКГ)]. Значимость этих методов диагностики многие авторы оценивают по-разному. В большинстве работ функции сердца у взрослых больных гемобластозами оценивали с помощью комплекса исследований: ЭКГ, ЭхоКГ, РАКГ. Признаки кардиотоксичности считают совокупность одной или более следующих аномалий.
Выраженность этих нарушений возрастала с увеличением времени наблюдения. С помощью нагрузочной РАКГ можно улучшить диагностику ранней субклинической кардиотоксичности, однако, специфичность этого исследования без динамического серийного тестирования низкая, а значительные повторные нагрузки ослабленные больные могут переносить крайне трудно. Таким образом, для мониторинга за развитием антрациклин-индуцированной кардиотоксичности, несмотря на ограниченную чувствительность наиболее широко используют РАКГ и Эхо-КГ.
Учитывая, что одним из возможных механизмов кардиотоксического действия антрациклиновых антибиотиков служит нарушение функций адренергических нейронов, был предложен метод оценки целостности сердечных адренергических нейронов. Для этого применяют радиоактивный препарат (метайодобензилгуанидин-123), по накоплению которого в неповрежденных нейронах судят о величине повреждения кардиомиоцитов. Испытывают также моноклональные антитела против кардимиоцитов, меченые индием, которые реагируют только с поврежденными кардиомиоцитами. Достоинства и недостатки этих методов всё ещё обсуждают.
Лечение
Мероприятия, направленные на снижение кардиотоксического влиияния антрациклиновых антибиотиков, не должны затрагивать противоопухолевую активность этих лекарственных средств. Выделяют 3 подхода для предупреждения лекарственной токсичности.
-
Метод лекарственного разведения. Было замечено, что у взрослых риск развития кардиотоксичности при длительной инфузии доксорубицина (от 48 до 96 ч) меньше, чем при короткой инфузии или болюсном введении препарата. Однако в настоящее время недостаточно данных о том, что противоопухолевая активность лекарственного средства при длительной инфузии не снижается по сравнению с традиционным способом введения.
-
Другим подходом предупреждения лекарственной токсичности служит направленный транспорт лекарства в опухолевые клетки. Антрациклины, заключенные в липосомы, преимущественно попадают в опухоль, а не в миокард. При этом было обнаружено резкое снижение накопления антибиотика в ткани миокарда, из-за чего, возможно, и уменьшается кардиотоксичность. Один из подобных препаратов - пегилированный липосомальный доксорубицина гидрохлорид, который имеет значительно больший период полувыведения (52-55 ч) по сравнению с традиционной лекарственной формой доксорубицина (менее 10 мин). Липосомы, благодаря пролонгированной циркуляции и способности проникать через "дефекты" капилляров, питающих опухоль, аккумулируются в опухолевой ткани, в результате чего, внутриклеточная концентрация лекарственного средства в новообразовании в 10 раз превышает данный показатель в нормальных тканях. При введении пегилированного липосомального доксорубицина свободного доксорубицина практически нет в плазме крови, поэтому токсическое воздействие препарата на нормальные ткани уменьшается (в том числе на миокард).
-
Третий подход заключается в использовании веществ со специфическим защитным влиянием на миокард. Поскольку наиболее вероятным механизмом кардиальной токсичности антрациклиновых антибиотиков служит повреждающее влияние свободных радикалов и перекиси водорода при участии ионов железа, то проводили испытания препаратов с железосвязывающей и антиоксидантной активностью (витамин E, ацетилцистеин, цистамин, дефероксамин, пробукол, флавоноиды) в качестве возможных кардиопротекторов. К сожалению, результаты данных исследований противоречивы, и достоверного снижения кардиотоксического влияния антрациклиновых антибиотиков не было отмечено. Наибольшее число работ посвящено исследованию кардиопротективного влияния дексразоксана (ICRF-187). Механизм действия этого препарата не вполне изучен. Известно, что дексразоксан проникая внутриклеточно, связывает ионы железа и блокирует образование свободных радикалов и перекиси водорода. При первом клиническом испытание дексразоксана кардиопротективное действие препарата было отмечено у 92 женщин, принимавших фторурацил, циклофосфамид и доксорубицин по поводу РМЖ. В нескольких клинических испытаниях, проведённых на взрослых пациентах, основной задачей было не только установить степень кардиопротективного действия дексразоксана при включении его в программы химиотерапии с назначением антрациклиновых антибиотиков, но также определить влияние дексразоксана на вероятность достижения ремиссии и её продолжительность. Открыт вопрос о возможности увеличения дозы антрациклиновых антибиотиков с целью эрадикации опухоли при одновременном назначении дексразоксана, если новообразование оказывается чувствительной к химиотерапии. Имеются данные о том, что дексразоксан может усиливать цитотоксическую активность противоопухолевых препаратов (выраженность и длительность миелосупрессии была выше в группе больных, получавших дексразоксан).
Раннее лечение субклинической антрациклин-индуцированной систолической дисфункции ингибиторами АПФ и, возможно, b-адреноблокаторами следует считать разумным подходом снижения смертности у пациентов. Терапия застойной сердечной недостаточности, обусловленной антрациклиновыми антибиотиками, не отличается от лечения сердечной недостаточности, вызванной другими причинами, т.е. показано комплексное применение ингибиторов АПФ, диуретиков, сердечных гликозидов и вазодилататоров. Длительное (до 1,5-2 лет) назначение этих препаратов приводит, как правило, к регрессии признаков хронической сердечной недостаточности и помогает поддерживать функцию сердца в относительно компенсированном состоянии. К сожалению, это в дальнейшем возможны рецидив и прогрессирования заболевания. Прогноз у больных с антрациклиновой кардиотоксичностью (как ранней, так и отсроченной) также как и при других формах сердечной недостаточности плохой. У пациентов с длительной и устойчивой ремиссией онкологического заболевания и развившейся в результате терапии антрациклиновыми антибиотиками застойной сердечной недостаточностью трансплантацию сердца рассматривают в качестве мероприятия для увеличения продолжительности и улучшения качества жизни.
По прогнозам ВОЗ в следующие 5 лет только в США 1 из 900 молодых людей в возрасте от 15 до 45 лет излечится от рака. К 2010 г. число таких лиц достигнет 250 000. Во многих случаях успех лечения будет достигнут благодаря назначению антрациклиновых антибиотиков. Поскольку, значительное миокардиальное повреждение возможно даже при низкодозной антрациклиновой терапии и весьма часто развивается при использовании препаратов в терапевтических дозах, заболеваемость и смертность, обусловленные антрациклин-индуцированной кардиотоксичностью, вероятно, будут возрастать в ближайшие годы. Положение усугубляется тем, что в настоящее время нет достаточно чувствительного метода диагностики незначительных повреждений сердечной мышцы на ранних этапах лечения. Эффективные фармакологические средства кардиопротекции только разрабатываются.
Гепаторенальная система
Поражение почек
Нарушения функций почек нередко осложняют течение онкологических заболеваний и проведение противоопухолевого лечения. Поражение почек часто отмечают при неходжкинских лимфомах, лимфогранулематозе, лейкозах и миеломной болезни. Солидные опухоли в почки метастазируют редко. Специфические формы нарушения функций почек у онкологических больных перечислены ниже.
Большинство противоопухолевых препаратов выделяется почками, а некоторые лекарственные средства (тиотепа, метотрексат, блеомицин, цисплатин и другие) метаболизируются в этих органах. Экскреция с мочой происходит путём клубочковой фильтрации и канальцевой секреции. Большое значение имеет реабсорбция препаратов в почечных канальцах. При почечной недостаточности клубочковая фильтрация снижается, и выведение лекарственных средств нарушается, что приводит к увеличению их концентрации в крови.
Основным механизмом повреждающего действия цитостатиков на почки служит непосредственная цитотоксичность и аутоиммунный характер поражения.
Степень токсического поражения почек зависит от дозы препарата, наличия сопутствующей почечной патологии, клиренса креатинина, объёма конечной мочи и изменения метаболизма цитостатиков в печени. Чаще нарушения функций почек у онкологических больных проявляются в виде канальцевой дисфункции, острой почечной недостаточности (вследствие острого канальцевого некроза) или хронической почечной недостаточностью (развившейся в результате необратимого уменьшения количества функционирующих нефронов). Остро возникающие в процессе лечения или опухолевой прогрессии почечные осложнения обычно можно предотвратить или добиться обратного развития при их своевременной диагностике и лечении.
Основным маркером функционального состояния почек считают клиренс креатинина (показатель клубочковой фильтрации), который определяют по формуле
клиренс креатинина = (концентрация креатинина в моче ¸ концентрация креатинина в крови) ´ минутный диурез
или по формуле Cockroft.
клиренс креатинина = [К ´ (140 - возраст) ´ масса тела (в кг)] ¸ концентрация креатинина в крови (в ммоль/л), где К = 1,05 для женщин и 1,23 для мужчин.
Большое значение имеет возраст, поскольку с его увеличением даже при нормальном содержании креатинина в крови может снижаться клиренс креатинина.
Нарушение функциональных возможностей почек сопровождается увеличением токсичности противоопухолевых агентов, экскретируемых почками или метаболизируемых в них. Нефротоксичность проявляется различными патологическими процессами в почках: цисплатин вызывает тубулярный некроз, митомицин - гломерулярный васкулит, ифосфамид - нарушения в проксимальных канальцах, гематурию и химический (акролеиновый) цистит, циклофосфамид - острый геморрагический цистит, производные нитрозомочевины - хронический интерстициальный нефрит, а при назначении метотрексата возможна преципитации препарата в почечных канальцах.
Нарушение функций почек влияет на фармакокинетику и фармакодинамику противоопухолевых препаратов, поскольку приводит к изменениям концентрации лекарственных средств в крови, которая характеризуется показателем площади под фармокинетической кривой "концентрация-время" - AUC (Area Under the Curve).
Клиренс большинства цитостатиков коррелирует с клиренсом креатинина. В частности, такая связь доказана для карбоплатина, что используют при расчёте дозы препарата: доза карбоплатина = AUC ´ (клиренс креатинина + 25). AUC при использовании карбоплатина в комбинациях равна 4-6, при монотерапии - 5-7.
Наиболее выраженные нарушения функций почек в процессе проведения химиотерапии отмечают при использовании соединений, содержащих платину. Механизм цитостатической тубулопатии в достаточной степени изучен экспериментально. В конечном итоге развивается апоптоз эпителиальных клеток проксимальных канальцев, обусловленный накоплением в клетках железа и гидроксильных радикалов с последующим перекисным окислением жиров и резким снижением содержания глутатиона.
Небольшой нефротоксический потенциал карбоплатина, по сравнению с цисплатином возможно обусловлен тем, что карбоплатин почти полностью выводится путём клубочковой фильтрации (в почечных канальцах обнаруживают очень маленькую концентрацию данного препарата). Риск развития нефротоксичности на фоне терапии карбоплатином повышается при увеличении дозы препарата, а также у пациентов, которые раньше получали терапию цисплатином.
Цисплатин характеризуется экстенсивным распределением в биологических жидкостях организма и тканях. Наиболее высокие концентрации данного лекарственного средства отмечают в почках, печени и простате. Цитотоксическим эффектом обладают только цисплатин, не связанный с белками плазмы крови, и его платиносодержащие метаболиты. При повторных курсах лечения происходит постепенная кумуляция платины в тканях. Поражение почек, при котором развивается повреждение почечных канальцев, впервые можно выявить на 2-й неделе после введения препарата. С целью максимального уменьшения нефротоксического действия цисплатина проводят форсированный диурез путём создания состояния гипергидратации до и после введения препарата платины и назначения осмотических диуретиков (маннитол).
Метотрексат выводится преимущественно почками, в неизменённом виде путём клубочковой фильтрации и канальцевой секреции. С желчью выводится до 10% препарата. При повторных введениях лекарственное средство накапливается в тканях в виде метаболитов. Риск развития нарушения функции почек зависит от дозы. При назначении высоких доз, для предупреждения преципитации препарата и/или его метаболитов в почечных канальцах, метотрексат вводят в течение 4-6 ч в виде внутривенной инфузии на фоне усиленной гидратации и ощелачивания мочи. Во время терапии метотрексатом в высоких дозах необходимо следить за pH мочи: в день введения и в последующие 2-3 сут pH мочи должен быть 7,4 и выше. Для этого назначают внутривенно раствор гидрокарбоната натрия. Лечение метотрексатом в дозе 2 г/м2 поверхности тела и выше или у больных с нарушенной функцией почек проводят под контролем концентрации препарата в крови. Через 24 ч после окончания инфузии метотрексата каждые 6 ч в течение 2-3 сут обязательно вводят фолинат кальция.
Для предупреждения нефротоксичности показан постоянный динамический контроль общего анализа мочи и содержания креатинина в крови и моче.
При повышении концентрации креатинина, выявлении протеинурии, цилиндрурии и гематурии назначение цисплатина, метотрексата, митомицина, проспидия хлорида и кармустина противопоказано. Корректировать дозу в зависимости от степени нарушения почечных функций не нужно при использовании следующих химиопрепаратов: бусульфан, винбластин, гемцитабин, дактиномицин, даунорубицин, доксорубицин, доцетаксел, идарубицин, мелфалан, меркаптопурин, митоксантрон, паклитаксел, тенипозид, тиогуанин, тиотепа, фторурацил, хлорамбуцил. Дозы других цитостатиков снижают на 25-50% в зависимости от уровня клиренса креатинина.
При назначении высоких доз циклофосфамида и ифосфамида возможно развитие геморрагического цистита. Экспериментально было доказано, что цистит обусловлен уротоксическим действием метаболита этих препаратов - акролеина, высвобождающегося в моче после клубочковой фильтрации. Фатальным осложнением бывает тотальный некроз мочевого пузыря с его тампонадой. Для предупреждения развития химических циститов ифосфамид и высокие дозы циклофосфамида используют только с одновременным назначением специфического антидота акролеина (месна) в дозе, составляющей от 60 до 120% дозы ифосфамида, обязательным ощелачиванием мочи до и после введения химиопрепарата и форсированием диуреза. При лечении лекарственных циститов рекомендуют соблюдать диету, расширенный водный режим, проводить инстилляции противовоспалительных вяжущих средств, обезболивающих растворов и назначать спазмолитические лекарственные средства.
Осложнением химиотерапии или лучевого лечения, часто бывает острая почечная недостаточность, обусловленная мочекислой канальцевой нефропатией. При высокой чувствительности опухоли к терапии, быстрое значительное уменьшение опухолевой массы (синдром распада опухоли) может сопровождаться гиперурикемией (увеличением содержания мочевой кислоты в крови). Гиперурикемия при отсутствии профилактики аллопуринолом может осложниться обструктивной мочекислой нефропатией (с летальным исходом в 1% случаев). Мочекислая нефропатия возникает из-за отложения мочевой кислоты и последующего повреждения преимущественно дистальных канальцев и собирательных трубочек. Для профилактики этого осложнения при онкологических заболеваниях, высокочувствительных к химиотерапии и при больших размерах новообразования, до проведения противоопухолевой терапии необходимо назначить аллопуринол (ингибитор ксантиноксидазы) в дозе 400-600 мг/сут на фоне гидратации. Лечение следует продолжать в течение всего периода уменьшения размеров опухоли. Поскольку мочекислая нефропатия бывает острым осложнением противоопухолевого лечения, при развитии олигурии показаны гемодиализ и плазмаферез.
У пациентов со злокачественными новообразованиями нарушения функций почек могут быть вызваны несколькими различными факторами, в том числе не связанные с опухолевым заболеванием. При выборе тактики лечения почечной недостаточности, прежде всего, необходимо установить этиологию данного нарушения. Если почечная недостаточность обусловлена опухолевой инфильтрацией паренхимы, функции почек после проведения эффективного противоопухолевого лечения обычно значительно улучшаются. Зачастую, даже длительно существующая почечная недостаточность, связанная с онкологическим заболеванием, купируется при проведении этиотропного лечения.
Симптоматическая терапия почечной недостаточности заключается в восполнении объёма циркулирующей крови, поддержании адекватного перфузионного давления [рекомендовано проводить инфузии допамина в дозе 2-4 мкг/(кг´мин) (почечно-инотропный режим)], а при олигурии показана стимуляция диуреза фуросемидом в средней дозе 100 мг (не следует превышать дозу 600 мг, так как в этом случае возможен вазоконстрикторный эффект).
При развитии тяжёлой почечной недостаточности необходима заместительная терапия: гемодиализ, перитонеальный диализ, гемофильтрация или трансплантация почки.
Поражение Печени
Большинство химиопрепаратов, включенных в современные программы лечения злокачественных новообразований, в различной степени гепатотоксичны. Выраженность поражения печени при проведении химиотерапии может варьировать в широких пределах: от бессимптомного подъёма активности трансаминаз в крови до фульминантного гепатита с развитием печёночной недостаточности.
Большое значение в патогенезе лекарственного поражения печени придают процессам биотрансформации с участием цитохрома Р-450, который локализуется в эндоплазматическом ретикулуме и катализирует реакции гидроксилирования, дезалкилирования и дегидрогенирования. Процесс биотрансформации протекает в 2 фазы.
-
Первая фаза включает совокупность реакций, приводящих к образованию активных промежуточных метаболитов, которые собственно и обладают гепатотоксическими свойствами.
-
Во 2-й фазе происходит конъюгация этих метаболитов с глутатионом, сульфатом или глюкуронидом в результате чего образуются нетоксичные гидрофильные соединения, которые далее из печени попадают в кровь или желчь.
Механизм лекарственного поражения печени заключается либо в непосредственном действии токсического вещества на гепатоциты, либо в выработке аутоантител, вызывающих цитолиз гепатоцитов. В некоторых случаях определённое значение имеют нарушение микроциркуляции и внутридольковый холестаз. Формы токсического поражения печени и основные патогенетические механизмы их развития представлены в табл. 14-1.
Таблица 14-1. Формы токсического поражения печени
| Вид токсического поражения | Основные патогенетические факторы |
|---|---|
Острые и хронические гепатиты |
Усиление перекисного окисления липидов |
Истощение запасов детоксицирующих веществ (глутатион и др.) |
|
Образование токсических метаболитов в гепатоцитах |
|
Иммунные реакции |
|
Жировой гепатоз |
Блокада синтеза транспортных белков, участвующих в выведении липидов из гепатоцитов |
Ингибирование ферментов, участвующих в образовании липопротеидов |
|
Снижение синтеза и запасов гликогена |
|
Холестаз |
Нарушение проницаемости мембран гепатоцитов |
Ингибирование Na+,K+ АТФазы и других мембранных переносчиков |
|
Нарушение целостности эпителия и проходимости желчных протоков |
|
Нарушение состава желчи |
Спектр клинико-морфологических вариантов поражения печени, вызываемых противоопухолевыми препаратами, весьма широк. Например, при длительной терапии метотрексатом в небольших дозах возможен печёночный фиброз различной степени выраженности. Однако также существуют наблюдения о развитии острого гепатита при использовании этого препарата однократно в высоких дозах. Гепатотоксическое действие 6-меркаптопурина характеризуется некрозом гепатоцитов, формированием фиброза портальных трактов и холестазом. Аспарагиназа может вызывать тяжёлый токсический гепатит с выраженным нарушением белковосинтетической функции печени и жировой гепатоз. Имеются наблюдения о развитии токсических гепатитов при назначении циклофосфамида в высоких дозах, дакарбазина, производных нитрозомочевины. Редкой патологией печени, которая может появиться на фоне терапии бусульфаном, считают нодулярную регенеративную гиперплазию.
Больные со злокачественными новообразованиями крайне подвержены инфекционным заболеваниям из-за выраженной иммуносупрессии на фоне цитостатической и гормональной терапии. По этой причине данным пациентам часто показана интенсивная сопутствующая терапия антибактериальными, противогрибковыми и противовирусными лекарственными средствами, многие из которых вызывают нарушения функций печени. Известны случаи развития тяжёлых гепатотоксических реакций при назначении некоторых антибактериальных и противогрибковых препаратов, используемых при лечении онкологических больных (эритромицин, сульфаниламиды, кларитромицин, изониазид, рифампицин, флуконазол, итраконазол, амфотерицин B). Применение тетрациклина в больших дозах может привести к острой жировой дистрофии печени или холестазу, ципрофлоксацина - к тяжёлому некрозу печени, а амоксициллина + клавулановой кислоты и эритромицина - к холестатическому поражению печени. Сочетание цитостатиков с антибактериальными и противогрибковыми препаратами может приводить к потенцированию гепатотоксичности.
Вероятность развития токсического поражения печени при химиотерапии существенно возрастает у пациентов с предшествовавшими нарушениями функций печени при наличии фоновых заболеваний данного органа (вирусные гепатиты, гепатозы, циррозы). Поскольку печень - основной орган метаболизма лекарственных препаратов, то любое нарушение её функционального состояния отражается на их фармакокинетике. Снижение скорости метаболизма в печени сопровождается увеличением периода полувыведения препаратов, что приводит к нарастанию концентрации лекарственных средств и возможности относительной передозировки. При заболеваниях печени нарушается не только функция гепатоцитов, но и кровоснабжение печени. Особенно сильно изменяется фармакокинетика и биодоступность препаратов с высоким печёночным клиренсом, что обусловлено не только снижением метаболизма, но и наличием портокавальных анастомозов, из-за которых значительная часть лекарственных средств поступает в системный кровоток, минуя печень. В связи с этим при наличии печёночной недостаточности дозу препаратов, быстро метаболизирующихся в печени и с высоким печёночным клиренсом, следует уменьшать. Например, дозу таких лекарственных средств, как винкристин, винбластин, этопозид рекомендуют уменьшать на 50% при повышении концентрации билирубина в крови до 30-60 мкмоль/л и активности АЛТ в крови. При более высоком содержании билирубина и активности печёночных ферментов в крови от использования данных химиопрепаратов рекомендовано воздержаться. В случае нарушений функций печени также необходимо корригировать режим введения следующих химиопрепаратов: доксорубицин, даунорубицин, циклофосфамид, метотрексат, паклитаксел и меркаптопурин.
Следует помнить, что при поражении печени усиливается влияние многих химиопрепаратов на ЦНС, из-за чего резко увеличивается частота развития энцефалопатий.
Выделяют также гепаторенальный синдром, при котором снижается фильтрационная функция почек, что отрицательно сказывается не только на метаболизме, но и на почечной экскреции препаратов.
Перед началом химиотерапии необходимо тщательно собрать анамнез, провести исследование функционального состояния печени, скрининг на вирусные гепатиты B и C. При выявлении вирусного гепатита следует определить репликативную активность вируса (табл. 14-2).
Таблица 14-2. Лабораторная диагностика вирусных гепатитов
| Диагноз | Результаты скрининговых методов диагностики | Результаты методов диагностики репликации вируса |
|---|---|---|
Хронический вирусный гепатит B, фаза репликации |
В крови обнаруживают HBSAg, анти-HBc (класса IgM), активность АсАТ, АлАТ повышена или нормальная |
В крови выявляют ДНК вируса гепатита B, HBEAg |
Хронический вирусный гепатит B, нерепликативная фаза |
В крови HBSAg не обнаруживают, активность АсАТ и АлАТ нормальная |
В крови не обнаруживают ДНК вируса гепатита B, но выявляют анти-HBE |
Хронический вирусный гепатит C |
В крови обнаруживают анти-HCV |
В крови обнаруживают РНК вируса гепатита C |
Для оценки функционального состояния печени проводят также биохимические тесты. Количество функциональных проб печени достаточно велико и спектр их непрерывно расширяется. Однако в практической деятельности используют ряд традиционных методов исследований, с помощью которых определяют активность патологического процесса, наличие холестаза и состояние белковосинтетической функции гепатоцитов (табл. 14-3).
Таблица 14-3. Клиническое значение изменений лабораторных показателей при заболеваниях печени
| Лабораторные показатели | Изменение | Клиническое значение |
|---|---|---|
Активность АсАТ, АлАТ в крови |
Повышенная |
Некроз гепатоцитов |
Активность АсАТ, АлАТ в крови |
Нормальная |
Отсутствие некрозов, низкая активность патологического процесса |
Концентрация общего билирубина в крови |
Повышена |
Некроз гепатоцитов, холестаз |
Активность щелочной фосфатазы, g-глутамилтрансферазы, и концентрация холестерина в крови |
Повышены |
Холестаз |
Активность g-глутамилтрансферазы в крови |
Повышенная |
Токсическое поражение печени |
Концентрация альбумина в крови, протромбиновый индекс |
Снижены |
Гепатоцеллюлярная недостаточность |
Проведение химиотерапии у больных с вирусными гепатитами считают проблемным. Следует отметить, что среди пациентов со злокачественными новообразованиями отмечают высокую частоту инфицирования вирусами гепатитов B и C. Это обусловлено частыми парентеральными вмешательствами, интенсивной гемотрансфузионной терапией (особенно у больных гемобластозами), глубокой иммуносупрессией, при которой создаются благоприятные условия для репликации и персистенции вируса. Диагностика и течение вирусных гепатитов на фоне ПХТ имеют особенности.
-
Во-первых, такие клинические признаки, как тошнота, рвота, слабость, увеличение печени, желтуха нельзя однозначно расценить в качестве проявлений гепатита, поскольку они могут быть следствием химиотерапии.
-
Во-вторых, у пациентов со злокачественными новообразованиями отсутствует корреляция между вирусной репликацией и результатами исследования активности печёночных ферментов (при наличии вирусной ДНК или РНК показатели активности АлАТ и АсАТ в крови могут быть нормальными или повышаться незначительно) в крови. По этой причине показатели, полученные с помощью данного лабораторного метода исследования, нельзя использовать в качестве надежного критерия диагностики и оценки течения вирусных гепатитов у больных онкологическими заболеваниями.
При активном гепатите с выраженными нарушениями функций печени может возникнуть необходимость в прерывании лечения или уменьшении доз химиопрепаратов, из-за чего снижается эффективность терапии. Кроме того, высокая частота хронизации вирусных гепатитов у больных с онкологическими заболеваниями на фоне химиотерапии существенно ухудшает качество жизни пациентов после окончания химиотерапевтического лечения и отрицательно влияет на отдалённые результаты терапии.
Отмена препарата, вызвавшего острое токсическое поражение печени, бывает достаточным условием для обратного развития патологических изменений или прекращения их дальнейшего прогрессирования. В комплекс лечения пациентов с заболеваниями печени целесообразно включать гепатопротекторы (адеметионин), хотя их эффективность оценивают достаточно противоречиво. При развитии холестаза показано назначение энтеросорбентов, урсодезоксихолевой кислоты.
Особенности проведения химиотерапии у пожилых пациентов
Организм людей старшей возрастной группы имеет физиологические особенности, которые в той или иной степени могут ограничивать применение лекарственного метода лечения. Пожилой возраст больного - не абсолютное противопоказание для проведения химиотерапии. Вместе с тем, клинические ситуации, при которых назначение химиотерапевтических ЛС у данной категории больных если и не совершенно невозможно, но существенно ограничено, не редкость.
Старение организма сопровождается снижением функциональных возможностей и резервов многих органов и систем, что существенно повышает риск развития осложнений химиотерапии:
Физиологические предпосылки повышенного риска проведения химиотерапии у пожилых больных:
Всё это способствует увеличению токсичности цитостатиков (антрациклинов, эпиподофилатоксинов, таксанов), связывающихся с белками и эритроцитами.
Токсическое воздействие на гемопоэз оказывают большинство химиопрепаратов, возраст - фактор риска развития выраженной миелосупрессии. У пожилых больных из-за физиологического снижения резервов костного мозга следует ожидать развития малопредсказуемой миелотоксичности, которая отличается, как правило, большей степенью выраженности на стандартные дозы препаратов и имеет большую продолжительность. Развитие тяжёлой миелосупрессии чревато не только геморрагическим синдромом с последующей активной инфузионной терапией препаратами крови, но и фебрильной нейтропенией со всем разнообразием инфекционных осложнений, некоторые из которых могут оказаться фатальными у пациентов данной возрастной категории. Всё перечисленное может потребовать активного применения колониестимулирующих факторов.
Развитие лёгочной токсичности - не самое частое осложнение у пожилых людей, но частота его в возрасте 70 лет и старше в 3 раза выше, чем в 40 лет. При первых симптомах лекарственного пульмонита, препарат, вызвавший развитие лёгочной токсичности, отменяют. В качестве профилактики этого осложнения недопустимо превышать рекомендуемые дозы препаратов, потенциально опасных в отношении развития лёгочной токсичности. У пациентов старшей возрастной группы при предполагаемом назначении таких препаратов, в первую очередь блеомицина и митомицина, показано проведение функционального исследования лёгких - спирометрии, его же целесообразно использовать в качестве мониторинга.
С возрастом развиваются функциональные изменения печени: уменьшается кровоток, снижается продукция альбумина. Уменьшение печёночного кровотока, приводит, соответственно, к уменьшению печёночного клиренса для группы ЛС, активно экскретируемых печенью. Наиболее значимы изменения метаболической функции печени. Нарушения в механизме активации и дезактивации изменяют активность и токсичность химиопрепаратов, чей метаболизм осуществляется посредством указанного механизма - циклофосфамида ифосфамида, идарубицина.
-
При нарушении функции печени токсичность антиметаболитов, эпиподофилотоксинов и большинства алкилирующих препаратов не нарастает.
-
При повышении концентрации билирубина до 1,5 мг/дл и 3,0 мг/дл (25 и 50 мкмоль/л) дозы винбластина и антрациклинов должны быть снижены на 50% и 75%, соответственно.
-
Коррекцию дозы таксанов, которые также метаболизируются в печени, проводят по аналогии с поправкой дозы антрациклинов.
-
В соответствии с имеющимися рекомендациями доза доцетаксела подлежит коррекции до 75% при одновременном повышении активности печёночных аминотрасфераз и щелочной фосфатазы даже при нормальном уровне билирубина.
Развитие почечной токсичности обусловлено одним из наиболее стойких возрастных функциональных изменений - снижением гломерулярной фильтрации. Стандартное биохимическое определение уровня креатинина не даёт объективной оценки функциональным возможностям почек. Объясняется это тем, что в пожилом возрасте физиологическая потеря мышечной массы приводит к уменьшению продукции креатинина, и, как следствие, к фиктивной нормализации его уровня. Более точно функцию почек отражает клиренс креатинина, причём использование формулы Кокрофта более достоверно, чем оценка на основе рутинного сбора суточной мочи. Снижение гломерулярной фильтрации приводит к увеличению токсичности химиопрепаратов, выводимых почками, в первую очередь цисплатина, метотрексата, блеомицина, а также тех противоопухолевых агентов, метаболизм которых связан с образованием активных или токсических продуктов. Особенности печёночного метаболизма винкаалкалоидов, антрациклинов, эпиподофилотоксинов, таксанов таковы, что позволяют вводить их в полной дозе даже при нарушении функции почек.
Нельзя недооценивать развитие кардиотоксичности у пожилого пациента, возможно, уже имеющего какие-либо кардиологические проблемы к моменту назначения химиотерапии. Безусловные факторы риска:
Основной метод профилактики кардиотоксичности антрациклинов - соблюдение предельных суммарных доз препаратов - 550 мг/м2 для доксорубицина и 1100 мг/м2 для эпирубицина. Рекомендуется внутривенное капельное, а не внутривенное струйное введение антрациклинов. Необходимо помнить о возможном повышении кардиотоксичности при комбинированной химиотерапии. Так, повышенной кардиотоксичностью отличаются комбинации доксорубицина с паклитакселом и трастузумабом У пациентов старшей возрастной группы при предполагаемом назначении антрациклинов, показано проведение ЭКГ и ЭхоКГ, эти же исследования целесообразно проводить в качестве мониторинга.
Нейротоксические качества характерны для таких химиопрепаратов, как винкаалкалоиды, эпиподофилотоксины, производные платины, таксаны. Последствия применения этих ЛС виде снижения периферической чувствительности, слуха или развития центральной нейротоксичности в пожилом возрасте встречаются чаще, а тяжесть их проявлений существенно ухудшает качество жизни больных.
При лечении пожилых больных необходима адекватная оценка химиопрепаратов, коррекция доз, адаптация режимов введения, а также понимание механизмов развития возможных осложнений, путей их профилактики и устранения. Если при проведении лекарственного противоопухолевого лечения пациентам молодого и среднего возраста назначение средств поддерживающей терапии - возможная опция, то в химиотерапии пожилых людей препараты поддерживающего лечения должны назначаться более активно, сообразно большей тяжести предполагаемых осложнений.
Осложнения противоопухолевой терапии, их коррекция
Проведение цитостатического лечения помимо ожидаемого терапевтического эффекта практически всегда сопровождается развитием многочисленных побочных реакций со стороны различных органов и систем организма. Это связано с отсутствием специфичности цитостатиков, которые, обладая способностью подавления митотической активности, одинаково реализуют её в отношении как опухолевых, так и нормальных клеток.
В спектре токсичности противоопухолевой терапии преобладают осложнения, обусловленные неблагоприятным воздействием или непосредственным поражением интенсивно пролиферирующих клеток органов кроветворения и иммунной системы, а также яичников, яичек и волосяных фолликулов. Гематологические и желудочно-кишечные побочные явления составляют до 80-90% всех осложнений химиотерапии.
Кроме вышеуказанных систем и органов цитостатики способны повреждать практически все нормальные ткани и органы. Осложнения со стороны печени и желчевыводящих путей, мочевыделительной и сердечно-сосудистой систем составляют до 40-50% от общего числа побочных реакций. Несколько реже (до 20-25%) возникают осложнения со стороны нервной, мышечной и дыхательной систем.
Шкалы побочных реакций противоопухолевой терапии
ВОЗ разработана общая для всех побочных реакций шкала, отражающая степень их интенсивности, угрозу для жизни больного и необходимость коррекции.
Шкала побочных реакций противоопухолевой терапии (ВОЗ)
-
Осложнения степени I. Характерны минимальные изменения самочувствия больного и лабораторных показателей, не требующие медикаментозной коррекции.
-
Осложнения степени II. Необходимо осуществлять лечение возникших нарушений, поскольку они влияют на общую активность больного и вызывают умеренные изменения лабораторных показателей.
-
Осложнения степени III. Характерно значительное ухудшение самочувствия и состояния больного, а также лабораторных параметров, требующее активного симптоматического лечения, отсрочки очередного цикла химиотерапии и/или снижения доз цитостатиков.
-
Осложнения степени IV. Возникают побочные реакции, представляющие непосредственную угрозу для жизни больного.
Аналогичная шкала токсичности (СТС) разработана NCIC в США.
На степень тяжести осложнений оказывает влияние исходное общее состояние больного. Снижение функциональной активности больного ниже степени II (по шкале ECOG) требует тщательного контроля его состояния на всём протяжении противоопухолевого лечения, а в ряде случаев, осуществления изменения дозы цитостатиков и назначения сопутствующей симптоматической терапии.
Кроме индивидуальных особенностей организма больного интенсивность побочных реакций зависит от механизма действия того или иного цитостатика, его дозы, а также режима химиотерапии. Комбинации двух и более противоопухолевых лекарственных средств в подавляющем большинстве случаев обусловливают более широкий спектр и тяжесть осложнений.
Таким образом, врачебную тактику необходимо основывать на знании побочных эффектов выбранного режима химиотерапии, осуществлении профилактических мероприятий, а также своевременного лечения возникших осложнений.
Токсическое действие на кроветворение
Периферические цитопении вследствие подавления митотической активности ростков кроветворения относят к наиболее частым и клинически значимым побочным реакциям химиотерапии. Кроме них выделяют группу хронических гематологических осложнений, не связанных с непосредственным поражением костного мозга (вторичные миелодисплазии, гемолитические анемии, коагулопатии, злокачественные новообразования системы крови, иммунодефицитные состояния).
Факторы риска развития миелотоксичности:
Степень выраженности миелосупрессии зависит также от исходных резервных возможностей костного мозга, данные о которых получают при исследовании его пунктата (например, из грудины). Поскольку общая клеточность костного мозга уменьшается с возрастом, некоторые авторы рекомендуют изначально уменьшать дозы цитостатиков у лиц пожилого возраста.
Острые повреждения костного мозга
Их относят к одним из основных дозолимитирующих побочных эффектов противоопухолевого лечения. Воздействие цитостатиков вызывает подавление пролиферации клеток-предшественников всех трёх ростков кроветворения (гранулоцитарного, эритроцитарного и мегакариоцитарного). Транзиторный характер миелосупрессии связан с тем, что 25-50% стволовых клеток костного мозга находятся в фазе G0, поэтому они устойчивы к повреждению цитостатиками.
Манифестация повреждения костномозгового кроветворения со стороны периферической крови зависит от функциональных особенностей зрелых клеток крови. Так, период полужизни гранулоцитов не превышает 6 ч, для тромбоцитов аналогичный показатель составляет 10 дней, для эритроцитов - 115-120 дней. В результате, наиболее раннее проявление индуцированной цитостатиками миелотоксичности - нейтропения, в дальнейшем (на 10-14 сут от введения препаратов) развивается тромбоцитопения. Анемию регистрируют в достаточно поздние сроки, нередко к окончанию 2-4 циклов химиотерапии. Тем не менее, тщательный контроль показателей периферической крови необходимо осуществлять в течение 6-8 нед после окончания химиотерапии. Для начала и продолжения химиотерапевтического лечения уровень нейтрофилов в периферической крови должен превышать 1,5x109/л, тромбоцитов - 100x109/л и гемоглобина - 100 г/л.
Поскольку в большинстве противоопухолевых схем цитостатики назначают в средних (немиелоаблативных) дозах, лишь кратковременно повреждающих костный мозг, наиболее часто среди осложнений регистрируют транзиторную нейтропению и тромбоцитопению, как правило, степени I. Значительно реже отмечают развитие нормо- или гипохромной анемии. В то же время, существует немногочисленная группа цитостатиков (блеомицин, винкристин), не обладающих миелосупрессивными эффектами.
Особенности влияния противоопухолевых препаратов на костномозговое кроветворение
Особенности повреждения костномозгового кроветворения различными цитостатиками зависят от механизмов их противоопухолевого действия. Наиболее отчётливо эти отличия выявляют у химиотерапевтических лекарственных средств с антиметаболической и алкилирующей активностью.
Наиболее выраженное миелодепрессивное воздействие оказывают алкилирующие препараты (хлорэтиламины, этиленимины, производные нитрозомочевины и платины), а также антрациклиновые антибиотики и препараты растительного происхождения (винкаалкалоиды, таксаны). Вышеуказанные цитостатики обладают наибольшей токсичностью в отношении примитивных стволовых клеток, имеющих минимальную митотическую активность.
Напротив, цитотоксичность антиметаболитов, в первую очередь, антагонистов пиримидиновых и пуриновых оснований, ингибиторов тимидилат синтетазы напрямую зависит от интенсивности клеточной пролиферации и реализуется в отношении более зрелых клеток-предшественников кроветворения.
Клинические проявления вышеуказанных различий - более ранняя (в ближайшие 7-14 дней после введения) и менее глубокая миелосупрессия, индуцируемая антиметаболитами, и, как правило, отсроченная и выраженная панцитопения, вызываемая цитостатиками с алкилирующей активностью (например, кармустин, цисплатин).
Для ряда химиотерапевтических лекарственных средств характерно избирательное поражение эритроцитарного ростка кроветворения. При этом механизмы развития постцитостатической анемии различны. Например, производные платины (в первую очередь, цисплатин) подавляют синтез эндогенных эритропоэтинов, флударабин вызывает гемолиз, хлорамбуцил оказывает непосредственное повреждающее действие.
Небольшая группа цитостатиков, к которой относят кармустин, ломустин, гемцитабин, обладают ингибирующей активностью в отношении мегакариоцитов, приводя к развитию тромбоцитопении. Наибольшую опасность представляет тромбоцитопения IV степени, часто осложняющаяся развитием геморрагического диатеза. К наиболее частым клиническим проявлениям геморрагического синдрома относят геморрагическую сыпь на коже и слизистых оболочках, склерах, экхимозы, носовые, дёсневые и желудочно-кишечные кровотечения, кровотечения после экстракции зубов, в ткань головного мозга и др. Критический уровень тромбоцитов составляет 10x109/л. Для профилактики геморрагических осложнений необходимо проводить неоднократные трансфузии тромбовзвеси или тромбоконцентрата.
Факторы, влияющие на степень гематологической токсичности противоопухолевых препаратов
Различная степень гематологической токсичности противоопухолевых препаратов зависит от индивидуальной способности организма к их абсорбции, распределению, метаболизму и выведению.
Наиболее важный фактор - клиренс цитостатиков и/или их метаболитов. Также в последние годы активно изучают механизмы инактивации цитостатиков. Классическим примером рассматривают редкий феномен дефицита фермента дигидропиримидиндегидрогеназы, приводящий к значительному усилению токсических, в том числе и миелосупрессивных, эффектов фторурацила.
Наконец, степень выраженности гематологической токсичности того или другого цитостатика зависит от его дозы, способа и частоты введения. Например, миелотоксичность фторурацила (препарат из группы антиметаболитов) значительно выше при болюсной (по сравнению с длительной) внутривенной инфузии.
Нейтропения
Степень тяжести нейтропении оценивают в соответствии со шкалой токсичности ВОЗ.
Степени тяжести нейтропении (ВОЗ):
Наибольшую потенциальную опасность для больного, получающего цитостатическое лечение, представляет умеренная и выраженная нейтропения, при которой значительно повышен риск развития серьёзных инфекционных осложнений, обусловленных условно-патогенными микроорганизмы, а также внутрибольничной микрофлорой.
К дополнительным факторам риска относят иммуносупрессию, обусловленную как опухолевым процессом, так и назначением цитостатиков и/или глюкокортикоидов, предшествующие обширные оперативные вмешательства, наличие центральных венозных катетеров, повреждения слизистых оболочек (мукозиты), глубина и длительность нейтропении. Так, при нейтропении менее 0,5x109/л, продолжающейся более 7 сут, частота инфекционных осложнений достигает 50%. Для предотвращения инвазии резидентной условно-патогенной флоры с кожного покрова, слизистых оболочек дыхательных путей и пищеварительного тракта рекомендуют профилактическое назначение пероральных антибактериальных препаратов.
Фебрильная нейтропения
Нейтропению степени III-IV в сочетании с не менее, чем двукратным в течение суток повышением температуры тела выше 38,0° (или однократным - более 38,3°) определяют термином фебрильная нейтропения и относят к угрожающим жизни больного осложнениям.
Около 80% случаев фебрильной нейтропении связаны с развитием инфекционного процесса, который протекает без классических симптомов воспаления, при этом основной критерий активности инфекционного процесса - высокая лихорадка. Выявление у больного фебрильной нейтропении рассматривают показанием для немедленного назначения эмпирической антибактериальной терапии, а также для проведения ряда обязательных диагностических процедур.
-
Микробиологическая верификация возбудителя инфекции. Её удаётся осуществить не ранее, чем через 5-7 сут с момента возникновения фебрильной нейтропении лишь у трети больных.
Наиболее частые возбудители:-
аэробные грамположительные кокки (Staphylococcus aureus, Staphylococcus epidermidis, стрептококки, энтерококки);
-
аэробные грамотрицательные бактерии (Escherichia coli, Pseudomonas аeruginosa, Klebsiella spp.) (реже);
-
анаэробные бактерии (Bacteroides spp., Clostridium spp.) (реже);
-
грибы в 10-15% случаев (наиболее часто Candida spp. или грибы рода Aspergillus).
-
-
Лечение зависит от вида возбудителя.
-
Антибактериальная терапия. Основу современного антибактериального лечения составляют b-лактамные антибиотики. К препаратам первого ряда эмпирической терапии относят цефалоспорины III (цефтазидим) (как правило, в комбинации с аминогликозидами) и IV (цефепим) поколения, а также карбопенемы (имипенем, меропенем) и гликопептиды (ванкомицин, тейкопланин).
-
Противогрибковая терапия. С учётом трудностей диагностики микозов рекомендуют назначать противогрибковые препараты больным при сохранении в течение 5 сут на фоне антибактериальной терапии повышенной температуры. В последние годы наиболее широко применяют противогрибковые препараты из групп полиенов (амфотерицин В, липидные амфотерицины), азолов (флуконазол, итраконазол, вориконазол), эхинокандинов (каспофунгин), аналогов нуклеозидов (флуцитозин).
-
Противовирусная терапия. У больных с фебрильной нейтропенией нередко возникает обострение вирусной инфекции (вирус простого герпеса типа I и типа II, цитомегаловирус, герпес Zoster). Для профилактики и лечения герпетической и цитомегаловирусной инфекций используют ацикловир, ганцикловир, фоскарнет натрий.
-
Гемоцитокины. Больным с высоким риском развития угрожающих жизни инфекционных осложнений (инфекционно-токсический шок, сепсис с полиорганной недостаточностью) можно назначать гемоцитокины - рекомбинантные гранулоцитарные колониестимулирующие факторы (филграстим, ленограстим). Однако, результаты большинства рандомизированных исследований показали недостаточную эффективность данных препаратов. Использование гемопоэтических факторов обеспечивает достоверное снижение длительности нейтропении лишь на 1-2 дня и не влияет на продолжительность лихорадки, длительность антимикробной терапии и уровень смертности больных от инфекционных осложнений.
-
Анемия
Токсическое воздействие цитостатиков на эритроцитарный росток кроветворения приводит к развитию анемии. Кроме того, производные платины могут нарушать синтез эндогенного эритропоэтина в паренхиме почек.
Степени тяжести анемии (ВОЗ)
Клинические проявления анемии зависят не только от уровня гемоглобина крови, но и скорости его снижения. К характерным симптомам относят различные проявления тканевой гипоксии (утомляемость, снижение работоспособности, нарушение памяти, сна, головокружение, депрессия), у пожилых больных - ухудшение течения сопутствующих сердечно-сосудистых и других хронических заболеваний.
Лечение. Осуществляют переливание эритроцитарной массы, используют рекомбинантные эритропоэтины.
-
Переливание эритроцитарной массы - традиционный метод лечения постцитостатической анемии степени III-IV (при концентрации гемоглобина менее 70-80 г/л), что обеспечивает быстрое увеличение концентрации гемоглобина крови и уменьшение клинической симптоматики. В то же время, гемотрансфузия - дорогостоящий метод коррекции анемии, требующий госпитализации больного и тщательного обследования донорской крови на наличие инфекций.
-
Эритропоэтины. В последние 15 лет в онкологическую практику активно внедряют рекомбинантные эритропоэтины - специфичные факторы стимуляции эритропоэза. Их применение позволяет компенсировать дефицит эндогенных факторов роста, что приводит к увеличению уровня гемоглобина крови.
В соответствии с современными рекомендациями, экзогенные стимуляторы эритропоэза следует назначать при определении у больного постцитостатической анемии с уровнем гемоглобина менее 100 г/л. Длительность применения препаратов зависит от их эффективности. Как правило, курс лечения эритропоэтинами завершают при достижении концентрации гемоглобина, равной 120 г/л, не позднее 3 мес после окончания химиотерапии. Эритропоэтины не рекомендуют назначать онкологическим больным, имеющим уровень гемоглобина выше 100-110 г/л, с целью улучшения качества их жизни.
Хронические повреждения костного мозга
Характерно развитие миелодиспластических синдромов, вторичных иммунодефицитных состояний, аутоиммунных гемолитических анемий, лейкозов.
Миелодиспластические синдромы. Для миелодиспластических синдромов, развивающихся, как правило, после применения алкилирующих химиотерапевтических средств, характерно возникновение длительных и стойких панцитопений или макроцитарной анемии, продолжающихся в течение многих месяцев и даже лет (до 5-10 лет).
Лейкозы. В литературе описаны случаи развития острого миелобластного лейкоза после терапии этопозидом, выявления различных цитогенетических нарушений (делеций, транслокаций хромосом).
Гемолитическая анемия. Она часто возникает в рамках "гемолитического уремического синдрома", который впервые описали в 1982 г. как осложнение терапии митомицином. Синдром включает патологическую триаду (гемолиз, тромбоцитопению и почечную недостаточность). Позднее была установлена его связь с предшествующим лечением блеомицином, производными платины (цисплатином, карбоплатином), производными нитрозомочевины (кармустином), флударабином, интерфероном. Лечение гемолитической анемии заключается в назначении иммунодепрессантов, проведении процедур плазмафереза.
Постцитостатическая анемия при химиотерапии злокачественных опухолей
Анемия - наиболее частое осложнение злокачественного процесса; это спутник заболевания и побочный эффект противоопухолевого лечения. Анемия проявляется снижением концентрации гемоглобина (Hb), уменьшением количества или объёма эритроцитов. Всемирная Организация Здравоохранения определяет нижнюю границу нормальной концентрации Hb у взрослых на уровне 130/120 г/л (мужчины/женщины); Национальный противораковый институт США определяет норму Hb как 120-160 г/л для женщин и 140-180 г/л для мужчин. С точки зрения клинической значимости, выделяют тяжёлую анемию (<80 г/л) и жизне-угрожающую анемию (<65 г/л). Умеренную анемию диагностируют при содержании Hb в пределах 80-94 г/л.
Выраженность симптомов анемии и, соответственно, качество жизни больных зависит от скорости и величины снижения уровня Нb, а также от достаточности компенсаторных механизмов организма. Качество жизни пациентов снижают такие симптомы, как утомляемость, одышка при нагрузке, снижение толерантности к нагрузкам, сердцебиение, головокружение, ухудшение памяти и познавательной функции, снижение внимания.
В клинической онкологии чаще всего встречают так называемую раковую анемию (или анемию опухолевого процесса), когда уровень Hb снижается под действием опухолевого процесса, и пост-цитостатическую анемию, относящуюся к осложнениям противоопухолевого лечения. Ведущая причина уменьшения концентрации Hb при злокачественном процессе - анемия хронического заболевания (АХЗ). Проводя дифференциальный диагноз анемии, следует помнить и о других механизмах изменения числа и морфологии эритроцитов: кровотечении, гемолизе, гиперспленизме, дефиците кофакторов гемопоэза (например, железа, эндогенного эритропоэтина, витамина В12, фолиевой кислоты), поражении костного мозга опухолевым процессом.
Синдром АХЗ развивается в результате активации иммунной системы опухолевым процессом, что приводит к увеличению концентрации в крови и тканях фактора некроза опухоли (TNF-a), липополисахарида, g-интерферона, интерлейкина-1 и интерлейкина-6 - так называемой цитокиновой буре. Цитокины подавляют процесс дифференцировки клеток-предшественников эритроидного ряда, нарушают обмен железа и негативно влияют на выработку эритропоэтина (ЭПО) - ключевого гормона регуляции эритропоэза. Опухолевые клетки также вырабатывают процитокины воспаления и свободные радикалы, повреждающие клетки-предшественники эритроидного ряда. Отмечают укорочение времени жизни эритроцита до 90-60 дней.
В настоящее время основным звеном в патогенезе АХЗ считают нарушение обмена железа в организме: клетки ретикуло-эндотелиальной системы активно захватывают железо и не возвращают его в кровь. Этот процесс ведёт к перераспределению железа из циркулирующей крови в ретикуло-эндотелиальную систему, ограничению доступности железа для созревания клеток-предшественников эритроидного ряда и железодефицитному эритропоэзу. Гепцидин, белок острой фазы воспаления - ключевой элемент регуляции гомеостаза железа, вырабатываемый гепатоцитами. Интерлейкин-6 стимулирует выработку гепцидина в печени, тогда как гипоксия блокирует его синтез. Гиперэкспрессия гепцидина у мышей сопровождается выраженной железодефицитной анемией. Гепцидин нарушает процесс абсорбции железа в двенадцатиперстной кишке и блокирует высвобождение железа из макрофагов.
Противоопухолевое лечение, в свою очередь, может значительно уменьшить количество эритроцитов в крови за счёт миелосупрессии и нарушения синтеза гемопоэтических факторов, в том числе эритропоэтина, вырабатываемого в почках. Этот вариант развития малокровия относят к осложнениям противоопухолевого лечения и называют пост-цитостатической анемией. Большинство противоопухолевых препаратов подавляют гемопоэз. Платиновые и неплатиновые цитостатики угнетают клетки костного мозга и гемопоэтические клетки предшественники не только напрямую, но и косвенно - через повреждение микроокружения клеток костного мозга, возможно, повреждая клетки микроокроокружения или факторы, регулирующие гемопоэз. Особое внимание уделяют платиновым производным, не только проявляющим цитостатические свойства и вызывающим кумулятивную миелосупрессию, но и обладающим нефротоксичностью.
Гормон ЭПО синтезируется в основном перитубулярными интерстициальными и эндотелиальными клетками почек. Исследования не выявили значимой зависимости продукции эндогенного ЭПО от степени нефротоксичности химиотерапии (повышения уровня креатинина). Интересно, что повышение уровня эндогенного ЭПО у пациентов отмечают через 10-14 дней после введения цисплатина. Поскольку от химиотерапии платиновыми химиопрепаратами страдают именно те структуры, которые синтезируют ЭПО, можно предположить, что цитостатик нарушает функцию сенсоров кислорода, что ведёт к кратковременному увеличению продукции гематогормона.
Несомненно, конкретный случай анемии у пациента, получающего химиотерапию в связи с диссеминированным процессом, как правило, обусловлен комплексом причин (таких, как хроническая кровопотеря, дефицит кофакторов гемопоэза, нарушение обмена железа, сопутствующий воспалительный процесс). В клинической практике сложно выделить изолированную пост-цитостатическую анемию, можно лишь предположить, что ведущий фактор в возникновении анемии в данном случае - проводимая химиотерапия.
Эритропоэтин и регуляция эритропоэза
Эритропоэтин (ЭПО) - гликопротеиновый гормон, играющий главную роль в регуляции выработки эритроцитов, но не влияющий на тромбопоэз и другие составляющие гемопоэза. Уровень эндогенного ЭПО в норме составляет 20 МЕ/мл; при анемии и/или развитии артериальной гипоксемии содержание ЭПО может увеличиваться до 20000 МЕ/мл. Более чем у 50% онкологических больных отмечают низкий уровень эндогенного эритропоэтина. Гипоксия - главный стимул для продукции эндогенного эритропоэтина. При низком насыщении крови кислородом гетеродимер HIF (hypoxia-inducible factor - фактор, индуцируемый гипоксией, состоящий из двух субъединиц: a и b) стимулирует экспрессию не только ЭПО, но и целого ряда других генов, индуцируемых гипоксией: VEGF - гена фактора роста эндотелия сосудов, PDGF-b - тромбоцитарного фактора роста b, TGF-a - трансформирующего фактора роста a. При достаточном насыщении крови кислородом О2-зависимая пропил-гидроксилаза связывается с субъединицей HIF-1a, после чего гидроксилированный HIF-1a соединяется с белком фон Гиппель-Линдау (von-Hippel Lindau, рVHL). Образованный комплекс HIF-1a+рVHL служит мишенью для внутриклеточных протеасом, разрушающих HIF-1a. Гипоксия или недостаток рVHL ведут к избытку HIF и гиперэкспресии семейства гипоксия-индуцируемых генов, что увеличивает синтез не только ЭПО, но и фактора роста эндотелия, тромбоцитарного фактора роста b и трансформирующего фактора роста a.
Описанный механизм отвечает за выработку эритроцитов в условиях высокогорья, при заболеваниях сердца или лёгких, осложнённых гипоксемией, и при вариантах Hb, обладающих низким сродством к кислороду. В Чувашии выявлена семейная форма эритроцитоза - так называемая чувашская полицитемия. Заболевание вызвано мутацией гена VHL 598C3T, кодирующего синтез рVHL, и проявляется эритроцитозом, сосудистыми мальформациями и частыми тромбоэмболическими осложнениями. В плазме крови пациентов, гомозиготных по гену VHL 598C3T, отмечают высокие концентрации сосудистого эндотелиального фактора роста и почти 10-кратное повышение концентрации эритропоэтина. Однако повышение уровня ЭПО в плазме пациентов не сопровождается увеличением частоты онкологических заболеваний.
На поверхности эритроидных клеток-предшественников (BFU-E - розеткобразующие и CFU-E - колониеобразующие) ЭПО связывается с рецепторами эритропоэтина, стимулируя пролиферацию и дифференцировку эритроидных клеток. ЭПО не только стимулирует пролиферацию клеток-предшественников эритроидного ряда, но и увеличивает их выживаемость посредством увеличения выработки белка BCLXL, блокирующего апоптоз.
Поскольку увеличение числа зрелых эритроцитов сопровождается возрастанием кислородной ёмкости крови, гипоксия как стимул для коррекции Hb нивелируется, и секреция эндогенного ЭПО уменьшается. Таким образом, количество циркулирующих эритроцитов регулируется эндогенным ЭПО по принципу обратной связи.
Образование новых эритроцитов в костном мозге зависит от уровня эндогенного ЭПО в плазме. Продукция ЭПО, неадекватная степени гипоксии, может привести к развитию анемии. Кроме этого, необходимые условия полноценного эритропоэза - достаточное содержание в организме витамина В12, фолиевой кислоты и железа. Витамин В12 и фолиевая кислота необходимы для синтеза ДНК, а железо - для синтеза гемоглобина. Без адекватных запасов и/или своевременного поступления в организм этих веществ нормальный процесс эритропоэза невозможен даже в условиях избыточного содержания ЭПО в плазме. Большинство пациентов имеют достаточный запас кобаламина, тогда как доступность фолиевой кислоты и железа может быть ограничена. При ускоренном эритропоэзе возможно развитие функционального дефицита, в первую очередь, железа и фолиевой кислоты.
В исследованиях последних лет показано, что рецепторы ЭПО присутствуют во многих органах и тканях, а эритропоэтин может способствовать выживанию и дифференцировке неэритроидных клеток. ЭПО обладает широким спектром активности, особенно в таких органах, как головной мозг, яичники, матка и маточные трубы, яички. ЭПО важен для развития и функционирования головного мозга, показано его значение в стимуляции неоангиогенеза.
В последние годы опубликованы результаты исследований рецепторов ЭПО в различных культурах опухолевых клеток. На поверхности клеток рака молочной железы, рака яичников и других злокачественных опухолей обнаружены рецепторы, аналогичные по строению рецепторам ЭПО, но функционально отличающиеся от них. Введение эритропоэтина не приводило к стимуляции роста опухолевых клеток. Экспериментальные исследования не подтвердили теории стимуляции опухолевого роста экзогенным эритропоэтином.
Гипоксия - универсальный повреждающий фактор
Недостаток кислородной ёмкости крови может компенсироваться несколькими механизмами. Например, выработка в эритроцитах дополнительного количества 2,3-дифосфоглицерата приводит к уменьшению сродства кислорода к гемоглобину и к увеличению диссоциации кислорода из эритроцитов в тканях. Этот механизм может компенсировать до половины дефицита потребности в кислороде при анемии. Следующий рубеж защиты организма - увеличение сердечного выброса и частоты дыхания, стимуляция выработки эндогенного эритропоэтина.
При снижении уровня Hb кислородная ёмкость крови уменьшается, и развивается тканевая гипоксия. Хроническая гипоксия может существенно влиять на рост опухоли и процесс метастазирования. Как было упомянуто ранее, гипоксия индуцирует продукцию сосудистого эндотелиального фактора роста (VЕGF) и других факторов, стимулирующих неоангиогенез; приводит к нарушению процесса апоптоза и формированию резистентных клонов опухолевых клеток.
Гипоксия приводит к увеличению частоты спонтанных мутаций. Одно из следствий такого гипермутабельного состояния - поломки гена р53, определяющего способность клетки к апоптозу. Нарушение работы этого гена может значительно снизить чувствительность опухоли к химиолучевой терапии.
Снижение уровня Hb при проведении адъювантной химиотерапии ухудшает выживаемость больных раком молочной железы. Анализируя 129 случаев лечения операбельного процесса, исследователи выявили статистически достоверную корреляцию между снижением отдалённой безрецидивной и общей выживаемости и анемией, развившейся в процессе проведения адъювантной химиотерапии (HR 1,54; 95% ДИ, 1,04-2,32). При развитии анемии относительный риск рецидива заболевания и смерти от прогрессирования процесса увеличивался в 1,5 раза.
Химиотерапия и факторы прогноза развития пост-цитостатической анемии
Анемия - хорошо известное осложнение злокачественного заболевания и побочный эффект его лечения. Снижение концентрации Hb в крови может быть одним из первых признаков заболевания, однако между степенью выраженности анемии и тяжестью злокачественного процесса, определившего её появление, нет прямой зависимости. Частота развития анемии при онкопатологии варьирует в зависимости от типа опухоли и характера лечения. Идентификация групп риска развития пост-цитостатической анемии позволяет предупредить клинически значимые осложнения гипоксемии.
По данным, полученным в Европейском Исследовании Анемии при Раке (European Cancer Anemia Survey, ECAS, 2001), анемию отмечали у 35% пациентов с впервые выявленным онкологическим процессом, у 49% пациентов, получающих противоопухолевое лечение, и у 31% больных, находившихся в стадии ремиссии. Отмечено, что на протяжении болезни (6 мес наблюдения) анемию (Нb<120 г/л) наблюдали у 72% пациентов с гематологической патологией и у 66% больных с солидными новообразованиями. В таблице Х-1 приведены данные ECAS по влиянию вида лечения и типа опухоли на вероятность появления анемии в процессе лечения.
Таблица Х-1. Частота развития анемии на фоне противоопухолевого лечения
Лечение |
Тип опухоли |
|||
Химиотерапия |
Лучевая терапия |
Гемобластозы |
Солидные |
|
Без анемии при включении |
2101 |
514 |
297 |
- |
Анемия на фоне противоопухолевого лечения |
1317 (63%) |
100 (20%) |
154 (52%) |
1228 (54%) |
Ретроспективное исследование определило ряд закономерностей:
-
химиотерапия приводит к снижению уровня Hb крови при всех онкологических заболеваниях;
-
исходно низкий уровень Нb определяет большую необходимость в гемотрансфузиях при последующем лечении;
-
высокую вероятность развития анемии прогнозируют при использовании в лечении платиносодержащих режимов;
-
высокую вероятность развития анемии на фоне химиотерапии прогнозируют при уровне Hb<120 г/л.
Многофакторный анализ показал, что уровень Нb<120 г/л, неудовлетворительный объективный статус больного и число лимфоцитов менее 700 кл/мм3 до начала химиотерапии коррелируют с высокой вероятностью развития клинически значимой анемии в процессе лечения.
Анализ 2070 случаев развития анемии на фоне химиотерапии (исследование ECAS) выявил несколько клинических факторов, статистически значимых для прогноза развития анемии при проведении лекарственного лечения.
-
Сниженный начальный уровень Hb (<129 г/л для женщин и <134 г/л для мужчин) означал 4-кратное увеличение вероятности развития анемии.
-
Тип опухоли: у больных раком лёгкого, яичников, тела и шейки матки вероятность анемии в 3 раза выше, чем в случае рака желудочно-кишечного тракта/толстой кишки (ЖКТ); лечение злокачественных опухолей других локализаций осложнялось анемией в 2,3 раза чаще, чем при опухолях ЖКТ.
-
Вид химиотерапии: платино-содержащая химиотерапия осложнялась анемией в 2,1 раза чаще неплатиновой.
-
Пол: у женщин анемия развивалась в 1,5 раза чаще, чем у мужчин.
В таблице Х-2 приведены значения факторов риска развития анемии.
Таблица Х-2. Значения факторов прогноза развития анемии при химиотерапии
| Фактор прогноза | ОР | 95% ДИ | Значение (Wald) р | Коэффициент β | Значение риска |
|---|---|---|---|---|---|
Начальный уровень Hb, г/л |
2,98 |
2,2-4,1 |
<0,0001 |
1,09 |
11 |
Лёгкое/гинекол vs ЖКТ/КРР |
3,05 |
1,8-5,1 |
<0,0001 |
1,12 |
11 |
Другие vs ЖКТ/КРР |
2,23 |
1,5-3,4 |
0,0002 |
0,80 |
8 |
Лечение с препаратами платины |
2,28 |
1,5-3,4 |
<0,0001 |
0,82 |
8 |
Пол: женщины vs мужчины |
1,78 |
1,3-2,4 |
0,0002 |
0,57 |
6 |
Hb - гемоглобин, ОР - относительный риск; ДИ - доверительный интервал; ЖКТ/КРР - опухоли желудочно-кишечного тракта/колоректальный рак
Авторы исследования предлагают удобный и надёжный инструмент определения вероятности развития анемии на основании клинических данных. Суммируя значения риска для конкретного случая, можно оценить вероятность (низкая, промежуточная и высокая) развития анемии при проведении данного лечения у конкретного пациента. Группа "низкой вероятности" определена как сумма значений риска от 1 до 15 баллов: только у 45% больных из этой группы развивается анемия. Группа "промежуточной вероятности" - сумма баллов риска 16-23: у 71% больных развивается анемия; если сумма значений риска>24 - пациент относится к группе "высокого риска" с вероятностью анемии 84%. Уровень Hb может значительно снизиться сразу после начала химиотерапии и углубляться с каждым последующим курсом лечения. В исследовании ECAS отмечено, что после 1 курса химиотерапии анемия развивалась в 19,5% случаев, после 2-го курса - в 34,3% случаев и после каждого последующего цикла - в 40% случаев. К моменту выявления анемии параметры качества жизни пациента могут существенно ухудшиться, а уровень Hb может упасть ещё ниже, чем до начала лечения анемии.
Вероятность развития и степень выраженности анемии зависят от выбранного режима лечения. В таблице Х-3 приведены сводные данные по вероятности развития анемии при некоторых вариантах химиотерапии.
Таблица Х-3. Частота анемии при проведении химиотерапии
| Режим | Тип опухоли | Степень I или II, %* | Степень III или IV, %* |
|---|---|---|---|
CAF |
Рак молочной железы (n=165) |
55% |
11% |
Топотекан |
Рак яичников (n=111) |
68% |
32% |
CHOP |
Неходжкинская лимфома (n=212) |
49% |
17-79% |
Паклитаксел/карбоплатин |
Немелкоклеточный рак лёгкого (n=81) |
10-59% |
5-34% |
* Шкалы ВОЗ или NCI.
Классификация и симптоматология анемии опухолевого процесса
Анемия проявляется целым рядом симптомов, обусловленных развитием тканевой гипоксии в органах и тканях с последующим нарушением их функций. Степень выраженности этих симптомов зависит от таких факторов, как глубина анемии, скорость развития компенсаторных механизмов, наличия сопутствующей патологии и функционального статуса пациента. В таблице Х-4 приведены основные параметры классификации пост-цитостатической анемии как осложнения химиотерапии.
Степень выраженности проявлений анемического синдрома зависит не только от абсолютной величины концентрации гемоглобина крови, но и от скорости снижения уровня гемоглобина. Медленно развивающаяся анемия у молодого человека остаётся клинически незаметной долгое время, как правило, до значительного или резкого уменьшения концентрации Hb или до эпизода перегрузки. Для пожилого больного с "букетом" сопутствующих заболеваний даже незначительное, но быстрое снижение уровня гемоглобина может иметь тяжёлые последствия: ухудшение течения ишемической болезни сердца, неврологические, психотические расстройства и т.д. Анемия при хронической сердечной недостаточности сама по себе ухудшает выживаемость. Снижение уровня Hb ниже 80 г/л у пациента, страдающего ишемической болезнью сердца, достоверно повышает вероятность эпизода коронарной недостаточности.
Таблица Х-4. Классификация анемии по степени выраженности
Система |
Степень выраженности |
||||
0 |
1 |
2 |
3 |
4 |
|
NCI |
Нет |
Лёгкая |
Умеренная |
Выраженная |
Тяжёлая |
WHO |
>110 г/л |
110-95 |
95-80 |
80-65 |
<65 |
EORTC |
>110 |
110-95 |
95-75 |
75-60 |
<60 |
Таблица Х-5. Симптомы анемии (Ludwig & Strasser, 2001)
| Орган, страдающий при декомпенсации | Симптомы |
|---|---|
Головной мозг |
Утомляемость, усталость |
Глаза |
Повреждение сетчатки глаза |
Сердце |
Сердцебиение, |
Лёгкие |
Учащение дыхания |
Почки |
Задержка жидкости, отёки |
Кишечник |
Потеря аппетита |
Мышцы |
Утомляемость |
Кожа |
Бледность |
Репродуктивная система |
Нарушение менструальной функции (дисменорея) |
Отдельного внимания заслуживает утомляемость. Утомляемость (fatigue) - состояние слабости, наступающее после эпизода физического/умственного напряжения и характеризующееся уменьшением работоспособности и снижением эффективности ответа на стимуляцию. Этот симптом встречается у 75% онкологических больных. Более того, в условиях доступности полноценного обезболивания утомляемость описывают как самый частый симптом рака. Исследование Фогельзанг (Vogelzang N.J) показало, что в группе из 419 пациенток с различными онкологическими заболеваниями, выбранных случайно из 100 тысяч домохозяек при телефонном опросе, 78% больных испытывали утомляемость в процессе болезни и лечения. Более 60% пациенток отмечали, что утомляемость ухудшала повседневную жизнь сильнее, чем боль, вызванная опухолью. Пациенты определяют утомляемость как основной побочный эффект химиотерапии, более значимый, чем тошнота и боль. Экономически это выражается в уменьшении работоспособности пациентов с ежемесячной потерей 4,2 рабочих дня.
Таблица Х-6. Утомляемость онкологических больных в зависимости от вида лечения
Утомляемость и рак (без лечения) |
78% |
Утомляемость и химиотерапия |
60-90% |
Утомляемость и лучевое лечение |
75-100% |
Несколько исследований выявили взаимосвязь между частотой утомляемости и противоопухолевым лечением (таблица Х-6). Исследования качества жизни при анемии доказали прямое влияние уровня Hb на утомляемость и остальные параметры качества жизни. Повышение уровня Hb сопровождается достоверным улучшением субъективной оценки больными своего состояния (таблица Х-7).
Таблица Х-7. Взаимосвязь анемии и утомляемости Hb>120 vs Hb<120 г/л
| Параметры качества жизни | Значение Р |
|---|---|
Выше показатели качества жизни |
0,003 |
Меньше утомляемость |
0,01 |
Менее выражены другие симптомы анемии |
0,02 |
Лучше физическое благополучие |
0,003 |
Лучше функциональное благополучие |
0,001 |
Лечение анемии: как, когда, как долго?
В лечении анемии условно выделяют 2 подхода: патогенетический и симптоматический. К патогенетическому варианту можно отнести устранение причин анемии, в том числе эффективное противоопухолевое лечение; коррекцию дефицита кофакторов гемопоэза (железа, фолиевой кислоты) и алиментарных нарушений. Отдельно следует рассматривать необходимость устранения абсолютного или относительного дефицита эндогенного эритропоэтина. Пример симптоматического лечения - трансфузия эритроцитарной массы, временно восполняющая количественный дефицит эритроцитов.
Трансфузия эритроцитарной массы - признанный вариант лечения острой симптомной анемии. В ситуации, угрожающей жизни больного, осложнения, свойственные аутогемотрансфузии, отходят на второй план. Однако возможность развития побочных эффектов при лечении хронической анемии гемотрансфузиями часто определяет отказ от этого метода и доктором, и пациентом. Поскольку переливание консервированной крови (в консервированных эритроцитах быстро уменьшается содержание 2,3-диглцерофосфата, регулирующего аффинитет кислорода и гема) не ведёт к увеличению кислородной ёмкости крови реципиента, простое увеличение показателя содержания Hb клинически незначимо.
При анализе крови доноров на наличие инфекции современные лаборатории используют наиболее точные методики, что минимизирует вероятность передачи вирусных инфекций: вируса иммунодефицита человека, сывороточного гепатита (В и С), цитомегаловируса и т.д. Однако среди осложнений многократных гемотрансфузий по-прежнему актуальны сывороточный гепатит, СПИД, цитомегаловирусная инфекция, а также аллергические реакции, анафилаксия, перегрузка железом (гемосидероз печени и миокарда).
Типичные осложнения гемотрансфузии:
В реальной клинической ситуации (особенно в случаях малосимптомной анемии) лечебные мероприятия, как правило, ограничиваются перерывом в проведении противоопухолевого лечения с последующей редукцией доз цитостатиков, назначением препаратов железа, поливитаминов. Одна стандартная доза эритромассы увеличивает концентрацию Hb на 10 г/л. В клинической практике США и стран Европы взрослым однократно переливают 2 дозы с интервалом в среднем 1 раз в 4-5 нед. Для достижения и поддержания уровня Hb в пределах физиологической нормы необходимы неоднократные гемотрансфузии.
Средний уровень Hb крови в странах Европы, при котором назначают переливания эритроцитарной массы, составляет 82 г/л. Принимая во внимание новые данные о значении анемии для качества жизни, эта точка отсчёта в большинстве случаев неадекватна. Однако, даже если показанием к гемотрансфузии считать уровень Hb<90 г/л, большую часть времени пациенты будут оставаться в состоянии гипоксии. Главное преимущество трансфузии эритроцитарной массы - быстрое и дозируемое увеличение концентрации Hb крови - следует использовать в случаях острой симптомной анемии.
Эпоэтин-альфа - первый рекомбинантный человеческий эритропоэтин-a (эпрексª, Procrit®) был зарегистрирован в 1989 г. для лечения нефрогенной анемии, а в 1993 г - для лечения анемии при онкологических заболеваниях. Аналогично эндогенному гормону ЭПО, этот препарат стимулирует клеточную пролиферацию и дифференцировку, блокирует апоптоз, индуцируемый цитостатиками в клетках-предшественниках эритроидного ряда. Позднее появились другие препараты, стимулирующие эритропоэз: эпоэтин-бета (рекормонª), дарбепоэтин-a (Аранесп®). Сегодня на фармацевтическом рынке Российской Федерации представлены несколько стимуляторов эритропоэза: эпрексª, неорекормон®, Аранесп®, а также препараты биоаналоги: эритростимª и вероэпоэтин® в дозах, применяемых при нефрогенной анемии.
Дарбепоэтин-a - полусинтетический аналог ЭПО. Молекула дарбепоэтина-a отличается большим количеством гликозилированных связей, что определяет её стабильность в плазме. Увеличение периода полувыведения дарбепоэтина-a нивелирует меньшее сродство молекулы препарата к рецептору эритропоэтина и позволяет использовать режим введения с интервалом 1 раз в 2-3 нед.
Стимуляторы эритропоэза назначают при пост-цитостатической анемии I-III степени, при быстром (10 г/л за 1 месяц) снижении уровня Hb на фоне лечения, при наличии противопоказаний к гемотрансфузии в случаях анемии IV степени. Стандартный дозовый режим коррекции предполагает подкожное введение эпоэтина-a по 10 000 MЕ 3 раза в неделю. При подкожном введении время полувыведения эпоэтина-a существенно выше, чем при внутривенном. На основании результатов многих исследований к практическому применению рекомендованы следующие режимы использования эпоэтина-a: 10 000 МЕ 3 раза в нед и 40 000 Ед 1 раз в нед. Оба режима хорошо переносимы, эффективно повышают уровень Hb, снижают потребность в гемотрансфузиях и улучшают качество жизни больных, получающих химиотерапию в связи с различными опухолевыми заболеваниями.
Применение эпоэтина-a в дозе 10 000 МЕ 3 раза в нед у пациентов с анемией на фоне платино- и неплатино-содержащей химиотерапии эффективно повышало уровень Hb в среднем на 18 г/л и 20 г/л соответственно (P<001) от исходного, независимо от противоопухолевого эффекта химиотерапии. Рандомизированное плацебо-контролируемое исследование подтвердило эффективность режима еженедельного введения эпоэтина-a в дозе 40 000 МЕ: прирост концентрации Hb в группе, получающей эпоэтин-a, составил 28 г/л, что достоверно выше, чем группе, получавшей плацебо (9 г/л; P<0,001). Эффективность лечения выражалась в достоверном уменьшении потребности в гемотрансфузиях и улучшении параметров качества жизни.
Клинические исследования дарбепоэтина-a подтвердили эффективность препарата при лечении пост-цитостатической анемии, он зарегистрирован в качестве стимулятора эритропоэза у онкологических больных. В двойном слепом плацебо-контролируемом рандомизированном исследовании III фазы 320 пациентов получали дарбепоэтин-a или плацебо в дозе 2,25 мкг/кг массы тела в неделю. Пациенты из группы, получавшей дарбепоэтин-a, реже нуждались в гемотрансфузиях по сравнению с больными, получавшими плацебо (27% против 52%; P<0,001).
В двух других исследованиях оценили возможность использования более длительного периода полувыведения дарбепоэтина-a для увеличения интервала между введениями препарата. Гласпи (Glaspy) с соавторами провели исследование I/II фазы, в котором 128 пациентов получали дарбепоэтин-a в дозе 3,0; 5,0; 7,0 или 9,0 мкг/кг 1 раз в 2 нед либо эпоэтин-a 40 000 ЕД еженедельно. Повышение дозы эпоэтина-a проводили так же, как в предшествующих исследованиях. Клинически эффективные дозы дарбепоэтина-a составили 3,0 и 5,0 мкг/кг при введении 1 раз в 2 нед. При лечении этими дозами повышение уровня гемоглобина на 20 г/л или достижение уровня Hb 120 г/л составило 66 и 84%, соответственно. Авторы исследования сделали вывод, что введение дарбепоэтина-a 1 раз в 2 нед вызывает хороший гематопоэтический эффект. Изученный режим применения дарбепоэтина-a по эффективности сопоставим со стандартами эпоэтина-a.
Сравнительное фармакодинамическое исследование дозовых режимов эпоэтина-a по 40 000 МЕ раз в нед и по 10 000 МЕ 3 раза в нед подтвердило их равную эффективность: динамика прироста уровня Hb на фоне применения препарата одинакова. Для определения оптимального режима использования эпоэтина-a при пост-цитостатической анемии (Hb<105 г/л, платино-содержащая химиотерапия, длительность лечения эпоэтином-a - 12 нед), исследователи взяли за эталон стандартный дозовый режим: 10 000 МЕ (150 МЕ/кг при средней массе тела 70 кг) 3 раза в нед. Авторы сравнили эффективность плацебо и однократных еженедельных введений эпоэтина-a в дозах 20 000 МЕ (300 МЕ/кг), 30 000 МЕ (450 МЕ/кг), 40 000 МЕ (600 МЕ/кг) и 60 000 МЕ (900 МЕ/кг). Результаты исследования подтвердили линейную зависимость клинической эффективности эпоэтина-a от используемой дозы: как по степени, так и по скорости роста уровня Hb наиболее эффективным был режим еженедельного использования препарата в дозе 60 000 МЕ (900 МЕ/кг). Эффективность еженедельного режима в дозе 40 000 МЕ совпадала с режимом-эталоном (прирост содержания Hb 28 г/л и 26 г/л). Эффект дозы 20 000 МЕ достоверно не отличался от применения плацебо, значимый прирост уровня Hb отмечался при дозе 30 000 МЕ и выше, наибольший прирост содержания Hb отмечен в группе, получавшей препарат в дозе 60 000 МЕ (38 г/л). Время достижения эффекта зависело от дозовой интенсивности: при уменьшении недельной дозы увеличивался период до получения эффекта.
Длительность применения эпоэтина-a, как правило, зависит от эффективности препарата, но в любом случае составляет не менее 4 недель. В случае эффекта - повышения содержания Hb на 10 г/л за 4 недели лечения препаратом в дозе 10 000 МЕ 3 раза в неделю - терапию продолжают в течение 12-16 нед или до достижения границы физиологической нормы Hb (120 г/л). При достижения уровня Hb=120 г/л на фоне продолжающейся химиотерапии использование препарата может быть продолжено с редукцией дозы приблизительно на 30% (эпоэтин-a по 10 000 МЕ 2 раза в нед) уже с целью поддержания достигнутого уровня Hb. При быстром приросте содержания Hb (>15 г/л за 2 нед) оправдана модификация режима с уменьшением дозовой интенсивности препарата (например, 10 000 МЕ п/к 2 раза в нед, 40 000 МЕ 1 раз в 9-10 дней). При медленном увеличении концентрации Hb (менее 10 г/л за 4 нед лечения эпоэтином-a) Руководство по лечению анемии Американского Общества Клинической Онкологии (ASCO) считает оправданным увеличение разовой дозы эпоэтина-a до 20 000 МЕ. Поскольку эффективность эпоэтина-a зависит от дозы вводимого препарата, эта стратегия результативна ещё для 25% пациентов, первично рефрактерных к эпоэтину-a.
Эффективность лечения анемии с использованием более редкого введения (1 раз в нед) при одновременном увеличении разовой дозы эпоэтина-a (600 МЕ/кг и более) соответствует стандартному дозовому режиму; повышает уровень Hb в 68-80% случаев и достоверно уменьшает необходимость гемотрансфузий. Снижение частоты введения препарата позволяет снизить затраты на медицинское обслуживание.
Лечение анемии стимуляторами эритропоэза в стандартных дозах малоэффективно приблизительно у 30% пациентов (прирост Hb<10 г/л за 4 нед), однако это количество может быть сокращено при уточнении противопоказаний. Основные причины неэффективности рекомбинантных стимуляторов эритропоэза: высокий уровень цитокинов воспаления, генетический вариант рецепторов ЭПО, абсолютный или функциональный дефицит железа.
Эпоэтин эффективен при рецидиве пост-цитостатической анемии, алгоритм лечения анемии прежний. Эффективность эпоэтина не зависит от концентрации в крови эндогенного ЭПО, уровня сывороточного железа и объективного статуса пациента. Абсолютный дефицит эндогенного ЭПО в условиях анемии (<100 Ед/л) - прямое показание к назначению стимуляторов эритропоэза. Ответ на введение экзогенного эпоэтина часто зависит от способности организма пациента вырабатывать собственный ЭПО в ответ на гипоксемию. Введение эпоэтина эффективно, если в организме онкологического больного при анемии вырабатывается свой ЭПО, но его количество недостаточно для адекватной стимуляции эритропоэза. С другой стороны, введение гормона малоэффективно у гематологических больных при превышении эндогенным ЭПО уровня 500 mIU/мл.
Препараты железа и пост-цитостатическая анемия
Препараты железа при лечении пост-цитостатической анемии необходимы только в случае истинного железодефицитного состояния или при функциональном дефиците железа. Низкий уровень сывороточного железа, как правило, свидетельствует о нарушении обмена железа, но не о его дефиците. Низкое содержание сывороточного железа может указывать на нарушение процесса всасывания элемента в двенадцатиперстной кишке. При распространённых опухолевых заболеваниях, также как и после травмы, и при хронических воспалительных заболеваниях, высокий уровень интерлейкина-6 стимулирует синтез гепатоцитами белка гепцидина; гепцидин блокирует абсорбцию железа энтероцитами и процесс высвобождения Fe из депо. Низкий уровень железа плазмы при этих заболеваниях сочетается со значительными запасами железа в организме; уровень ферритина плазмы превышает норму в несколько раз. В таких случаях, вследствие отложения гемосидерина в органах (печень, сердце) и развития органной недостаточности, существует угроза развития гемосидероза. При этом использование препаратов железа и переливание эритромассы противопоказаны. Так, при миелодиспластическом синдроме частые переливания крови осложняются гемосидерозом миокарда и застойной сердечной недстаточностью.
Истинный дефицит железа при пост-цитостатической анемии отмечают редко. Чаще описывают феномен функционального дефицита железа - несоответствие количества Fe2+, доступного для синтеза гема, потребностям ускоренного эритропоэза при применении стимуляторов эритропоэза. Функциональный дефицита железа может быть одной из причин недостаточной эффективности эпоэтина-a. Для диагностики функционального дефицита необходимо определение уровня ферритина плазмы и процента насыщения трансферрина железом. Признаки функционального дефицита железа: снижение концентрации ферритина плазмы <100 нг/мл и снижение показателя насыщения трансферрина плазмы железом <20%. При коррекции железодефицита, сопутствущего нефрогенной и пост-цитостатической анемии, в нефрологии и онкологии препараты железа для приёма внутрь часто неэффективны, что объясняется гиперэкспрессией гепцидина при анемии хронического заболевания. В этом случае используют парентеральные препараты - соединения Fe с сахарами. Для использования в клинической практике доступны железа глюконат+марганца глюконат+меди глюконат, железа [III] гидроксид декстран и железа [III] гидроксид сахарозный комплекс. Перед началом лечения сахарами железа необходимо вводить пробные дозы препарата. Для минимизации побочных эффектов пациентам, которым назначены указанные препараты, необходимо предварительно вводить дифенилгидрамин или парацетамол (ацетаминофенª). Препараты можно применять еженедельно в дозе 100 мг (в/в медленная инъекция или короткая инфузия), или в виде нагрузочной дозы 400 мг в/в 1 раз в 3 нед.
Рандомизированное исследование М. Ауэрбаха (Auerbach М.) оценило влияние различных методов введения препаратов железа (1 группа - без железа, 2 группа - приём железа внутрь, 3 и 4 группы - препарат внутривенно еженедельно или 1 раз в 3 нед соответственно) на эффективность лечения пост-цитостатической анемии эпоэтином-a (10 000 МЕ 3 р/нед в течение 6 нед). Лечение эпоэтином-a было достоверно эффективнее при парентеральном введении железа по сравнению с приёмом железа внутрь или с лечением без применения железа. Эффективность эпоэтина-a при приёме препаратов железа внутрь была такой же, как и в группе пациентов, не получавших железа.
Когда начинать терапию пост-цитостатической анемии?
Выявление сниженного уровня Hb - показание к уточнению патогенеза анемии и началу её лечения. Исследование Литлвуд (Littlewood, 2001) показало, что раннее назначение эпоэтина позволяет добиться прироста содержания Hb быстрее, чем при отложенном начале лечения анемии (138 г/л vs 128 г/л), и минимизировать потребности в гемотрансфузиях (7% vs 28%). Задачей проспективного рандомизированного исследования в группе пациентов (n=315), получавших химиотерапию с производными платины, было сравнение эффективности эпоэтина-a с наилучшим лечением при анемии. Анализ показал, что при, казалось бы, клинически незначимой анемии I ст. (Hb=100-120 г/л) применение эпоэтина-a привело к достоверному улучшению параметров качества жизни, повышению уровня гемоглобина и уменьшению потребности в гемотрансфузиях. Подобное исследование Дж. Чанг (Chang J.) подтвердило целесообразность раннего назначения эпоэтина-a по 40 000 Ед еженедельно: отмечено, что вероятность гемотрансфузии при раннем начале терапии анемии (6,9%) в несколько раз меньше, чем при отсроченном лечении (24%), а эффективность раннего лечения достоверно выше (Hb+11 г/л vs Hb-5 г/л).
Американское общество клинических онкологов рекомендует начинать лечение эпоэтином-a при уровне Hb ниже 120 г/л. Задачи лечения - улучшение качества жизни и уменьшение потребности в гемотрансфузиях; лечение продолжают до нормализации содержания Hb.
Сегодня можно с уверенностью говорить о целесообразности ранней коррекции анемии. Необходимо учитывать не только абсолютное значение содержания Hb, но и его динамику на фоне лечения. Быстрое снижение уровня Hb (на 15 г/л за 6-8 нед) существенно повышает вероятность развития анемии (до 70-85%) и необходимость в гемотрансфузиях (до 30-50%). Следует помнить, что введение эпоэтина не даёт моментального эффекта: гематологический и клинический эффект можно ожидать не ранее, чем через 3-4 нед от начала применения гормона.
Стимуляторы эритропоэза: функциональное состояние пациента и качество жизни
Множество данных указывает на взаимосвязь анемии и утомляемости, одной из главных причин ухудшения качества жизни онкологических больных. В нескольких рандомизированных плацебо-контролируемых исследованиях при применении эпоэтина-a одновременно с химиотерапией зарегистрировано статистически значимое улучшение параметров качества жизни пациентов. По шкале LASA (оценка по линейной аналоговой шкале) в группе, получавшей эпоэтин-a, отмечено среднее повышение уровня качества жизни по сравнению с пациентами из группы, получавшей плацебо (энергия = P <0,001; выполнение повседневных дел = P <0,01 и качество жизни в целом = P <0,01). Остальные данные, подтверждающие наличие связи между анемией и усталостью, получены в нерандомизированных клинических исследованиях, в частности, в трёх открытых популяционных исследованиях примерно 7 000 пациентов. В двух из этих исследований пациенты получали эпоэтин-a в дозе 10 000 МЕ 3 раза в нед, а в исследовании Габрилова (Gabrilove J., 2001) пациентам подкожно вводили эпоэтин-a по 40 000 МЕ один раз в нед. Результаты оценки повышения уровня Hb, снижения потребности в гемотрансфузиях и улучшения качества жизни при всех трёх исследованиях сходны. В каждом из исследований отмечено статистически значимое повышение уровня гемоглобина по сравнению с исходным и статистически значимое снижение частоты гемотрансфузий. С помощью инструментов оценки качества жизни, используемых самими пациентами (например, FACT-An (оценка функционирования при противоопухолевой терапии) или, как в двух последних исследованиях, шкала оценки выраженности проявлений анемии), показана зависимость между повышением уровня Hb и значимым улучшением качества жизни.
Отмеченное улучшение основных параметров качества жизни (энергия, ежедневная активность, качество жизни в целом) напрямую зависело от степени прироста концентрации Hb и не зависело от эффективности противоопухолевого лечения. Максимальное статистически достоверное улучшение параметров качества жизни выявлено при приросте концентрации Hb >20 г/л.
В рандомизированном плацебо-контролируемом исследовании Ванстеенкисте (Vansteenkiste) с соавторами, где участвовали 320 больных раком лёгкого, применение дарбэпоэтина-a повышало качество жизни пациентов достоверно эффективнее плацебо (Р=0,052), (шкала Functional Assessment of Сancer Therapy-Fatigue, FACT-F).
Стимуляторы эритропоэза: безопасность применения и влияние на выживаемость
Увеличение выживаемости - главная цель лечения онкологических больных. Данные о взаимосвязи умеренной и глубокой анемии с худшим прогнозом жизни и лечения позволили предположить, что при коррекции анемии можно увеличить выживаемость. В исследовании Литтлвуда (Littlewood’а) (n=375 больных) медиана выживаемости пациентов, получавших эпоэтин-a, составила 17 мес, а в группе плацебо - 11 мес (Р-0,13). Увеличение выживаемости (статистически незначимое) при лечении анемии эпоэтином-a vs плацебо на фоне химиотерапии отмечено в недавнем рандомизированном исследовании NCCTG.
При исследовании влияния профилактического использования эпоэтина-b (с целью повышения уровня Hb >140/150 г/л) на выживаемость больных раком головы и шеи (n=351) на фоне лучевой терапии неожиданно получен отрицательный результат. В группе больных, получавших эпоэтин-b, зарегистрировано ухудшение локо-регионарного контроля (сравнит. риск 1,62, p=.0008), снижение выживаемости (сравнит. риск 1,39, p=.02), повышение частоты сосудистых осложнений (11%) по сравнению с группой, получавшей плацебо (5%).
Не подтвердилась также идея увеличения выживаемости больных метастатическим раком молочной железы (n=939) при использовании эпоэтина-a для профилактики пост-цитостатической анемии. Исследование было преждевременно остановлено в связи с ухудшением годичной выживаемости в группе пациентов, получавших эпоэтин-a, в сравнении с группой, получавшей плацебо: 70% vs 76%, p<0,01. Анализ полученных данных выявил несколько существенных моментов, возможно, искажающих результаты. При одном и том же времени до прогрессирования заболевания и одинаковой эффективности химиотерапии в сравниваемых группах в группе, получавшей эпоэтин-a, количество случаев раннего (<4 мес) прогрессирования было выше. Возможно, негативно повлияли токсичность химиотерапии и повышение частоты тромбоэмболических осложнений (14 случаев в группе, получавшей эпоэтин-a, и 4 - в группе, получавшей плацебо). В ранних клинических исследованиях отмечен рост числа тромбоэмболических осложнений при использовании препаратов эпоэтина с профилактической целью: показано, что высокий гематокрит (42±3%) сопровождался повышенной смертностью вследствие увеличения частоты сосудистых осложнений (артериальных и венозных тромбозов).
Последний метаанализ подтвердил, что при использовании в онкологии стимуляторов эритропоэза (рекомбинантных эритропоэтинов) у больных возрастает вероятность развития тромбоэмболических осложнений. Увеличение числа тромбоэмболических осложнений при лечении нефрогенной, пост-цитостатической и раковой анемии отмечено в нескольких клинических исследованиях. Тромбоэмболические осложнения при онкологических заболеваниях - третья по частоте причина смерти больных. В рандомизированном исследовании CLOT сравнивали эффективность низкомолекулярного гепарина (далтепарина натрия) и варфарина в профилактике тромбоэмболических осложнений. По результатам исследования далтепарин натрия оказался вдвое эффективнее варфарина: риск рецидива тромбоэмболических осложнений составил 9% и 17%, соответственно. В настоящее время ряд клинических руководств рекомендует длительное профилактическое использование низкомолекулярных гепаринов (далтепарин натрия) у пациентов, входящих в группу риска по тромбоэмболическим осложнениям, в том числе и для онкологических больных, получающих химиотерапию, лучевую терапию и гематогормоны. В исследовании эффективности эпоэтина-a vs плацебо у пациентов после тяжёлых травм отмечено, что одновременное назначение гепарина натрия и эпоэтина-a не сопровождалось увеличением числа тромбоэмболических осложнений, в отличие от группы, получавшей только эпоэтин-a.
Последний анализ безопасности использования стимуляторов эритропоэза, опубликованный Наблюдательным Советом по Онкологическим препаратам при Комиссии по контролю над пищевыми продуктами и лекарствами США (ODAC FDA), отметил ухудшение выживаемости и увеличение числа тромбоэмболических осложнений при применении стимуляторов эритропоэза за пределами разрешённых показаний к использованию этих лекарств. Наблюдательный совет, подчеркнув недопустимость профилактического использования стимуляторов эритропоэза, подтвердил их безопасность в лечении пост-цитостатической анемии для уменьшения потребности в гемотрансфузиях и установил целевой уровень гемоглобина на уровне 120 г/л.
Противопоказания к применению рекомбинантных стимуляторов эритропоэза:
Эффективность препаратов снижается при острой инфекции (высоком уровне цитокинов воспаления), прогрессирующем ухудшении белково-синтетической функции печени, значительном снижение резервов костномозгового кроветворения после многократных курсов химиотерапии и лучевого лечения.
Несколько лет назад в научной литературе активно обсуждали случаи аплазии красного кровяного ростка (PRCA - pure red cell aplasia) на фоне лечения нефрогенной анемии стимуляторами эритропоэза. В мире зарегистрировано всего около 200 таких случаев при длительном (в среднем, более 6 мес) применении рекомбинантных эритропоэтинов. Быстрое и глубокое снижение числа эритроцитов обусловлено выработкой аутоантител к эндогенному ЭПО. Анализ случаев показал, что осложнение характерно для всех представителей данного класса препаратов при их длительном использовании. Хотя при клинических исследованиях в онкологии не было отмечено ни одного подобного случая, эта проблема может иметь особое значение при использовании препаратов-биоаналогов эпоэтина.
На международном конгрессе нефрологов в апреле 2007 г. были представлены результаты сравнительного исследования препаратов-биоаналогов эпоэтина-альфа, используемых за пределами стран Евросоюза и США. Проведён всесторонний анализ 47 образцов биоаналогов эпоэтина по следующим параметрам: физические характеристики (идентичность эритропоэтину, содержание, наличие изоформ и агрегатов), активность in vitro и in vivo (мыши), наличие бактериального эндотоксина. Исследования проводили в лабораториях Европы и США согласно требованиям качества Европейской Фармакопеи для эпоэтина-a. В качестве эталона использовали эпоэтин-альфа (эпрексª). Из 47 изученных образцов 41 имел значимые отклонения от стандарта. Изменение числа изоформ, различия в биоактивности, наличие агрегатов и бактериальных токсинов в коммерчески доступных образцах препаратов эпоэтина ставят под сомнение безопасность их применения как по причине недостаточной эффективности, так и из-за возможных побочных эффектов: тромбогенности и иммуногенности. Аналогично другим препаратам, сходным по механизму действия с оригинальным препаратом, Европейская Фармакопея предъявляет к биоаналогам, в том числе и к биоаналогам эпоэтина, особые требования: необходимость дополнительного лабораторного тестирования, сравнительных клинических исследований активности/иммуногенности, применения системы фармакологического контроля в ходе использования биоаналогов. После регистрации биоаналогов на фармацевтическом рынке такие меры абсолютно необходимы для обеспечения мониторинга иммуногенности, безопасности и эффективности препаратов.
Заключение
Проблема анемии в онкологии по-прежнему остаётся в тени забот о непосредственных эффектах химиотерапии. Широко распространено мнение о неизбежности лёгкой или умеренной анемии при онкологическом заболевании. Онкологи, радиологи, хирурги и терапевты считают, что снижение уровня гемоглобина до 100 г/л и даже до 80 г/л не приносит значимого вреда. Исследования связи качества жизни пациентов с анемией показали, насколько ошибочна подобная точка зрения. Своевременная и адекватная коррекция анемии существенно улучшает благополучие пациентов.
Значимость проблемы улучшения качества жизни онкологических больных при своевременном и эффективном лечении пост-цитостатической анемии подтверждена формированием целого класса препаратов, стимулирующих эритропоэз. Помимо известных аналогов эндогенного эритропоэтина (рекомбинантные человеческие эпоэтины альфа и бета, дарбепоэтин) изучают биодженерики, пролонгированные формы (CERA) и синтетические аналоги ЭПО, ЭПО-миметики (низкомолекулярные вещества, стимулирующие ЭПО-рецепторы), стабилизаторы HIF-1a и т.д.
Результаты проспективных и ретроспективных исследований, проведённых за последнее десятилетие, убедительно свидетельствуют, что анемия и её влияние на больного недооценены клинической онкологией. Внедрение в клиническую практику ряда новых цитостатиков, активное использование агрессивных режимов лечения, включая одновременную химио- и лучевую терапию (например, при локализованном мелкоклеточном раке лёгкого), длительное использование иммуномодуляторов позволяет улучшить непосредственные и отдалённые результаты лечения злокачественного заболевания. Однако интенсификация лечения часто ухудшает качество жизни пациентов и требует активной поддерживающей терапии.
Своевременная и эффективная коррекция пост-цитостатической анемии при использовании эпоэтина-a, эпоэтина-b, дарбепоэтина-a быстро улучшает качество жизни и функциональный статус больного, снижает потребность в гемотрансфузиях и потому считается неотъемлемой частью противоопухолевого лечения.
Тошнота и рвота
Тошнота - неприятное субъективное ощущение приближающейся рвоты.
Рвота - активный выброс содержимого желудка через пищевод и рот за счёт сильного сокращения мускулатуры диафрагмы и брюшной стенки.
До настоящего времени большинство больных относят тошноту и рвоту к наиболее тягостным последствиям противоопухолевого лечения. Эти осложнения возникают практически у 80% больных, получающих современные схемы химиотерапии, при этом не менее трети из них страдают от преждевременной тошноты и рвоты, которые возникают до введения цитостатиков.
Частота и степень тяжести этих осложнений зависит от механизма действия и дозы цитостатика, схемы химиотерапии, а также от индивидуальных особенностей больного (пол, возраст, психологический настрой, злоупотребление алкоголем и др.) Наиболее тяжело тошноту и рвоту переносят женщины и больные моложе 30 лет, что обусловлено как применением более эметогенных лекарственных комбинаций, включающих цисплатин, дакарбазин, производные нитрозомочевины, так и эмоциональной лабильностью, склонностью к вегето-сосудистой дистонии, редким употреблением крепких спиртных напитков у данной группы больных.
Кроме негативного влияния на психологический статус больных тошнота и рвота обусловливают развитие нарушений электролитного баланса, обезвоживания, анорексии, снижения веса и аспирационной пневмонии. Вышеуказанные патологические состояния не только значительно ухудшают качество жизни больных, но и могут стать причиной для переноса очередных циклов химиотерапии, снижения доз цитостатиков или отказа от продолжения противоопухолевого лечения.
Виды тошноты и рвоты: острая, отсроченная, преждевременная, рефрактерная.
-
Острая тошнота и рвота возникают в течение первых суток после начала химиотерапии. Наиболее характерно её возникновение в пределах 1-2 ч после введения цитостатиков. Исключение составляют циклофосфамид и карбоплатин; тошнота и/или рвота при их использовании возникает обычно через 10-18 ч.
-
Отсроченная тошнота и рвота возникают в течение последующих 2-6 сут от начала химиотерапии. Наиболее часто они возникают при назначении производных платины, комбинаций антрациклиновых антибиотиков и циклофосфамида.
-
Преждевременная (или психогенная) тошнота и рвота возникают в пределах нескольких часов до введения цитостатиков, как правило, у больных, подвергавшихся ранее высокоэметогенной химиотерапии и страдавших от её осложнений.
Факторы риска преждевременной тошноты и рвоты:
Часто тошноту и рвоту могут провоцировать запахи, вкусовые ощущения, вид предметов и обстановки, напоминающих о лечении.
Стандартная антиэметическая терапия, как правило, неэффективна для купирования преждевременной тошноты и рвоты. Особое значение необходимо уделять её профилактике. Помимо этого рекомендуют назначать транквилизаторы, проводят психотренинг, гипноз для коррекции психического состояния больного.
Критерии оценки эффективности противорвотной терапии: полный и частичный контроль, отсутствие эффекта.
-
Полный контроль - отсутствие рвоты в течение 24 ч после введения антиэметиков, наличие только слабой тошноты;
-
Частичный контроль - один эпизод рвоты в течение 24 ч, наличие умеренной или сильной тошноты;
-
Отсутствие эффекта - два и более эпизода рвоты в течение 24 ч, наличие сильной тошноты, что требует дополнительного назначения противорвотных средств.
Патогенез тошноты и рвоты
Ключевая роль в механизме возникновения тошноты и рвоты принадлежит центру рвоты, который расположен в области дна четвёртого желудочка. Он координирует сложный рвотный рефлекс, проявляющийся гиперсаливацией, сокращением гладкой мускулатуры глотки, пищевода и желудка, мышц брюшного пресса, учащением сердцебиения и дыхания.
Стимуляторы рвотного центра - хеморецепторы триггерной зоны, которая расположена в промежуточном мозге, блуждающий нерв, передающий возбуждение из верхних отделов желудочно-кишечного тракта, а также психогенные стимулы из коры головного мозга.
Пути активации хеморецепторной триггерной зоны: периферический и центральный.
-
Периферический механизм. Метаболиты цитостатиков, попадающие с желчью в просвет желудочно-кишечного тракта, вызывают высвобождение серотонина из энтерохромаффинных клеток слизистой оболочки, который возбуждает 5-НТ3-рецепторы окончаний блуждающего нерва. Нервные импульсы поступают в хеморецепторную зону и далее в центр рвоты.
-
Центральный механизм. Происходит активация серотонином 5-НТ3-рецепторов, непосредственно расположенных в триггерной зоне ствола головного мозга. В результате происходит высвобождение различных нейротрансмиттеров, стимулирующих рвотный центр.
Нейротрансмиттеры, участвующие в патогенезе тошноты и рвоты. К ним относят серотонин, допамин, гистамин, субстанцию Р, вазопрессин, ацетилхолин, простагландины, энкефалин. Индуцировать развитие рвоты могут как один, так и нескольких медиаторов. Значение каждого из них окончательно не определено, поэтому адекватная антиэметическая терапия должна предполагать одновременное назначение нескольких препаратов, блокирующих активность большинства нейротрансмиттеров.
Антиэметические препараты: блокаторы рецепторов допамина, глюкокортикоиды, антагонисты рецепторов серотонина, антагонисты нейрокининовых рецепторов.
-
Блокаторы рецепторов допамина. До недавнего времени основным медиатором постцитостатической рвоты считали допамин. Метоклопрамид (церукал©) - антиэметический препарат, блокирующий рецепторы допамина. Он достаточно эффективно купирует как острую, так и отсроченную тошноту и рвоту, особенно в комбинации с глюкокортикоидами. Метоклопрамид в высоких дозах обладает значительно большей эффективностью за счёт способности неселективно инактивировать рецепторы серотонина. Однако, применение высоких доз препарата ограничено из-за возможности развития экстрапирамидных нарушений, особенно у больных молодого возраста.
-
Глюкокортикоиды. К широко применяемым до настоящего времени антиэметическим препаратам относят кортикостероиды, в первую очередь - дексаметазон, точный механизм действия которого не установлен. По некоторым данным, он обладает способностью снижать концентрацию вазопрессина и простагландинов в плазме. Их считают медиаторами тошноты и рвоты. Помимо этого, препарат потенцирует эффект антагонистов рецепторов серотонина и допамина, увеличивая частоту полного контроля над тошнотой и рвотой с 50% до 80-85%.
Результаты нескольких рандомизированных клинических исследований показали, что максимальный антиэметический эффект антагонистов 5-НТ3-рецепторов достигают при однократном введении 20 мг дексаметазона непосредственно перед назначением цитостатиков. В соответствии с современными стандартами, считают обязательным включение глюкокортикоидов (дексаметазона) в комбинированные схемы антиэметической терапии.
-
Антагонисты рецепторов серотонина. Важнейшее достижение противорвотной терапии последних 10-15 лет - применение антагонистов рецепторов серотонина (ондансетрон, трописетрон, гранисетрон), которые эффективно купируют острую тошноту и рвоту в 75-80% случаев. В отличие от метоклопрамида препараты этой группы малотоксичны. Они могут возникать головную боль, запор, возможно транзиторное повышение уровня трансаминаз, отсутствуют экстрапирамидные нарушения.
Все известные антагонисты 5-НТ3-рецепторов в эквивалентных дозах обладают одинаковой эффективностью. Предпочтительно использовать пероральные формы из-за большего удобства применения. Антагонисты рецепторов серотонина рекомендуют использовать однократно перорально за 30 мин до введения цитостатиков.
-
Антагонисты нейрокининовых рецепторов. В последние годы получены новые данные относительно роли субстанции Р в развитии тошноты и рвоты. Субстанция Р - регуляторный пептид из группы тахикининов, реализующий свой эметогенный потенциал посредством активации нейрокининовых рецепторов. В отличие от серотонина он играет ключевую роль в патогенезе не только острой, но и отсроченной тошноты и рвоты.
Антагонисты нейрокининовых рецепторов способны эффективно предупреждать развитие постцитостатической рвоты в течение первых 3-6 сут от начала химиотерапии. Наиболее изученный препарат этой группы - апрепитант, обладающий способностью блокировать до 100% рецепторов субстанции Р. В комбинации с антагонистами рецепторов серотонина и дексаметазоном апрепитант обеспечивает достижение полного контроля над острой и отсроченной тошнотой и рвотой практически у 90% больных. Однако, монотерапию препаратом не рассматривают в качестве альтернативы комбинации антиэметиков различных групп. Апрепитант - первый антиэметический препарат, обладающий одинаковой эффективностью как у мужчин, так и у женщин. Рекомендуют однократно перорально принимать 125 мг препарата в первый день цикла химиотерапии и по 80 мг в последующие 2 дня за 30 мин до введения цитостатиков.
Современные принципы адекватной противорвотной терапии
-
Антиэметическая терапия должна обеспечивать профилактику и достижение полного контроля над тошнотой и рвотой наряду с максимальным удобством в применении как для больных, так и для медицинского персонала.
-
Выбор антиэметика необходимо основывать на эметогенном потенциале цитостатика, который зависит от его химического состава, метаболизма и дозы препарата, с учётом особенностей больного, его возраста, пола, психоэмоциональных черт.
-
С учётом эквивалентной эффективности и безопасности парентеральных и пероральных лекарственных форм предпочтение следует отдавать последним. Рекомендуют однократно назначать наименее эффективную дозу препарата за 30-60 мин до начала химиотерапии.
Выделяют пять основных групп цитостатиков в зависимости от их эметогенной активности.
Группы цитостатиков в зависимости от эметогенной активности
-
Высокоэметогенные цитостатики. К ним относят цисплатин (в дозе, превышающей 75 мг/м2), дакарбазин, мелфалан, производные нитрозомочевины, циклофосфамид в высоких дозах.
-
Цитостатики с умеренной эметогенностью: цисплатин (в дозе 60-75 мг/м2), цитарабин, циклофосфамида и доксорубицина в стандартных дозах, этопозид.
-
Цитостатики со слабой эметогенностью: метотрексат, доксорубицин в малых дозах, фторурацил, блеомицин, винкристин.
Особенности назначения антиэметогенных препаратов
-
Назначение высокоэметогенной химиотерапии. В соответствии с современными алгоритмами противорвотной терапии, при проведении высокоэметогенной химиотерапии рекомендуют за 30 мин до введения цитостатиков перорально назначать апрепитант в дозе 125 мг, дексаметазон в дозе 12 мг, один из антагонистов 5-НТ3-рецепторов (ондансетрон, гранисетрон) в дозе 24-32 мг и лоразепам. При невозможности перорального приёма все препараты, кроме апрепитанта, можно вводить внутривенно. В случае многодневных введения цитостатиков указанную схему повторяют ежедневно.
Для профилактики отсроченной рвоты на 2-3 сут продолжают приём апрепитанта в дозе 80 мг, дексаметазона в дозе 8 мг, ондансетрона или гранисетрона.
На 2-4 сут для профилактики отсроченной рвоты продолжают приём дексаметазона в сочетании с антагонистами рецепторов серотонина или метоклопрамидом, или, при необходимости, с апрепитантом в дозе 80 мг.
Адекватная противорвотная терапия позволяет эффективно купировать острую и отсроченную тошноту и рвоту у 80-90% больных, получающих противоопухолевое лечение. Это обеспечивает хорошее качество жизни больных и значительно облегчает работу медицинского персонала.
Поражение печени
Метаболизм большинства цитостатиков происходит в печени. При проведении современных схем комбинированной химиотерапии гепатотоксичность возникает в 15-20% случаев. Как правило, она имеет дозозависимый, ожидаемый и обратимый характер, лёгкую или умеренную степень выраженности.
Выделяют группу цитостатиков, обладающих повышенной повреждающей способностью в отношении печени и желчевыводящих путей. В первую очередь, к ним относят бусульфан (при длительном применении), производные нитрозомочевины (кармустин), доксорубицин, паклитаксел, этопозид. Развитие тяжёлой печёночной недостаточности при назначении стандартных доз противоопухолевых препаратов отмечают редко, что обычно обусловлено индивидуальными особенностями обмена веществ у больного (идиосинкразия).
Особенности гепатотоксичности противоопухолевых препаратов
Выделяют наиболее характерные поражения печени и желчевыводящих путей, свойственные цитостатикам различных групп.
-
Алкилирующие препараты (циклофосфамид, мелфалан, хлорамбуцил, бусульфан). Развитие гепатотоксичности не относят к типичным осложнениям терапии. Непереносимость циклофосфамида в виде развития цитолитического синдрома с повышением уровня трансаминаз, как правило, имеет характер идиосинкразии. В тяжёлых случаях может возникать тотальный некроз печени. Для мелфалана в средних дозах гепатотоксичность не характерна, однако при назначении высоких доз может происходить транзиторное повышение уровня трансаминаз и щелочной фосфатазы. Развитие холестатического гепатита может осложнять длительное использование бусульфана.
-
Винкаалкалоиды и производные платины. Гипербилирубинемия и повышение уровня ферментов печени возникают редко.
-
Антиметаболиты (фторурацил, капецитабин, меркаптопурин, метотрексат). Токсические реакции со стороны печени возникают редко, что позволяет использовать препараты практически в полных дозах даже при выявлении умеренных нарушений её функции. Метотрексат, как правило, обладает токсичностью при назначении его в высоких дозах, которая носит обратимый (в течение 1-2 мес) характер.
-
Производные нитрозомочевины (кармустин, ломустин) и таксаны (паклитаксел) обладают ожидаемой и достаточно высокой (25-60%) гепатотоксичностью, проявляющейся повышением уровня трансаминаз, щелочной фосфатазы и билирубина.
-
Антрациклиновые антибиотики (доксорубицин, эпирубицин, даунорубицин) обладают гепатотоксическими свойствами. Они активно подвергаются метаболизму в печени. Экскреция метаболитов с желчью происходит в течение 7-10 дней. Как правило, происходит повышение уровня трансаминаз, щелочной фосфатазы и билирубина.
Определение клинических и/или лабораторных признаков поражения печени у больных, получающих противоопухолевое лечение, требует проведения углублённой дифференциальной диагностики с целью уточнения причин возникновения данного патологического состояния.
Основные причины нарушения функции печени (помимо проводимого цитостатического лечения):
-
сопутствующие острые или хронические заболевания печени и желчевыводящих путей (холецистит, инфекционный или токсический гепатит);
-
предшествующие химиотерапия, осложнённые гемотрансфузии или применение ряда других гепатотоксичных лекарственных средств;
-
поражение органа опухолевым (метастазы, тромбоз портальной вены) или паранеопластическим (например, амилоидоз, холестаз) процессом.
Основные типы гепатотоксических реакций, осложняющих цитостатическое лечение:
Веноокклюзионная болезнь - патологическое состояние, обусловленное цитостатическим повреждением эндотелия и соединительной ткани мелких внутрипечёночных вен, которое приводит к их нетромботической облитерации. Наиболее часто (до 20% случаев) она осложняет проведение высокодозной комбинированной химиотерапии с трансплантацией аллогенного костного мозга или стволовых клеток (как проявление реакции гиперчувствительности замедленного типа "трансплантат против хозяина"). Значительно реже веноокклюзионная болезнь развивается при назначении дакарбазина (например, в схеме ABVD, применяемой для лечения болезни Ходжкина), высоких доз циклофосфамида, бусульфана, кармустина, митомицина, гемцитабина. Риск её возникновения возрастает при проведении сопутствующей терапии ацикловиром, ванкомицином, предшествующем облучении брюшной полости, метастатическом поражении печени.
Клиническая картина. Выделяют острую фазу, а также фазу атрофии и фиброза.
-
Острая фаза. Возникают боли в правом подреберье, гепатомегалия, асцит, персистирующая тромбоцитопения, центрилобулярные кровотечения и кровоизлияния.
-
Фаза атрофии и фиброза. Формируется атрофия и прогрессирующий фиброз паренхимы печени. Диагноз подтверждают результатами морфологического исследования биоптата печени.
При неблагоприятном течении в исходе веноокклюзионной болезни может возникать фатальный гепатоцеллюлярный некроз. Летальность достигает 30-50%.
Специфическое лечение отсутствует. С целью профилактики рекомендуют назначать малые дозы гепарина, простагландина ЕÃ, пентоксифиллина.
Оценку функциональной способности печени осуществляют на основании результатов ряда лабораторных тестов (определение уровня общего и конъюгированного билирубина, альбумина, мочевины, фибриногена, сывороточного железа, церуллоплазмина, глюкозы, протромбинового времени и др.).
В зависимости от концентрации в плазме крови печёночных ферментов, билирубина и альбумина выделяют четыре степени тяжести поражения печени (в соответствии с критериями Национального Института Рака США) (NCIC CTC).
Степени тяжести поражения печени (NCIC CTC)
-
Лёгкая степень - повышение уровня трансаминаз, щелочной фосфатазы, лактат дегидрогеназы менее, чем в 2,5 раза от верхней границы нормы (ВГН), билирубина менее, чем в 1,5 раз от ВГН, снижение уровня альбумина до 30 г/л.
-
Умеренная степень - повышение уровня трансаминаз, щелочной фосфатазы, лактат дегидрогеназы в 2,5-5,0 раз от ВГН, билирубина в 1,5-3,0 раза от ВГН, снижение уровня альбумина до 20 г/л.
-
Тяжёлая степень - повышение уровня трансаминаз, щелочной фосфатазы, лактат дегидрогеназы в 5,0-20,0 раз от ВГН, билирубина в 3,0-10,0 раз от ВГН, снижение уровня альбумина менее 20 г/л.
-
Крайне тяжёлая степень - повышение уровня трансаминаз, щелочной фосфатазы, лактат дегидрогеназы более, чем в 20,0 раз от ВГН, билирубина более, чем в 10,0 раз от ВГН.
Проведение оценки исходного функционального состояния печени до начала химиотерапии - обязательное условие безопасности противоопухолевого лечения. Дальнейшее наблюдение за лабораторными показателями обеспечивает своевременное выявление гепатотоксичности, что рассматривают показанием для изменения доз цитостатиков или режима химиотерапии.
Принципы изменения дозы цитостатиков в зависимости от степени их гепатотоксичности
В 1991 г. Beretta и соавторы разработали рекомендации, касающиеся изменения дозы цитостатиков в зависимости от степени гепатотоксичности. Учитывая пополнение арсенала современных цитостатиков новыми препаратами, данные рекомендации периодически обновляют, однако стандартные принципы остаются неизменными.
-
Лёгкая степень гепатотоксичности не требует изменения доз препарата.
-
Умеренная степень гепатотоксичности - показание для снижения дозы большинства препаратов (доксорубицин, митоксантрон, винбластин, винкристин, этопозид, паклитаксел) на 50%, реже (доцетаксел, даунорубицин) - на 25%. В то же время, циклофосфамид, метотрексат, фторурацил, капецитабин назначают в полной дозе.
-
Тяжёлая степень гепатотоксичности. Необходимо снизить дозы большинства противоопухолевых препаратов на 50-75%, прекратить лечение винкаалкалоидами, этопозидом. Фторурацил возможно применять в полной дозе.
-
Крайне тяжёлая степень. Дальнейшее нарастание лабораторных признаков цитолитического и/или холестатического синдромов - показание к отмене любых противоопухолевых лекарственных средств.
Лечение
Лечебные мероприятия, которые проводят для коррекции токсического повреждения печени, соответствуют стандартам лекарственной терапии гепатитов. Больному назначают диетическое питание, проводят инфузионную терапию, включающую витамины, спазмолитики, гепатопротекторы (эссенциале H©, адеметионин), глюкокортикоиды (преднизолон).
Поражение желудочно-кишечного тракта
Стандартная противоопухолевая терапия часто приводит к развитию осложнений со стороны органов ЖКТ: повреждение и инфицирование слизистых оболочек (мукозит, эзофагит, гастрит, энтероколит), диарея, запор, кровотечения, изъязвление слизистой оболочки. Мишенью для цитостатиков эпителиальные клетки слизистых оболочек ЖКТ становятся благодаря их высокой пролиферативной активности.
Мукозиты (стоматит, эзофагит)
Наиболее часто постцитостатические поражения пищеварительного тракта возникают в ротовой полости, несколько реже - в пищеводе. Общая частота развития мукозитов при проведении различных схем химиотерапии достигает 30%. До настоящего времени их относят к тем осложнениям противоопухолевого лечения, профилактика которых малоэффективна.
Мукозит - сложный симптомокомплекс, включающий болевые ощущения в ротовой полости и за грудиной (при развитии эзофагита); трудности при приёме пищи и лекарственных препаратов; изменение вкуса, нарушение слюноотделения; появление эрозий, изъязвлений и кровоточивости слизистых оболочек; одинофагию, дисфагию; изжогу и рвоту (при развитии тяжелого эзофагита), анорексию.
При тяжёлом мукозите может присоединяться вторичная инфекция, происходить нарушение энтерального питания, возникать потеря веса, обезвоживание. Вследствие этого помимо значительного ухудшения качества жизни больного возникает необходимость увеличения интервалов между циклами и снижения доз цитостатиков, что негативно влияет на результат проводимого противоопухолевого лечения.
Основные причины развития мукозитов:
Предрасполагающие факторы развития мукозитов:
Факторы, определяющие степень тяжести постцитостатического мукозита: механизм действия цитостатика, длительность цитостатического воздействия, доза цитостатика, особенности больного.
-
Механизм действия цитостатика. Наибольшим повреждающим действием обладают:
-
Длительность цитостатического воздействия. Например, при инфузии высоких доз метотрексата в течение 4-6 ч (при лечении остеогенной саркомы) стоматит возникает редко, в то время как пролонгированное (в течение 24-36 ч) введение средних доз препарата весьма часто приводит к развитию тяжёлого мукозита. Аналогичная картина характерна при использовании доксорубицина: инфузия препарата на протяжении 72-96 ч вызывает развитие выраженного стоматита у 60-90% больных в отличие от его болюсного введения.
-
Доза цитостатика. Проведение высокодозной ПХТ, включающей мелфалан, этопозид или циклофосфамид, приводит к развитию выраженного мукозита у большинства больных.
-
Особенности больного. Существенное значение имеют возраст больного, исходное состояние иммунитета и др. факторы.
Первые проявления стоматита, как правило, отмечают на 7-10 сут от начала химиотерапии, его продолжительность составляет 2-3 нед и зависит от правильности проводимых лечебных мероприятий, наличия нейтропении, присоединения вторичной бактериальной, грибковой или вирусной инфекции. Постцитостатическая нейтропения степени III-IV значительно повышает риск проникновения бактерий и грибов через повреждённую слизистую оболочку ЖКТ в кровяное русло, что приводит к генерализации инфекционного процесса и усугубляет тяжесть состояния больного.
В соответствии с общепринятыми критериями токсичности Национального Института Рака США (CTC NCIC) выделяют четыре степени тяжести мукозитов.
Степени тяжести мукозитов (CTC NCIC)
-
Лёгкая степень - гиперемия слизистых оболочек, наличие отёка, безболезненных эрозий, изъязвлений (в том числе в пищеводе при эзофагогастроскопии).
-
Умеренная степень - выраженная гиперемия и отёк слизистых оболочек, наличие болезненных изъязвлений, требующих лечения; приём пищи не затруднён.
-
Тяжёлая степень - выраженная гиперемия и отёк слизистых оболочек, вторичная инфекция, наличие болезненных изъязвлений, продолжающихся более 14 сут несмотря на лечение; приём пищи затруднён.
-
Крайне тяжёлая степень - некротические изменения слизистых оболочек, приём пищи невозможен, обезвоживание, потеря массы тела, необходимость дополнительного энтерального или парентерального питания и госпитализации больного.
Профилактика и лечение мукозитов у больных, которым проводят системную химиотерапию, требуют повышенного внимания.
Полноценная санация полости рта подразумевает лечение или экстракцию кариозных зубов, ликвидацию полостей периодонтита, лечение гингивита, удаление дефектных зубных протезов. Гигиенические мероприятия включают чистку зубов мягкой щёткой, частую смену зубной щетки при развитии воспаления, полоскание ротовой полости специальными зубными эликсирами, слабым раствором натрия гидрокарбоната, растворами нитрофурала (фурацилина©) (1:5000), хлоргексидина.
-
Лечение мукозитов включает соблюдение диеты, обезболивание, местное лечение, лечение инфекционных осложнений.
-
Соблюдение диеты - употребление механически и термически обработанных продуктов, не острой, не горячей пищи.
-
Местное лечение направлено на удаление из ротовой полости зубного налёта и поддержание влажности слизистой оболочки ротовой полости. Назначают полоскание ротовой полости 0,1% раствором этакридина, нитрофурала (фурацилина©) (1:5000), 0,1% раствором пероксида водорода, экстрактом цветка ромашки, коры дуба, хлоргексидином, смазывание слизистой оболочки ротовой полости метиленовым синим, маслом облепихи, Метрогил Дента©, суспензией сукральфата. В случае развития эзофагита применяют антацидные препараты, обволакивающие средства, сукральфат, блокаторы продукции соляной кислоты, спазмолитики.
-
Лечение инфекционных осложнений осуществляют с учётом возбудителя.
-
Антибактериальная терапия должна включать препараты широкого спектра действия. Препарат обычно выбирают эмпирически, реже - по результатам микробиологических анализов.
При выявлении кандидоза назначают полоскание ротовой полости 2-3% раствором натрия гидрокарбоната, раствором перманганата калия (1:5000). Рекомендуют использовать таблетки нистатина для рассасывания (не менее 8 млн ЕД в сутки за 4-5 приёмов), в тяжёлых случаях препарат выбора - флуконазол (200-400 мг в сутки).
В случае вирусной инфекции применяют ацикловир (местно в виде крема, перорально или внутривенно в течение 7-10 дней).
Ксеростомия
Ксеростомия, или сухость слизистой оболочки ротовой полости, как правило, осложняет лучевую терапию на область головы и шеи, реже возникает при проведении системной химиотерапии (на фоне нейтропенического мукозита, обезвоживания, приёма диуретиков, опиоидных анальгетиков, антигистаминных средств и др.). Сухость во рту приводит к нарушению приёма пищи, изменению вкусовых ощущений, затруднению речи, ухудшению качества жизни больного.
Лечение ксеростомии включает мероприятия, направленные на коррекцию вызывающих её факторов и поддержание оптимальной гигиены ротовой полости. Рекомендуют использовать заменители слюны (перед приёмом пищи и на ночь), пилокарпин (5-10 мг 3 раза в сутки, перед едой).
Диарея
Диарея - учащение дефекации, при котором каловые массы имеют жидкую консистенцию. В норме частота стула не превышает двух раз в сутки. При развитии токсической диареи она возрастает до 3-10 и более раз в сутки. Учащение стула возникает из-за избыточного содержания воды в просвете кишечника, которое обусловлено или усилением её секреции (секреторная диарея), или снижением реабсорбции, или повышением концентрации растворённых веществ (осмотическая диарея).
Диарею относят к наиболее частым осложнениям системного противоопухолевого лечения (до 30% от общего числа побочных эффектов). Она часто выходит на первый план среди осложнений химиотерапии, при этом не только существенно ухудшает качество жизни больных, но и может приводить к развитию угрожающих жизни состояний (дегидратации, электролитным нарушениям, псевдомембранозному колиту и др.).
Основные клинические проявления диареи:
В соответствии с критериями токсичности NCIC выделяют четыре степени тяжести диареи.
Степени тяжести диареи (NCIC)
-
Лёгкая степень - 2-3 эпизода жидкого стула в сутки, небольшое увеличение объёма отделяемого из колостомы.
-
Умеренная степень - 4-6 эпизодов жидкого стула в сутки или диарея в ночные часы, умеренное увеличение объёма отделяемого из колостомы.
-
Тяжёлая степень - 7-9 эпизодов жидкого стула в сутки, недержание стула, развитие синдрома мальабсорбции, значительное увеличение объёма водянистого отделяемого из колостомы.
-
Крайне тяжёлая степень - более 10 эпизодов жидкого стула в сутки, обильная диарея с примесью крови, обезвоживание, необходимость парентерального питания и восстановления водного баланса.
В патогенезе постцитостатической диареи, в первую очередь, следует отметить непосредственное повреждающее воздействие цитостатиков или их метаболитов на интенсивно пролиферирующий эпителий пищеварительного тракта. В результате слущивания эндотелиальных клеток в просвет кишечника запускается механизм развития осмотической диареи, реализующийся, как правило, в течение 3-48 ч. Наибольшей токсичностью в отношении слизистой оболочки ЖКТ обладают цитостатики из группы антиметаболитов (фторурацил, капецитабин, метотрексат, цитарабин), а также иринотекан, дактиномицин, паклитаксел, производные нитрозомочевины. Диарея нередко развивается при назначении иммуномодуляторов (интерлейкин-2, интерферон альфа).
Диарея - дозолимитирующее осложнение при использовании иринотекана. При его назначении характерно развитие ранней и поздней (или отсроченной) диареи. Ранняя диарея, которая возникает в течение первых 24-48 ч после окончания инфузии иринотекана, входит в симптомокомплекс острого холинергического синдрома, купируемого подкожным введением 0,1% раствора атропина. Поздняя диарея, обусловленная особенностями метаболизма иринотекана, возникает на 5-7 сут от начала лечения. Это более серьёзное осложнение. В процессе метаболизма препарата в печени образуется активный агент SN-38, который в дальнейшем превращается в SN-38-глюкуронид. Этот метаболит с желчью поступает в просвет тонкой кишки, где под влиянием бактериальной b-глюкуронидазы вновь происходит образование SN-38, повреждающего кишечный эндотелий. Отсутствие адекватного лечения поздней диареи приводит к развитию обезвоживания и электролитных нарушений не менее, чем у трети больных.
Лечение
Назначают лоперамид, октреотид, адсорбирующие лекарственные средства, по показаниям - другие препараты.
-
Лоперамид. Для купирования осложнения назначают лоперамид, угнетающий перистальтику кишечника, по стандартной схеме: 4 мг (2 капсулы) per os сразу после начала диареи, затем по 2 мг (1 капсула) каждые 2 ч до прекращения диареи и ещё в течение 12 ч после последнего эпизода жидкого стула, но не более 16 капсул в сутки.
-
Октреотид назначают при недостаточной эффективности лоперамида в дозе 0,05-0,1 мг 3 раза в сутки подкожно в течение 3-5 дней. В случае тяжёлой, рефрактерной диареи возможно увеличение дозы препарата до 1,8 мг в сутки.
-
-
абсорбирующие лекарственные средства (препараты каолина, метилцеллюлозы);
-
ингибиторы простагландинов (ацетилсалициловая кислота, НПВС);
-
оральная регидратация (регидрон© [до 1500 мл в сутки per os], питьевая смесь, состоящая из 1000 мл питьевой воды, одной чайной ложки натрия хлорида, одной чайной ложки гидрокарбоната натрия и одного стакана фруктового сока);
-
калообразующие сложные порошки на основе кальция карбоната; настои и отвары вяжущих средств растительного происхождения;
-
инфузионная терапия показана при продолжительности диареи более 48 ч для предотвращения электролитных нарушений, гиповолемии и гиповолемического шока;
-
купирование болевого синдрома осуществляют спазмолитиками, обезболивающими средствами, вплоть до назначения наркотических анальгетиков;
-
При сочетании диареи и постцитостатической нейтропении значительно возрастает риск присоединения бактериальной или грибковой инфекции. Всем больным с подозрением на возникновение вторичного инфекционного процесса необходимо выполнять микробиологическое исследование каловых масс. Наиболее опасно развитие псевдомембранозного энтероколита, обусловленного Clostridium difficile. Лечение проводят с использованием антибиотиков (назначают ванкомицин по 125 мг каждые 6 ч или метронидазол по 400 мг каждые 8 ч).
Запоры
Запор - нерегулярный стул или затруднение при акте дефекации с отхождением уменьшенного количества стула.
Причины запора у больных, получающих цитостатическое лечение:
Наиболее часто (до 30-40% случаев) запоры возникают у больных, подвергшихся химиотерапии винкаалкалоидами, цисплатином или этопозидом.
К клиническим проявлениям запора относят уменьшение частоты опорожнения кишечника и объёма каловых масс вплоть до полного отсутствия стула с возникновением симптомов интоксикации. При выраженных запорах могут возникать анорексия, тошнота, рвота.
Профилактика и лечение. Рекомендуют употреблять достаточное количество жидкости и пищи, обладающих слабительным действием (кисломолочные продукты, свёкла, чернослив и др.), продуктов с большим содержанием растительной клетчатки, своевременно назначать слабительные препараты и свечи.
Группы слабительных препаратов отличаются механизмом действия:
При рефрактерных запорах возможно назначение неостигмина метилсульфата (например, прозерин [по 1 мл 0,05% раствора 4-6 раз в сутки подкожно]), очистительных клизм.
Редкие осложнения
В редких случаях назначение цитостатических препаратов (например, ифосфамида, цитарабина, цисплатина) может осложняться развитием острого панкреатита с типичной клинической картиной.
Кроме того, постцитостатические тромбоцитопении и коагулопатии значительно повышают риск возникновения кровотечений из различных отделов пищеварительного тракта. К предрасполагающим факторам их возникновения относят сопутствующие заболевания (язвенная болезнь желудка или двенадцатиперстной кишки, эрозивные поражение различных отделов желудочно-кишечного тракта, дивертикулы, сосудистые мальформации), а также инфекции ЖКТ (например, псевдомембранозный колит).
Поражение мочевыделительной системы
Поражение мочевыделительной системы при проведении цитостатического лечения имеет многофакторный характер. Степень выраженности токсических реакций зависит от механизма действия, дозы и особенностей метаболизма цитостатика, наличия сопутствующей патологии со стороны органов мочевыделительной системы, возраста больного, исходного клиренса креатинина, величины диуреза.
Основной показатель функционального состояния почек - клиренс креатинина, величина которого снижается у больных с сопутствующей почечной недостаточностью. Замедленная экскреция цитостатиков и/или их метаболитов приводит к увеличению общей цитотоксичности и нефротоксичности.
С целью предупреждения нефротоксичности у больных с повышенным риском развития этого осложнения необходимо осуществлять постоянный динамический контроль общего анализа мочи, уровня креатинина, мочевины в сыворотке крови.
Ожидаемой токсичностью в отношении почек и мочевыводящих путей обладают цисплатин, метотрексат, ифосфамид, кармустин, цитарабин, аспарагиназа, интерлейкин-2. Их назначение может сопровождаться развитием острой или хронической почечной недостаточности, а также специфическими повреждениями (например, возникновение геморрагического цистита при использовании ифосфамида).
Наиболее типичные осложнения со стороны органов мочевыделительной системы, вызываемые нефротоксичными цитостатиками
Формы токсичности цисплатина. К ним относят острое и хроническое поражение почек, электролитные нарушения.
-
Острое поражение почек. Наиболее значительные повреждения возникают в трубочках нефронов с развитием тубулярного некроза. Острая форма нефротоксичности, как правило, характерна для больных, не получивших адекватную гидратацию во время введения цисплатина. В тяжёлых случаях развивается почечная недостаточность (повышение уровня креатинина, олигурия, сменяющаяся полиурией).
-
Хроническое поражение почек. Для него, как правило, характерно снижение скорости клубочковой фильтрации, которое далеко не всегда сочетается со значимым повышением уровня креатинина или снижением его клиренса. Повреждение тубулярного аппарата проявляется повышенной экскрецией ряда ферментов (например, аланинамино пептидазы), белка, магния и снижением реабсорбции воды и натрия в проксимальных отделах трубочек.
-
Электролитные нарушения. Наибольшую клиническую значимость имеет гипомагниемия, к симптомам которой относятся мышечная слабость, тетания, парестезии, головокружения. В тяжелых случаях снижение концентрации магния сопровождается развитием гипокальциемии.
К редким формам нефротоксичности цисплатина относят развитие гемолитического уремического синдрома, вторичной артериальной гипертензии.
Профилактика нефротоксичности цисплатина включает:
-
снижение дозы препарата на 50% при уменьшении величины клиренса креатинина ниже 60 мл/мин и его отмена при уровне данного показателя ниже 30 мл/мин;
-
коррекцию дозы цисплатина при его сочетанном назначении с другими нефротоксичными лекарственными средствами (например, аминогликозидами);
-
соблюдение режима гипергидратации, заключающийся во внутривенном введении до 3000-4000 мл солевых растворов, препаратов магния, калия, диуретиков (маннитол 25-50 г) в течение 8-12 ч.
Производные нитрозомочевины (ломустин, кармустин) могут вызывать развитие хронического тубулоинтерстициального нефрита и тубулярной атрофии (в том числе - спустя месяцы и годы после завершения лечения). В результате развивается хроническая почечная недостаточность, часто требующая проведения гемодиализа.
-
Митомицин. При его назначении в ряде случаев возникает хроническая почечная недостаточность, сочетающаяся с микроангиопатической гемолитической анемией. В симптомокомплекс, развивающийся, как правило, в течение 6 мес после завершения лечения, входят тромбоцитопения, азотемия, протеинурия, гематурия, вторичная артериальная гипертензия.
Ифосфамид и циклофосфамид
Ифосфамид вызывает развитие геморрагического цистита, обусловленного повреждением эпителия мочевыводящих путей его метаболитом акролеином. Аналогичное осложнение возникает примерно у 40% больных, получающих циклофосфамид в режиме высокодозной ПХТ. Клинические проявления цистита - микро- и макрогематурия, учащённое и болезненное мочеиспускание.
С профилактической целью назначают уропротектор месна (например, уромитексан©), доза которого составляет от 60 до 120% от дозы ифосфамида.
Лечение химического цистита неспецифическое. Оно включает соблюдение диеты, расширенный водный режим, инстилляции аминокапроновой кислоты, противовоспалительных вяжущих средств, обезболивающих растворов, спазмолитиков, установление мочевого катетера и промывание мочевого пузыря для предупреждения обструкции уретры сгустками крови).
-
Метотрексат в стандартных дозах, как правило, не обладает нефротоксичностью, несмотря на то, что около 90% его метаболитов выделяются с мочой. Однако, при наличии у больного хронической почечной недостаточности экскреция препарата существенно замедлена, что вызывает развитие выраженной миелосупрессии и мукозитов.
Наибольшую опасность представляет назначение высоких доз метотрексата, при котором происходит подавление активной секреции метаболитов препарата в почечных канальцах. Кроме того, в условиях кислой реакции мочи значительно повышен риск образования преципитатов в тубулярном аппарате почек. Для предупреждения этого осложнения необходимо проводить сопутствующую гипергидратацию и ощелачивание мочи путём введения раствора натрия гидрокарбоната. При снижении клиренса креатинина менее 30 мл/мин, протеинурии введение метотрексата противопоказано.
Синдром распада опухоли
Индуцированная цитостатиками массивная гибель опухолевых клеток приводит к развитию ряда метаболических нарушений, которые обобщённо называют синдромом распада опухоли (СРО). Наиболее часто он возникает у больных, страдающих лимфопролиферативными опухолями и гемобластозами, характеризующихся высокой скоростью роста, большой фракцией активно делящихся клеток и чувствительностью к цитостатической терапии. У больных солидными опухолями СРО выявляют значительно реже, однако в этом случае смертность более высокая вследствие, как правило, поздней диагностики заболевания и отсроченного начала лечения.
Факторы риска развития синдрома распада опухоли:
Метаболические нарушения при синдроме распада опухоли
Как правило, симптомы СРО возникают спустя несколько часов или дней после начала цитостатического лечения. Активно пролиферирующие опухолевые клетки имеют высокое содержание нуклеотидов и фосфата. Их гибель приводит к высвобождению калия, фосфора, мочевой кислоты, других метаболитов пурина, которые поступают в межклеточное пространство. Внезапное поступление большого количества продуктов клеточного распада может превысить способность организма к их выделению, что приводит к острому нарушению электролитного и кислотно-щелочного равновесия, снижению почечного клиренса, развитию резистентной гиперкалиемии, гиперурикемии, гиперфосфатемии с вторичной гипокальциемией. При отсутствии адекватной коррекции метаболические нарушения прогрессируют вплоть до развития лактатацидоза и острой почечной недостаточности.
-
Гиперкалиемия - наиболее угрожающий жизни больного симптом, требующий немедленного лечения. Следует помнить, что повышение уровня калия в сыворотке крови более 6,0 ммоль/л может привести к остановке сердечной деятельности в диастолу.
-
Гиперурикемия. Причина повышения уровня мочевой кислоты в сыворотке крови - катаболизм в печени пуриновых нуклеотидов (гуанина и аденозина). В ходе этого процесса пурины последовательно превращаются в инозин, затем - в гипоксантин и ксантин, после чего окисляются до мочевой кислоты. Высокое её содержание в сыворотке крови приводит к неблагоприятным последствиям в виде повышенной экскреции уратов почками. При уровне рН 5,0-5,4 мочевая кислота плохо растворима в моче, образуются её кристаллы в паренхиме почек, дистальных канальцах, собирательных трубочках, лоханках и мочеточниках. Острая обструкция мочевыводящих путей - основной фактор в патогенезе олигоанурии и азотемии.
-
Острая почечная недостаточность. К основным патогенетическим факторам её развития относят уменьшение объёма циркулирующей крови и преципитация метаболитов нуклеиновых кислот, в первую очередь, кристаллов мочевой кислоты и фосфата кальция в почечных трубочках (острый нефрокальциноз).
Проявления СРО варьируют от бессимптомных отклонений от нормы лабораторных показателей до клинических симптомов электролитного дисбаланса.
Наиболее характерные проявления синдрома распада опухоли: поражение сердечно-сосудистой, нервной, мочевыделительной систем и желудочно-кишечного тракта.
-
Поражение сердечно-сосудистой системы: нарушения проводимости и сердечного ритма, вплоть до остановки сердечной деятельности в диастолу (при гиперкалиемии), удлинение интервала QT.
-
Поражение нервной системы: парестезии, тетанические и эпилептиформные судороги, изменение психики, нарушение сознания, вплоть до развития комы.
-
Поражение мочевыделительной системы: острая почечная недостаточность (при гиперурикемии и гиперфосфатемии), метаболический ацидоз (лактатацидоз).
-
Поражение желудочно-кишечного тракта: тошнота, рвота, диарея, спазмы гладкой мускулатуры, кишечная непроходимость.
Профилактика
Несмотря на высокую смертность при выраженном СРО, своевременная профилактика этого осложнения обеспечивает благоприятный исход. Планируя проведение цитостатической терапии больному с высоким риском развития СРО, необходимо помнить, что предупредить возникновение это осложнения легче, чем осуществлять его коррекцию, зачастую - по неотложным показаниям. Профилактику СРО необходимо начинать за 24-48 ч до введения цитостатиков.
Основные меры профилактики синдрома распада опухоли
Ä Избыточная гидратация. Как правило, внутривенное введение 0,9% раствора хлорида натрия со скоростью 3000 мл/м2 в сутки в сочетании с однократным введением 20 мг фуросемида обеспечивает форсирование диуреза и уменьшение концентрации мочевой кислоты, фосфатов и калия, что значительно снижает риск образования кристаллов мочевой кислоты и/или фосфата кальция и их преципитации в почечных канальцах.
Лечение направлено на коррекцию возникших метаболических нарушений.
-
Гиперкалиемия - одно из наиболее угрожающих жизни больного проявлений СРО, которое требует немедленного лечения в сочетании с непрерывным мониторингом ЭКГ и лабораторных показателей. Лечебная тактика направлена на снижение уровня калия в сыворотке за счёт его усиленного транспорта в клетки и выделения через почки и кишечник. Она зависит от исходного уровня калия в сыворотке крови.
-
Умеренное повышение уровня калия в сыворотке крови (до 5,6 ммоль/л) проводят внутривенную гипергидратацию 0,9% раствором натрия хлорида в сочетании с однократным введением 20 мг фуросемида.
-
Значительное повышение уровня калия в сыворотке крови (5,8-6,0 ммоль/л). В этом случае показаны неотложные лечебные мероприятия.
-
Внутривенно медленно (в течение 3-5 мин) струйно вводят 10-30 мл 10% раствор глюконата кальция, 200-300 мл 4,2-8,4% раствор гидрокарбоната натрия, гипертонический раствор декстрозы (50 мл 50% раствора) в сочетании с 10 ЕД препарата инсулина короткого действия.
-
Петлевые диуретики (фуросемид в дозе 20-40 мг внутривенно струйно) на фоне усиленной гидратации обеспечивают выведение избытка калия у больных без признаков острой почечной недостаточности. В случае развития почечной недостаточности показано выполнение гемодиализа.
-
Ионно-обменную смолу (Kayexalate) назначают в дозе 25-50 г внутрь (запить 50 мл 70% раствора сорбитола) или в дозе 50 г в прямую кишку (в 20% растворе сорбитола).
-
Гиперурикемия также требует безотлагательного лечения, поскольку она играет основную роль в развитии острой почечной недостаточности. Для коррекции нарушения назначают аллопуринол, аналоги фермента урат оксидазы.
-
Аллопуринол - основной препарат, который используют для коррекции мочекислого диатеза. Этот аналог пуринового основания гипоксантина снижает уровень мочевой кислоты в сыворотке крови путём ингибирования ксантин оксидазы - фермента, ответственного за превращение гипоксантина в ксантин и далее - в мочевую кислоту. Её активный метаболит, оксипуринол, также подавляет активность ксантин оксидазы. Поскольку и аллопуринол, и оксипуринол ингибируют синтез мочевой кислоты, не влияя на уже имеющееся её количество, содержание этого вещества в сыворотке крови снижается не ранее, чем через 48-72 ч от начала лечения.
-
-
Наиболее часто аллопуринол назначают в дозе 300 мг в сутки (однократно или по 100 мг 3 раза в сутки) в течение 1-2 нед. Реже используют высокие (600-900 мг в сутки) дозы препарата. Альтернативный вариант - внутривенное введение лекарственного средства в дозе 200-400 мг/м2 в сутки. К недостаткам аллопуринола относят риск развития аллергических реакций (в первую очередь, кожной сыпи и зуда), а также нарушение метаболизма ряда цитостатиков.
-
Аналоги фермента урат оксидазы. Урат оксидаза катализирует превращение мочевой кислоты в аллантоин, для которого характерна высокая растворимость в моче, облегчающая его выведение из организма через почки. В отличие от аллопуринола, блокирующего дальнейший синтез мочевой кислоты, урат оксидаза вызывает её непосредственное разрушение, поэтому её можно с успехом применять при необходимости быстрого (в течение 3-4 ч) снижения уровня уратов в сыворотке крови.
Быстрое наступление эффекта, заключающееся в нормализации уровня мочевой кислоты, - преимущество препаратов на основе урат оксидазы по сравнению с аллопуринолом. В частности, их назначение позволяет избежать отсрочек начала цитостатической терапии, что имеет особенное значение у больных с интенсивно пролиферирующими злокачественными новообразованиями.
Позднее начало или отсутствие своевременной коррекции гиперурикемии, как правило, приводит к развитию острой почечной недостаточности.
Обструкция мочевыводящих путей и/или уровень мочевой кислоты в сыворотке крови выше 20 мг в 100 мл - абсолютные показания для проведения немедленного гемодиализа.
Поражение сердечно-сосудистой системы
Патогенез поражения миокарда, крупных и мелких сосудов при проведении химиотерапии окончательно не установлен.
Факторы риска возникновения осложнений со стороны сердечно-сосудистой системы:
Основные механизмы кардиотоксичности:
Эти токсические реакции характерны для блеомицина, производных нитрозомочевины (кармустин, ломустин), винкаалкалоидов (винкристин, винбластин), доксорубицина и других антрациклиновых антибиотиков, циклофосфамида.
Повреждение сердечной мышцы
Клинические формы повреждения сердечной мышцы
К проявлениям острого повреждения миокарда относят гипотонию, тахикардию, нарушения сердечного ритма, дисфункцию левого желудочка (в том числе снижение фракции выброса левого желудочка), кардиалгии, изменения ЭКГ (снижение вольтажа, удлинение интервала QT), повышение концентрации тропонина Т в сыворотке крови.
Как правило, обратимые и непродолжительные проявления острой кардиомиопатии возникают при превышении стандартной разовой дозы цитостатика (например, 60 мг/м2 для доксорубицина). Значительное повышение двигательной активности больного, развитие фебрильной нейтропении, инфекционных осложнений химиотерапии могут способствовать декомпенсации и ухудшению течения острой кардиомиопатии.
Применение ряда цитостатиков, таких как винкаалкалоиды, цисплатин, этопозид, циклофосфамид, фторурацил (в виде многочасовой инфузии), может осложняться развитием ишемии или острого инфаркта миокарда. Проявления ишемии миокарда варьируют от бессимптомных нарушений электрокардиограммы до приступов стенокардии, кардиогенного отёка лёгких и летального исхода.
Клиническая картина отсроченной (поздней) кардиомиопатии развивается в течение нескольких недель или месяцев после завершения цитостатического лечения. У больных определяют симптомы миокардита, перикардита, дилатационной кардиомиопатии, застойной сердечной недостаточности, реже - инфаркта миокарда.
Наиболее характерно возникновение хронической сердечной недостаточности при превышении кумулятивной дозы антрациклиновых антибиотиков, которая составляет 550 мг/м2 для доксорубицина, 1000 мг/м2 - для эпирубицина и 140 мг/м2 - для митоксантрона. Риск развития данного осложнения значительно возрастает у женщин пожилого возраста, получавших комбинацию доксорубицина с другими кардиотоксичными препаратами (например, циклофосфамидом, трастузумабом).
Диагностика повреждения сердечной мышцы и ведение больных
Назначение комбинаций цитостатиков, включающих антрациклиновые антибиотики, требует тщательного контроля функционального состояния сердечно-сосудистой системы на всём протяжении лечения и в течение 1-2 лет после его окончания.
К основным диагностическим методам относят ЭКГ (в том числе суточное холтеровское мониторирование ЭКГ), ЭхоКГ, определение уровня сердечных тропонинов, MB-фракции креатин фосфокиназы в сыворотке больного. Реже выполняют радионуклидную сцинтиграфию миокарда.
Начальное обследование выполняют до первого введения цитостатиков, в последующем - перед каждым очередным циклом химиотерапии. Особое внимание следует уделять результатам мониторинга, осуществляемого после достижения кумулятивной дозы доксорубицина более 300 мг/м2. При отсутствии признаков кардиотоксичности возможно продолжение терапии антрациклиновыми антибиотиками в полных дозах до достижения максимальной кумулятивной дозы. Большинство авторов в этом случае рекомендуют дополнительно назначать лекарственные средства, улучшающие обменные процессы в миокарде (кокарбоксилаза, триметилгидразиния пропионат [милдронат©], пиридоксин, инозин), и/или внутриклеточный антиоксидант дексразоксан, который уменьшает кардиотоксичность доксорубицина. Как правило, его назначают в дозе, превышающей дозу доксорубицина в 10-20 раз (1000 мг/м2), за 30 мин до введения цитостатика.
При развитии симптомов хронической сердечной недостаточности необходимо прекратить приём антрациклиновых антибиотиков и назначить общепринятую в этих случаях терапию.
Активация свёртывающей системы крови и агрегации тромбоцитов - довольно редкий механизм развития кардиотоксичности, характерный для цисплатина, блеомицина, тамоксифена.
Ряд цитостатиков, в первую очередь, винкаалкалоиды, вызывая повреждение периферической нервной системы, оказывают таким образом опосредованное негативное влияние на сердечно-сосудистую систему.
Повреждение крупных и мелких сосудов
Постцитостатическое повреждение сосудов может затрагивать как крупные артерии и вены, так и систему микроциркуляции. Наиболее часто возникают веноокклюзионная болезнь, синдром Рейно, тромботический микроангиопатический синдром, тромбозы и тромбоэмболии, артериальная гипотония и гипертония.
Веноокклюзионная болезнь - патологическое состояние, обусловленное цитостатическим повреждением эндотелия и соединительной ткани мелких вен, в результате чего происходит их нетромботическая облитерация. Наиболее часто в процесс вовлечены сосуды печени (см. раздел "Поражения желудочно-кишечного тракта") и лёгких.
При морфологическом исследовании аутопсийного материала выявляют окклюзию мелких лёгочных вен и венул, картину интерстициального фиброза лёгочной ткани. Это возникает, как правило, вследствие повреждения эндотелиоцитов лёгочных сосудов блеомицином, митомицином, реже - кармустином.
В клинической картине преобладают симптомы дыхательной недостаточности и лёгочной гипертензии, от умеренных до несовместимых с жизнью. Специфическое лечение веноокклюзионной болезни лёгких отсутствует. Проводят симптоматическую терапию (глюкокортикоиды, бронхолитики).
Синдром Рейно
Возникает транзиторный спазм мелких сосудов кистей (вазоспастические атаки), которые, как правило, провоцируют холод, употребление алкоголя, эмоциональный стресс. Преходящая ишемия приводит к изменению цвета кожи кистей (бледность кончиков пальцев, сменяющаяся синюшностью и локальным отёком). Крайне редко возникает гангрена пальцев, требующая выполнения ампутации. Синдром Рейно в большинстве случаев носит персистирующий характер (в течение 5 и более лет после завершения химиотерапии).
Наиболее часто (до 40% от всех описанных случаев) развитие этого синдрома осложняет терапию блеомицином и его комбинациями с винкаалкалоидами, цисплатином, этопозидом, доксорубицином, интерфероном.
Лечение - местное применение мазей, содержащих нитроглицерин, блокаторы кальциевых каналов.
Тромботический микроангиопатический синдром
Для него характерно развитие гемолитической анемии, тромбоцитопении и почечной недостаточности. Он наиболее часто возникает при назначении митомицина (при превышении его кумулятивной дозы, равной 60 мг), реже - цисплатина, блеомицина, карбоплатина, кармустина, интерферона альфа. Первые признаки синдрома на фоне приёма митомицина регистрируют в течение 2-15 мес после последнего введения препарата.
Клиническая картина. Могут возникать выраженная гемолитическая анемия, гематурия, протеинурия, лихорадка, сыпь; возможно развитие интерстициального пневмонита или отёка лёгких, неврологических расстройств, вторичной артериальной гипертензии, перикардита, сердечной и почечной недостаточности. Наибольшую опасность представляет быстро прогрессирующая почечная недостаточность, требующая проведения гемодиализа.
Основные патоморфологические признаки: поражение паренхимы почек (отложения фибрина, пролиферация эндотелия капилляров клубочков и приносящих артериол, утолщение клубочковой базальной мембраны, инфаркты и некроз клубочков).
Лечение неспецифическое (глюкокортикоиды, трансфузия эритроцитарной массы, плазмаферез) и, как правило, малоэффективное.
Тромбозы и тромбоэмболии
При назначении цисплатина, блеомицина, этопозида, паклитаксеал, интерферона альфа могут возникать осложнения в виде тромбозов и тромбоэмболий в результате активации свёртывающей системы крови.
Факторы риска тромбозов:
Описаны нередкие случаи развития тромбоэмболии лёгочной артерии, тромбоза глубоких вен нижних конечностей и мезентериальных сосудов, интерстициального инфаркта лёгкого, нарушения мозгового кровообращения при назначении вышеупомянутых цитостатиков у больных герминогенными опухолями, раком органов головы, шеи и пищевода, неходжкинскими лимфомами.
Лечение неспецифическое (антикоагулянты, дезагреганты, препараты, улучшающие микроциркуляцию).
Артериальная гипотензия
Гипотензивные реакции часто возникают на фоне быстрого введения некоторых цитостатиков (этопозид, тенипозид, дакарбазин, кармустин, винкристин) и носят ортостатический характер. Артериальная гипотензия может быть также одним из проявлений реакции гиперчувствительности немедленного типа при назначении таксанов, аспарагиназы, антрациклиновых антибиотиков, высоких доз метотрексата.
Артериальная гипертензия
Повышение артериального давления наблюдают при внутриартериальном введении цисплатина, прокарбазина. Также возможно развитие вторичной гипертензии вследствие склероза почечных артериол (позднее осложнение при использовании цисплатина).
Поражение лёгких
Различные варианты постцитостатического повреждения лёгочной ткани регистрируют у каждого пятого больного, подвергавшегося химиотерапии.
Основные факторы риска постцитостатического поражения лёгких:
Механизмы постцитостатического повреждения лёгких:
Непосредственное цитотоксическое повреждение лёгких
К цитостатикам, обладающим повышенной токсичностью в отношении лёгочной ткани, относят блеомицин, митомицин, циклофосфамид, бусульфан, метотрексат, цитарабин, кармустин, винкаалкалоиды, паклитаксел.
Факторы риска:
Патогенез
Ключевое звено патогенеза - гиперпродукция эндогенных факторов воспаления (простагландины, лейкотриены), которую стимулируют свободные радикалы, образующиеся в ходе метаболизма ряда цитостатиков. В результате запуска воспалительных реакций происходит повреждение лёгочной ткани (особенно - альвеолярной мембраны). Некроз эндотелиальных клеток альвеол приводит к усилению пролиферации фибробластов и синтеза коллагена, что сопровождается нарушением проницаемости капилляров, лимфоцитарной и эозинофильной инфильтрацией, интраальвеолярным и интерстициальным отёком. При дальнейшем прогрессировании процесса наблюдают типичную патоморфологическую картину, включающую признаки интерстициального фиброза, облитерирующего бронхиолита, окклюзии мелких венул.
Профилактика
С целью профилактики не рекомендуют превышать максимально допустимые кумулятивные дозы препаратов, которые составляют 330 мг/м2 для блеомицина, 1000 мг/м2 для кармустина и 250 мг/м2 для митомицина.
Целесообразно проводить динамическую оценку функционального состояния дыхательной системы до начала курса химиотерапии, на всём его протяжении и в течение 1-2 лет после окончания. При ухудшении показателей функции внешнего дыхания на 10-15% необходимо отменить блеомицин из-за значительного повышения риска развития необратимых изменений лёгочной ткани.
Клиническая картина
Сроки развития цитотоксического поражения лёгких существенно различаются и составляют от нескольких недель и месяцев при использовании блеомицина до 3-4 лет при назначении циклофосфамида и бусульфана.
Для клинической картины характерны одышка, непродуктивный иногда мучительный приступообразный кашель, иногда возникают боли в грудной клетке, лихорадка. При аускультации лёгких выслушивают сухие хрипы, крепитацию, шум трения плевры. Выраженность симптоматики может различной: от лёгких и преходящих нарушений до быстро прогрессирующей дыхательной недостаточности.
В соответствии с критериями токсичности, разработанными Национальным Институтом Рака (США) выделяют четыре степени тяжести пульмонита.
Степени тяжести пульмонита
-
Лёгкая степень - бессимптомное течение, при котором патологическое состояние лёгочной ткани выявляют только рентгенологическим методом.
-
Умеренная степень. Возникает клиническая симптоматика, для купирования которой необходимо назначение глюкокортикоидов.
-
Тяжёлая степень. Характерна дыхательная недостаточность, требующая применения оксигенотерапии.
-
Крайне тяжёлая степень - выраженная, угрожающая жизни больного дыхательная недостаточность, которую рассматривают показанием к искусственной вентиляции лёгких.
У 10-30% больных, получавших блеомицин, митомицин, кармустин в высоких дозах, развивается интерстициальный фиброз лёгких, приводящий в 25-65% случаев к летальному исходу. При лёгкой степени тяжести (до 20% больных) клиническая симптоматика отсутствует. Выраженный интерстициальный фиброз может осложняться развитием пневмоторакса, лёгочного кровотечения, зачастую фатального.
Для рентгенологической картины постцитостатического пульмонита характерны интерстициальный отёк, двусторонние узловые инфильтраты с преимущественным субплевральным расположением, реже определяют плевральный выпот, увеличение размеров средостения. При интерстициальном фиброзе выявляют рубцовые изменения лёгочной ткани, утолщение плевры, редко -признаки пневмоторакса.
Морфологическое подтверждение патологического процесса осуществляют при исследовании биоптата лёгочной ткани, полученного путём трансторакальной пункции.
Лечение постцитостатического пульмонита неспецифическое. Отменяют цитостатик, вызвавший развитие осложнения, назначают глюкокортикоиды, бронхолитики, дериваты нуклеиновых кислот (например, актовегин©), витамины группы А, С, Е. При возникновении лёгочного кровотечения проводят активную гемостатическую терапию (аминокапроновая кислота, кальций хлорид назначают внутривенно, выполняют лечебную фибробронхоскопию.
Реакции гиперчувствительности замедленного типа
Они наиболее часто возникают у больных, получающих блеомицин, прокарбазин, метотрексат, паклитаксел. К основным симптомам относят сухой непродуктивный кашель, одышку вследствие бронхоспазма и/или отёка слизистой оболочки верхних дыхательных путей, лихорадку (редко). Они возникают остро при повторном или очередном введении препарата. В периферической крови, бронхиальной лаважной жидкости выявляют эозинофилию, лимфоцитоз, в биоптате лёгочной ткани - признаки эозинофильной пневмонии.
Лечебные мероприятия заключаются в прекращении введения цитостатика, вызвавшего развитие осложнения, срочном внутривенном назначении глюкокортикоидов, бронхолитиков, оксигенотерапии.
Воспаление эндотелия мелких сосудов и капилляров
Диффузное воспаление лёгочных капилляров, артериол и венул могут вызывать митомицин, доксорубицин, паклитаксел, интерлейкин-2, препараты ретиноевой кислоты (третиноин). Для клинической картины характерны острое, реже подострое начало, развитие инспираторной одышки, лихорадки, тахикардии, гипотензии, плеврального выпота. При осложнённом течении может развиваться некардиогенный отёк лёгких, летальность при котором достигает 60%.
Лечение неспецифическое: назначают глюкокортикоиды, НПВС, ингаляции кислорода.
Острый бронхоспазм
Изолированный бронхоспазм относят к редким осложнениям цитостатической терапии. Наиболее часто он возникает при назначении митомицина, винкаалкалоидов, таксанов. Основные симптомы бронхоспазма - острое возникновение экспираторной одышки, болей в грудной клетке и за грудиной, сухого приступообразного кашля, дистантных хрипов, цианоза кожи, реже возникает кровохаркание. Летальность при развитии острого бронхоспазма достигает 3-5%.
Экстренные лечебные мероприятия включают парентеральное введение глюкокортикоидов, бронхолитиков, оксигенотерапию.
Поражение нервной системы
Из всех вариантов токсических реакций со стороны нервной системы наиболее часто возникает периферическая полинейропатия (более 30% от всех случаев нейротоксичности) и ототоксичность (до 10-15%).
Повреждение нервной системы наиболее характерно для цитостатиков, которые воздействуют на микротубулярный аппарат опухолевых клеток. В первую очередь, к ним относят таксаны и винкаалкалоиды. В механизме развития периферической нейротоксичности цисплатина основное значение придают непосредственному накоплению препарата в дорсальных ганглиях, что приводит к их повреждению.
Группы противоопухолевых лекарственных средств в зависимости от степени нейротоксичности: высокотоксичные, умереннотоксичные, малотоксичные.
-
Высокотоксичные цитостатики. К ним относят винкристин (частота нейротоксичности >90%), цисплатин в кумулятивной дозе более 300 мг/м2 (частота нейротоксичности >85%), паклитаксел в цикловой дозе более 175 мг/м2 (частота нейротоксичности >60%), метотрексат при интратекальном введении (частота центральной нейротоксичности достигает 40%), оксалиплатин.
-
Умереннотоксичные цитостатики (ифосфамид, цитарабин, этопозид, винорелбин, флударабин, цисплатин в кумулятивной дозе менее 300 мг/м2, темозоломид, прокарбазин). Частота развития нейротоксичности составляет 10-25%.
-
Малотоксичные цитостатики (фторурацил, тегафур, гемцитабин, иринотекан). Частота повреждения нервной системы не превышает 5-10%.
Выявление и определение степени тяжести нейротоксических реакций осуществляют в ходе оценки неврологического статуса больного квалифицированный специалист, окулист, а также при проведении электрофизиологических исследований (энцефалографии, аудиографии и др.).
Позднее развитие большинства симптомов нейротоксичности рассматривают основанием для изменения доз цитостатиков уже при выявлении лёгкой степени их выраженности. Возникновение третьей степени тяжести осложнений со стороны нервной системы требует безусловной отмены препарата.
Поражение периферической нервной системы
Периферическая нервная система в большей степени подвержена повреждающему воздействию со стороны цитостатиков, поскольку, в отличие от головного и спинного мозга, они не защищены гематоэнцефалическим барьером.
Механизмы нейротоксического действия
-
Воздействие на микротрубочки и микрофиламенты аксонов периферических нервов - основной механизм действия большинства нейротоксичных препаратов. Например, винкристин вызывает деполимеризацию микротрубочек нейронов в соответствии со своим основным противоопухолевым механизмом действия. Таксаны, в частности паклитаксел, напротив, стабилизируют микротубулярный аппарат, препятствуя деполимеризации микротрубочек. Нейротоксичность паклитаксела дозозависима, возрастает при назначении цикловой дозы более 175 мг/м2, а также при уменьшении продолжительности скорости инфузии менее 3 ч и у пожилых больных.
-
Аккумуляция цитостатиков или их метаболитов в нейронах с непосредственным разрушением их цитоскелета (например, при использовании цисплатина).
Риск возникновения постцитостатических осложнений со стороны периферической нервной системы значительно выше у больных, страдающих сопутствующим сахарным диабетом, алкоголизмом.
Токсическую периферическую (или аксональную) полинейропатию подразделяют на преимущественно моторные, преимущественно сенсорные и преимущественно вегетативные нарушения.
Моторная полинейропатия
Моторная полинейропатия наиболее часто развивается при назначении винкаалкалоидов. Возникает парез кишечника, сопровождающийся запорами, болями в животе разлитого характера, атония мочевого пузыря, мышечная слабость, приводящая к затруднениям при ходьбе, выполнении мелких движений.
В эту же группу включают вестибулярную нейротоксичность, которую вызывает цисплатин и ряд других цитостатиков. После окончания лечения в течение длительного времени больные могут предъявлять жалобы астенического характера (повышенная возбудимость, утомляемость, головные боли, головокружения).
Сенсорная нейротоксичность
Возникают симметричные, как правило, дистальные парестезии и дизестезии по типу "носков" и "перчаток" в кистях и стопах, которые в большей степени беспокоят больного в состоянии покоя. Для выраженной сенсорной нейротоксичности характерна значительная и стойкая потеря чувствительности, которая затрудняет привычный образ жизни больного. При неврологическом осмотре выявляют снижение глубоких сухожильных рефлексов. С целью уменьшения симптоматики назначают поливитамины (например, нейромультивит©), антидепрессанты (амитриптилин).
Вегетативные нарушения
К нарушениям со стороны вегетативной нервной системы относят острый холинэргический синдром, осложняющий терапию иринотеканом, синдром Рейно, синдром пальмарно-плантарной эритродизестезии (ладонно-подошвенный синдром), развивающийся при назначении капецитабина, липосомального доксорубицина.
Поражение центральной нервной системы
Оно проявляется двигательными расстройствами (пирамидными, мозжечковыми, экстрапирамидными), изменением сознания и памяти, а также психовегетативными нарушениями (вегетативные кризы, тревожный и астенодепрессивный синдромы, головная боль).
Основные синдромы постцитостатического повреждения центральной нервной системы: синдром раздражения мозговых оболочек (менингизм), острая мозжечковая атаксия, острая и хроническая токсическая энцефалопатия, симптоматические эпилептические припадки, инсультоподобный синдром.
-
Синдром раздражения мозговых оболочек (менингизм). Он наиболее часто возникает при интратекальном введении метотрексата или цитарабина. Для него характерно острое (в течение 2-4 ч) возникновение сильной головной боли, головокружения, тошноты, рвоты, диплопии, светобоязни, парезов, дезориентации, нарушения сознания, ригидности затылочных мышц. При подостром течение синдрома симптоматика развивается в течение 7-10 дней после введения препаратов.
Нейротоксические реакции при интратекальном введении цитостатиков, как правило, носят обратимый характер. Лечебные мероприятия включают соблюдение постельного режима, назначение обезболивающих и мочегонных препаратов (фуросемид, маннитол), глюкокортикоидов.
-
Острая мозжечковая атаксия - спонтанная, обычно обратимая реакция, возникающая при интратекальном или системном введении цитарабина в высоких дозах. Степень выраженности осложнения может быть различной: от лёгкого нарушения координации и речи, тремора, нистагма до тяжёлой двигательной атаксии и даже некроза мозжечка (в крайне тяжёлых случаях).
-
Острая и хроническая токсическая энцефалопатия. Она может осложнять проведение химиотерапии практически всеми известными цитостатиками. К клиническим проявлениям острой токсической энцефалопатии относят возникновение сонливости, головокружения, обмороков, галлюцинаций, возбуждения, транзиторной кортикальной слепоты. Длительное проведение лекарственного лечения приводит к нарушению внимания, кратковременной и долговременной памяти, эмоционально-волевыми расстройствам, астении, тревоге, депрессии. К серьёзным осложнения относят кому или симптоматические психические расстройства (токсический психоз), при возникновении которого показана консультация психиатра. Для купирования симптомов энцефалопатии назначают седативные средства, транквилизаторы, ноотропные и сосудистые препараты.
-
Симптоматические эпилептические припадки. Реактивные эпилептические припадки, как правило, носят генерализованный характер. Их купируют по общим принципам. Они не трансформируются в эпилепсию.
-
Инсультоподобный синдром. Он возникает у небольшой части больных, получающих метотрексат в высоких дозах (более 1000 мг/м2). Для него характерно развитие в течение нескольких часов после введения препарата снижения уровня сознания вплоть до развития глубокой комы. Продолжительность коматозного состояния составляет от 24 до 72 ч, после чего происходит полное восстановление сознания.
Поражение кожи и её придатков
В общей структуре токсических реакций химиотерапии поражение кожи и её придатков занимает преимущественную часть, что связано с интенсивной пролиферацией клеток кожи, слизистых оболочек и волосяных фолликулов. По этой причине они наряду с опухолевыми клетками становятся мишенями для большинства цитостатиков. Дерматологические осложнения практически никогда не представляют угрозы для жизни больного, однако значительно ухудшают её качество. Большая их часть проходит самостоятельно после окончания курса химиотерапии и не требует дополнительного лечения или изменения доз цитостатиков.
Частота возникновения и степень выраженности дерматологических осложнений значительно изменяется в зависимости от применяемого цитостатика и его дозы. Некоторые осложнения носят индивидуальный или отчётливо аллергический характер.
Побочные реакции со стороны кожи и её придатков: ранние и поздние (отсроченные)
-
Ранние осложнения. К ним относят эритему, различные виды высыпаний и сыпи, кожный зуд, алопецию, десквамацию эпителия. В дальнейшем в ряде случаев могут возникать стойкие дерматопатии, среди которых выделяют гипер- и паракератозы, склеродермию, гиперпигментацию кожи, ногтей, слизистых оболочек.
-
Поздние осложнения: гидрадениты, фолликулиты, васкулиты, в том числе, вследствие присоединения вторичной инфекции.
Алопеция
Выпадение волос - следствие непосредственного цитотоксического повреждения быстропролиферирующих клеток волосяных фолликулов, при котором происходит полное или частичное подавление их митотической активности. В результате изменяется нормальная структура волос (истончение, ослабление, изменение цвета) или их потеря.
Наиболее часто (в 85-95% случаев) алопеция возникает при назначении антрациклиновых антибиотиков, таксанов, иринотекана, винкристина, ифосфамида, идарубицин, несколько реже (в 30-50%) - при использовании циклофосфамида, этопозида, топотекана, блеомицина, цисплатина, кармустина.
Как правило, полная или частичная алопеция затрагивает волосистую часть головы, значительно реже отмечают повреждение волосяных фолликулов бровей, ресниц, подмышечной и лобковой области. Обычно выпадение волос начинается спустя 1-2 нед после введения цитостатика и продолжается в течение 1-2 мес после завершения курса химиотерапии.
Алопеция - дозозависимое осложнение, выраженность которого уменьшается после снижения дозы цитостатика. Иногда рост волос возобновляется на фоне продолжающегося цитостатического лечения. Обратимый характер алопеции обусловлен тем, что не менее 10-15% клеток волосяных фолликулов во время введения цитостатика находятся в непролиферативной фазе. После восстановления волосяного покрова у части больных наблюдают изменение цвета и структуры волос. В то же время, описаны случаи необратимой алопеции, как правило, после проведения высокодозной ПХТ, включающей алкилирующие лекарственные средства циклофосфамид и бусульфан.
В соответствии с критериями Национального Института Рака (США) выделяют три степени выраженности алопеции.
Степени выраженности аллопеции
С целью уменьшения степени выраженности алопеции используют методику гипотермии волосистой части головы. Охлаждающий шлем одевают за 20-30 мин до введения цитостатиков и снимают через 40-60 мин.
Гиперпигментация кожи
Гиперпигментация наиболее часто осложняет химиотерапию алкилирующими лекарственными средствами и противоопухолевыми антибиотиками (циклофосфамид, бусульфан, ифосфамид, блеомицин), а также цисплатином, карбоплатином, дакарбазином, метотрексатом, дактиномицином. Гиперпигментация может иметь локализованный или генерализованный характер, сопровождаться гиперпигментацией волос, ногтей, слизистой оболочки ротовой полости (доксорубицин, митоксантрон).
Основной механизм патогенеза - стимуляция синтеза меланина в меланоцитах дермы. Гиперпигментация возникает спустя несколько недель после начала курса химиотерапии и разрешается самостоятельно в течение нескольких месяцев после её завершения. Специального лечения не требует.
Дерматит при назначении блеомицина
У трети больных после терапии блеомицином отмечают развитие диффузной или локализованной (линейной) гиперпигментации кожи как исход эритемы или буллёзной сыпи (реже). Преимущественное расположения очагов поражения - участки тела, испытывающие контактное давление (локти, лопатки, шея, плечевой пояс, колени), а также область наружных половых органов. Гиперпигментация кожи постепенно разрешается в течение 6-18 мес после завершения лечения. При развитии выраженного дерматита можно использовать глюкокортикоиды. Блеомицин может также приводить к развитию ониходистрофии, склеротических изменений кожи, гиперкератоза.
Экзема
Назначение многих цитостатиков (блеомицин, дактиномицин, фторурацил, гемцитабин, ифосфамид, метотрексат, меркаптопурин и др.) может сопровождаться возникновением дерматологических аллергических реакций типа IV. Для экземы характерна везикулопапулёзная сыпь, гиперемия и мацерация кожи, кожный зуд. Лечение заключается в системном и местном (в виде мазей, гелей) применении глюкокортикоидов.
Мультиформная эритема, синдром Стивенса-Джонсона, токсический некроз эпидермиса
Эти осложнения возникают редко, чаще всего при назначении хлорамбуцила, циклофосфамида, дактиномицина, блеомицина, этопозида, метотрексата, митомицина, азатиоприна.
Мультиформная эритема - поражение кожи в виде сливающейся макулёзной и папулёзной сыпи. Генерализованная форма мультиформной эритемы, осложнённая эрозиями и изъязвлениями кожи, носит название синдрома Стивенса-Джонсона.
Наиболее опасным осложнением считают диффузный токсический некроз эпидермиса. Клиническая картина, развивающаяся при тотальном поражении эпидермиса кожи, аналогична манифестации термического ожога степени II.
Лечение заключается в назначении системных глюкокортикоидов и обезболивающих препаратов, местной терапии (обезболивающая, противовоспалительная, антисептическая).
Синдром пальмарно-плантарной эритродизестезии (ладонно-подошвенный синдром)
Синдром может возникать при назначении капецитабина, фторурацила в виде длительной инфузии, липосомального доксорубицина, блеомицин, реже его вызывают таксаны, цитарабин, циклофосфамид. Характерно поражение кожи ладоней и подошв.
Степени тяжести ладонно-подошвенного синдрома: лёгкая, умеренная, тяжёлая.
-
Лёгкая степень (безболезненные эритема и отёк, сухость и шелушение кожи ладоней и стоп, лёгкие парестезии).
-
Умеренная степень (болезненные эритема и отёк, парестезии, вызывающие дискомфорт и ограничение повседневной активности больного).
-
Тяжёлая степень (развитие влажной десквамации эпителия, изъязвлений, трещин, сопровождающихся болевым синдромом и резким ограничением всех видов повседневной деятельности больного).
Применение глюкокортикоидов, пиридоксина, диметилсульфоксида малоэффективно. Обычно рекомендуют отложить проведение очередного цикла химиотерапии и/или снизить дозу цитостатика.
Изменения ногтевых пластинок
Различные изменения формы, структуры или цвета ногтей относят к редким осложнениям химиотерапии.
Виды изменения ногтевых пластинок:
-
поперечная исчерченность ногтевых пластинок (при назначении бусульфана, цисплатина, циклофосфамида, ифосфамида, доксорубицина);
-
онихолизис (при назначении блеомицина, доксорубицина, этопозида, фторурацила, митоксантрона);
-
гиперпигментация (при использовании бусульфана, идарубицина, блеомицина, дакарбазина, метотрексата, митомицина);
-
дистрофия ногтей (при применении производных нитрозомочевины).
Длительное постцитостатическое повреждение ногтевых пластинок может осложняться присоединением вторичной грибковой инфекции (онихомикоз).
Фотосенсибилизация
Фотосенсибилизация - повышенная чувствительность к ультрафиолетовому излучению. Для неё характерно возникновение эритемы, макулопапулёзной сыпи на лице и других открытых участках тела, подвергающихся воздействию солнечного света. Наиболее часто это осложнение возникает при назначении дакарбазина, фторурацила, метотрексата, меркаптопурина, митомицина, доцетаксела, винкаалкалоидов.
С целью профилактики её развития рекомендуют избегать инсоляции. В случае развития тяжёлой формы фотодерматита назначают системное и местное лечение глюкокортикоидами.
Васкулит
Васкулит относят к редким осложнениям противоопухолевого лечения. Он чаще возникает при назначении азатиоприна, бусульфана, циклофосфамида, цитарабина, мелфалана, митоксантрона, метотрексата. Возникает диффузное, как правило, транзиторное поражение кожи по типу пурпуры с участками изъязвлений. В тяжёлых случаях рекомендуют назначать глюкокортикоиды.
Сыпь
Выделяют макулопапулёзный, псориазоподобный и акнеформный вариант сыпи. Наиболее часто она возникает при назначении блеомицина, метотрексата, карбоплатина, доцетаксела, паклитаксела, этопозида, доксорубицина, цитарабина, ингибиторов тирозин киназ (гефитиниб, эрлотиниб), интерферона альфа, интерлейкина-2.
С лечебной целью возможно местное применение глюкокортикоидов.
Экстравазация
Частота возникновения экстравазаций у больных, получающих системную химиотерапию, достигает 5-6%.
Факторы риска:
Экстравазация и последующий некроз кожи и подкожной жировой клетчатки наиболее часто возникают при назначении доксорубицина, митоксантрона, дактиномицина, блеомицина, митомицина, мелфалана, кармустина, винбластина, винкристина, этопозида, цисплатина, паклитаксела, цитарабина.
Степень тяжести осложнения может варьировать от лёгкой болезненности и эритемы в месте инъекции до развития выраженного химического воспаления подкожной жировой клетчатки (целлюлит) и сосудистой стенки (флебит), сопровождающихся изъязвлениями и некрозом кожи, повреждением сухожилий и суставов с формированием контрактур. Тяжесть поражения зависит от цитостатика, его концентрации, объём раствора, поступившего в ткани, места инфильтрации, правильности лечебных мероприятий, предпринятых медицинским персоналом.
Наиболее эффективно профилактировать возникновение экстравазации.
Основные профилактические мероприятия:
-
выполнение венепункций и введение цитостатиков квалифицированным медицинским персоналом;
-
использование хорошо определяемых периферических вен с достаточным просветом или центральных вен;
-
запрет на введение цитостатиков в вены, расположенные дистальнее предшествующей венепункции;
-
немедленное прекращение инфузии при появлении жалоб больного возникновение болей или дискомфорта по ходу вены.
Появление болей при введении цитостатика даже при отсутствии видимых изменений можно рассматривать признаком повышенного риска развития местных токсических реакций.
Клиническая картина
Время развития клинической картины находится в зависимости от вида цитостатика. Например, для антрациклиновых антибиотиков характерно появление болей во время введения препарата, спустя 7-10 дней возникает эритема, значительно усиливается боль, в дальнейшем развивается изъязвление кожи и подкожной клетчатки, сохраняющееся в течение 2-3 мес. В исходе развивается некроз кожи и подкожной жировой клетчатки, а в тяжёлых случаях - расположенных рядом сухожилий, сосудисто-нервных структур, суставной сумки с формированием контрактуры сустава, особенно при экстравазации вблизи локтевого сустава, суставов запястья, кисти.
Лечение
-
Немедленное прекращение дальнейшего введения цитостатика, попытка аспирации препарата через иглу до её удаления из вены.
-
Местное применение льда (на 20 мин 3 раза в день в течение 3 дней).
-
Обкалывание места поражения дексаметазоном, гидрокортизоном, гепарином натрия. Рекомендуют также внутривенно струйно в повреждённую вену вводить 20-60 мл 0,9% раствора натрия хлорида с глюкокортикоидами.
-
В случае экстравазации винкаалкалоидов используют теплые компрессы на 20 мин 4 раза в сутки в течение первых 24-48 ч.
-
Диметилсульфоксид, тиосульфат натрия и альфа-токоферола ацетат можно использовать в качестве активных антидотов, однако, их клиническое значение не доказано. Ряд авторов рекомендуют выполнять аппликации диметилсульфоксида 6 раз в день в течение 7-14 дней.
-
Показан осмотр хирурга на 2-3 сут. При наличии изъязвлений или прогрессирующего некроза выполняют широкое иссечение кожи и подкожной клетчатки.
Редкие дерматологические осложнения
-
Угри (при назначении цисплатина, дактиномицина, доксорубицина, метотрексата).
-
Буллёзная сыпь (при назначении блеомицина, цитарабина, метотрексата, гемцитабина, винбластина).
-
Фолликулит (при назначении цисплатина, дактиномицина, доксорубицина).
-
Гипергидроз (при назначении цисплатина, циклофосфамида, дакарбазина, доксорубицина, метотрексата).
Аллергические реакции
Аллергические реакции различной степени тяжести возникают у 5-7% больных, получающих системную химиотерапию. Выделяют группу из четырёх цитостатиков (аспарагиназа, паклитаксел, доцетаксел и тенипозид), для которых развитие реакций гиперчувствительности типа I - наиболее характерный и дозолимитирующий вид токсичности. Значительно реже аллергические реакции возникают при назначении цисплатина, антрациклиновых антибиотиков, циклофосфамида, ифосфамида, винкаалкалоидов и ряда других препаратов.
Большинство из них носят иммунологически опосредованный характер. В то же время, для аллергических реакций немедленного типа существуют и другие механизмы возникновения: дегрануляция базофилов с высвобождением гистамина и других биологически активных веществ; активация системы комплемента по альтернативному пути. Основной медиатор анафилактических реакций - иммуноглобулин E.
В соответствии с критериями токсичности Национального Института Рака (США) выделяют четыре степени тяжести аллергических реакций.
Степени тяжести аллергических реакций
-
Лёгкая степень - преходящая сыпь на коже (крапивница), слабые проявления сенной лихорадки (аллергический ринит).
-
Умеренная степень - крапивница в сочетании с выраженным кожным зудом, умеренные проявления сенной лихорадки, повышение температуры тела до 38 °С, купирующиеся пероральным применением антигистаминных препаратов и глюкокортикоидов.
-
Тяжёлая степень - развитие бронхоспазма, отёка Квинке, гипотензии, сывороточной болезни, требующие парентерального введения лекарственных средств.
-
Крайне тяжёлая степень - развитие анафилактического шока, представляющего угрозу для жизни больного.
Характеристика отдельных препаратов
Аспарагиназа, которую назначают при лечении острого лимфобластного лейкоза, вызывает развитие аллергических реакций в 40-50% случаев, что связано с бактериальным происхождением препарата. Наиболее часто возникают острые анафилактические реакции. Клиническая картина представлена генерализованной кожной сыпью по типу крапивницы, отёком слизистых оболочек верхних дыхательных путей и ротовой полости, бронхоспазмом, возбуждением больного, снижением артериального давления, разлитого характера болями в брюшной полости.
Таксаны
Применение таксанов (паклитаксела, доцетаксела) сопровождается развитием аллергических реакций типа I у 35-40% больных, при этом частота возникновения угрожающего жизни больного анафилактического шока достигает 2%.
Острая аллергическая реакция в случае использования паклитаксела возникает в результате попадания в кровяное русло его растворителя кремофора. Высвобождение биологически активных веществ происходит в течение первых 10 мин после введения препарата. Механизм развития патологического процесса окончательно не установлен, однако высокая частота осложнений, возникающих уже при первом введении препарата, свидетельствует о его неиммунологическом характере.
Профилактика. С целью предупреждения аллергических осложнений паклитаксела необходимо придерживаться нескольких рекомендаций.
-
Необходимо соблюдать рекомендуемую продолжительность инфузии (60-180 мин).
-
Необходимо выполнять стандартный режим премедикации (назначают 10-20 мг дексаметазона перорально или внутримышечно за 13 и 7 ч, 50 мг дифенгидрамина, 50 мг ранитидина или 300 мг циметидина и 20 мг дексаметазона внутривенно, струйно за 30-60 мин до введения препарата). Премедикация не обеспечивает полной профилактики аллергических реакций, поэтому необходимо динамическое наблюдение за больным в течение 2 ч после завершения инфузии.
Схема премедикации и постмедикации разработана и для доцетаксела. Рекомендуют перорально или внутримышечно назначать дексаметазон в дозе 8-12 мг за 13 и 7 ч и 30-60 мин до инфузии препарата, затем - в дозе 8 мг через 6 и 18 ч после её завершения.
Тенипозид, реже этопозид. Они обладают способностью вызывать аллергические реакции у 6-13% больных солидными опухолями и у 30-40% больных гемобластозами и лимфопролиферативными заболеваниями. В большинстве случаев возникают аллергические реакции лёгкой степени. Они могут развиваться в течение нескольких минут или часов после введения любой дозы препарата, у трети больных уже при первом введении препаратов. Клиническая картина представлена гиперемией кожи, одышкой вследствие отёка верхних дыхательных путей или бронхоспазма, гипотензией, кожной сыпью.
Препараты платины (цисплатин, карбоплатин) могут вызывать развитие аллергических осложнений у 15-20% больных. Как правило, в течение нескольких часов после завершения инфузии возникают психомоторное возбуждение, сухой непродуктивный кашель, инспираторная одышка, тошнота, кожная сыпь, гипотензия.
Антрациклиновые антибиотики (прежде всего доксорубицин) способны запускать развитие, как правило, тяжёлых генерализованных аллергических реакций типа I, патогенез которых окончательно не установлен.
Циклофосфамид, ифосфамид, несмотря на иммуносупрессивные свойства, иногда вызывают реакции гиперчувствительности типа I, включая анафилактический шок.
Метотрексат в высоких дозах может вызывать развитие аллергических реакций типа I, а также реакций гиперчувствительности типа III, проявляющиеся васкулитом, уртикарной сыпью, пневмонитом, двусторонним плевральным выпотом, медиастинальной лимфаденопатией и эозинофилией в периферической крови.
Фторурацил, гемцитабин, иринотекан, топотекан в редких случаях вызывают развитие макулопапулёзной кожной сыпи, бронхоспазма.
Лечение
Лечебная тактика зависит от степени тяжести аллергических осложнений.
При развитии бронхоспазма и/или ангионевротического отёка верхних дыхательных путей показано проведение экстренных лечебных мероприятий, направленных на максимально быстрое устранение угрозы для жизни больного. В первую очередь, определяют проходимость дыхательных путей. При её сохранении обеспечивают дополнительную оксигенотерапию, в крайне тяжёлых случаях выполняют эндотрахеальную интубацию или трахеостомию.
Из лекарственных средств назначают эпинефрин (0,3-0,5 мг внутривенно каждые 10 мин до максимальной дозы, равной 1 мг), аэрозоли сальбутамола (при бронхоспазме), дифенгидрамин (по 25 мг внутривенно 1-2 раза), гидрокортизон (100-500 мг внутривенно) или метилпреднизолон (125 мг внутривенно). При развитии гипотонии осуществляют инфузию 0,9% раствора натрия хлорида, назначают вазопрессоры (допамин).
Развитие тяжёлой аллергической реакции - безусловное основание для прекращения дальнейшего применения вызвавшего её цитостатика. В случае умеренной выраженности осложнений повторное введение цитостатика возможно на фоне адекватной профилактики (назначение антигистаминных средств, глюкокортикоидов).
Поражения костно-мышечной системы
При противоопухолевом лечении они возникают редко. К клиническим проявлениям относят миалгии и артралгии (при назначении паклитаксела, гемцитабина, препаратов цитокинов), миастению (при длительном назначении глюкокортикоидов), судороги мышц вследствие периферической постцитостатической нейропатии.
Токсические гипертермические реакции
Наиболее характерно возникновение гипертермии при использовании блеомицина (до 60-80% наблюдений) и препаратов цитокинов (интерферон альфа, интерлейкин-2), несколько реже (до 25-30% случаев) - при введении аспарагиназы, цитарабина, флударабина, гемцитабина, доксорубицина, ритуксимаба, темозоломида, ралтитрексида, препаратов колониестимулирующих факторов. В зависимости от степени повышения температуры тела выделяют четыре степени тяжести осложнения.
Степени тяжести токсических гипертермических реакций
К токсической гипертермии можно относить и проявления гриппоподобного синдрома, включающего, помимо лихорадки, миалгии, артралгии, головную боль, общее недомогание. Наиболее часто он возникает при назначении гемцитабина, препаратов цитокинов.
С профилактической и лечебной (при лихорадке выше 37,5-38,0 °С) целью назначают жаропонижающие (парацетамол, ацетилсалициловая кислота) и антигистаминные препараты.
Бесплодие
Бесплодие у мужчин
Поскольку в последние годы значительно увеличилось число больных, излеченных от неходжкинских лимфом, лимфогранулематоза, герминогенных опухолей, появляются более полные данные, касающиеся частоты мужского бесплодия после проведенного цитостатического лечения.
По неизвестным до настоящего времени причинам, до 30% молодых мужчин, страдающих лимфомой Ходжкина, уже до начала химиотерапии имеют признаки субфертильности виде нарушение числа и морфологии сперматозоидов. Этот феномен не связан со степенью распространения опухолевого процесса и возрастом больного.
Проведение 6 циклов ПХТ по схеме МОРР приводит к развитию азооспермии практически у всех больных. В 85% случаев азооспермия имеет необратимый характер. В течение 1,5-2 лет после завершения лечения сперматогенез восстанавливается не более, чем у 10-15% больных. Схема ABVD несколько менее токсична в отношении функции гонад как у мужчин, так и у женщин. Прогноз в отношении восстановления сперматогенеза значительно ухудшается в случае проведения предшествующего или последующего облучения области малого таза или брюшной полости.
У молодых мужчин, страдающих герминогенными опухолями яичка, нарушение сперматогенеза выявляют ещё более часто, чем у больных лимфомой Ходжкина. Практически у 80% больных отмечают олигозооспермию, у 15-20% - азооспермию. После завершения трёх циклов ПХТ по схеме ВЕР азооспермия развивается у 90-95% больных. По окончании 6 циклов лечения выраженную олигоспермию выявляют в 75-100% случаев. Однако, в отличие от схемы МОРР, которую назначают при лимфоме Ходжкина, в большинстве случаев отмечают восстановление нормального сперматогенеза (у 50% больных - в течение первых 2 лет, у оставшихся - в течение 3 лет).
Циклофосфамид при достижении кумулятивной дозы, равной 9000 мг, вызывает азооспермию практически в 100% случаев. Она имеет обратимый характер. Полное восстановление нормального сперматогенеза происходит через 3-4 года после завершения лечения.
Прокарбазин, который назначают как в режиме монотерапии, так и в комбинациях, - наиболее токсичный в отношении функции гонад у мужчин цитостатик. Вызванная им олигоспермия продолжается в течение 10-12 лет.
Метотрексат, винкаалкалоиды обладают минимальным повреждающим воздействием на процесс сперматогенеза даже при длительном применении. При назначении метотрексата в высоких дозах частота возникновения олигоспермии может достигать 50%, однако она разрешается в течение 1-2 лет после завершения химиотерапии.
Доксорубицин. При проведении монотерапии для препарата характерна малая токсичность в отношении гонад у мужчин; в комбинации с циклофосфамидом частота развития различных нарушений сперматогенеза значительно возрастает, однако практически во всех наблюдениях они имеют обратимый характер. У трети больных, получавших доксорубицин, отмечают полное восстановление функции яичек.
Глюкокортикоиды, которые длительно применяют в средних дозах, вызывают, как правило, обратимое подавление сперматогенеза.
Наиболее эффективный способ сохранения жизнеспособности сперматозоидов - криоконсервация спермы, полученной до начала курса ПХТ.
Бесплодие у женщин
Поскольку биопсию яичников практически никогда не выполняют, их функциональную способность оценивают с учётом косвенных признаков, к которым относят острую или хроническую аменорею, дисменорею, уровень гормонов в плазме, фертильность и др.
Наибольший объём клинического материала накоплен в отношении комбинаций цитостатиков, используемых для лечения лимфомы Ходжкина. Частота возникновения аменореи при проведении схем МОРР или СОРР находится в пределах от 15 до 80% (в среднем, составляет около 50%). Предшествующее или последующее облучение малого таза значительно увеличивает риск снижения фертильности.
Темпы развития аменореи отчётливо связаны с возрастом больных. Так, у пациенток моложе 25 лет подавление функции яичников развивается медленно, в течение нескольких лет после завершения курса химиотерапии. У женщин более старшего возраста аменорея возникает в течение первого года и, как правило, на фоне цитостатической терапии.
Практически у всех больных, получающих схемы химиотерапии на основе препаратов платины (например, по поводу герминогенных опухолей), аменорея развивается на фоне лечения, однако более, чем у 90% пациенток менструальный цикл восстанавливается в течение ближайших месяцев.
У больных раком молочной железы, находящихся в пременопаузе и получающих комбинацию CMF, менопауза наступает в течение 8-10 мес после начала лечения. На фоне терапии комбинацией CAF развитие аменореи наблюдают в течение первых 2-3 месяцев.
С целью профилактики постцитостатической аменореи рекомендуют назначать оральные контрацептивы или агонисты рилизинг-гормонов.
ЛИТЕРАТУРА
Abraham J. Bethesda Handbook of Clinical Oncology / J. Abraham, J.L. Gulley, C.J. Allegra. - 2005.
Cella D. The effect of anemia and anemia treatment on the quality of life of people with cancer / D. Cella // Oncology. - 2002. - Vol. 16, suppl. 10. - P. 125-132.
Central Venous Catheters: care and complications in cancer chemotherapy and biotherapy: principles and practice / ed. by B.A. Chabner, D.L. Longo. - 4th ed. - Philadelphia, 2006.
CTCAE v3.0: development of a comprehensive grading system for the adverse effects of cancer treatment / A. Trotti [et al.] // Semin. Radiat. Oncol. - 2003.
Management of drug toxicity in the chemotherapy source book / ed. by M.C. Perry. - 3rd ed. - Philadelphia, 2001.
Petersen C.S. Cytostatic agents: effects on the skin, mucous membranes, hair, and nails / C.S. Petersen. - 2001.
Skeel R.T. Handbook of cancer chemotherapy / R.T. Skeel. - 2003.