Наследственные болезни : национальное руководство / Под ред. Н. П. Бочкова, Е. К. Гинтера, В. П. Пузырева - Москва : ГЭОТАР-Медиа, 2012. - 936 с. (Серия "Национальные руководства") - ISBN 978-5-9704-2231-1 |
Аннотация
Национальные руководства - первая в России серия практических руководств по основным медицинским специальностям, включающих всю основную информацию, необходимую врачу для непрерывного последипломного образования.
Национальное руководство "Наследственные болезни" содержит актуальную, современную информацию о геноме человека, общих вопросах медицинской генетики, клинической генетике. Руководство состоит из двух частей, в которых излагаются теоретические и клинические вопросы медицинской генетики. В первой части представлены новейшие данные по теоретическим вопросам медицинской генетики. Сведения об организации и функциях генома, генов и хромосом изложены в понятной для врачей форме, но без излишнего упрощения. Во второй части представлены вопросы клинической генетики, а именно методы диагностики наследственных болезней (от клинического уровня до секвенирования ДНК и РНК), принципов лечения и профилактики отдельных нозологических форм. Поскольку в национальных руководствах по другим специальностям описаны многочисленные наследственные болезни, на них можно найти ссылки [см. "Перечень наследственных болезней (синдромов), описание которых представлено в других национальных руководствах" на компакт-диске]. Приложение к руководству на компакт-диске включает более полную информацию по некоторым главам, электронную версию руководства, обширный иллюстративный материал, приложения, перечень наследственных болезней, описанных в других руководствах, фармакологический справочник. В подготовке настоящего издания в качестве авторов-составителей и рецензентов принимали участие ведущие ученые разных специальностей: генетики, иммунологи, невропатологи, фармакологи, онкологи и другие специалисты. Все рекомендации прошли этап независимого рецензирования.
Руководство предназначено для врачей-генетиков, врачей лаборантов-генетиков, врачей смежных специальностей, интернов, ординаторов, аспирантов, особенно по таким дисциплинам, как педиатрия, акушерство-гинекология, нервные болезни.
Гриф
Национальное руководство рекомендовано Российским обществом медицинских генетиков и Ассоциацией медицинских обществ по качеству
Глава 25. Врожденные пороки развития. Тератогенные синдромы
ИСТОРИЧЕСКАЯ СПРАВКА
Врожденные пороки развития (ВПР) известны с древнейших времен. До нашего времени дошли древнеегипетские (свыше 5000 лет назад) изображения больных с ахондроплазией. В вавилонской клинописи (3800-2000 лет до н.э.) перечислены 62 вида пороков развития. Изучение ВПР началось с определения закономерностей развития эмбриона. Основоположниками учения о развитии эмбриона следует считать Гиппократа (а также примыкавших к нему авторов «Гиппократовского сборника») и Аристотеля. Гиппократ и его последователи особое внимание уделяли изучению развития зародыша человека, рекомендуя для сравнения наблюдать за формированием цыпленка в яйце. Наиболее известное произведение Гиппократа, где изложены его взгляды на развитие зародыша человека, - «О семени и природе ребенка». В сочинениях Аристотеля «История животных» и «О возникновении животных» есть данные о развитии человека, млекопитающих, птиц, пресмыкающихся и рыб, а также многих беспозвоночных. Учение Аристотеля о последовательном формировании органов в эмбриогенезе связано с эпигенетическими представлениями. Он критиковал взгляды некоторых исследователей о существовании в отцовском или материнском семени всех частей будущего плода (теория преформизма). Эмбриологические воззрения Аристотеля сохранялись в течение всего Средневековья, вплоть до XVI в., без существенных изменений. В период возрождения сформировалась наука эмбриология.
В России начало изучению пороков развития было положено указом Петра I о создании в Петербурге Музея «уродливостей». В 1717 г. Петр I купил у знаменитого голландского анатома Ф. Рюйша уникальную коллекцию анатомических препаратов: более 1000 предметов, как он выразился, «для своей забавы и услады». Затем Петр I сам стал собирать разные курьезы природы, позднее они стали экспонатами Кунсткамеры, которая вначале помещалась в одном из зданий при Академии наук.
Существенный сдвиг в развитии эмбриологии произошел в середине XVII в., когда появилось сочинение У. Гарвея «Исследования о зарождении животных» (1651), материалом для которого послужило изучение развития цыпленка и млекопитающих. Основатель современной эмбриологии К.М. Бэр открыл и описал в 1827 г. яйцо в яичнике млекопитающих животных и человека. В классическом труде «История развития животных» К.М. Бэр впервые детально описал главные черты эмбриогенеза ряда позвоночных. Он развил понятие о зародышевых листках как основных эмбриональных органах и проследил их дальнейшую судьбу. Сравнительные наблюдения над эмбриональным развитием птиц, млекопитающих, пресмыкающихся, земноводных и рыб привели К.М. Бэра к теоретическим заключениям, важнейшим из которых является закон сходства зародышей разных классов позвоночных, что было подтверждено исследованиями А.О. Ковалевского и является убедительным доказательством правильности теории Ч. Дарвина.
Основоположником генетики развития, или феногенетики, стал немецкий зоолог и генетик В. Хеккер (V. Hecker), который предложил термин «феногенетика» в 1918 г. Феногенетика - раздел генетики, изучающий пути реализации наследственной информации в процессе индивидуального развития организма. Основным принципом феногенетики он считал установление фенокритических фаз, т.е. выявление тех этапов развития, начиная с которых можно обнаружить различия между нормальными и мутантными особями. По характеру таких различий можно судить о месте и механизме действия исследуемых генов.
Важным этапом в развитии феногенетики стало изучение закономерностей проявления генов, контролирующих морфологические признаки. Для количественной и качественной характеристики изменчивости проявления таких генов были введены понятия «пенетрантность», «экспрессивность» (Тимофеев-Ресовский, 1927) и область действия гена (Рокицкий, 1929).
Задача современной феногенетики - изучение генетических механизмов оплодотворения, дробления, образования зародышевых листков, органогенеза, гистогенеза, значения провизорных органов и различных проявлений патологического развития. Много исследований посвящено стимуляции развития организма химическими агентами, выявлению движущих сил эмбриогенеза, поискам генетических и цитологических основ дифференцировки клеток. В настоящее время наряду с эмбриологией в отдельную самостоятельную науку выделена тератология - учение о врожденных пороках развития.
ВРОЖДЕННЫЕ ПОРОКИ РАЗВИТИЯ
Знание генетики развития, включая механизмы, ответственные за нормальное развитие эмбриона и плода, важно для практикующих врачей, разрабатывающих рациональные методы диагностики и лечения врожденных дефектов. ВПР представляют значительную проблему для здравоохранения, так как они вносят существенный вклад в структуру детской смертности (15-20%), перинатальной смертности (25-30%), младенческой смертности (25%). Частота ВПР среди новорожденных составляет 2-3%, пороков, выявляемых в более поздние сроки - до 5%.
Механизмы эмбрионального развития ВПР возникают внутриутробно в результате нарушений эмбрионального развития. Эмбриональное (внутриутробное) развитие человека длится примерно 265-270 дней. В течение этого времени из одной оплодотворенной яйцеклетки образуется более 200 млн клеток, несколько сотен четко различающихся типов клеток и десятки тканей, а размер эмбриона увеличивается от микроскопического до полуметрового. Этот процесс должен происходить надежным и предсказуемым образом и в определенные временные рамки. Развитие определяется действием продуктов генов, взаимодействующих с клеточным и средовым окружением. Продукты генов включают регуляторы транскрипции, факторы диффузии и другие белки, направляющие клетки по специфическим путям развития.
В целом развитие человеческого эмбриона условно можно разделить на три стадии. Первая стадия - это период от оплодотворения яйцеклетки до конца 2-й недели внутриутробной жизни, когда развивающийся зародыш внедряется в стенку матки и начинает получать питание от матери. После имплантации происходит гаструляция, зародыш в эту фазу состоит из трех групп клеток (эктодермы, мезодермы, энтодермы), называемых первичными эмбриональными листками. Три эмбриональных листка формируют разные структуры. Клетки энтодермального происхождения формируют внутреннюю выстилку органов (клетки стенок кишечника, дыхательных путей и др.). Мезодермальное происхождение имеют почки, сердце, сосуды, кости, мышцы и др. Из эктодермы формируются ЦНС, периферическая нервная система и кожа. Вторая стадия длится с 3-й до конца 8-й недели. В течение этого времени формируются все основные органы и эмбрион приобретает черты человеческого организма. По окончании второй стадии развития он уже называется плодом. Протяженность третьей стадии, называемой иногда фетальной (от лат. fetus - плод), - от 3-го месяца до рождения. На этой заключительной стадии происходят созревание и дальнейшая дифференцировка органов, и плод постепенно приобретает способность существовать самостоятельно. Однако для некоторых систем органов развитие не прекращается и после рождения ребенка. Например, мозг подвергается значительному развитию после рождения, а конечности продолжают эпифизарный рост, заканчивающийся только к 18-20 годам. На рис. 25-1 представлено развитие зародыша человека.
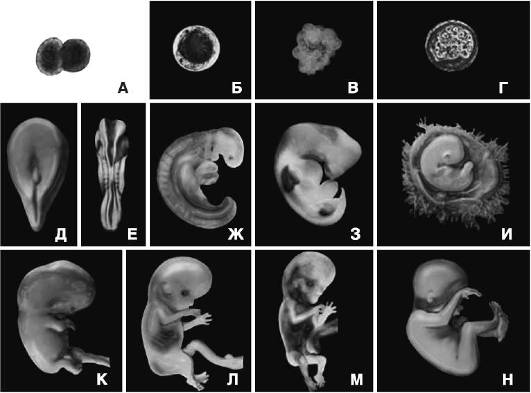
Рис. 25-1. Развитие человеческого эмбриона: А-Г - деление оплодотворенной яйцеклетки и образование бластулы; Д-Е - формирование центральной нервной системы; Ж-З - появление временного хвоста, формирование зачатков конечностей, развитие печени и сердца; И - эмбрион в зародышевом листке; К - плод на 8-й неделе развития; Л-Н - дальнейшее развитие плода вплоть дo рождения.
В ходе развития плода сильно изменяются не только его размеры и масса, но и пропорции тела. Например, у двухмесячного плода голова составляет почти половину длины тела. В оставшиеся месяцы она растет медленнее, так что к моменту рождения составляет только четверть длины тела. Шея и конечности становятся длиннее, при этом ноги растут быстрее, чем руки. Другие внешние изменения связаны с развитием наружных половых органов, ростом волос и ногтей. Кожа становится более гладкой из-за развития подкожной жировой клетчатки. Одно из наиболее значительных внутренних изменений связано с заменой хряща костными клетками в процессе становления скелета. Отростки многих нервных клеток покрываются миелином (белково-липидным комплексом). Процесс миелинизации наряду с формированием связей между нервами и мышцами приводит к увеличению подвижности плода в матке. К 7-му месяцу плод полностью покрывается первородной смазкой, которая исчезает после рождения.
Классификация врожденных пороков развития В Международной классификации болезней применяются термины «врожденная аномалия» (congenital anomaly) или «врожденный дефект» (birth defect). По содержанию они включают в себя обширный круг патологических состояний:
Врожденные пороки развития в узком смысле слова (congenital abnormalities) - это стойкие морфологические изменения органа или всего организма, выходящие за пределы вариаций их строения. Более полное определение звучит так: врожденный порок развития - это патологическое состояние, которое представляет собой стойкий структурный или морфологический дефект органа или его части, возникающий внутриутробно и нарушающий функцию пораженного органа.
Выделяют следующие типы пороков развития.
Мальформация (malformation) - морфологический дефект органа, части органа или большого участка тела в результате внутреннего нарушения процесса развития (генетические факторы). Примерами могут служить симптомы практически всех наследственных синдромов. Так, образование дополнительных пальцев при цефалополисиндактилии Грейга вызвано мутацией в гене фактора транскрипции GLI3, одного из компонентов сложной сети взаимодействующих факторов транскрипции и сигнальных молекул.
Дизрупция (disruption) - морфологический дефект органа, части органа или большого участка тела в результате внешнего препятствия или воздействия на изначально нормальный процесс развития. Дизрупции могут быть результатом нарушения имплантации, сосудистой недостаточности или действия тератогенных факторов. Одним из примеров могут быть амниотические перетяжки.
Деформация (deformation) - нарушение формы, вида или положения части тела, обусловленное механическими воздействиями со стороны матери (маловодие , миома и др.). Они особенно часто встречаются во II триместре беременности, когда плод сдавливается амниотической оболочкой или маткой. Например, сдавление плода при многоплодной беременности сопровождается деформацией суставов конечностей.
Дисплазия (displasia) - нарушенная организация клеток в тканях и ее морфологический результат (процесс и следствие дисгистогенеза). Примерами этого морфологического дефекта могут быть различные нарушения соединительной ткани.
Схематически эти варианты ВПР представлены на рис. 25-2.
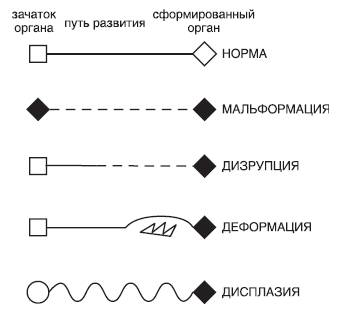
Рис. 25-2. Схема разных типов ошибок морфогенеза
Проявления врожденных пороков развития различной этиологии могут перекрываться. Например, порок развития сосудов может привести к дизрупции дистальных структур и пороку развития мочеполовой системы, в свою очередь вызывающему маловодие, приводящее к деформациям у плода.
Классификация ВПР в зависимости от частоты встречаемости:
Частота всех ВПР - 600 на 10 000 живорожденных (6%).
Классификация по тяжести проявления ВПР:
Классификация по проявлению ВПР:
Классификация по этиологии ВПР:
В зависимости от стадии пренатального онтогенеза, на которой начинает формироваться патология, различают гаметопатии, бластопатии, эмбриопатии и фетопатии.
Гаметопатии связаны с возникновением (или наличием) мутаций в половых клетках родителей. Основное содержание гаметогенеза заключается в кодировании морфогенетической информации, в процессе реализации которой из зиготы развивается многоклеточный организм. Примерами гаметопатий являются наследственные синдромы.
Бластопатии - поражение бластоцисты (зародыша первых 15 дней после оплодотворения). Бластогенез обозначают как первый критический период, когда на зародыш действуют правила закона «все или ничего». Первые деления зародыша осуществляются за счет генетической информации, полученной ооцитом еще в период гаметогенеза. Зародыш человека обладает достаточным запасом белков, рибонуклеопротеиновых комплексов, необходимых для синтеза новых белков, а также питательных веществ и энергетических ресурсов, полученных от матери. Переключение индивидуальной генетической программы с материнской ДНК и РНК на геном зародыша происходит постепенно. Этот процесс начинается со стадии 4-8 бластомеров. Следствием бластопатий могут являться двойниковые пороки, циклопия , сиреномелия . Возможно, что определенная часть моносомий и трисомий также является следствием бластопатий.
Эмбриопатии - поражение эмбриона (зародыша от 16-го дня до конца 8-й недели). Эмбриональный морфогенез включает гистогенез и органогенез, которые представлены в основном процессами размножения, миграции, дифференцировки и апоптоза клеток. Эти процессы контролируются сложным взаимодействием генетических, эпигеномных и внешних факторов, определяющих временную и пространственную последовательность экспрессии генов. «Включение» одних и «выключение» других генов происходит на протяжении всего эмбриогенеза. Нарушение любого механизма влечет за собой отклонение от нормального развития и может реализоваться во врожденные пороки развития. Нарушение размножения клеток (снижение митотической активности) ведет к торможению пролиферативной активности клеток и даже к ее полной остановке. Например, гипоплазия или аплазия органа, дизрафии (расщелина губы и/или нёба, дефекты невральной трубки). Нарушение миграции клеток приводит к гетеротопии, агенезии органа и другим порокам.
Программируемое перемещение клеток играет основную роль в развитии ЦНС, которая возникает из нервной трубки (цилиндра клеток, формирующегося в течение первых 4-5 нед эмбриогенеза). ЦНС строится волнами миграции клеток - предшественниц нейронов. Нейроны, заполняющие внутренние слои коры мозга, начинают мигрировать на более ранних стадиях развития, и каждая последующая волна нейронов, формируя очередной внешний слой, проходит через ранее заполненные внутренние слои. При наличии мутации в одной из копий гена LIS1 при синдроме Миллера-Дикера волны миграции кортикальных нейронов не происходят. В результате образуется плотная кора мозга с большим количеством клеток и плохо сформированными извилинами, что делает поверхность мозга гладкой (лиссэнцефалия ). Дифференцировка клеток, происходящая в течение всего эмбриогенеза, может прекратиться на любом этапе развития, что повлечет за собой рост бесформенной массы недифференцированных клеток (ранние абортусы), агенезию или морфологическую незрелость органа, персистирование (сохранение) эмбриональных структур. Апоптоз - программируемая смерть клеток. Она происходит везде, где ткани должны перестраиваться в ходе морфогенеза, например при разделении пальцев, перфорации анальной мембраны, при создании сообщения между маткой и влагалищем. В основе некоторых форм врожденных заболеваний сердца также лежат дефекты апоптоза.
В сложном процессе эмбрионального развития принимают участие не только взаимодействующие между собой гены и их комплексы, но и среда, в которой эти наследственные факторы должны реализоваться. Такая пренатальная (внутренняя) среда формируется организмом матери и, естественно, зависит как от ее здоровья и питания, так и от воздействия на организм матери и плода факторов (химических, физических и др.) внешней среды. Более того, и в развивающемся зародыше создается определенная среда, которая может оказать модифицирующее действие на реализацию нормального или мутантного гена. Например, хорошо известны различия в пренатальном развитии генетически идентичных монозиготных близнецов, имеющих различную площадь бассейна плацентарного кровообращения. Точно так же определяются различия при ряде наследственно обусловленных пороков развития мочевой системы (двусторонние арении, атрезии уретры, тяжелые формы инфантильного поликистоза), связанных со значительным изменением условий развития зародыша. Подавляющее большинство ВПР, независимо от этиологии, образуется в этот период.
Фетопатии - повреждение плода в период от 9 нед до окончания беременности. ВПР этой группы сравнительно редки, так как они формируются после завершения основных процессов органогенеза. Обычно это персистирование эмбриональных структур: урахус, очажки метанефрогенной бластемы в почках, сохранение первоначального расположения органов (например, крипторхизм , тазовая почка), пороки, вызванные сахарным диабетом матери, и другие метаболические фетопатии.
Генетика врожденных пороков развития Из всего вышесказанного ясно, что ВПР - это гетерогенная группа аномалий развития, к возникновению которых приводят как генетические нарушения, так и неблагоприятные факторы внешней среды. В ходе внутриутробного развития целый комплекс генов последовательно включается в работу, обеспечивая сложные процессы дифференцировки тканей. Таким образом, сбой механизма на любом этапе внутриутробного развития может привести к формированию ВПР различной степени тяжести. Действие генов, контролирующих морфогенез и раннее развитие зародыша человека, изучено недостаточно. Однако в настоящее время идентифицированы многие гены и генные семейства, которые играют важную роль в раннем периоде развития. Одним из представителей семейства эмбриональных транскрипционных генов являются гомеобоксные гены (Hox). Продукты этих генов - транскрипционные факторы осевой дифференцировки эмбриона. Вероятно, любые мутации этих генов приводят к гибели эмбриона, однако известно, что белки группы Hox обладают выраженной гомологией, это расширяет компенсаторные возможности. У человека 40 генов Hox организованы в четыре группы: A, B, C и D - в четырех разных хромосомах. На ранних этапах развития эмбриона факторы транскрипции генов Hox определяют переднезаднюю ось: группы Hox А и Hox В, например, действуют вдоль рострально-каудальной оси, определяя последовательную дифференцировку сомитов. На последних этапах развития группы Hox А и Hox D определяют последовательную детерминацию локальных структур вдоль оси развивающейся конечности. Таким образом, семейство генов Hox выполняет аналогичные общие задачи в разное время и в разных частях эмбриона.
Морфогенетический белок SHH экспрессируется в раннем эмбриогенезе. Результатом его действия является активация экспрессии генов группы PAX . Спаренные гены РАХ представлены восемью генами. Мутации в гене РАХЗ приводят к развитию синдрома Варденбурга (аутосомно-доминантный тип наследования) (глухота, гетерохромия радужки, белая прядь волос надо лбом), мутации в гене РАХ6 - к аниридии (отсутствию радужной оболочки).
Транскрипционные факторы семейства SOX обнаружены в спинном и головном мозге плода, но более детально их функция еще не изучена, хотя известны места их локализации: SOX2 - в хр. 3, SOX3 - в хр. 10, SOX4 - в хр. 6. Описан ген SOX9 (хр. 17), мутации в котором ведут к камптомелической дисплазии.
Таким образом, большинство генов эмбрионального развития ответственны за выработку белков, называемых транскрипционными факторами, которые могут активизировать или подавлять экспрессию генов, участвующих в координации таких эмбриогенетических процессов, как сегментация, индукция, миграция, дифференцировка клеток, апоптоз. Эти процессы, очевидно, определяются факторами роста, клеточными рецепторами и др. Мутации в определенных локусах могут нарушать процесс морфогенеза в эмбриональном и постэмбриональном развитии.
Суммарный вклад наследственных факторов в период раннего развития зародыша человека составляет примерно 20% всего генома. По литературным данным, не более 5-10% всех генов активны в каждую стадию развития, остальные остаются репрессированными. На первых стадиях развития после формирования бластоцисты происходит преимущественно экспрессия тканеспецифических генов; в стадии органогенеза активизируются органоспецифические гены; к началу функционирования органов экспрессируются гены, регулирующие специфические функции специализированных клеток. Таким образом, гены, контролирующие раннее развитие, функционируют лишь на определенной стадии до достижения клетками или тканями определенных этапов дифференцировки. Нарушение любой из стадий этого процесса может привести к нарушению или прекращению дальнейшего развития зародыша.
Типы связей между врожденными пороками развития Возникновение множественных ВПР у больного может быть обусловлено различными причинами. Они могут выражать этиологическую или патогенетическую связь, а могут представлять случайные сочетания. Исходя из уровня наших знаний о причинах и механизмах их возникновения, в настоящее время для выражения типа связи существуют следующие понятия.
Синдром - комплекс множественных пороков и аномалий развития, этиологически и патогенетически связанных между собой. Это устойчивое сочетание двух и более не индуцированных друг другом пороков развития в разных системах органов. Примеры: синдром Дауна, синдром Марфана, синдром Тричера-Коллинза, синдром Смита-Лемли-Опитца и другие наследственные синдромы (всего более 4000 нозологических единиц). В основе формирования синдрома лежит плейотропное (множественное) действие гена. Например, синдром бранхио-оторенальной дисплазии состоит из аномалий развития улитки и наружного уха, кист и фистул шеи, дисплазии почек и порока развития мочевыводящей системы. Этот синдром вызван мутацией в гене EYA1, кодирующем белок с функцией фосфатазы, которая также участвует в развитии слухового аппарата и почек.
Следствие (синонимы аномалад, вторичный порок) - комплекс пороков развития, возникающий в результате действия одного врожденного порока или физического фактора, который вызывает каскад вторичных нарушений, т.е. связь между пороками патогенетическая, а этиология их может быть различной. Примеры: миеломенингоцеле приводит к парезу нижних конечностей, атрофии мышц, косолапости, поражению почек. Маловодие приводит к аномалии Поттера (причины маловодия могут быть различными). Аномалия Робена развивается вследствие ограничения роста нижней челюсти до 9-й недели беременности, что заставляет язык лежать больше кзади, чем в норме, создавая помехи нормальному закрытию нёбных пластинок, вызывая расщелину нёба.
Ассоциации - неслучайное сочетание нескольких пороков и аномалий развития, не известных как синдром или следствие. Тип связи статистический, т.е. этиологически и патогенетически эти пороки не связаны между собой. Причины возникновения таких комплексов неизвестны.
Примеры
VACTERL-ассоциация: дефекты позвоночника (V), атрезия ануса (A), аномалии развития сердца (C), трахеопищеводная фистула (TE), аномалия развития почек и/или лучевых костей (R), дефекты конечностей (L). В связи с тем что подавляющее большинство новорожденных с этими признаками рождаются от матерей, больных сахарным диабетом, появился термин «синдром VACTERL-ассоциация».
CHARGE-ассоциация: колобома глаз (C), порок сердца (H), атрезия хоан (A), отставание в росте и развитии (R), гипогонадизм (G), аномалии ушей и/или глухота (E).
MURCS-ассоциация: аплазия мюллерова протока (MU), почечные аплазии (R), дефект шейно-грудных сегментов С5-Т1 (C), отсутствие влагалища и матки (S).
Таким образом, приведенные выше примеры иллюстрируют положение о том, что клиническая практика дисморфологии базируется на научном фундаменте биологии развития, знаниях о функциях генов, нарушающих нормальное развитие, и их взаимодействии с другими генами и с окружающей средой.
Тератогенные синдромы
Тератология - область медицины, изучающая причины происхождения, механизмы формирования и проявления различных нарушений роста и развития плода. Эти нарушения могут проявляться как сразу, так и через некоторое время после рождения. Важнейшим разделом этой науки является медицинская тератология, которая уделяет основное внимание клиническим проявлениям, вопросам диагностики этих состояний, разработке методов их лечения и профилактики. По статистике примерно 30% всей патологии человека приходится дифференцировать между наследственными и ненаследственными заболеваниями, которые могут быть обусловлены тератогенными воздействиями. Тератология представляет интерес и для биологии развития, так как отклонения и период их возникновения под влиянием тератогенов или мутагенов служат одним из способов познания контролирующих механизмов нормального развития человека.
Тератогенезом называют возникновение пороков развития у плода под влиянием вредных факторов (радиация, химические, лекарственные вещества, инфекции). Вредные факторы, вызывающие аномальное развитие плода, называются тератогенами. Тератогенным считается такое влияние, которое приводит к пороку развития эмбриона или плода, нормально развивавшегося до этого воздействия.
Тератогенные факторы можно разделить на отдельные группы:
-
заболевания матери, например метаболические нарушения (фенилкетонурия, сахарный диабет, токсикоз беременности);
-
инфекционные агенты, особенно острые инфекционные заболевания (краснуха, цитомегаловирусная инфекция, герпетическая инфекция и др.) и хронические инфекции (токсоплазмоз, сифилис и др.);
-
различные лекарственные средства (противосудорожные, гормональные и другие препараты, применяемые во время беременности);
-
физические факторы (высокая температура производственных помещений, шум, пыль, повышенная физическая нагрузка, вынужденное положение тела, ионизирующее излучение);
-
вредные привычки матери и окружающих (курение, употребление алкоголя, наркомания, токсикомания).
Влияние некоторых тератогенных факторов, например лекарственных препаратов, можно предсказать экспериментально. Для других факторов такие исследования в отношении человека в принципе невозможны, об их тератогенном эффекте возможно судить лишь постфактум. Так было выявлено, что, например, прием талидомидаρ вызывал ВПР не у всех детей, матери которых принимали этот препарат. Для одних эмбрионов действие талидомида прошло совершенно бесследно, а у других сформировались тяжелые врожденные аномалии. Впервые частичный ответ на эти вопросы нашел русский ботаник П.И. Броун. Работая с сеянцами злаков, всходами картофеля и некоторыми другими растениями, он пришел к выводу, что в развитии растений существуют периоды, когда организм более или менее стоек к действию различных внешних агентов, и периоды, когда чувствительность к тем же агентам значительно повышается. Периоды, в которых чувствительность к тератогенным факторам была повышена, он назвал критическими. В 1921 г. Ц. Стоккард предложил различать такие критические периоды и в развитии животных. Индивидуальное развитие, по мнению Ц. Стоккарда, представляет собой ряд последовательных этапов, различающихся скоростью развития органов или их систем. Наибольшая скорость развития наблюдается в критические (узловые) периоды эмбриогенеза, такие как имплантация, образование плаценты, период активного органогенеза.
На ранних стадиях эмбриогенеза критические периоды относятся к развитию всего организма; позднее они выявляются в развитии отдельных органов или систем, которые в данный момент претерпевают наиболее активные формообразовательные процессы. Внешние факторы, к которым организм (или отдельный орган) чувствителен в определенные периоды, могут существенным образом влиять на его развитие. Причем различные факторы, действующие в одном и том же периоде, могут вызывать сходные отклонения. И наоборот, один и тот же фактор, действующий на различных этапах, вызывает разные изменения. Ц. Стоккардом были сформулированы три основные положения тератогенеза:
Результаты классических исследований эмбриолога П.Г. Светлова (1960) указали на два критических периода в развитии плацентарных млекопитающих, связанных с периодами имплантации и плацентации. Однако в процессе закладки каждого органа также существуют особо чувствительные периоды, когда воздействие неблагоприятных факторов среды может вызвать то или иное отклонение в его развитии. В критические периоды эмбрион или плод становится высокочувствительным к действию внешних факторов. Аномалии развития возникают при этом в силу того, что регуляторная морфогенетическая функция органов и систем плода в эти периоды может быть ослаблена. Непосредственной причиной аномалии может послужить либо остановка развития той или иной системы организма в критический период, либо нарушение скорости компенсаторных ответных реакций систем развивающегося плода. Краткосрочное возрастание чувствительности в эти периоды эмбриологи объясняют тем, что именно в данные моменты в зародыше происходят важнейшие формообразовательные процессы, определяющие судьбу зачатков отдельных органов или зародыша в целом. Например, первые деления зиготы, имплантация, плацентация, начало образования нервной системы или закладка других крупных систем органов (рис. 25-3).
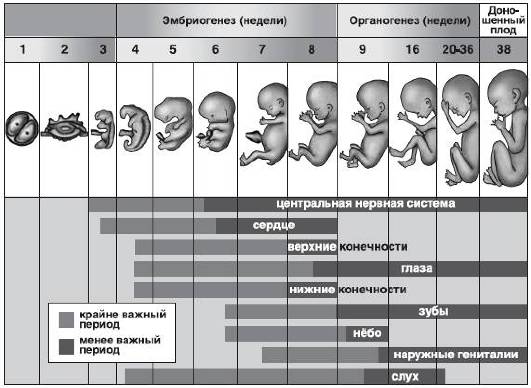
Рис. 25-3. Критические периоды эмбриогенеза человека (в неделях)
Таким образом, в настоящее время принято считать, что:
-
эмбрион более чувствителен к внешним воздействиям, чем взрослый организм;
-
на протяжении всей беременности восприимчивость зародыша к действию тератогенных факторов различна, на одних сроках беременности действие тератогена может быть максимальным и вызывать гибель зародыша или формирование анатомических дефектов, на других - оно может быть минимальным или отсутствовать совсем;
-
на ранних этапах развития тератогенные эффекты зачатков различных органов зародыша представлены в большей степени анатомическими дефектами (ВПР), на более поздних сроках сравнительно возрастает частота функциональных нарушений органов и систем. Согласно современным представлениям, тератогены, действующие в периоды раннего эмбрионального развития, приводят либо к гибели зародыша, либо к аномалиям его строения.
Антенатальная гибель плода, вызванная нарушениями внутриутробного развития, по некоторым данным, достигает 70%, т.е. из каждых десяти зачатий семь заканчиваются смертью зародыша. Большинство зародышей гибнет в первые дни своего существования в связи с патологией первых делений зиготы и нарушением имплантации. ВПР возникают главным образом в период органогенеза - когда, согласно теории критических периодов, зачатки органов наиболее активно развиваются (когда происходят процессы дифференциации, миграции клеток, устанавливаются их форма, соотношения частей). Органогенез заканчивается примерно к началу 3-го месяца беременности. Последующие месяцы также чрезвычайно важны для нормального развития плода. Тератогенные воздействия в плодном периоде приводят к различным функциональным отклонениям, в том числе к нарушениям обмена веществ и другим нарушениям, не носящим выраженный анатомический характер. Более того, крайне важным является и период гаметогенеза, предшествующий эмбриогенезу и фетальному периоду. Формирующиеся гаметы легко подвергаются патологическим воздействиям.
Таким образом, нормальное эмбриональное развитие возможно лишь при оптимальном сочетании внутренних и внешних условий. Каждая последующая стадия развития эмбриона или плода связана с предыдущей и зависит от действующих в данный момент условий развития. Если какого-либо внешнего или внутреннего условия недостаточно или возникает необычный внешний фактор, способный повлиять на ход развития плода, эмбриогенез может отклониться от нормального пути.
Патогенетические механизмы формирования врожденных пороков развития и функциональных нарушений под воздействием тератогенов
Известно, что выраженность тератогенного воздействия зависит от:
Как было сказано выше, число и спектр возникающих ВПР зависят от срока беременности (от стадии развития зародыша). В соответствии с современными представлениями биологии развития в каждой клетке зародыша подавляющая часть генетической информации, закодированной в ДНК, находится в неактивном состоянии. Экспрессируют лишь те гены, белковые продукты которых в данный момент нужны клетке для выполнения определенных функций. Таким образом, начало образования новых для зародыша систем органов связано с реализацией новых объемов генетической информации. Процессы активного органогенеза и гистогенеза неразрывно связаны со способностью группы клеток воспринимать внешние по отношению к ней сигналы, которые исходят от других клеток. Эти сигналы необходимы для возникновения качественных различий между частями развивающегося организма.
Однако клетка может получить «неправильный» сигнал, который нарушит нормальный ход событий. Клетки могут воспринять его, поскольку еще недостаточно дифференцированы для того, чтобы принимать сигналы и отвечать на них избирательно. Но даже если они такой сигнал и различают, то не могут ему противостоять, если действие внешнего фактора превышает некий физиологический порог (физиологическую норму). Таким образом, начинает формироваться ВПР.
Возникновение дефектов в закладке того или иного органа будет зависеть от сродства этих клеток к конкретному альтерирующему (от лат. alteratio - изменение) фактору, т.е., например, клетки нервной системы должны иметь сродство к сигналу конкретного тератогена, к которому клетки, например, сердечной мышцы такой чувствительности не имеют. В таких случаях у зародыша поражаются не все закладки, а только те, которые воспринимают сигнал этого тератогена. Критические периоды в таком случае не будут совпадать по времени. Для некоторых альтерирующих факторов характерен широкий спектр тератогенного действия. В результате происходит поражение всех зачатков органов и тканей, находящихся в это время в стадии активного формирования. Примером такого воздействия может служить эмбриотоксическое действие тератогенов, приводящее к гибели зародыша.
В зависимости от того, на какой стадии закладки органов клетки получат альтерирующий сигнал, сродством к которому они обладают, будет поражен тот или иной орган и сформируется соответственно порок определенной системы. Например, сигнал, влияющий на процесс закрытия нервной трубки, поступивший к клеткам в период формирования нервной системы, приведет к анатомическим дефектам нервной системы. Однако если этот же сигнал поступит к зародышу после смыкания нервных валиков, то анатомического дефекта не будет, но тератогенное воздействие может привести к функциональным нарушениям системы.
Известны варианты, когда альтерирующие факторы вызывали различные аномалии развития в зависимости от периода воздействия тератогена. Например, для талидомида определены такие критические периоды:
-
применение этого вещества на 21-22-й день беременности приводит к недоразвитию или полному отсутствию ушей и параличу черепно-мозговых нервов;
-
прием талидомида на 24-27-й день вызывает максимальную фокомелию рук, а еще через 2 дня - ног;
-
34-36-дневный зародыш отреагирует на талидомид недоразвитием пальцев и сужением некоторых отделов кишечника.
При длительном приеме лекарства беременной у зародыша могут возникнуть все эти аномалии. Если же талидомид применялся изредка, от случая к случаю, то ребенок приобретет лишь отдельные «талидомидные» пороки: пострадают органы, морфогенез которых по времени совпал с употреблением препарата.
На поздних сроках беременности, как отмечалось выше, плод иначе реагирует на тератогены. Анатомические aномалии у плода в это время не возникают, а альтернирующее воздействие приводит к возникновению функциональных нарушений.
Механизмы проникновения тератогена к формирующемуся органу (маршруты тератогена) разные. Пути эти определяются природой воздействующего фактора. Существуют две возможности поступления тератогенных агентов к развивающемуся организму.
Прямой путь, т.е. в обход материнского организма (например, ионизирующая радиация, микроволны, ультразвук). В этом случае альтерирующий сигнал не изменяется качественно. При прохождении через организм матери может незначительно снизиться лишь интенсивность, но не количество. Таким образом, тератогенный эффект зависит непосредственно от агента и от состояния зародыша, а состояние материнского организма играет незначительную роль.
Непрямой путь (например, тепло, холод). Действие таких тератогенных факторов будет вначале компенсироваться специальными механизмами поддержания постоянства внутренней среды, т.е. механизмами, противодействующими такому влиянию в организме матери.
Еще более сложные механизмы формирования тератогенных эффектов характерны для химических агентов.
В большинстве случаев возникает прямая пропорциональная зависимость выраженности тератогенного эффекта от дозы и продолжительности воздействия тератогена. Однако этот принцип справедлив не для всех тератогенов. Один и тот же тератоген может проявлять на начальных сроках беременности только эмбриотоксическую активность, позднее - как эмбриотоксическую, так и тератогенную, причем иногда при очень небольшом изменении дозы. Например, актиномицин Д вызывает гибель у одних эмбрионов практически в той же концентрации, при которой у других наблюдается возникновение ВПР. В ряде экспериментов с заведомыми тератогенами показано, что увеличение дозы в несколько раз вовсе не обязательно вызывает пропорциональное возрастание числа зародышей с ВПР. В то же время иногда возрастание концентрации тератогена лишь вдвое может привести к изменению эффекта от минимального до максимального. Примером может служить клинический полиморфизм фетального алкогольного синдрома. Дети матерей, принимавших во время беременности от 100 до 200 мл алкоголя ежедневно на протяжении всей беременности, могут иметь как функциональные изменения нервной системы, так и задержку физического развития, не всегда сочетающуюся с ВПР. Кроме того, выявлено, что только у 6% женщин, злоупотреблявших алкоголем во время беременности, дети имеют те или иные признаки истинного синдрома алкогольного плода. Такой феномен до конца не ясен, однако изучение этой проблемы позволяет определить пороговые дозы тератогена - предельную концентрацию, ниже которой он не будет вызывать уродства или гибель зародыша.
Показано, что некоторые тератогены являются еще и мутагенами, т.е. вызывают изменения в наследственном аппарате клеток. При этом иногда особенно страдают формирующиеся половые клетки. Иными словами, неблагоприятный эффект оказывается отсроченным, он проявляется лишь в следующем поколении. Для мутагенов пороговых доз не существует: достаточно вызвать нарушения в одной клетке, и аналогичные нарушения в результате делений измененной клетки будут скопированы в очень широких пределах. Пока точно неизвестно, все ли тератогены обладают подобными свойствами. В случае выявления мутагенной активности у агента необходимо говорить о полном его устранении.
При формировании некоторых врожденных пороков развития существенную роль может сыграть генетическая предрасположенность. Так, например, введение кортизона вызывает незаращение нёба у некоторых видов лабораторных мышей, в то время как у крыс и человека не описано такого эффекта данного препарата. Достоверно известно, что риск возникновения расщелины нёба повышается у плода курящей женщины. Проведенные исследования показали, что величина этого риска еще более возрастает у курящих женщин, которые являются носительницами определенных полиморфизмов в генах факторов роста. Еще одним примером может являться повышенный риск развития аминогликозидиндуцированной тугоухости у детей, матери которых имеют определенную мутацию митохондриального генома.
Таким образом, тератогенез подчиняется следующим основным принципам:
-
основное воздействие тератогена происходит в критический период;
-
воздействие тератогена может быть как прямым (на организм эмбриона или плода), так и опосредованным через организм матери (мутации половых клеток, хроническая гипоксия плода);
-
воздействие одного тератогена вызывает подобные типы аномалий у различных особей одного вида;
-
большинство изученных тератогенных агентов имеют специфические тканимишени и формируют хорошо идентифицируемые дефекты, характерные для каждого тератогена.
В настоящее время известны общие характерные признаки действия различных тератогенов, такие как бесплодие и выкидыши (гибель зародыша), пренатальный дефицит роста плода, нарушения морфогенеза (врожденные аномалии), нарушение развития и функции ЦНС. Поскольку молекулярные и клеточные пути, используемые в ходе развития, часто уникальны и не используются после созревания, тератогены, вызывающие тяжелые врожденные пороки, могут не иметь побочных эффектов у взрослых людей.
Выделяют три группы факторов тератогенного воздействия: инфекционные, физические и химические. Для инфекционных факторов тератогенного действия имеются общие характерные признаки: смерть плода (выкидыши), врожденные пороки развития (дизрупции), прямая инфекция плода.
Характеристики наиболее распространенных тератогенов и описание тератогенных эффектов представлены в табл. 25-1-25-3.
Таблица 25-1. Характеристики наиболее распространенных тератогенов инфекционной природы
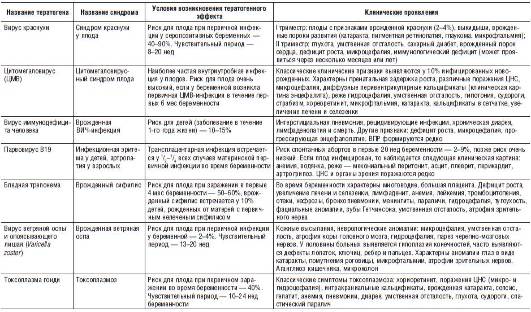
Таблица 25-2. Характеристики наиболее распространенных тератогенов физической природы

Таблица 25-3. Характеристики наиболее распространенных тератогенов химической природы
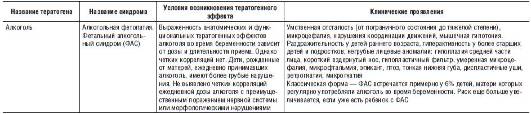
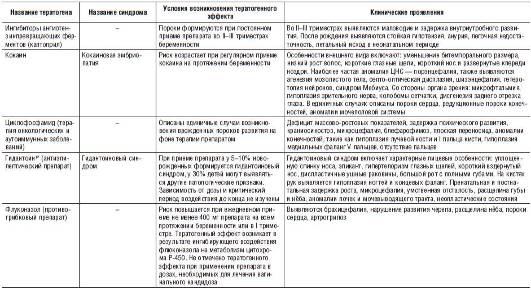
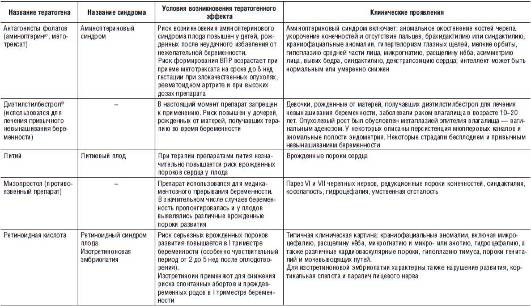
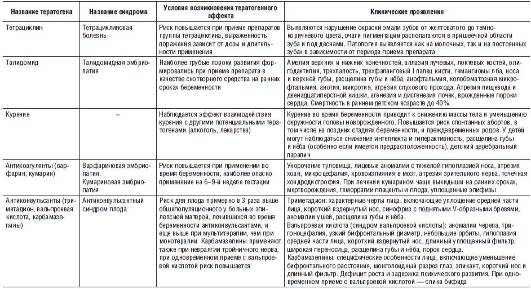
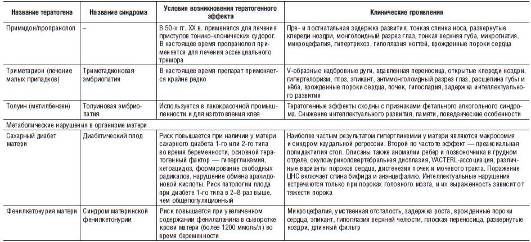
Во врачебной практике обычно встречаются три ситуации, когда можно заподозрить воздействие какого-либо тератогена:
-
по истории болезни или протоколу патологоанатомического вскрытия можно сделать предположение о тератогенном воздействии. В этом случае нужен определенный скептицизм, так как, ориентируясь только на предположение, можно ошибиться в прогнозе;
-
женщина планирует беременность и обращается по поводу лекарства, которое она принимает, или по поводу других вредностей дома или на работе. В этом случае врач должен ответить на вопрос, вредно ли это средство для плода. Если да, то, по возможности, исключить, заменить или, по крайней мере, минимизировать контакт с тератогенами во время критических периодов;
-
женщина принимала лекарство или алкоголь, когда еще не знала, что беременна. В этом случае врач должен прежде всего снять чувство страха у женщины, затем оценить риск для плода, включающий риск непосредственно тератогенного эффекта и фоновый риск по родословной. В зависимости от величины риска рекомендовать прерывание беременности или пренатальную диагностику.
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
Барашнев Ю.И., Бахарев В.А., Новиков П.В. Диагностика и лечение врожденных и наследственных заболеваний у детей (путеводитель по клинической генетике). - М.: Триада-Х, 2004. - 385 с.
Козлова С.И., Демикова Н.С. Наследственные синдромы и медико-генетическое консультирование - М.: Товарищество научных изданий КМК, 2007. - 448 с.
Лазюк Г.И. Тератология человека / Под ред. Г.И. Лазюка. - М.: Медицина, 1979. - 440 с.
Новиков П.В. Семиотика наследственных болезней у детей. - М.: Триада-Х, 2009. - 432 с.
Ньюссбаум Р.Л., Мак-Иннес Р.Р., Виллард Х.Ф. Медицинская генетика: Пер. с англ. - М.: ГЭОТАР-Медиа, 2010. - 619 с.
Hennekam R., Krantz I., Allanson J. Gorlin?s Syndromes of the Head and Neck. 5th ed. - Oxford University Press, 2010. - P. 1452.