Детские болезни : учебник / Геппе Н. А. - Москва : ГЭОТАР-Медиа, 2018. - 760 с. - ISBN 978-5-9704-4470-2 |
12.3. Герпетические инфекции
Герпетические инфекции (МКБ-10: В00–09) — группа заболеваний, вызываемых вирусами семейства Herpesviridae.
По данным ВОЗ, вызываемые вирусами герпеса заболевания занимают второе место по распространенности среди вирусных инфекций, уступая только гриппу. В настоящее время отмечают отчетливую тенденцию к увеличению заболеваемости различными формами герпетической инфекции.
Этиология
Вирусы герпеса — повсеместно распространенные ДНК-содержащие вирусы. После первичного инфицирования они пожизненно персистируют в организме человека и при реактивации вызывают рецидивы заболевания. В настоящее время известно около 80 представителей семейства Herpesviridae, в том числе 8 патогенных для человека видов: вирусы простого герпеса типов 1 и 2, вирус ветряной оспы/опоясывающего герпеса, вирус Эпшейна–Барр, цитомегаловирус, вирусы герпеса человека типов 6, 7 и 8. Современная систематика разделяет семейство Herpesviridae на подсемейства Alphaherpesviruses, Betaherpesviruses и Gammaherpesviruses (табл. 12.3).
| Alpha-herpesviruses | Beta- herpesviruses | Gamma-herpesviruses |
|---|---|---|
HSV-1 |
CMV |
EBV |
HSV-2 |
HHV-6 |
HHV-8 |
VZV |
HHV-7 |
-
Alpha-herpesviruses проявляют высокую цитопатическую активность. В эту группу входят вирусы простого герпеса типов 1 и 2 (англ. HSV-1, HSV-2), вирус ветряной оспы/опоясывающего герпеса (англ. VZV).
-
Beta-herpesviruses проявляют менее выраженную цитопатичность. К ним относят цитомегаловирус (англ. CMV), вирусы герпеса человека типов 6 и 7 (англ. HHV-6, HHV-7).
-
Gamma-herpesviruses обладают тропностью к В- и Т-лимфоцитам и способны к длительной персистенции на них. К этой группе относят вирус Эпштейна–Барр (англ. EBV) и вирус герпеса человека типа 8 (англ. HHV-8).
Вирусы герпеса термолабильны, быстро инактивируются под действием эфира и ультрафиолетового облучения, устойчивы к низкой температуре и высушиванию. Вирусы герпеса — классические внутриклеточные паразиты. Полный цикл их репродукции и образование полноценных вирионов происходят только в клетках определенного типа. Синтез дочерних ДНК в значительной мере зависит от ферментных и синтезирующих свойств клетки-хозяина. Наиболее подходят для репликации вирусов герпеса клетки с высоким темпом деления — эпителиальные и лейкоциты.
12.3.1. Инфекция, вызываемая вирусами простого герпеса типов 1 и 2
Эпидемиология
Вирусом простого герпеса инфицированы более 90% населения мира. Принято считать, что 80% жителей планеты переносят первичную герпетическую инфекцию в возрасте до 13 лет, а к 50 годам 90% населения имеют АТ к вирусам простого герпеса. Источник инфекции — больные различными формами герпетической инфекции и вирусоносители. Пути передачи инфекции разнообразны: контактный (прямой и непрямой контакт), воздушно-капельный, трансплацентарный. Естественная восприимчивость населения высокая. Иммунитет после перенесенного заболевания нестойкий. Заболеваемость спорадическая, возможны небольшие вспышки в организованных коллективах, среди ослабленных детей, в зимнее время года. Распространению инфекции способствуют плохие санитарно-гигиенические условия, скученность населения и т.д.
Патогенез
Первично возбудитель проникает через слизистые оболочки губ, полости рта, глаз, гениталий и т.д. После проникновения в эпителиальные клетки слизистых оболочек возбудитель активно в них размножается. Инфицированные клетки погибают с образованием очагов некроза и местных воспалительных изменений в виде везикул. Некоторая часть вирусов из первичного очага мигрирует по аксонам к телам нервных клеток, расположенных в чувствительных и вегетативных узлах. Проникнув в нервные клетки, вирусная ДНК интегрируется с геномом клетки, где сохраняется в латентном состоянии на протяжении всей жизни человека. Рецидивы заболевания обусловлены реактивацией вируса. Механизмы реактивации вируса изучены недостаточно. Реактивации вируса и его репродукции способствуют переохлаждение, избыточная инсоляция, переутомление, прием глюкокортикоидов и цитостатиков, лучевая терапия. По центробежным отросткам нервных клеток дочерние популяции вируса достигают нервных окончаний, проникают в эндотелий капилляров кожи и эпителиальные клетки, затем репродуцируются в них, что сопровождается появлением везикул. При нормальном иммунном ответе процесс ограничен местными проявлениями, вирус элиминируется из органов и тканей (за исключением чувствительных узлов). При иммунодефиците активация вируса становится все более частой, в процесс вовлечены новые нервные узлы, изменена локализация и увеличена распространенность очагов поражения кожи и слизистых оболочек. При тяжелом иммунодефиците возникающая виремия может привести к генерализации инфекции и поражению ЦНС, печени, селезенки, легких и других органов и тканей.
Классификация
Общепринятой классификации заболеваний, вызываемых вирусами простого герпеса у детей, не существует. При постановке диагноза учитывают локализацию, распространенность и течение заболевания.
-
По локализации процесса выделяют поражения слизистых оболочек, глаз, кожи, генитальный герпес, поражение ЦНС, висцеральные формы.
-
В зависимости от распространенности процесса — локализованные, распространенные и генерализованные формы.
-
Течение заболевания может быть острым, абортивным и рецидивирующим.
Клиническая картина
При инфекции, вызываемой вирусами простого герпеса типов 1 и 2, поражены преимущественно кожные покровы и слизистые оболочки (стоматит и гингивостоматит). Заболевание начинается остро. Возникают признаки общей интоксикации, температура тела повышена до 40–41 °C. Почти одновременно с общими симптомами на слизистой оболочке щек, десен, языка, внутренней поверхности губ, мягкого и твердого нёба, нёбных дужек и миндалин возникают типичные герпетические высыпания — сгруппированные пузырьки с серозным содержимым, окруженные венчиком гиперемии. Пузырьки быстро вскрываются, образуя болезненные эрозии с остатками отслоившегося эпителия (афты), рис. 12.2. Болезнь обычно продолжается 1–2 нед.
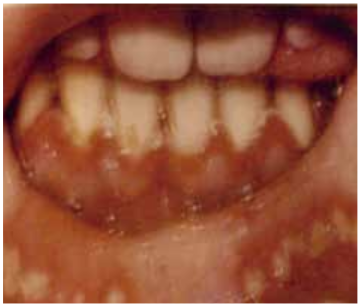
Характерно длительное латентное течение с периодическими рецидивами. Инфицирование вирусом простого герпеса типа 1 происходит в первые 3 года жизни ребенка, с 5–7-летнего возраста возрастает и количество детей, имеющих АТ к вирусу простого герпеса типа 2. Продолжительность инкубационного периода при первичном инфицировании в среднем составляет 4–6 дней (от 2 до 14).
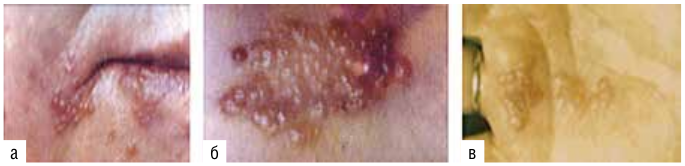
Поражение кожи сопровождается появлением везикулярных высыпаний в области красной каймы губ, крыльев носа, ушных раковин, реже — туловища, конечностей (рис. 12.3). Пузырьки расположены группами, окружены венчиком гиперемии. Появлению высыпаний нередко предшествует ощущение зуда, жжения или боли. Через несколько дней пузырьки вскрываются или подсыхают, на их месте образуются корочки. Образование везикул может сопровождаться увеличением регионарных лимфатических узлов.
-
При распространенной (диссеминированной) форме возникают лихорадка, общая слабость, головная боль, миалгии, увеличиваются лимфатические узлы, печень, селезенка. К концу первых суток заболевания на различных участках тела одновременно появляются везикулы, проходящие все стадии развития, описанные ранее (уплотнение, вскрытие, корочка, пигментация).
-
К генерализованным формам герпеса кожи относят герпетическую экзему (болезнь Капоши, вакциноформный пустулез), возникающую у детей с экземой, атопическим дерматитом и другими поражениями кожи. У ослабленных детей одновременно развиваются герпетический стоматит, ларинготрахеит, кератит, поражения ЦНС и внутренних органов.
Возможно развитие изолированного офтальмогерпеса, но чаще наблюдают сочетанные поражения глаз, кожи, слизистых оболочек.
Генитальный герпес обычно развивается у подростков, реже у детей младших возрастных групп (инфицирование последних происходит контактным путем от родителей). Высыпания локализованы на слизистых оболочках половых органов, на коже мошонки, промежности, внутренней поверхности бедер, реже на слизистой оболочке мочеиспускательного канала и мочевого пузыря.
Поражение ЦНС может протекать по типу энцефалита, менингита, менингоэнцефалита, менингоэнцефалорадикулита. Чаще всего выявляют энцефалит и/или менингит. Энцефалит может развиться как на фоне герпетического поражения кожных покровов и слизистых оболочек, так и при первичной генерализованной инфекции. Заболевание дебютирует остро с общих симптомов: озноб, лихорадка, рвота. Затем возникают расстройства сознания (спутанность, дезориентация, психомоторное возбуждение, кома), судороги и нарастают очаговые неврологические симптомы. Летальность высокая. После выздоровления часто остаются тяжелые остаточные явления (выраженное снижение интеллекта, нарушения вкуса и обоняния, параличи и т.д.), нередко приводящие к стойкой инвалидизации. В ликворе обнаруживают умеренный смешанный или лимфоцитарный плеоцитоз, незначительное повышение концентрации белка. Нередко наблюдают ксантохромию вследствие кровоизлияний в оболочки и вещество головного мозга. При КТ на 3–7-й день болезни, а при МРТ несколько раньше можно обнаружить поражение лобных и височных долей головного мозга.
Герпетическая инфекция новорожденных
Инфицирование новорожденных происходит от больной матери во время родов или сразу после них, а также от ухаживающего персонала или членов семьи. Заболевание протекает тяжело, сопровождается выраженными симптомами интоксикации. Продолжительность инкубационного периода обычно составляет 5–10 дней. При отсутствии специфического лечения исход неблагоприятный (развиваются инфекционно-токсический шок, ДВС-синдром, поражение ЦНС, массивный некроз печени).
Генерализованные формы
Генерализованные формы герпетической инфекции наблюдают у новорожденных и детей с врожденными и приобретенными иммунодефицитами. В частности, генерализованная инфекция может развиться у детей, длительно получающих глюкокортикоиды или цитостатики, а также у ВИЧ-инфицированных.
Диагностика
Диагностика типичных форм герпетической инфекции обычно не представляет затруднений и основана на характерной клинической картине и эпидемиологических данных. Лабораторные тесты — вирусологические исследования биологических субстратов (культуральная диагностика, электронная микроскопия), цитологические (гистологические) методы, позволяющие обнаружить характерные многоядерные гигантские клетки со специфическими включениями, серологические реакции (нарастание титра АТ в РСК, реакции РПГА). Вирусные частицы в соскобах можно выявить с помощью реакции иммунофлюоресценции. Высокой информативностью отличаются ИФА и ПЦР.
Дифференциальная диагностика
Герпетические поражения кожи чаще всего надо дифференцировать с опоясывающим герпесом и ветряной оспой (см. ниже раздел «Заболевания, вызываемые вирусом герпеса человека типа 3»).
Герпетический стоматит следует дифференцировать с герпетической ангиной (см. главу «Энтеровирусные инфекции»), грибковыми стоматитами.
Лечение
Наиболее эффективен ацикловир (Зовиракс♠). Препарат можно применять местно, внутрь и парентерально. Даже при локализованных формах заболевания наиболее оптимальна терапия, сочетающая местное и пероральное применение ацикловира. При генерализованных формах ацикловир вводят внутривенно. Продолжительность курса лечения — 7–10 дней. У детей старше 10–12 лет широко применяют валацикловир (Валвир♠), фамцикловир, ганцикловир, фоскарнет натрия, рибавирин. Все перечисленные препараты обладают только вирусостатическим эффектом.
-
При локализованных поражениях кожи и слизистых оболочек можно применять мази [например, 2% с тетрагидроксиглюкопиранозилксантеном (Алпизарином♠), 1–2% с диоксотетрагидрокситетрагидронафталином (Оксолином♠), 2% с теброфеном℘, 1% с тромантадином, 1% риодоксовую мазь℘] и кремы [например, с рибавирином (Виразолом♠)] с противовирусным действием.
-
Хороший санирующий эффект при герпетических стоматитах оказывает лизатов бактерий смесь [L. acidophilus + L. delbrueckii ss lactis + L. helveticus + L. fermentum + S. pyogenes groupe A + S. sanguis groupe H + S. Aureus + E. faecium + E. faecalis + K. pneumoniae ss pneumoniae + F. nucleatum ss fusiforme + C. Pseudodiphtheriticum + C. albicans] (Имудон♠). Для уменьшения боли и облегчения приема пищи рекомендуют полоскание полости рта растворами местных анестетиков (например, лидокаина).
-
При выраженном иммунодефиците необходимо применение интерферонов [интерферон альфа-2b (например, Реаферон-ЕС♠, Интрон А♠), интерферон альфа (Вэллферон♠)], оказывающих неспецифическое подавляющее действие на вирусы герпеса.
Профилактика
Ведущее значение в предупреждении распространения инфекции имеют неспецифические профилактические мероприятия — формирование общих гигиенических навыков, санитарно-просветительная работа, устранение провоцирующих факторов, закаливание детей. Для предотвращения ВУИ необходимо обследование беременных на вирусы герпеса (особенно если ранее были неблагоприятные исходы беременности).
Для предотвращения рецидивов инфекции в период реконвалесценции применяют общеукрепляющие средства: витамины С, Е, А в сочетании с микроэлементами, растительные адаптогены. По индивидуальным показаниям при частых рецидивах герпетической инфекции проводят профилактические курсы лечения ацикловиром или валацикловиром.
Прогноз
При локализованных формах инфекции прогноз благоприятный. Менее благоприятен прогноз при генерализованной герпетической инфекции.
12.3.2. Заболевания, вызываемые вирусом герпеса человека типа 3
Вирус герпеса человека типа 3 вызывает ветряную оспу (varicella) и опоясывающий лишай (herpes zoster). Первичная инфекция протекает как ветряная оспа, а ее рецидивы — как опоясывающий лишай.
Ветряная оспа
Ветряная оспа (varicella) (МКБ-10: В01) — высококонтагиозное острое вирусное инфекционное заболевание, протекающее с умеренно выраженной интоксикацией и характерной пятнисто-папулезно-везикулярной сыпью на коже и слизистых оболочках. Ветряная оспа — одно из наиболее распространенных инфекционных заболеваний у детей.
Эпидемиология
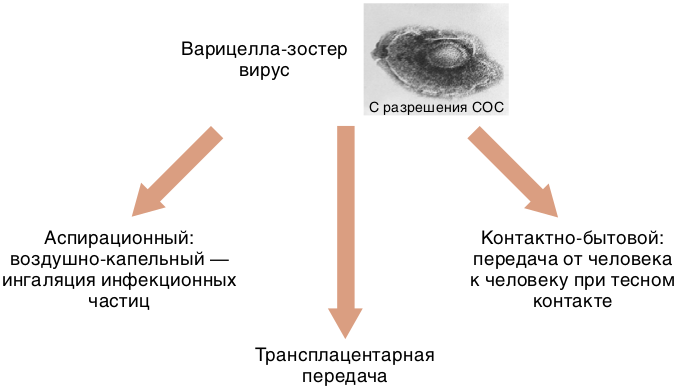
Источник инфекции — больной ветряной оспой или опоясывающим герпесом. Больной контагиозен с последнего дня инкубационного периода до 5-го дня с момента появления последнего элемента сыпи. Передача инфекции происходит воздушно-капельным, реже контактным путем (рис. 12.4). Описаны случаи внутриутробного заражения. Восприимчивость к инфекции чрезвычайно высока. Наибольшую заболеваемость регистрируют среди детей дошкольного возраста в холодное время года (осенне-зимний период). После заболевания формируется стойкий иммунитет, повторные заболевания возникают крайне редко. Дети первых месяцев жизни практически не болеют ветряной оспой в связи с наличием пассивного иммунитета (АТ к вирусу ветряной оспы, полученные трансплацентарно от матери).
Патогенез
Возбудитель первично размножается в эпителии слизистой оболочки верхних дыхательных путей. Затем вирус по лимфатическим путям попадает в регионарные лимфатические узлы, а потом в кровь. В результате гематогенной диссеминации возбудителя, обладающего выраженной тропностью к эпителиальным клеткам, происходит диффузное поражение кожных покровов. Репродукция вируса в клетках шиповатого слоя кожи приводит к их баллонирующей дегенерации (рис. 12.5). В результате накопления межтканевой жидкости в полостях, образующихся при некрозе эпителия, формируются типичные везикулярные высыпания. В дальнейшем пузырьки разрываются или их содержимое резорбируется с образованием корочек. Поврежденный эпителий постепенно восстанавливается. При этом не образуется рубцов, так как некроз эпителия не распространяется на подлежащую соединительную ткань.

Вирус ветряной оспы/опоясывающего герпеса также обладает тропностью к нервной ткани, поэтому в некоторых случаях может развиться поражение ЦНС (менингоэнцефалит). При выраженном иммунодефиците возможна генерализация инфекции с поражением внутренних органов (легких, печени, надпочечников и т.д.).
Клиническая картина
Продолжительность инкубационного периода составляет 11–21 день (чаще 14 дней). Иногда отмечают непродолжительный продромальный период, проявляемый недомоганием, субфебрильной лихорадкой, появлением предвестниковой сыпи — кореподобной или скарлатиноподобной, исчезающей бесследно через несколько часов. Чаще заболевание дебютирует остро с повышения температуры тела до 37,5–38,5 °C и появления сыпи. На коже лица, волосистой части головы, туловища возникают мелкие пятнисто-папулезные элементы, превращающиеся через несколько часов в однокамерные пузырьки округлой или овальной формы, окруженные венчиком гиперемии, с прозрачным, а позднее мутным содержимым. Через 1–2 дня везикулы подсыхают, на их месте образуются корочки. После отхождения корочек следов не остается. Типичные элементы также могут появляться на слизистой оболочке рта, глаз, гортани, половых органов. Высыпания на слизистых оболочках иногда предшествуют появлению сыпи на коже. На ладонях и подошвах сыпи обычно не бывает.
Для ветряной оспы характерно одновременное присутствие на коже элементов во всех стадиях развития (пятен, папул, везикул, корочек). Все элементы — последовательные фазы развития единого воспалительного процесса в дерме (ложный полиморфизм сыпи, рис. 12.6).
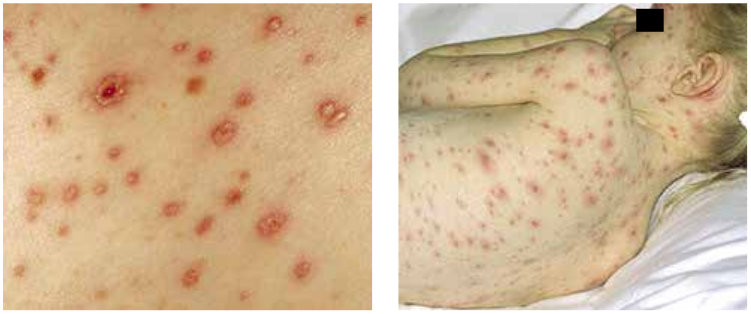
Одновременное присутствие на коже элементов в различных стадиях развития связано с феноменом ежедневного подсыпания: первые пятна появляются на 1–2-й день, последние — на 3–6-е сут. При каждом новом высыпании отмечают подъем температуры тела, нарушение самочувствия. В настоящее время заболевание чаще протекает в легкой и среднетяжелой формах. Температура тела обычно нормализуется на 3–5-й день, корочки отпадают через 7–14 дней. В тяжелых случаях заболевания наблюдают специфическое поражение внутренних органов (легких, печени, почек, селезенки и др.).
Классификация
Выделяют типичные и атипичные формы заболевания, легкую, среднетяжелую и тяжелую формы К типичной ветряной оспе относят случаи, проявляемые характерными пузырьковыми высыпаниями.
-
При легких формах сыпь скудная, слизистые оболочки обычно не поражены. Температура тела повышена до 37,5–38 °C. Общие симптомы интоксикации практически отсутствуют.
-
При среднетяжелой форме высыпания обильные, температура тела повышена до 39 °C. Симптомы интоксикации выражены умеренно.
-
При тяжелой форме высыпания чрезвычайно обильные, температура тела бывает выше 39 °C.
К атипичной ветряной оспе относят рудиментарную, генерализованную, гангренозную и геморрагическую формы.
-
Рудиментарная форма обычно развивается у детей, получавших в инкубационном периоде Ig, и проявляется розеолезно-папулезными высыпаниями с единичными пузырьками. Лихорадка, как правило, отсутствует, общее состояние ребенка не страдает.
-
Генерализованная форма характерна тяжелым течением с поражением различных органов (легких, почек, головного мозга и т.д.). Эта форма обычно развивается у детей с иммунодефицитом или новорожденных.
-
Гангренозная форма чаще возникает у ослабленных больных при присоединении вторичной бактериальной инфекции.
-
Геморрагическая форма может развиться у детей с различными нарушениями свертывающей системы крови. В таких случаях содержимое везикул становится геморрагическим. Также могут быть кровоизлияния в кожу и слизистые оболочки, носовые кровотечения и т.д.
Осложнения
Осложнения встречают редко. Различают специфические осложнения, обусловленные действием самого вируса (энцефалит, менингоэнцефалит, миелит мио-, пери- и эндокардит и пр.) и бактериальные, развивающиеся в результате присоединения вторичной инфекции (флегмона, абсцесс, гнойный конъюнктивит, пневмония и пр.)
Опоясывающий герпес (Herpes zoster)
Опоясывающий герпес, или опоясывающий лишай (МКБ-10: В02), — спорадическое заболевание, представляющее собой реактивацию латентной инфекции, вызываемой вирусом герпеса человека типа 3.
Эпидемиология
Заболеваемость спорадическая, эпидемических вспышек не бывает. Заболеваемость выше в холодные месяцы.
Патогенез
Развитие заболевания рассматривают как результат реактивации вируса, персистирующего в чувствительных нервных узлах у лиц, переболевших ветряной оспой. Пусковые механизмы реактивации связаны с нарушениями иммунитета. Кожные проявления возникают в дерматоме, иннервируемом пораженным чувствительным узлом, что обусловлено неврогенным распространением вируса. Излюбленное место персистенции вируса герпеса человека типа 3 — ганглий тройничного нерва и ганглии задних корешков грудного отдела спинного мозга.
Клиническая картина
Заболевание дебютирует остро с повышения температуры тела и появления интенсивных жгучих болей на месте будущих высыпаний. Через 1–3 дня появляется характерная сыпь — тесно расположенные красные папулы, быстро превращающиеся в пузырьки, заполненные прозрачным, а затем мутным содержимым. Приблизительно через неделю пузырьки подсыхают и превращаются в корочки. После отпадения корочек остается легкая пигментация. Боли и сыпь локализованы в дерматоме, соответствующем пораженному нерву.
Особенности опоясывающего герпеса у детей
Возможны атипичные формы болезни: буллезная, геморрагическая, гангренозная, абортивная, генерализованная.
Осложнения при опоясывающем герпесе обычно связаны с присоединением бактериальной инфекции.
Диагностика
Диагностика ветряной оспы основана на клинических данных (типичная везикулярная сыпь, характерная динамика развития высыпаний). Лабораторные исследования включают обнаружение многоядерных гигантских клеток в соскобах с основания элементов сыпи в мазках, окрашенных по Тцанку; выделение вируса из культуры фибробластов человека; выявление Аг вируса с помощью реакции иммунофлюоресценции, ПЦР в содержимом везикул; серологические исследования.
Дифференциальная диагностика
Заболевание чаще всего надо дифференцировать с импетиго и генерализованной герпетической инфекцией (см. выше раздел «Инфекция, вызываемая вирусами простого герпеса типов 1 и 2»).
Опоясывающий герпес в начальном периоде нередко принимают за острый холецистит, почечную колику, плеврит и другие заболевания, сопровождаемые выраженным болевым синдромом.
Лечение
При легких формах ветряной оспы лечение сводится к обработке элементов сыпи лечебными и косметическими средствами в виде гелей, лосьонов, мазей [поксклин, каламин, цинка оксид (Циндол♠) и пр.], способствующих подсушиванию элементов и профилактике вторичного инфицирования, соблюдению правил личной гигиены. При гнойных осложнениях назначают антибиотики: местно [мазь с мупироцином (Бактробан♠), бацитрацин + неомицин (Банеоцин♠)] либо системно. При тяжелых формах, иммунодефицитных состояниях, развитии генерализованных форм применяют ацикловир в дозах 20 мг/кг 4 раза в сут в течение 5–7 дней, Анаферон детский♠.
При опоясывающем герпесе назначают ацикловир или фамцикловир и симптоматическое лечение (анальгетики, физиотерапию, прокаиновые (Новокаиновые♠) блокады). Перспективно в лечении опоясывающего герпеса применение человеческого иммуноглобулина против вируса герпеса человека типа 3℘ и специфической вакцины.
Профилактика
Больного ветряной оспой изолируют на срок контагиозности (до 5-го дня с момента появления последних высыпаний). Контактные и не болевшие ветряной оспой дети разобщаются на 21 день с момента контакта. Если точно известна дата контакта, разобщение начинают с 11-го дня после контакта. Аналогичные профилактические меры следует применять и в отношении больных опоясывающим герпесом. Заключительную дезинфекцию в очаге инфекции не проводят.
Специфическую профилактику ветряной оспы проводят живой ослабленной вакциной для профилактики ветряной оспы живой аттенуированной (Варилриксом♠) в 1 год, ревакцинацию проводят в 6–7 лет. Специально для борьбы с опоясывающим герпесом у лиц старше 60 лет разработана и внедрена новая вакцина против вируса герпеса человека типа 3 (зоставакс℘).
Прогноз
Прогноз при типичной ветряной оспе благоприятный. Тяжелые атипичные формы (генерализованные, гангренозные, геморрагические) могут привести к летальному исходу. У пациентов с иммунодефицитом летальность при ветряной оспе достигает 20%. При опоясывающем герпесе прогноз в целом благоприятный, однако следует учитывать, что заболевание склонно к рецидивированию.
12.3.3. Инфекция, вызываемая вирусом Эпштейна–барр
Вирусный инфекционный мононуклеоз Эпштейна–Барр (МКБ-10: В27) — острое инфекционное заболевание, характерное поражением ретикулоэндотелиальной и лимфатической систем и протекающее с лихорадкой, тонзиллитом, полиаденитом, увеличением печени и селезенки, лейкоцитозом с преобладанием мононуклеаров.
Эпидемиология
Вирус Эпштейна–Барр — В-лимфотропный вирус человека, обладающий уникальной способностью вызывать не гибель инфицированных клеток, а их пролиферацию. В раннем возрасте инфекцию сопровождают стертые проявления либо она протекает бессимптомно. Первичное инфицирование, а также реактивация инфекции, обусловленная хронической персистенцией вируса Эпштейна–Барр в подростковом или более старшем возрасте могут вызвать заболевание, известное как инфекционный мононуклеоз. Клинические проявления вариабельны. Хроническая активная инфекция, связанная с вирусом Эпштейна–Барр, может также проявляться прогрессирующими лимфопролиферативными заболеваниями или лимфомами ЦНС, обычна для больных с иммунодефицитными состояниями.
Вирус Эпштейна–Барр распространен повсеместно, специфические АТ выявляют у 90% лиц старше 40 лет. Следует учитывать, что симптомокомплекс инфекционного мононуклеоза вызывает не только вирус Эпштейна–Барр, но и другие возбудители (ВИЧ, цитомегаловирус, вирус герпеса человека типа 6, токсоплазмоз и др.), поэтому в настоящее время термин «инфекционный мононуклеоз» используют только как синдромальный диагноз.
Источник инфекции — человек, инфицированный вирусом Эпштейна–Барр, независимо от наличия или отсутствия у него клинической симптоматики. Основной механизм передачи инфекции — контактно-бытовой и половой. Возможен и воздушно-капельный путь передачи инфекции. Инфекция также может передаваться трансплацентарно, при гемотрансфузиях и трансплантации.
МКБ-10: В27.0. Мононуклеоз, вызванный гамма-герпетическим вирусом.
Патогенез
При инфекционном мононуклеозе Эпштейна–Барр вирус размножается в верхних отделах дыхательных путей и лимфоидных образованиях ротоглотки, что сопровождается развитием местных воспалительных реакций. Возбудитель может гематогенно диссеминировать в периферические лимфатические узлы, селезенку, печень и другие органы. Инфицирование макрофагов и лимфоидных клеток приводит к появлению крупных мононуклеарных клеток. Длительное персистирование вируса в организме обусловливает возможность хронического мононуклеоза и реактивации инфекции при ослаблении иммунитета. Латентное инфицирование В-лимфоцитов вызывает их поликлональную активацию с образованием низкоспецифичных гетерофильных АТ, агглютинирующих эритроциты различных животных.
Клиническая картина
Продолжительность инкубационного периода — 5–20 дней (иногда до 2 мес). Заболевание дебютирует постепенно, симптоматика нарастает в течение нескольких дней и максимальной выраженности достигает обычно к концу первой недели. Температура тела может быть субфебрильной, но нередко достигает 38–39,5 °C. Продолжительность лихорадочного периода составляет от нескольких дней до 3 нед.
Характерным признаком заболевания считают увеличение лимфатических узлов шейной группы, расположенных по заднему краю грудино-ключично-сосцевидной мышцы.
Лимфатические узлы увеличены до 1–3 см в диаметре (от горошины до грецкого ореха), расположены в виде цепочки или пакета, не спаяны между собой, подвижны, мало болезненны при пальпации. Назофарингит проявляется нарушением носового дыхания, гнусавостью голоса, слизистым отделяемым, иногда симптоматика ограничена только заложенностью носа. Изменения в ротоглотке обнаруживают почти у всех больных. Обычно развивается лакунарно-фолликулярная (реже катаральная) ангина с неплотным, легко снимающимся налетом, не распространяющимся на дужки и мягкое небо. Увеличены селезенка и в меньшей степени печень. Иногда повышена активность ферментов печени (АЛТ). В некоторых случаях появляется желтуха, возможна скудная полиморфная сыпь (рис. 12.7).
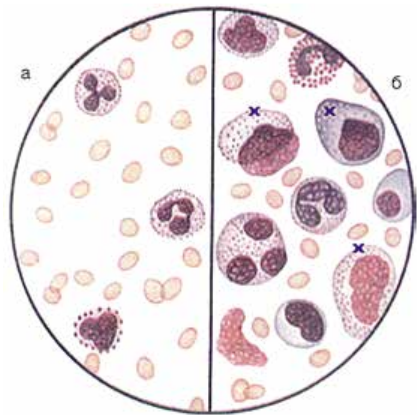
При исследовании периферической крови обнаруживают мононуклеарный лейкоцитоз (лимфоциты 35–50% и более, моноциты до 10–15% и более), количество атипичных мононуклеаров превышает 10%. Атипичные мононуклеары представляют собой B-лимфоциты, изменившие свои морфологические и функциональные свойства под воздействием вируса (рис. 12.8).
К 3–4-й нед болезни основные симптомы исчезают, до 2 мес и более могут сохраняться незначительная гепатоспленомегалия и изменения в крови. Осложнения развиваются редко. Возможны развитие гемолитической анемии, тромбоцитопении, неврологических расстройств, пневмонии, разрыв селезенки.
Классификация
Выделяют типичные и атипичные формы заболевания. К атипичным формам относят случаи, характерные слабой выраженностью или полным отсутствием какого-либо из основных симптомов заболевания (ангины, лимфаденопатии, гепатоспленомегалии). Типичные формы заболевания по степени тяжести подразделяют на легкие, среднетяжелые и тяжелые. Основные показатели тяжести: выраженность интоксикации, затруднения носового дыхания и изменений в ротоглотке, степень увеличения лимфатических узлов, печени и селезенки, выраженность гематологических нарушений.
Диагностика
Для подтверждения диагноза вирусного инфекционного мононуклеоза Эпштейна–Барр применяют преимущественно серологические методы. Наиболее информативно обнаружение АТ класса IgM к Аг вирусного капсида определяют их авидность. Эти АТ появляются в инкубационном периоде и исчезают через 2–3 мес после выздоровления. АТ к Аг вирусного капсида класса IgG после перенесенной болезни сохраняются в течение всей жизни. В настоящее время редко в качестве ориентировочных используют неспецифические реакции агглютинации, основанные на способности сыворотки больного агглютинировать эритроциты животных (реакции Пауля–Буннеля). Широко используют молекулярно-генетическую ПЦР диагностику.
Дифференциальная диагностика
Вирусный инфекционный мононуклеоз Эпштейна–Барр необходимо дифференцировать от других инфекционных заболеваний, сопровождаемых поражением зева и лимфаденопатией (дифтерия зева, краснуха, аденовирусная инфекция) и др. При выраженных гематологических изменениях иногда возникает необходимость исключить острый лейкоз. Для последнего характерны выраженное повышение СОЭ, анемия, длительная лихорадка. Окончательно диагноз устанавливают по результатам стернальной пункции. Дифференциальная диагностика синдрома инфекционного мононуклеоза, вызванного другими возбудителями, основана преимущественно на результатах лабораторных исследований с определением специфических АТ.
Лечение
Применяют противовирусные средства: интерферон альфа-2b + таурин (Генферон лайт♠), меглюмина акридонацетат (Циклоферон♠), Анаферон детский♠, Эргоферон♠, симптоматическое лечение. В острой фазе заболевания необходимо соблюдение постельного режима. При высокой температуре тела назначают анальгетики (парацетамол, ибупрофен). При бактериальных суперинфекциях необходима антибиотикотерапия. При развитии обструкции дыхательных путей назначают глюкокортикоиды (преднизолон по 2 мг/кг в сут с постепенным снижением дозы в течение 5–7 сут).
Профилактика
Специфическая профилактика не разработана. Госпитализацию больных осуществляют по клиническим показаниям. Наблюдение за контактными не устанавливают. Необходимость в проведении дезинфекционных мероприятий отсутствует.
Прогноз
Прогноз обычно благоприятный.
12.3.4. Цитомегаловирусная инфекция
Цитомегаловирусная инфекция (МКБ-10, В25) — широко распространенное вирусное заболевание с полиморфными клиническими проявлениями, выраженность которых зависит от иммунного статуса больного.
Эпидемиология
Большинство людей переносят латентную или инаппарантную форму болезни в раннем детском возрасте, о чем свидетельствует наличие специфических АТ у 70–96% взрослых. Вирус содержится в слюне, бронхиальном секрете, моче, кале, грудном молоке, сперме, слизи цервикального канала. Инфицирование происходит контактным путем, реже воздушно-капельным и пищевым. Возможна передача инфекции при трансплантации органов и переливании крови, а также трансплацентарно. Возможно инфицирование новорожденных через молоко матери. Восприимчивость к инфекции высокая. После инфицирования человек остается вирусоносителем в течение всей жизни. Персистирование вируса в организме какой-либо симптоматикой чаще всего не сопровождается. Количество детей, инфицированных внутриутробно, — от 0,5 до 7%, из них у 10–15% развиваются манифестные формы врожденной цитомегаловирусной инфекции. Во многих регионах мира большинство детей инфицированы уже к 5 годам.
Патогенез
Цитомегаловирус может поражать практически все органы и ткани. Характерная особенность возбудителя — способность к образованию гигантских цитомегалических клеток (размером 25–40 мкм), содержащих тельца включений — «совиный глаз». Цитомегаловирус способен инфицировать клетки различных органов и систем, а также иммунокомпетентные клетки и латентно в них персистировать. Механизм развития цитомегаловирусной инфекции зависит от многих факторов, в частности имеют значение путь заражения, индивидуальные (генетические) особенности организма, состояние иммунной системы в момент инфицирования. Активная репликация вируса в клетках сопровождается изменением иммунологической реактивности (реакции гиперчувствительности замедленного типа, иммунодепрессия). Контроль активности инфекции и санации от возбудителя обеспечивают компоненты клеточного иммунитета. Фактор риска развития тяжелых манифестных форм — дефицит клеточного иммунитета (ВИЧ-инфекция, онкологические процессы, иммуносупрессивная терапия).
Клиническая картина
Единой классификации цитомегаловирусной инфекции не существует, что связано с широким спектром ее клинических вариантов. Выделяют врожденную (острая и хроническая формы) и приобретенную цитомегаловирусную инфекцию.
Врожденная цитомегаловирусная инфекция
Характер поражения плода зависит от времени инфицирования. Инфицирование на ранних сроках беременности обычно приводит к внутриутробной гибели плода и выкидышам или рождению детей с хронической формой врожденной цитомегаловирусной инфекции. В последнем случае в клинической картине доминируют множественные пороки развития (сужение легочного ствола и аорты, дефект межпредсердной перегородки и дефект межжелудочковой перегородки, фиброэластоз, гипоплазия легких, атрезия пищевода, микро- или гидроцефалия и т.д.) и резидуальные признаки со стороны органов, пораженных внутриутробно (атрезия желчевыводящих путей, ЦП, хроническая пневмония и т.п.). При инфицировании на поздних сроках беременности пороки развития не формируются, но с первых дней жизни ребенка возникают симптомы заболевания (острая врожденная цитомегаловирусная инфекция). Состояние детей сразу после рождения бывает тяжелым. Отмечают вялость, лихорадку, плохой аппетит, срыгивание, недостаточную прибавку массы тела, снижение тургора тканей, неустойчивый стул. Характерны желтуха, обусловленная как поражением печени, так и повышенным гемолизом эритроцитов, геморрагическая пурпура, гепатоспленомегалия. Также поражаются легкие (интерстициальная пневмония), ЦНС (гидроцефалия, менингоэнцефалит), ЖКТ (энтерит, колит, фиброз и поликистоз поджелудочной железы), почки (нефрит). Нередко в клинической картине доминирует геморрагический синдром (экхимозы и петехии на коже, рвота «кофейной гущей», тромбоцитопения). Часто развивается гипохромная анемия. Острая форма врожденной цитомегаловирусной инфекции обычно бывает генерализованной, часто осложнена присоединением вторичных инфекций и нередко приводит к летальному исходу в первые недели жизни ребенка. Если ребенок выживает, у него очень часто формируются различные остаточные явления (задержка нервно-психического развития, гипертензионно-гидроцефальный синдром, перивентрикулярная кальцификация мозга и др.). Возможны и более легкие варианты течения болезни без признаков генерализации: абортивное или бессимптомное, а также изолированное поражение того или иного органа.
Все патологические проявления, приведенные выше, объединяют термином «явный цитомегаловирусный синдром». Он составляет 10–15% всех случаев врожденной цитомегалии. Намного более распространенный «скрытый цитомегаловирусный синдром» включает нарушения, выявляемые на более поздних стадиях развития ребенка (хориоретинит с атрофией зрительных нервов, глухота, нарушения речи, снижение интеллекта).
Приобретенная цитомегаловирусная инфекция
Продолжительность инкубационного периода составляет 15–90 дней. При интранатальном и раннем постнатальном инфицировании клинические признаки болезни обычно появляются через 1–2 мес после рождения ребенка. Заболевание может протекать с изолированным поражением слюнных желез или внутренних органов. Исходя из ведущего клинического синдрома выделяют респираторную, церебральную, желудочно-кишечную, гепатобилиарную, почечную, гематологическую формы. Также могут быть поражены надпочечники, щитовидная железа, яички и яичники, глаза, кожные покровы, вилочковая железа. Заболевание отличается длительным течением и часто рецидивирует. Инфицирование детей старшего возраста и взрослых в большинстве случаев приводит к формированию бессимптомного вирусоносительства или развитию субклинической инаппарантной формы хронической цитомегаловирусной инфекции. Иногда развивается симптомокомплекс, напоминающий инфекционный мононуклеоз [острое начало с повышением температуры тела, симптомами интоксикации, катаральными явлениями со стороны верхних дыхательных путей, лимфаденопатией, увеличением печени и селезенки, лимфомоноцитозом, атипичными мононуклеарами в крови (не более 5–10%)].
Реактивация цитомегаловирусной инфекции возникает при различных иммунодефицитах (ВИЧ-инфекции, злокачественных опухолях, тяжелых ожогах, после трансплантации органов, на фоне длительного приема цитостатиков и глюкокортикоидов и т.д.). Клиническая манифестация заболевания у лиц с иммунодефицитом сопровождается разнообразной симптоматикой — от сиалоаденита (увеличения слюнных желез, регионарного лимфаденита) до тяжелых диссеминированных форм. Заболевание обычно начинается с продолжительной лихорадки, недомогания, анорексии, ночных потов, миалгии, артралгии. Развиваются лейкопения, тромбоцитопения. Часто поражены печень (цитомегаловирусный гепатит с холестатическим компонентом), легкие (интерстициальная пневмония), ЖКТ (энтероколит, в том числе язвенно-некротический; панкреатит, эзофагит), глаза (ретинит), ЦНС (энцефалит). При тяжелых формах отмечают полиорганные поражения. Клиническая симптоматика в таких случаях напоминает сепсис (длительная лихорадка, выраженная интоксикация, увеличение лимфатических узлов и т.д.).
Диагностика
На основании клинических данных диагностировать цитомегалию крайне сложно. Во всех случаях необходимо подтверждение диагноза с помощью дополнительных методов исследования. Используют цитологические, вирусологические, серологические и молекулярно-биологические методы.
-
Цитологическое исследование позволяет выявить гигантские эпителиальные клетки, содержащие внутриядерные включения.
-
Из серологических методов используют РСК и РПГА с парными сыворотками, а также ИФА. Для обнаружения Аг вируса при экспресс-диагностике используют реакцию иммунофлюоресценции.
-
В последнее время все большее распространение для диагностики цитомегаловирусной инфекции получают молекулярно-биологические методы (ДНК-гибридизация и ПЦР) — высокочувствительные и достоверные исследования, позволяющие обнаружить вирусную ДНК и определить ее концентрацию.
Дифференциальная диагностика
Врожденную цитомегаловирусную инфекцию необходимо дифференцировать с ГБН, сепсисом, врожденными токсоплазмозом, листериозом и сифилисом. При приобретенной цитомегалии, протекающей с синдромом мононуклеоза, необходимо исключить инфекционный мононуклеоз, вызываемый вирусом Эпштейна–Барр или вирусом герпеса человека типа 6, и раннюю фазу ВИЧ-инфекции. Во всех случаях ведущее значение имеют результаты лабораторных исследований.
Лечение
Из противовирусных препаратов назначают ганцикловир, валацикловир (Валвир♠). Широко применяют специфические [иммуноглобулин человека антицитомегаловирусный (НеоЦитотект♠)] или неспецифические (иммуноглобулин человека нормальный) Ig. Иммуноглобулин человека антицитомегаловирусный (НеоЦитотект♠) содержит АТ не только к цитомегаловирусу, но и к вирусам простого герпеса типов 1 и 2, вирусу Эпштейна–Барр, вирусу герпеса человека типа 3. При осложненных формах необходима антибактериальная и патогенетическая терапия.
Профилактика
Специфическая профилактика не разработана. Необходимо повторное серологическое обследование беременных. При наличии факторов риска серонегативным больным вводят Ig человека, содержащий АТ к цитомегаловирусу [иммуноглобулин человека антицитомегаловирусный (Цитотект♠)].
Прогноз
При врожденной цитомегаловирусной инфекции прогноз часто неблагоприятный. При приобретенной форме прогноз в значительной мере зависит от того, насколько успешно удается купировать иммунодефицитные состояния, способствующие реактивации цитомегаловирусной инфекции.
12.3.5. Инфекции, вызываемые вирусами герпеса человека типов 6, 7 и 8
МКБ-10: В00.08.
Инфекция, вызываемая вирусом герпеса человека типа 6
Заболевания, вызываемые вирусом герпеса человека типа 6, довольно распространены. Первичное инфицирование обычно происходит в течение первых 3 лет жизни. Механизм и пути передачи инфекции изучены недостаточно. Вирус обнаруживают в слюне, смывах из носоглотки, гортани, секрете бронхиальных желез. Инфекция, вероятно, передается контактным и воздушно-капельным путями, а также трансплацентарно, при переливании крови и трансплантации органов. У подавляющего большинства инфицированных заболевание протекает латентно. Широко распространенная первичная манифестация инфекции у детей раннего возраста — внезапная экзантема (шестая болезнь, трехдневная лихорадка с сыпью, псевдокраснуха). У детей старшего возраста и взрослых с вирусом герпеса человека типа 6 связывают бессимптомную мочевую инфекцию. Вирус может латентно персистировать в ЦНС, при его реактивации возможно развитие миелита, менингоэнцефалита. Существуют сведения, что вирус герпеса человека типа 6 может вызывать лимфопролиферативные заболевания — как доброкачественные (лимфаденопатию), так и злокачественные (лимфому). Выявлена причастность вируса герпеса человека типа 6 к развитию острых и злокачественных форм гепатитов у детей.
Клинические формы инфекции, вызванные HHV-6 Calo R., 1986
Первичная манифкстация инфекции
Внезапная экзантема
Клиническая картина. Заболевание дебютирует остро с повышения температуры тела до 39–40 °C и незначительных симптомов интоксикации. Продолжительность лихорадочного периода обычно составляет 3 дня. В период снижения температуры тела появляется бледно-розовая пятнистая или пятнисто-папулезная сыпь, покрывающая все тело и конечности. Через 2–3 дня высыпания исчезают, не оставляя следов. Патогномоничным признаком внезапной экзантемы считают отсутствие сыпи на лице. Однако в некоторых случаях единичные пятна могут появиться на щеках, крыльях носа, ушных раковинах. Иногда развиваются диспептические расстройства, реже — неврологические нарушения (судороги, преходящие парезы). Заболевание протекает, как правило, без осложнений. При исследовании периферической крови обнаруживают выраженную лейкопению, эозинопению, гранулоцитопению (вплоть до агранулоцитоза) с относительным лимфоцитозом (до 80–90%). Нередко заболевание протекает под маской аллергической реакции, особенно в ситуации, когда педиатр на стадии лихорадки назначает антибактериальные препараты.
Диагностика. Диагноз внезапной экзантемы основывают на характерной клинической картине. Возможно проведение серологических исследований. Для выявления вируса используют ПЦР.
Лечение. Симптоматические средства.
Инфекция, вызываемая вирусом герпеса человека типа 7
Сведения о заболеваниях, вызываемых вирусом герпеса человека типа 7, весьма немногочисленны. Некоторые авторы связывают с этим вирусом развитие синдрома хронической усталости. Для последнего характерны субфебрильная лихорадка, боли в горле, лимфаденопатия, генерализованная мышечная слабость, мигрирующие артралгии и миалгии, расстройства сна, раздражительность, повышенная физическая утомляемость. Существуют сообщения о случаях специфических менингоэнцефалитов, вызванных вирусом герпеса человека типа 7. Предполагают наличие этиологической связи вируса герпеса человека типа 7 с лимфопролиферативными заболеваниями, эритемой новорожденных, реактивация инфекции протекает как миалгический энцефаломиелит.
Инфекция, вызываемая вирусом герпеса человека типа 8
Вирус герпеса человека типа 8 обнаруживают у 25% взрослого населения и 90% ВИЧ-инфицированных. Предполагают, что вирус может вызывать поражения кожи, внутренних органов и лимфатических узлов. Клинические проявления инфекции изучены недостаточно. По биологическим свойствам вирус герпеса человека типа 8 подразделяют на варианты А, В и С.
-
С вирусом герпеса человека типа 8A связывают развитие классической саркомы Капоши и ассоциированных с синдромом приобретенного иммунодефицита (СПИД) поражений кожи.
-
Вирусы герпеса человека типа 8B и 8C могут привести к развитию лимфопролиферативных заболеваний (лимфомы, генерализованной лимфаденопатии и т.д.).
Ситуационные задачи
-
Что из нижеперечисленного нехарактерно для инфекции вызванной простым герпесом типа 1:
-
Врач детского сада при осмотре детей средней группы обнаружил у ребенка 5 лет 2 пузырька на волосистой части головы и единичные папулы на груди. Заподозрена ветряная оспа. Укажите возможные источники инфицирования:
-
Ребенок 15 лет болен 2 нед. Заболевание начиналось постепенно с появления субфебрильной температуры тела, затруднения носового дыхания. В последние 3 дня температура повысилась до 38–39 °С. При осмотре обращает на себя внимание «гнусавость» голоса, увеличение лимфатических узлов всех групп, особенно заднешейных. Они эластичные, подвижные, не спаяны между собой, мало болезненны. Отмечена гиперемия зева. На миндалинах — налеты беловато-желтоватого цвета, легко снимающиеся, не распространяющиеся на дужки и мягкое нёбо. Печень выступает из-под края реберной дуги на 3 см, селезенка — на 2 см. В анализе крови: эритроциты 4,5×1012/л, гемоглобин 135 г/л, цветной показатель 0,9, лейкоциты 16×109/л, палочкоядерные 1%, сегментоядерные 34%, эозинофилы 1%, лимфоциты 48%, моноциты 16%, СОЭ — 12 мм/ч, атипичные мононуклеары — 12%. Сформулируйте предположительный диагноз. Обоснуйте ответ. У данного ребенка наиболее вероятен диагноз:
-
В детскую больницу поступила девочка 12 лет с жалобами на слабость, головокружение, субфебрильную температуру тела в течение 2 нед. В статусе: кожа бледная, отмечена субиктеричность склер. Миндалины увеличены, разрыхлены. Пальпируются передне- и заднешейные, подмышечные, паховые лимфатические узлы до 0,3–0,5 см, не спаянные между собой и с окружающими тканями, безболезненные. Отмечена пастозность лица. По органам без патологии. Пальпация живота: поверхностная — безболезненная,. печень +3 см, край печени гладкий. Селезенка пальпируется у края реберной дуги. Общий анализ крови: эритроциты 3,6×1012/л, гемоглобин 109 г/л, цветовой показатель 0,8, лейкоциты 7×109/л, палочкоядерные 1%, сегментоядерные 35%, эозинофилы 5%, лимфоциты 38%, моноциты 16%, СОЭ 19 мм/ч. Биохимический анализ крови: АЛТ 7 норм, АСТ 5 норм, общий билирубин 52 мкмоль/л, ДНК вируса ВГВ и РНК HCV — отрицательно. Сформулируйте предположительный диагноз. Обоснуйте ответ. У данного ребенка наиболее вероятен диагноз:
-
Ребенок 7 лет болен 3-й день. Заболевание началось остро с повышения температуры тела до 38,5 °С, появления единичных везикул на лице и волосистой части головы. При осмотре — на коже лица, туловища, конечностей — полиморфная сыпь в виде папул, везикул, корочек. На слизистой оболочке полости рта — везикулы и поверхностные язвочки. Температура тела 37,5 °С. У данного ребенка наиболее вероятен диагноз:
Ответы: 1 — b; 2 — b; 3 — a; 4 — a; 5 — a; 6 — c.