|
Russian Association of Oncological Mammology http://www.breastcancersociety.ru/ http://www.bcguidelines.ru/ Клинические рекомендации РООМ по неоадъювантной и адъювантной терапии РМЖ.(электронная версия). |
Клинические рекомендации РООМ по диагностке и лечению рака молочной железы in situ
Семиглазов В.В.
Член правления РООМ.
Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П.Павлова
НМИЦ онкологии им. Н.Н.Петрова Минздравсоцразвития России, Санкт-Петербург
© Общероссийская общественная организация «Российское общество онкомаммологов».
2018г.
Все права защищены. Никакая часть данной книги не может быть воспроизведена в какой бы то ни было форме и какими бы то ни было средствами без письменного разрешения правообладателя.
Совет Экспертов РООМ
|
Семиглазов Владимир Федорович Академик РАЕН, Член-корреспондент РАН, доктор медицинских наук, профессор. Президент Российского общества онкомаммологов |
|
Манихас Георгий Моисеевич Главный врач Санкт-Петербургского Государственного Учреждения Здравоохранения «Городской клинический онкологический диспансер». Доктор медицинских наук. Заслуженный врач РФ. Зав. кафедрой онкологии факультета последипломного образования ГМУ им. акад. И.П. Павлова. Вице-президент Российского общества онкомаммологов |
|
Палтуев Руслан Маликович Старший научный сотрудник ФГБУ НИИ Онкологии им. Н.Н. Петрова. Исполнительный директор Российского общества онкомаммологов |
|
Апанасевич Владимир Иосифович Главный врач Санкт-Петербургского Государственного Учреждения Здравоохранения «Городской клинический онкологический диспансер». Доктор медицинских наук. Заслуженный врач РФ. Зав. кафедрой онкологии факультета последипломного образования ГМУ им. акад. И.П. Павлова. Председатель регионального отделения Российского общества онкомаммологов Приморского края |
|
Артамонова Елена Владимировна Доктор медицинских наук, ведущий научный сотрудник отделения изучения новых противоопухолевых лекарств РОНЦ им. Н.Н.Блохина МЗ РФ. Член Российского общества онкомаммологов |
|
Бесова Наталия Сергеевна Кандидат медицинских наук, старший научный сотрудник отделения химиотерапии ФГБУ Российского онкологического центра им. Н. Н. Блохина МЗ РФ. Член Российского общества онкомаммологов |
|
Божок Алла Александровна (Ученый секретарь РООМ) Доктор медицинских наук, онколог высшей квалификационной категории, пластический хирург. Ученый секретарь Российского общества онкомаммологов |
|
Владимиров Владимир Иванович Доктор медицинских, профессор. Член Российского общества онкомаммологов |
|
Возный Эдуард Кузьмич Заведующий отделением химиотерапии ГКБ №57, президент московского общества химиотерапевтов. Член Российского общества онкомаммологов |
|
Высоцкая Ирина Викторовна Профессор, кафедры онкологии ГБОУ ВПО 1МГМУ им. И.М.Сеченова. Член Российского общества онкомаммологов |
|
Горбунова Вера Андреевна Заведующая отделением химиотерапии ГУ Российский онкологический научный центр им. академика Н.Н. Блохина МЗ РФ, доктор медицинских наук, профессор. Член Российского общества онкомаммологов |
|
Дашян Гарик Альбертович Ведущий научный сотрудник отделения опухолей молочной железы ФГБУ «НИИ онкологии им. Н.Н. Петрова» Минздрава, доктор медицинских наук. Член правления Российского общества онкомаммологов |
|
Демидов Сергей Михайлович Доктор медицинских наук, заведующим кафедрой онкологии и медицинской радиологии. Член Российского общества онкомаммологов |
|
Ермощенкова Мария Владимировна К.м.н, научный сотрудник Московского научно-исследовательского онкологического института имени П.А. Герцена. Член Российского общества онкомаммологов |
|
Зикиряходжаев Азиз Дильшодович Доктор медицинских наук, заведующий отделением опухолей молочной железы, ведущий научный сотрудник ФГБУ "НИИ онкологии им. Н.Н. Петрова" МЗ РФ, профессор кафедры онкологии СЗГМУ им. И.И. Мечникова. Член Российского общества онкомаммологов |
|
Захарова Наталья Александровна Доктор медицинских наук, профессор кафедры онкологии, лучевой диагностики и лучевой терапии Ханты-Мансийской государственной медицинской академии. Член Российского общества онкомаммологов |
|
Исмагилов Артур Халитович Доктор медицинских наук, профессор кафедры онкологии и хирургии КГМА, ведущий научный сотрудник отдела реконструктивной хирургии Приволжского филиала ФГБУ «РОНЦ им. Н.Н. Блохина» МЗ РФ. Член Российского общества онкомаммологов |
|
Константинова Мария Михайловна доктор медицинских наук, профессор, заместитель директора по лечебной работе, главный врач ФГБУ «Институт хирургии имени А.В. Вишневского». Член Российского общества онкомаммологов |
|
Корытова Луиза Ибрагимовна Заслуженный деятель науки, доктор медицинских наук, профессор. Член правления Российского общества онкомаммологов |
|
Криворотько Петр Владимирович доктор медицинских наук, заведующий отделением опухолей молочной железы, ведущий научный сотрудник ФГБУ «НИИ онкологии им. Н.Н. Петрова» МЗ РФ, профессор кафедры онкологии СЗГМУ им. И.И. Мечникова. Член Российского общества онкомаммологов |
|
Кудайбергенова Асель Галимовна К.м.н., старший научный сотрудник лаборатории клинической цитологии ФГБУ «Российский онкологический научный центр им. Н.Н.Блохина» МЗ РФ, врач-патологоанатом патологоанатомического отделения ФГБУ «НИИ онкологии им. Н.Н. Петрова» МЗ РФ. Член Российского общества онкомаммологов |
|
Лазарев Александр Федорович Главный врач КГБУЗ «Алтайский краевой онкологический диспансер», директор Алтайского филиала ФГБУ РОНЦ им.Н.Н. Блохина МЗ РФ, заведующий кафедрой онкологии ГОУ ВПО «Алтайский государственный медицинский университет». Член Российского общества онкомаммологов |
|
Летягин Виктор Павлович Профессор, главный научный сотрудник этого хирургическим отделением опухолей молочных желез. Член Российского общества онкомаммологов |
|
Манзюк Людмила Валентиновна Доктор медицинских наук, профессор. Член Российского общества онкомаммологов |
|
Манихас Алексей Георгиевич Доктор медицинских наук, врач первой категории, хирург, онколог, заведующего 1 хирургическим (маммологическим) отделением СПб ГУЗ ГКОД. Член правления Санкт-Петербургского регионального отделения Российского общества онкомаммологов |
|
Маслюкова Елизавета Александровна К.м.н., научный сотрудник отделения лучевой терапии онкологических заболеваний ФГБУ «Российский научный центр радиологии и хирургических технологий», врач-радиотерапевт. Член Российского общества онкомаммологов |
|
Орлова Рашида Вахидовна Доктора медицинских наук, профессор кафедры онкологии Медицинской Академии последипломного образования, профессор кафедры госпитальной хирургии с курсом клинической онкологии медицинского факультета СПБГУ, ведущий научный сотрудник ФГУ Российского научного центра радиологии и хирургических технологий. Член Российского общества онкомаммологов |
|
Переводчикова Наталия Иннокентьевна Профессор, доктор медицинских наук – является ведущим научным сотрудником отделения химиотерапии ФГБУ «Российский онкологический центр им. Н.Н. Блохина». Член Российского общества онкомаммологов |
|
Пожарисский Казимир Марианович Зав. лабораторией, профессор, доктор медицинских наук, академик РАЕН, член международной академии патологии. Член правления Российского общества онкомаммологов |
|
Портной Сергей Михайлович Ведущий научный сотрудник Российский онкологический научный центр им. Н.Н. Блохина МЗ РФ |
|
Савёлов Никита Александрович К.м.н., ведущий специалист по ИГХ и ISH диагностике патологоанатомического отделения ГАУЗ «Московская городская онкологическая больница № 62» ДЗМ. Член Российского общества онкомаммологов |
|
Семиглазов Владислав Владимирович Доктор медицинских наук, заведующий кафедрой онкологии Санкт-Петербургского Государственного медицинского университета им. акад. И.П.Павлова, ведущий научный сотрудник отделения общей онкологии НИИ онкологии им. Н.Н.Петрова. Член Российского общества онкомаммологов |
|
Семиглазова Татьяна Юрьевна Старший научный сотрудник отдела терапевтической онкологии ФГБУ «НИИ онкологии им. Н.Н. Петрова» Минздравсоцразвития, доцент кафедры Северо-Западного государственного медицинского университета им. И.И. Мечникова, врач высшей категории, кандидат медицинских наук. Член правления Российского общества онкомаммологов |
|
Слонимская Елена Михайловна Доктор медицинских наук, профессор, руководитель отделения общей онкологии НИИ онкологии СО РАМН, профессор кафедры онкологии Сибирского Государственного медицинского университета, Заслуженный врач РФ. Член правления Томского регионального отделения Российского общества онкомаммологов |
|
Строяковский Даниил Львович К.м.н., зав. химиотерапевтическим отделением МГОБ №62. Член Российского общества онкомаммологов |
|
Топузов Эльдар Эскендерович доктора медицинских наук , заведующий кафедрой госпитальной хирургии ГБОУ ВПО СЗГМУ им. И.И.Мечникова. Член Российского общества онкомаммологов |
|
Трофимова Оксана Петровна Доктор медицинских наук, профессор, ведущий научный сотрудник ФГБУ «РОНЦ им. Н.Н.Блохина» МЗ РФ. Член Российского общества онкомаммологов |
|
Хайленко Виктор Алексеевич Доктор медицинских наук, профессор, академик РАЕН, заведующий кафедрой онкологии Факультета усовершенствования врачей Российского национального исследовательского медицинского университета. Член Российского общества онкомаммологов |
|
Чагунава Олег Леонтьевич Главный врач Федерального государственного бюджетного учреждения здравоохранения Санкт-Петербургской клинической больницы Российской академии наук, кандидат медицинских наук,врач-хирург, онколог-маммолог. Член Российского общества онкомаммологов |
|
Шатова Юлиана Сергеевна Ведущий научный сотрудник ФГБУ «Ростовский научно-исследовательский онкологический институт» МЗ РФ, отделение опухолей костей, кожи, мягких тканей и молочной железы №1, Председатель регионального отделения Российского общества онкомаммологов Ростовской области |
|
Шинкарев Сергей Алексеевич Доктор медицинских наук. Член Российского общества онкомаммологов |
| Уровень | Тип доказательности |
|---|---|
I |
Доказательства получены в результате мета-анализа большого числа хорошо спланированных контролируемых исследований. Рандомизированные исследования с низким уровнем ложно-позитивных и ложно-негативных ошибок |
II |
Доказательства основаны на результатах не менее одного хорошо спланированного эспериментального исследования. Рандомизированные исследования с высоким уровнем ложно-позиивных и ложно-негативных ошибок |
III |
Доказательства основаны на результатах хорошо спланированных экспериментальных исследований. Нерандомизированные контролируемые исследования с одной группой больных, исследования с группой исторического контроля и т.д. |
IV |
Доказательства получены в результате хорошо спланированных не экспериментальных исследований. Непрямые сравнительные, описательно корреляционные исследования и исследования клинических случаев |
V |
Доказательства основаны на клинических случаях и примерах |
| Уровень | Тип доказательности |
|---|---|
A |
Рекомендации подготовлены на основе мета-анализа рандомизированных контролируемых испытаний или на основе данных одного рандомизированного контролируемого клинического испытания |
B |
Рекомендации подготовлены на основе данных контролируемого нерандомизированного испытания или на основе данных испытания с высоким уровнем дизайна, например, когортные исследования |
C |
Рекомендации подготовлены на основе данных описательных исследований: исследования «случай-контроль», сравнительные исследования, корреляционные исследования, одномоментные исследования |
D |
Рекомендации подготовлены на основе исследований отдельных случаев. |
Глубокоуважаемые коллеги!
Одна из первоочередных задач Российского общества онкомаммологов (РООМ) – создать клинические рекомендации по диагностике и лечению рака молочной железы (РМЖ), учитывающие международный опыт и в то же время доступные к использованию во всех регионах Российской Федерации.
В Европе и Америке врачи опираются на клинические рекомендации, издаваемые профессиональными сообществами. Рекомендации – это обобщенный опыт авторитетных экспертов, основанный на доказательной медицине.
Представленные клинические рекомендации основаны на согласительных документах
При этом учтены результаты анализа кумулятивной базы данных по методам лечения РМЖ
Сейчас много говорится о необходимости введения единых стандартов лечения онкологических заболеваний.
Мы хотим, чтобы все российские специалисты были в курсе самых последних диагностических и лечебных стратегий. При этом в основе наших рекомендаций лежат методики, доступные к использованию на всей территории Российской Федерации; схемы лечения и препараты размещены в соответствии с регистрационными удостоверениями Минздрава России. Таблицы лекарственной терапии составлены с учетом биологических подтипов РМЖ, различных вариантов течения заболевания, а также принимая во внимание неодинаковую ситуацию с лекарственным обеспечением в различных регионах РФ.
Конечно, подобные материалы не могут быть прямым руководством к действию, болезнь каждой пациентки имеет свои особенности. Но они могут быть хорошим подспорьем в работе врача, стремящегося лечить пациентов согласно самым последним достижениям современной онкологии.
Общероссийская общественная организация «Российское общество онкомаммологов» (РООМ)
Президент Общества – член-корр. РАМН, проф. В. Ф. Семиглазов
Вице-президент Общества – член-корр. РАН, проф. Г. М. Манихас
Исполнительный директор Общества – к. м. н. Р. М. Палтуев
Клинические рекомендации РООМ по диагностке и лечению рака молочной железы in situ
|
Семиглазов В.В. Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П.Павлова |
Результатом широкого внедрения программ маммографического срининга явилось значительное увеличение частоты выявления неинвазивных форм рака молочной железы (РМЖ). Среди неинвазивных эпителиальных опухолей более чем в 80 % случаев клиницисты сталкиваются с протоковым раком in situ (DCIS).
Карцинома in situ является формой рака, представленного пулом злокачественных эпителиальных клеток, не вовлекающих в процесс базальную мембрану, но потенциально способных к инвазии. Экспрессия рецепторов эстрогенов, генов р53, HER-2 / neu, циклина D и уровень генетической нестабильности может достигать пика уже при раке in situ (CIS). Это свидетельствует о том, что большинство генетических ступеней в развитие опухоли происходят до инвазивного этапа. В этом смысле карцинома in situ мало чем отличается от инвазивного рака молочной железы. Однако до сих пор остается неясным, какие факторы определяют инвазивный потенциал DCIS, так как не все случаи протоковой карциномы in situ даже высокой степени злокачественности или HER2‑позитивные в конечном счете заканчиваются развитием инвазивного рака.
Истинная карцинома in situ, как и инвазивный рак является гетерогенным, но относительно благоприятным заболеванием при условии правильного подхода к ее диагностике и лечению. Несмотря на схожесть многих морфо-генетических параметров, эти заболевания отличаются по течению, прогнозу и ответу на локальные и системные методы воздействия.
Современная стратегия ведения больных с DCIS включает широкий спектр лечебных мероприятий, основным из которых является хирургическое вмешательство. Объем операций варьирует от секторальной резекции до мастэктомии. Органосохраняющие операции нередко сочетаются с лучевой терапией и гормонотерапией. Такое разнообразие вариантов лечения обусловлено не только клинико-морфологической гетерогенностью DCIS, но и, как указывалось выше, отсутствием надежных факторов, определяющих инвазивный потенциал и соответственно прогноз CIS.
Наиболее эффективным методом лечения карциномы in situ по‑прежнему остается хирургическое вмешательство.
Мастэктомия при истинной CIS сопровождается практически 100 %-й безрецидивной и общей выживаемостью. До настоящего времени нет убедительных рандомизированных клинических исследований, сравнивающих эффективность мастэктомии и органосохраняющих операций при DCIS, тем не менее, первая остается «стандартом», с которым сравнивают остальные методы лечения.
Показания к мастэктомии: 1) больные с большим размером опухоли (более 5 см), не позволяющим выполнить органосохраняющую операцию радикально; 2)больные с мультицентричной или мультифокальной формами DCIS при относительно малом размере молочной железы; 3) больные с пограничным размером опухоли, которые не могут подвергаться лучевой терапии (например, из‑за сопутствующей патологии или предыдущей лучевой терапии на грудную клетку по поводу другого заболевания).
В настоящее время широко применяются кожесохраняющие мастэктомии, которые по показателям общей выживаемости не уступают обычной мастэктомии. Однако вероятность рецидива при подобных операциях увеличивается, так как могут сохраняться резидуальные ткани железы в проекции кожного лоскута. Риск рецидива снижается при уменьшении толщины лоскута. Однако уменьшение толщины лоскута может осложниться его некрозом, что связано с нарушением кровоснабжения кожи. По данным Timbrell at al. (25) фактором риска рецидива при подкожной мастэктомии помимо позитивного хирургического края является молодой возраст женщин с ER-негативными формами DCIS. Как правило, рецидив (чаще инвазивный) возникает у женщин с агрессивным типом опухоли (высокая степень злокачественности, HER2+, ER-).
Органосохраняющее лечение. Многие исследования указывают на то, что при CIS общая выживаемость после сохранных и радикальных операций практически идентична. В результате, последние годы все больше больных при определенных показаниях подвергаются органосохраняющему лечению. Однако возрастает вероятность возникновения рецидива при уменьшении объема операции. При проведенном в НИИ онкологии им. Н. Н. Петрова патоморфологическом исследовании препаратов после операций по поводу рецидивов после сохранного лечения в 58 % случаев выявлено наличие не CIS, а потенциально угрожающего жизни инвазивного рака. Это говорит о необходимости оценки факторов риска развития местного рецидива при планировании органосохраняющего лечения. Проанализировано множество факторов, среди которых наибольшее прогностическое значение имели лишь несколько: степень гистологической злокачественности, размер опухоли, ширина резекции и возраст.
Степень гистологической злокачественности. Степень гистологической злокачественности является признанным морфологическим прогностическим маркером при инвазивном раке. Данный признак наряду с наличием некроза используют и в классификации протоковых форм карциномы in situ. В его основу положен размер и строение ядра. В исследованиях показано, что частота местного рецидивирования резко возрастает при карциноме in situ промежуточной и высокой степени злокачественности после экономных иссечений. Необходимо отметить, что при выполнении сегментарной резекции и квадрантэктомии местные рецидивы регистрируются редко и не зависят от степени злокачественности, т. е. данный фактор теряет свою прогностическую значимость при увеличении ширины краев резекции.
Размер первичной опухоли (характер роста). Размер является одним из важных факторов риска развития местных рецидивов при минимальном инвазивном и инвазивном РМЖ. Доказано, что увеличение размера опухоли сопровождается увеличением частоты рецидивов при сохранных операциях. По данным Lagios и соавт. [16], увеличение размера опухоли при раке in situ с 15 мм до 40 мм сопровождается удвоением количества рецидивов (25.5 % и 57 % соответственно).
Наибольшее количество местных рецидивов фиксируется при наличии дополнительных микрофокусов опухоли, т. е. при мультифокальном (мультицентричном) росте, когда сложно измерить истинный объем опухоли и определить адекватные края резекции с достаточным (> 1 см) отступлением от края опухоли. Именно из‑за недооценки хирургом того, что при карциноме in situ опухоль зачастую распространяется за пределы ее клинически и макроскопически определяемых краев, значительно увеличивается риск местного рецидива.
Ширина резекции. Статус краев резекции. По данным M. Lagios и соавт. [15, 16] увеличение ширины краев резекции от 1 мм до 10 мм приводит к снижению частоты местного рецидивирования практически в 5 раз (c 42 % до 8.3 %). M. Silverstein [23] утверждает, что при достаточной ширине резекции (10 мм и более) размер опухоли и степень гистологической злокачественности практически не влияют на риск развития местного рецидива.
Мета-анализ рандомизированных исследований эффективности лечения DCIS (EBCTCG), показал, что у пациентов с позитивными краями резекции, несмотря на проведенную лучевую терапию, удваивался риск возникновения местных рецидивов по сравнению с пациентами с негативными краями (10‑летняя частота рецидивов 24 % против 12 %) и приблизительно у 50 % наблюдались инвазивные рецидивы (4).
По данным исследования Van Zee и соавт. (26), в которое включено 1266 пациентов, подвергшихся только операции по поводу DCIS, 10‑летняя частота местных рецидивов равнялась 16 % при ширине краев резекции > 10 мм, 23 % – 2,1–10 мм, 27 % – > 0–2 мм и 41 % при позитивных краях.
В мета-анализе, проведенном Marinovich и соавт. (19) выполнена оценка влияния ширины края резекции (0, 1 мм против 2 мм, 3 или 5 мм и 10 мм) на прогноз. В исследовании участвовало 7883 пациентов со средним периодом наблюдения 6,5 лет. В исследовании не было обнаружено существенных различий в частоте местных рецидивов при ширине краев резекции – 2 мм, 3 мм, 5 мм и 10 мм (P> 0,40), выявлен рост частоты рецидивов при ширине резекции менее 2 мм. В этой модели прогнозируемая 10‑летняя вероятность развития местного рецидива для негативных краев резекции 2 мм равнялась 10,1 % (95 % ДИ 6,3 % – 16,0 %), в сравнении с 8,5 % при 3 или 5 мм (95 % ДИ 3,6 % – 18,9 %), и 11,7 % при крае резекции в 10 мм (95 % ДИ 6,7 % – 19,4 %).
В результате, в соответствии с рекомендациями SSO, ASTRO, ASCO, основанных на мета-анализе 20 исследований (20), допустимая ширина резекции при выполнении органосохраняющих операций при DCIS составляет не менее 2 мм при условии проведения послеоперационной лучевой терапии. Увеличение ширины резекции не приводит к достоверному улучшению результатов лечения. Ширина краев резекции менее 2 мм сопровождается ростом частоты местных рецидивов. При позитивных краях резекции ЛТ не позволяет достоверно снизить частоту местных рецидивов. По мнению экспертов такая рекомендация позволит уменьшить число неоправданных повторных операций, улучшить кометические результаты лечени, а также снизит затраты на лечение. Оптимальная ширина резекции при выполнении только сохранной операции без адъювантного лечения пока не определена, но должна быть не менее 2 мм.
Существуют определенные трудности в оценке краев резекции. В частности при оккультной мультицентричности отсутствие опухоли в крае резекции не говорит об отсутствии очагов рака in situ в оставшейся молочной железе. Кроме того, нередко встречаются технические ограничения оценки края резекции. Например, края резекции искусственно изменяется в условиях ex-vivo, когда препараты сокращается из‑за отсутствия окружающей поддерживающей ткани. Кроме того, краситель может проникать в более глубокие слои препарата, что создает значительные проблемы в определении истинной локализации края резекции. Наконец, расстояние от опухоли до красителя на любом одном срезе может не соответствовать расстоянию в целом хирургическом препарате. «Адекватный» край резекции на одном срезе может стать позитивным при исследовании дополнительных или более глубоких секций препарата. Существует два самых распространенных метода оценки краев резекции: секционирование перпендикулярно окрашенной поверхности (для определения расстояние от опухоли до красителя) или исследование поверхности «бритых» краев (где наличие любой остаточной опухоли в «бритом» крае говорит о том, что он позитивен). Хотя преимуществом «бритого» метода является более тщательное исследование поверхности края резекции, известным его недостатком является более высокая частота обнаружения ложно-позитивных краев резекции, которые фактически являются негативными при перпендикулярном методе исследования. Это, в свою очередь, может привести к ненужной реэксцизии или даже мастэктомии (11).
Эффективность секционирования операционного препарата может варьировать: даже полная последовательная вырезка позволяет оценить лишь малую часть поверхности края резекции (<1 %). Вместе эти исследования подчеркивают существенную вариабельность оценки края резекции вне зависимости от используемой методики
Возраст больных. Ряд исследований показал, что на риск развития местного рецидива влияет и возраст. У женщин 40 лет и моложе выявлено достоверное увеличение частоты развития местных рецидивов по сравнению со старшей группой. Скорее всего, это связано с преобладание у молодых DCIS высокой степени гистологической злокачественности и камедонекроза. В исследовании Kim K. (14) больные, подвергшиеся органосохраняющему лечению без лучевой терапии стратифицированы в две группы: ≤ 50 лет и > 50 лет. При 6‑летнем наблюдении в старшей возрастной группе местных рецидивов не зарегистрировано, а у больных ≤ 50 лет частота рецидивов при ширине края резекции ≥ 1 см составила 1.2 %, а < 1 см – 13.1 %
Таким образом, ширина резекции, т. е. расстояние от края опухоли до границы хирургического препарата является одним из наиболее важных факторов, определяющих риск рецидива заболевания. Несмотря на увлечение сверхэкономными операциями, при макроскопически видимой опухоли ширина резекции не должна быть меньше 1 см, при отсутствии видимых границ необходимо все внимание сосредоточить на патоморфологическом исследовании краев резекции. Оптимальная ширина резекции, оцененная при патоморфологическом исследовании должна быть не менее 2 мм.
Подмышечная лимфаденэктомия. Подмышечная лимфаденэктомия у больных с DCIS, особенно при небольших, маммографически выявленных опухолях, как правило, не производится, так как количество оккультных инвазивных карцином, сопровождающихся метастазированием в аксиллярные лимфатические узлы, не превышает 1–3 %. Больным, которым производится мастэктомия при пальпируемом поражении, при высокой степени гистологической злокачественности и диффузной микрокалицификации, т. е. при высоком риске микроинвазии, в последнее время выполняется биопсия сигнальных узлов (sentinel node biopsy).
При DCIS с микроинвазией метастазы в подмышечных лимфатических узлах выявляются в 10 % случаев, поэтому целесообразно выполнение биопсии сигнальных лимфатических узлов.
Лучевая терапия (ЛТ). Результаты исследований эффективности послеоперационной лучевой терапии больных с DCIS, полученные в настоящее время, достаточно противоречивые.
В рамках NSABP (протокол В-17) было проведено проспективное исследование роли ЛТ при выполнении органосохраняющего лечения у больных с протоковой карциномой in situ. Восемьсот восемнадцать больных подвергались либо одним органосохраняющим операциям, либо сохранным операциям c последующей лучевой терапией. В результате было зарегистрировано значительное снижение частоты развития местных рецидивов, в особенности рецидивов с инвазивным компонентом среди больных, подвергшихся послеоперационной лучевой терапии. Восьмилетняя частота рецидивирования составила 27 % и 12 %соответственно, а через 10 лет (август 1999 г.) – 31 % и 13 % соответственно. Полученные данные позволили NSABP рекомендовать проведение послеоперационной лучевой терапии всем больным с протоковой карциномой in situ, которым планируется выполнение сохранных операций (7).
Однако приблизительно для 30–40 % больных с протоковой карциномой in situ, которым выполняются органосохраняющие операции, последующая ЛТ, как и мастэктомия, является избыточным лечением. Поэтому в ряде работ делается акцент на тщательном подборе больных, у которых вероятность дополнительного положительного эффекта ЛТ высокая.
М. Lagios [15] в своем исследовании попытался оценить эффективность ЛТ при DCIS с учетом факторов риска развития местных рецидивов. Отмечена высокая эффективность ЛТ при DCIS высокой степени гистологической злокачественности, но не обнаружено никакого преимущества ЛТ при низкой степени гистологической злокачественности. ЛТ оказала положительный эффект в группе больных с DCIS высокой степени гистологической злокачественности при ширине края резекции 10 мм и 1–9 мм (частота рецидивов 0 % и 29 % соответственно, против 8.3 % и 40.5 % без ЛТ), при крае более 10 мм ЛТ не влияла на прогноз.
L. Hughes и соавт. [13] (протокол ECOG 5194, 2009 г.) проанализировали эффективность широкого иссечения DCIS без адъювантной ЛТ. В исследование были включены больные с DCIS низкой и промежуточной степенями злокачественности размером ≤ 2,5 см (I группа) и высокой степенью злокачественности размером ≤ 1 см (II группа) с шириной резекции более 3 мм.
При среднем времени наблюдения 6,2 года в I-й группе и 6,7 лет во II-й группе зарегистрированы местные рецидивы в 6,1 % и 15,3 % случаев соответственно. Результаты исследования указывают на достаточно высокую частоту местных рецидивов у больных с DCIS высокой степени злокачественности, что свидетельствует о неадекватности одного лишь экономного иссечения даже при минимальном размере (<10 мм) опухоли. В первой группе отмечена низкая частота выявления местных рецидивов, что не требует проведения дополнительных лечебных мероприятий. Однако этот факт, по мнению авторов, может быть доказан только после более длительного наблюдения за этой группой пациентов. В 2015 году представлены данные о 12‑летней частоте развития рецидивов. Местный рецидив выявлен у 14,4 % пациентов с DCIS низкой степени злокачественности, размером не более 2,5 см и 24,6 % при DCIS высотой степени злокачественности, размером до 1 см. Однако частота рецидивов существенно не различалась при краях резекции <5 мм, 5–9 мм или 10 мм (P = 0.85) (24).
Полученные в данной работе результаты инициировали два сравнительных исследования, посвященных эффективности дистанционной лучевой терапии и брахитерапии у больных, подвергшихся органосохраняющим операциям. Критерии включения в исследования были абсолютно идентичны критериям, использованным в ECOG 5194. S. Motwani и соавт. [21], используя дистанционную ЛТ в адъювантном режиме, отмечают снижение частоты местных рецидивов (при среднем периоде наблюдения 6.9 лет) в обеих группах: 1,5 % по сравнению с 6.1 % в ECOG 5194 в первой группе; 2,0 % и 15,3 % соответственно – во второй. Таким образом, дистанционная ЛТ уменьшила вероятность развития рецидива более чем на 70 % в обеих группах. При этом число билатеральных опухолей в этих исследованиях было одинаковым.
В работе S. Goyal и соавт. [10] (Mammosite Registry Trial) относительно небольшая группа пациентов (N=70) в течение 5–7 дней подвергалась брахитерапии на ложе опухоли. При среднем сроке наблюдения 52,7 мес. (0–88,4), с учетом критериев и отдаленных результатов исследования ECOG 5194, в I и II группах зарегистрированы местные рецидивы в 0 % и 5,3 % случаев соответственно. Частота рецидивов в общей группе больных вне зависимости от размера опухоли, степени злокачественности и состояния краев резекции в данном исследовании не превышала 3 %. Учитывая хорошие результаты лечения, а также короткий, удобный для больных курс лечения, авторы предлагают более детально исследовать и чаще использовать данную методику, которая возможно расширит показания к органосохраняющим операциям.
Практически все исследования, сравнивающие комбинированное лечение с одним хирургическим демонстрируют явное снижение частоты местных рецидивов при проведении адъювантной лучевой терапии, хотя это преимущество у больных с прогностически благоприятными признаками остается сравнительно небольшим и спорным. В частности в работе Kim K. (14), результаты которой указаны выше, в группе больных старше 50 лет, подвергшихся сохранному лечению с шириной резекции более 1 см без последующей ЛТ, частота рецидивов при 6‑летнем наблюдении составила 0 %. М. Lagios проанализировал влияние ширины краев резекции на эффективность ЛТ. Частота местных рецидивов при ширине хирургического края 10 мм или более равнялись 4.5 % без ЛТ и 5 % в группе с ЛТ.
Учитывая незначительный эффект ЛТ у определенной группы пациентов, вопрос о ее целесообразности требует дальнейшего изучения в рандомизированных исследованиях.
Адъювантная терапия. Адъювантная цитотоксическая терапия у больных с DCIS не проводится.
Если у пациентки, подвергшейся оперативному вмешательству по поводу предполагаемой DCIS, обнаруживают инвазивный фокус, то последующее лечение должно соответствовать лечению больных с установленной патологической стадией и биологическим подтипом РМЖ.
Иначе дело обстоит с гормональным лечением. Рандомизированные клинические испытания, проведенные B. Fisher в проекте NSABP, показали, что назначение тамоксифена в дозе 20 мг / сут в течение 5 лет больным с DCIS, подвергшимся органосохраняющему лечению и ЛТ, снижает частоту инвазивных рецидивов в той же молочной железе (6). Кроме того, гормонотерапия существенно снижает частоту как инвазивных, так и неинвазивных ER-позитивных опухолей в контрлатеральной молочной железе, не влияя на частоту ER-негативных опухолей.
В данном проекте при 15‑летнем наблюдении частота местных рецидивов в группе лампэктомия+ЛТ+плацебо достигала 17,4 % у пациентов с позитивными краями и 7,4 % у пациентов с негативными краями резекции. При добавлении тамоксифена частота рецидивов при позитивных краях достигла 11.5 %, а при негативных – 7.5 %. [27]. Таким образом, тамоксифен снижает риск местного рецидива у пациентов с позитивными краями резекции и не влияет на риск рецидива при негативных На показатели общей выживаемости назначение препарата не влияет.
Кооперативное исследование UK / ANZ (Великобритания, Австралия и Новая Зеландия) не выявило существенного эффекта гормонотерапии у больных, подвергавшихся ЛТ, что, видимо, связано с исключением из исследования пациентов с позитивными краями [12], хотя по последним обновленным данным выявлено снижение риска развития неинвазивного рецидива низкой и промежуточной степени злокачественности.
В проектах IBIS-II и NSABP В-35 оценена роль ингибиторов ароматазы (анастрозола) у постменопаузальных больных DCIS, которые подвергались сохранным операциям + ЛТ. Цель исследований – определить промежуток времени от момента рандомизации до выявления рака (рецидива или нового случая) и оценить общую выживаемость и качество жизни (Рис. 1).
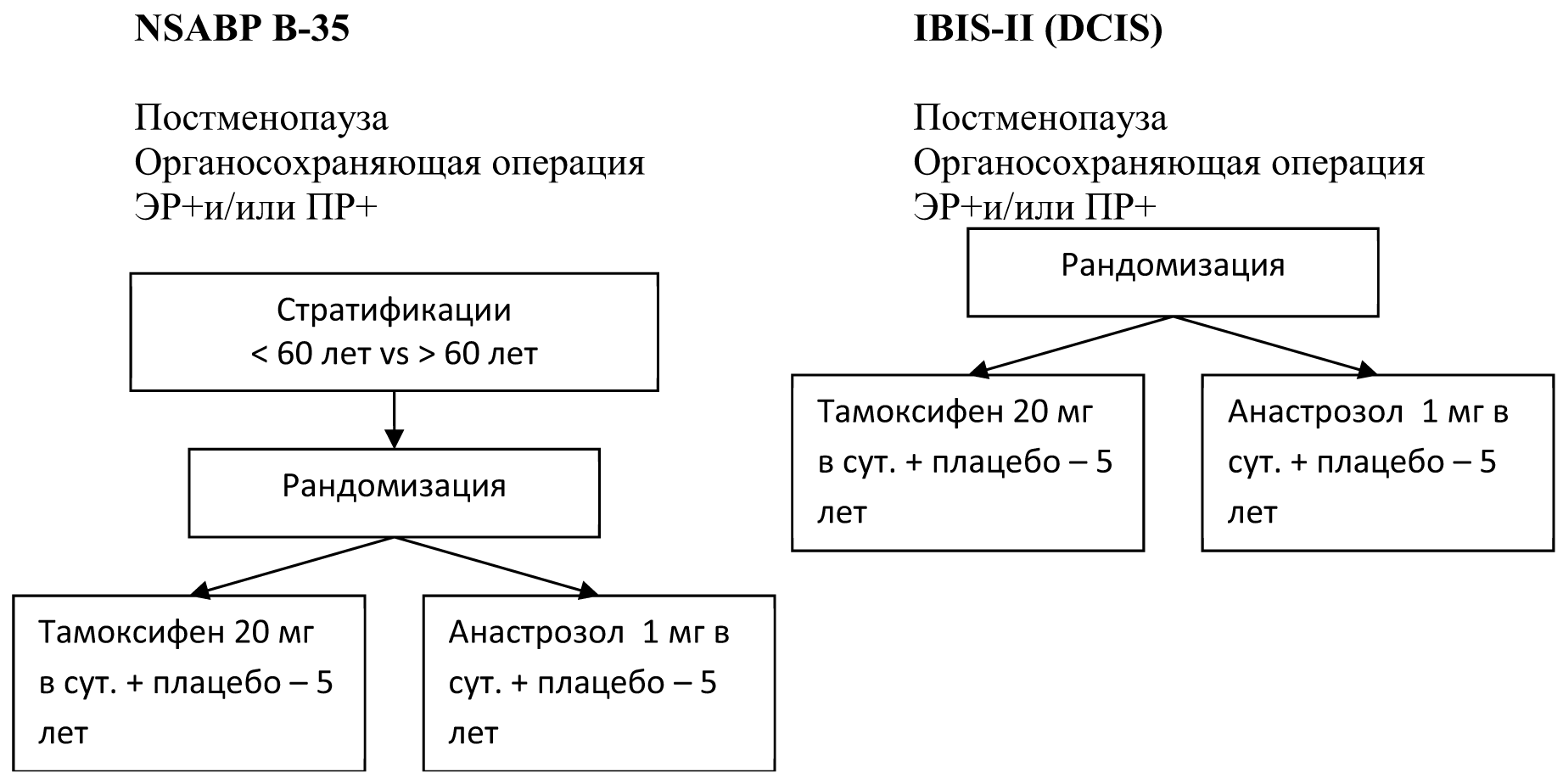
По данным проекта NSABP В-35 показатели 10‑летней безсобытийной выживаемости оказались лучше в группе анасторозола по сравнению с тамоксифеном (83 % и 78 %, соответственно). Однако преимущество анастрозола зарегистрировано только у больных в постменопаузе моложе 60 лет (18). Не выявлено существенного влияния гормонотерапии на риск развития инвазивого рака в ипсилатеральной молочной железе, однако зарегистрировано снижение данного риска в контрлатеральной железе, с наибольшей достоверностью в группе анастрозола.
В проекте IBIS-II при 10‑летнем наблюдении не выявлено достоверных отличий показателей безрецидивной выживаемости между группами больных, подвергавшихся терапии тамоксифеном или анастрозолом (частота рецидивов 7.3 % и 6.6 %, соответственно). Однако выявлено существенное преобладание инвазивных ЭР+HER2‑отр. рецидивов при терапии тамоксифеном по сравнению с анастрозолом (9). Кроме того, зарегистрировано снижение риска контрлатерального РМЖ. В данном проекте не было стратификаци по возрасту.
Гормонотерапия не влияет на показатели общей выживаемости, позволяет снизить риск рецидива при позитивных краях, а также риск развития опухоли
вконтрлатеральной молочной железе. Однако такой вид лечения не снижает риск рецидива в ипсилатеральной железе у больных, которым выполнена адекватная операция с негативными хирургическими краями и проведена лучевая терапия. Кроме того, гормонотерапия нередко сопровождается серьезными побочными эффектами, которые могут приводить к инвалидизации больных. Таким образом, при назначении гормонотерапии больным с DCIS необходимо учитывать объем предшествующего лечения, а также возможные негативные последствия эндокринотерапии, особенно у больных с сопутствующей патологией.
Лечение больных с рецидивами после органосохраняющего лечения. При инвазивном рецидиве лечение соответствует лечению инвазивного РМЖ аналогичной стадии.
Лечение неинвазивного рецидива зависит от первоначального лечения. Если больная подвергалась только локальному иссечению, то методами выбора являются реэксцизия, реэксцизия и ЛТ или мастэктомия. Если же проводилась лучевая терапия, то при наступлении рецидива, как правило, выполняется мастэктомия.
Наблюдение. Все больные, подвергшиеся лечению по поводу DCIS, нуждаются наблюдении в течение всей жизни. Маммография и УЗИ выполняется всем больным, подвергшимся органосохраняющему лечению ежегодно, причем первые два года после лечения маммография и УЗИ должны выполняться каждые 6 месяцев. Клиническое обследование больных в течение первых лет также должно выполняться каждые 6 месяцев, а затем ежегодно. Другие дополнительные методы диагностики имеют относительные показания.
Дольковая карцинома in situ (LCIS) выявляется обычно случайно при биопсии, производимой по поводу какого‑либо доброкачественного заболевания молочной железы. В отличии от протоковой карциномы in situ LCIS обычно не выявляется при пальпации, не характеризуется выделениями из сосков и, как правило, не имеет отчетливой маммографической симптоматики. Такой характерный рентгенологический симптом DCIS, как микрокальцификация, при LCIS встречается крайне редко. Морфологическая интерпретация также может быть затруднена, так как в процесс нередко вовлекаются как ацинусы долек, так и терминальные отделы протоков, поэтому при гистологическом исследовании нелегко отличить LCIS от протоковой карциномы in situ или от атипической дольковой гиперплазии. Дольковая карцинома in situ наиболее часто встречается у женщин в репродуктивном возрасте (90 %) или реже, у женщин в постменопаузальном периоде, получающих заместительную гормонотерапию. Пик выявления LCIS приходится на возраст 45 лет.
По данным SEER с 1978 по 1998 отмечено четырехкратное увеличение частоты выявления LCIS (17). Такие показатели связаны в большей степени с широким распространением маммографического скрининга, что привело к увеличению числа эксцизионных биопсий и числа случайных хирургических находок. Однако не исключен и рост заболеваемости в популяции из‑за широкого распространения заместительной гормонотерапии.
Первоначально LCIS рассматривалась, как предшественник инвазивного рака, так как нередко выявлялась одновременно с инвазивной дольковой карциномой. Однако дальнейшие эпидемиологические исследования установили, что риск развития инвазивного рака не так высок, как ожидалось, а сама LCIS растет медленно и может ассоциироваться с инвазивным раком как в пораженной, так и в контрлатеральной молочной железы. В результате LCIS рассматривается многими не в качестве предшественника инвазивного рака, а скорее – индикатора повышенного риска развития инвазивного рака молочной железы любого типа.
Однако некоторые исследования указывают на наибольшую частоту выявления инвазивного рака (долькового и неспецифического) именно в области предшествующей биопсии по поводу LCIS. В большей степени это касается плеоморфоного варианта LCIS. При классическом варианте LCIS инвазиный рак в большинстве случаев имеет другую локализацию (в т. ч. и в контрлатеральной железе). Эти находки указывают на то, что LCIS все же может быть как индикатором повышенного риска инвазивного рака, так и предшественником инвазивного долькового рака. При этом риск перехода в инвазию при LCIS ниже, чем при DCIS и варьирует от 4 % до 36 % (2), с преимущественным переходом в инвазивный дольковый рак (ИДК).
Частота выявления LCIS при эксцизионной биопсии не превышает 5 % и составляет приблизительно 3 % при трепан-биопсии. Однако в последнем случае диагноз LCIS, установленный на основании результатов морфологического исследования биоптатов, не всегда является точным и окончательным. В ряде исследований указано, что при последующей эксцизионной биопсии в 25–31 % случаев может выявляться DCIS и инвазивный рак (1,3). Риск выявления (при доказанной LCIS) инвазивного рака в контрлатеральной молочной железе возрастает при длительном наблюдении: с 14 % при 10‑летнем наблюдении до 18 % – при 25‑летнем. Риск развития инвазивного рака при LCIS в ипсилатеральной железе зависит от возраста. При выявлении LCIS у женщин моложе 40 лет частота обнаружения инвазивного рака при 25‑летнем наблюдении не превышает 8.3 %, тогда как у женщин после 60 лет она возрастает до 25 %.
В настоящее время выделяют две основные формы LCIS: классическую и ее разновидность – плеоморфную. Плеоморфный вариант характеризуется высокой степенью геномной нестабильности как в отношении амплификаций, так и делеций, низкой частотой экспрессии рецепторов эстрогенов и высокой частотой экспресии HER2. Морфологически этот вариант отличается высокой степенью пролиферативной активности, а так же наибольшей частотой некрозов. Это биологически агрессивный вариант LCIS, который, по мнению ряда авторов, нуждается в широком иссечении до негативных краев, что, однако требует изучения. Плеоморфный вариант в настоящее время в большей степени считается предшественником развития инвазивного РМЖ и в меньшей – индикатором (маркером) риска возникновения инвазивного рака. По своим биологическим характеристикам и клиническому течению данный вариант находится ближе к протоковой форме рака in situ.
Клиническое течение LCIS зачастую бессимптомное – отсутствуют пальпаторные и рентгенологические признаки. Однако плеоморфный вариант LCIS нередко сопровождается комедо-некрозом и, следовательно, формированием кальцинатов, которые хорошо визуализируются при маммографии.
LCIS склонна к мультицентрическому и билатеральному поражению молочных желез. При обнаружении LCIS при биопсии одного из участков молочной железы вероятность выявления других фокусов в оставшейся части железы превышает 50 %, а вероятность обнаружения фокусов LCIS в противоположной железе приближается к 50 %.
При отсутствии признаков инвазии частота метастатического поражения подмышечных лимфоузлов при LCIS не превышает 1–2 % (22). Обнаружение этих метастазов, скорее, является результатом недиагностированного фокуса оккультной инвазии.
Лечение LCIS. До сих пор остается открытым вопрос, касающийся тактики лечения при выявлении LCIS при трепан-биопсии. В таких случаях риск обнаружения сопутствующего LCIS инвазивного рака оценить очень сложно, и он варьирует по данным ряда небольших исследований от 4 % до 50 %. В одном из исследований в 3 из 10 случаев LCIS, при дальнейшем оперативном вмешательстве выявлена инвазия. Все случаи имели дольковую структуру. Эти находки подтвердили необходимость выполнять эксцизионную биопсию (т. е. секторальную резекцию молочной железы) в случае выявления при трепан-биопсии LCIS.
По мнению большинства авторов обнаружение LCIS при сохранной операции по поводу предполагаемого доброкачественного процесса не требует дополнительного хирургического вмешательства. Такое мнение основано на том, что органосохраняющие операции при ИДК с положительными краями в виде классического варианта LCIS не сопровождаются увеличением риска местного рецидива. При плеоморфном варианте LCIS позитивные края теоретически могут увеличивать риск рецидива. В некоторых исследованиях выявлены единичные рецидивы при позитивных или близких (менее 1 мм) краях. Риск рецидива в данных небольших ретроспективных варьировал от 3.8 % до 19 %. Однако убедительных достоверных доказательств, что позитивные края при плеоморфном варианте существенно увеличивают риск рецидива пока явно недостаточно. В отличие от классического варианта LCIS, при плеоморфном варианте необходимо выполнять оперативное вмешательство (по крайней мере эксцизионную биопсию), так как более чем в 50 % (0–65 %) случаев в области первичной биопсии обнаруживается DCIS или инвазивный рак, которые и будут определять прогноз заболевания (8). При этом примерно в половине случаев приходится выполнять мастэктомию, так как при таком варианте рака in situ сложно, а иногда и невозможно достичь негативных хирургических краев из‑за диффузного роста опухоли и мультифокальности (в т. ч. в виде очагов инвазивного рака).
Таким образом, существует два пути ведения больных с дольковой карциномой in situ: либо наблюдение в течение жизни (что касается прежде всего классического варианта LCIS), либо хирургическое вмешательство. Целью наблюдения является наиболее ранняя диагностика инвазивной карциномы (в т. ч. в контрлатеральной железе), а оперативное вмешательство, скорее, преследует профилактические, чем лечебные цели. Причем экономные операции типа эксцизионной биопсии (секторальной резекции) не имеют успеха, так как риск развития в дальнейшем инвазивной карциномы остается прежним. Наиболее радикальной (профилактической) операцией является двусторонняя мастэктомия. Однако эффективность хирургического лечения при плеоморфном варианте LCIS еще требует дальнейшего изучения. В настоящее время эксперты Всемирной организации здравоохранения не поддерживают широкое применение объемных операций при плеоморфном варианте LCIS с учетом хорошего эффекта у данной группы больных профилактической эндокринотерапии.
Лучевая терапия и системное лечение при отсутствии признаков инвазии при LCIS не проводятся, хотя терапия тамоксифеном, скорее всего, была бы эффективной. Назначение тамоксифена по данным NSABP P-1 снижает риск развития инвазивного рака по сравнению с плацебо на 49 % в общей группе и на 56 % в группе пациенток с LCIS в анамнезе (5). В настоящее время недостаточно данных, касающихся прямого сравнения эффективности билатеральной мастэктомии и химиопрофилактики антиэстрогенами с динамическим наблюдением. Поэтому вопрос о выполнении билатеральной мастэктомии обсуждается с больной, получившей от лечащего врача все сведения о величине риска развития РМЖ и возможных вариантах его предотвращения, включая и химиопрофилактику.
Заключение. В мире накопился огромный опыт, как диагностики, так и лечения CIS. Во многих странах предложены стандарты лечения данной патологии. Однако до сих пор не известен молекулярный профиль тех вариантов CIS, которые не обладают инвазивным потенциалом, не прогрессируют, и, соответственно требуют лишь наблюдения. В любом случае карцинома in situ с прогностической точки зрения является относительно благоприятным заболеванием. Однако успех терапии во многом зависит от выбора адекватного лечения, который основан, прежде всего, на тщательной оценке всех известных к настоящему времени критериев прогноза заболевания.
РЕКОМЕНДАЦИИ РООМ
Тактика лечения DCIS
-
Ширина краев резекции при органосохраняющем лечении DCIS (в сочетании с лучевой терапией) должна быть не менее 2 мм.
-
Частота регионарного метастазирования при карциноме in situ не превышает 1–3 %, поэтому лимфаденэктомия для большинства больных является излишней. Больным, которым производится мастэктомия при пальпируемом поражении и / или диффузной микрокалицификации, т. е. при высоком риске микроинвазии рекомендовано выполнение биопсии сигнальных лимфатических узлов.
-
Лучевая терапия показана больным, подвергшихся органосохраняющим операциям
-
Адъювантная гормонотерапия снижает риск рецидива у большинства больных (в основном при позитивных краях), однако не влияет на показатели общей выживаемости
-
Успех лечения карциномы in situ зависит от выбора оптимального объема лечения, который основывается на тщательной оценке прогностических критериев и оценке риска рецидива.
Тактика лечения LCIS
-
При классическом варианте LCIS большинству больных может быть рекомендовано наблюдение.
-
При плеоморфном варианте LCIS всем больным рекомендовано выполнение эксцизионной биопсии для исключения инвазивного рака и DCIS
-
При любом варианте возможно назначение профилактического лечения: профилактические операции, профилактическая гормонотерапия
Литература
-
Brown K.Breast cancer chemoprevention: risk-benefit effects of the antioestrogen tamoxifen// Expert Opin Drug Saf. -2002.-Vol.1.-p.253-267.
-
Carder PJ, Shaaban A, Alizadeh Y, et al. Screen-detected pleomorphic lobular carcinoma in situ (PLCIS): risk of concurrent invasive malignancy following a core biopsy diagnosis//Histopathology. - 2010.-Vol.57.-p.472-478.
-
Chuba PJ, Hamre MR, Yap J, et al. Bilateral risk for subsequent breast cancer after lobular carcinoma-in-situ: analysis of surveillance, epidemiology, and end results data//J Clin Oncol.- 2005.-Vol.23.-p.5534-5541.
-
Correa C, McGale P, Taylor C, et al: Overview of the randomized trials of radiotherapy in ductal carcinoma in situ of the breast// J Natl Cancer Inst Monogr.2010.-Vol. 41.-p.162-177/
-
Fisher B., Constantino J.P, Wickerham D.L., et al. Tamoxifen for prevention of breast cancer: report of the National Surgical Adjuvant Breast and Bowel Project P-1 Study// J. Natl. Cancer Inst.1998.- Vol. 90.- p.1371-1388.
-
Fisher B., Dignam J., Wolmark N., et al. Tamoxifen in treatment of intraductal breast cancer: NSABP B-24 randomized controlled trial. // Lancet.- 1999.- Vol. 353.- p.1993-2000.
-
Fisher E.R., Dignam J., Tan-Chiu E., Costantino J. Pathologic findings from the national surgical adjuvant breast project (NSABP) eight-year update of Protocol B-17 // Cancer.- 1999.- Vol. 86.- N 3.- p.429-438.
-
Flanagan M.R., Rendi M.H., Calhoun K.E., Anderson B.O., Javid S.H. Pleomorphic Lobular Carcinoma In Situ: Radiologic-Pathologic Features and Clinical Management//Ann Surg Oncol.-2015.- Vol.22.-p.4263-4269.
-
Forbes J.F., Sestak I., Howell A., Bonanni B., Bundred N., Levy C., von Minckwitz G., Eiermann W., Neven P., Stierer M., Holcombe C., Coleman R.E., Jones L., Ellis I., Cuzick J.; IBIS-II investigators. Anastrozole versus tamoxifen for the prevention of locoregional and contralateral breast cancer in postmenopausal women with locally excised ductal carcinoma in situ (IBIS-II DCIS): a double-blind, randomised controlled trial//Lancet.-2016.- Vol.387.-p.866-873.
-
Goyal S., Vicini F., Beitsch D. et al. Ductal carcinoma in situ treated with breast-conserving surgery and accelerated partial breast irradiation: comparison of the Mammosite Registry trial with Intergroup Study E5194// Cancer.- 2011.- Vol. 117 – P.1149-1155.
-
Guidi AJ, Connolly JL, Harris JR, et al: The relationship between shaved margin and inked margin status in breast excision specimens// Cancer.-1997.-Vol. 79.-p.1568-1573.
-
Houghton J., George W.D., Cuzick J., Duggan C., Fentiman I.S., Spittle M. Radiotherapy and tamoxifen in women with completely excised ductal carcinoma in situ of the breast in the UK, Australia, and New Zealand: randomised controlled trial. // Lancet. – 2003. – Vol. 1362(9378).- P.95-102.
-
Hughes L.L., Wang M., Page D.L. et al. Local excision alone without irradiation for ductal carcinoma in situ of the breast: a trial of the Eastern Cooperative Oncology Group// J. Clin. Oncol.- 2009.- Vol. 27.- P. 5319-5324.
-
Kim K., Jung S.Y., Shin K.H., Kim J.H., Han W., Lee H.B., Huh S.J., Choi D.H., Park W., Ahn S.D., Kim S.S., Kim J.H., Suh C.O., Kim Y.B., Kim I.A., Kim S., Kim Y.J. Recurrence outcomes after omission of postoperative radiotherapy following breast-conserving surgery for ductal carcinoma in situ of the breast: a multicenter, retrospective study in Korea (KROG 16-02)// Cancer Res Treat. -2017.-Vol.162.-p.77-83.
-
Lagios M.D. Heterogeneity of ductal carcinoma in situ: Relationship of grade and subtype analysis to local recurrence and risk of invasive transformation. // Cancer Letters. -1995. -Vol. 90 - p.97- 102.
-
Lagios M.D. Lagios experience // Silverstein M.J. (Ed.) Ductal carcinoma in situ of the breast.-Baltimore: Williams and Wilkins. - 1997. - p.363-364.
-
Li CI, Anderson BO, Daling JR, Moe RE. Changing incidence of lobular carcinoma in situ of the breast//Breast Cancer Res Treat. -2002.-Vol.75.-p.259-268.
-
Margolese R.G., Cecchini R.S., Julian T.B., et al: Anastrozole versus tamoxifen in postmenopausal women with ductal carcinoma in situ undergoing lumpectomy plus radiotherapy (NSABP B-35): A randomised, double-blind, phase 3 clinical trial//Lancet.-2016.-Vol. 387.-p.849-56.
-
Marinovich ML, Azizi L, Macaskill P, et al: The association of surgical margins and local recurrence in women with ductal carcinoma in situ treated with breast-conserving therapy: A meta-analysis//Ann Surg Oncol.-2016.-Vol.23.-p. 3811-3821/
-
Morrow M., Van Zee., Solin L. et al. Society of Surgical Oncology–American Society for Radiation Oncology–American Society of Clinical Oncology Consensus Guideline on Margins for Breast-Conserving Surgery With Whole-Breast Irradiation in Ductal Carcinoma In Situ// J. Clin. Oncol. - 2016. Vol. 34. – pp. 4040–4046.
-
Motwani S.B., Goyal S., Moran M.S. et al. Ductal carcinoma in situ treated with breast-conserving surgery and radiotherapy: a comparison with ECOG Study 5194// Cancer.- 2011.- Vol. 117. – P. 1156-1162.
-
Rosen P.P. Axillary lymph node metastases in patients with occult noninvasive breast carcinoma//Cancer.-1980.-Vol. 46.-P. 1289-1306.
-
Silverstein MJ.Ductal carcinoma in situ of the breast. //Annu. Rev. Med.- 2000.- Vol.51.- P.17-32.
-
Solin LJ, Gray R, Hughes LL, et al: Surgical excision without radiation for ductal carcinoma in situ of the breast: 12-year results from the ECOG-ACRIN E5194 study//J Clin Oncol.-Vol. 33.-p.3938-3944.
-
Timbrell S., Al-Himdani S., Shaw O., Tan K., Morris J., Bundred N. Comparison of Local Recurrence After Simple and Skin-Sparing Mastectomy Performed in Patients with Ductal Carcinoma In Situ.// Ann Surg Oncol.-2017.- Vol.24.-p.1071-1076.
-
Van Zee KJ, Subhedar P, Olcese C, et al: Relationship between margin width and recurrence of ductal carcinoma in situ: Analysis of 2996 women treated with breast-conserving surgery for 30 years// Ann Surg.-2015.-Vol. 262.-p.623-631.
-
Wapnir IL, Dignam JJ, Fisher B, et al: Longterm outcomes of invasive ipsilateral breast tumor recurrences after lumpectomy in NSABP B-17 and B-24 randomized clinical trials for DCIS.//J Natl Cancer Inst.-2011.-Vol. 103.-p.478-488.











































