
Неврология. Национальное руководство. Краткое издание
Неврология. Национальное руководство. Краткое издание / под ред. Е. И. Гусева, А. Н. Коновалова, А. Б. Гехт. - М. : ГЭОТАР-Медиа, 2018. - 688 с. - ISBN 978-5-9704-4405-4. |
Общая характеристика и классификация
Головная боль (ГБ) - одна из наиболее частых жалоб на приеме невролога и терапевта - является причиной значительного социально-экономического ущерба для общества и входит в десятку самых частых причин нетрудоспособности в Европе. По данным Всемирной кампании по преодолению бремени головной боли (2010 г.), из расчета на 1 000 000 человеческой популяции:
По данным популяционного исследования, проведенного в России в 2009-2011 гг. с помощью подворного опроса, головные боли «не связанные с лихорадкой, похмельным синдромом, простудными заболеваниями или травмой головы» и возникающие хотя бы 1 раз за год, предшествующий исследованию, отмечали 63% опрошенных. Частота хронических ГБ в этом исследовании составила 10,5%, что значительно превышает показатели других стран.
Международная классификация головных болей (МКГБ) (2004). Принципы диагностики цефалгий
В соответствии с МКГБ-2[3] головные и лицевые боли подразделяются на первичные, когда не удается выявить органическую причину боли, вторичные, или симптоматические, обусловленные органическими заболеваниями головного мозга, других структур, расположенных в области головы и шеи, или системными заболеваниями, а также краниальные невралгии и лицевые боли.
Многочисленные клинико-эпидемиологические популяционные исследования, проведенные в большинстве стран мира, подтверждают преобладающее распространение в популяции первичных цефалгий (95-98%). Вторичные, или симптоматические, ГБ встречаются существенно реже (в среднем 2-8% среди всех форм цефалгий). Наиболее часто в практике терапевтов и неврологов встречаются четыре типа цефалгий:
-
Пучковая (кластерная) ГБ и другие тригеминальные вегетативные цефалгии.
-
ГБ, связанная с избыточным применением лекарственных препаратов [медикаментозно индуцированная (МИГБ), или абузусная, ГБ (АГБ)][4].
Оглавление МКГБ-2
Часть I. Первичные головные боли
Часть II. Вторичные головные боли
-
Головные боли, связанные с сосудистыми поражениями черепа и шейного отдела позвоночника.
-
Головные боли, связанные с несосудистыми внутричерепными поражениями.
-
Головные боли, связанные с различными веществами или их отменой.
-
Головные и лицевые боли, связанные с нарушением структур черепа, шеи, глаз, ушей, носовой полости, пазух, зубов, ротовой полости или других структур черепа и лица.
Часть III. Краниальные невралгии, центральные и первичные лицевые боли
Необходимо отметить, что у пациента может быть одновременно несколько типов ГБ (например, сочетание двух первичных форм, первичная и вторичная ГБ), следовательно, одному пациенту можно поставить несколько диагнозов. Примеры диагнозов: «мигрень без ауры, эпизодическая ГБН», «хроническая мигрень, цервикогенная головная боль».
Хотя большинство пациентов испытывают ГБ периодически, у ряда больных с годами происходит трансформация эпизодических цефалгий в хронические. Для обозначения очень частых цефалгий введено понятие хронической ежедневной (или почти ежедневной) головной боли, когда частота болевых эпизодов составляет 15 дней и более в месяц на протяжении более 3 мес. Трансформация эпизодических ГБ в хронические происходит под действием факторов хронизации. Основными из них являются психические нарушения, лекарственный абузус и особенности личности пациента.
Факторы хронизации первичных головных болей
Дифференциально-диагностические мероприятия
Согласно МКГБ-2, при первичных формах головной боли анамнез, физикальный и неврологический осмотры, а также дополнительные методы исследования не выявляют органической причины боли, т.е. исключают вторичный характер цефалгии. Поэтому диагностика первичных ГБ является исключительно клинической, т.е. базируется на тщательном анализе жалоб, анамнеза пациента и объективном осмотре и при типичной клинической картине не требует проведения дополнительных исследований.
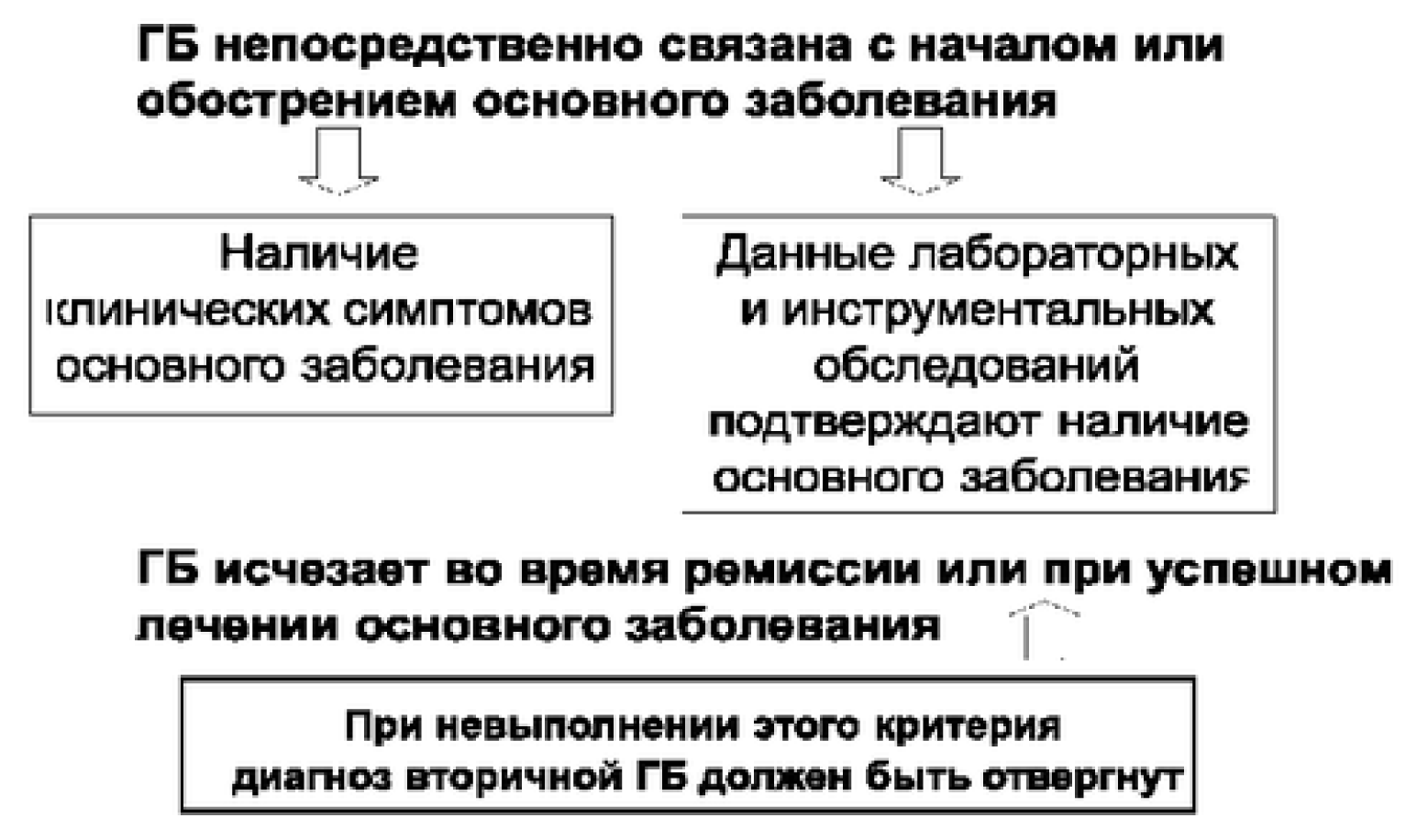
Для вторичных головных болей характерны наличие тесной временной связи между началом цефалгии и дебютом заболевания, усиление клинических проявлений головной боли при обострениях заболевания и облегчение течения цефалгии при уменьшении симптомов или излечении заболевания. Диагностические критерии вторичных форм ГБ представлены на рис. 11.1.
Клиническое обследование
Клиническое интервью включает анализ жалоб, анамнеза, наследственного анамнеза, выявление провокаторов болевых эпизодов и факторов, облегчающих ГБ, оценку степени нарушения качества жизни и работоспособности пациента, связанные с ГБ, анализ состояния в межприступном периоде, сопутствующих/коморбидных нарушений, а также «фармакологическое» интервью, направленное на получение сведений о предшествующей терапии, ее эффективности и количестве принимаемых обезболивающих препаратов. План расспроса пациента с жалобой на ГБ приведен в табл. 11.1.
Сколько типов ГБ имеется у пациента? Поскольку один пациент может иметь несколько типов ГБ, следует расспросить о каждом из них. Для каждого типа ГБ жалобы и анамнез собираются отдельно |
|
Анамнез ГБ и временные характеристики ГБ |
|
Частота и продолжительность ГБ |
|
Характер ГБ |
|
Причины и провокаторы ГБ |
|
Влияние ГБ на качество жизни и работоспособность пациента |
|
Состояние между приступами ГБ |
|
«Фармакологическое» интервью (лечение, применяемое в прошлом и в настоящее время для купирования и профилактики ГБ) |
|
При наличии нескольких типов головной боли для уточнения их природы можно предложить пациенту ведение дневника цефалгий, который поможет ему научиться отличать один тип головной боли от другого. Врачу такой дневник облегчит постановку диагноза и объективную оценку количества обезболивающих препаратов, используемых пациентом.
Физикальное обследование
Как правило, при первичных цефалгиях и МИГБ объективный осмотр не выявляет никаких патологических изменений в соматическом и неврологическом статусе. У пациентов с ГБН и мигренью (М) могут обнаруживаться напряжение и болезненность при пальпации мышц лица, затылка и шеи (мышечно-тонический синдром), признаки вегетативной дисфункции: ладонный гипергидроз, изменение окраски пальцев кистей (синдром Рейно). Во время приступа мигрени - бледность лица, повышение АД, гиперемия конъюнктивы, сонливость. Приступ пучковой ГБ сопровождается психомоторным возбуждением и вегетативными проявлениями на лице: слезотечением, покраснением конъюнктивы, отеком века, ринореей, нередко синдромом Горнера.
Лабораторные и инструментальные исследования
Согласно международным принципам, дополнительные инструментальные, лабораторные исследования и консультации специалистов в большинстве случаев не являются информативными и не имеют диагностической ценности при первичных формах ГБ и МИГБ. Это обусловлено тем обстоятельством, что у подавляющего большинства пациентов с первичными цефалгиями при проведении дополнительных исследований (ЭЭГ, реоэнцефалография, рентгенография черепа, методы нейровизуализации - КТ и МРТ) не выявляется никаких специфических изменений, которые могли бы указывать на причину или механизм возникновения ГБ. Изменения, которые могут выявляться при этих обследованиях, как правило, имеют неспецифический характер (т.е. могут обнаруживаться и у людей без жалоб на ГБ) и не могут считаться признаками той или иной формы ГБ.
Дополнительные и лабораторные исследования следует проводить пациентам с жалобой на ГБ только при наличии показаний, основным из которых является подозрение на вторичный (симптоматический) характер ГБ. Показания для дополнительных исследований у пациентов с жалобой на ГБ, уточненные РОИГБ, представлены ниже.
Показания для дополнительных исследований у пациентов с жалобой на головную боль (РОИГБ, 2011)
Основные настораживающие симптомы или «сигналы опасности», а также их возможные причины перечислены в табл. 11.2. Выявление одного и более сигналов опасности - основание для проведения тщательного обследования пациента, в первую очередь нейровизуализационных методов исследования.
| «Сигналы опасности» | Возможные причины |
|---|---|
Громоподобная ГБ (интенсивная ГБ с «взрывоподобным» или внезапным началом, стремительно нарастающая в течение 1 мин) |
Субарахноидальное кровоизлияние, синдром обратимого церебрального вазоспазма |
ГБ с атипичной аурой (длительностью > 1 ч или с двигательной слабостью) |
ТИА или инсульт |
Аура без ГБ без указаний на мигрень с аурой в анамнезе |
ТИА, инсульт, синдром Фишера (мигренозное сопровождение пожилого возраста) |
Аура, впервые возникшая у пациентки, принимающей комбинированные оральные контрацептивы |
Риск возникновения инсульта |
Впервые возникшая ГБ у пациента старше 50 лет |
Височный артериит или внутричерепная опухоль (внутричерепную опухоль также следует заподозрить при возникновении ГБ у детей в препубертатном периоде) |
Нарастающая ГБ, усиливающаяся в течение нескольких недель и более |
Внутричерепное объемное образование |
ГБ, усиливающиеся при изменении позы или нагрузках, повышающих внутричерепное давление (кашель, чихание, натуживание) |
Внутричерепное объемное образование |
Другие «сигналы опасности» |
Впервые возникшая ГБ у пациента с онкологическим заболеванием, ВИЧ-инфекцией или иммунодефицитом в анамнезе. Внезапное возникновение новой, необычной для пациента ГБ. Изменения в сфере сознания (оглушенность, спутанность или потеря памяти) или психические нарушения. Фокальные неврологические знаки или симптомы системного заболевания (лихорадка, артралгии, миалгии) |
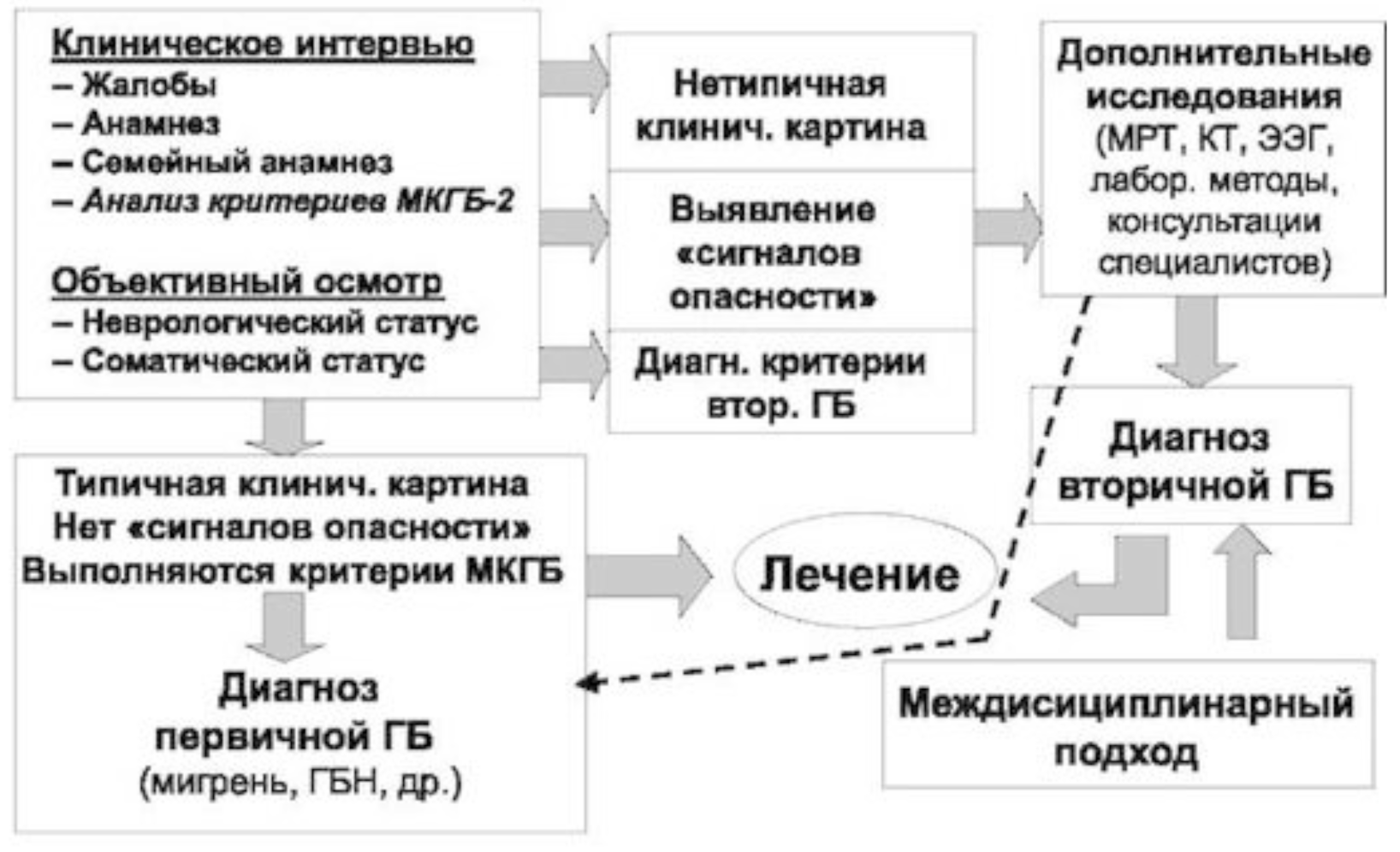
В завершение приведем краткий алгоритм диагностики ГБ (рис. 11.2). При типичной клинической картине, отсутствии при объективном осмотре органической патологии и «сигналов опасности» и при соответствии симптомов ГБ диагностическим критериям МКГб-2 врач может сразу без направления пациента на дополнительные исследования установить диагноз первичной формы ГБ (М, ГБН и др.) и назначить лечение. При нетипичной клинической картине, наличии «сигналов опасности» и/или при выполнении критериев вторичной ГБ следует провести необходимые дополнительные обследования с целью выявления возможной вторичной природы цефалгии. При выявлении соответствующих отклонений и нарушений, подтверждающих симптоматическую природу ГБ, устанавливается диагноз вторичной цефалгии и проводится лечение заболевания, послужившего ее причиной. При необходимости для ведения пациента с вторичной ГБ могут быть привлечены специалисты другого профиля (офтальмолог, оториноларинголог, психиатр, инфекционист, нейрохирург и т.п.).
Мигрень
Синонимы
Синонимы для мигрени без ауры - простая мигрень, hemicrania simplex. Синонимы для мигрени с аурой - классическая мигрень, ассоциированная мигрень, офтальмическая, гемипарестетическая или афатическая мигрень, осложненная мигрень.
Определение и эпидемиология
Мигрень - первичная эпизодическая форма головной боли, проявляющаяся интенсивными, чаще односторонними приступообразными головными болями, а также различным сочетанием неврологических, желудочно-кишечных и вегетативных проявлений. Мигрень занимает второе место по частоте после ГБН. Ее распространенность колеблется у женщин от 11 до 25%, у мужчин - от 4 до 10%. Обычно впервые мигрень проявляется в возрасте от 10 до 20 лет. Перед пубертатом распространенность мигрени выше у мальчиков, затем она быстрее увеличивается у девочек и остается значительно выше у женщин, чем у мужчин, даже после 50 лет. В возрасте 35-45 лет частота и интенсивность мигренозных приступов достигают максимума, после 55-60 лет у большинства больных мигрень прекращается. У 60-70% пациентов заболевание имеет наследственный характер.
Классификация мигрени (МКГБ-2, 2004)
Клиническая картина
Мигренозная боль чаще бывает пульсирующего и давящего характера, обычно захватывает половину головы и локализуется в области лба и виска, вокруг глаза. Иногда может начинаться в затылочной области и распространяться кпереди в область лба. У большинства больных сторона боли может меняться от приступа к приступу. Строго односторонний характер боли не типичен для мигрени, его считают показанием к дополнительному обследованию, цель которого - исключить органическое поражение головного мозга. Продолжительность приступа у взрослых обычно колеблется от 3-4 ч до 3 сут и в среднем составляет 20 ч. При эпизодической мигрени частота приступов варьирует от одного приступа в 2-3 мес до 15 в месяц, наиболее типичная частота приступов - 2-4 в месяц.
У некоторых пациентов за несколько часов или даже суток до приступа может возникать продром (предвестники головной боли), включающий различные сочетания таких симптомов, как слабость, ухудшение настроения, трудности концентрации внимания, иногда, напротив, повышенную активность и аппетит, напряжение в области мышц шеи, повышенную чувствительность к световым, звуковым и обонятельным раздражителям. После приступа у части пациентов в течение некоторого времени сохраняются сонливость, общая слабость и бледность кожи, нередко возникает зевота (постдром).
Провоцирующие факторы приступа мигрени: эмоциональный стресс, изменение погоды, менструация, голод, яркий свет, духота, прием алкоголя, недостаток или избыток ночного сна, некоторые пищевые продукты (жирные сыры, шоколад, цитрусовые, бананы).
Сопутствующие симптомы. Мигренозный приступ, как правило, сопровождается тошнотой, повышенной чувствительностью к яркому свету (фотофобия), звукам (фонофобия) и запахам, ухудшением аппетита. Несколько реже могут возникать рвота, головокружение, обморочное состояние. Из-за выраженной фото- и фонофобии большинство пациентов во время приступа предпочитают находиться в затемненной комнате, в спокойной, тихой обстановке. Боль при мигрени усугубляется от обычной физической активности, например при ходьбе или подъеме по лестнице. Для детей и молодых пациентов типично появление сонливости, а после сна головная боль нередко проходит.
Основные признаки мигрени следующие:
Мигрень имеет тесную связь с женскими половыми гормонами. Так, менструация становится провокатором приступа более чем у 35% женщин, а менструальную мигрень, при которой приступы возникают в течение 48 ч после начала менструации, встречают у 5-10% пациенток. У 2/3женщин после некоторого учащения приступов в I триместре беременности во II и III триместрах наблюдается значительное облегчение головной боли, вплоть до полного исчезновения мигренозных приступов. На фоне приема гормональных контрацептивов и заместительной гормональной терапии 60- 80% пациенток отмечают более тяжелое течение мигрени.
Клинические разновидности мигрени
Самая распространенная форма - мигрень без ауры (ранее простая М), которая встречается у 85-90% пациентов (клиническая характеристика приведена выше). Значительно меньшее число пациентов (10-15%) имеют мигрень с аурой, когда болевой фазе предшествует мигренозная аура - комплекс обратимых неврологических симптомов, возникающих непосредственно перед или в начале мигренозной ГБ. Не следует путать ауру с продромальными симптомами.
Аура развивается в течение 5-20 мин, сохраняется не более 60 мин и с началом болевой фазы полностью исчезает. Наиболее часто встречается зрительная или «классическая» аура, проявляющаяся различными зрительными феноменами: фотопсии, мушки, одностороннее выпадение поля зрения, мерцающая скотома или зигзагообразная светящаяся линия («фортификационный спектр»). Реже могут отмечаться односторонняя слабость или парестезии в конечностях (гемипарестетическая аура), преходящие речевые расстройства, у ряда больных - типичная аура без ГБ (синонимы: безболевая форма, мигренозное сопровождение пожилого возраста или синдром Фишера).
Семейная гемиплегическая мигрень - разновидность Μ с аурой, сопровождающаяся моторной слабостью, а также характеризующаяся наличием по меньшей мере одного родственника I или II степени родства с аналогичной аурой и моторной слабостью.
Мигрень базилярного типа (ранее использовались термины «Μ базилярной артерии» и «базилярная Μ») описывается как Μ с симптомами ауры, происходящими из ствола мозга и/или обоих полушарий, не сопровождающаяся моторной слабостью.
Ретинальная мигрень характеризуется повторяющимися приступами монокулярного расстройства зрения, которые включают сцинтилляции (мерцание), скотому или слепоту и сочетаются с мигренозной ГБ.
У 50% женщин, страдающих мигренью, существует тесная связь приступов с менструальным циклом. Большинство приступов, связанных с менструацией, - приступы мигрени без ауры. Предложено деление таких приступов на истинную менструальную (катемениальную) мигрень (когда приступы возникают только в «околоменструальный» период) и мигрень, связанную с менструацией (когда приступы могут быть вызваны не только менструацией, но и другими мигренозными провоцирующими факторами: переменой погоды, стрессом, алкоголем и др.). Истинная менструальная мигрень встречается не более чем у 10% женщин. Основным механизмом развития приступа катамениальной мигрени считают падение содержания эстрогенов в поздней лютеиновой фазе нормального менструального цикла (чаще в овуляцию).
У некоторых пациентов во время приступа могут возникать вегетативные симптомы: усиленное сердцебиение, отек лица, озноб, гипервентиляционные проявления (нехватка воздуха, чувство удушья), слезотечение, предобморочное состояние, гипергидроз. У 3-5% больных вегетативные проявления настолько многочисленны и ярки, что достигают степени типичного панического приступа с чувством тревоги, страха. Это так называемая вегетативная, или паническая, мигрень.
Периодические синдромы детства, предшествующие мигрени. У детей появлению типичных болевых приступов могут предшествовать некоторые патологические состояния, к которым относятся циклическая рвота, абдоминальная мигрень и доброкачественное пароксизмальное головокружение детского возраста. По достижении подросткового возраста эти проявления, как правило, прекращаются и «замещаются» типичными мигренозными приступами.
Осложнения мигрени. В отличие от первого, во второе издание МКГБ включен раздел «Осложнения мигрени», к которым относятся: хроническая мигрень, мигренозный статус, мигренозный инфаркт (инсульт) и эпилептический припадок, вызванный приступом М. Необходимо подчеркнуть, что исходный клинический вариант М и ее осложнение следует кодировать отдельно. Примеры диагнозов: 1. «М без ауры. Хроническая М». 2. «М с типичной аурой. Мигренозный инсульт». Хотя самое грозное осложнение - мигренозный инфаркт, наиболее распространенным в практике невролога и труднокурабельным является хроническая мигрень.
Хроническая мигрень (ХМ) - одно из осложнений М, когда ГБ возникают на протяжении 15 дней и более в месяц в течение 3 мес и более. Большинство случаев ХМ начинаются как М без ауры, поэтому хронизация рассматривается как осложнение эпизодической М. Диагностические критерии ХМ (в соответствии с дополненной версией МКГБ-2R) включают:
-
пять и более приступов в месяц, отвечающих критериям М без ауры (МКГБ-2);
-
8 дней и более в месяц ГБ[5] отвечает критериям М без ауры и/или облегчается при приеме триптанов либо препаратов эрготамина;
-
может сочетаться или не сочетаться со злоупотреблением обезболивающими препаратами (лекарственным абузусом);
К диагностическим признакам ХМ также относятся:
-
типичные приступы эпизодической Μ в анамнезе, начавшиеся до 20 лет;
-
нарастание на определенном этапе заболевания частоты ГБ (период трансформации);
-
по мере учащения Гб уменьшаются их интенсивность и выраженность типичных мигренозных черт (тошнота, фото- и фонофобия);
-
могут сохраняться односторонний характер боли и типичные для Μ провоцирующие факторы;
-
появление постоянной диффузной «фоновой» ГБ легкой интенсивности[6].
В трансформации эпизодической мигрени в хроническую форму играют роль два основных фактора: злоупотребление обезболивающими препаратами (так называемый лекарственный абузус) и депрессия, возникающая, как правило, на фоне хронической психотравмирующей ситуации. Поэтому в соответствии с пересмотренными критериями ХМ подразделяется на сочетающуюся и не сочетающуюся со злоупотреблением обезболивающими препаратами. ХМ и хроническая ГБН (ХГБН) - основные клинические разновидности хронической ежедневной ГБ.
Таким образом, больные с ХМ - это пациенты, имевшие в прошлом типичные приступы эпизодической Μ без ауры, у которых под действием факторов хронизации произошла трансформация ГБ: увеличение приступов, вплоть до появления ежедневных ГБ, и утрата типичных симптомов Μ.
Самый тяжелый вариант течения ХМ - рефрактерная М (РМ) - форма, резистентная к стандартной противомигренозной терапии. Критерии РМ и вопрос о ее рубрификации в МКГБ-3 в настоящее время обсуждаются. Рабочие критерии РМ представлены ниже.
Рабочие критерии рефрактерной мигрени
-
ГБ отвечает критериям эпизодической Μ (МКГБ-2) или ХМ (МКГБ-2R).
-
ГБ значительно нарушает функционирование и качество жизни пациента, несмотря на коррекцию триггеров, образа жизни и адекватную профилактическую терапию препаратами с доказанным противомигренозным эффектом (2-месячный курс в адекватной дозе):
-
Неэффективность адекватного купирования приступов препаратами следующих классов (при условии, что они не противопоказаны):
Для постановки диагноза РМ необходимо наличие у пациента эпизодической или хронической мигрени, а также выявление неэффективности большинства средств как для профилактики приступов, так и для их купирования.
Клиническая картина РМ в целом схожа с проявлениями ХМ: по мере учащения приступов они утрачивают типичные мигренозные черты, возникает постоянная «фоновая» боль, кроме того, РМ может сочетаться или не сочетаться с лекарственным абузусом. Наличие абузуса - один из главных факторов, осложняющих ведение этих пациентов.
Характерная черта РМ - наличие в анамнезе указаний на многократные малоэффективные, неэффективные или с непродолжительным эффектом попытки профилактической терапии. Облигатные спутники РМ - эмоционально-аффективные нарушения (депрессия и тревожные расстройства), нередко обнаруживаются другие формы психиатрической патологии и/или расстройств личности.
Мигрень нередко сочетается с коморбидными нарушениями, которые в значительной степени утяжеляют течение приступа, ухудшают состояние пациентов в межприступном периоде и в целом приводят к выраженному ухудшению качества жизни. К таким нарушениям относят депрессию и тревогу, вегетативные расстройства (гипервентиляционные проявления, панические атаки), нарушение ночного сна, напряжение и болезненность перикраниальных мышц, желудочно-кишечные расстройства (дискинезия желчных путей у женщин и язвенная болезнь желудка у мужчин), сопутствующие ГБН. Лечение коморбидных расстройств - одна из целей профилактической терапии мигрени. Доказана коморбидная связь мигрени и таких неврологических нарушений, как эпилепсия, инсульт, синдром Рейно и эссенциальный тремор.
Этиология и патогенез приступа мигрени
Этиология и патогенез М имеют комплексный характер. Среди основных механизмов обсуждаются генетические, нейрохимические и нейрогенные факторы. Доказано, что М имеет нейроваскулярную природу. Важнейшим механизмом, запускающим приступ М и обусловливающим развитие и сохранение боли, является активация тригемино-васкулярной системы, которая рассматривается как ключевая система реализации болевой фазы приступа (рис. 11.3). Другие компоненты патофизиологии боли при мигрени включают нейрогенное воспаление с вазодилатацией интракраниальных сосудов, в первую очередь сосудов твердой мозговой оболочки (ТМО), и экстравазацию - выделение в кровь болевых нейропептидов: кальцитонин-ген-родственного пептида, оксида азота, гистамина. Механизм активации тригемино-васкулярной системы связывают с повышенной возбудимостью коры головного мозга, присущей пациентам с М. Многочисленные клинические наблюдения и электрофизиологические исследования подтверждают концепцию центральной гипервозбудимости как базового патофизиологического феномена, предполагающего наличие определенного «мигренозного порога». Этот порог может быть преодолен под воздействием целого комплекса эндогенных и зкзогенных провоцирующих факторов; мигренозные триггеры являются лишь одним из них.
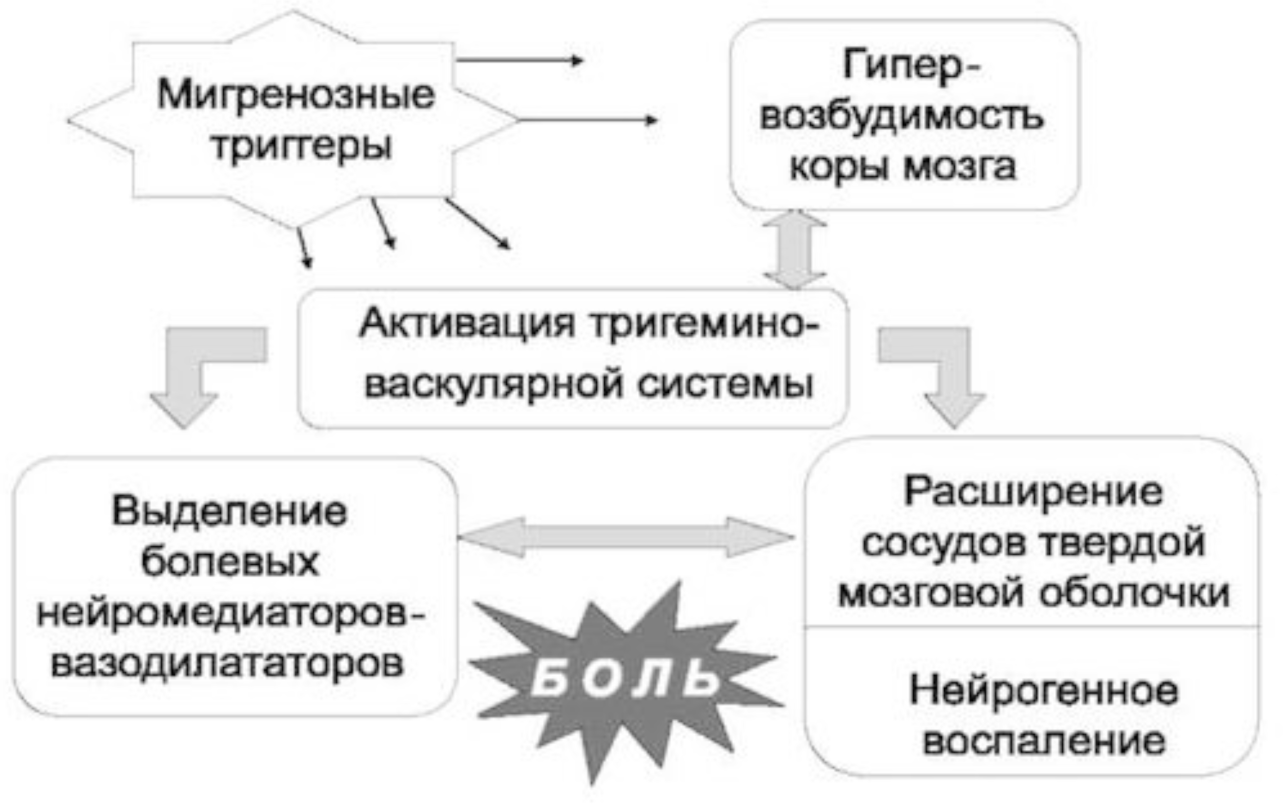
Показано, что у пациентов с частыми приступами (более трех в месяц) и длительно болеющих развивается избыточная чувствительность (сенситизация) тригеминоваскулярных волокон и других болевых структур. Феномен центральной сенситизации, клинически проявляющийся симптомами кожной аллодинии и тесно связанный с повышенной нейрональной возбудимостью, лежит в основе хронизации М.
Дифференциально-диагностические мероприятия
Как и при других первичных цефалгиях, диагноз «мигрень» полностью базируется на жалобах и данных анамнеза, и в большинстве случаев нет необходимости в проведении дополнительных методов исследования. Тщательный расспрос - основа правильной диагностики М. Дополнительные исследования показаны при нетипичном течении и наличии «сигналов опасности» (см. выше «Показания к проведению дополнительных исследований пациентам с жалобой на головную боль»). Ниже приведены диагностические критерии двух наиболее распространенных форм: М без ауры и М с аурой.
Диагностические критерии мигрени без ауры и мигрени с аурой (МКГБ- 2, 2004)
-
4) головная боль усиливается от обычной физической активности или требует ее прекращения (например, ходьба, подъем по лестнице).
-
1) полностью обратимые зрительные симптомы, в том числе позитивные (мерцающие пятна или полосы) и/или негативные (нарушение зрения);
-
2) полностью обратимые чувствительные симптомы, в том числе позитивные (ощущение покалывания) и/или негативные (онемение);
-
1) гомонимные зрительные нарушения и/или односторонние чувствительные симптомы;
-
2) как минимум один симптом ауры постепенно развивается на протяжении 5 мин и более и/или различные симптомы ауры возникают последовательно на протяжении 5 мин и более;
-
3) каждый симптом имеет продолжительность не меньше 5 мин, но не больше 60 мин.
В большинстве случаев при объективном осмотре не выявляют органических неврологических симптомов. У многих пациентов выявляются напряжение и болезненность в одной или нескольких перикраниальных мышцах (так называемый мышечно-тонический синдром), признаки вегетативной дисфункции: ладонный гипергидроз, изменение окраски пальцев кистей (синдром Рейно), признаки повышенной нервно-мышечной возбудимости (симптом Хвостека). Как уже было сказано, дополнительные обследования при М не бывают информативными и показаны только при нетипичном течении и подозрении на симптоматическую природу мигрени.
К дополнительным признакам, не входящим в диагностические критерии, но существенно облегчающим постановку диагноза, можно отнести: положительный наследственный анамнез, осмофобию в приступе, сведения об облегчении течения М во время беременности, положительный эффект триптанов и препаратов эроготамина. Чаще всего приходится дифференцировать М от эпизодической ГБН. В отличие от М, боль при ГБН бывает, как правило, двусторонней, менее интенсивной, имеет сжимающий, а не пульсирующий характер, реже сопровождается такими симптомами, как тошнота, свето- и звукобоязнь, не усиливается при обычной физической нагрузке.
Лечение
Современная лекарственная терапия М складывается из нескольких подходов, главные из которых - купирование уже развившегося приступа и профилактическое лечение, направленное на предотвращение атак, а также выявление и лечение коморбидных расстройств и борьба с факторами хронизации М; большое значение имеет и поведенческая терапия (рис. 11.4).

Купирование приступа
Терапию приступа М следует назначать в зависимости от его интенсивности (стратифицированный подход). При нечастых приступах слабой или умеренной интенсивности и при незначительной дезадаптации показаны простые или комбинированные анальгетики, в том числе НПВП: ацетилсалициловая кислота, ибупрофен, диклофенак, напроксен, парацетамол (табл. 11.3). При назначении терапии необходимо предупредить пациентов о возможном риске лекарственного абузуса и развитии МИГБ (головной боли при избыточном применении препаратов) и привыкания. Особенно высок этот риск у больных с большой частотой атак М (≥10 в месяц).
Во время приступа мигрени у многих пациентов выражена атония желудка и кишечника, поэтому всасывание препаратов, принимаемых внутрь, нарушается. В связи с этим, особенно при наличии тошноты и рвоты, за 30 мин до приема анальгетиков показаны противорвотные средства, одновременно стимулирующие перистальтику и улучшающие всасывание: метоклопрамид [по 2-3 чайных ложки раствора (10-20 мг) внутрь, 10 мг внутримышечно или внутривенно либо в свечах 20 мг), домперидон (по 10-20 мг внутрь)].
| Анальгетики | Противорвотные |
|---|---|
Ацетилсалициловая кислота 900-1000 мг (только для взрослых), или ибупрофен 400-800 мг, или диклофенак 50-100 мг, или напроксен 500-1000 мг, или (если есть противопоказания) парацетамол 1000 мг |
Домперидон 20 мг или метоклопрамид 10 мг |
При большой интенсивности боли и значительной дезадаптации показано назначение специфической терапии (2-й этап, табл. 11.4). Наибольшей эффективностью обладают агонисты серотониновых рецепторов типа 5НТ1 - триптаны, которые блокируют выделение болевых нейропептидов, избирательно суживают расширенные сосуды твердой мозговой оболочки и прерывают приступ М.
| Препарат | Форма |
|---|---|
Суматриптан |
Таблетки по 50 мг и 100 мг, назальный спрей 20 мг, ректальные свечи 25 мг |
Элетриптан |
Таблетки по 20 и 40 мг |
Золмитриптан |
Таблетки по 2,5 мг |
Наратриптан |
Таблетки по 2,5 мг |
* Указаны триптаны, доступные в России на декабрь 2012 г.
Триптаны могут иметь различную и непредсказуемую эффективность у разных пациентов, поэтому пациенты должны попробовать несколько триптанов и выбрать наиболее подходящий. Эффективность триптанов гораздо выше при их раннем назначении, когда интенсивность боли еще незначительная (в течение 30-60 мин приступа).
Несколько реже используются эрготаминсодержащие препараты, также обладающие вазоконстрикторным действием.
Профилактика приступов
Показания и основные цели превентивного лечения перечислены ниже. Продолжительность курсового лечения должна быть достаточной (от 3 до 12 мес, в среднем 4-6 мес, в зависимости от тяжести мигрени). У некоторых пациентов на фоне адекватного профилактического курса может наступить временная ремиссия - полное прекращение приступов на 1-3 мес. У большинства удается существенно снизить частоту болевых пароксизмов, уменьшить интенсивность и продолжительность ГБ.
Цели профилактического лечения мигрени
Показания к профилактическому лечению мигрени
-
Большая частота атак (три и более в месяц) или две продолжительные тяжелые атаки (2 дня и более) с выраженной дезадаптацией.
-
Наличие лекарственного абузуса (>15 доз анальгетиков/триптанов в месяц).
-
Коморбидные нарушения в межприступном периоде, нарушающие качество жизни (депрессия, диссомния, дисфункция перикраниальных мышц, сопутствующие ГБН).
-
Гемиплегическая М или приступы М с продолжительной (>60 мин) гемипарестетической аурой.
Профилактическое лечение мигрени включает препараты различных фармакологических групп (табл. 11.5). Их индивидуально подбирают каждому пациенту с учетом патогенетических механизмов заболевания, провоцирующих факторов, характера эмоционально-личностных и коморбидных нарушений.
У пациентов с нечастой эпизодической мигренью препаратами выбора являются бета-блокаторы и блокаторы кальциевых каналов. Среди антидепрессантов наибольше эффективностью (особенно при хронической мигрени) обладает амитриптилин. При наличии выраженной депрессии показано применение других антидепрессантов: пароксетина, флуоксетина, циталопрама, эсциталопрама, сертралина, венлафаксина, дулоксетина.
Антиконвульсанты показаны пациентам с тяжелыми частыми приступами мигрени, устойчивыми к другим видам лечения, в том числе с хронической мигренью. У многих больных целесообразно применение комплексной терапии, т.е. сочетание двух или трех профилактических средств.
| Препараты | Доза |
|---|---|
Бета-блокаторы (неселективные) |
Атенолол 25-100 мг 2 раз в день, или бисопролол 5-10 мг 1 раз в день, или метопролол 50-100 мг 2 раза в день, или пропранолол 40-80 мг 2 раза в день |
Блокаторы кальциевых каналов Флунаризин* |
5-10 мг 1 раз в день |
Антиконвульсанты Топирамат Вальпроевая кислота |
25 мг 1 раз в день - 50 мг 2 раза в день 600-1500 мг в день в 2-3 приема |
Антидепрессанты Амитриптилин |
10-100 мг на ночь |
* В России не зарегистрирован.
Другие подходы к профилактике мигрени включают: курсы ацетилсалициловой кислоты (по 125-300 мг 2 раза в сутки) или напроксена (по 250-500 мг 2 раза в сутки) в течение 12 мес, дигидроэргокриптин (вазобрал* по 4 мг 2 раза в сутки в течение 2-3 мес), рибофлавин (витамин В2*) в высоких дозах (по 400 мг в день) в течение 2-3 мес, препараты, содержащие коэнзим Q*10 в дозе 100 мг 2 раза в сутки в течение 3 мес, тиоктовая (α-липоевая) кислота, магния сульфат.
При наличии у пациента с мигренью коморбидных расстройств, существенно нарушающих состояние в межприступный период, лечение должно быть направлено на их коррекцию: лечение депрессии и тревоги, панических атак и других вегетативных нарушений, нормализацию ночного сна и др.
Одной из стратегий профилактического лечения является воздействие на модифицируемые факторы хронизации мигрени: профилактика и лечение эмоционального стресса, депрессии и тревожных расстройств, преодоление лекарственного абузуса, лечение болевых синдромов другой локализации и мышечной дисфункции.
Наряду с лекарственными могут быть рекомендованы и немедикаментозные методы: психотерапия, психологическая релаксация, биологическая обратная связь, акупунктура, постизометрическая релаксация, массаж воротниковой зоны, мануальная терапия, лечебная гимнастика. При наличии выраженной дисфункции перикраниальных мышц показаны миорелаксанты (тизанидин, баклофен). В последние годы, особенно при хронической и рефрактерной мигрени, все большее распространение приобретают методы нейростимуляции.
Методами выбора в терапии ХМ являются антидепрессанты, антиконвульсанты, глюкокортикоиды, препараты ботулинического токсина типа А и нейростимуляция.
Головная боль напряжения
Головная боль напряжения (ГБН) - преобладающая форма первичной головной боли, проявляющаяся цефалгическими эпизодами продолжительностью от нескольких минут до нескольких суток. Боль обычно двусторонняя, сжимающего или давящего характера, легкой или умеренной интенсивности, не усиливается при обычной физической нагрузке, не сопровождается тошнотой, однако возможна фотоили фонофобия. Распространенность в течение жизни в общей популяции, по данным различных исследований, варьирует от 30 до 78%. Синонимы - головная боль мышечного напряжения, психомиогенная головная боль, стрессовая головная боль, психогенная головная боль, идиопатическая головная боль.
Классификация
В МКГБ-2 ГБН разделяют на эпизодическую, возникающую не чаще 15 дней в течение 1 мес (или менее 180 дней в течение года), и хроническую - более 15 дней в месяц (или более 180 дней в течение года), а эпизодическую ГБН разделяют на частую и нечастую. В среднем, по европейским данным, эпизодическая ГБН встречается у 50-60% в популяции, хроническая ГБН - у 3-5%. Чаще врачу приходится иметь дело с двумя разновидностями: частой эпизодической и хронической ГБН. Кроме того, обе формы подразделяют (в зависимости от наличия или отсутствия мышечной дисфункции) на подтипы «с напряжением» и «без напряжения перикраниальных мышц».
Головная боль напряжения (МКГБ-2, 2004)
Клиническая картина
Пациенты с ГБН описывают головную боль как диффузную, слабую или умеренную, чаще двустороннюю, непульсирующую, сжимающую по типу «обруча» или «каски». Боль не усиливается при обычной физической нагрузке, редко сопровождается тошнотой, однако возможна фото или фонофобия. Появляется, как правило, вскоре после пробуждения, присутствует на протяжении всего дня, то усиливаясь, то ослабевая.
Большинство пациентов жалуются на повышенную тревожность, сниженный фон настроения, тоску, апатию или, наоборот, агрессивность и раздражительность, плохое качество ночного сна. Это проявление тревожных и депрессивных расстройств, их степень у пациентов с ГБН варьирует от легкой до тяжелой. Значительная депрессия может отмечаться у пациентов с хронической ГБН, она поддерживает мышечное напряжение и болевой синдром, приводя к серьезной дезадаптации пациентов.
Наряду с цефалгией отмечаются жалобы на преходящие или постоянные болевые ощущения либо чувство напряжения и дискомфорта в области затылка, задней поверхности шеи и надплечий (так называемый мышечно-тонический синдром). Жалобы на болезненность и напряжение мышц шеи и затылка нарастают по мере усиления интенсивности и учащения эпизодов головной боли, а также по мере нарастания силы боли во время самого эпизода.
Среди основных провокаторов ГБН - «мышечный фактор» (позное напряжение, обусловленное длительным вынужденным положением шеи и головы) и эмоциональный стресс, который, в свою очередь, вызывает и усиливает мышечный спазм.
Дифференциально-диагностические мероприятия
Диагностика ГБН, как и других первичных ГБ, является клинической; дополнительные исследования не показаны и неинформативны. При типичной клинической картине следует поставить диагноз ЭГБН или ХГБН и назначить лечение. Инструментальные методы и консультации специалистов показаны только при подозрении на симптоматический (вторичный) характер цефалгии.
Важный элемент осмотра пациента с ГБН - исследование перикраниальных мышц, других неврологических проявлений у этих пациентов, как правило, не обнаруживают. Из трех диагностических приемов: обычная пальпация, ЭМГ с поверхностными электродами и алгометрия - только пальпаторный метод наиболее чувствителен для выявления дисфункции перикраниальных мышц у больных с ГБН и М.
Дисфункцию перикраниальных мышц (ДПМ) легко выявляют при пальпации мелкими вращательными движениями II и III пальцами, а также при надавливании в области лобных, височных, жевательных, грудино-ключично-сосцевидных и трапециевидных мышц. Наличие ДПМ необходимо учитывать при выборе стратегии лечения. При беседе с пациентом нужно разъяснить ему механизм мышечного напряжения и его значение для течения заболевания. При наличии болезненности перикраниальных мышц при пальпации следует поставить диагноз эпизодической ГБН (хронической ГБН) с напряжением перикраниальных мышц.
Критерии диагностики головной боли напряжения (МКГБ-2, 2004)
Дополнительные диагностические признаки головной боли напряжения
Клинические разновидности головной боли напряжения
При нечастой эпизодической ГБН (ЭГБН) пациенты редко обращаются к врачу; как правило, специалистам приходится сталкиваться с частой ЭГБН и ХГБН.
Хроническая форма ГБН, при которой ГБ возникает не менее 15 дней в месяц на протяжении в среднем более 3 мес (не менее 180 дней в течение года), так же как и хроническая мигрень - одна из форм хронической ежедневной головной боли - всегда сопряженная с выраженной дезадаптацией. При тяжелом течении пациенты испытывают ГБ ежедневно или постоянно. Важным диагностическим признаком ХГБН является предшествующее наличие ЭГБН (так же как для установления диагноза ХМ необходимо наличие в анамнезе типичных эпизодических мигренозных атак).
Как и при ХМ, основными факторами трансформации ЭГБН в ХГБН являются эмоциональные нарушения и избыточное применение обезболивающих препаратов для купирования эпизодов головной боли. Факторы риска хронизации цефалгий перечислены в начале раздела.
У некоторых пациентов отмечают сочетание эпизодической М и ЭГБН. Как правило, это пациенты с типичным анамнезом мигрени, у которых со временем появляются приступы ЭГБН. Ввиду явных различий этих двух форм цефалгии пациенты, как правило, отличают приступы мигрени от приступов ЭГБН.
Если пациент с ХГБН злоупотребляет лекарственными средствами, следует установить диагноз «ХГБН с лекарственным абузусом» или «ХГБН. Медикаментозно-индуцированная головная боль (комбинированные анальгетики)».
ГБН-подобные цефалгии могут быть одним из проявлений интракраниальной венозной дисфункции. Для венозной дисфункции в большей степени характерны распирающая, а не сжимающая боль, преобладание ночных и утренних цефалгий, усиление боли при физической нагрузке, кашле и при выполнении пробы с наклоном головы (антиортостатическая проба), а также недостаточная эффективность анальгетиков и кофеинсодержащих препаратов. Кроме того, у пациентов с ГБ «венозной» природы выявляются признаки окклюзии венозных синусов на МР-венографии.
Как было показано в нескольких российских работах, типичные эпизоды ГБН у пациентов, страдающих гипертонической болезнью, многими неврологами и особенно врачами общей практики часто ошибочно трактуются как ГБ, связанные с повышением АД.
Патогенез
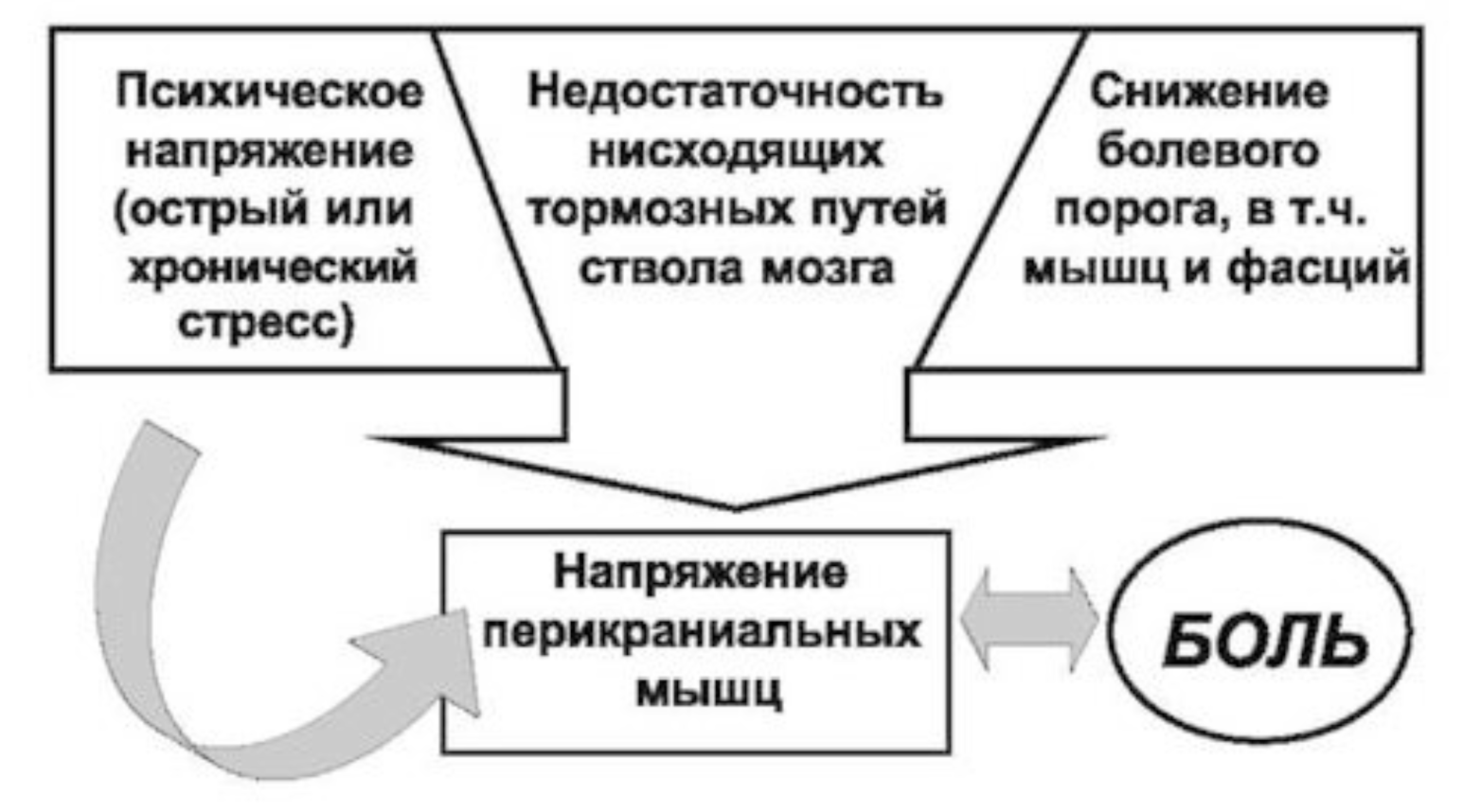
Хотя изначально ГБН рассматривалась как преимущественно психогенное расстройство, исследования, проведенные в последние годы, подтвердили ее нейробиологическую природу. В происхождении ГБН принимают участие как периферические, так и центральные ноцицептивные механизмы; среди последних - снижение активности антиноцицептивной системы, в частности недостаточность ингибиторных механизмов ствола мозга. Боль при ГБН связана с болезненным напряжением перикраниальных мышц. В основе формирования мышечно-тонического синдрома лежит механизм «порочного круга», когда повторяющееся напряжение мышцы, возникающее в ответ на эмоциональный стресс, приводит к ее рефлекторному напряжению (спазму). В результате повышается возбудимость нонцицептивных нейронов в структурах ЦНС, в том числе мотонейронов передних рогов спинного мозга; длительное тоническое напряжение приводит к гипоксии мышцы, ее воспалению, позднее формируется вторичная гипералгезия, усиливающая мышечный спазм и приводящая к хронизации боли (рис. 11.5). Высокие уровни депрессии и тревожности, выявляемые у большинства пациентов с ГБН, также облегчают болевую трансмиссию и способствуют хронизации болевого синдрома.
Лечение
Так же как и при М, лечение ГБН начинается с поведенческой терапии: необходимо объяснить пациенту, что его ГБ имеет доброкачественный характер, т.е. не сопряжена с заболеванием головного мозга и мозговых сосудов. Важно разъяснить механизм формирования ГБ: роль напряжения перикраниальных мышц и психических факторов (тревоги и депрессии), а также хронического эмоционального стресса в поддержании мышечного спазма. Пациентам с ХГБН, злоупотребляющим обезболивающими препаратами, следует дополнительно разъяснить значение лекарственного абузуса в хронизации ГБ.
Исходя из основных механизмов формирования ГБ, лечение ГБН является комплексным и должно в первую очередь быть направлено на нормализацию эмоционального состояния пациента и устранение мышечного напряжения, при необходимости - на коррекцию других коморбидных нарушений и лекарственного абузуса. Как и при М, терапия ГБН включает купирование болевого эпизода и профилактическое лечение.
Купирование приступов
Симптоматическое лечение болевого эпизода безрецептурными анальгетиками может применяться у пациентов с ЭГБН при частоте приступов не более 2 раз в неделю (8 болевых дней в месяц): ацетилсалициловая кислота по 600-1000 мг (только взрослым), ибупрофен по 400-800 мг и парацетамол по 100 мг. Есть данные об эффективности при ГБН диклофенака (50-100 мг) и флупиртина (100 мг).
Профилактическое лечение
При хронической форме ГБН эти препараты обладают сомнительной эффективностью и повышают риск абузусной ГБ, поэтому при частоте болевых дней более 2 в неделю (более 8 в месяц) показано профилактическое лечение. Доказанной эффективностью обладают амитриптилин по 10-100 мг в сутки и нортиптилин в тех же дозах (в России не зарегистрирован).
У пациентов с выраженными тревожно-депрессивными нарушениями возможно применение антидепрессантов из групп СИОЗС (пароксетин, флуоксетин, эсциталопрам, флувоксамин и др.) и СИОЗСН (венлафаксин, дулоксетин) в общепринятых для лечения депрессии дозах. Пациентам с выраженной болезненностью и напряжением перикранаильных мышц могут быть назначены миорелаксанты (тизанидин 2-6 мг в сутки, баклофен 10-25 мг 2-3 раза в сутки).
Учитывая данные об эффективности антиконвульсантов (препараты вальпроевой кислоты, габапентин, топирамат) при хронической ежедневной ГБ, целесообразно их применение и при ХГБН, особенно в случае резистентности пациентов к традиционным видам терапии.
При сочетании М и ГБН следует применять традиционные средства для профилактики М: бета-адреноблокаторы, НПВП, блокаторы кальциевых каналов (см. раздел «Профилактика мигрени»).
Хотя в ряде исследований показана эффективность ботулинического токсина при ХГБН, сочетающейся с напряжением перикраниальных мышц, другие исследования не подтвердили целесообразность применения препаратов этой группы.
Комплексная терапия ГБН также может включать немедикаментозные методы: психотерапию, психологическую релаксацию, биологическую обратную связь, постизометрическую мышечную релаксацию, массаж воротниковой зоны, фитнес, водные процедуры. Важными компонентами терапии, наряду с разъяснением пациенту механизмов ГБН, являются обучение методикам психологической и мышечной релаксации.
Кластерная головная боль и другие тригеминальные вегетативные (автономные) цефалгии
Понятие «тригеминальные вегетативные цефалгии» (ТВЦ) объединяет несколько редких форм первичной головной боли, сочетающих в себе как черты цефалгии, так и типичные черты краниальных парасимпатических невралгий. Среди всех ТВЦ наиболее распространена кластерная, или пучковая, ГБ (ПГБ), реже встречаются пароксизмальная гемикрания и кратковременные односторонние невралгические головные боли с инъецированием конъюнктивы и слезотечением (синдром КОНКС).
Классификация
Кластерная головная боль и другие тригеминальные вегетативные цефалгии (МКГБ-2, 2004)
Этиология и механизм развития тригеминальных вегетативных цефалгий
Патогенез ТВЦ до конца не изучен. Экспериментальные и функциональные нейровизуализационные исследования показали, что ТВЦ сопровождаются активацией тригеминопарасимпатического рефлекса с клиническими признаками вторичной симпатической дисфункции. Механизм собственно болевого приступа при ПГБ схож с таковым при мигрени: активация тригеминоваскулярной системы, выделение болевых нейропептидов, вазодилатация (см. раздел «Мигрень»). Полагают, что в основе патогенеза ПГБ лежит нарушение пейсмекерной функции гипоталамуса, которая определяет возникновение болевых периодов и сезонность обострений, клинически проявляется в суточной периодичности приступов, зависимости атак от периодов сна, своеобразном поведении пациентов, а также смешанной симпатической и парасимпатической дисфункциях во время атаки. С помощью механизма, который пока остается не изученным, периферические или центрально обусловленные триггеры вызывают активацию определенных зон гипоталамуса (серое вещество, в том числе супрахиазмальное ядро), что соответствует периоду болевого пучка. Ритмическая активация гипоталамической области, в свою очередь, приводит к активации тригеминоваскулярной системы, дилатации сосудов твердой мозговой оболочки, выделению болевых нейропептидов (CGRP, субстанция Р) и собственно болевому приступу. Стихание обострения и наступление ремиссии свидетельствуют о нормализации гипоталамической активности. Природа пароксизмальной гемикрании (ПГ) и кратковременных односторонних невралгических головных болей с инъецированием конъюнктивы и слезотечением остается неясной.
Пучковая (кластерная) головная боль
Пучковая (кластерная) головная боль (ПГБ) - самая частая форма ТВЦ (от англ. cluster - пучок). Частота ее в популяции невысока - 0,1-0,4%, мужчины страдают в 3-4 раза чаще, чем женщины, дебют заболевания происходит в 20-40 лет. При описании ПГБ используют следующие основные понятия: атака - единичный приступ боли, «пучок», или кластерный период, - период времени, в течение которого у пациента возникают множественные повторные болевые приступы, ремиссия - период, свободный от приступов боли. От других форм цефалгий ПГБ отличает периодичность течения заболевания - смена болевых «пучков» и ремиссий.
Синонимы - пучковая мигрень, гистаминная цефалгия, синдром Хортона, мигренозная невралгия Харриса, цилиарная невралгия, эритромелалгия головы, эритропрозопалгия Бинга.
Клиническая картина
Для ПГБ характерны приступы чрезвычайно интенсивной строго односторонней боли, продолжительностью от 15 до 180 мин, локализующейся вокруг глаза, надбровной, височной или в нескольких из этих областей; возможна иррадиация в верхнюю или нижнюю челюсть. Приступы возникают с частотой от 1 раза в 2 дня до 8 раз в сутки, типично их возникновение в ночное время. В период «болевого пучка» боль почти всегда возникает с одной и той же стороны; возможна смена стороны боли во время следующего обострения. Из-за невыносимой боли пациенты не могут находиться в покое, у них отмечаются двигательное беспокойство, плач, агрессия и ажитация. На высоте боли на болевой стороне у большинства пациентов наблюдаются типичные вегетативные симптомы: покраснение конъюнктивы, слезотечение, заложенность носа, ринорея, потливость лба и лица, миоз, птоз, отечность век.
При эпизодической форме ПГБ приступы возникают сериями («пучками»), продолжительностью от нескольких недель до нескольких месяцев; болевые периоды сменяются ремиссиями (от нескольких месяцев до нескольких лет); характерна сезонность обострений - чаще весной и осенью. У 10% пациентов отмечается хроническое течение с ремиссиями менее 6 мес или без ремиссий.
Провоцирующие факторы
Кластерный период (в том числе первый «пучок») может возникать после нарушения привычного суточного ритма: при смене часовых поясов при воздушных перелетах, бессонных ночах, суточном графике работы и др. Во время болевого «пучка», а также при хронической форме ПГБ приступы могут быть спровоцированы приемом алкоголя, гистамина или нитроглицерина. Отмечена тесная связь приступов и ночного сна: ночные приступы считаются облигатными для этой формы цефалгии. Любопытно, что в период ремиссии никакие провокаторы не способны вызвать приступ.
Клинические разновидности пучковой головной боли
Наиболее часто наблюдают эпизодическую форму пучковой головной боли, реже - хроническую, когда ремиссии или отсутствуют совсем, или не превышают 1 мес. Хроническая форма пучковой головной боли (10-15% случаев) может возникать de novo или происходить из эпизодической формы. У некоторых пациентов отмечают переход хронической формы в эпизодическую. У некоторых пациентов было описано сочетание пучковой головной боли и тригеминальной невралгии (так называемый кластер-тик синдром).
Дифференциально-диагностические мероприятия
Диагноз «пучковая головная боль» базируется на типичной клинической картине (строго односторонние боли в половине лица и головы, сопровождающиеся вегетативными проявлениями на лице: слезотечением, ринореей и др.) и на характерном течении заболевания (чередование болевых периодов, «пучков», со светлыми промежутками, ремиссиями). Дополнительные критерии пучковой головной боли - ее невыносимый характер и двигательное возбуждение, а также возникновение приступов во время ночного сна. Традиционные методы исследования (ЭЭГ, МРТ, УЗДГ) неинформативны и проводятся только при нетипичной кинической картине с целью исключения симптоматической природы ПГБ. Диагностические критерии представлены ниже.
Пучковая головная боль (МКГБ-4)
Дифференциальную диагностику проводят с другими формами ТВЦ и невралгией тройничного нерва (табл. 11.6)
| Характеристика | ПГБ | ХПГ | ЭПГ | КОНКС (SUNCT) | НТН |
|---|---|---|---|---|---|
Соотношение М:Ж |
9:1 |
1:3 |
1:1 |
2.3:1 |
Ж > М |
Продолжительность атак |
15-180 мин |
2-30 мин |
1-30 мин |
2-240 с |
От нескольких секунд до минут |
Частота атак |
1-8/сут |
1-40/сут |
3-30/сут |
1/сут-30/ч |
Различная |
Вегетативные симптомы |
+ |
+ |
+ |
+ |
- |
Алкоголь - провокатор атак |
+ |
+ |
+ |
+ |
- |
Положительный эффект индометацина |
+.- |
+ |
+ |
- |
- |
Вторичная природа ПГБ может быть заподозрена при наличии следующих атипичных симптомов: недостаточная интенсивность боли (менее 10 баллов по ВАШ), пациент способен находиться в покое во время приступа, отсутствие ночных атак, наличие «фоновой» головной боли между приступами ПГБ, наличие в статусе пациента неврологических симптомов (кроме миоза и птоза), неэффективность традиционных средств купирования приступов (триптаны, эрготамин, ингаляции кислорода). Наиболее информативными методами при исключении вторичной природы ПГБ являются МРТ и КТ с контрастированием.
Лечение
Во время болевого периода пациенты должны избегать возможных провокаторов приступов: не принимать алкоголь, лекарственные препараты или продукты, обладающие сосудорасширяющими свойствами, а также соблюдать режим сна- бодрствования. Терапия ПГБ, так же как и мигрени, включает купирование приступов и профилактическое лечение болевых периодов.
Доказанной эффективностью при купировании атак ПГБ обладают: триптаны (суматриптан, элетриптан, золмитриптан), препараты эрготамина (см. раздел «Мигрень») и ингаляции 100% кислорода (7-10 л/мин в течениие 15 мин). Есть данные об эффективности местных анестетиков, в частности 4% лидокаина в виде назальных капель или аэрозоля (1 мл интраназально), а также препаратов, содержащих капсаицин. Анальгетики, включая опиоиды, не должны использоваться для купирования приступов ПГБ.
Профилактика эпизодической формы ПГБ должна начинаться как можно раньше после начала болевого периода, а у пациентов с предсказуемыми обострениями - за 2-3 нед до начала ожидаемого болевого периода (табл. 11.7). Даже при заметном улучшении в течение первых 1-2 нед терапии пациенты не должны прерывать курс: лечение необходимо продолжать в течение всего ожидаемого болевого «пучка» и завершить через 2 нед после достижения полной ремиссии. Препараты должны подбираться с учетом эффективности и токсичности. Неэффективность одного лекарственного средства не означает неэффективности другого; возможно применение их комбинации. В связи с потенциальной токсичностью препаратов необходимо следовать инструкциям по их применению.
Есть данные об эффективности антиконвульсантов (габапентин, топирамат) у пациентов с продолжительными болевыми периодами и хронической формой ПГБ. При неэффективности медикаментозных подходов и тяжелых хронических формах могут применяться хирургические методы лечения: радиочастотная термокоагуляция тригеминального ганглия, радиочастотная ризотомия, микроваскулярная декомпрессия, а также методы нейростимуляции.
При эпизодической форме и относительно легком течении хорошим эффектом обладают лития карбонат и верапамил, при необходимости возможно сочетание этих препаратов. При более тяжелом течении (более пяти приступов в сутки, большая продолжительность болевого пучка - более 2 мес) показано применение антиконвульсантов и габапентина.
| Лекарственный препарат | Особенности применения |
|---|---|
Верапамил по 240-960 мг в сутки |
Необходим контроль АД |
Преднизолон по 60-80 мг 1 раз в день в течение 2-4 дней с последующим снижением дозы в течение 2-3 нед |
Может потребоваться повторный курс, так как при снижении дозы возможно возобновление болевых приступов |
Лития карбонат по 600-1600 мг/сут |
Необходимо контролировать уровень препарата в крови |
Эрготамина тартрат по 2-4 мг в день ректально |
Обычно после 7 дней лечения делается перерыв. Нельзя сочетать с суматриптаном |
Метисергид* по 1-2 мг в таблетках |
Необходимо делать перерыв как минимум на 1 мес каждые полгода. Не рекомендуется сочетать с суматриптаном |
* В России не зарегистрирован.
Лечение хронической формы ПГБ представляет трудности. При неэффективности перечисленных подходов возможно применение глюкокортикоидов. Наряду с хирургическими методами для лечения резистентной к другим видам терапии хронической формы пучковой головной боли применяют методы нейростимуляции: глубокую стимуляцию задней гипоталамической области, большого затылочного, блуждающего и других нервов.
Пароксизмальная гемикрания
ПГ - редкая разновидность ТВЦ, развивающаяся преимущественно у женщин (соотношение Ж:М = 3:1) в возрасте от 20 до 30 лет, с характеристиками боли и сопутствующими симптомами, аналогичными симптомам ПГБ, но более кратковременными, возникающими с большей частотой и отвечающими на терапию индометацином. Диагностические критерии представлены ниже.
Клиническая картина
Боль при ПГ имеет строго односторонний характер, как правило, без смены стороны, максимально выражена в вокруг глаза, в области виска, лба и верхней челюсти, реже в носовой, затылочной и ретроорбитальной областях; может иррадииро-вать в плечо и руку на ипсилатеральной стороне. Большинство пациентов описывают боль как пульсирующую, ноющую или колющую; интенсивность болевых ощущений колеблется от умеренной до невыносимой. Отличительными симптомами ПГ являются кратковременность приступов (от 2 до 30 мин) и их большая частота, которая может достигать 40 в сутки (в среднем 5-10 атак в сутки); продолжительность боли колеблется от 2 до 120 мин (в среднем - 2-25 мин). Такие признаки, как возникновение приступов в ночное время и их провокация алкоголем, при ПГ отмечаются существенно реже, чем у больных с ПГБ. Во время приступа большинство больных предпочитают находиться в покое, в постели, у некоторых отмечается двигательное возбуждение, характерное для ПГБ. Для ПГ, также как и для кластерной ГБ, характерны вегетативные симптомы, являющиеся отражением локальной парасимпатической активации. Специфическим диагностическим признаком ПГ, отличающим эту форму ТВЦ от других, является эффективность индометацина.
Клинические разновидности ПГ
Так же как и при ПГБ, различают эпизодическую (с ремиссиями 1 мес и более) и хроническую формы пароксизмальной гемикрании, при которой приступы повторяются дольше 1 года без ремиссий или с ремиссиями менее 1 мес. Известны случаи пароксизмальной гемикрании, сочетающейся с тригеминальной невралгией (так называемая пароксизмальная гемикрания - тик-синдром).
Дифференциально-диагностические мероприятия
Диагноз базируется на типичной клинической картине и эффективности индометацина. Дополнительные исследования показаны только при подозрении на симптоматический характер болевых эпизодов и наличии сигналов опасности. Диагностические критерии приведены ниже.
Пароксизмальная гемикрания (МКГБ-4)
-
Приступы интенсивной односторонней боли орбитальной, супраорбитальной или височной локализации продолжительностью 2-30 мин.
-
Головная боль сопровождается как минимум одним из следующих симптомов:
-
Преимущественная частота приступов более 5 раз в сутки, иногда несколько реже.
-
Приступы полностью предотвращаются при приеме индо-метацина в терапевтической дозе.
В ряде случаев ПГ может иметь вторичный (симптоматический) характер, что следует учитывать при неэффективности лечения.
Лечение
У подавляющего большинства пациентов регулярный прием индометацина в достаточных дозах позволяет полностью купировать или существенно уменьшить болевые проявления уже в течение первых 48 ч лечения. В среднем рекомендованная доза составляет 150 мг внутрь (50 мг 3 раза в сутки) или в свечах, а также 100 мг в виде инъекций с последующим снижением до поддерживающей (50-100 мг). Учитывая возможность развития нежелательных явлений, в первую очередь со стороны ЖКТ, целесообразно применение индометацина совместно с омепразолом (20 мг/сут). При полной неэффективности максимальной терапевтической дозы индометацина диагноз «ПГ» должен быть поставлен под сомнение.
Кратковременные односторонние невралгические головные боли с инъецированием конъюнктивы и слезотечением (КОНКС, SUNCT-синдром)
В связи с крайне низкой распространенностью и малочисленностью описаний эпидемиология этого синдрома очень мало изучена. КОНКС чаще встречается у мужчин (М:Ж = 4,25:1) и обычно начинается между 40 и 70 годами.
Клиническая картина
Боль во время атаки локализуется в области иннервации первой ветви тройничного нерва: вокруг глаза, в области виска и лба строго с одной стороны; возможна иррадиация боли в область носа, щеки и нёба на болевой стороне; чрезвычайно редко боль может возникать с обеих сторон. Продолжительность болевых эпизодов при КОНКС значительно меньше, чем при других формах ТВЦ, - от 5 до 240 с (в среднем 10- 60 с), частота достигает в среднем 30 атак в сутки (от 1 до 80). Приступы могут возникать в любое время суток. Интенсивность боли колеблется от умеренной до сильной и описывается пациентами как колющая, жгучая, нередко с ощущением прохождения электрического тока. В то же время вегетативные симптомы (особенно слезотечение и покраснение конъюнктивы) могут быть выражены более значительно, чем при ПГБ.
Большинство приступов развивается спонтанно, однако описаны случаи провокации такими стимулами, как жевание, кашель, усиленное дыхание носом, прикосновение к векам или области лба, движения шеи, а также при употреблении холодных продуктов и напитков. В отличие от приступа невралгии тройничного нерва, при КОНКС отсутствует рефрактерный период, так что следующий приступ может начаться сразу после предыдущего. Большинство приступов возникает во время бодрствования.
КОНКС характеризуется ремиттирующим течением, причем болевой период может длиться от нескольких дней до нескольких месяцев; большинство пациентов имеют одно-два обострения в год. Ремиссии имеют продолжительность от нескольких месяцев, иногда лет; с течением времени наблюдается тенденция к утяжелению и учащению болевых эпизодов.
Дифференциально-диагностические мероприятия
Диагноз КОНКС базируется на типичной клинической картине. Диагностические критерии приведены ниже.
Кратковременные односторонние невралгические головные боли с инъецированием конъюнктивы и слезотечением (SUNCT-синдром)
Приступы при синдроме КОНКС иногда приходится дифференцировать от приступов невралгии тройничного нерва с вовлечением офтальмической ветви. Аналогичные болевые эпизоды возможны при поражениях, локализующихся в задней черепной ямке или вовлекающих гипофиз. Поэтому диагноз «КОНКС» можно поставить только после того, как тщательное обследование (включая методы нейровизуализации) исключит вторичную природу симптомов. Учитывая вышесказанное, всем пациентам с клинической картиной, напоминающей КОНКС, необходимо проведение МРТ головного мозга для исключения вторичной природы приступов.
Лечение
КОНКС плохо поддается терапии. Учитывая кратковременность атак, целью лечения является не их купирование, а уменьшение частоты болевых эпизодов. Синдром КОНКС не чувствителен к индометацину и большинству других препаратов, применяющихся для лечения первичных форм головной боли. В последнее время получены свидетельства эффективности в виде снижения частоты атак КОНКС таких антиконвульсантов, как ламотриджин, топирамат и габапентин.
Медикаментозно индуцированная (абузусная) головная боль
В этом разделе, посвященном первичным формам цефалгий, необходимо остановиться на одной из вторичных форм головной боли, тесно связанной с мигренью и ГБН, - абузусной, или лекарственной («рикошетная» головная боль, лекарственная головная боль). В последние годы проблема лекарственного абузуса приобретает в нашей стране все большее значение. Это связано с широким распространением и доступностью разнообразных обезболивающих препаратов. МИГБ может возникать при злоупотреблении любыми препаратами, купирующими головную боль.
Определение и эпидемиология
Медикаментозно-индуцированная, или абузусная, головная боль (МИГБ, АГБ) является одной из форм хронической ежедневной головной боли и занимает третье место по частоте после ГБН и мигрени. Распространенность АГБ в популяции составляет 1%, а среди пациентов специализированных центров головной боли - 10%; у пациентов с жалобами на хронические головные боли частота МИГБ достигает 60%. Хотя АГБ относится ко вторичным цефалгиям, она чаще всего развивается у пациентов с первичными головными болями при регулярном приеме обезболивающих препаратов на протяжении продолжительного времени.
Среди всех видов абузусной головной боли наибольшее клиническое значение в России, как и в мире, имеет цефалгия, связанная со злоупотреблением анальгетиками или комбинированными препаратами (т.е. комбинациями анальгетиков с другими медикаментами: кодеином, кофеином и т.д.). К развитию МИГБ могут приводить и препараты, предназначенные для специфического лечения приступа мигрени: триптаны и эрготаминсодержащие средства.
Классификация
Головные боли при избыточном применении лекарственных препаратов составляют один из подразделов МКГБ-2 (глава 8 «Головные боли, связанные с различными веществами или их отменой»). Классификация МИГБ (с учетом ревизии 2005 г.) представлена ниже.
Медикаментозно-индуцированная (абузусная) головная боль (МКГБ-2R. 2005)
-
Головная боль при избыточном применении комбинированных анальгетиков.
-
Головная боль при избыточном применении нескольких классов обезболивающих препаратов[7].
-
Головные боли, вызванные избыточным применением других лекарственных препаратов.
Клиническая картина
МИГБ может иметь разнообразные клинические проявления у разных пациентов даже на протяжении суток, от мигренеподобных до присущих ГБН. Чаще всего МИГБ проявляется почти ежедневными тупыми болями во всей голове давящего или сжимающего характера, незначительной или умеренной интенсивности; наибольшая сила боли отмечается, как правило, в утренние часы; часто бывают ощущения усталости, дурноты, снижение работоспособности, раздражительность, нарушения сна.
У пациентов с мигренью на фоне постоянной тупой боли несколько раз в месяц могут возникать более или менее типичные приступы мигрени: сильная пульсирующая односторонняя боль, сопровождающаяся тошнотой/рвотой, чувствительностью к звукам и свету (хроническая мигрень). В развернутой стадии МИГБ возникает ежедневно, как правило, сохраняется на протяжении всего дня, варьируя по интенсивности. Значительное усиление болевых ощущений может происходить при малейшей физической или интеллектуальной нагрузке, а также в случаях, когда прием препаратов прерывают. Обезболивающие препараты вызывают преходящее и обычно неполное облегчение цефалгии, что вынуждает пациентов вновь и вновь принимать лекарства.
Показано, что абузус - наиболее частая причина учащения мигренозной боли до 15 дней в месяц и более, а также развития смешанной цефалгии, характеризующейся как мигренозными чертами, так и клиническими признаками ГБН, также возникающей с периодичностью более 15 дней в месяц.
Этиология и патогенез
Установлено, что МИГБ может возникать при злоупотреблении любыми препаратами, купирующими ГБ. К числу потенциально опасных медикаментов относятся: комбинированные анальгетические препараты, производные эрготамина, опиоиды, специфические препараты для купирования приступов мигрени - агонисты серотониновых рецепторов (триптаны), в меньшей степени НПВП.
Из двух факторов - количество доз обезболивающих в месяц и регулярность приема - второй является более значимым для формирования лекарственного абузуса. Так, если пациент будет принимать всего 2 таблетки анальгетика, но практически ежедневно, то вероятность развития АГБ существенно возрастет. Чередование периодов частого применения препарата с относительно продолжительными периодами без лечения гораздо реже приводит к формированию МИГБ.
Обычно в начале у пациентов с МИГБ бывает эпизодическая мигрень или ЭГБН, затем происходит учащение болевых эпизодов. В роли факторов хронизации чаще всего выступают эмоциональный стресс (депрессия, тревога), присоединение другого типа головной боли, напряжение перикраниальных мышц. Нарастание частоты болевых приступов ведет к увеличению приема обезболивающих, что в конце концов приводит к ежедневному и многократному приему препаратов. С течением времени облегчение от обезболивающих становится преходящим и неполным, что вынуждает пациентов вновь и вновь принимать лекарства. Наряду со злоупотреблением лекарственными препаратами к патогенетическим факторам абузусной головной боли относят аффективные расстройства - депрессию и тревогу, способствующие развитию психологической зависимости от лекарственных средств.
С течением времени и увеличением частоты атак у пациентов с МИГБ формируется дисфункция ноцицептивных систем мозга: сенситизация периферических и активация «немых» ноцицепторов тригеминоваскулярной системы, гиперчувствительность нейронов ядра тройничного нерва, а также недостаточность нисходящих ингибиторных (антиноцицептивных) путей. В качестве одного из ведущих механизмов формирования МИГБ обсуждается феномен гипералгезии, возникающий на фоне длительного приема обезболивающих препаратов, например опиатов.
Дифференциально-диагностические мероприятия
Диагностика МИГБ является клинической, т.е. основывается на описании пациентом своей ГБ, анамнестических сведениях и анализе обезболивающей терапии; дополнительные исследования не выявляют патологии. Наиболее информативный метод, подтверждающий наличие лекарственного абузуса, - ведение пациентом дневника головной боли, в котором он отмечает время возникновения болевых эпизодов и количество принимаемых обезболивающих препаратов. Ниже представлены обобщенные диагностические критерии АГБ и (для примера) критерии ГБ при избыточном применении анальгетиков.
Обобщенные диагностические критерии медикаментозно-индуцированной головной боли (МКГБ-2R. 2005)
-
ГБ, присутствующая на протяжении 15 дней или более в месяц, отвечающая критериям С и D.
-
Регулярное на протяжении более чем 3 мес злоупотребление одним препаратом или более для купирования острого приступа и/или симптоматического лечения головной боли.
-
ГБ развилась или значительно ухудшилась во время избыточного приема препарата(-ов).
-
ГБ прекращается или возвращается к прежнему паттерну в течение 2 мес после прекращения приема «виновного» препарата[8].
Диагностические критерии ГБ при избыточном применении анальгетиков (МКГБ-2R 2005)
Примеры диагнозов при наличии лекарственного абузуса:
Лечение
Лечение МИГБ следует начинать сразу после ее выявления. Прогноз зависит от длительности злоупотребления препаратами. Профилактика (разъяснение риска развития МИГБ при злоупотреблении обезболивающими препаратами пациентам с большой частотой эпизодов ГБ) более эффективна, чем лечение уже развившейся АГБ.
Необходимо, с одной стороны, разъяснить пациенту, что лечение, которое он принимает, чтобы снять ГБ, по существу является ее причиной; с другой - убедить пациента, что отмена препарата - единственный путь к облегчению ГБ.
Основные цели ведения пациентов с МИГБ
Предпочтительна резкая, одномоментная отмена препарата. В течение 48 ч после отмены могут возникнуть усиление ГБ, тошнота или рвота, тревожность, нарушения сна, которые сохраняются максимум 2 нед. В связи с этим процесс отмены должен быть запланирован таким образом, чтобы он не оказывал заметного влияния на жизнь пациента (может возникнуть потребность в 1-2-недельном больничном листе). Через 12 нед ГБ обычно начинает уменьшаться. Даже если, несмотря на отмену препарата, ГБ сохраняются, они становятся более легкими и лучше отвечают на правильно подобранное лечение. Большинство пациентов после 2 мес отмены возвращаются к исходной форме цефалгии. Полное восстановление может занимать недели или даже месяцы. Для оценки динамики цефалгического синдрома рекомендуется ведение календаря (дневника ГБ) для регистрации симптомов и количества принимаемых препаратов.
Большинство пациентов с МИГБ при отмене абузусного препарата нуждаются в подборе заместительного средства для купирования ГБ. Обычно в качестве замены рекомендуется препарат другой фармакологической группы (например, если абузус у пациента с М был вызван простым анальгетиком, для купирования приступов могут быть рекомендованы триптаны, препараты эртогамина или НПВС). Для купирования постоянной (фоновой) ГБ у пациентов с мигренью и ГБН может быть рекомендован флупиртин (катадолон*), который назначается на регулярной основе в дозе 100 мг 3 раза в сутки в течение первых 3-4 нед периода отмены.
При тяжелом абузусе и выраженной психологической зависимости можно применять парентеральное дезинтоксикационное лечение, которое включает: утром внутривенно дексамета-зон 6-8 мг + магнезия 25% 10 мл + физиологический раствор 100 мл (№ 7 капельниц), вечером внутривенно амитриптилин 2мл + физиологический раствор 100 мл (№ 7 капельниц). Возможно внутривенное введение эрготамина (если абузус не обусловлен применением эрготов).
Параллельно с отменой «виновного» препарата и дезинтоксикацией назначается традиционная профилактическая терапия в зависимости от первичной формы ГБ (мигрень или ГБН). Следует разъяснить пациенту, что эффект профилактической терапии будет недостаточным, если не происходит отмена препарата, вызвавшего абузус. Наиболее эффективными средствами для лечения МИГБ у пациентов как с мигренью, так и с ГБН являются антидепрессанты (амитриптилин, флуоксетин, эсциталопрам, дулоксетин, милнаципран, венлафаксин) и анти-конвульсанты (топирамат, габапентин, препараты вальпроевой кислоты). Дозы антиконвульсантов необходимо титровать до рекомендованной дозы. Например, начальная доза топирамата составляет 25 мг/сут однократно вечером (в течение 1 нед), затем повышается на 25 мг каждые 7-10 дней до достижения терапевтической дозы 100 мг/сут. Продолжительность профилактической терапии МИГБ в среднем составляет 6-12 мес.
Рецидив АГБ в течение последующих 5 лет отмечается у 40% пациентов, поэтому большинство пациентов требуют длительного наблюдения. После успешного снятия абузуса важно разъяснить пациенту риск возврата МИГБ и необходимость строго контролировать количество обезболивающих препаратов. Желательно максимально отсрочить возврат к приему абузусного препарата; предпочтительно перейти на препарат другой фармакологической группы. При необходимости обезболивающий препарат можно вновь с осторожностью начать принимать через 2 мес (кратность приема не должна превышать 2 раз в неделю).
Эффективность и безопасность ибупрофена в фармакотерапии первичных головных болей изучена в многочисленных рандомизированных сравнительных плацебо-контролируемых клинических исследованиях.
В частности, в исследовании, где ибупрофен применялся для лечения мигрени (Pearce, Frank et al., 1983), ибупрофен в дозе 400 мг значительно превосходил Аспирин® по уменьшению интенсивности и продолжительности головной боли как при оценке эффективности врачом, так и по предпочтениям пациентов. Ибупрофен также уменьшает выраженность ассоциированных состояний: тошноту, рвоту, сопутствующие явления фоно-, фотофобии и функциональные расстройства. (Suthisisang C., Poolsup N., Kittikulsuth W. et al., 2007).
Последнее, вероятно, связано со способностью ибупрофена уменьшать агрегацию тромбоцитов или синтез простагландинов, поскольку оба эти механизма участвуют в развитии симптоматики при мигрени.
Изучение тензионных головных болей в привычной для больного социальной среде (Noyelle, Crossland et al., 1987) показало, что ибупрофен (Нурофен®) в дозе 400 мг значительно превосходил по обезболивающему эффекту и ацетилсалициловую кислоту (Аспирин®) 1000 мг, и парацетамол 1000 мг, принимаемые в соответствующих безрецептурных дозировках. Также было продемонстрировано более быстрое начало обезболивающего действия ибупрофена по сравнению с Аспирином® и парацетамолом.
В современном многоцентровом рандомизированном плацебо-контролируемом сравнительном исследовании эффективности ацетилсалициловой кислоты, ибупрофена и суматриптана в купировании приступов мигрени установлено, что ибупрофен превосходит по эффективности в купировании приступа мигрени ацетилсалициловую кислоту, плацебо и как минимум не уступает суматриптану по оценке в первые 2 ч. Снижение интенсивности боли с высокой до умеренной или полное устранение умеренной боли в первые 2 ч отмечали 60,2% пациентов в группе ибупрофена 400 мг, 55,8% в группе суматриптана 50 мг, 52,5% в группе ацетилсалициловой кислоты и 30,6% в группе плацебо (Diener H.C., Bussone G., de Liano H. et al., 2004). Как правило, ибупрофен хорошо переносился участниками данных исследований и сообщений о серьезных побочных эффектах препарата не поступало.
Двойное слепое рандомизированное плацебо-контролируемое перекрестное исследование неотложного лечения мигрени у детей в возрасте от 4 до 16 лет показало, что ибупрофен в дозе 10 мг/кг был более эффективным, чем парацетамол в дозе 15 мг/кг (Hämäläinen, Hoppu et al., 1997).
В РФ ибупрофен известен как Нурофен® - оригинальный препарат, разработанный в Великобритании, доступный в настоящее время в различных формах выпуска. Таблетированные лекарственные формы содержат: ибупрофен 200 мг (Нурофен®), ибупрофен 400 мг (Нурофен® Форте), ибупрофена натрия дигидрат 256 мг (Нурофен® Экспресс Нео).
Нурофен® Форте содержит 400 мг ибупрофена, поэтому может быть рекомендован в случае тяжелых и средней степени тяжести приступов мигрени, а также при головной боли напряжения значительной интенсивности.
Ибупрофена натрия дигидрат (Нурофен® Экспресс Нео) отличается своими фармакокинетическими свойствами, которые заключаются в том, что эта лекарственная форма быстрее абсорбируется в ЖКТ (максимальная концентрация в сыворотке крови достигается в среднем через 35 мин). В связи с этой особенностью терапевтический эффект в виде облегчения или полного купирования головной боли наступает быстрее.
Таким образом, результаты проведенных многочисленных клинических исследований позволяют заключить, что высокая аналгетическая активность и безопасность делают Нурофен* препаратом выбора при купировании приступов мигрени и лечении головной боли напряжения.
Печатается на правах рекламы.