Детские болезни : учебник / Геппе Н. А. - Москва : ГЭОТАР-Медиа, 2018. - 760 с. - ISBN 978-5-9704-4470-2 |
9.1. Ревматические болезни суставов у детей
9.1.1. Ювенильный идиопатический (ревматоидный) артрит
Ювенильный идиопатический (ревматоидный) артрит (ЮИА) — хроническое, тяжелое прогрессирующее заболевание детей и подростков с преимущественным поражением суставов неясной этиологии и сложным, аутоиммунным патогенезом, которое приводит к постепенной деструкции суставов, нередко сопровождается внесуставными проявлениями, нарушает рост и развитие ребенка, негативно влияет на качество всей жизни.
Эпидемиология
Частота составляет 1–3 на 10 тыс. детей в год. В Европе и Северной Америке ЮИА встречается чаще, чем в Азии. Распространенность ЮИА составляет примерно 6 на 10 тыс. детей, у девочек встречается в 2 раза чаще, чем у мальчиков. В России распространенность ЮИА у детей до 14 лет составляет 49,57 на 100 тыс. детского населения, а в возрасте 15–17 лет ЮИА регистрируют у 121,53 на 100 тыс. подростков.
Этиология и патогенез
Этиология ЮИА неизвестна до настоящего времени. ЮИА, как и ревматоидный артрит взрослых, — мультифакториальное заболевание с полигенным типом наследования, в развитии которого принимают участие ряд наследственных и средовых факторов, среди которых определенное значение придают инфекции. О роли наследственных факторов в развитии ЮИА свидетельствует достоверно более высокое, чем в популяции, число случаев ревматоидного артрита у родственников 1-й степени родства. В монозиготных (однояйцевых) парах, где один ребенок болен ЮИА, второй близнец страдает артритом более, чем в 44%, в то время как в дизиготных — только в 4%. Выявлены ассоциации ЮИА с Аг гистосовместимости (HLA) — A2, B27, B35 и HLA DR-5, DR-8.
Роль средовых (инфекционных) факторов в развитии ЮИА остается в рамках гипотез. Существует множество провоцирующих факторов, запускающих механизм развития болезни. Наиболее частые — вирусная или бактериально-вирусная инфекция, травмы, инсоляция или переохлаждение, психологические стрессы и даже профилактические прививки. Предполагают также первичную патологию самой иммунной системы в развитии ЮИА. В основе заболевания лежит активация клеточного и гуморального звена иммунитета. Чужеродный или измененный собственный Аг воспринимается и обрабатывается макрофагами или другими антигенпрезентирующими клетками, которые представляют его Т-лимфоцитам, приводя к активации и пролиферации Т-лимфоцитов. Макрофаги, активированные Т-лимфоциты, фибробласты, синовиоциты вырабатывают провоспалительные цитокины, вызывающие каскад патологических изменений с развитием прогрессирующего воспаления в полости сустава и системных проявлений заболевания. Выработка большого количества аутоантител свидетельствует о вовлеченности В-клеточного звена иммунной системы. Центральный провоспалительный цитокин, который определяет активность воспалительных и деструктивных изменений в суставах, — ФНОα. Системные проявления ЮИА — лихорадка, сыпи, лимфаденопатия, похудание и другие преимущественно связывают с повышением синтеза и активностью ИЛ-1 и ИЛ-6 (рис. 9.1). Активированные лимфоциты вырабатывают большое количество протеолитических ферментов, что приводит к резорбции хряща и даже костной ткани. Деструкция всех компонентов сустава вызвана формированием паннуса, состоящего из активированных макрофагов, фибробластов, активно пролиферирующих синовиальных клеток.
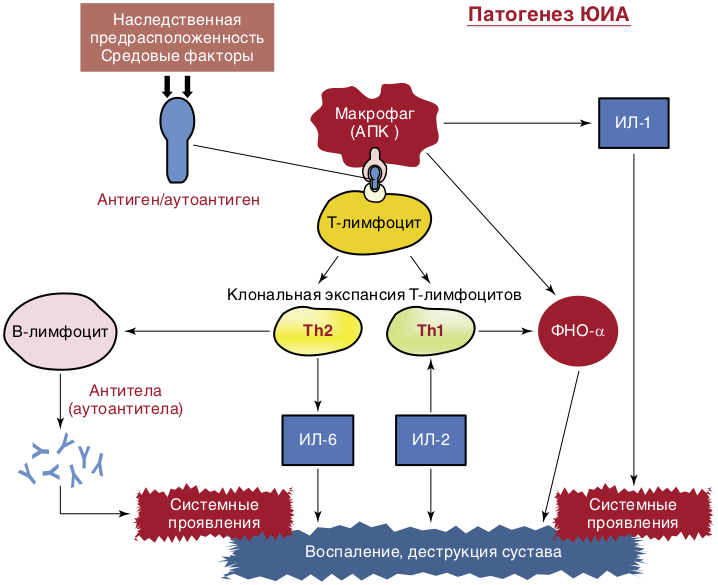
Таким образом, неконтролируемые реакции иммунной системы приводят к развитию хронического воспаления, необратимым изменениям в суставах, развитию экстраартикулярных проявлений.
Классификация и номенклатура
Современные классификационные критерии были приняты постоянным комитетом международной противоревматической лиги (ILAR) в апреле 1997 г. и скорректированы в 2001 г., когда был введен объединяющий термин — «ювенильный идиопатический артрит» (ЮИА).
ЮИА определяют как артрит неустановленной этиологии, присутствующий в течение 6 нед, возникший до 16-летнего возраста, при исключении других заболеваний.
Варианты течения ЮИА.
Системный артрит определяют при наличии артрита, сопровождаемого или предшествуемого лихорадкой в течение 2 нед в сочетании с 2 или более признаками: преходящими, летучими эритематозными высыпаниями; серозитом, генерализованной лимфаденопатией, гепатомегалией и/или спленомегалией.
Полиартрит негативный по РФ определяют при поражении 5 или более суставов в течение первых 6 мес заболевания, РФ-отрицательный.
Полиартрит позитивный по РФ определяют при поражении 5 и более суставов в течение первых 6 мес заболевания, наличии положительного РФ в двух тестах на протяжении 3 мес.
Олигоартрит: определяют при наличии артрита 1–4-го суставов в течение первых 6 мес заболевания:
Энтезитный артрит определяют при наличии артрита (чаще олигоартрита) и энтезита, или артрита и энтезита с двумя из следующих признаков:
ПсА определяют при наличии артрита и кожного псориаза или при наличии артрита и 2 из перечисленных симптомов:
Другие артриты определяют при наличии артрита в течение 6 нед и более, который не соответствует ни одной из предыдущих категорий классификации или отвечает критериям более чем 1 категории.
Предложенная классификация существенно отличается от международной классификации болезней (МКБ-10), см. ![]() .
.
Клиническая картина
ЮИА гетерогенное заболевание, клинические проявления которого зависят от пола, возраста начала заболевания, наличия маркеров наследственной предрасположенности.
Суставной синдром. Основное проявление ЮИА — артрит, для которого характерны типичные признаки воспаления — отечность (припухлость), гиперемия, локальное повышение температуры, боль, нарушение функции (ограничения подвижности в суставе). Признак активного артрита — отечность, или сочетание боли и ограничения подвижности. Могут поражаться все суставы, имеющие синовиальную оболочку. У детей чаще всего поражаются коленные суставы (80–90%), несколько реже голеностопные и лучезапястные. Вовлечение в процесс суставов шейного отдела позвоночника — одно из типичных проявлений ЮИА. Тазобедренный сустав страдает значительно чаще, чем у взрослых. Поражение височно-нижнечелюстного сустава довольно типично для ЮИА, особенно при системной форме с полиартритом и начале заболевания в возрасте до 3 лет. Воспалительный процесс замедляет рост нижней челюсти, в результате чего развивается типичная деформация лица с прогнатизмом, сохраняющимся на всю жизнь. Характерный признак ЮИА — симптом утренней скованности — тугоподвижность в суставах в утренние часы продолжительностью от 10–15 мин до нескольких часов.
При системной форме ЮИА помимо поражения суставов могут отмечаться поражения внутренних органов — миоперикардит, плеврит, серозный перитонит, а также гепатомегалия, спленомегалия, лимфаденопатия.
Поражения глаз при ЮИА могут протекать в форме острого переднего иридоциклита/увеита и хронического переднего иридоциклита, лентовидной дистрофии роговицы с осложнением катарактой. Клинически начало острого переднего иридоциклита сопровождается слабо выраженным покраснением глаз, светобоязнью. Хронический передний иридоциклит характерен вялым, почти бессимптомным течением, но может приводить к значительному снижению остроты зрения и слепоте.
Олигоартикулярный вариант
В дебюте в раннем детском возрасте преимущественно у девочек отмечают моно- или ассиметричный олигоартрит, преимущественно суставов ног, чаще всего поражены коленный сустав, реже — голеностопные и/или лучезапястные суставы. Средний возраст начала заболевания — 2,5 года (от 6 мес до 6 лет) (рис. 9.2).
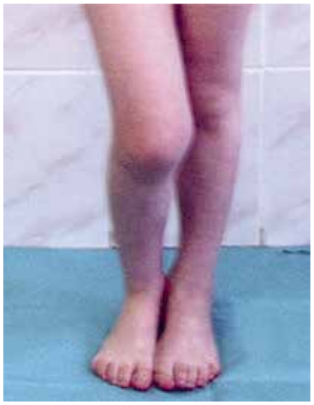
Раздражение зон роста в области пораженного сустава приводит к удлинению конечности. Поражения внутренних органов нетипичны для данного варианта ЮИА. Неблагоприятное внесуставное проявление этого варианта ЮИА — увеит у 50% больных. Среди иммунологических особенностей этого варианта у 40% выявляют антинуклеарный фактор в невысоких титрах (1:80–1:320).
Полиартикулярный вариант
Серопозитивный по РФ субтип ЮИА развивается преимущественно у девочек подросткового возраста и не отличается от серопозитивного по РФ полиартрита у взрослых. Характерно симметричное поражение проксимальных межфаланговых, пястно-фаланговых, лучезапястных суставов (рис. 9.3). Возможно симметричное поражение голеностопных и мелких суставов стопы. Больные отмечают утреннюю скованность, нарастающее ограничение подвижности суставов. Лабораторная активность умеренная, однако при этом варианте выявляют РФ. Иммуногенетический маркер этого субтипа, как и при ревматоидном артрите взрослых, — HLA DR4. Поражение суставов характеризуется также быстрым развитием деструктивно-пролиферативных изменений.
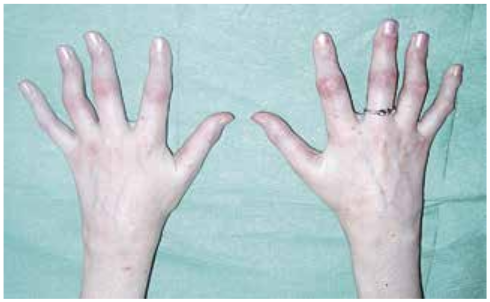
Серонегативный по РФ субтип полиартрита также чаще встречают у девочек. Характерно симметричное поражение крупных и мелких суставов с относительно доброкачественным (чем при серопозитивном субтипе) течением.
Энтезитный вариант
Дебютирует чаще в виде олигоартрита, с преимущественным поражением суставов нижних конечностей, сопровождается поражением суставов свода стопы, болями в пятках (талалгиями), болями или болезненностью при пальпации в области прикрепления связок и сухожилий (энтезитами), вовлечением крестцово-подвздошных сочленений. Этот вариант характерен для мальчиков старше 8 лет и может рассматриваться как начальная стадия ювенильного спондилоартрита. Для него характерна ассоциация с HLA-В27. У 10% больных может развиваться передний увеит.
Системная форма
Выделяют 2 варианта системной формы ЮИА: с преобладанием внесуставных проявлений (аллергосептический вариант) и активным полиартритом (вариант Стилла).
Для системной формы с преобладанием внесуставных проявлений (аллергосептический вариант) характерно внезапное начало с высокой длительной лихорадкой. Температура обычно повышается в ранние утренние часы до 39–40 °С и снижается самостоятельно или под действием жаропонижающих средств. Сыпь — пятнисто-папулезная, появляется одновременно с лихорадкой или через 2–3 нед, локализуется над суставами, на туловище и разгибательных поверхностях, обычно полиморфна, типична так называемая линейная сыпь (рис. 9.4).
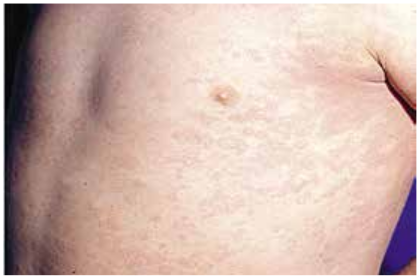
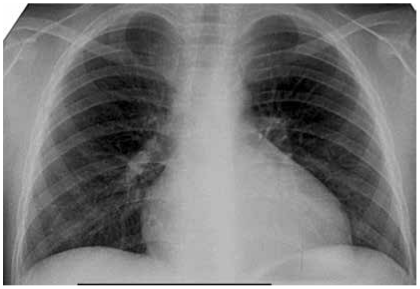
Характерны лимфаденопатия, гепато- и/или спленомегалия. Довольно часто развивается перикардит или миоперикардит, значительно утяжеляющий клиническую картину болезни. Характерны полисерозиты: плеврит, редко — серозный перитонит (рис. 9.5). Как правило, в процесс вовлечены крупные суставы — коленные, часто — тазобедренные реже — голеностопные и очень редко — суставы кистей и стоп. Довольно быстро в суставах развиваются деструктивные изменения. В анализе крови — высокий лейкоцитоз до 30–40×109/л лейкоцитов, нейтрофиллез с палочкоядерным сдвигом (до 15–20%), тромбоцитоз, увеличение СОЭ до 60–80 мм/ч.
Системная форма с активным артритом (вариант Стилла). Встречается преимущественно у детей дошкольного возраста. Для него характерно острое начало, уже в дебюте помимо внесуставных проявлений выражен полиартрит с вовлечением большого числа суставов, в том числе шейного отдела позвоночника и височно-нижнечелюстных суставов.
Диагностика и дифференциальная диагностика
Специфических диагностических маркеров ЮИА нет. Диагноз ставят по клиническим проявлениям при исключении других артритов.
Диагностические критерии ЮИА, рекомендуемые Американской ревматологической ассоциацией, следующие.
Помимо клинических проявлений артрита большое значение имеют лабораторные методы, выявляющие общую активность заболевания — повышение СОЭ, СРБ, иммунологические показатели — повышение IgМ и IgG. РФ и АЦЦП (антитела к циклическому цитруллиновому пептиду), являющиеся маркерами ревматоидного артрита взрослых, в детском возрасте выявляются только у 5–6%, преимущественно у девочек-подростков. Важное значение для диагностики и особенно для контроля за прогрессированием ЮИА имеют лучевые методы диагностики (рентгенологическое исследование суставов, МРТ и КТ суставов), а также ультразвуковые методы визуализации пораженных суставов.
Диагностика ЮИА наиболее сложна в случае развития аллергосептического синдрома, когда суставной синдром отсутствует или слабо выражен, а в клинической картине доминирует фебрильная лихорадка, сыпь, поражение внутренних органов. Диагноз системной формы ЮИА в этом случае ставят методом исключения таких патологий, как сепсис, инфекции (иерсиниоз, токсоплазмоз и др.), онкогематология, солидные опухоли, диффузные болезни соединительной ткани (СКВ, системные васкулиты), хронические заболевания кишечника (неспецифический ЯК, БК) (см. раздел «Аутовоспалительные наследственные заболевания»).
Лечение
Лечение ЮИА зависит от варианта течения заболевания. В дебюте заболевания, когда проводят диагностический поиск, и в период обострения назначают нестероидные противовоспалительные препараты (НПВП). При необходимости проводят внутрисуставное введение глюкокортикоидов, при неэффективности лечения и подтверждении диагноза ЮИА начинают терапию базисными противоревматическими препаратами, при их неэффективности в течение 3–6 мес назначают генно-инженерные биологические препараты.
Нестероидные противовоспалительные препараты оказывают только симптоматический эффект, не влияя на прогрессирование заболевания. Они не способны предотвратить развитие деформаций, деструкции суставов. Характеристика отдельных НПВП дана в приложении (см. приложение на ![]() ).
).
Глюкокортикоиды (ГК). При лечении ЮИА используют преднизолон и метилпреднизолон (метипред, солюмедрол), обладающие как противовоспалительными, так и иммуносупрессивными свойствами. Предпочтительно введение ГК внутрисуставно или в виде пульс-терапии — внутривенное капельное введение 6-метилпреднизолона из расчета 10–15 мг/кг на введение 1 раз в день в течение 3–4 дней. Проведение пульс-терапии позволяет избежать перорального назначения ГК у большинства больных ЮИА. Назначение глюкокортикоидов при ЮИА внутрь в дозе 0,5 мг/кг в сутки не более чем на 2–3 нед проводят по строгим показаниям при наличии жизнеугрожающих состояний.
Базисные противоревматические препараты
Группа препаратов, обладающих болезнь-модифицирующим действием, т.е. способных замедлять прогрессирование заболевания, в частности деструкцию хряща и кости.
Метотрексат — иммуносупрессивный препарат, «золотой стандарт» для лечения больных ревматоидным артритом, как взрослых, так и детей.
Являясь антиметаболитом, влияет на синтез провоспалительных и иммунорегуляторных цитокинов. Рекомендуется использовать дозу метотрексата из расчета 10–15 мг/м2 в неделю, предпочтительно парентеральное введение (подкожно, внутримышечно). Эффект от лечения наступает не ранее чем через 3–5 нед от начала терапии. Одновременно используется фолиевая кислота в дозе 1 мг/сут, за исключением дней, когда пациент получает метотрексат. Сульфасалазин назначают при олигоартикулярных и энтезитных вариантах ЮИА из расчета 30–40 мг/кг массы в сутки в два приема.
Циклоспорин А (ЦиА) в дозе 3,5–5,0 мг/кг в день может использоваться для лечения ЮИА с ревматоидным увеитом.
Генно-инженерные биологические препараты (см. приложение 3 на ![]() ) получены с помощью методов генной инженерии, представляют собой моноклональные антитела против определенных антигенов иммунокомпетентных клеток и провоспалительных цитокинов, ингибиторы цитокинов, противовоспалительные цитокины и др.
) получены с помощью методов генной инженерии, представляют собой моноклональные антитела против определенных антигенов иммунокомпетентных клеток и провоспалительных цитокинов, ингибиторы цитокинов, противовоспалительные цитокины и др.
Этанерцепт — синтезированный генно-инженерным методом растворимый рецептор к ФНО-α (содержит человеческий белок) и является конкурентным ингибитором ФНО-α и β. С 2-летнего возраста вводится подкожно 1 раз в неделю из расчета 0,8 мг/кг. Эффективен при олигоартикулярном, полиартикулярном, энтезитном вариантах ЮИА, псориатическом артрите.
Адалимумаб — рекомбинантное моноклональное антитело, является первым препаратом, полностью идентичным человеческому иммуноглобулину IgGl. Адалимумаб селективно связывается с ФНО-α, нейтрализует как растворимый, так и мембранный ФНО-α. Рекомендуется для лечения детей с 2-летнего возраста, подкожно 1 раз в 2 нед из расчета 0,24 мг/м2. Эффективен при олигоартикулярном, полиартикулярном, энтезитном варианте ЮИА. При развитии ревматоидного увеита адалимумаб является препаратом выбора.
Абатацепт — рецептор, селективно блокирующий костимуляцию Т-лимфоцитов и модулирующий ранний иммунный ответ иммунного каскада, что принципиально отличает этот препарат от ингибиторов ФНО-α. Показан для детей от 6 лет с умеренно выраженным или тяжелым течением активного ЮИА с множественным поражением суставов. Абатацепт вводится внутривенно из расчета 10 мг на 1 кг массы тела по схеме.
Тоцилизумаб — первое рекомбинантное гуманизированное моноклональное антитело к человеческому рецептору интерлейкина-6 (ИЛ-6) из подкласса иммуноглобулинов IgGl. Тоцилизумаб селективно связывается и подавляет как растворимые, так и мембранные рецепторы ИЛ-6. Применяют для лечения активного системного ЮИА у пациентов с 2 лет в виде монотерапии или в комбинации с метотрексатом. Препарат вводится внутривенно из расчета 8 мг/кг 1 раз каждые 2 нед у пациентов с массой тела >30 кг; 12 мг/кг 1 раз каждые 2 нед у пациентов с массой тела <30 кг.
Побочные эффекты генно-инженерных биологических препаратов
К основным побочным эффектам терапии генно-инженерными биологическими препаратами относят инфекции, активацию туберкулеза, что требует постоянного контроля (1 раз в 6 мес) за туберкулиновыми пробами и проведение компьютерной томографии грудной клетки.
Прогноз
Применение генно-инженерных биологических препаратов позволило у большинства детей добиться стойкой ремиссии или низкой активности заболевания, что снижает инвалидизацию и улучшает качество жизни.
Профилактика
Первичной профилактики не существует. Перспективно выделение групп риска ЮИА на основании иммуногенетических маркеров из семей с отягощенным по ревматическим заболеваниям анамнезом.
Тестовые задания
Ответы: 1 — a; 2 — d; 3 — a; 4 — c.
Ситуационная задача
У девочки 5 лет после перенесенного ОРВИ с кишечным синдромом в течение 1,5 мес отмечают артралгии, артриты голеностопных, лучезапястных суставов, лихорадку в утренние часы до 39 °С, пятнисто-папулезную, местами сливную, сыпь. Проводимая терапия с использованием антибиотиков пенициллинового ряда, НПВП — без эффекта. При осмотре отмечена бледность кожных покровов, на боковых поверхностях туловища бледно-розовая пятнистая сыпь со сгущением в области подмышек, единичные элементы на передней поверхности бедер. Выраженная лимфаденопатия всех групп лимфатических узлов, тахикардия до 150 уд. в мин. Увеличение печени до +4,0 см из-под края реберной дуги, пальпируется край селезенки. Суставной синдром: лучезапястные и голеностопные суставы дефигурированы за счет экссудативного компонента, движения резко ограничены, болезненны, ограничено разведение тазобедренных суставов, больше справа. В анализе крови нейтрофильный лейкоцитоз (лейкоциты 21,0×109/л, палочкоядерные 4%, сегментоядерные 92%), СОЭ 60 мм/ч, СРБ +++, РФ и антинуклеарный фактор отрицательные: IgA 240 мг/%, IgM 190 мг/%, IgG 2150 мг/%.
Ответы: 1 — c; 2 — e; 3 — a; 4 — d.
9.1.2. Псориатический артрит
Псориатический артрит (ПсА) — хроническое воспалительное заболевание суставов, которое развивается приблизительно у трети больных псориазом. ПсА у взрослых относят к группе серонегативных спондилоартритов, у детей — к ЮИА по классификации Дурбан 1998 г. Псориаз — распространенное хроническое генетически детерминированное заболевание кожи, частота встречаемости которого — 1–3%.
Эпидемиология
ПсА составляет 4–9% в структуре ювенильных артритов. Популяционная частота его — от 0,05 до 1%, а заболеваемость ПсА составляет 3,6–6 на 100 тыс. населения. В 2 раза чаще его наблюдают у девочек. Пик заболеваемости приходится на пубертатный возраст.
Этиология
Этиология ПсА до сих пор не выяснена. Предполагают, что наиболее существенное значение в возникновении и течении псориаза и ПсА имеют генетические, иммунологические и средовые факторы.
Патогенез
Механизмы поражения суставов при ПсА, вероятно, сходны с таковыми при других ревматических заболеваниях, прежде всего ревматоидном артрите и анкилозирующем спондилите. Ведущую роль в патогенезе синовита и деструктивных изменений суставов играет ФНОα, который активирует клетки эндотелия, стимулирует пролиферацию фибробластов, способствует экспрессии матриксных металлопротеиназ, стимулирует синтез коллагеназы и простагландина Е2, активирует остеокласты, регулирует продукцию ряда хемокинов.
Клиническая картина
У детей в 50% случаев артрит предшествует появлению псориаза.
Однако даже при наличии у ребенка симптомов данного дерматоза он обычно не столь явно выражен, как у взрослых, поэтому нередко просматривается врачами. Наиболее часто заболевание начинается с моно-, олигоартрита суставов кистей. У 40–80% детей процесс постепенно распространяется на другие суставы, хотя и в этом случае он может носить асимметричный характер.
ПсА может дебютировать постепенно, исподволь (первые симптомы: повышенная утомляемость, миалгии, артралгии, энтезопатии, потеря массы тела). Приблизительно у трети детей в начале заболевания отмечают приступообразную резкую болезненность, отек и скованность в суставах, выраженную в утренние часы.
У подавляющего большинства (80%) больных ПсА чаще проявляется моно- или олигоартритом дистальных, проксимальных межфаланговых суставов пальцев кистей, коленных суставов, реже — пястно- и плюснефаланговых, а также плечевых суставов.
Для данной патологии свойственно и вовлечение в дебюте болезни так называемых суставов-исключений (межфалангового сустава I пальца и проксимального межфалангового — V пальца кисти). Особенностью ПсА является поражение всех суставов одного пальца кисти — аксиальный, или осевой, артрит. Нередко при этом наблюдают тендовагинит сухожилий сгибателей, что придает пораженному пальцу сосискообразный вид.
Мутилирующий (обезображивающий) артрит — своеобразная форма ПсА, проявляемая тяжелым деструктивным артритом дистальных отделов конечностей, преимущественно пальцев кистей и стоп. В результате остеолиза пальцы укорачиваются, развивается их характерная деформация (телескопический палец) или деформация кисти (рука с лорнетом).
У 40% пациентов с ПсА наблюдают вовлечение в процесс позвоночника (псориатический спондилит). Изменения позвоночника при ПсА могут ничем не отличаться от изменений, свойственных болезни Бехтерева Эти больные часто — носители Аг гистосовместимости HLA-В27.
Диагностика
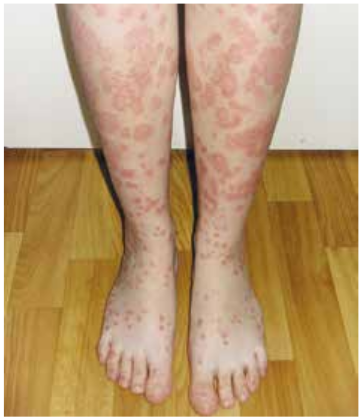
Классическими проявлениями псориаза у детей — эритематозные папулы, покрытые серебристыми чешуйками, которые сливаются в бляшки различной формы. Чаще всего поражена кожа локтей, коленей, паховой области, волосистой части головы (рис. 9.6). Ключ к диагнозу — локализация и характер поражения суставов (например, асимметрия поражения, наличие дактилита, поражение дистальных межфаланговых суставов), которые являются основанием для тщательного осмотра паховой области, пупка и волосистой части головы с целью выявления псориатических поражений.
Для постановки диагноза используют Ванкуверские диагностические критерии ювенильного ПсА (1989). Определенный ювенильный ПсА выявляют при наличии:
-
артрита и хотя бы 3 из следующих «малых» признаков:
-
дактилита (рис. 9.7; ПсА, дактилит, псориатическое поражение ногтей).
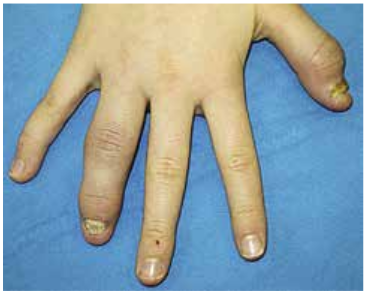
Вероятный ювенильный ПсА определяют при наличии артрита и хотя бы 2 из «малых» признаков.
Дифференциальная диагностика
Сходную с ПсА симптоматику наблюдают при синдроме Рейтера, особенно протекающем с кератодермией. Наличие синдрома Рейтера подтверждает характерная триада: артрит, конъюнктивит, уретрит или диарея.
Для болезни Бехтерева в отличие от ПсА характерны выраженная субъективная симптоматика (боль и скованность в пояснично-крестцовом и других отделах позвоночника), равномерный двусторонний сакроилеит, последовательное, снизу вверх, вовлечение в процесс отделов позвоночника, отсутствие псориаза, поражение чаще крупных и средних суставов нижних конечностей, отчетливый эффект пиразолоновых и индольных препаратов.
Лечение
В настоящее время средства для полного излечения ПсА и псориаза не существует, но есть множество методик, способных уменьшать болезненные проявления. Применяют следующие основные группы препаратов.
-
НПВП — диклофенак 2–3 мг/кг в сут, индометацин 2–3 мг/кг в сут.
-
Глюкокортикоиды, главным образом в виде периодических внутрисуставных инъекций [метилпреднизолон (Метипред♠), бетаметазон (Дипроспан♠)], пульс-терапии метилпреднизолоном (Метипредом♠; 5–15 мг/кг в течение 3 дней).
-
Базисные противовоспалительные препараты. Сульфасалазин 30 мг/кг в сут (дозу распределяют на 2 приема). Метотрексат применяют в основном в дозе 10–15 мг/м2 в нед в таблетках или в виде внутримышечных инъекций. Лефлуномид назначают сначала в дозе 100 мг в сут в течение 3 дней, далее ежедневная доза составляет 20 мг (10/20 мг у детей весом до 40 кг) в сут. Циклоспорин применяют в дозе 3 мг/кг.
При отсутствии эффекта от двух базисных средств, наличии стабильной клинической активности заболевания, острого дактилита, поражении сухожилий, изолированного псориатического спондилоартрита пациенту предлагают терапию биологическими агентами: инфликсимаб (Ремикейд♠), адалимумаб (Хумира♠), этанерцепт.
Пациентам с ПсА советуют вести подвижный образ жизни и ежедневно заниматься ЛФК. Также им рекомендуют местную терапию псориаза, см. ![]() .
.
Профилактика
Специфической профилактики нет. Необходимо избегать переохлаждения, инсоляции, физических и психологических перегрузок.
Прогноз
В целом благоприятный. Стойкой ремиссии достигают у 20—50% детей, приблизительно у четверти больных отмечают хронический полиартрит, а у 10% процесс приводит к инвалидизации.
тестовые задания
Ответы: 1 — a; 2 — a; 3 — a; 4 — a; 5 — a.
9.1.3. Реактивный артрит
Реактивный артрит — асептическое воспалительное заболевание суставов, развивающееся в ответ на внесуставную инфекцию, преимущественно кишечную и урогенитальную.
Эпидемиология
По данным отдела медицинской статистики Минздрава России, распространенность реактивного артрита в 2007 г. среди детей до 14 лет составила 90,76 на 100 тыс. детского населения, а среди подростков 15–17 лет — 139,64 на 100 тыс.
Этиология
Реактивный артрит развивается вследствие иммунных нарушений, связанных с кишечной и/или урогенитальной инфекцией, преимущественно у генетически предрасположенных лиц (носителей HLA-B27). Многие ревматологи относят его к группе серонегативных спондилоартритов.
Инфекционная причина развития реактивного артрита в большинстве случаев — острая или персистирующая кишечная инфекция, вызванная энтеробактериями Schigella flexneri, Schigella zonne, Schigella newcastle, Salmonella enteritidis, Salmonella typhimurium, Yersinia enterocolitica, Yersinia pseudotuberculosis и острая или персистирующая урогенитальная инфекция, вызываемая Chlamydia trachomatis, Chlamydophilla pneumonia, U. urealyticum.
Патогенез
При развитии хламидийного реактивного артрита иммунный ответ на внедрение микроорганизмов представлен активацией макрофагов; локальным образованием секреторного IgA, активацией клеточного звена иммунитета; выработкой АТ класса IgM против хламидийных Аг в течение 48 ч после заражения. Происходит также синтез АТ класса IgG.
Выработка АТ, а также фагоцитоз макрофагами возможен, только когда хламидийная клетка находится в стадии элементарного тельца в межклеточном пространстве. Чтобы полностью избавиться от хламидий АТ недостаточно. Когда хламидия находится в стадии ретикулярного тельца внутри клетки, она абсолютно недоступна как для АТ, так и для лимфоцитов и макрофагов. Поэтому при вяло текущем или бессимптомном процессе количество АТ в крови обычно небольшое.
У больных с хроническим хламидийным реактивным артритом выявляют аномалии иммунного ответа: нарушение соотношения между Т-супрессорами и Т-хелперами (снижение количества Т-хелперов), выраженное снижение относительного и абсолютного количества В-клеток, снижение количества естественных киллерных клеток. Все указанные изменения в иммунном ответе организма больных способствуют развитию хронизации процесса.
В происхождении реактивных артритов, связанных с кишечной инфекцией, основное значение также придают инфекции и генетической предрасположенности. Однако истинный характер взаимоотношений микро- и макроорганизма все еще не ясен.
«Артритогенные» микроорганизмы проникают в слизистую оболочку кишечника и размножаются внутри полиморфноядерных лейкоцитов и макрофагов. В дальнейшем происходит транспорт бактерий и продуктов их жизнедеятельности из первичного очага в органы мишени. По данным экспериментальных исследований, наиболее длительное время микроорганизмы персистируют в клетках, экспрессирующих HLA В27.
В реализации генетически детерминированной предрасположенности индивидуума к развитию реактивного артрита придают значение носительству HLA-B27.
Клиническая картина
Синдром Рейтера
Классическое клиническое проявление реактивного артрита — болезнь Рейтера, или уретро-окуло-синовиальный синдром, который характерен классической триадой клинических симптомов — уретритом, конъюнктивитом, артритом. Синдром Рейтера развивается в хронологической связи с перенесенной инфекцией мочеполового тракта или кишечника или на фоне персистирующей инфекции.
Особенности клинической картины синдрома Рейтера у детей. Синдром Рейтера, развивающейся на фоне хламидийной инфекции, у детей имеет ряд особенностей. В дебюте чаще всего отмечают симптомы поражения урогенитального тракта. В последующем присоединяются симптомы поражения глаз и суставов. Поражение урогенитального тракта характерно стертостью клинической картины. Поражение глаз — развитием конъюнктивита, чаще катарального.
Поражение опорно-двигательного аппарата характеризуют развитием ограниченного асимметричного, моно-, олиго- и полиартрита, преимущественно вовлечение суставов ног с наиболее частым поражением коленных, голеностопных суставов. Артрит может начинаться остро, с выраженными экссудативными изменениями, возможно повышение температура до фебрильных цифр.
Поражение суставов при этом характерно длительным отсутствием деструктивных изменений, несмотря на рецидивирующий синовит. Типично для реактивного артрита поражение первого пальца стопы, формирование «сосискообразной» деформации пальцев стоп, развитие теносиновита и бурсита, развитие ахиллобурсита (рис. 9.8).
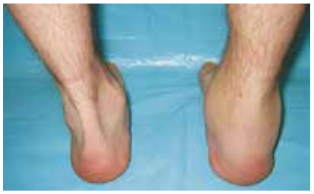
У ряда больных отмечают развитие энтезита и энтезопатий, частые боли в пятках, боли, скованность, ограничение подвижности в шейном и поясничном отделе позвоночника, что характерно для мальчиков-подростков, с наличием HLA-B27. У этих детей высокий риск формирования ювенильного спондилоартрита.
Синдром Рейтера, ассоциированный с кишечной инфекцией, протекает более остро, агрессивно, чем ассоциированный с хламидийной инфекцией. Заболевание может протекать с выраженными симптомами интоксикации, лихорадкой, острым суставным синдромом, высокой лабораторной активностью.
Вероятный реактивный артрит (без отчетливых внесуставных поражений)
В ряде случаев реактивный артрит протекает без отчетливых внесуставных проявлений, относящихся к симптомокомплексу синдрома Рейтера (конъюнктивит, уретрит, кератодермия). В таких случаях ведущим в клинической картине является суставной синдром, который характерен преимущественным поражением суставов нижних конечностей асимметричного характера.
Диагностика
Диагноз реактивного артрита ставят на основании Берлинских диагностических критериев (1996; табл. 9.1).
| Показатель | Диагностический критерий |
|---|---|
Периферический артрит |
Асимметричный. |
Инфекционные проявления |
Диарея. |
Лабораторное подтверждение инфекции |
Необязательно, но желательно при наличии выраженных кинических проявлений инфекции. |
Критерии исключения |
Установленная причина развития моно- или олигоартрита:
|
Этиологическая диагностика включает следующие методы.
-
-
Выявление Аг хламидий в эпителиальных клетках, полученных в результате соскобов из уретры и конъюнктивы, а также в синовиальной жидкости (прямой иммунофлюоресцентный анализ др.).
-
Выявление АТ к Аг хламидий в сыворотке крови и в синовиальной жидкости — реакция связывания комплемента (РСК), прямая и непрямая иммунофлюоресценция.
-
Выявление АТ к бактериям кишечной группы в сыворотке крови — реакция пассивной гемагглютинации (РПГА), РСК.
-
-
Морфологический метод — выявление морфологических структур возбудителя (с использованием иммунофлюоресцентного анализа).
-
Выделение хламидий в культуре клеток, на куриных эмбрионах, лабораторных животных.
-
Молекулярно-биологические методы — выявление ДНК возбудителя (ПЦР и др.) в крови и синовиальной жидкости.
Лечение
Этиотропная терапия
Этиотропное лечение реактивного артрита, ассоциированного с хламидийной инфекцией
Поскольку хламидия — внутриклеточный паразит, то выбор антибактериальных препаратов ограничен только теми, которые способны накапливаться внутриклеточно. К таким антибиотикам относят макролиды, тетрациклины и фторхинолоны.
Тетрациклины и фторхинолоны достаточно токсичны, обладают побочными эффектами, которые ограничивают их применение в детской практике. В связи с этим наиболее часто для лечения хламидиоза у детей используют макролиды [азитромицин (Сумамед♠), рокситромицин (Рулид♠), спирамицин (Ровамицин♠), джозамицин (Вильпрафен♠)] в стандартной дозировке 7–10 дней (табл. 9.2).
| Антибактериальный препарат | Дозировка | Длительность курса |
|---|---|---|
Азитромицин (Сумамед♠) |
1-й день 10 мг/кг в сут в 1 прием, последующие дни 5 мг/кг |
7–10 дней |
рокситромицин (Рулид♠) |
5–8 мг/кг в сут в 2 приема |
10 дней |
Джозамицин (Вильпрафен♠) |
30–50 мг/кг в сут в 3 приема |
10 дней |
Спирамицин (Ровамицин♠) |
1,5 млн МЕ/10 кг в сут в 2–3 приема для детей весом более 20 кг. |
10 дней |
Доксициклин (Юнидокс солютаб♠) для детей старше 8 лет |
4 мг/кг в 1-й день, 2 мг/кг в сут в последующие дни |
10 дней |
Этиотропное лечение реактивного артрита, ассоциированного с кишечной инфекцией
Всем детям с реактивным артритом, у которых выявлены АТ к бактериям кишечной группы в диагностических титрах или при бактериологическом обследовании кала высеваются бактерии кишечной группы, необходимо проведение антибактериальной терапии. Препараты выбора — аминогликозиды — амикацин (Амикин♠ для внутривенного введения), гентамицин, фторхинолоновые препараты (для детей старше 12 лет).
Патогенетическая терапия
Монотерапия антибиотиками оказывает недостаточный эффект при затяжном и хроническом течении реактивного артрита, ассоциированном с персистирующей хламидийной инфекцией. Для лечения реактивных артритов хламидийной этиологии у детей разработаны и апробированы схемы терапии с использованием следующих иммуномодуляторов: глюкозаминилмурамилдипептида (Ликопида♠), тимуса экстракта (Тактивина♠), азоксимера бромида (Полиоксидония♠). Схемы комбинированной терапии, см. ![]() .
.
Для купирования островоспалительных изменений в суставах больным целесообразно внутрисуставное введение глюкокортикоидов, а также применение НПВП в возрастных дозах.
В ряде случаев возможно реинфицирование после успешно проведенного лечения, что требует повторного назначения противохламидийной терапии. Важный фактор успешного лечения ребенка с реактивным артритом, ассоциированного с хламидийной инфекцией, — диагностика и лечение членов семьи больного.
В случае высокой иммунологической активности заболевания, появления признаков ювенильного спондилоартрита использование иммуномодуляторов противопоказано.
Симптоматическая терапия
С целью лечения суставного синдрома при реактивном артрите применяют НПВП в возрастных дозировках.
Локальная терапия глюкокортикоидами: метилпреднизолон (Депо-медрол♠, Метипред♠) и бетаметазон (Дипроспан♠).
Пульс-терапия метилпреднизолоном. Под термином «пульс-терапия» обычно подразумевают быстрое (в течение 30–60 мин) введение больших доз глюкокортикоидов. Для лечения реактивного артрита используют низкие дозы метилпреднизолона (Метипреда♠; 5–15 мг/кг в течение 3 дней).
Иммуносупрессивная терапия. В дальнейшем при хроническом течении артрита, особенно у HLA-B27-позитивных больных, при появлении признаков спондилоартрита, высоких лабораторных показателях СОЭ, СРБ, IgG применяют иммуносупрессивную терапию сульфасалазином 30–40 мг/кг массы в сут в 2 приема, реже метотрексатом.
Прогноз
У большинства детей реактивный артрит заканчивается полным выздоровлением. У части больных эпизоды реактивного артрита рецидивируют и в дальнейшем появляются признаки спондилоартрита, особенно у HLA-B27 позитивных больных.
Тестовые задания
Ответы: 1 — a; 2 — a; 3 — a; 4 — a.
Ситуационные задачи
Задача 1
На прием пришел мальчик 5 лет с жалобами на боли в правом коленном суставе.
Anamnesis morbi: боли в суставе появились 2 нед назад. 1 мес назад ребенок перенес кишечную инфекцию.
Anamnesis vitae: в раннем возрасте частые ОРВИ. Профилактические прививки по календарю.
При осмотре: состояние удовлетворительное. Температура тела 36,8 °С. Кожные покровы чистые. Зев спокоен. Походка нарушена. Отмечен выпот, болезненность при движении, повышение местной температуры в правом коленном суставе. Остальные суставы интактны. Энтезопатий нет. Ригидности позвоночника нет.
При обследовании: клинический анализ крови: лейкоциты 10,7×109/л, СОЭ 13 мм/ч.
Ответы: 1 — a; 2 — a.
Задача 2
На прием пришел мальчик 6 лет с жалобами на выпот в левом голеностопном суставе, покраснение глаз, слезотечение.
Anamnesis morbi: месяц назад ребенок жаловался на частое мочеиспускание и болезненность при мочеиспускании. К врачу не обращались. Лечились домашними средствами. 10 дней назад появился выпот в левом голеностопном суставе, 3 дня назад присоединился конъюнктивит.
Anamnesis vitae: без особенностей. Профилактические прививки по календарю.
При осмотре: состояние удовлетворительное. Температура 36,8 °С. Кожные покровы чистые. Зев спокоен. Походка не нарушена. Отмечены экссудативные изменения в левом голеностопном суставе, повышение местной температуры в левом голеностопном суставе. Остальные суставы интактны. Энтезопатий нет. Ригидности позвоночника нет.
Ответы: 1 — a; 2 — a.
Задача 3
На прием пришла девочка 8 лет с жалобами на выпот в левом коленном суставе.
Anamnesis morbi: полгода назад девочка отдыхала на юге. Через месяц после возвращения домой в области пупка у девочки появились эритематозные папулы, покрытые серебристыми чешуйками. Врач поставил диагноз «дерматит», назначил местную терапию. Месяц назад появились боли и выпот в левом коленном суставе.
Anamnesis vitae: без особенностей. Профилактические прививки по календарю.
При осмотре: состояние удовлетворительное. Температура 36,8 °С. В околопупочной области бляшки, покрытые серебристыми чешуйками. Зев спокоен. Походка нарушена. Отмечены экссудативные изменения в левом коленном суставе, повышение местной температуры в левом коленном суставе, ограничение подвижности в нем. Остальные суставы интактны. Энтезопатий нет. Ригидности позвоночника нет.
Ответы: 1 — b; 2 — d.
Задача 4
На прием пришел мальчик 10 лет с жалобами на боли в правом тазобедренном суставе.
Anamnesis morbi: боли в суставе появились 2 нед назад. 2 мес назад ребенок отдыхал на юге, месяц назад перенес ОРВИ, осложнившееся бронхитом.
Anamnesis vitae: в раннем детстве частые ОРВИ. Профилактические прививки по календарю.
При осмотре: состояние удовлетворительное. Температура тела 36,8 °С. Кожные покровы чистые. Зев спокоен. Походка нарушена. Отмечены ограничение подвижности, болезненность при движении в правом тазобедренном суставе, наружная ротация. Остальные суставы интактны. Энтезопатий нет. Ригидности позвоночника нет.
Ответы: 1 — a; 2 — d.